一种不锈钢植入体复合材料及其制备与应用的制作方法
本发明涉及一种具有良好生物相容性的不锈钢多层生物复合材料的制备方法,即通过基于多层螺旋CT三维重建的3D打印技术、水热处理法和表面生物高分子层制备等方法制备具有羟基磷灰石/生物高分子多层复合涂层的不锈钢植入体。(二)
背景技术:
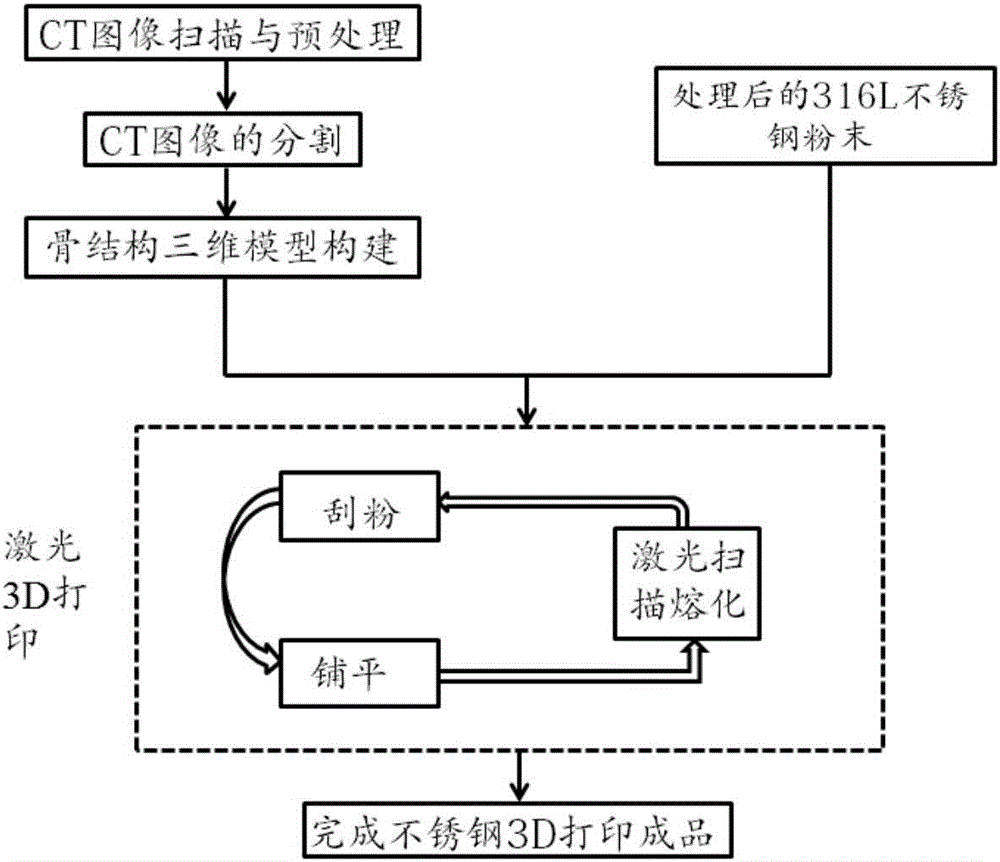
:目前在临床应用领域,医用金属材料主要有不锈钢、钴基合金以及钛合金等几大类材料,这其中不锈钢因其具有强度高、韧性好、耐久、成本低等特点,而被广泛应用于生物医用领域。目前制备生物医用不锈钢的方法主要还维持着传统的机械生产方式,缺乏对个体的个性化设计,从而限制了其在医用领域的进一步发展。而新型的激光增材制造技术(3D打印),不仅具有精度高的优势且在成形过程中能达到真正的冶金结合。同时,3D打印技术是以数字模型为基础,运用粉末状金属或塑料等材料,通过逐层熔化和堆积的方式来构造物体的技术。现有的生物工程领域可以通过多层螺旋CT三维重建进行3D打印在骨结构方面的构建,基于多层螺旋CT的三维重建将共同提高实体世界和数字世界之间形态转换的分辨率,可以扫描、编辑和复制实体对象,创建精确的副本或优化原件。因此,采用基于多层螺旋CT三维重建的3D打印工艺制备修复体,使获得的个性化三维结构与患者缺损部位高度匹配,克服了传统工艺制备存在的个性化差、匹配度低等问题。生物医用金属材料存在导电、导热性能差,与其他金属接触易腐蚀,金属离子释放等问题。为了解决这些问题,羟基磷灰石(HA:Ca10(PO4)6(OH)2)因其具有良好的骨结合性能、生物相容性而受到广泛的关注。羟基磷灰石和骨组织具有类似的化学成分和晶体结构,这种材料植入生物体后在短时间内就具有较大的附着力,可使材料/骨界面形成牢固结合,有利于移植材料的初始固位,可有效抑制金属离子向生物体内的释放,此外羟基磷灰石还可以延长植入体的使用寿命。目前,有许多方法可以制备HA涂层,包括溶胶-凝胶法、离子束沉积法、电化学沉积法和仿生合成法等。利用溶胶-凝胶法对不锈钢基体进行羟基磷灰石的制备,较目前常见的水热法和热喷涂法制备羟基磷灰石相比,该方法具有制备条件温和、成本低廉、成分易于控制等优点。然而单纯的羟基磷灰石涂层在性能上会存在易脱落的倾向,导致涂层的使用寿命降低。因此,为进一步提高羟基磷灰石涂层的结合力和复合材料的生物相容性,对表面的羟基磷灰石层可进行生物高分子涂层的制备。本发明通过对原始的骨结构多层螺旋CT扫描进行三维重建,采用3D打印技术进行生物医用不锈钢材料的制备,然后对其表面进行溶胶-凝胶法制备羟基磷灰石的制备,并为接下来的涂层制备做准备。在生物高分子溶剂中进行生物高分子层的薄膜制备,通过一系列的工艺处理实现了生物医用不锈钢多层生物复合涂层的制备,获得高匹配性、高性能的复合结构。而截至目前,这种系统性、高还原性、高相容性的不锈钢生物复合材料的制备还未见报道。(三)技术实现要素:本发明目的是提供一种具有良好生物相容性的不锈钢多层生物复合材料及其制备方法与应用,以多层螺旋CT三维重建为基础,进行不锈钢植入体的3D打印、并对不锈钢基体进行溶胶-凝胶以及生物高分子层制备等一系列表面处理,最终获得从内至外依次为不锈钢植入体基体/羟基磷灰石(HAP)层/生物高分子层的复合材料。本发明解决了传统不锈钢植入体材料生物相容性差,成骨细胞依附性低等问题,提高了不锈钢植入体的耐腐蚀性能和生物活性,为不锈钢植入体材料的进一步应用提供了思路。本发明采用的技术方案是:本发明提供一种不锈钢植入体复合材料,所述不锈钢植入体复合材料以不锈钢粉经3D打印制作的模型为不锈钢植入体基体,在不锈钢植入体基体表面采用溶胶-凝胶法形成羟基磷灰石层,然后再在羟基磷灰石层表面浸渍形成聚乳酸层。进一步,所述羟基磷灰石层厚度为5μm~15μm。进一步,所述羟基磷灰石层按如下方法制备:将Ca(NO3)2、P2O5和磷酸三乙酯(C3H5O3PO)溶于无水乙醇(优选将Ca(NO3)2无水乙醇溶液缓慢滴加到P2O5和磷酸三乙酯的混合无水乙醇溶液(P2O5:C3H5O3PO=2:1,摩尔比)中),用氨水调节pH值至8-9(优选8.5),混匀,充分搅拌6小时,75℃回流18h,然后80℃静置反应2h,形成溶胶;所述Ca(NO3)2与P2O5和磷酸三乙酯物质的量之比为10:2:1,所述无水乙醇总体积用量以Ca(NO3)2物质的量计为50~100ml/mol;将所述的不锈钢植入体基体浸入所述的溶胶中,室温浸渍2-4min(优选3min),以15-25mm/min(优选20mm/min)的恒定速度垂直向上提拉成膜,再于75℃干燥1h,重复提拉、干燥操作5次,然后在氩气或真空保护气氛下350-500℃(优选400℃)保温30min进行退火,自然冷却,用去离子水反复清洗,23℃干燥,获得表面形成羟基磷灰石层的不锈钢植入体基体。进一步,所述聚乳酸层的厚度为5μm~10μm。进一步,所述聚乳酸层按如下方法制备:将聚乳酸粉末(重均分子量15万)加入到二氯甲烷中,室温均匀搅拌6小时,获得质量浓度2.5%的聚乳酸溶液;所述聚乳酸粉末与二氯甲烷的质量比为2.5:97.5;将表面形成羟基磷灰石层的不锈钢植入体基体浸入聚乳酸溶液中,室温浸泡20-30s(优选25s)后,以15-25mm/min(优选20mm/min)的恒定速度提出,在通风厨内室温晾干,然后去离子水洗净,室温晾干,即在不锈钢植入体基体表面由内至外依次形成羟基磷灰石层和聚乳酸层。进一步,所述不锈钢植入体基体按如下方法制备:(1)将受损骨结构进行CT扫描,获得受损骨结构的CT扫描数据,并输入到Materialise三维建模软件,进行阈值划分,然后使用区域增长法去除导入图像的噪音,进行冗余数据的去除、分割受损骨结构区域;(2)通过Materialise三维建模软件开运算获得受损骨结构的三维结构数据,然后将获得的三维结构数据输入UG软件,获得数字化骨缺损三维模型;(3)根据数字化骨缺损三维模型,使用CAD软件设计骨缺损模块,获得STL模型;(4)将不锈钢粉末在球磨机(XQM-0.4L行星式球磨机)混合均匀,磨转速为250r/min,球磨时间为30min,采用氮气作为保护气体,获得球磨后的不锈钢粉末(粒径为50μm~70μm);将STL模型输入3D打印设备中,再将球磨后的不锈钢粉末置于3D打印设备中,采用激光3D打印成型,激光的功率为100~200W,脉宽1~3ms,频率0.0Hz,离焦量2~3mm,光斑直径0.5mm(优选激光的功率为150W,脉宽2ms,频率0.0Hz,离焦量2.5mm,光斑直径0.5mm),氩气或者真空保护气氛下打印,单层打印厚度0.04mm,获得的胚料置于电化学工作站(IviumStat)配有搅拌装置的电解槽中,电解槽内抛光液为体积比1:1:20的高氯酸、甘油和冰醋酸的混合液,在30V恒压模式,加液氮降温至-20℃,在搅拌速度100~200r/min(优选150r/min)的条件下进行电化学抛光操作,获得电化学抛光后的基体,再依次用无水酒精、丙酮和去离子水超声清洗,室温下干燥,获得所述的不锈钢植入体基体。进一步,所述不锈钢粉为316L不锈钢粉末,粒径为100μm~120μm。本发明还提供一种所述不锈钢植入体复合材料的制备方法,所述方法为:(1)将受损骨结构进行CT扫描,获得受损骨结构的CT扫描数据,并输入到Materialise三维建模软件,进行阈值划分,然后使用区域增长法去除导入图像的噪音,进行冗余数据的去除、分割受损骨结构区域;(2)分割好受损骨结构区域后,进一步通过Materialise三维建模软件开运算获得受损骨结构的三维结构数据,实现将原始数据转为三维结构数据,然后将获得的三维结构数据输入UG软件,获得数字化骨缺损三维模型;(3)根据数字化骨缺损三维模型,使用CAD软件设计骨缺损模块,获得STL模型;(4)将不锈钢粉末在球磨机(XQM-0.4L行星式球磨机)中混合均匀,磨转速为250r/min,球磨时间为30min,并且采用氮气作为保护气体,获得球磨后的不锈钢粉末;将STL模型输入3D打印设备中,再将球磨后的不锈钢粉末置于3D打印设备中,采用激光3D打印成型,激光的功率为100~200W,脉宽1~3ms,频率0.0Hz,离焦量2~3mm,光斑直径0.5mm(优选激光的功率为150W,脉宽2ms,频率0.0Hz,离焦量2.5mm,光斑直径0.5mm),氩气或者真空保护气氛下打印,单层打印厚度0.04mm,获得的胚料置于电化学工作站(IviumStat)配有搅拌装置的电解槽中,电解槽内抛光液为体积比1:1:20的高氯酸、甘油和冰醋酸的混合液,在30V恒压模式,加液氮降温至-20℃,在搅拌速度100~200r/min(优选150r/min)的条件下进行电化学抛光操作,获得电化学抛光后的基体,,再依次用无水酒精、丙酮和去离子水超声清洗,室温下干燥,获得所述的不锈钢植入体基体;(5)将Ca(NO3)2、P2O5和磷酸三乙酯与无水乙醇混合,用氨水调节pH值至8-9(优选8.5),混匀,充分搅拌6小时,75℃回流18h,然后80℃静置反应2~4h,形成溶胶;所述Ca(NO3)2与P2O5和磷酸三乙酯物质的量之比为10:2:1,所述无水乙醇总体积用量以Ca(NO3)2物质的量计为50~100ml/mol;将所述的不锈钢植入体基体浸入所述的溶胶中,室温浸渍2-4min(优选3min),以15-25mm/min(优选20mm/min)的恒定速度垂直向上提拉成膜,再于75℃干燥1h,重复提拉、干燥操作5次,然后在氩气或真空保护气氛下350-500℃(优选400℃)保温30min进行退火,自然冷却,用去离子水反复清洗,23℃干燥,获得表面形成羟基磷灰石层的不锈钢植入体基体;(6)将聚乳酸粉末加入到二氯甲烷中,室温均匀搅拌6小时,获得质量浓度2.5%聚乳酸溶液;所述聚乳酸粉末与二氯甲烷质量比为2.5:97.5;将表面形成羟基磷灰石层的不锈钢植入体基体浸入聚乳酸溶液中,室温浸泡20-30s(优选25s)后,以15-25mm/min(20mm/min)的恒定速度提出,在通风厨内室温晾干,然后去离子水洗净,室温晾干,即在不锈钢植入体基体的表面由内至外依次形成羟基磷灰石层和聚乳酸层,获得所述的不锈钢植入体复合材料。此外,本发明还提供一种所述不锈钢植入体复合材料在制备骨修复材料中的应用。所述的应用为:根据受损骨结构,通过多层螺旋CT扫描构建模型,将不锈钢粉末进行3D打印,个性化进行骨植入体的制备,进而进行羟基磷灰石涂层与生物高分子层的制备,通过体外活性成骨细胞的培养实验与在Hank溶液中的动极化腐蚀测试显示,本发明制备的不锈钢植入体复合材料显著提升了不锈钢基体的耐腐蚀性能,并且具有更好的生物活性,成骨细胞的附着性良好。本发明所述室温指25-30℃。本发明中羟基磷灰石层厚度通过反应时间来控制,聚乳酸层厚度通过反复浸渍、提拉来控制。与现有制备不锈钢植入体的技术相比,本发明的有益效果主要体现在:(1)本发明在基体的制备上采用基于多层螺旋CT三维重建的3D打印技术,解决了传统铸造、烧结等制备方法所引起的工艺复杂,易氧化,植入体复原精度低等问题,提高了不锈钢植入体的结构精度和生物相容性;(2)利用溶胶-凝胶法对不锈钢表面制备羟基磷灰石层较传统的等离子喷涂等方法具有制备条件温和、成本低廉、成分易于控制等优点,同时羟基磷灰石层的引入增强了膜层表面的亲水性,有利于蛋白在表面的吸附,显著改善细胞的迁移与增长,提高材料的骨整合,从而有利于骨组织的愈合;(3)本发明利用浸渍提拉机对溶胶-凝胶处理后的不锈钢植入体进行表面生物高分子层的制备,提高了涂层在体内的耐腐蚀性,进一步促进了骨组织的修复。本发明从原始受损骨结构的数据采集到最终多涂层复合结构的制备,实现了不锈钢植入体材料的个性化开发,获得了高质量的不锈钢植入体复合材料,其中通过对制备前后的材料进行极化测试显示,制备后放入不锈钢植入体复合材料的抗腐蚀性能得到2~3个数量级的提升,而体外成骨细胞培养结果也显示制备后的不锈钢植入体复合材料具有更好的骨细胞依附促进能力。(四)附图说明图1是本发明316L不锈钢/羟基磷灰石/聚乳酸层复合材料的结构示意图;图2是本发明基于多层螺旋CT三维重建进行不锈钢材料3D打印的加工流程示意图。(五)具体实施方式下面结合具体实施例对本发明进行进一步描述,但本发明的保护范围并不仅限于此:下述实例中,不锈钢植入体材料具有多层结构(如图1),包括羟基磷灰石和聚乳酸生物高分子层。不锈钢基体的制备流程如图2所示;包括粉末的处理,CT扫描数据收集与处理,模型的构建和3D打印成型及样品后处理等流程组成。实施例11、不锈钢植入体复合材料的制备(1)将患者骨结构进行CT扫描(GELightSpeed16层螺旋CT),进行受损骨结构数据的采集,数据保存为DICOM格式;(2)将获得的CT扫描数据输入到Materialise三维建模软件(MaterialiseMagics20),进行常规的计算机阈值划分,然后通过计算机使用区域增长法去除导入图像的噪音,进行冗余数据的去除、分割受损骨结构区域;(3)通过在Materialise软件中进行开运算操作,获得受损骨结构的三维结构数据,然后将获得的三维数据输入UG软件(NX9.0)获得数字化骨缺损三维模型,进行骨缺损的修复设计;(4)使用计算机辅助软件(CAD)(AutoCAD2010)根据骨缺损和肢体力线设计进行骨缺损模块的设计,根据骨缺损情况进行修复,获得高质量的数字化模型。(5)将获得的数字化模型数据以标准的物体STL模型输入到3D打印机(华中科大研制的HRPM-Ⅱ型SLM系统)中,将316L不锈钢粉末(粒径100μm)在球磨机(XQM-0.4L行星式球磨机)中进行混合均匀,磨转速为250r/min,球磨时间为30min,采用氮气作为保护气体,获得球磨后的不锈钢粉末,粒径为50μm~70μm。将球磨后的不锈钢粉末置于3D打印设备中,采用激光3D打印成型,激光的功率为150W,脉宽2ms,频率0.0Hz,离焦量2.5mm,光斑直径0.5mm,氩气或者真空保护气氛下打印,单层打印厚度0.04mm,获得的胚料置于电化学工作站(IviumStat)配有搅拌装置的电解槽中,电解槽内抛光液为体积比1:1:20的高氯酸、甘油和冰醋酸的混合液,在30V恒压模式,加液氮降温,搅拌速度150r/min的条件下进行电化学抛光操作,获得表面粗糙度在70μm左右的不锈钢植入体基体;分别采用无水酒精、丙酮、去离子水各自15分钟的超声清洗,进行不锈钢基体表面的脱油脱脂,室温下干燥,获得电化学抛光后的不锈钢植入体基体。(6)将Ca(NO3)2与无水乙醇混合制成Ca(NO3)2溶液,同时将P2O5和磷酸三乙酯与无水乙醇混合制成P2O5溶液,无水乙醇总体积用量为100ml。其中保证物质的量之比为Ca(NO3)2:P2O5:C3H5O3PO=10:2:1,配成Ca/P原子比=1.67的混合溶液。再将50mlCa(NO3)2溶液缓慢加入到50mlP2O5溶液中,并不断搅拌6小时,用氨水的缓冲溶液调节pH值至8.5,75℃回流18h,然后80℃静置反应2h形成溶胶;(7)将步骤(5)获得的电化学抛光后的不锈钢植入体基体放入步骤(6)的溶胶中,室温浸渍3min,利用提拉浸渍机(上海三研科技产SYDC-100型浸渍提拉镀膜机)以20mm/min的恒定速度垂直向上提拉成膜,再放入电热鼓风干燥箱中于75℃干燥1h,重复提拉、干燥操作5次,以得到较厚的涂层。然后放入电阻炉中,在氩气或真空保护气氛下,400℃保温30min,自然冷却;获得溶胶-凝胶处理后的不锈钢植入体基体。取出,用去离子水反复清洗,在23℃的烘箱中进行干燥,获得表面厚度10μm羟基磷灰石涂层的不锈钢植入体基体;(8)采用聚乳酸(PLA:polylacticacid,重均分子量为15万)作为生物高分子涂层进行不锈钢基体最外层的处理,即将PLA粉末加入到二氯甲烷(DCM:dichloromethane)中,室温均匀搅拌6小时,获得质量浓度2.5%聚乳酸溶液。(9)将步骤(7)的表面形成羟基磷灰石层的不锈钢植入体基体浸入步骤(8)的聚乳酸溶液中,室温浸泡25s后,在浸渍提拉机(上海三研科技产SYDC-100型浸渍提拉镀膜机)的作用下,以20mm/min的恒定速度下将样品提出,在通风厨内室温晾干,以去除二氯甲烷。然后去离子水洗净,室温晾干,在羟基磷灰石层表面形成8μm厚度的聚乳酸层,即可制得具有不锈钢植入体基体/羟基磷灰石层/聚乳酸层的不锈钢植入体复合材料。2、不锈钢植入体复合材料性能测试(1)电化学动极化测试对本实施例获得的不锈钢植入体复合材料在Hank溶液(组分为8g/LNaCl,0.4g/LKCl,0.25g/LNaH2PO4·H2O,0.35g/LNaHCO3,0.06g/LNa2HPO4·2H2O,0.19g/LMgCl2,0.19g/LCaCl2·2H2O,0.06g/LMgSO4·7H2O和1g/L葡萄糖,超纯水配制,pH7.8)中进行电化学动极化测试,采用设备为电化学工作站(IviumStat),其具体测试参数为:扫描速度为1mV·s-1,扫描范围为-2.0V到1.0V,制得不锈钢植入体复合材料作为工作电极,铂电极作对电极,饱和甘汞电极作为参比电极,在37℃温度下进行测试,以步骤(5)制备的不锈钢植入体基体为对照,测得的实验数据如下表1所示:表1.Hank溶液中极化曲线的分析结果样品Icorr(A/cm2)Ecorr(V)不锈钢基体1.98×10-6-0.28不锈钢植入体复合材料8.41×10-80.22由表1可以得到,本案例制备的不锈钢植入体复合材料的腐蚀电位从未进行处理前的-0.28V提升到0.22V。一般而言,一个更高的腐蚀电位表明其具有更好的耐腐蚀性能,因此,本案例制备的不锈钢植入体复合材料显著提升了不锈钢基体的耐腐蚀性能。从腐蚀电流密度可以看出处理后的基体的腐蚀电流密度降低了2~3个数量级,这表明本案例制备的不锈钢植入体复合材料有效地降低了基体的腐蚀速率。动极化测试结果可以说明,制备的不锈钢植入体复合材料可以有效提高不锈钢基体的耐腐蚀性能。(2)体外成骨细胞培养实验对本实施例获得的不锈钢植入体复合材料进行体外成骨细胞培养实验,以研究其生物活性:将从成年兔体内获取的成骨细胞用pH=7.5磷酸缓冲液清洗两遍,离心,收集细胞沉淀,将细胞沉淀接种至DMEM培养液中,在标准的培养环境下培养(5%CO2,37℃)1周,收集细胞沉淀用pH=7.5磷酸缓冲液配制成5×105/ml成骨细胞悬液。将步骤(5)制备的不锈钢植入体基体和步骤(9)制备的不锈钢植入体复合材料分别在110℃水蒸汽中灭菌40分钟,然后分别置于六孔板中,加入设定密度为5×105/ml成骨细胞悬液1ml,再加入含有10%胎牛血清(FBS)的DMEM培养基10ml,5%CO2,37℃培养24h,之后用pH=7.5磷酸缓冲溶液洗板三次移除未附着的细胞,然后加入0.5ml消化液(胰酶-EDTA)消化,再加入0.5ml的标准消化液(胰酶抑制剂)终止消化,制成细胞悬液,用Z2型细胞粒度计数仪进行细胞计数。其计数结果如下表2所示:表2.成骨细胞24小时培养后各组的细胞计数样品附着细胞数目不锈钢基体34000±1000不锈钢植入体复合材料42000±1000由表2可得本案例制得的不锈钢植入体复合材料具有更多的附着成骨细胞,这表明制备的不锈钢植入体复合材料具有更好的促进骨细胞生长能力,有效地提高了不锈钢基体材料的生物活性。实施例2步骤(1)~(4)与实施例1中的条件相同;步骤(5)将实施例1步骤(5)中激光的功率改为100W,脉宽1ms,离焦量2mm,其余条件不变;步骤(6)将实施例1步骤(6)中的pH值改为8,静置反应时间改为3h,其余条件不变;步骤(7)将实施例1步骤(7)中的浸渍时间改为3min,提拉速度改为15mm/min,退火温度改为400℃,其余条件不变;步骤(8)与实施例1中步骤(8)的条件相同;步骤(9)将实施例1步骤(9)中的浸泡时间改为20s,提升速度改为以15mm/min的恒定速度,其余条件不变。获得羟基磷灰石层厚度为5μm,聚乳酸层厚度为5μm的不锈钢植入体复合材料。实施例3步骤(1)~(4)与实施例1中的条件相同;步骤(5)将实施例1步骤(5)中激光的功率改为200W,脉宽3ms,离焦量3mm,其余条件不变;步骤(6)将实施例1步骤(6)中的pH值改为9,静置反应时间改为4h,其余条件不变;步骤(7)将实施例1步骤(7)中的的浸渍时间改为4min,提拉速度改为25mm/min,退火温度改为500℃,其余条件不变;步骤(8)与实施例1中步骤(8)的条件相同;步骤(9)将实施例1步骤(9)中的浸泡时间改为30s,提升速度改为以25mm/min的恒定速度,其余条件不变。获得羟基磷灰石层厚度为15μm,聚乳酸层厚度为10μm的不锈钢植入体复合材料。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1