相关申请
本申请要求于2015年4月10日提交的美国临时申请号no.62/146,205的优先权。本申请的全部内容通过引用并入本文。
背景技术:
在自身免疫和肿瘤性疾病的情况下,免疫系统的细胞在区分外源和自身抗原中发挥核心作用。胸腺(中枢)耐受的过程为免疫细胞在两种疾病状态之间赋予体内平衡提供了基础。一方面,从系统中消除高亲和力的自身抗原特异性的t细胞,导致自身免疫的预防。另一方面,不能完全地识别自身抗原的细胞也被消除,和这确保了肿瘤细胞被控制。这种复杂过程的结果是只有识别具有中等亲和力的自身抗原的t细胞被幸免并允许繁殖。外周耐受的这种发展对于保护潜在自身反应性的淋巴细胞在控制中是关键的,因为在非炎症状况下暴露于组织抗原的再循环淋巴细胞通常处于耐受的无能性状态。然而,在存在诸如由感染和组织损伤引起的那些的危险刺激的情况下,耐受性和自身免疫之间的平衡可能被破坏。相反,如果自身反应性细胞从免疫组库中耗尽,则免疫系统可能无法识别表达改变水平或模式的自身抗原的肿瘤。
现在已经认识到许多自身免疫性疾病是由自身反应性t细胞反应介导的。例如,在1型糖尿病的情况中,自身反应性t细胞已经涉及胰腺β细胞的破坏。同样地,多发性硬化的病理生理学通常以自身反应性t细胞介导的神经元细胞的靶向和凋亡为特征。然而,自身免疫性疾病的适当诊断和鉴定充满困难,因为它们通常需要进行许多实验室检查(通常涉及完全血细胞计数、综合代谢组检查、急性期反应物、免疫学研究、血清学、流式细胞术、细胞因子分析和hla分型)。这些测试的施用是麻烦的和昂贵的。
在细胞水平上,基于免疫细胞核型分析诊断自身免疫性疾病也类似地存在问题,因为缺乏对于组织破坏部位的功能性t细胞的可及性。在许多疾病中,自身反应性细胞发生在如此低的频率(1:100,000细胞)下以至于特异性免疫细胞的检测在技术上是具有挑战性的。此外,在许多情况下,自身反应性细胞的群体不一定是疾病特异性的。即使疾病特异性t细胞被分离,它们在诊断或治疗应用中的用途有限,因为它们不能在不影响其功能性能力的情况下被冷冻或培养。
类似地,在癌症的背景下,现有的治疗策略通常涉及从宿主中提取的抗原特异性t细胞的过继转移。在这些情况下,从肿瘤活检或外周血中提取肿瘤浸润性白细胞(tils),进行操作以增加抗原特异性或归巢能力,离体扩增,并注射入患者中以靶向肿瘤细胞。然而,这些细胞在血液或病变部位中的量通常是低频率的,并且缺乏理想的功能性。
因此,未满足对于允许分离可以被分析而用于诊断自身免疫性疾病和癌症的免疫细胞,以及用于治疗人类疾病,例如自身免疫性疾病、癌症和感染性疾病的组合物和方法的需要。下面详细描述的本发明的实施方式满足了这些需求。
技术实现要素:
本发明提供了对于鉴定和收集稀有细胞或在身体中以低频出现的细胞的问题的解决方案。本文描述的特定实施方式涉及可用于收集这些细胞的收集装置、细胞捕获装置。所述装置包括支架组合物,其掺入或涂覆有多种抗原以及任选的募集剂,从而允许该装置吸引、粘附于和捕获或隔离靶细胞如免疫细胞。该装置通过包括与抗原、募集剂或其中存在的其它分子的直接或间接相互作用的各种方法来执行这些功能。根据该装置所使用的应用,该装置通过支架本身的物理或化学特性来调节靶细胞的捕获和存活。例如,支架组合物是差异渗透性的,仅允许细胞在支架的某些物理区域中通过。例如通过选择或加工材料以具有更大或更小的孔径、密度、聚合物交联、刚度、韧性、延展性或粘弹性,支架组合物的渗透性被调节。支架组合物可以包含物理通道或路径,目标细胞通过其与装置相互作用和/或移动到装置的特定隔室或区域中。为了便于区室化,该支架组合物任选地被组织在各自具有不同渗透性的隔室或层中,使得细胞被分选或过滤以允许仅接近某些细胞亚群。装置中靶细胞群体的隔离也可以通过降解、脱水或复水、氧合、化学或ph变化或者支架组合物的持续自组装来调节。在捕获之后,靶细胞,例如免疫细胞可以借助于装置中存在的刺激性分子、细胞因子和其它辅因子使得在装置内生长或扩增。在一些实施方式中,可以使用负向选择剂排除或去除否则渗透该装置的非靶细胞。
被捕获在本发明的装置内的细胞主要是免疫细胞。在某些实施方式中,本发明涉及t-细胞捕获器(traps)。在其它的实施方式中,本发明涉及b-细胞捕获器。然而在其它的实施方式中,本发明涉及捕获器的组合,例如t-细胞捕获器和b-细胞捕获器的组合。本文所描述的捕获器还可以被配置为捕获抗原呈递细胞(apc),例如自身反应性apc。可能被捕获的自身反应性apc的实例包括例如树突状细胞(dc)、巨噬细胞或其组合。在其他实施方式中,可以采用多种捕获器,例如被配置用于捕获淋巴细胞和apc两者的捕获器。例如,可以单独地或一起捕获抗原特异性细胞或疾病特异性细胞例如t细胞、树突状细胞(dc)或巨噬细胞,用于分析、重编程或耗尽。被捕获的免疫细胞,例如淋巴细胞和apc,任选地被收获和分析以鉴定和表征用于疾病诊断或免疫治疗的靶标。被捕获的细胞也可以被重新编程或被扩增以用于开发用于治疗中的组合物或制剂。
因此,一方面,本发明提供了一种免疫细胞捕获装置,其包含生理上相容的多孔聚合物支架和多种纯化的抗原,其中所述多种抗原吸引并捕获对于该装置中的所述多种抗原特异性的多种免疫细胞。该抗原可以被吸收至聚合物支架上或被聚合物支架包封。
另一方面,本发明提供了一种免疫细胞捕获装置,其包含生理上相容的多孔聚合物支架和多种纯化的抗原,其中所述多种抗原通过结合于该多种免疫细胞而吸引并捕获对于该装置中的所述多种抗原特异性的多种免疫细胞。
另一方面,本发明提供了一种免疫细胞捕获装置,其包含生理上相容的多孔聚合物支架和多种纯化的抗原,其中所述多种抗原吸引并捕获对于该装置中的所述多种抗原特异性的多种免疫细胞,且该装置中不包含杀死或者消除免疫细胞的试剂。
而另一方面,本发明提供了一种免疫细胞捕获装置,其包含生理上相容的多孔聚合物支架和多种纯化的抗原,其中所述多种抗原吸引并捕获对于该装置中的所述多种抗原特异性的多种免疫细胞且该装置还包含免疫细胞募集剂。所述免疫细胞募集剂可以是,例如,t细胞募集剂、树突状细胞募集剂和巨噬细胞募集剂或其组合。特别地,所述免疫细胞募集剂可以是自然杀伤(nk)细胞募集剂、cd3+t细胞募集剂、cd4+t细胞募集剂、cd8+t细胞募集剂、cd8+t细胞募集剂、调节性t细胞(treg)募集剂或其组合。在相关的方面,所述免疫细胞募集剂可以是生长因子、细胞因子、白细胞介素、粘附信号分子、整联蛋白信号分子、干扰素、淋巴因子或趋化因子或者其片段或其组合。特别地,所述免疫细胞募集剂可以是选自于il-1、il-2、il-4、il-5、il-10、il-12和il-17中的白细胞介素。
另一方面,本发明提供了一种免疫细胞捕获装置,其包含生理上相容的多孔聚合物支架和多种纯化的抗原,其中所述多种抗原吸引并捕获对于该装置中的所述多种抗原特异性的多种免疫细胞且该装置包含增强免疫细胞渗透到所述装置中的试剂。
另一方面,本发明提供了一种免疫细胞捕获装置,其包含生理上相容的多孔聚合物支架和多种纯化的癌症抗原,其中所述多种癌症抗原吸引并捕获对于该装置中的多种癌症抗原特异性的多种免疫细胞。根据该方面,该癌症抗原可以选自于mage-1、mage-2、mage-3、cea、酪氨酸酶、中期因子(midkin)、bage、casp-8、β-连环蛋白、β-连环蛋白、γ-连环蛋白、ca-125、cdk-1、cdk4、eso-1、gp75、gp100、mart-1、muc-1、mum-1、p53、pap、psa、psma、ras、trp-1、her-2、trp-1、trp-2、il13rα、il13rα2、aim-2、aim-3、ny-eso-1、c9orf112、sart1、sart2、sart3、brap、rtn4、glea2、tnks2、kiaa0376、ing4、hsph1、c13orf24、rbpsuh、c6orf153、nktr、nsep1、u2af1l、cynl2、tpr、sox2、golga、bmi1、cox-2、egfrviii、ezh2、licam、livin、livinβ、mrp-3、巢蛋白(nestin)、olig2、art1、art4、b-细胞周期蛋白、gli1、cav-1、组织蛋白酶b、cd74、e-钙粘蛋白、epha2/eck、fra-1/fosl1、gage-1、神经节苷脂/gd2、gnt-v、β1,6-n、ki67、ku70/80、prox1、psca、sox10、sox11、存活素、upar、wt-1、二肽基肽酶iv(dppiv)、腺苷脱氨酶结合蛋白(adabp)、亲环蛋白b、结肠直肠相关抗原(crc)-c017-1a/ga733、t细胞受体/cd3-ζ链、肿瘤抗原gage家族、rage、lage-i、nag、gnt-v、rcasl、α-胎蛋白、pl20ctn、pmel117、prame、脑糖原磷酸化酶、ssx-i、ssx-2(hom-mel-40)、ssx-i、ssx-4、ssx-5、scp-i、ct-7、cdc27、腺瘤性结肠息肉病蛋白(apc)、胞衬蛋白(fodrin)、pla、连接蛋白37、ig-个体遗传型、pl5、gm2、gd2神经节苷脂、肿瘤抗原smad家族、lmp-1、ebv-编码的核抗原(ebna)-i、ul16-结合蛋白样转录物1(mult1)、rae-1蛋白、h60、mica、micb和c-erbb-2或其免疫原性肽,及其组合。
另一方面,本发明提供了一种免疫细胞捕获装置,其包含生理上相容的多孔聚合物支架和多种纯化的非自身抗原,其中所述多种非自身抗原吸引并捕获对于装置中的多种非自身抗原特异性的多种免疫细胞。根据该方面,该非自身抗原可以是源自病原体的病原性抗原,其中所述病原体选自于病毒、细菌、原生动物、寄生虫和真菌。此外,根据该方面,所述病原体可以选自于牛型结核分枝杆菌(mycobacteriumbovis)、人乳头瘤病毒(hpv)、人免疫缺陷病毒、痘病毒、天花病毒、埃博拉病毒、马尔堡病毒、登革热病毒、流感病毒、副流感病毒、呼吸道合胞病毒、麻疹病毒、水痘带状疱疹病毒、单纯疱疹病毒、巨细胞病毒、爱泼斯坦-巴尔病毒(epstein-barrvirus)、jc病毒、棒状病毒、轮状病毒、鼻病毒、腺病毒、乳头瘤病毒、细小病毒、细小核糖核酸病毒、脊髓灰质炎病毒、导致腮腺炎的病毒、引起狂犬病的病毒、呼肠孤病毒、风疹病毒、披膜病毒、正粘病毒、逆转录病毒、嗜肝dna病毒、柯萨奇病毒、马脑炎病毒、日本脑炎病毒、黄热病毒、裂谷热病毒、甲型肝炎病毒、乙型肝炎病毒、丙型肝炎病毒、丁型肝炎病毒、戊型肝炎病毒、sars冠状病毒、mers冠状病毒、肠病毒、包柔氏螺旋体种、炭疽芽孢杆菌、伯氏疏螺旋体、百日咳博德特氏菌、空肠弯曲杆菌、衣原体属的种、鹦鹉热衣原体、沙眼衣原体、梭菌属的种、破伤风杆菌、肉毒杆菌、产气荚膜梭菌、白喉棒状杆菌、柯克斯体属的种、肠球菌属的种、埃利希氏体属的种、大肠杆菌、土拉热弗朗西丝菌、嗜血杆菌属的种、流感嗜血杆菌、副流感嗜血杆菌、乳杆菌属的种、军团杆菌属的种、嗜肺军团菌、问号钩端螺旋体、李斯特菌属的种、单核细胞增生利斯特氏菌、分枝杆菌属的种、结核分枝杆菌、麻风分枝杆菌、支原体属的种、肺炎支原体、奈瑟氏菌属的种、脑膜炎奈瑟氏菌、淋病奈瑟氏菌、肺炎球菌属的种、假单胞菌属的种、铜绿假单胞菌、沙门氏菌属的种、伤寒沙门氏菌、肠道沙门氏菌、立克次体属的种、rickettsiaricketsii、斑疹伤寒立克次体、志贺氏菌属的种、葡萄球菌属的种、金黄色葡萄球菌、链球菌属的种、肺炎链球菌、酿脓链球菌、变形链球菌、密螺旋体属的种、苍白密螺旋体、弧菌属的种、霍乱弧菌、鼠疫耶尔森氏菌、耐甲氧西林金黄色葡萄球菌、曲霉菌属的种、烟曲霉、黄曲霉、棒曲霉、念球菌属的种、白色念珠菌、热带念珠菌、隐球菌属的种、新型隐球菌、溶组织内阿米巴、荚膜组织胞浆菌、利什曼原虫属的种、星形诺卡氏菌、恶性疟原虫、黑葡萄穗霉(stachybotryschartarum)、刚地弓形虫、阴道毛滴虫、弓形虫种、布鲁斯锥虫、曼氏血吸虫、镰刀菌属的种、毛癣菌属的种、疟原虫属的种、弓浆虫种、内阿米巴属的种、巴贝虫属的种、锥虫属的种、leshmania种、肺孢子虫属的种、耶氏肺孢子虫、毛滴虫属的种、贾第虫属的种、裂体吸虫属(schisostoma)的种、隐孢子虫属的种、疟原虫属的种、内阿米巴属的种、纳氏虫属的种、棘阿米巴属的种、巴拉姆希阿米巴(balamuthia)种、弓形虫属的种、贾第虫属的种、毛滴虫属的种、利什曼原虫属的种和锥虫属的种。
另一方面,本发明提供了一种免疫细胞捕获装置,其包含生理上相容的多孔聚合物支架和多种纯化的自身抗原,其中所述多种自身抗原吸引并捕获对于装置中的所述多种自身抗原特异性的多种免疫细胞。根据该方面,该自身抗原可以源自自身免疫反应所针对的细胞的裂解物。此外,根据该方面,所述抗原可以是胰β细胞抗原、神经元细胞抗原、骨或关节相关的自身免疫疾病相关抗原或胃肠道疾病相关抗原。再此外,根据该方面,该抗原可以是与i型糖尿病相关的抗原;与多发性硬化相关的抗原;与类风湿关节炎相关的抗原;与炎性肠病相关的抗原;或与克罗恩病相关的抗原。
另一方面,本发明提供了一种免疫细胞捕获装置,其包含生理上相容的多孔聚合物支架、多种纯化的抗原和另一种试剂,该试剂是rgd肽、cpg寡核苷酸或粒细胞-巨噬细胞集落刺激因子(gm-csf)细胞因子或者其片段或其组合,其中所述多种抗原吸引并捕获对于所述装置中的所述多种抗原特异性的多种免疫细胞。在另一方面,本发明提供了一种免疫细胞捕获装置,其包含生理上相容的多孔聚合物支架和多种纯化的抗原,但该装置不含有rgd肽、cpg寡核苷酸或粒细胞-巨噬细胞集落刺激因子(gm-csf)细胞因子或者其片段或其组合。
另一方面,本发明提供了一种免疫细胞捕获装置,与其他免疫细胞相比,其优先吸引t细胞。根据该方面,该装置包含生理上相容的多孔聚合物支架和多种纯化的抗原,其中所述多种抗原吸引并捕获对于在所述装置中的所述多种抗原特异性的多种免疫细胞,且所述装置还包含趋化因子,其选自于ccl1、ccl2(mcp-1)、ccl-3、ccl-4、ccl-5(rantes)、ccl-17、ccl-22、cxcl12和xcl1或者其片段或其组合。再此外,根据该方面,所述趋化因子可以选自于以下:
(a)ccl1(人类同源物的登录号:nm_002981.2;gi:523498696,和小鼠同源物的登录号:nm_011329;gi:257153404),
(b)ccl2(mcp-1)(人类同源物的登录号:nm_002982.3;gi:56119169,和小鼠同源物的登录号:nm_011333.3;gi:141803162),
(c)ccl3(人类同源物的登录号:nm_002983.2;gi:121582465,和小鼠同源物的登录号:nm011337.2;gi:126432552),
(d)ccl4(人类同源物的登录号:nm002984.3;gi:748585189nm013652.2,和小鼠同源物的登录号:nm_013652.2;gi:126366031),
(e)ccl5(rantes)(人类同源物的登录号:nm_002985.2;gi:22538813,和小鼠同源物的登录号:nm_013653.3;gi:164698427),
(f)ccl17(人类同源物的登录号:nm_002987.2;gi:22538801和nm_011332.3;小鼠同源物的登录号:nm_011332.3;gi:225735578),
(g)ccl19(人类同源物的登录号:nm_006274.2;gi:22165424,和小鼠同源物的登录号:nm011888.2;gi:10518345),
(h)ccl22(人类同源物的登录号:nm_002990.4;gi:300360575,和小鼠同源物的登录号:nm_009137.2;gi:154240695),
(i)cxcl12(人类同源物的登录号:nm_199168.3;gi:291045298,和小鼠同源物的登录号:nm_001277990.1;gi:489406389),和
(j)xcl1(人类同源物的登录号:nm_002995.2;gi:312434026,和小鼠同源物的登录号:nm_008510.1;gi:6678711)。
另一方面,本发明提供了一种与其他免疫细胞相比优先吸引树突状细胞(dc)的免疫细胞捕获装置。根据该方面,该装置包含生理上相容的多孔聚合物支架和多种纯化的抗原,其中所述多种抗原吸引并捕获对于在所述装置中的所述多种抗原特异性的多种免疫细胞,并且所述装置还包含趋化因子,其选自于ccl2、ccl3、ccl5、ccl7、ccl8、ccl13、ccl17和ccl22或者其片段或其组合。再此外,根据该方面,所述趋化因子可以选自于以下:
(a)ccl2(人类同源物的登录号:nm_002982.3;gi:56119169,和小鼠同源物的登录号:nm_011333.3;gi:141803162),
(b)ccl3(人类同源物的登录号:nm_002983.2;gi:121582465,和小鼠同源物的登录号:nm_011337.2;gi:126432552),
(c)ccl5(变体1)(人类同源物的登录号:nm_002985.2;gi:22538813,和小鼠同源物的登录号:nm_013653.3;gi:164698427),
(d)ccl7(人类同源物的登录号:nm_006273.3;gi:428673540,和小鼠同源物的登录号:nm_013654.3;gi:226958664),
(e)ccl8(人类同源物的登录号:nm_005623.2;gi:22538815,和小鼠同源物的登录号:nm_021443.3;gi:255708468),
(f)ccl13(人类同源物的登录号:nm_005408.2;gi:22538799,和小鼠同源物的登录号:nm_011333.3;gi:141803162),
(g)ccl17(人类同源物的登录号:nm_002987.2;gi:22538801,和小鼠同源物的登录号:nm_011332.3;gi:225735578),和
(h)ccl22(人类同源物登录号:nm_002990.4;gi:300360575,和小鼠同源物登录号:nm_009137.2;gi:154240695)。
另一方面,本发明提供了免疫细胞捕获装置,与其他免疫细胞相比,其优先吸引t细胞和树突状细胞(dc)。根据该方面,该装置包含生理上相容的多孔聚合物支架和多种纯化的抗原,其中所述多种抗原吸引并捕获对于在所述装置中的所述多种抗原特异性的多种免疫细胞,并且所述装置还包含选自ccl17和ccl22或者其片段或其组合的趋化因子。再此外,根据该方面,所述趋化因子可以选自以下:
(a)ccl17(人类同源物的登录号:nm_002987.2;gi:22538801,和小鼠同源物的登录号:nm_011332.3;gi:225735578),和
(b)ccl22(人类同源物的登录号:nm_002990.4;gi:300360575,和小鼠同源物的登录号:nm_009137.2;gi:154240695)。
而在另一方面,本发明提供了一种免疫细胞捕获装置,其包含生理上相容的多孔聚合物支架、多种纯化的抗原和多种粘附受体,其中所述多种抗原吸引并捕获对于装置中的多种抗原特异性的多种免疫细胞。根据该方面,该粘附受体可以是选自于lfa-1、madcam-1、vcam-1、cd28和ctla-4或者其片段或其组合的t细胞的粘附受体。再此外,根据该方面,所述粘附受体可以选自于以下:
(a)lfa(人类同源物的登录号:nm_000211.4;gi:735367774,和小鼠同源物的登录号:m60778.1;gi:198785),
(b)madcam-1(人类同源物登录号:nm_130760.2;gi:109633021,和小鼠同源物登录号:d50434.2;gi:60391311),
(c)vcam-1(人类同源物的登录号:nm_001078.3;gi:315434269,和小鼠同源物的登录号:x67783.1;gi:298116),
(d)cd28(人类同源物的登录号:nm_006139.3;gi:340545506,和小鼠同源物登录号:bc064058.1;gi:39850201),和
(e)ctla-4(人类同源物的登录号:nm_005214.4;gi:339276048,和小鼠同源物的登录号:u90270.1;gi:4099836)。
另一方面,本发明提供了一种免疫细胞捕获装置,其包含生理上相容的多孔聚合物支架和多种纯化的抗原,其中所述多种抗原吸引并捕获对于在该装置中的多种抗原特异性的多种免疫细胞,和该装置包含约10μg至约2.0mg的抗原。
另一方面,本发明提供了一种免疫细胞捕获装置,其包含生理上相容的多孔聚合物支架和多种纯化的抗原,其中所述多种抗原吸引并捕获对于装置中的多种抗原特异性的多种免疫细胞,和该装置包含每克干重支架约0.1μg至约400μg的所述抗原。
另一方面,本发明提供了一种免疫细胞捕获装置,其包含生理上相容的多孔聚合物支架和多种纯化的抗原,其中所述多种抗原吸引并捕获对于装置中的多种抗原特异性的多种免疫细胞,和该装置具有介于约40%至约90%之间的孔隙率。
另一方面,本发明提供了一种免疫细胞捕获装置,其包含具有直径约10μm至约500μm的孔隙的生理上相容的多孔聚合物支架和多种纯化的抗原,其中所述多种抗原吸引并捕获对于在该装置中的多种抗原特异性的多种免疫细胞。
另一方面,本发明提供了一种免疫细胞捕获装置,其包含生理上相容的多孔聚合物支架和多种纯化的抗原,其中所述多孔聚合物支架含有选自于聚乳酸(pla)、聚乙醇酸(pga)、聚(丙交酯-共-乙交酯)(plga)、藻酸盐或其衍生物、明胶、胶原蛋白、纤维蛋白、透明质酸(ha)、琼脂糖、多糖、聚氨基酸、多肽、聚酯、聚酐、聚磷腈、聚乙烯醇(pva)、聚环氧烷(pao)、聚丙烯酸胺(pam)、聚丙烯酸酯、改性苯乙烯聚合物、pluronic多元醇、polyoxamer、聚糖醛酸和聚乙烯吡咯烷酮或其共聚物或其接枝聚合物的化合物,其中所述多种抗原吸引并捕获对于在所述装置中的所述多种抗原特异性的多种免疫细胞。
又另一方面,本发明提供了包含免疫细胞捕获装置和药学上可接受的载体的药物组合物,其中所述装置包含生理上相容的多孔聚合物支架和多种纯化的抗原,其中所述多种抗原吸引并捕获对于在该装置中的多种抗原特异性的多种免疫细胞。根据该方面,该药物组合物可以被配制用于静脉内施用、皮下施用、腹膜内施用或肌肉内施用。此外,根据该方面,该药物组合物可以被配制成作为微针贴片用于皮下施用。
另一方面,本发明提供了一种用于治疗有此需要的受试者的疾病的方法,包括向所述受试者施用免疫细胞捕获装置,其中所述装置包含生理上相容的多孔聚合物支架和多种纯化的对该疾病特异性的抗原,其中所述多种抗原吸引并捕获对于所述装置中的所述多种抗原特异性的多种免疫细胞;收集捕获在装置中的多种免疫细胞;以及将所述多种免疫细胞施用于受试者,从而治疗受试者的疾病。根据该方面,可以通过从受试者中移植出(explant)该装置来收集免疫细胞。此外,根据该方面,该治疗方法可以包括扩增多种免疫细胞,从而产生对疾病特异性的免疫细胞的扩增群体;并将该扩增的免疫细胞群体施用于受试者。根据该方面,待治疗的受试者优选为人类受试者。此外,根据该方面的方法可以包含将该装置皮下或静脉内施用于受试者。在治疗方面的一个实施方式中,在将该装置施用于受试者后约1天至约60天收集多种免疫细胞。
在相关的方面,本发明提供了一种在有需要的受试者中治疗癌症的方法,包括向所述受试者施用免疫细胞捕获装置,其中所述装置包含生理上相容的多孔聚合物支架以及多种纯化的对于该癌症特异性的抗原,其中所述多种癌症抗原吸引并捕获对于癌症抗原特异性的多种免疫细胞;收集被捕获在装置中的多种免疫细胞;以及将所述多种免疫细胞施用于所述受试者中,从而治疗所述受试者的癌症。根据该方面,该方法可以用于治疗癌症,所述癌症选自于头颈癌、乳腺癌、胰腺癌、前列腺癌、肾癌、食管癌、骨癌、睾丸癌、子宫颈癌、胃肠癌、胶质母细胞瘤、白血病、淋巴瘤、套细胞淋巴瘤、肺中的肿瘤前病变、结肠癌、黑素瘤和膀胱癌。根据该方面,待治疗的受试者优选为人类受试者。
在另一相关方面,本发明提供了在有需要的受试者中治疗自身免疫性疾病的方法,包括对所述受试者施用免疫细胞捕获装置,其中所述装置包含生理上相容的多孔聚合物支架,和对自身免疫性疾病特异性的多种纯化抗原,其中对所述自身免疫性疾病特异性的多种抗原吸引并捕获对该抗原特异性的多种免疫细胞;收集被捕获在装置中的多种免疫细胞;以及将多种免疫细胞施用于受试者,从而治疗受试者的自身免疫性疾病。根据该方面,该方法可以用于治疗自身免疫性疾病,所述自身免疫性疾病选自i型糖尿病、多发性硬化、类风湿性关节炎、炎性肠病和克罗恩病。仍然根据这个方面,被捕获的免疫细胞可以包括调节性或抑制性t细胞。根据该方面,待治疗的受试者优选为人类受试者。
在另一个相关方面,本发明提供了一种在有需要的受试者中治疗病原体性疾病(pathogenicdisease)的方法,包括向所述受试者施用免疫细胞捕获装置,其中所述装置包含生理上相容的多孔聚合物支架,和针对病原体性疾病特异性的多种纯化抗原,其中所述多种抗原吸引并捕获针对所述病原体性疾病特异性抗原特异性的多种免疫细胞;收集捕获在装置中的多种免疫细胞;以及将所述多种免疫细胞施用于所述受试者,从而治疗所述受试者的病原体性疾病。根据该方面,该病原体选自于病毒、细菌、原生动物、寄生虫和真菌。根据该方面,待治疗的受试者优选为人类受试者。
另一方面,本发明提供了用于获得对抗原特异性的免疫细胞的方法。该方法包括施用免疫细胞捕获装置,其包含生理上相容的多孔聚合物支架和多种纯化的抗原,其中所述多种抗原吸引并捕获对在施用于受试者的装置中的多种抗原特异性的多种免疫细胞;并收集捕获在该装置中的免疫细胞,从而获得对抗原特异性的免疫细胞。可以从受试者移植出该装置以收集免疫细胞。根据该方面,从其中获得免疫细胞的受试者优选为人类受试者。根据该方面,该装置可以被皮下或静脉内施用于受试者。仍然根据这个方面,可以在将该装置施用于受试者后约1天至约60天后收集多种免疫细胞。
另一方面,本发明提供了用于确定受试者是否具有自身免疫性疾病的方法。所述方法包括施用免疫细胞捕获装置到受试者中,其中所述装置包含生理上相容的多孔聚合物支架和对自身免疫性疾病特异性的多种纯化的抗原,其中所述多种抗原吸引并捕获对于装置中的多种抗原特异性的多种免疫细胞;收集捕获在所述装置中的免疫细胞,其中所述免疫细胞对自身免疫性疾病是特异性的;以及测定被捕获在所述装置中的对于自身免疫性疾病特异性的免疫细胞的数量,从而确定受试者是否具有自身免疫性疾病。可以从受试者移植出该装置以收集免疫细胞。根据该方面,从其中获得免疫细胞的受试者优选为人类受试者。根据该方面,该装置可以皮下或静脉内施用于受试者。仍然根据这个方面,可以在将该装置施用于受试者后约1天至约60天收集多种免疫细胞。
在另一方面,本发明提供了一种用于制备免疫细胞捕获装置的方法,所述免疫细胞捕获装置包含生理上相容的多孔聚合物支架和多种纯化的抗原,其中所述多种抗原吸引并捕获对于装置中的多种抗原特异性的多种免疫细胞。该方法包括将多种纯化的抗原与生理上相容的聚合物一起孵育以产生聚合物-抗原混合物;将该聚合物-抗原混合物冷冻、冻干和与致孔剂混合;将混合物模压成型以产生圆盘;使该圆盘经受高压co2环境并迅速降低压力以膨胀该聚合物和将该聚合物融合成互连的支架结构;和通过将该结构浸入水中以从支架结构中浸出致孔剂以产生多孔制品,从而制造该装置。根据该方面,该聚合物可以包括丙交酯和乙交酯的共聚物(plg)或藻酸盐。进一步根据这个方面,该致孔剂是nacl或蔗糖。
从以下对本发明的优选实施方式的描述和从权利要求书中,本发明的其它特征和优点将变得显而易见。引用的参考文献通过引用并入本文。
附图说明
可以充分明白本文所描述的实施方式的各种特征和优点,因为当根据附图考虑时可以更好地理解本文所描述的实施方式:
图1a是显示基于plg的t细胞捕获器的表面微计算机断层摄影和横截面sem图像的照片。
图1b是显示来自ova-t细胞捕获器的作为模型抗原的卵清蛋白(ova)蛋白质的累积释放的线图。
图1c是显示在小鼠背部皮下植入的捕获器位点处14天的mip-1a和rantes的局部细胞因子浓度的条形图。b和c中的值表示平均值和标准偏差(n=5)。图1a-c显示了模型t细胞捕获器的表征。
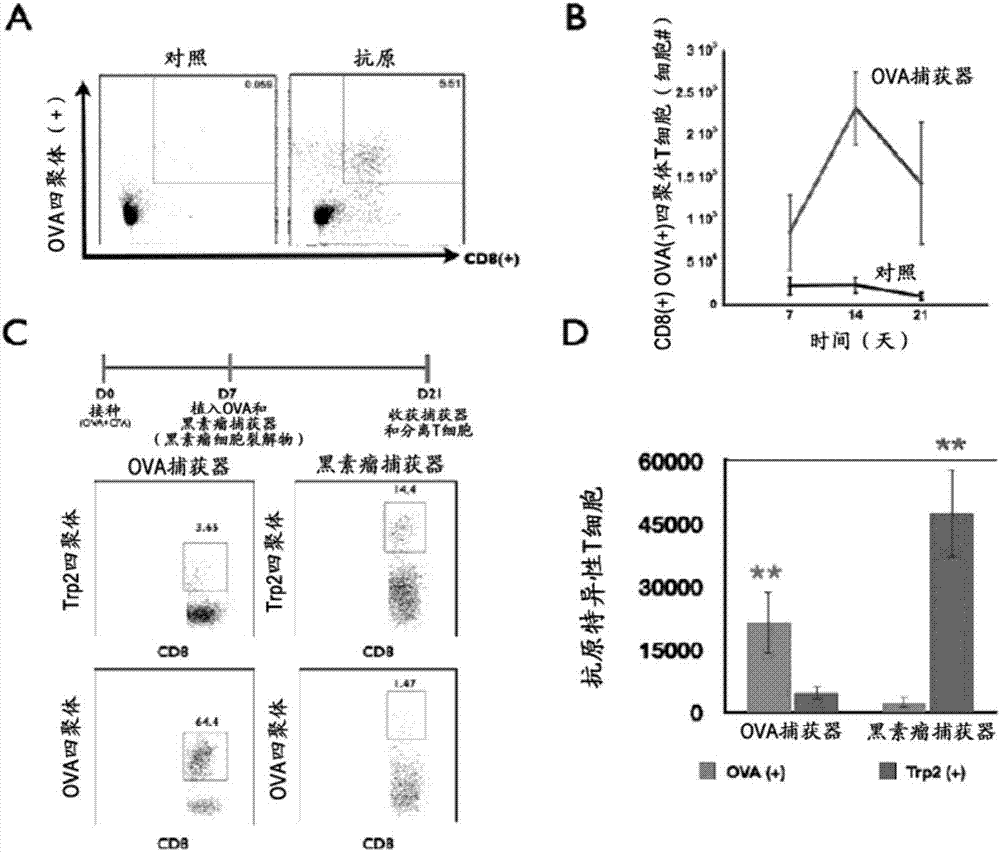
图2a是从对照(对照)和卵清蛋白(ova;抗原)加载的捕获器分离的细胞的一系列荧光激活细胞分选(facs)图。细胞用抗cd8和ovai类四聚体染色。门(gates)表示ova特异性的,cd8(+)t细胞且数字提供阳性细胞的百分比。将捕获器植入ot-1小鼠中14天。
图2b是显示在捕获器(ov捕获器)和对照(对照)中累积的cd8(+)ova四聚体(+)t细胞的动力学的线图。将支架植入ot-1小鼠中7、14和28周。
图2c是一系列facs图。在第7天(d7)向在第0天(d0)用cfa-ova接种的小鼠植入含有ova(ova捕获器)和黑素瘤细胞裂解物(黑素瘤捕获器)的捕获器,然后在第21天(d21)分析该捕获器。从ova和黑素瘤捕获器中分离并分选cd3(+)t细胞,和用抗cd8、trp2四聚体和ova四聚体染色。facs图中的门代表ova或trp2四聚体染色阳性的cd8(+)t细胞,且数字表示所指示的cd8t细胞的百分比。
图2d是显示从ova捕获器和黑素瘤捕获器分离的ova特异性和trp2特异性t细胞数量的柱状图。b和d中的值表示平均值和标准偏差(n=5)。**p<0.01。图2a-d表明捕获器可用于通过抗原定向归巢(antigendirectedhoming)区分t细胞。
图3a是显示来自加载有胰腺β细胞裂解物抗原的捕获器的蛋白质累积释放的线图。
图3b是表示t细胞捕获器植入期间nod小鼠胰岛中的t细胞浸润程度的示意图。当nod小鼠在9、12和15周龄时植入捕获器,并在2周后测定。
图3c是一系列facs直方图,其显示从11、14和17周龄nod小鼠分离的对照(实心蓝色)和β-细胞捕获器(空心红线)收获的cd3(+)t细胞的水平。
图3d是显示从11、14和17周龄nod小鼠移植的对照(对照)和-细胞加载的捕获器(捕获器)分离的cd3(+)细胞的总数量的线图。
图3e是显示分离自捕获器和对照的作为cd3(+)cd4(+)和cd3(+)cd8(+)t细胞的总细胞百分比的柱状图。a、d和e中的值表示平均值和标准偏差(n=5)。**p<0.01。这些图形表明在非肥胖糖尿病小鼠的糖尿病进展期间的t细胞捕获。
图4a是用从抗原加载的捕获器和对照收获的t细胞培养的β细胞靶标的il-2elispot分析结果的照片。t细胞在植入11、14和17周龄的nod小鼠中后14天收获。每个孔表示从单个小鼠收获的t细胞的反应。
图4b是显示从捕获器相对于脾提取的t细胞所产生的il-2阳性斑点数目(相对于1600个t细胞归一化)的比较的线图。斑点是在含有用来自抗原加载的捕获器(捕获器)、对照支架(对照)、植入捕获器的小鼠的脾脏(脾-捕获器)或植入对照支架的小鼠的脾(脾-对照)的t细胞培养的β细胞的孔中显影和定量。β细胞靶标被修饰以过表达mhci类h2(kd)(β-细胞i(d))或mhcii类i-a(g7)(β-细胞g7)。t细胞(仅t细胞)和β细胞(β-细胞)单独作为对照分析。b中的值代表平均值和标准偏差。这些图形表明,捕获器对于β细胞特异性t细胞的富集是有效的。
图5a是描绘cd3(+)t细胞渗透到空白(对照)和卵清蛋白加载(抗原)的捕获器中的柱状图。描绘cd8(+)ova四聚体(+)t细胞渗透空白(对照)和卵清蛋白加载(抗原)的捕获器的点图。门和数字表示从捕获器分离的ova(+)细胞毒性t细胞的百分比。
图5b是显示在空白(对照)和卵清蛋白加载(捕获器)的藻酸盐晶胶(cryogel)中捕获的cd3(+)t细胞的数量的柱状图。
图5c是显示在空白(对照)和抗原加载(捕获器)的藻酸盐晶胶中捕获的cd8(+)ova(+)t细胞的数量的柱状图。b和c中的值表示平均值和标准偏差(n=4)。*p<0.05。图5a-c中所示的数据证明了成功的t细胞捕获和保留在含有抗原诱饵的藻酸盐晶胶捕获器中。具有单独抗原的捕获器是足够的,并且将gm-csf和cpg作为佐剂添加到抗原中增强了t细胞渗透。
图6a-d显示体内癌症特异性t细胞的募集。
图6a显示了从对照(对照)和卵清蛋白加载(ova;抗原)的捕获器(其被植入ot-1小鼠中14天)分离的细胞的facs图。细胞用抗cd8和ovai类四聚体染色。门代表ova特异性的cd8(+)t细胞,和数字提供阳性细胞的百分比。
图6b显示了cd8(+)ova四聚体(+)t细胞在捕获器(ova捕获器)和对照(对照)中累积的动力学。将支架植入ot-1小鼠中7、14和28周。
图6c显示cd3(+)t细胞的facs分析。小鼠在第0天(d0),用cfa-ova接种,并在第7天(d7)植入含有ova(ova捕获器)和黑素瘤细胞裂解物(黑素瘤捕获器)的捕获器。然后在第21天(d21)分析捕获器。从ova和黑素瘤捕获器分离cd3(+)t细胞并分选,和用抗cd8、trp2四聚体和ova四聚体染色。facs图中的门代表对ova或trp2四聚体染色阳性的cd8(+)t细胞,和数字表示如所示的cd8t细胞的百分比。
图6d显示从ova捕获器和黑素瘤捕获器分离的ova特异性和trp2特异性t细胞的数目。b和d中的值表示平均值和标准偏差(n=5)。**p<0.01。
图7显示了从细胞捕获器转移后糖尿病发病率的动力学。15周龄的nod小鼠植入空白plg支架(对照)或含有β-细胞裂解物的支架(捕获器)。在17周时,将从对照和捕获器支架提取的2×106个细胞与来自未处理的nod小鼠的脾细胞(脾)一起静脉内注射到nod-scid小鼠中。每周监测小鼠中的血糖水平,并在连续两周记录高于250mg/dl的血糖水平后将小鼠考虑为有糖尿病(n=8或9)。
具体实施方式
本发明提供了鉴定和收集稀有细胞或在身体中以低频存在的细胞的问题的解决方案。本文描述的特定实施方式涉及可用于收集这些细胞的收集装置,例如细胞捕获器。该装置包含掺入或涂覆有多种抗原以及任选的募集剂的支架组合物,使得该装置能够吸引、粘附并捕获或隔离靶细胞。该装置通过包括与抗原、募集剂或其中存在的其它分子直接或间接相互作用的各种方法来执行这些功能。根据该装置所使用的应用,该装置通过支架本身的物理或化学特性来调节靶细胞的捕获和存活。例如,该支架组合物是差异渗透性的,其仅允许细胞在支架的某些物理区域中通过。例如通过选择或加工材料以具有更大或更小的孔径、密度、聚合物交联、刚度、韧性、延展性或粘弹性来调节支架组合物的渗透性。支架组合物可以包含物理通道或路径,目标细胞通过其与装置相互作用和/或移动到装置的特定隔室或区域中。为了便于区室化,支架组合物任选地被组织至各自具有不同渗透性的隔室或层中,使得细胞被分选或过滤以允许仅接近某些细胞亚群。装置中靶细胞群体的隔离也可以通过降解、脱水或复水、氧合、化学或ph变化或支架组合物的持续自组装来调节。在捕获之后,靶细胞可以允许借助于装置中存在的刺激性分子、细胞因子和其它辅因子在装置内生长或扩增。在其他情况下,可以使用负向选择剂排除或去除否则渗透该装置的非靶细胞。
被捕获在本发明的装置内的细胞主要是免疫细胞。在某些实施方式中,本发明涉及t-细胞捕获器。在其它的实施方式中,本发明涉及b-细胞捕获器。仍然在其它的实施方式中,本发明涉及捕获器的组合,例如,t-细胞捕获器和b-细胞捕获器的组合。本文所描述的捕获器还可以被配置为捕获抗原呈递细胞(apc),例如自身反应性apc。可能被捕获的自身反应性apc的实例包括例如树突状细胞(dc)、巨噬细胞或其组合。在其他实施方式中,可以采用多个捕获器,例如被配置为用于捕获淋巴细胞和apc的捕获器。例如,可以单独地或一起捕获抗原特异性细胞或疾病特异性细胞,例如t细胞、树突状细胞(dc)或巨噬细胞,用于分析、重编程或耗尽。被捕获的免疫细胞,例如淋巴细胞和apc,任选地被收获和被分析以鉴定和表征用于疾病诊断或免疫治疗的靶标。被捕获的细胞也可以被重新编程或被扩增以用于开发用于治疗的组合物或制剂。
将在下面的分节中进一步更详细地描述本发明。
i.用于募集和捕获免疫细胞的装置
一方面,本发明提供了细胞捕获装置。该装置含有生理上相容的多孔聚合物支架、多种抗原和任选的一种或多种吸引免疫细胞的募集剂。
在一个实施方式中,该装置包含由生理上相容性的和任选地可生物降解的聚合物构成的支架。可在该装置中使用的聚合物的实例是本领域已知的。参见,例如,美国公开号2011/0020216,其全部内容通过引用并入本文。这些聚合物的代表性实例包括但不限于聚(丙交酯)、聚(乙交酯)、聚(乳酸)、聚(乙醇酸)、聚酐、聚原酸酯、聚醚酯、聚己内酯、聚酯酰胺、聚碳酸酯、聚氰基丙烯酸酯、聚氨酯、聚丙烯酸酯及其共混物或共聚物。可生物降解的支架可以包含可生物降解的材料,例如胶原蛋白、藻酸盐、多糖、聚乙二醇(peg)、聚(乙交酯)(pga)、聚(l-丙交酯)(pla)或聚(丙交酯-共-乙交酯)(plga)或蚕丝(silk)。在一个实施方式中,支架或支架装置可以包含全部或部分地生物降解的生物相容性聚合物基质。水凝胶是合适的聚合物基质材料的一个实例。可以形成水凝胶的材料的实例包括聚乳酸、聚乙醇酸、plga聚合物、藻酸盐和藻酸盐衍生物、明胶、胶原、琼脂糖、天然和合成多糖、聚氨基酸如多肽,特别是聚(赖氨酸)、聚酯如聚羟基丁酸酯和聚-ε-己内酯、聚酐;聚磷腈、聚(乙烯醇)、聚(环氧烷)特别是聚(环氧乙烷)、聚(烯丙胺)(pam)、聚(丙烯酸酯)、改性苯乙烯聚合物如聚(4-氨基甲基苯乙烯)、普朗尼克多元醇、polyoxamers、聚(糖醛酸)、聚(乙烯基吡咯烷酮)及上述的共聚物,包括接枝共聚物。在另一个实施方式中,支架可以由各种合成聚合物和天然存在的聚合物制备,例如但不限于胶原蛋白、纤维蛋白、透明质酸、琼脂糖和富含层粘连蛋白的凝胶。在可生物降解结构的情况中,组合物通过物理或化学作用降解,例如水合水平、热或离子交换,或通过细胞作用,例如通过附近或驻留细胞加工酶、肽或其它化合物。稠度从软/柔韧(例如,凝胶)到玻璃状、橡胶状、脆性、韧性、弹性、刚性变化。该结构含有孔隙,其是纳米多孔的、多微孔的或大孔性的,并且孔隙的模式任选地是均匀的、不均匀的,对齐的,重复性的或随机的。
在一个实施方式中,聚合物是水凝胶形成剂,例如乙交酯类和/或藻酸盐。藻酸盐是多能多糖基聚合物,其可以通过控制分子量、降解率和支架形成方法而被配制用于特定应用。偶联反应可用于共价连接生物活性表位,如附着至聚合物主链的细胞粘附序列rgd。乙交酯/藻酸盐聚合物可以形成多种支架类型。可注射的水凝胶可以通过加入交联剂如钙离子从低mw藻酸盐溶液形成,而通过冻干高mw海藻酸盐圆盘形成大孔支架。支架配方的差异控制支架降解的动力学。形态发生剂(morphogen)或其他生物活性物质从海藻酸盐支架的释放速率通过支架配方控制以按照空间和时间受控的方式呈现形态发生剂。该受控释放不仅消除了全身性副作用和多次注射的需要,而且可用于产生激活植入位点处的宿主细胞和将移植细胞接种在支架上的微环境。
制备支架组合物的方法是本领域已知的。参见,例如,martinsen等(biotech.&bioeng.,33(1989)79-89),(matthew等(biomaterials,16(1995)265-274),atala等(jurology,152(1994)641-643)和smidsrod(tibtech8(1990)71-78),其公开内容通过引用整体并入本文。
示例性的装置利用相对较低分子量的乙交酯或藻酸盐,优选其大小在溶解后处于人体清除的肾阈值下,例如,该藻酸盐或多糖被降低到1000至80,000道尔顿的分子量。优选地,分子量为1000至60000道尔顿,特别优选为1000至50,000道尔顿。使用高古罗糖醛酸含量的藻酸盐材料也是有用的,因为与甘露糖醛酸单元相反,古罗糖醛酸单元提供通过二价阳离子进行离子交联以胶凝聚合物的位点。例如,通过引用并入本文的6,642,363号美国专利公开了制备和使用含有如藻酸盐的多糖的聚合物的方法。
本发明的支架可以是多孔的,使得支架可以维持抗原呈递并且吸引和捕获免疫细胞。在一个实施方式中,所述装置包含多孔支架,其中孔隙的直径在10nm至500μm之间。在这些实施方式中,本发明利用包含纳米多孔支架的装置,其中孔隙的直径小于约10nm(例如,约0.5nm、约1nm、约3nm、约5nm、约7nm、约9nm和更大)。在另一个实施方式中,支架是多微孔的,其中孔隙的直径范围为约100nm-20μm(例如,约200nm、约500nm、约700nm、约1μm、约2μm、约5μm、约7μm、约10μm、约12μm、约15μm、约17μm、约20μm或更大)。在另一个实施方式中,支架是大孔性的,其中孔隙的直径为约20μm至500μm(例如,30μm、50μm、70μm、100μm、200μm、300μm、400μm或以上)。特别地,孔隙的直径大于约100μm,和优选大于约400μm。在示例性实施方式中,支架是大孔性的,具有约200-500μm直径的排列孔隙。
制备具有所需孔径和孔排列的聚合物基质的方法在本领域中描述,例如美国公开号2011/0020216和美国专利号6,511,650中,其相关公开内容通过引用并入本文。
ii.抗原
本发明的装置包括一种或多种抗原,其可以是天然存在的、合成产生的或重组的化合物,例如肽、多肽、蛋白质、核酸、小分子、半抗原、碳水化合物或其它试剂,包括其片段或其组合。更具体地,抗原是肽或蛋白质或其免疫活性片段。在一个实施方式中,本文所述的抗原是纯化的。纯化的化合物含有至少60%重量(干重)的目的化合物。特别地,抗原为至少75%纯的,优选至少90%纯的,更优选至少99%纯的。纯度通过任何适当的标准方法测量,例如通过柱色谱、聚丙烯酰胺凝胶电泳或hplc分析。
抗原可以是自身抗原或非自身抗原。
非自身抗原的代表性实例包括例如,源自选自于病毒、细菌、原生动物、寄生虫和真菌的病原体的抗原。在这些实施方式中,非自身抗原可以源自牛型结核分枝杆菌、人乳头瘤病毒(hpv)、人免疫缺陷病毒、痘病毒、天花病毒、埃博拉病毒、马尔堡病毒、登革热病毒、流感病毒、副流感病毒、呼吸道合胞病毒、麻疹病毒、水痘带状疱疹病毒、单纯疱疹病毒、巨细胞病毒、爱泼斯坦-巴尔病毒、jc病毒、棒状病毒、轮状病毒、鼻病毒、腺病毒、乳头瘤病毒、细小病毒、细小核糖核酸病毒、脊髓灰质炎病毒、导致腮腺炎的病毒、引起狂犬病的病毒、呼肠孤病毒、风疹病毒、披膜病毒、正粘病毒、逆转录病毒、嗜肝dna病毒、柯萨奇病毒、马脑炎病毒、日本脑炎病毒、黄热病毒、裂谷热病毒、甲型肝炎病毒、乙型肝炎病毒、丙型肝炎病毒、丁型肝炎病毒、戊型肝炎病毒、sars冠状病毒、mers冠状病毒、肠病毒、包柔氏螺旋体种、炭疽芽孢杆菌、伯氏疏螺旋体、百日咳博德特氏菌、空肠弯曲杆菌、衣原体属的种、鹦鹉热衣原体、沙眼衣原体、梭菌属的种、破伤风杆菌、肉毒杆菌、产气荚膜梭菌、白喉棒状杆菌、柯克斯体属的种、肠球菌属的种、埃利希氏体属的种、大肠杆菌、土拉热弗朗西丝菌、嗜血杆菌属的种、流感嗜血杆菌、副流感嗜血杆菌、乳杆菌属的种、军团杆菌属的种、嗜肺军团菌、问号钩端螺旋体、李斯特菌属的种、单核细胞增生利斯特氏菌、分枝杆菌属的种、结核分枝杆菌、麻风分枝杆菌、支原体属的种、肺炎支原体、奈瑟氏菌属的种、脑膜炎奈瑟氏菌、淋病奈瑟氏菌、肺炎球菌属的种、假单胞菌属的种、铜绿假单胞菌、沙门氏菌属的种、伤寒沙门氏菌、肠道沙门氏菌、立克次体属的种、rickettsiaricketsii、斑疹伤寒立克次体、志贺氏菌属的种、葡萄球菌属的种、金黄色葡萄球菌、链球菌属的种、肺炎链球菌、酿脓链球菌、变形链球菌、密螺旋体属的种、苍白密螺旋体、弧菌属的种、霍乱弧菌、鼠疫耶尔森氏菌、耐甲氧西林金黄色葡萄球菌、曲霉菌属的种、烟曲霉、黄曲霉、棒曲霉、念球菌属的种、白色念珠菌、热带念珠菌、隐球菌属的种、新型隐球菌、溶组织内阿米巴、荚膜组织胞浆菌、利什曼原虫属的种、星形诺卡氏菌、恶性疟原虫、黑葡萄穗霉、刚地弓形虫、阴道毛滴虫、弓形虫种、布鲁斯锥虫、曼氏血吸虫、镰刀菌属的种、毛癣菌属的种、疟原虫属的种、弓浆虫种、内阿米巴属的种、巴贝虫属的种、锥虫属的种、leshmania种、肺孢子虫属的种、耶氏肺孢子虫、毛滴虫属的种、贾第虫属的种、裂体吸虫属的种、隐孢子虫属的种、疟原虫属的种、内阿米巴属的种、纳氏虫属的种、棘阿米巴属的种、巴拉姆希阿米巴种、弓形虫属的种、贾第虫属的种、毛滴虫属的种、利什曼原虫属的种和锥虫属的种。
或者,装置包含多种自身抗原,其可任选地与疾病或病症联系或相关联。优选地,该自身抗原与人类疾病或病症特异性地相关。在一个实施方式中,自身抗原与选自以下的自身免疫性疾病相关:类风湿性关节炎、狼疮、乳糜泻、炎性肠病或克罗恩病、
在另一个实施方式中,该自身抗原与癌症相关。癌症抗原的代表性类型包括例如mage-1、mage-2、mage-3、cea、酪氨酸酶、中期因子(midkin)、bage、casp-8、β-连环蛋白、β-连环蛋白、γ-连环蛋白、ca-125、cdk-1、cdk4、eso-1、gp75、gp100、mart-1、muc-1、mum-1、p53、pap、psa、psma、ras、trp-1、her-2、trp-1、trp-2、il13ralpha、il13ralpha2、aim-2、aim-3、ny-eso-1、c9orf112、sart1、sart2、sart3、brap、rtn4、glea2、tnks2、kiaa0376、ing4、hsph1、c13orf24、rbpsuh、c6orf153、nktr、nsep1、u2af1l、cynl2、tpr、sox2、golga、bmi1、cox-2、egfrviii、ezh2、licam、livin、livinβ、mrp-3、巢蛋白、olig2、art1、art4、b-细胞周期蛋白、gli1、cav-1、组织蛋白酶b、cd74、e-钙粘蛋白、epha2/eck、fra-1/fosl1、gage-1、神经节苷脂/gd2、gnt-v、β1,6-n、ki67、ku70/80、prox1、psca、sox10、sox11、存活素、upar、wt-1、二肽基肽酶iv(dppiv)、腺苷脱氨酶结合蛋白(adabp)、亲环蛋白b、结肠直肠相关抗原(crc)-c017-1a/ga733、t细胞受体/cd3-ζ链、肿瘤抗原gage家族、rage、lage-i、nag、gnt-v、rcasl、α-胎蛋白、pl20ctn、pmel117、prame、脑糖原磷酸化酶、ssx-i、ssx-2(hom-mel-40)、ssx-i、ssx-4、ssx-5、scp-i、ct-7、cdc27、腺瘤性结肠息肉病蛋白(apc)、胞衬蛋白、pla、连接蛋白37、ig-个体遗传型、pl5、gm2、gd2神经节苷脂、肿瘤抗原smad家族、lmp-1、ebv-编码的核抗原(ebna)-i、ul16-结合蛋白样转录物1(mult1)、rae-1蛋白、h60、mica、micb和c-erbb-2或其免疫原性肽,及其组合。
iii.支架组合物和抗原的组合
可以使用任何已知的方法,包括共价和非共价相互作用,将抗原与支架组合物结合。非共价相互作用的类型包括例如静电相互作用、范德华力相互作用、π效应、疏水相互作用等。抗原也可以通过共价相互作用粘着或系着到支架组合物上。用于将抗原粘着到支架/表面的方法是本领域已知的,例如表面吸附、物理固定,例如使用相变将物质截留到支架材料中。在一个具体实施方式中,将含有蛋白质的抗原性组合物与在水相或液相中的支架组合物混合,并且在环境条件(例如,ph、温度、离子浓度)改变之后,该液体胶凝化或固化从而截留抗原。或者,可以使用通过烷化或酰化剂的共价偶联以提供抗原在确定构象的支架上的稳定的长期呈现。将肽/蛋白质共价偶联到聚合物的示例性试剂和方法是本领域已知的。参见例如美国专利no.6,001,395,其涉及本发明的内容通过引用并入本文。在其它实施方式中,抗原被包封到支架中。将抗原包封到合适的支架例如plga微球中的方法是本领域已知的。参见例如美国专利号no.6,913,767和wo/1995/011010,其涉及本发明的内容通过引用并入本文。
抗原可被配制为通过直接结合或间接结合与免疫细胞相互作用。直接结合的类型包括,例如抗原与同源受体(例如b细胞受体或t细胞受体)的接合或偶联。间接结合可以通过一种或多种二级试剂或细胞类型的中介而发生。例如,抗原可以首先结合b细胞或抗原呈递细胞(apc),被加工(例如降解)并呈现在细胞表面的主要组织相容性复合体(mhc)上,其中靶细胞群体(例如t细胞)与该主要组织相容性复合体结合。或者,抗原可以募集分泌各种细胞因子、生长因子、趋化因子等的其他中介细胞,其又将目标免疫细胞群体吸引到装置。不管机制可能是什么,所述的成分协同地起作用以将免疫细胞募集和隔离到本发明的装置中。
抗原可以衍生自细胞裂解物、分级分离的细胞裂解物、新鲜收获的细胞、生物流体(包括血液、血清、腹水)、组织提取物等。在一个实施方式中,抗原衍生自所需的免疫细胞(例如b细胞或t细胞)与其结合的靶细胞的裂解物。在这些实施方式中,抗原首先在细胞裂解物中分级分离,然后再加载细胞捕获器。裂解物可以源自自身免疫性疾病特异性的细胞,例如与i型糖尿病相关的胰腺β细胞、与多发性硬化相关的神经元细胞、与类风湿性关节炎相关的骨/关节抗原、与炎性肠病或克罗恩病疾病相关的抗原。或者,裂解物可以衍生自癌细胞,例如从肿瘤样品或组织培养物获得的个体细胞或从活组织检查或组织学制备物获得的大块肿瘤细胞。
iv.募集剂
本发明的装置还可以包含一种或多种募集剂。该募集剂可以是选自于t细胞募集剂、b细胞募集剂、树突状细胞募集剂和巨噬细胞募集剂或其组合的试剂。
在一个实施方式中,所述装置包含t细胞募集剂。该t细胞募集剂的非限制性实例包括,但不限于ccl1、ccl2(mcp-1)、ccl-3、ccl-4、ccl-5(rantes)、ccl-17,ccl-22,cxcl12和xcl1,或其片段、其变体或其组合。上述t细胞募集剂(包括其功能性片段或其变体)的各种同源物是本领域已知的。该同源物的代表性实例包括来自苍蝇、小鼠、大鼠、猪、牛、猴、人等的相关蛋白质。同源物优选包括具有表1中所示的ncbi登录号的上述募集剂的人或小鼠同源物。
表1:用于捕获t细胞的趋化因子,包括相关的ncbi登录号:
该装置还可以含有上述募集剂的任何组合,例如表1中所列的募集剂中的至少2种、至少3种、至少4种、至少5种、至少6种、至少7种、至少8种、至少9种或更多种。在相关的实施方式中,该装置包含表1中所列的所有的募集剂。
在其它实施方式中,本发明提供了用于募集树突状细胞或巨噬细胞或其组合的装置。树突状细胞/巨噬细胞募集剂的非限制性实例包括,但不限于ccl2、ccl3、ccl5、ccl7、ccl8、ccl13、ccl17和ccl22或其功能性片段、其变体或其组合。该树突状细胞/巨噬细胞募集剂的同源物的代表性实例包括来自苍蝇、小鼠、大鼠、猪、牛、猴子、人等的相关蛋白质。同源物优选包括具有表2中所示的ncbi登录号的上述募集剂的人或小鼠同源物。
表2.用于捕获树突状细胞和/或巨噬细胞的趋化因子,包括相关的ncbi登录号:
用于募集dc/巨噬细胞募集的上述装置可以包含上述募集剂的任何组合,例如,表2中列出的募集剂中的至少2种、至少3种、至少4种、至少5种、至少6种、至少7种或更多种。在相关的实施方式中,该装置包含表2中所列出的所有募集剂。
在相关的实施方式中,本发明提供了用于募集b细胞的装置。b细胞募集剂的非限制性实例包括,但不限于sdf-1、blc、bcl-2和bca-1或其功能性片段、其变体或其组合。该b细胞募集剂的同源物的代表性实例包括苍蝇、小鼠、大鼠、猪、牛、猴子、人等中的上述蛋白质的同源物。该同源物优选包括具有表3中所示的ncbi登录号的上述募集剂的人或小鼠的同源物。
表3.用于捕获b细胞的趋化因子,包括相关的ncbi登录号:
用于募集b细胞的上述装置可以包含上述募集剂的任何组合,例如,表3中所列的募集剂中的至少2种、至少3种或全部4种或其变体或其片段。优选地,该装置包含表3中列出的所有募集剂或其片段。
另外的实施方式涉及含有能够募集多种免疫细胞(例如,t细胞和dc/巨噬细胞的组合、t细胞和b细胞的组合、b细胞和dc/巨噬细胞的组合等)的试剂的装置。因此,在一个实施方式中,本发明所提供的装置募集t细胞和树突状细胞/巨噬细胞两者,其包含选自表1中的至少一种试剂和表2中的至少一种试剂的募集剂。在相关实施方式中,本发明所提供的装置募集b细胞和树突状细胞/巨噬细胞两者,其包含选自表2中的至少一种试剂和表3中的至少一种试剂的募集剂。在另一个实施方式中,本发明所提供的装置募集t细胞和b细胞两者,包含选自表1中的至少一种试剂和表3中的至少一种试剂的募集剂。
在能够募集免疫细胞的组合的装置中,可以采用来自上述表格的募集剂的各种组合和子组合。例如,被设计用于募集t细胞和dc/巨噬细胞两者的装置可以包含来自表1的一种试剂和来自表2的两种试剂、来自表1的两种试剂和来自表2的1种试剂、来自表1和表2的两种试剂,等。类似地,被设计用于募集b细胞和dc/巨噬细胞两者的装置可以包含来自表2的一种试剂和来自表3的两种试剂、来自表2的两种试剂和来自表3的一种试剂、来自表2和3的两种试剂,等。被设计用于募集t细胞和b细胞两者的装置可以包含来自表1的一种试剂和来自表3的两种试剂、来自表1的两种试剂和来自表3的一种试剂、来自表1和3的两种试剂等。因此在一个代表性实施方式中,该装置适应于募集t细胞和树突状细胞/巨噬细胞的组合,其包含ccl17、ccl22,其变体或其片段,或其组合。募集剂(包括其片段或变体)的同源物的代表性实例包括来自苍蝇、小鼠、大鼠、猪、牛、猴子、人等的相关蛋白质。同源物优选包括具有表2所示的ncbi登录号的上述募集剂的人类或小鼠的同源物。
与其他造血细胞(例如血小板、红细胞等)相比,该装置/捕获器还可以适应于优先募集某些类型的免疫细胞组合,例如淋巴细胞和apc的组合。这样的装置可以包含在表1、2和3中所列出的募集剂的任何组合。
本发明的装置适应于优先募集单一类型或单一亚型的细胞,例如优先募集t细胞和特别是treg细胞或nk细胞的子集。优先募集的特征在于,与装置中的其他类型的免疫细胞(或在没有募集剂的对照捕获器中)相比,在装置中一种或多种特定类型的免疫细胞(例如,t细胞、b细胞、dc/巨噬细胞)增加至少10%、至少20%、至少30%、至少50%、至少75%、至少100%、至少2倍、至少5倍、至少8倍、至少10倍或更多的累积。在适应于募集免疫细胞的组合(例如t细胞和dc/巨噬细胞的组合)的装置中,优先募集的特征在于,其中募集细胞的总百分比相比于装置中的其他类型的免疫细胞(或在对照捕获器中)高至少10%、至少20%、至少30%、至少50%、至少75%、至少100%、至少2倍(即200%)、至少5倍、至少8倍、至少10倍或更多。特别地,优先募集的特征在于,目标细胞的数量与其他免疫细胞相比增加1-10倍。
v.另外的试剂
本发明的实施方式还提供了用于捕获免疫细胞的装置,其包含多种另外的试剂。在这样的实施方式中,另外的试剂可包含生长因子、细胞因子、趋化因子、白细胞介素、粘附信号分子、整联蛋白信号分子或其片段,或其组合。
生长因子/细胞因子的代表性实例包括但不限于肾上腺髓质素(am)、血管生成素(ang)、自分泌运动因子、骨形态发生蛋白(bmp)、脑源性神经营养因子(bdnf)、表皮生长因子(egf)、红细胞生成素(epo)、成纤维细胞生长因子(fgf)、胎牛生长激素(fbs)胶质细胞系衍生的神经营养因子(gdnf)、粒细胞集落刺激因子(g-csf)、粒细胞巨噬细胞集落刺激因子(gm-csf)、生长分化因子-9(gdf9)、肝细胞生长因子(hgf)、肝癌源性生长因子(hdgf)、胰岛素样生长因子(igf)、角化细胞生长因子(kgf)、迁移刺激因子(msf)、肌生成抑制素(gdf-8)、神经生长因子(ngf)、神经营养因子、血小板源生长因子(pdgf)、血小板生成素(tpo)、t细胞生长因子(tcgf)、转化生长因子(tgf-α或tgf-β)、肿瘤坏死因子-α(tnf-α)、血管内皮生长因子(vegf)、wnt、胎盘生长因子(pgf)或其功能性片段,或其组合。
白细胞介素的代表性类型包括但不限于il-1(激活t细胞、b细胞、nk细胞和巨噬细胞)、il-2(激活b细胞和nk细胞)、il-3(刺激非-淋巴细胞)、il-4(用于活化的b细胞、静息t细胞和肥大细胞的生长因子)、il-5(用于激活的b细胞的分化)、il-6(浆细胞和t细胞的生长因子)、il-7(前b细胞/前t细胞和nk细胞的生长因子)、il-10(激活巨噬细胞、b细胞、肥大细胞、th1/th2细胞)、il-12(激活t细胞和nk细胞)、il-17(激活th细胞)。也可以使用白细胞介素的功能性片段,其特征在于调节靶细胞活性的能力。在表4中提供了代表性类型的白细胞介素分子,包括其人和/或小鼠同源物的ncbi登录号。
表4.可以在装置中使用的白细胞介素的类型。
任选地,该装置可以含有粘附分子,其也可以用作信号传导剂。粘附信号传导分子的代表性实例包括但不限于纤连蛋白、层粘连蛋白、胶原蛋白、血小板反应蛋白1、玻连蛋白、弹性蛋白、腱生蛋白、聚集蛋白聚糖、聚集蛋白、骨唾液蛋白,软骨基质蛋白、纤维蛋白原(fibronogen)、纤维蛋白、腓骨蛋白(fibulin)、粘蛋白、巢蛋白(entactin)、骨桥蛋白、纤溶酶原、限制蛋白、丝甘蛋白聚糖(serglycin)、sparc/骨结合素、多能蛋白聚糖、血管性血友病因子、多糖硫酸肝素、连接蛋白、胶原蛋白、rgd(arg-gly-asp)和yigsr(tyr-ile-gly-ser-arg)肽和环肽、糖胺聚糖(gag)、透明质酸(ha)、软骨素(chondroitin)-6-硫酸、整联蛋白配体、选择素、钙粘蛋白和免疫球蛋白超家族的成员。其他实例包括神经细胞粘附分子(ncam)、细胞间粘附分子(icam)、血管细胞粘附分子(vcam-1)、血小板-内皮细胞粘附分子(pecam-1)、l1和chl1。还可以使用粘附分子的功能性片段,其特征在于其调节靶细胞与本发明的装置的结合的能力。特别地,粘附分子包括含有氨基酸序列精氨酸-甘氨酸-天冬氨酸(rgd)的肽或环肽,其被称为细胞附着配体并且存在于各种天然细胞外基质分子中。具有这种修饰的聚合物基质提供了对本发明的支架的细胞粘附性质,并且维持哺乳动物细胞系统的长期存活,以及支持细胞生长和分化。可以使用本领域普通技术人员通常已知的并且在实施例中描述的合成方法来实现粘附分子与聚合物基质的偶联。参见例如hirano等,advancedmaterials,p.17-25(2004);hermanson等,bioconjugatetechniques,p.152-185(1996);massia和hubbell,j.cellbiol.114:1089-1100(1991;mooney等,j.cellphys.151:497-505(1992);和hansen等,mol.biol.cell5:967-975,(1994),其通过引用并入本文。
根据靶细胞类型,可以优选使用对靶细胞特异性的粘附信号传导分子。因此,在一个实施方式中,该装置含有可用于募集t细胞的粘附受体。在其它实施方式中,所述装置含有可用于募集树突状细胞/巨噬细胞的粘附受体。在另一个实施方式中,该装置含有可用于b细胞募集的粘附受体。
在这些实施方式中,该装置可以含有t细胞特异性粘附分子,例如选自lfa-1、madcam-1、vcam-1、cd28和ctla-4或其变体、其片段或其组合的受体。表5中提供了这些t细胞特异性粘附分子的人和小鼠同源物的代表性实例。
表5.各种类型的t细胞粘附受体和其已知人和小鼠同源物的ncbi和gi登录号:
用于募集dc/巨噬细胞或b细胞的装置可以被类似地配制成含有对dc/巨噬细胞或b细胞特异性的粘附分子。b细胞特异性粘附分子的代表性实例包括,例如,n-cam(2型)、层粘连蛋白或纤连蛋白等。对巨噬细胞或树突状细胞特异性的粘附分子的代表性实例包括,例如,icam-1或vcam-1。根据需要,可以将该装置特异性地配制成含有上述表1-5中的募集剂和粘附分子的子集。例如,用于募集t细胞和树突状细胞两者的装置可以被配制为含有ccl17和ccl22(来自趋化因子的列表)与vcam-1(来自粘附分子的列表)的组合。用于募集t和b淋巴细胞两者的装置可以类似地通过选择性并入各种募集剂和粘附分子来配制,其任选地并入一种或多种白细胞介素和/或细胞因子。
vi.用于募集免疫细胞的特定亚型的装置
通过使用特异性结合于在细胞中表达的细胞表面标志物的试剂,本发明的装置还可以被配制成优先募集一种或多种细胞亚群。例如,在t细胞的情况下,该装置可以适应用于优先募集辅助性t细胞(th细胞;其差异表达cd4+)、细胞毒性t细胞(tc细胞;其差异表达cd8+)、记忆性t细胞(tm细胞;其差异表达cd45ro)、抑制性t细胞(ts,该细胞)、调节性t细胞(treg;进一步表征为foxp3+treg细胞和foxp3-treg)、自然杀伤t细胞(nk细胞;其差异表达cd1d+)、粘膜相关不变t细胞(maits;差异表达mr1)、gammadeltat细胞(γδt细胞;包含含有一条γ链和一条δ链的tcr)。结合细胞表面标志物的此类试剂可包括例如,半抗原、肽、配体、抗体等。用于富集具有一种或多种细胞亚型的分离物的其它常规技术可以任选地原位或非原位使用。
同样,在b细胞的情况下,可以使用选择性地结合特定b细胞亚型中表达的细胞表面标志物的试剂来配制装置以优先募集特定b细胞亚型。可以被优先捕获的b细胞亚型的代表性实例包括成浆细胞、浆细胞(差异表达cd27+/cd138+/cd319+)、记忆性b细胞(差异表达airoldi等人,clincancerresearch,200410;144中公开的标志物的组合)、滤泡性(fo)b细胞(表达高水平的cd23但对cd1或cd5是阴性的)、边缘区(mz)b细胞(对cd21、cd1、cd9是阳性的,但对cd23、cd5和cd11b是阴性的)、b-1细胞(具有标志物谱,例如cd20+cd27+cd43+cd70-)、b-2细胞(类似于fob细胞和mzb细胞)、调节性b(breg)细胞(例如,具有标志物谱cd24+/cd38+)等。
所述装置还可以适应于优先募集各种亚型的抗原呈递细胞。例如,在树突状细胞的情况下,与浆细胞样树突状细胞(pdc)相比,该装置可适应于募集骨髓树突状细胞(mdc,其包括更常见的mdc-1和较不常见的mdc-2),或反之亦然。在巨噬细胞的情况下,与m2(即,活化的巨噬细胞)相比,该装置可适应于优先募集m1(即,“杀伤”巨噬细胞),反之亦然。两者之间的差异在本领域中是公认的。例如,m1亚型分泌高水平的il-12和低水平的il-10;对于m2亚型则是相反的。肿瘤相关巨噬细胞主要是m2表型的,和似乎积极促进肿瘤生长。
该装置还可以适应于募集对于疾病特异性的免疫细胞。例如,可以募集对于特定类型的自身免疫性疾病特异性的多种t细胞。因此,在一个实施方式中,可用于诊断自身免疫性疾病的装置可以被配制成含有对涉及该病症的免疫细胞特异性的募集剂。这样的募集剂可以对,例如,调节性t细胞(treg)、抑制性t细胞(ts)或其组合是特异性的。在相关的实施方式中,可以用于诊断癌症的装置可被配制成包含用于优先募集癌症特异性t细胞类型(例如细胞毒性t细胞(tc)、自然杀伤细胞(nk)或其组合)的募集剂。
在某些实施方式中,该装置可用于淘选疾病特异性细胞。这些可以包括例如,直接促进疾病进展的细胞。在许多自身免疫性疾病的情况下,该疾病可以通过靶向杀伤特定的细胞群体(例如t1d中的胰腺β细胞和多发性硬化中的神经元细胞)来介导和促进。在其他自身免疫性疾病中,该疾病可以通过靶向攻击特定表位来沉淀,例如,在类风湿性关节炎的情况中的类风湿因子(rf)和瓜氨酸化肽(acpa)以及在克罗恩病的情况中的肠道菌群中存在的抗原。细胞的靶向破坏通常涉及免疫细胞的特定类型或子集。因此,基于细胞靶标的特性和性能,可以使用本发明的装置优先捕获对其特异性的免疫细胞。
在上述实施方式中,所述装置被提供疾病特异性免疫细胞(例如t细胞、b细胞、树突状细胞、巨噬细胞等)与其结合的抗原。这些自身免疫细胞可被捕获并任选地重新编程为非自身免疫表型。将t细胞重编程为多能性的方法是本领域已知的。参见nishimura等,stemcell12,114–126(2013);themeli等,naturebiotechnology31,928-933(2013)。在某些情况下,特别是在癌症特异性t细胞的情况下,重编程的细胞可以被复原以靶向癌症。或者,在对自身免疫性疾病特异性的t细胞的情况下,被捕获的细胞可以被去除(从体内除去)或被杀伤。
vii.制造/使用装置的方法
本发明的装置是被工程化以维持抗原呈递的多孔装置。该装置的代表性示例在图1a和1b中示出。如附图所示,孔隙给予了t细胞渗透和扩增的空间。在本领域中已经描述了多孔支架的制造方法。参见,例如,美国公开号2011/0020216、2013/0202707、2011/0020216和美国专利号8,067,237,其公开内容通过引用并入本文。例如,可以使用丙交酯和乙交酯的共聚物(plg)制造捕获器,以使用气体形成过程(如实施例中所详细描述的)产生plg细胞捕获器。通过孵育聚合物和抗原的组合物,将抗原物理吸附到plg聚合物上。可选地,可以使用标准双重乳液制备包封抗原的plg微球。然后将plg-抗原球冷冻和冻干并与致孔剂或孔形成剂混合,并且模压成型。使得所得到的圆盘在高压co2环境中平衡,并且压力的快速降低使得聚合物颗粒膨胀并融合成互连的支架结构。致孔剂通过浸入水中从支架中浸出,产生约90%多孔的抗原负载的细胞捕获器。可以通过常规方法改变孔隙率,例如通过改变致孔剂的浓度和/或使用其它生物聚合物作为支架形成剂。装置的所得孔隙率在40%至99%之间,优选在50%至90%之间,特别优选在60%至80%之间或更高。
装置植入/移除
装置可以通过本领域已知的任何方式植入,例如静脉内施用、植入(例如皮下植入或作为微针贴片植入),腹膜内施用或肌内注射。足以使目标细胞迁移到多孔基质中的植入时间段可以在两个小时至几个月之间,例如0.5、1、2、5、7、14、25、30、35、38、45、50、60或更多天。植入时间可以是至少一天,在此期间,1×109至1×1010个细胞在装置居留在身体组织中之后从装置累积和/或提取。
可以将多个装置植入受试者中。在一个实施方式中,将至少1个、至少3个、至少10个、至少30个、至少50个、至少100个、至少300个、至少500个、至少1000个或更多个装置植入受试者中。装置的应用可以是均一的(例如,每个装置含有相同的抗原)或变化的(例如,含有不同抗原的多个装置)。
为了细胞的分离、表征、分析和/或扩增/重编程,不需要从体内移除该装置。在一个实施方式中,移除细胞而不从植入物的位置物理移除装置。在一个实施方式中,位于装置外围的细胞,例如,位于装置的约1μm、约2μm、约5μm、约10μm、约20μm、约60μm、约100μm、约300μm、约0.5mm、约1.0mm、约3.0mm、5.0mm、约10mm、50mm等的半径内的细胞可以被去除并任选地扩增或重编程。也可以通过细胞分选技术(facs或macs)或分辨技术(例如使用ficoll梯度)来纯化细胞以实现更均质的细胞群体。在另一个实施方式中,附着到装置上或位于装置内的细胞可以被去除并且任选地扩增或重新编程而不移除装置。用于从植入装置去除细胞的方法是本领域已知的。这些可以包括例如,化学或酶学处理。例如,低剂量的不同类别的洗涤剂(例如非离子洗涤剂、tritonx-100和阴离子洗涤剂、十二烷基硫酸钠)的组合可以破坏膜并有助于从植入物中除去细胞。或者,可以使用结缔组织酶如胶原酶、胰蛋白酶、分散酶来驱出细胞。捕获器也可以经受灵敏的机械破坏(例如mortor和pistal或组织匀浆),以增强居留细胞的去除。可以采取额外的步骤来消除组织基质中的任何残留的洗涤剂或酶,以避免干扰活细胞随后再定植植入物。类似的途径被描述于美国公开号no.2008/0131966中,其通过引用并入本文。
在另一个实施方式中,从植入物的位置移除该装置。可以通过本领域已知的任何方法去除装置。为了有助于去除,该装置可以具有小的引线长度或小的唇缘,这将允许机械地移除装置而不损坏装置。该装置可以被部分地或完全地去除以便取回细胞。
在移除装置之后,捕获的细胞可通过本领域已知的任何方法进行回收,例如通过消化对多孔基质的细胞贴附。这可以通过例如使含胰蛋白酶的缓冲液流过该装置来实现。然后可以通过本领域已知的任何方法从装置中排出捕获的细胞。在优选的实施方式中,该装置包含由膜覆盖的出口,该膜可以,例如通过施加穿过该装置的正压力而使其爆裂,从而使得被捕获的细胞从装置中排出。或者,具有捕获的细胞的多孔基质可以从装置中排出,然后可以通过本领域已知的任何方法将捕获的细胞从多孔膜分离。在优选的实施方式中,该装置包含由膜覆盖的出口,该膜可以,例如通过施加穿过该装置的正压力而使其爆裂,从而使得具有捕获细胞的多孔基质从装置中排出。
一旦从装置中获取捕获的细胞,可以将捕获的目标细胞与其他被捕获的细胞分离。这可以通过本领域已知的任何方式进行,例如,将捕获的细胞与带有结合伴体的微珠组合,该结合伴体是对于存在于其它的捕获细胞上而不存在于捕获的目标细胞上的表面标志物。将结合其他的捕获细胞的微珠去除只留下被捕获的目标细胞。在另一个实施方式中,被捕获的目标细胞可以通过将捕获的细胞与带有结合伴体的微珠混合与其它捕获的细胞分离,该结合伴体是对于存在于被捕获的目标细胞上而不存在于其它的捕获细胞上的表面标志物。被捕获的目标细胞与微珠结合并可被移除。例如,可以通过使用特异性结合t细胞表面受体或标志物但不与b细胞、树突状细胞或巨噬细胞结合的结合伴体来移除t细胞。
或者,可以使用能够结合于其它浸润细胞而不与目标细胞结合的结合伴体,其中该结合伴体能够(共价或非共价地)结合到微珠上。例如,这样的结合伴体可以包括适体,或优选抗体或抗体片段,其中结合位点优选对于存在于这种浸润细胞而不是目标细胞的表面上的细胞表面标志物特异性的。或者,可以使用采用对于目标细胞特异性的结合伴体的反向途径。例如,当被捕获的目标细胞是巨噬细胞时,优选的微珠具有对巨噬细胞特异性细胞表面受体特异性的抗体。本领域技术人员可以配制对于任何特定目标细胞或其组合的结合伴体。
适体是与特定的靶分子(如蛋白质或小分子)结合的单链寡核苷酸或寡核苷酸类似物。因此,适体是抗体的寡核苷酸类似物。rna和单链dna或dna类似物适体都是已知的。可以通过使用称为selex(通过指数富集的配体的系统进化)的迭代过程来选择实际上与任何特定靶标相结合的适体。
抗体或抗体片段可以是多克隆的、单克隆的或重组的,并且可以是任何动物的,例如啮齿动物或人类,或者动物的混合,如人源化小鼠。
可以使用任何类型的微珠来结合其他被捕获的细胞。例如,该微珠可以是在离心条件下沉淀的重颗粒,但是该离心条件不会沉淀所捕获的目标细胞。或者,微珠可以是在沉淀所捕获的目标细胞的离心条件下不沉淀的浮动颗粒。在优选的实施方式中,该微珠是磁性珠。
可以对分离的细胞进行进一步分析。这样的进一步分析可以包括细胞的定量,或mrna或蛋白质表达的分析。例如,可以量化所捕获的目标细胞,以便在给定量的组织中近似出被捕获的目标细胞的数量,以便将被捕获的目标细胞的数量与其他被捕获的细胞的量进行比较。可以通过本领域已知的任何方法对捕获的目标细胞进行定量,例如通过显微镜观察。
优选地,使用细胞计数技术,例如荧光激活细胞分选(facs),分离和/或分选捕获的细胞用于分析。这可以使用上述多种抗体或其它结合分子和其它二级试剂来完成。可以使用本领域已知的方法对捕获的细胞进行表型分型。参见autissier等,jimmunolmethods.360(1-2):119-128(2010)。例如,t细胞通过细胞表面标志物如cd4或cd8进行表征或鉴定。树突状细胞通过cd11c的表达来表征或鉴定。巨噬细胞通过cd11c和/或cd68的表达来表征或鉴定。示例性标志物(以正向地鉴定以及排除其他细胞)包括cd11c(以选择dc)、gr-1(以选择巨噬细胞)、cd204(以选择巨噬细胞)、cd16(以选择单核细胞和负向选择(例如,排除)非单核细胞,即不具有单核细胞表型或细胞表面标志物表型的细胞)、cd45(以选择造血细胞,例如免疫细胞)、cd49b[以选择自然杀伤细胞(nk细胞)以及表达该标志物的t细胞亚群]、cd3(以选择t细胞)、cd4(t细胞)、cd8(t细胞)、cd19和b220。
在一些优选的实施方式中,在所捕获的目标细胞中测定mrna或蛋白质表达。例如,捕获的细胞的t细胞和b细胞受体可以被测序以鉴定疾病的抗原特异性和自身免疫的药物靶标。在相关的实施方式中,然后可以将被捕获的目标细胞的mrna或蛋白质表达与其它细胞类型或来自其他受试者的相同细胞中的一种或多种相同基因的表达进行比较。当需要分析多于一种基因的mrna或蛋白质表达时,可以使用微阵列技术。这种良好建立的技术可以一次性分析许多基因的mrna或蛋白质表达模式,从而允许例如所捕获的目标细胞和其他细胞的整个基因组之间的比较。在从装置回收的生物材料的量不足以用于分析的情况下,可以在测定基因表达之前扩增来自捕获的目标细胞的mrna。这种扩增可以通过本领域已知的任何方法进行,例如通过逆转录和cdna扩增。
抗原特异性的细胞
在一些实施方式中,抗原特异性的捕获细胞或其亚群(例如,抗原特异性t细胞或b细胞)被操作以配制适于诊断或治疗用途的组合物。操作的实例包括,例如,激活、分裂、分化、生长、扩增、重编程、无能性、静息、衰老、凋亡或死亡。细胞不需要从装置中物理去除以进行操作。因此,在一个实施方式中,细胞原位操作(例如,在植入位点处或附近)。在其它实施方式中,细胞被非原位操作(例如,在与植入位点不同的位点处)。
在一些实施方式中,抗原特异性细胞,例如t细胞通过提供其中含有多种抗原任选地与抗原呈递细胞(或吸引这种apc的抗原)一起的装置原位地操作(例如,激活和/或扩增)。在其它实施方式中,抗原特异性细胞通过与抗原(例如,自身免疫抗原)任选地与抗原呈递细胞一起孵育在细胞培养物中操作。一旦激活,细胞经历细胞信号传导的复杂级联,其导致许多基因产物的转录和表达。可以进一步分析对活化细胞特异性的基因产物以鉴定和分离具有所需抗原特异性的细胞。
(a)t-细胞
本文描述的实施方式涉及用于非原位操作抗原特异性t细胞的方法。应当注意,本文描述的技术可以变化以便原位进行该过程。将包含t细胞的样品与特定的抗原一起孵育,其导致对目标抗原特异性的t细胞的活化。含有t细胞的样品可与抗原一起孵育约1天至7天。然后通过选择表达如上所述活化的t细胞的基因产物的t细胞来分离抗原特异性的t细胞。目标抗原可以是自身抗原或非自身抗原或其片段。目标抗原也可以是两种或更多种单个目标抗原的组合。
用于鉴定或负向选择活化的t细胞的基因产物可以是细胞表面标志物或细胞因子,或其组合。用于识别活化的t细胞的细胞表面标志物包括,但不限于cd69、cd4、cd8、cd25、hla-dr、cd28和cd134。cd69是在b和t淋巴细胞、nk细胞和粒细胞上发现的早期活化标志物。cd25是il-2受体,且是活化的t细胞和b细胞的标志物。cd4是tcr共受体,且是胸腺细胞(thymoctes)、th1-和th2-型t细胞、单核细胞和巨噬细胞的标志物。cd8也是tcr共受体,且是细胞毒性t细胞的标志物。cd134仅在活化的cd4+t细胞中表达。
用于负向选择活化的t细胞的细胞表面标志物包括,但不限于,cd36、cd40和cd44。cd28作为独立于t细胞受体途径的刺激性t细胞活化途径发挥作用,并在cd4+和cd8+细胞上表达。cd36是膜糖蛋白,且是血小板、单核细胞和内皮细胞的标志物。cd40是b细胞、巨噬细胞和树突状细胞的标志物。cd44是巨噬细胞和其他吞噬细胞的标志物。可以通过使用对于辅助性t细胞或细胞毒性t细胞的细胞表面基因产物(例如,cd4与cd8)的表达的正向选择、负向选择或其组合来分离t细胞的亚群。用于鉴定本发明的活化t细胞的细胞因子包括,但不限于th1型t细胞(细胞介导的应答)和th2型t细胞(抗体应答)产生的细胞因子。用于鉴定活化的th1型t细胞的细胞因子包括,但不限于il-2、γ干扰素(γifn)和组织坏死因子α(tnfα)。用于识别活化的th2型t细胞的细胞因子包括,但不限于il-4、il-5、il-10和il-13。也可以通过使用对于辅助t细胞或细胞毒性t细胞的细胞因子基因产物(例如,γifn相对il4)的表达的正向选择、负向选择或其组合来分离t细胞的亚群。
可以通过鉴定表达cd69、cd4、cd25、il-2、ifnγ、tnfα或其组合的细胞来分离对目标抗原特异的活化的th1型t细胞。也可以通过鉴定与ifnγ或tnfα一起表达cd69和cd4的细胞来分离对目标抗原特异的活化的th1型t细胞。可以通过鉴定表达cd69、cd4、il-4、il-5、il-10、il-13或其组合的细胞来分离对目标抗原特异性的活化的th2型t细胞。可以通过鉴定表达cd69、cd4、cd25、il-2、ifnγ、tnfα或其组合的细胞以及表达cd69、cd4、il-4、il-5、il-10、il-13或其组合的细胞来分离对目标抗原特异性的活化的th1型t细胞和th2型t细胞的组合。
可以通过本领域技术人员已知的利用抗体的免疫选择技术鉴定用于本发明的活化t细胞的正向或负向选择的基因产物,包括,但不限于荧光激活细胞分选(facs)、磁性细胞分选、淘选和色谱法。可以在一个或多个步骤中进行活化t细胞上的两种或更多种标志物的免疫选择,其中每个步骤对于一种或多种标志物进行正向或负向选择。当使用facs在一个步骤中进行两种或更多种标志物的免疫选择时,可以用不同的荧光团标记两种或更多种不同的抗体。或者,如上所述,可以使用微珠对细胞进行分选。
对于细胞表面表达的基因产物,抗体可以直接结合基因产物并可用于细胞选择。对于以低浓度表达的细胞表面基因产物,磁性荧光脂质体可被用于细胞选择。在低的表达水平下,常规荧光标记的抗体可能不足够灵敏以检测细胞表面表达的基因产物的存在。含有荧光团的脂质体可以与具有目标特异性的抗体缀合,从而使其能够检测细胞表面标志物。
对于细胞内基因产物,如细胞因子,抗体可以在渗透细胞后使用。或者,为了避免细胞通过渗透杀死,细胞内基因产物可以在最终从细胞分泌时利用在细胞表面上的“捕捉”抗体在通过细胞膜分泌时被检测。捕捉抗体可以是对两种不同抗原具有特异性的双重抗体:(i)分泌的目标基因产物和(ii)细胞表面蛋白质。细胞表面蛋白质可以是通常存在于t细胞(特别是淋巴细胞)上的任何表面标志物(例如cd45)。捕捉抗体可以首先结合细胞表面蛋白,和然后当细胞内目标基因产物通过膜分泌时结合到细胞内目标基因产物,从而将基因产物保留在细胞表面上。然后可以将对于捕获的基因产物特异性的标记抗体用于与所捕获的基因产物结合,其允许选择活化的t细胞。细胞因子的某些形式还发现在细胞表面上以低浓度表达。例如,γifn以低浓度显示在细胞表面上,具有与细胞内γifn表达类似的动力学(assenmacher等,eurj.immunol,1996,26:263-267)。对于在细胞表面上表达的细胞因子的形式,常规的荧光标记抗体或含荧光团的脂质体可被用于检测目标细胞因子。本领域普通技术人员能够认识到,用于检测和选择对活化的t细胞特异性的细胞外和细胞内基因产物的其它技术。
通过本发明分离的t细胞可以从全血至少40%-90%富集。t细胞也可以从全血至少95%富集。t细胞也可以从全血至少98%富集。t细胞也可以从全血至少99.5%富集。类似的方法可用于b细胞的原位或非原位操作。
(b)b细胞
可以使用对上述方法的轻微变化来获得抗原特异性b细胞。例如,dynabead-m-450可用于偶联疾病特异性抗原,然后将其与含有用本发明的装置捕获的细胞的组合物一起孵育。任选地,可以对捕获的细胞进行筛选过程以对样品进行富集,例如使用结合到对b细胞特异的细胞表面标志物的试剂。然后将b细胞与抗原偶联的dynabeads一起孵育,并培养约7-10天的时间以产生莲座细胞。莲座细胞任选地通过分析分泌的抗体,例如基于其与疾病特异性抗原结合的能力,进行分型。可以使用常规技术转化被鉴定为阳性的克隆以产生杂交瘤。
本文描述的实施方式还涉及对目标抗原特异性的分离细胞,所述细胞通过上述方法分离。分离的细胞可以是单克隆细胞或多克隆抗原特异性免疫细胞,例如,抗原特异性t细胞。
本发明的实施方式还涉及通过测定捕获在本发明的装置中的免疫细胞的数目来测定抗原特异性免疫细胞的相对频率的方法。优选地,该抗原特异性免疫细胞是t细胞或b细胞。特别优选的是,该抗原特异性免疫细胞是t细胞。
疾病/病症的诊断
本文所描述的实施方式还涉及用于检测或诊断受试者的疾病或病症的方法。在一个实施方式中,该疾病是癌症。在另一个实施方式中,该疾病是自身免疫性疾病。在第三实施方式中,疾病是病原体性疾病。
在这些实施方式中,可以通过首先向受试者施用本发明的装置来诊断患有疾病的受试者,其中该装置中的抗原对该疾病是特异性的。然后使得这些装置在受试者中保持一段时间,例如0.5天、1天、2天、5天、7天、14天、25天、30天、35天、38天、45天、50天、60天或更长时间,并且使用一种或多种上述技术分析其中包含的细胞。例如,在自身免疫性疾病的情况下,被分析的细胞可以包括t细胞、b细胞、抗原呈递细胞或其组合。在癌症诊断的情况下,被分析的细胞可以包括t细胞或b细胞。在病原体性疾病的情况下,被分析的细胞可以包括抗原呈递细胞。
可以使用任何常规方法进行分析步骤。因此,在一个实施方式中,分析步骤可以包括测定对自身免疫性疾病特异性的免疫细胞的数量。可以使用任何常规技术来测定免疫细胞的抗原结合特异性,例如将细胞样品加载到抗原包被的表面上,洗去非特异性结合的细胞,并使用检测剂(例如,结合位于抗原特异性细胞上的细胞表面表位的抗体)定量抗原特异性细胞的数量(以通过释放结合的细胞的游离形式或结合的形式)。在另一个实施方式中,分析步骤可以涉及测定抗原特异性免疫细胞的物理或生物学特征。物理特征的实例包括,例如,尺寸、形状、反射率、形态、密度。生物学特征的实例包括,例如,特定细胞表面标志物的表达、细胞因子的分泌、对特定抗原或试剂的反应性、基因表达的模式。
分析步骤可以结合于关联步骤,其中,分析步骤的结果与目标参数相关联。代表性的参数类型包括:疾病的存在(或不存在)、疾病类型(例如,侵袭性与非侵袭性自身免疫性疾病;可药物控制与非可药物控制的疾病,例如抗生素易感性与抗生素抗性的细菌感染,免疫治疗-抗性与免疫治疗敏感性的癌症)、疾病阶段、疾病的进展/消退(随时间)等。在一个实施方式中,该参数涉及疾病的存在或不存在(其可以用二元形式表示)。在另一个实施方式中,该参数涉及疾病分期(其可以以定类尺度表示,例如i-iv期,以iv期为最高)。然而在另一个实施方式中,该参数涉及疾病发生的几率或可能性,例如,至少20%、30%、40%、50%、60%、70%、80%、2倍、3倍、5倍、10倍、20倍或更高。
在上述诊断方法中,可将参数与基线值进行比较。基线值可以是预先确定的值,例如在健康受试者的群体中。例如,其中目标抗原是类风湿性关节炎(ra)抗原的情况下,健康受试者中ra特异性抗体(或t细胞)的基线水平可以用于关联步骤中。或者,可以使用合适的对照来实验性地确定基线值,例如仅含有支架(即抗原、募集剂或两者均为阴性)的装置或含有随机或非疾病特异性抗原的装置。本领域技术人员可以使用常规技术来关联和/或得出各个受试者组之间的推断。
例如,在一个实施方式中,将含有疾病特异性抗原(例如,源自牛型结核分枝杆菌的mbp70)的装置植入被怀疑已暴露于病原体的受试者组和健康(或随机)受试者组中给定的时间段(如两周)。单独地,向每个组中的少数受试者提供对照装置(含有随机或非mbp抗原)。装置被移植出,并测量和比较实验组(例如,植入mbp70+装置的疑似组)和对照组中的抗原特异性t细胞的数量。如果在从疑似组中回收的装置中检测到比从对照组回收的那些装置中更多的(例如在统计学意义上)抗原特异性t细胞,则进行阳性诊断。另外地,根据诊断,可以用治疗剂治疗疑似组。治疗的受试者中抗原特异性t细胞的数量可以随时间进行比较,并且也与健康受试者中存在的那些相比较。根据结果,研究人员可以推断治疗的有效性,并还能随时间推移监测治疗进展/疾病的消退。类似的方案可用于癌症患者和患有自身免疫性疾病的受试者的诊断、监测和管理中。
受试者是动物,优选哺乳动物或鸟。特别优选的是,受试者选自人、狗、猫、猪、牛、水牛和马。最优选地,受试者是人。
任何免疫细胞可用于诊断疾病或病症。优选地,用淋巴细胞,例如t细胞、b细胞、树突状细胞或apc,例如巨噬细胞或其组合进行诊断。特别优选在诊断中使用t细胞。
可以使用上述方法检测或诊断任何疾病或病症。特别优选地,该疾病是自身免疫性疾病,其选自于类风湿性关节炎、狼疮、乳糜泻、炎性肠病或克罗恩病、
在另一个实施方式中,该疾病是选自于细菌性疾病、病毒性疾病和真菌性疾病或其组合的病原体性疾病。
因此,本发明的实施方式涉及通过施用含有对自身免疫性疾病、癌症疾病或病原体性疾病特异性的抗原的本发明装置来检测或诊断受试者中的自身免疫性疾病、癌症或病原体性疾病,并分析其中含有的免疫细胞。可以任选地移植出装置以回收免疫细胞。在原位进行检测/分析步骤是可能的。
相关的实施方式涉及监测受试者中的疾病进展的方法。该方法包括对受试者施用含有对该疾病特异性的抗原的本发明装置并分析其中所含的免疫细胞。捕获在装置中的免疫细胞的数量/类型可以提供关于疾病进展的有价值的线索。或者,在其中受试者已经经历了治疗性干预的情况中,可以使用类似的方法来监测疾病的治疗和/或疾病管理。
上述方法可用于监测自身免疫性疾病、癌症、病原体性疾病等的进展/治疗。优选地,用于诊断方法的免疫细胞是t细胞或b细胞。
在自身免疫性疾病的情况下,可以通过分析自身反应性t细胞的数量和/或类型来监测疾病的进展。根据分析的结果,可以设计干预和/或治疗方法以使症状的严重程度最小化。在其他情况下,可以进行预防方法,包括向受试者提供关于饮食、营养和/或其他生活方式改变的建议。
产生用于疾病治疗的新型组合物和疫苗
本文描述的实施方式还涉及用于设计和产生用于治疗疾病的新型组合物的方法。该方法包括向受试者施用含有疾病特异性抗原的本发明的装置,其然后捕获对疾病特异性的免疫细胞,任选地分离、富集和扩增在该装置中捕获的免疫细胞,然后将免疫细胞施用回到受试者中。或者,可以向受试者施用衍生自这些免疫细胞的产物。衍生自免疫细胞的产物的实例包括核酸(包括载体和含有此类核酸的细胞)、肽、蛋白质、抗体、细胞因子等。
优选地,该疾病是自身免疫性疾病。在该实施方式中,通过前述方法分离(和任选地如本文所述的在培养物中扩增)的自身反应性t细胞可以被原位或非原位灭活。灭活t细胞的方法是本领域已知的。实例包括,但不限于化学灭活或照射。可以使用本领域技术人员已知的许多技术,包括但不限于冷冻保存,在灭活之前或之后保存自身反应性t细胞。如下所述,组合物可以用作在自身免疫患者中消耗自身反应性t细胞的疫苗。
在一个实施方式中,该疫苗可以包含自身反应性t细胞,其包含vβ-dβ-jβ基因使用的均质(“单克隆”)或异质(“多克隆”)模式。临床研究表明,接受自体单克隆t细胞疫苗接种的自身免疫患者可以显示出对自身反应性t细胞的免疫性的逐渐下降。在一些情况下,再现的自身反应性t细胞可以来源于不同的克隆群体,这表明t细胞可能经历与正在进行的疾病过程潜在相关的克隆变换(clonalshift)或表位扩散。克隆变换或表位扩散可以是由自身反应性t细胞介导的自身免疫疾病中的问题。包含能够耗尽多种自身反应性t细胞群体的多克隆自身反应性t细胞的疫苗可以避免克隆变换或表位扩散的问题。
本文所述的实施方式还涉及通过上述方法制备的组合物和疫苗。组合物可以是药物组合物,其可以使用本领域熟知的方法制备。在治疗疾病或病症中用作临床前和临床治疗剂的药物组合物可以由本领域技术人员使用可接受的诊断和治疗原理来产生。
疾病的治疗
本文所述的实施方式还涉及用于治疗受试者的疾病或病症的方法。在一个实施方式中,该疾病是癌症。在另一个实施方式中,该疾病是自身免疫性疾病。在第三实施方式中,该疾病是病原体性疾病。
在这些实施方式中,可以通过首先向受试者施用本发明的装置来治疗患有疾病的受试者,其中该装置中的抗原对该疾病是特异性的。这些装置然后允许在受试者中保持一段时间,例如0.5天、1天、2天、5天、7天、14天、25天、30天、35天、38天、45天、50天、60天或更长时间,并且其中包含的细胞使用一种或多种上述技术操作。例如,在自身免疫性疾病的情况下,被操作的细胞可以包括t细胞、b细胞、抗原呈递细胞或其组合。在癌症治疗的情况下,被操作的细胞可以包括t细胞或b细胞。在病原体性疾病的情况下,被操作的细胞可以包括抗原呈递细胞。操作的实例包括例如激活、分裂、分化、生长、扩增、重编程、无能性、静息、衰老、细胞凋亡、死亡等。细胞不需要装置中物理移除以被操作。因此,在一个实施方式中,细胞在原位操作(例如,在植入位点处或附近)。在其它实施方式中,细胞被非原位操作(例如,在与植入位点不同的位点处)。
因此,本发明的实施方式提供了用于治疗受试者中的癌症的方法。该方法包括向受试者施用本发明的装置(其中所述多种抗原对癌症是特异性的),收集被捕获在该装置中的多种免疫细胞(其中所述多种免疫细胞对所述多种抗原是特异性的),并将多种免疫细胞或从其衍生的产物施用于受试者,从而治疗癌症。
癌症抗原的代表性实例包括但不限于mage-1、mage-2、mage-3、cea、酪氨酸酶、中期因子、bage、casp-8、β-连环蛋白、β-连环蛋白、γ-连环蛋白、ca-125、cdk-1、cdk4、eso-1、gp75、gp100、mart-1、muc-1、mum-1、p53、pap、psa、psma、ras、trp-1、her-2、trp-1、trp-2、il13rα、il13rα2、aim-2、aim-3、ny-eso-1、c9orf112、sart1、sart2、sart3、brap、rtn4、glea2、tnks2、kiaa0376、ing4、hsph1、c13orf24、rbpsuh、c6orf153、nktr、nsep1、u2af1l、cynl2、tpr、sox2、golga、bmi1、cox-2、egfrviii、ezh2、licam、livin、livinβ、mrp-3、巢蛋白、olig2、art1、art4、b-细胞周期蛋白、gli1、cav-1、组织蛋白酶b、cd74、e-钙粘蛋白、epha2/eck、fra-1/fosl1、gage-1、神经节苷脂/gd2、gnt-v、β1,6-n、ki67、ku70/80、prox1、psca、sox10、sox11、存活素、upar、wt-1、二肽基肽酶iv(dppiv)、腺苷脱氨酶结合蛋白(adabp)、亲环蛋白b、结肠直肠相关抗原(crc)-c017-1a/ga733、t细胞受体/cd3-ζ链、肿瘤抗原gage家族、rage、lage-i、nag、gnt-v、rcasl、α-胎蛋白、pl20ctn、pmel117、prame、脑糖原磷酸化酶、ssx-i、ssx-2(hom-mel-40)、ssx-i、ssx-4、ssx-5、scp-i、ct-7、cdc27、腺瘤性结肠息肉病蛋白(apc)、胞衬蛋白、pla、连接蛋白37、ig-个体遗传型、pl5、gm2、gd2神经节苷脂、肿瘤抗原smad家族、lmp-1、ebv-编码的核抗原(ebna)-i、ul16-结合蛋白样转录物1(mult1)、rae-1蛋白、h60、mica、micb和c-erbb-2或其免疫原性肽,及其组合。
优选地,免疫细胞是与一种或多种上述抗原特异性结合的t细胞或b细胞。可用于实施本发明的癌症治疗方法的细胞产物包括例如,b细胞的杂交瘤、t细胞的稳定谱系、源自b细胞或其杂交瘤的抗体、与癌症抗原结合的受体(结合呈递抗原的mhc分子的受体),包括其片段、编码受体或其抗原结合结构域的核酸、编码抗体的核酸,包括全细胞。
本发明的实施方式提供了用于治疗受试者中的病原体性疾病的方法。该方法包括向受试者施用本发明的装置(其中多种抗原对病原体性疾病是特异性的),收集被捕获在该装置中的多种免疫细胞(其中该多种免疫细胞对多种抗原是特异性的),并将多种免疫细胞或其衍生的产物施用于受试者,从而治疗病原体性疾病。在一些情况下,可以预防性施用免疫细胞或由其衍生的组合物,例如在受试者中的疾病症状发作之前。
可以根据上述实施方式治疗的病原体性疾病包括细菌性疾病、病毒性疾病、真菌疾病或其组合。
可用于治疗本发明的病原体性疾病的细胞产物包括例如,b细胞的杂交瘤、t细胞的稳定谱系、源自b细胞或其杂交瘤的抗体、与病原体性抗原结合的受体(和/或结合呈递病原体抗原的mhc分子的受体)、这种抗体或受体的片段、编码受体、抗体或其抗原结合结构域的核酸,包括全细胞。
本发明的实施方式提供了用于治疗受试者中的自身免疫性疾病的方法。该方法包括向受试者施用本发明的装置(其中多种抗原对于自身免疫性疾病是特异性的),收集被捕获在该装置中的多种免疫细胞(其中该多种免疫细胞对多种抗原是特异性的),并将多种免疫细胞或其调节剂施用于受试者,从而治疗自身免疫性疾病。
在自身免疫性疾病的情况下,可能优选的是不施用活性免疫细胞(因为它们是自身反应性的),而是静息、衰老或灭活的免疫细胞。优选地,免疫细胞是t细胞。或者,可以施用免疫细胞的调节剂。这些可以包括例如,抑制性t细胞或调节性t细胞。
因此,在一些实施方式中,本发明提供了一种通过向有需要的受试者施用本发明的装置治疗自身免疫性疾病的方法(其中所述装置中的多种抗原对于自身免疫性疾病是特异性的),收集装置中捕获的多种调节性或抑制性t细胞(其中所述多种调节性或抑制性t细胞对抗原是特异性的),并且将多种调节性t细胞或抑制t细胞或其衍生的产物施用于受试者中,从而治疗自身免疫性疾病。
可用于实行自身免疫性疾病的治疗的细胞产物包括例如,结合自身反应性细胞的抗体和受体、位于抑制子或调节性t细胞中的调节性蛋白,包括编码这些分子的核酸序列。
在上述治疗实施方式中,细胞可以以包括从约5×102个细胞/ml至约1×109个细胞/ml的总细胞浓度配制。t细胞的优选剂量范围为约2×106个细胞至约9×107个细胞。
本发明的实施方式还涉及通过施用一种或多种上述组合物来治疗疾病。组合物可以是通过实现其预期目的的任何方式施用的药物组合物。例如,施用可以通过胃肠外、皮下、静脉内、动脉内、皮内、肌内、腹膜内、经皮、经粘膜、脑内、鞘内或心室内途径。可选地或同时,可以通过口服途径施用。药物组合物可以通过浓注或随时间的逐步灌注而肠胃外施用。
施用的剂量可以取决于接受者的年龄、性别、健康和体重、同时治疗(如果有的话)的种类、治疗频率、以及所需效果的性质。用于施用药物组合物的剂量范围可以足够大以产生期望的效果,由此例如,自身反应性t细胞被耗尽和/或显著预防、抑制或治疗自身免疫性疾病。剂量可能不会太大以引起不良副作用,例如不期望的交叉反应、全身性免疫抑制、过敏性反应等。
与疾病相关的免疫细胞库的测定
本文公开的实施方式还涉及用于测定患有疾病的受试者中的编码一种或多种免疫细胞受体或其部分的核酸库的方法。所述方法包括扩增编码从由本发明的装置所捕获的细胞获得的一种或多种免疫细胞受体的核酸。优选地,该免疫细胞是t细胞或b细胞,和该免疫细胞受体分别是t细胞受体(tcr)和b细胞受体(bcr)。用于从全细胞裂解物靶向和扩增靶向核酸构建体的方法是本领域已知的。参见maryanski等,immunity,vol.4,47-55页,1996,其通过引用并入本文。
在这些实施方式中,受试者患有自身免疫性疾病,例如i型糖尿病、多发性硬化症、类风湿性关节炎(ra)、炎性肠病(ibd)或克罗恩病(cd),或其它胃肠道自身免疫病症。可以用与上述疾病相关的各种抗原对从装置收集的细胞群体进行进一步选择,且可以基于其中表达的细胞表面受体的序列来表征通过抗原引发选择的免疫细胞库。在一个代表性的方法中,免疫细胞是t细胞,并且基于参与与疾病抗原(例如与t1d相关的抗原)的结合的t细胞受体的序列来表征。
捕获细胞以分析病原体和/或其各种株系
免疫系统使用各种角色来检测和从身体中去除病原体。例如,病原体可以被巨噬细胞摄取,其消化并处理它们以将其呈递在细胞表面主要组织相容性复合物(mhc)分子上,从而允许淋巴细胞识别它们。因此,本发明的实施方式通过分析对病原体特异性的免疫细胞来提供对病原体的检测和分析。病原体可以是细菌、病毒、真菌或其组合。
因此,根据上述实施方式,本发明提供了募集免疫细胞,例如t细胞、b细胞、巨噬细胞或树突状细胞的捕获器,其中该免疫细胞对目的病原体是特异性的。特别地,免疫细胞是结合病原性抗原的t细胞或b细胞。或者,免疫细胞是抗原呈递细胞,例如树突状细胞或巨噬细胞。在这些实施方式中,将含有对病原体特异性的多种抗原的装置施用到受试者中一段时间(例如,1周至3周),并分析其中所含的免疫细胞的特异性和/或与病原体抗原的结合。基于它们对抗原中包含的特定表位的反应性,细胞可以被进一步分成不同的亚群。任选地,细胞可以被配制成用于治疗病原体性疾病的免疫组合物。优选地,免疫组合物是树突状细胞组合物。
表6中提供了病原体和病原性抗原的代表性列表,包括ncbi/gi登录号。
在相关的实施方式中,本发明提供了用于捕获对新细菌抗原特异性的免疫细胞的装置。例如,在分枝杆菌的背景下,mpb70和mpb83已被充分地研究并且被广泛了解。然而,由于它们在结核分枝杆菌中表达较少(在牛型结核分枝杆菌中表达更高),它们对结核分枝杆菌病原性的参与尚未明了。可以实施本发明的装置以识别可由免疫细胞和/或其产物特异性靶向的相关菌株中的新的/关键的病原性抗原。例如,可以将源自牛型结核分枝杆菌的含有mpb70和mpb83蛋白的装置植入受试者中以分离可以测试与结核分枝杆菌的交叉反应性的免疫细胞群体。交叉反应的免疫细胞可以被分型以用于测定参与交叉反应性的受体和分子。因此,可以鉴定与其结合的新靶标和治疗剂。
表6.各种类型的病原体、病原性抗原的示例性形式及其相应的ncbi和gi登录号:
viii.试剂盒
在某些实施方式中,本发明提供了在一个或单独的隔室中包含本发明的装置的试剂盒。该试剂盒还可以包含在一个或多个隔室中的另外的成分,例如胶凝剂、润肤剂、表面活性剂、湿润剂、粘度增强剂、乳化剂。试剂盒可以任选地包含用于配制用于诊断或治疗应用的装置的说明书。该试剂盒还可以包含在各种病症和/或疾病的治疗或诊断中单独或一起使用该组分的说明书。
在相关的实施方式中,本发明提供的试剂盒包含本发明的装置,以及用于选择、培养、扩增、维持和/或移植被捕获的目标细胞的试剂。用于t细胞、b细胞和抗原呈递细胞的细胞选择试剂盒、培养试剂盒、扩增试剂盒、移植试剂盒的代表性实例是本领域已知的。例如,当目标靶细胞是b细胞时,它们最初可以使用dynabeads,macs-珠(miltenyibiosciences)分类,维持在rosettesep培养基(stemcelltechnologies)中,和使用cellexvivo人b细胞扩增试剂盒(r&dsystems)扩增。可以通过使用本领域技术人员已知的离心技术(包括但不限于
通过以下实施例进一步说明本发明,这些实施例不应被理解为限制性的。在本申请中引用的所有参考文献、专利和公开的专利申请的全部内容以及附图和序列表通过引用并入本文。
实施例
实施例1:装置制造和表征
根据上述方法,用于装置的聚合支架被工程化以维持抗原呈递。简而言之,如下进行装置制造:丙交酯和乙交酯的共聚物(plg)(alkermes,cambridge,ma)用于气体发泡过程中以形成plg支架。为了将抗原物理吸附到plg聚合物上,使用气体发泡微粒浸出以制造用作捕获器的支架。图1a示出了用plg制成的模型装置的横截面扫描电子显微镜(sem)图像的显微照片(右侧的图显示了孔隙的放大视图)。或者,可以使用其它聚合物(如藻酸盐)作为装置的结构元件。该孔隙提供了t细胞渗透和扩张的空间。图1b显示ova-t细胞捕获器能够释放卵清蛋白(ova)蛋白(模型抗原)。
将装置进一步皮下植入小鼠背部中14天的时间。图1c是显示在植入位点处的mip-1a和rantes的局部细胞因子浓度的条形图。b和c中的值表示平均值和标准偏差(n=5)。可以看出,与对照相比,每种细胞因子的局部细胞因子浓度在捕获器植入位点处显著较高。通常,抗原特异性t细胞具有在t细胞受体(tcr)-抗原识别时进入呈递相应抗原并增殖的能力的发炎组织。当皮下施用显示抗原的t细胞捕获器时,它们促进局部mip-1a和rantes产生,其类似于炎症和自身免疫病变的位点。捕获器含有抗原(或抗原混合物),其与t细胞上的特定tcr结合以变为粘性的并保留在装置中。这种抗原相互作用也导致t细胞在装置内增殖,从而富集局部区域的这些细胞。
实施例2:装置的植入
将加载有模型抗原,卵清蛋白(ova)的捕获器和对照捕获器植入具有预先存在的ova特异性t细胞池的ot-1小鼠中。14天后,移植出支架,收获细胞并对于cd8和ova四聚体进行染色。含有ova的捕获器富集ova特异性t细胞(图2a),并且相对于对照具有约5-8倍多的t细胞(图2b)。当将含有独特抗原混合物(对于ova或黑素瘤抗原)的两种不同的捕获器植入小鼠中时,t细胞优先在加载有同源抗原的捕获器中累积(图2c)。ova特异性t细胞在ova捕获器中显著地累积,而trp2(黑素瘤抗原)特异性t细胞在黑素瘤捕获器中显著累积(图2c和图2d)。在不含相应抗原的捕获器中基本上不含ova和黑素瘤特异性细胞(图2c和图2d)。
实施例3:在糖尿病进展期间t细胞的捕获
在该领域公认的1型糖尿病的小鼠模型中证实了抗原特异性的捕获。通过用β-细胞裂解物加载plg支架制备糖尿病t细胞捕获器(图3a)。然后将这些捕获器移植至9、12和15周龄的非肥胖糖尿病(nod)小鼠中持续2周,此时测定他们的t细胞浸润(图3b)。在nod小鼠中,如图3b所示,胰岛的胰岛炎或t细胞浸润如所预测地随年龄而增加。特别地,发现捕获器相对于对照显著地累积t细胞,并且浸润与胰腺中的胰岛炎相关(图3b和图3d)。捕获器中的t细胞总数不仅随着糖尿病进展而增加,而且t细胞群体也被富集。与对照相比,捕获器中的t细胞数量有3到5倍的差异。
实施例4:捕获的t细胞的表征
在11、14和17周龄的nod小鼠中植入14天后收获t细胞。与收获的t细胞一起培养胰腺β细胞靶标。使用elispot测定法测量il-2分泌。结果示于图4a中。已经发现,如通过elispot所证实的(图4a),从捕获器分离的t细胞的大亚组(12%的t细胞)在体外对β细胞靶标有反应。相比之下,对照捕获器完全没有对胰腺β细胞反应性的t细胞。捕获器包含相对于对照捕获器和小鼠脾脏的富集的β细胞特异性t细胞的水平,表明相对于血液中的t细胞水平,可以从捕获器获得更高的t细胞数量和富集的特异性。分析捕获器中的t细胞并将其与脾脏中的t细胞进行比较以作为血液水平的标志物。鉴定在捕获器中的糖尿病特异性细胞,其相对于血液浓度富集约4000%(图4b)。
实施例5:捕获和收获癌症特异性t细胞
多孔支架加载有疾病的抗原和其他分子谱。一组捕获器含有ova抗原的独特混合物,另一组含有黑色素瘤抗原的独特混合物。已发现对抗原特异性的t细胞优先累积于加载有同源抗原的捕获器中(图5c)。更具体地,ova特异性t细胞在ova捕获器中显著累积,而trp2(黑素瘤抗原)特异性t细胞在黑素瘤捕获器中显著累积(图5d)。相反,在不含相应抗原的捕获器中不存在ova和黑素瘤特异性细胞(图5c和图5d)。这些结果表明,可以基于在支架中提供的抗原而捕获和收获抗原特异性t细胞。
实施例6:将功能性t细胞转移至宿主
将t细胞捕获器和空白支架皮下植入15周龄的nod小鼠中持续14天。然后从这些支架中分离细胞,并通过眶后注射将2×106个细胞转移到nodscid小鼠。作为阳性对照,将来自17周龄的nod小鼠的脾细胞也注射到nod-scid受体中。细胞转移后,通过测量血糖监测小鼠的糖尿病发病。
接受nod来源脾细胞的nod-scid小鼠在细胞注射后15周开始发生糖尿病,且88%在第20周变成糖尿病(图6)。捕获的细胞以较快动力学诱导糖尿病,因为20%的小鼠在第9周时变为糖尿病的,和100%的小鼠在20周时变为糖尿病的。从对照支架提取的细胞完全不能在scid小鼠中诱导糖尿病。这些数据表明,捕获器能够特异性地募集可以被转移到宿主中的功能性t细胞。
总的来说,实施例5和6表明,可以使用加载有疾病的抗原和分子谱的本发明的多孔支架原位产生和/或收获t细胞。结果表明,可以在可能被收获的这些体内捕获器处吸引和产生抗原特异性t细胞,其类似于它们如何在疾病的原发部位归巢和扩增。这些细胞在体内产生,并且还可以通过从捕获器递送生长因子/细胞因子而进一步扩增。令人惊奇的和意外地,发现被捕获的疾病特异性t细胞的功能性在过继转移到宿主中之后被维持。
实施例7:捕获用于临床或分析用途的细胞
使用上述制造方法构建t细胞捕获器、b细胞捕获器和/或树突状细胞捕获器。例如,t细胞捕获器可以利用表1所示的不同的趋化因子/细胞因子。同样,树突状细胞/巨噬细胞的示例性捕获器可以利用表2所示的细胞因子/趋化因子。类似地,b细胞捕获器可以包括如表3所示的各种细胞因子/趋化因子。对于每种类型的捕获器,可以任选地使用其它试剂,例如白细胞介素、生长因子、螯合剂、粘附受体或其它化合物/分子。表4提供了可以任选地在t细胞、b细胞或dc/巨噬细胞捕获器中使用的白细胞介素的列表。表5提供了t细胞粘附受体的列表。
抗原加载是区分t细胞与dc的有效归巢剂。然后分析这些免疫细胞以了解疾病发病机制并识别诸如抗原的治疗靶点。目前无法达到致病的t细胞,因为它们仅集中在自身免疫病变中。本文描述的捕获器技术提供了用于收集这些细胞的手段。
如上所述,将装置植入受试者中至少一天和最长14天或更长时间。细胞可以在装置内增殖,且加载有免疫细胞的装置可以在从第1-28天或更长时间,例如30天、60天、3个月、6个月、9个月、12个月、18个月、24个月、36个月、48个月或更长时间中的任何时间移植出。装置可以定期地监测。
等同:
本领域的技术人员可以认识到或者能够只使用常规实验确定本文所述的具体实施方式和方法的许多等同方式。这些等同方式意在被包含在以下的权利要求的范围中。
- 该技术已申请专利。仅供学习研究,如用于商业用途,请联系技术所有人。
- 技术研发人员:O·A-R·阿里;D·J·穆尼
- 技术所有人:哈佛学院院长等
- 我是此专利的发明人
- 该领域下的技术专家
- 如您需求助技术专家,请点此查看客服电话进行咨询。
- 1、司老师:1.制浆造纸 2.植物资源精细化工与化学 3.生物质精炼 4.天然产物化学
- 2、薛老师:1.CRISPR-Cas系统 2.基因编辑 3.基因修复 4.天然产物合成 5.单分子技术开发与应用
- 3、戴老师:1.天然药物(中药)合成生物学研究 2.酵母生物学与工程化研究
- 4、孟老师:1. 基于糖类的抗肿瘤药物的合成和活性评价及糖类疫苗的研制 2.功能糖类的化学酶法合成及构效关系研究 3.多糖及仿生材料功能的开发及应用
- 5、满老师:1.天然产品的提取分离与活性研究 2.天然产物活性与安全性评价 3.中药组方配伍机制研究
- 如您是高校老师,可以点此联系我们加入专家库。
- 还没有人留言评论。精彩留言会获得点赞!