用于治疗干型和湿型年龄相关性黄斑变性或糖尿病视网膜病变的可注射的多孔装置的制作方法
相关申请的交叉引用
根据35u.s.c.§119(e),本申请要求于2015年6月24日提交的美国临时申请第62/184,151号和于2015年8月13日提交的美国临时申请第62/204,877号的权益,在此将所述申请通过引用整体并入本文。
背景
本申请一般涉及年龄相关性黄斑变性(amd)和糖尿病视网膜病变,其为两种引起进行性视觉障碍和失明的常见眼部疾病。
相关技术描述:
年龄相关性黄斑变性(amd)是老年群体中严重视觉丧失的常见原因。amd分为两种亚型:萎缩型(干型)和渗出型(湿型)。干型(也被称为萎缩型)通常由导致视网膜色素内皮和感光器的退化的进行性原因来表征。渗透型与视网膜下黄斑区的脉络膜新生血管化以及随后的出血和/或流体渗漏相关,其可以导致视觉突然丧失;它是amd最快速的进行性形式。患有中期和晚期amd的所有人中,超过80%是干型,该形式可以发展为导致显著更多视觉损失的湿型。
年龄相关性黄斑变性的早期与最小视觉损伤相关,并且由黄斑中大的玻璃膜疣和色素异常来表征。玻璃膜疣是视网膜色素上皮基底膜下的非细胞的无定形碎片的积累。几乎所有超过50岁的人在其一个或两个眼中均具有至少一个小的玻璃膜疣。仅具有大的玻璃膜疣的眼具有晚期年龄相关性黄斑变性的风险。
玻璃膜疣的存在是两种类型amd的常见临床特征。在“干”型黄斑变性中,视网膜的变性与黄斑下的玻璃膜疣,即黄斑下小的黄色沉淀的形成相关。该现象据信导致黄斑变薄和干燥,引起功能的进行性损失。中央视觉损失的量与玻璃膜疣引起的视网膜变薄的位置和量直接相关。
干型黄斑变性比湿型黄斑变性更常见,并且其趋向于比湿型更慢发展。但是,一定比例的“干”型黄斑变性随着时间的流逝变为“湿”型。对于“干”型黄斑变性,并无已知的治愈方法。
可获得数种用于减缓湿型amd发展的疗法。这些疗法旨在封闭渗漏的血管或者防止血管再生长(抗血管生成疗法)。所有这些均需要重复治疗,并且这些均不能恢复已经损失的视觉。
糖尿病视网膜病变是引起血管肿胀和视网膜周围渗漏流体的眼部疾病。可获得的用于减缓糖尿病视网膜病变的发展的治疗包括激光密封血管和重复注射抗炎药。
发明概述
本文公开了能够预防amd(干型和湿型)的发展或者逆转amd(干型和湿型)的病理学症状的可注射的多孔装置,以及使用该装置治疗amd的方法。该装置还能够预防糖尿病视网膜病变的发展。
更具体地,本文提供降低或预防有需要的哺乳动物受试者的眼内玻璃膜疣的形成的方法,所述方法包括:
将一种或多种微孔装置植入眼内,各微孔装置具有装置主体和外表面,
其中所述微孔装置由生物相容性弹性材料形成,并且包含多个贯穿所述装置主体并延伸至所述外表面的互连孔,以及
其中所述微孔装置内基本上所有互连孔各自均与至少2个其它孔互连,所述孔的平均直径为约5至约50微米,并且任意两个相邻孔通过喉管连接,平均的喉管直径为至少5微米。
具体地,本文公开的装置含有多孔生物材料,其中优化孔的几何形状,以当手术植入软组织内时,将高浓度的巨噬细胞吸引至它的孔内。特别合适的材料是如美国专利第8,318,193号中所述的
装置的微孔结构使得在邻近视网膜处吸引并积累足够局部浓度的功能性巨噬细胞成为可能。这些吞噬性巨噬细胞的清除功能可以降低玻璃膜疣的积累或者将玻璃膜疣的浓度降低至非病理水平。
装置能够增加巨噬细胞趋化因子的局部浓度,这可以恢复身体吸引功能性巨噬细胞以清除并移除玻璃膜疣和已知的促进amd发展的其它细胞废弃产物的能力。
除了促进玻璃膜疣的清除之外,装置还可以预防引起玻璃膜疣形成的炎性细胞因子的局部积累。装置的孔结构促进植入物附近的组织中持久的“促进治愈(pro-healing)”区域的形成。具体地,多孔植入物周围富含有利的m2表型巨噬细胞。m2巨噬细胞“促进治愈”,因为它们释放保护细胞不受炎症的破坏性影响的抗炎性细胞因子。e.m.sussman等人,annalsofbiomedicalengineering,42(7),1508-1516(2014)。
装置的另一方面是,其降低组织中细菌的局部浓度。这通过缓解炎症水平来进一步帮助预防amd的发展。
装置的另一方面是,其能够恢复装置周围组织内生长因子的健康自然平衡。这能够预防作为更晚期“湿”型amd特征的渗漏血管的形成。装置的这一方面还使得其可用于治疗糖尿病视网膜病变。
如在美国专利第8,927,022号中所述,在一些实施方案中,装置可以包含单个装置,而在其它实施方案中,它可以包含多个多孔颗粒、杆状物或者其它形状,将该专利通过引用整体并入本文。
在一些实施方案中,可以通过经针或其它管状插入装置注射而将装置植入眼球后间隙、眼球周围间隙、特农氏间隙下(sub-tenon’sspace)、玻璃状液或者眼部其它组织。延长的杆状物对其特别适合。
在一些实施方案中,可以经切口进针(abinterno)法插入该装置(通过角膜插入针以到达期望的组织)。
本发明的另一方面是,优选实施方案是可压缩的(由于多孔性)并且是弹性的(由于弹性材料)。将装置压缩进具有比该装置直径更小的直径的管状针内是可能的。还允许该装置在植入期间从针中退出。
在一些实施方案中,可以组合使用多种注射以达到效力。
在一些实施方案中,装置可以大于可注射尺寸,在该情况下,可以通过切口将其手术置入巩膜下袋(subscleralpocket)或者眼部其它组织内。
在一些实施方案中,装置可以预装载药物或其它生物活性剂,如抗炎剂、抗生素或生物活性蛋白。在一些实施方案中,装载的药物可以随时间释放。在其它实施方案中,药物可以提供活性,且与装置永久相连。本发明的有利方面是,孔的几何形状对感染具有抗性。装置内孔的表面被粘附的抗菌表型的巨噬细胞完全覆盖。以这种方式,装置利用身体的天然防御机制来提供持久的抗菌活性。
附图简要描述
图1a是本公开一个实施方案所述的可注射的软的多孔杆状装置的示意图。
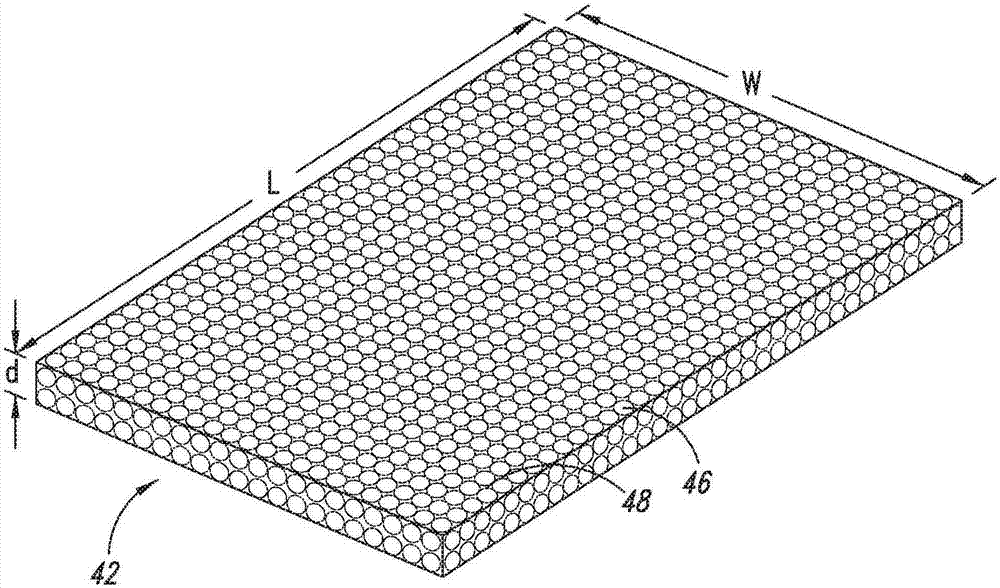
图1b是本公开一个实施方案所述的软的多孔片状装置的示意图。
图2是一个实施方案所述的可注射的软的多孔杆状装置的扫描电子显微镜(sem)图像。
图3显示了装置的开孔结构,指示了孔和喉管的尺寸。
图4a-4c示意性示出软的多孔可注射的杆状装置,其被径向压缩进注射针的孔内(图4a),从针的末端被部分推出(图4b),以及被完全推离针的尖端(图4c)。
图5示出了皮下植入小鼠28天的不同孔径的球状模块化微孔支架的组织切片;用bm8巨噬细胞标志物对切片进行染色。孔径:(a)20微米;(b)35微米;(c)50微米;(d)70微米(e)90微米。具有35微米孔的支架包含最高浓度的巨噬细胞。
详细描述
迄今为止,还没有可用于干型amd的有效治疗。amd发展的主要因素是玻璃膜疣的形成和积累。
本文公开了能够预防玻璃膜疣的形成和积累的可植入装置。被称为“玻璃膜疣”的细胞外沉淀已知随着人年龄的增长在其眼内积累。可在眼底检查下直接观察到玻璃膜疣,并且可以根据相对大小、丰度和形状将其分为软玻璃膜疣或硬玻璃膜疣。玻璃膜疣通常在视网膜色素上皮(rpe)基底膜和bruch膜内部胶原层下形成。黄斑内玻璃膜疣的过度(excessive)区域或融合(confluent)区域与脉络膜视网膜病症(如年龄相关性黄斑变性(amd))的发展相关。因此,装置能够预防amd的发展和/或减轻疾病的病理学症状。
装置能够为“干型”amd和“湿型”amd这两类患者提供益处。装置或植入物是多孔的,并且设计为注射进眼部组织内,如注射进视网膜后的眼球后间隙或眼球周围间隙内。装置的可选实施方案可以为注射进巩膜下间隙或玻璃状液内。
本文提供了降低或预防有需要的哺乳动物受试者眼内玻璃膜疣的形成的方法,所述方法包括将一种或多种微孔装置植入眼内,各微孔装置具有装置主体和外表面,其中所述微孔装置由生物相容性弹性材料形成,并且包含多个贯穿所述装置主体并延伸至外表面的互连孔。
因此,微孔装置具有开孔结构,其包含贯穿装置主体整块并延伸至装置表面的互连孔。
图1a是本公开的实施方案的示意图,其用长度(l)和直径(d)显示了具有延长的杆状的装置主体10。装置主体是软的多孔材料,其具有在装置主体内并延伸至外表面(18)的孔(16)。在不同实施方案中,长度范围为3-10mm,或者更典型地,范围为3-5mm。在不同实施方案中,直径范围为0.2-0.8mm,或者更典型地,范围为0.4-0.6mm。
尽管杆状与注射特别兼容,但是本公开的装置或植入物可以是任何形状,并且可以通过本领域技术人员已知的任何方式插入。在一些实施方案中,可以使用平的片状以允许为充足的效力提供足够的装置体积和表面积。通常而言,不管形状为何,装置的最长尺寸为约3-10mm;而装置的厚度(例如,杆状装置的直径或者片状装置的厚度)为约0.2-0.8mm。
图1b是装置主体42的另一实施方案的示意图,其是微孔材料片或微孔材料膜。如在杆状装置中,片具有贯穿其整个装置主体并延伸至外表面(48)的孔(46)。除了片适合于眼内的解剖间隙或手术产生的间隙之外,长度(l)、宽度(w)和厚度(d)并未具体限定。片的厚度应当足够薄,以适合所期望的组织间隙。例如,厚度(d)为约0.2mm至0.8mm,或者优选约0.2mm-0.5mm。
图2是扫描电子显微镜(sem)图像,其显示了本公开一个实施方案所述的杆状装置主体10。装置主体由生物相容性材料,例如弹性材料制成,并且包含多个基本互连的孔。在优选实施方案中,装置包括美国专利第8,318,193号所述的球状模块化的硅酮材料。
图3是扫描电子显微镜(sem)图像,其显示了特别适用于本发明的球状模块化多孔生物材料的装置的横截面。孔的结构包括本文称为孔20的互连的空隙空间网络。邻近的孔20通过开口或“喉管”30连接或相连。孔20可以是如图2的球状,或者它们可以是导致通常的开孔孔状结构的任何其它的孔形状。喉管30可以是如图2的圆形,或者它们可以是限定邻近孔20之间开口大小的任何其它2d形状。如果孔喉管不是圆形,则将喉管直径t定义为可以通过喉管30的最大球状物体的直径。
有利地是,可以控制孔的大小和喉管直径(即相邻孔之间开口的尺寸),以允许巨噬细胞或中性粒细胞浸润,并增加巨噬细胞和嗜中性粒细胞的可到达区域。因此,在某些实施方案中,微孔装置中基本上所有的互连孔(即至少90%,或者至少95%,或者至少98%)各与至少2个其它孔互连,孔的平均直径为约5至约50微米,并且任意两个相邻孔通过喉管相连,平均喉管直径为至少5微米,或者至少8微米(microns),或者至少10微米。在优选实施方案中,平均喉管直径为约8至约15微米。如本文所使用的,“基本上所有孔”意为所有孔的至少90%,或者至少95%,或者至少98%。此外,“约”指特定值±20%的数值范围。例如,短语“约10微米”包括10微米±20%的范围,即8-12微米。
根据本公开,喉管直径足够大,以允许宿主巨噬细胞和中性粒细胞浸润孔结构。这些细胞能够攻击并破坏细菌,并预防细菌定植。人巨噬细胞直径通常为15-20微米,但是其能够通过直径为5微米小的开口挤过去。中性粒细胞的大小与巨噬细胞类似。因此,喉管直径t应该为至少5微米。在不同实施方案中,喉管直径应该为至少8微米,或者至少10微米。
在产生多孔材料(例如,根据美国专利第8,318,193号中公开的方法)期间可能形成小于5微米的喉管直径而言,应该注意使这些较小喉管直径的比例最小化。细菌细胞比巨噬细胞小得多,其大小通常为1至2微米。具有1至5微米大小范围的喉管的孔可以允许细菌进入,而防止通常将攻击并破坏细菌的大得多的巨噬细胞和中性粒细胞接近。因此,在某些实施方案中,仅非常小比例的喉管(少于2%,更优选少于1%)的直径t大小范围为1至5微米。
在其它实施方案中,微孔装置中所有喉管的至少90%的直径为至少5微米。在多个其它实施方案中,微孔装置中所有喉管的至少95%或者至少98%或者至少99%的直径为至少5微米。
在其它实施方案中,微孔装置中所有喉管的至少90%的直径为至少5微米。在多个其它实施方案中,微孔装置中所有喉管的至少95%或者至少98%或者至少99%的直径为至少5微米。
在其它实施方案中,微孔装置中所有喉管的至少90%的直径为至少8微米。在多个其它实施方案中,微孔装置中所有喉管的至少95%或者至少98%或者至少99%的直径为至少8微米。
另一重要特征是,孔的结构具有高生物相容性表面积,其中“生物相容性表面积”被定义为巨噬细胞可接近的表面积。表面积与孔径成反比,因此孔20的大小是测量生物相容性表面积的重要参数。平均(average)或平均(mean)孔径p应小于50微米,更优选小于40微米,并且最优选小于30微米。优选的是,孔径是最小的可能大小,其中孔可以通过最优大小范围为8至15微米的喉管互连。优选地,喉管直径t应是孔径p的约40%,如30%至45%,或者35%至45%。喉管大小与孔大小的比例太大导致孔结构在机械上易碎,因此,比例大于45%不可取。相反地,比例小于30%可具有较大的孔,并因而具有较小的生物相容性表面积,使得装置在用于抗菌防御或治疗效力的有效浓度,不吸引巨噬细胞进入其孔内部。
较小的装置插入的侵入性更小,并且可以向眼部不同位置植入多个装置。在不同实施方案中,装置或植入物的总外表面积(无论植入物的形状或数目为何)的范围可以是3-250mm2或者25-200mm2。
可以由任何弹性聚合物来制造装置。特别适用的聚合物是硅酮橡胶。nusilmed-4830、med-4840、med-4850、med-4860和med-6215是特别适用的组合物。其它可能的生物稳定性材料包括聚氨酯、聚丙烯、聚乙烯、硝酸纤维素、醋酸纤维素、聚四氟乙烯或水凝胶。在一些实施方案中,装置可以由生物可降解的聚合物来制造。
在一些实施方案中,装置可以由具有非常接近玻璃状液的折射率的透明生物材料来制造。这对于向玻璃状液中注射装置的实施方案特别有利,因为多孔生物材料与孔内向内生长的玻璃状液之间的折射率的紧密匹配确保了半透明,使对向视网膜的光路的干扰最小化。示例性的透明生物材料是nusilmed-6250硅酮弹性体,其折射率为1.41。玻璃状液的折射率为1.37。
更优选地,当在其无孔状态下测量时,弹性聚合物应具有较低的硬度值,理想地为30至60邵氏硬度a(shorea)。与刚性较高的材料相比,低硬度值与多孔性组合对组织的刺激性更小且炎性更小。以及优选地,弹性聚合物的最大伸长应变应大于100%,更优选大于300%,并且最优选大于500%。在一些实施方案中,高度伸长促进通过针或插入工具的注射。
对于注射针或插入工具,具有小的直径(通常为0.2-0.3mmid)是可取的,使得插入过程期间对眼部组织的创伤最小化。为了使装置足够大以提供有效的治疗强度,并且足够强以抵御在装载进插入针的孔内期间的损伤,优选直径为至少0.5mm。管状针或者插入工具的内部直径优选远小于装置的外部直径的直径。因此,对于装置而言,在装载进插入工具之前压缩至小于其松弛直径的一半将是有利的。完成此类径向压缩的一种方式是在轴向拉力下将装置拉伸至少300%应变。硅酮和其它类似的弹性材料具有接近0.5的泊松比,因此,例如,300%的轴向拉伸应变产生压缩直径为松弛直径的约50%的径向压缩。
图4a显示了注射针40的横截面的图,其中径向压缩的软的多孔装置主体10完全在内部直径为d1的针的孔内。压缩装置具有等于内部直径d1的压缩直径。图4b显示了在针末端内部的装置主体10的径向压缩的近端11以及远离针的远端的装置主体10的部分推出的径向扩展的远端12。在针外的部分装置扩展为其松弛直径d2。图4c显示了装置主体10,其完全扩展并被完全推离注射针的远端。
另一实施方案提供预装载微孔装置的针,其包括:具有0.2-0.3mm的内部直径的针,具有0.3-0.8mm的松弛直径的微孔装置,其中所述微孔装置被径向压缩,并置于所述针中,使得所述针与所述微孔装置纵向对齐,并且其中所述微孔装置如本文所述。
“松弛直径”是微孔装置在其天然、非压缩形状下的直径,所述形状可以是在插入针内之前的形状、退出针之后的形状或者在植入眼内时的形状。
为了径向压缩微孔装置,可将装置轴向拉伸。存在多种将轴向拉伸的装置装载进孔或插入工具的孔内的方式。一种方法包括下述步骤:1)使装置的孔在水性生物相容性盐水溶液或者其它生物相容性水性物质中吸水,2)通过握紧末端并应用轴向应变来延伸装置,3)快速冻结在含水且被拉伸的装置的孔内的水性溶液(例如通过浸入液氮或者其它低沸点液体中),4)将变窄且延伸的装置(通过孔内的冷冻的水而变硬)装载进插入工具的管状鼻元件中,以及5)允许水性溶液解冻,导致装置抵靠管状针的内壁扩展。一旦以该种方式装载,则装置已准备好通过使用温和的流体压力来注射进眼球后间隙(或者与视网膜非常接近的其它合适位置)内。
图5显示了孔大小与巨噬细胞局部浓度的相关性。还参见marshallaj.poroushydrogelswithwell-definedporestructureforbiomaterialsapplications.ph.d.dissertation,universityofwashington.2004aat3151637。
根据前述,将会理解,尽管本文出于说明的目的描述了本发明的具体实施方案,但是可在不偏离本发明的精神和范围的情况下做出各种改进。因此,除了受所附权利要求的限制之外,本发明并不受限。
可将上述的各个实施方案组合,以提供其它实施方案。将本说明书中提及的和/或申请数据表中列出的所有美国专利、美国专利申请公开、美国专利申请、外国专利申请以及非专利出版物通过引用整体并入本文。如果需要,可对实施方案的方面进行改进,以采用不同专利、申请和出版物的概念,从而提供其它实施方案。
- 还没有人留言评论。精彩留言会获得点赞!