球囊导引导管的制作方法
本发明涉及一种球囊导引导管,尤其是一种低压状态下能实现有效血管封堵的球囊导引导管,可用于临时封堵血管血流,依靠负压吸除颅内神经血管血栓或辅助各类介入器械完成颅内血管机械取栓,属于医疗器械技术领域。
背景技术:
脑血管疾病的介入技术作为一项具有代表性的微创治疗方式,近年来随着影像学设备的进步、新型介入器材的引入得以快速的发展,脑神经介入医生已经可以处理越来越复杂的病变,临床应用的病例越来越多,涉及的病种也越来越广泛。
脑神经血管的常规治疗方法之一——缺血性脑卒中静脉溶栓治疗法,存在治疗时间窗较短(4.5h以内)及血运重建率低(约30%)等缺点,限制了其疗效及广泛应用。在血管内通过球囊导引导管输送介入取栓器械的机械取栓或使用球囊导引导管完成吸栓的治疗方法具有出血少、创伤小、并发症少、安全可靠、术后恢复快等优点,成为急性缺血性脑卒中治疗的亮点,有比静脉或动脉溶栓更高的血运重建率及更宽的治疗时间窗。
球囊导引导管使用时需在高级医学影像设备的监测下,通过经皮穿刺置入动脉鞘,辅助取栓器械到达血管血栓近端,通过球囊膨胀使其贴附于血管壁,形成局部封堵,在外部负压作用下,将取栓器械和血栓吸附进导管的内腔。然后通过球囊的收缩,回撤球囊导引导管,将血栓带出人体以达到血流重建的目的。球囊导引导管吸栓或辅助介入器械完成机械取栓的关键问题是如何以较低的球囊充盈压力,实现有效性封堵,降低对脑神经血管管壁的刺激,减少手术过程中各类并发症和球囊破裂的风险;并且导管本身应具有较好的柔顺性和通过性,能应对复杂迂曲血管的血栓病变;导管尖端和球囊应有良好的可视性,介入手术过程中能准确定位导管尖端和球囊的位置。
目前国外市场上现有的同类产品如美国Concentric Medical公司生产的Merci球囊导引导管和美国美敦力公司生产的Cello球囊导引导管。前者Merci的导管尖端为单一的同轴锥体结构,使得导管在复杂弯迂曲血管中推进时有局限性;后者Cello的导管外管采用钢丝网加强结构,提高了导管本身的硬度,也降低了导管的柔顺性,使得导管很难进入到复杂迂曲血管。
技术实现要素:
本发明的目的是克服现有技术中存在的不足,提供一种球囊导引导管,能够降低对脑神经血管管壁的刺激,减少手术过程中各类并发症和球囊破裂的风险,并增强了导管的追踪性和复杂迂曲血管的通过性,同时减少患者进行取栓手术的时间,提高介入手术的可操作性和效率。
按照本发明提供的技术方案,所述球囊导引导管,包括由近端至远端依次设置的阀、应力释放管和外管,外管内设置内管;其特征是:外管远端的侧壁设有通液孔,通液孔外侧设有球囊,在外管远端的端部连接导管尖端;所述阀具有主孔道和侧孔道,内管的内腔为导引腔,导引腔与主孔道连通、与侧孔道相隔离;所述内管和外管之间形成通液腔,通液腔与侧孔道、通液孔和球囊连通,且通液腔与主孔道相隔离;所述球囊外侧滑动设置球囊导引套管,球囊导引套管的内径与外管和应力释放管相配合。
进一步的,所述球囊导引套管包括外层套管和内层套管,外层套管的材质为尼龙,内层套管为润滑涂层。
进一步的,所述球囊导引套管为直型圆柱体、在直型圆柱体的一端设置喇叭口、或者在直型圆柱体的两端设置喇叭口。
进一步的,所述球囊导引套管的长度为10-100mm。
进一步的,所述外管采用内层外管材质和润滑添加剂共混通过双螺杆挤出机挤出得到具有一定润滑效果的外管。
进一步的,所述润滑添加剂采用亲水性高分子添加剂、亲水性纳米高分子添加剂、聚乙二醇硬脂酸酯类材料或自润滑高分子材料。
进一步的,所述外管的近端至远端的硬度呈2-20段的多段式递减。
进一步的,所述阀的侧孔道和主孔道在近端方向相交成锐角,并且在主孔道和侧孔道相交处的外周包围三段弧形面。
进一步的,所述导管尖端采用直型尖端或弯形尖端,直型尖端的长度为2-15mm,弯型尖端的长度为2-25mm。
进一步的,所述球囊采用顺应性材质制成;当充盈液体量在0.1-5ml时,球囊的最大直径为5-25mm。
进一步的,所述球囊导引导管上连接便携装置,便携装置包括三通延长管和注射器;所述阀的侧孔道和三通延长管的远端连接,微量注射器和三通延长管的近端连接;所述三通延长管的长度为5-25cm;所述微量注射器的容积为0.5-5ml。
现有技术相比,本发明具有以下优点:
1、本发明所述球囊导引套管采用尼龙内涂塑润滑涂层的设计,预装于球囊导引导管远端,能保护球囊免受外力影响。在介入手术穿刺和置鞘后可直接辅助球囊导引导管快速插入动脉鞘管中,提高介入手术的可操作性和效率。当球囊导引导管到达靶病变血管近端后,喇叭口可套住导管近端的应力释放管,避免应力释放管与动脉鞘管接触而引起误操作。
2、本发明设计了便捷装置,以提高手术效率;其中,特定长度的三通延长管和微量容积的注射器,与球囊导引导管组成封堵球囊导管系统。三通延长管、注射器、球囊导引导管的Y阀三者间可直接通过鲁尔接头适配,通过小容积注射器注入精确体积的膨胀液,能快速、精确的完成球囊的膨胀和收缩,节省介入手术的操作时间,避免球囊破裂。
3、本发明采用高顺应性低压球囊设计,能以极少的膨胀液注射量使得球囊膨胀到适合封堵颅内神经血管的直径,实现对血栓近端颅内神经血管的局部封堵,能较好的辅助取栓器械完成机械取栓或者在负压下完成吸栓,同时降低手术过程球囊破裂引起的各类并发症风险。并且由于球囊在充盈状态下处于低压状态,因此不易破裂,既能实现有效封堵,又能减轻球囊对血管管壁的压力和刺激,显著降低血管痉挛等并发症。
4、导管尖端采用直型或弯型的结构设计。其中直型椎体结构的导管尖端与管身同轴,能较好的贴合导丝或介入器械,使得球囊导引导管具有良好的追踪性;弯型的导管尖端能为导丝指引方向,在处理复杂迂曲血管时与血管内壁的贴合性好,通过性高。
5、球囊导引导管的Y阀采用小扭矩结构设计,在介入手术过程中,转动Y阀使其带动导管尖端旋转通过复杂迂曲血管时扭矩小,提高了导管的扭控性。Y阀的近端和远端分别设计有对称的注胶孔,便于Y阀与导管管身的固化连接。
附图说明
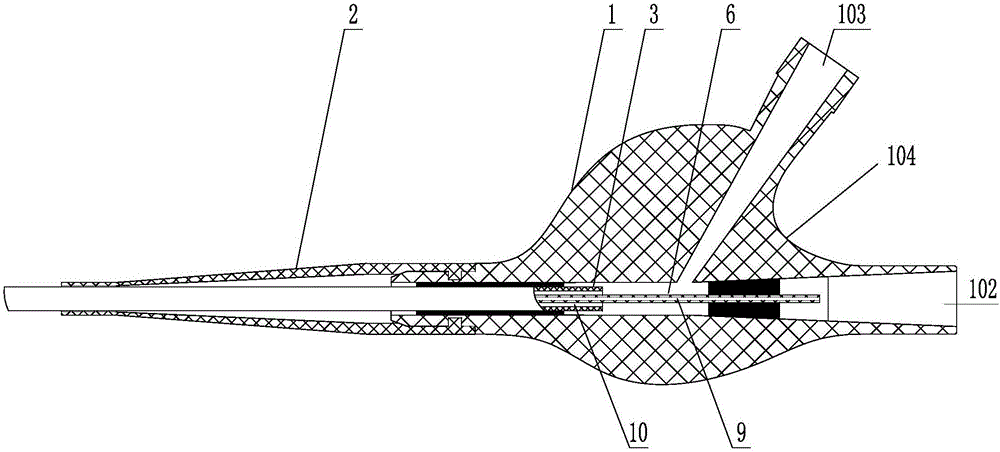
图1为本发明所述球囊导引导管的结构示意图。
图2为所述Y阀的结构示意图。
图3为所述图1的A-A剖视图。
图4为所述内管的示意图。
图5-1为所述内管第一种实施方式的剖面图。
图5-2为所述内管第二种实施方式的剖面图。
图5-3为所述内管第三种实施方式的剖面图。
图5-4为所述内管第四种实施方式的剖面图。
图5-5为所述内管第五种实施方式的剖面图。
图5-6为所述内管第六种实施方式的剖面图。
图6为所述球囊与导管尖端的连接示意图。
图6-1为所述导管尖端第一种实施方式的示意图。
图6-2为所述导管尖端第一种实施方式的示意图。
图7-1为所述球囊第一种实施方式的示意图。
图7-2为所述球囊第二种实施方式的示意图。
图7-3为所述球囊第三种实施方式的示意图。
图8为所述所述球囊导引套管的示意图。
图8-1为所述球囊导引套管第一种实施方式的示意图。
图8-2为所述球囊导引套管第二种实施方式的示意图。
图8-3为所述球囊导引套管第三种实施方式的示意图。
图8-4为所述球囊导引套管的剖视图。
图9为本发明所述球囊导引导管的工作状态示意图。
图10 取栓后急性观察期的实验动物颈总动脉切片分析图。
图11 取栓后一个月观察期的实验动物颈总动脉切片分析图。
图12 取栓后一个月观察期的实验动物颈外动脉切片分析图。
附图标记说明:1-Y阀、101-注胶孔、102-主孔道、103-侧孔道、104-弧形面、2-应力释放管、3-外管、301-外管近端、302-外管远端、303-通液孔、304-亲水涂层、305-内层外管、4-球囊、401-球体、402-椭圆体、403-圆柱体、5-显影标记、6-内管、601-金属编织网、602-润滑涂层、6011-圆形、6012-长方形、6013-方形、7-导管尖端、701-直型尖端、702-弯型尖端、8-球囊导引套管、801-外层套管、802-内层套管、8011-直型圆柱体、8012-直型单喇叭口、8013-直型双喇叭口、9-导引腔、10-通液腔、11-导管尖端与外管焊接处、12-三通延长管、13-微量注射器、14-球囊导引导管。
具体实施方式
下面结合具体附图对本发明作进一步说明。
如图1所示,本发明所述球囊导引导管14包括由近端至远端设置的Y阀1、应力释放管2、以及同轴设置的外管3和内管6,外管远端303的侧壁设有一个圆形或方形的通液孔303,通液孔303外侧设有球囊4,在球囊4内和外管远端302各设有一环状显影标记5,环状显影标记5的材质为铂铱合金或铂金,环状显影标记5镶嵌于内管6外壁上;在所述外管远端302的端部连接导管尖端7。如图2所示,所述Y阀1具有主孔道102和侧孔道103,内管6的近端延伸出外管3的近端,内管6的内腔为导引腔9,导引腔9与Y阀1的主孔道102连通,用于输送介入器械或导丝,完成颅内神经血管的机械取栓或吸栓。所述内管6和外管3之间形成通液腔10,通液腔10与侧孔道103、通液孔303和球囊4连通。所述Y阀1的主孔道102的近端和远端分别设有直径为0.3~0.7mm的圆形注胶孔101(如图1所示),用于注入紫外固化胶水。所述内管6的近端端部与主孔道102近端管壁通过紫外固化胶水形成密封连接,外管近端301的端部与主孔道102的远端管壁通过紫外固化胶水形成密封连接。
如图8所示,所述球囊4在未膨胀状态时外侧设有球囊导引套管8,球囊导引套管8的内径与外管3和应力释放管2相配合。如图8-4所示,所述球囊导引套管8包括外层套管801和内层套管802,外层套管801的材质为尼龙(牌号为GRILAMID L25),内层套管802为润滑涂层,材质为聚四氟乙烯(PTFE)、聚醚醚酮(PEEK)或改性聚醚砜(PES/ PTFE 共混)。所述球囊导引套管8的长度为10-100mm,外径为2.50-3.65mm,内径为2.0-3.15mm,内层套管802的厚度为0.03-0.08mm。如图8-1、图8-2、图8-3所示,所述球囊导引套管8的形状有直型圆柱体8011、直型单喇叭口8012或直型双喇叭口8013。直型圆柱体8011的球囊导引套管8具有良好的管身支撑性,能在介入手术过程中辅助球囊导引导管14快速插入经血管穿刺和置鞘后的动脉鞘管内,相比现有的微创介入手术操作方法,可节省手术时间。直型单喇叭口8012、直型双喇叭口8013的球囊导引套管8便于与球囊导引导管14装配;所述球囊导引套管8的喇叭口能套住外管近端301的应力释放管2,避免应力释放管2与动脉鞘管接触而引起误操作,提高微创介入手术的效率。
现有技术中球囊导引导管不具有球囊导引套管,在使用时,需要先取下保护球囊的包装,排除气泡,对导管管身浸水润滑后,方可沿着导丝缓慢插入动脉鞘管中,因鞘管的内径与导管的外径适配,插入过程中还需避免导管的插入角度发生倾斜,引起球囊或管身表面的刮伤;到达靶病变血管后,采用医疗机构提供的球囊膨胀装置,对球囊进行膨胀,封堵血流;若此时球囊或管身表面有刮伤,或医疗机构提供的外接膨胀装置规格不符,球囊将存在容易破裂或膨胀困难等情况,耽误脑血管介入取栓手术进程。本发明所述的球囊导引导管在实际使用时,主要有以下步骤:(1)在排气操作前可直接后撤球囊导引套管8,露出球囊4;(2)排除气泡后再前移球囊导引套管8至导管尖端7,使球囊导引套管8套在球囊4外侧,可以保护球囊4免受外力损伤;(3)球囊导引套管8的远端抵住动脉鞘管的管口,辅助球囊导引导管14准确、快速插入动脉鞘管,直至球囊4被推送至靶病变血管的近端;此操作过程中,球囊导引套管8不仅对导管的管身有良好的支撑性和导引性,便于准确、快速插入,且球囊导引套管8内壁的润滑涂层能保护球囊4免受鞘管的刮伤,避免球囊4进入人体后因表面刮伤、受损等缺陷引起的破裂或膨胀困难;(4)在球囊4推送至靶病变血管的过程中,球囊导引套管8向导管近端移动,直至喇叭口套住应力释放管2,避免应力释放管2与动脉鞘管接触而引起误操作;再配合三通延长管12和微量注射器13,完成球囊的顺利、精确膨胀,实现封堵脑血管血流,辅助取栓或吸栓的目的。本发明所述的球囊导引导管相对现有技术,通过球囊导引套管提高了介入手术的可操作性和效率,提供了更短的手术时间。一般情况下采用本发明所述的球囊导引导管相对现有技术能够节约2-10分钟,对于脑卒中手术来说,减小了患者的风险,具有重大的意义。
如图1、图2所示,所述Y阀1的侧孔道103和主孔道102在近端方向相交成锐角,并且在主孔道102和侧孔道103相交处的外周包围三段弧形面104,这种结构有助于对Y阀1施加较小的扭矩,获得球囊导引导管14较佳的扭控性。具体地,所述三段弧形面104分别设置于主孔道102和侧孔道103相交形成的近端夹角处、远端夹角处、以及相对于侧孔道103的另一侧;其中,位于主孔道102和侧孔道103远端夹角处和相对侧孔道103另一侧的弧形面104为向外侧凸出的弧形面,位于主孔道102和侧孔道103近端夹角处的弧形面104为向内凹进的弧形面。所述 Y阀1的材质为聚碳酸酯(PC)、改性聚碳酸酯(PMMA/ PC、PC/PP或PC/聚对苯二甲酸二已酯PET共混)、改性聚酰胺或聚甲基丙烯酸甲酯(PMMA)。
如图3所示,所述外管3包括内层外管305和涂覆在内层外管305外壁的亲水涂层304。所述外管3的外径为1.9~3.1mm,内径为1.8~3.0mm,有效长度为70~125cm。所述内层外管305材质为聚酰胺(PA6、PA66或PA12)、聚酰亚胺(PI)、嵌段聚醚酰胺弹性体(PEBAX)、聚氨酯(PU)、改性聚氨酯(PUA)、聚乙烯(PE)或聚四氟乙烯(PTFE)。所述亲水涂层304的厚度为0.015-0.075mm,材质为聚乙烯吡咯烷酮(PVP)。其中,亲水涂层304可以涂覆在整个内层外管305的外壁,或者也可以只涂覆于内层外管305远端一部分,内层外管305近端20-40cm的长度不涂覆亲水涂层304。所述外管3的近端至远端的硬度分级变化并递减(硬度呈2-20段的多段式递减),邵氏硬度范围为20D-86D;所述外管近端301硬度较高,能提升球囊导引导管的推送性能,且不易弯折,便于输送介入器械至导管远端;外管远端302硬度较低,能提升球囊导引导管管身的柔顺性和弯曲性能,便于通过迂曲血管。
上述的外管3结构由内层外管305和亲水涂层304组成,内层外管305大多采用Pebax,由于材质本身的特性外管3可能存在过于润滑的问题,难以手持,会滑出血管,从而影响使用效果;而且在环境潮湿状态下,亲水涂层表面会发粘。作为本发明的另一个实施例,所述外管3采用内层外管材质(高分子材料,如PI、Pebax、PA、PTFE等)和润滑添加剂共混通过双螺杆挤出机挤出得到自带亲水润滑效果的外管,以代替前述外管3上的亲水涂层304;具体如采用Pebax或PTFE材料和润滑添加剂共混。其中,所述润滑添加剂可以采用亲水性高分子添加剂、亲水性纳米高分子添加剂、聚乙二醇硬脂酸酯类材料或自润滑高分子材料。所述亲水性高分子添加剂可以采用聚乙烯醇PVA、聚乙二醇PEG或聚乙烯吡咯烷酮PVP,该亲水性高分子添加剂的添加量一般为5-20%,优选10%。所述亲水性纳米高分子添加剂采用PVA/PMMA或PEG/PMMA接枝共聚得到的亲水性核壳结构纳米微球,该亲水性纳米高分子添加剂的添加量一般为0.1%-5%,优选为0.1%-1%。所述聚乙二醇硬脂酸酯类材料采用PEG 1750单硬脂酸酯、PEG 1500单硬脂酸酯、PEG 600双妥尔油酸酯、PEG 400油酸酯等,聚乙二醇硬脂酸酯类材料的添加量一般为5-20%,优选10%。所述自润滑高分子材料采用PTEF、聚甲醛和低密度聚乙烯的共聚物(POM/LDPE)、聚四氟乙烯和聚甲醛的共聚物(PTFE/POM)、聚醚醚酮PEEK或聚甲苯POM,自润滑高分子材料的添加量为5-20%,一般不超过10%;具体如,采用15%-20%的PTFE共混高分子材料(如PI、Pebax、PA)通过双螺杆挤出机挤出得到外管3。本发明通过润滑添加剂和高分子材料共混挤出得到外管,润滑能够在合适的负载水平下实现COF(摩擦系数)降低25%左右,即减少摩擦,并允许基础材料的机械性能基本保持不变,显著降低了插入或缩回装置所需的力。
如图4、图5-1~图5-6所示,所述内管6包括管状的金属编织网601和涂覆在管状的金属编织网601内壁的润滑涂层602。所述内管6的外径为1.7~2.8mm,内径为1.3~2.5mm,有效长度为75~130cm;所述润滑涂层602的厚度为0.03-0.10mm,材质为聚四氟乙烯(PTFE)、聚醚醚酮(PEEK)或改性聚醚砜(PES/ PTFE共混),润滑涂层602用于降低介入器械在内管6内层中推进的阻力。所述金属编织网601采用金属丝编织而成,金属丝采用不锈钢丝或镍钛合金丝,金属丝的截面形状为圆形6011、长方形6012或方形6013。所述金属编织网601的编织密度由内管6的近端至远端递减,编织方式为采用相同形状的金属丝或不同形状的金属丝编织而成,以对外管3起到良好的支撑性。
如图6-1、图6-2所示,所述导管尖端7与外管远端302的端部采用激光焊接、超声波焊接或热熔焊接的方式连接,导管尖端与外管焊接处11与内管6的远端端部通过DYMAX胶水紫外固化形成密封连接。所述导管尖端7的材质为聚氨酯(PU)或改性聚氨酯(PUA),采用直型尖端701或弯形尖端702。所述直型尖端701的长度为2-15mm,直型尖端701与外管3、内管6同轴设置,能较好的贴合导引胶9内的导丝或介入器械,使得球囊导引导管14具有良好的导丝追踪性,并且提高球囊导引导管14在血管内的推送能力。所述弯型尖端702的长度为2-25mm,能为导丝指引方向,在处理复杂迂曲血管时与血管内壁的贴合性好,通过性高。
如图7-1、图7-2、图7-3所示,所述球囊4为高顺应性球囊,采用材质为聚氨酯(PU)或聚合物弹性体(TPU)。所述球囊4的形状为球体401、椭圆体402或圆柱体403。未充盈时的球囊4内径为1.82-3.05mm,壁厚为0.07-0.20mm,有效长度为8-15mm,充盈液体量为0.2-1.0ml;充盈状态下球囊4的最大直径为6-20mm。当充盈液体量在0.1-5ml时,球囊4的最大直径为5-25mm。本发明通过注入极少的液体充盈量实现对颅内血管的有效封堵,减少球囊破裂的风险。所述球囊4采用热熔焊接、超声波焊接、激光焊接或紫外胶水固化的方式与外管远端302连接。所述球囊4与外管远端302侧壁的通液孔303、外管3和内管6间的通液腔10、Y阀1的侧孔道103连通,可通过液射造影剂或生理盐水,使球囊4膨胀至合适直径,封堵颅内血管。本发明所述球囊4的材质、形状、参数等决定了球囊4的高顺应性,保证球囊4在膨胀状态下处于低压状态,既对血管进行有效封堵,也能降低球囊破裂引起各类并发症的风险。
本发明所述球囊导引导管14能够用于辅助机械取栓或者直接用于负压抽吸血栓,无论用于哪种形式,球囊4封堵血管的大致位置几乎不变,而球囊4到导管尖端7的长度根据使用的形式有所不同。在辅助机械取栓时,导管尖端7的位置不需要上到大脑中动脉,在这种情况下,球囊4位置和导管尖端7间的距离不长,大概为10-20mm。在用于负压抽吸血栓时,不需要使用辅助机械取栓装置,导管尖端7需到达大脑中动脉部位,所以球囊4到导管尖端7的距离一般在100mm左右。
如图9所示,所述球囊导引导管14上连接便携装置,便携装置包括三通延长管12和注射器13。所述Y阀1的侧孔道103和三通延长管12的远端通过鲁尔接头连接,微量注射器13和三通延长管12的近端通过鲁尔接头连接;通过旋转三通延长管12近端旋塞实现通液腔10和微量注射器13的连通或关闭,能够快速、精确的完成球囊4的膨胀和收缩。所述三通延长管12的长度为5-25cm,优选为10cm,长度适中,避免与其他器械发生扭结或缠绕,可操作性佳。所述微量注射器13的容积为0.5-5ml,优选为1.0ml,可实现所述球囊4中膨胀液的精确注射,确保球囊4在低压状态下膨胀到合适直径,对血管进行有效封堵。由于球囊4处于低压状态,因此不易破裂,既能实现有效封堵,又能减轻球囊4对血管管壁的压力和刺激,显著降低血管痉挛等并发症。
应用实施例:临床前动物试验
以动物双侧颈总动脉的血栓取出为例,详细说明本发明所述球囊导引导管14辅助介入器械完成动物双侧颈内动脉和颈外动脉内血栓的取出。实验对象为35千克的健康白猪,在白猪的双侧颈总动脉推入预先制作的适当大小的血栓。介入手术开始前,需预备直径为8F的球囊导引导管(直型导管尖端和弯型导管尖端,适配球囊导引套管、三通延长管和微量注射器)、血栓取出装置、0.035和0.014英寸的导引导丝、微导管(REBAR-18)、旋转止血阀、8F动脉鞘。采用标准方法完成经皮穿刺和置鞘,建立血管通路。在球囊导引套管的辅助下将球囊导引导管快速插入动脉鞘管中,并沿0.035英寸的导引导丝推进到颈总动脉内,直到球囊到达(内、外)颈动脉的分叉部位。撤出导丝,造影观察血栓位置。用0.014英寸的导丝经球囊导引导管将微导管推进至实验动物的血管内血栓位置,并使微导管的远端稍过血栓远端。将血栓取出装置经由微导管管腔输至微导管远端端部,固定取栓装置。在高级影像仪下慢慢将微导管回撤,使取栓装置在血栓中自膨展开,抓取血栓。将微量注射器、三通延长管、球囊导引导管Y阀三者通过鲁尔接头快速适配,对球囊精确注入0.2-0.6ml的膨胀液,使球囊膨胀至合适直径,临时封堵血管血流。在球囊导引导管的近端施加负压,同时将微导管和取栓装置一起回撤,直至血栓被拉或吸入球囊导引导管内。收缩球囊,将球囊导引导管和血栓带出人体,实现血流重建的目的。
取栓后组织病理学评价:将试验动物的双侧颈外动脉和颈总动脉分别切成4mm的片段,嵌入石蜡切片中,再重新切片成4μm的厚度,并用苏木素染色液(HE)进行染色。将装有切片的载玻片安装在盖玻片上,在光学显微镜下对其进行分析。选取急性观察期实验动物的颈总动脉切片和一个月观察期实验动物的颈总动脉切片、颈外动脉切片分析图为例,进行组织病理学评价研究,具体如图10-12所示。由图10-12可知,经组织学病理学分析表明,实验动物在颈外动脉和颈总动脉的内皮细胞未见损伤,平滑肌细胞未迁移或增殖。
临床动物试验可知,在血栓的顺利取出过程中,球囊导引导管具备良好的适配性能、推进性能、迂曲血管的通过性能、在X射线透射下可视性佳;球囊膨胀时具有良好的前向血流阻断效应,即以较低的膨胀液注射容积实现了血管的有效封堵。介入手术过程中连续重复三次将取栓装置在颈动脉内释放并回收入球囊导引导管,均能顺利完成,即球囊导引导管具备良好的可操作性。取栓完成后,没有造成新的血栓,也没有产生新的栓塞,在动物试验中显示出一定的安全性和有效性。
- 还没有人留言评论。精彩留言会获得点赞!