光生物测量装置的制作方法
本申请是原母案申请申请号201280072578.7,申请日2012年04月25日,发明名称为“光生物测量装置”的分案申请。
本发明涉及一种光生物测量装置,更详细来说涉及一种非侵扰地测定脑活动的光生物测量装置。
背景技术:
近年来,为了观察脑部的活动状况,而开发出一种使用光来简便且非侵扰地进行测定的光脑功能成像装置。此种光脑功能成像装置中,利用配置于被检者的头皮表面上的送光探针,而将不同的3种波长λ1、λ2、λ3(例如,780nm、805nm、830nm)的近红外光向脑部照射,且利用配置于头皮表面上的受光探针,分别检测从脑部放出的各波长λ1、λ2、λ3的近红外光的强度变化(受光量信息)δa(λ1)、δa(λ2)、δa(λ3)。
而且,为了根据如所述般获得的受光量信息δa(λ1)、δa(λ2)、δa(λ3),来求出脑血流中的氧合血红蛋白的浓度变化·光路长度的乘积[oxyhb]、脱氧血红蛋白的浓度变化·光路长度的乘积[deoxyhb],例如,使用改进型比尔–朗伯(modifiedbeerlambert)定律而制定关系式(1)、关系式(2)、关系式(3)所示的联立方程式,并对该联立方程式求解。此外,根据氧合血红蛋白的浓度变化·光路长度的乘积[oxyhb]与脱氧血红蛋白的浓度变化·光路长度的乘积[deoxyhb]来算出总血红蛋白的浓度变化·光路长度的乘积([oxyhb]+[deoxyhb])。
δa(λ1)=eo(λ1)×[oxyhb]+ed(λ1)×[deoxyhb]…(1)
δa(λ2)=eo(λ2)×[oxyhb]+ed(λ2)×[deoxyhb]…(2)
δa(λ3)=eo(λ3)×[oxyhb]+ed(λ3)×[deoxyhb]…(3)
另外,eo(λm)为波长λm的光下的氧合血红蛋白的吸光度系数,ed(λm)为波长λm的光下的脱氧血红蛋白的吸光度系数。
此处,对送光探针与受光探针之间的距离(通道)与测定部位的关系进行说明。图7(a)、图7(b)是表示一对送光探针及受光探针与测定部位的关系的图。送光探针12被抵压到被检者的头皮表面的送光点t,并且受光探针13被抵压到被检者的头皮表面的受光点r。而且,从送光探针12照射光,并且使从头皮表面放出的光入射到受光探针13。此时,从头皮表面的送光点t照射的光中的通过香蕉形状(测定区域)的光到达头皮表面的受光点r。即,光通过存在于送光点t附近的皮肤的血管、存在于脑部的血管、及存在于受光点r附近的皮肤的血管。
因此,公开了如下内容:为了获取仅存在于脑部的血管的受光量信息δa,包括将送光探针12与受光探针13之间的距离(通道)设为短距离r1的情况与设为长距离r2的情况(例如,参考专利文献1或非专利文献1)。图8是表示设为与送光探针12具有短距离r1的参考受光探针14及具有长距离r2的受光探针13与测定部位的关系的剖面图。由此,利用长距离r2的通道,获取存在于送光点t附近的皮肤的血管、存在于脑部的血管、存在于受光点r2附近的皮肤的血管的受光量信息δa2,并且利用短距离r1的通道,获取仅存在于送光点t附近的皮肤的血管(存在于受光点r1附近的皮肤的血管)的受光量信息δa1。
而且,根据如此获得的受光量信息δa1、δa2,使用式(4),求出仅存在于脑部的血管的受光量信息δa。
δa=δa2-kδa1…(4)
且说,式(4)中为了求出受光量信息δa而需要决定系数k,并公开了算出该系数k的算出方法(例如,参考非专利文献2)。该算出方法中,使用最小平方误差算出系数k。
而且,光脑功能成像装置中,分别进行测定关于脑部的多处测定部位的氧合血红蛋白的浓度变化·光路长度的乘积[oxyhb]、脱氧血红蛋白的浓度变化·光路长度的乘积[deoxyhb]及总血红蛋白的浓度变化·光路长度的乘积([oxyhb]+[deoxyhb])。
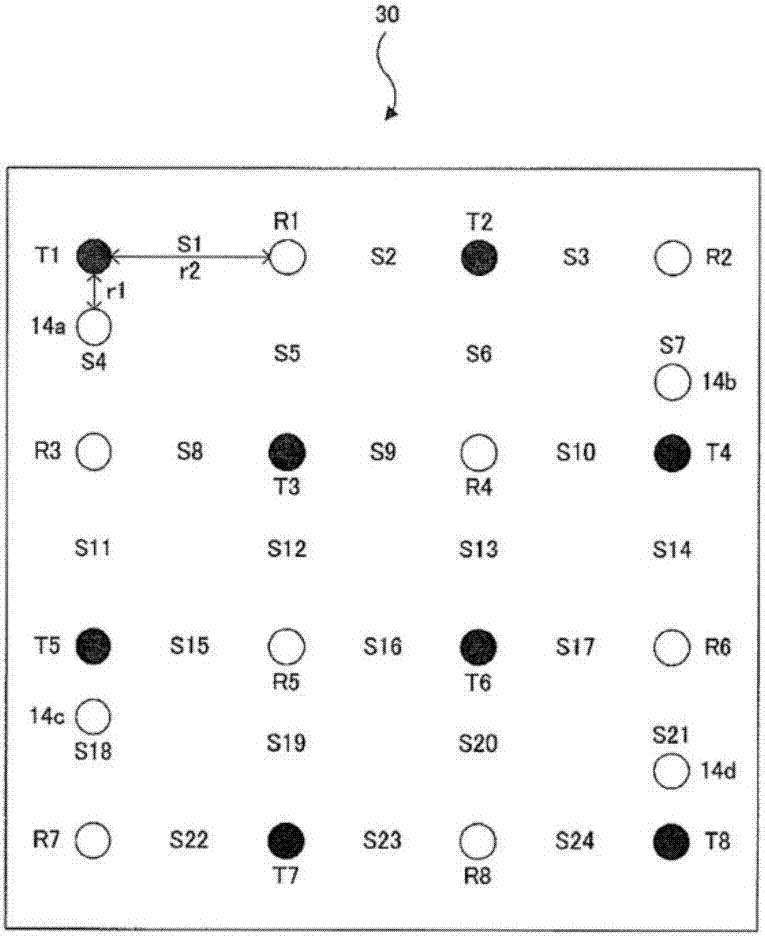
此种光脑功能成像装置中,为了将8个送光探针12与8个受光探针13以规定的排列与被检者的头皮表面接触,而使用支架(送受光部)130。图9是表示被插入8个送光探针与8个受光探针的支架130的一例的平面图。
送光探针12t1~送光探针12t8与受光探针13r1~受光探针13r8以沿纵方向4个进行交替且沿横方向4个进行交替的方式配置。此时,送光探针12t1~送光探针12t8与受光探针13r1~受光探针13r8之间的间隔(通道)即第二设定距离r2为30mm。由此,获得关于脑部的24处测量位置的受光量信息δa2(λ1)、δa2(λ2)、δa2(λ3)。
现有技术文献
专利文献
专利文献1:日本专利特开2009-136434号公报
非专利文献
非专利文献1:罗尔夫b.萨格尔、和安得烈j.伯杰“在两层浑浊介质间的直接表征与干扰吸收去除”,美国光学会志a辑第22卷,第9期,2005年9月(rolfb.saager,andandrewj.berger“directcharacterizationandremovalofinterferingabsorptiontrendsintwo-layerturbidmedia”j.opt.soc.am.a/vol.22,no.9/september2005.)
非专利文献2:弗朗西斯科法布里、安吉洛莎莎罗莉、迈克尔e亨利、塞尔吉奥凡蒂尼“双层扩散介质中的吸收变化的光学测量”物理医学生物学49(2004)1183-1201.(francescofabbri,angelosassaroli,michaelehenry,andsergiofantini“opticalmeasurementsofabsorptionchangesintwo-layereddiffusivemedia”phys.med.biol.49(2004)1183-1201.)
发明所要解决的问题
且说,虽由使用了所述受光量信息δa1、δa2或系数k的算出方法来算出受光量信息δa,但该算出中考虑了一对送光探针12及受光探针13的组合,而未考虑如所述的光脑功能成像装置的支架130般的多个送光探针12t1~送光探针12t8及多个受光探针13r1~受光探针13r8的组合。即,并非算出关于脑部的多处(24处)测量位置的受光量信息δa。
另外,为了利用所述算出方法来算出受光量信息δa,也考虑相对于所有送光探针12t1~送光探针12t8及受光探针13r1~受光探针13r8的组合而设置设为短距离r2的多个参考受光探针14,但相对于所有送光探针12t1~送光探针12t8及受光探针13r1~受光探针13r8的组合来设置参考受光探针14会耗费成本。
技术实现要素:
解决问题的手段
本案发明者等人为了解决所述课题,对如下方法进行了讨论:即便以少量的参考受光探针,也可关于脑部的多处测定部位而研究仅存在于脑部的血管的受光量信息δa。因此发现,显示被检者的脑部的规定范围内的测定数据,并且同时显示被检者的头皮的规定位置的皮肤血流数据。由此,医生或检查技师等可一边参考皮肤血流数据,一边研究测定数据。
即,本发明的光生物测量装置包括:送受光部,具有配置于被检者的头皮表面上的多个送光探针、及配置于所述头皮表面上的多个受光探针,且各受光探针配置于与送光探针隔开第二设定距离r2的位置;第二受光量信息获取部,使用从所述送光探针到受光探针为止的第二受光量信息δa2,来算出与脑活动有关的测定数据;以及数据显示控制部,表示被检者的脑部的测量位置并分别显示各测定数据,由此显示被检者的脑部的规定范围内的测定数据,所述光生物测量装置的特征在于包括:参考受光探针,配置于与所述送光探针隔开比第二设定距离r2短的第一设定距离r1的位置;以及第一受光量信息获取部,使用从所述送光探针到所述参考受光探针为止的第一受光量信息δa1,来算出与皮肤血流有关的皮肤血流数据,所述数据显示控制部显示被检者的脑部的规定范围内的测定数据,并且表示被检者的头皮的测量位置并显示皮肤血流数据,由此显示被检者的头皮的规定位置的皮肤血流数据。
此处,“第二设定距离r2”是用以获取存在于送光点t附近的皮肤的血管、存在于脑部的血管、及存在于受光点r附近的皮肤的血管的受光量信息的距离,“第一设定距离r1”是用以获取存在于送光点t或受光点r附近的皮肤的血管的受光量信息的距离。
而且,“被检者的脑部的规定范围”是指欲测量的任意的脑部的范围,由送受光部的大小等来决定,“被检者的头皮的规定位置”是指用以测量不存在于脑部的血管的位置,例如,可列举用以测量存在于离头皮1.5cm以内处的主动脉、主静脉、送受光部附近的动脉、或送受光部附近的静脉的位置等。
发明的效果
如以上般,根据本发明的光生物测量装置,医生或检查技师等可一边参考皮肤血流数据及其测量位置,一边研究测定数据,因而判断测定数据中是否产生假影,或可判断出哪一测定数据中产生哪一种假影。结果,医生或检查技师等可将某一测定数据废弃,从而能够正确地诊断出被检者的脑活动。
(用以解决问题的其他手段及效果)
而且,本发明的光生物测量装置中,所述数据显示控制部也能以映射图来显示被检者的脑部的规定范围内的测定数据,并且在该映射图中的被检者的头皮的规定位置附近显示皮肤血流数据。
此处,“映射图”是指在2维或3维空间内使位置相关联者。
而且,本发明的光生物测量装置中,也可包括多个参考受光探针,所述数据显示控制部以映射图来显示被检者的脑部的规定范围内的测定数据,并且以映射图来显示被检者的头皮的规定范围内的皮肤血流数据。
进而,本发明的光生物测量装置中,也可包括形态图像显示控制部,所述形态图像显示控制部获取并显示表示被检者的头皮表面的头皮表面形态图像及/或表示被检者的脑表面的脑表面形态图像,在头皮表面形态图像及/或脑表面形态图像上重叠显示所述映射图。
此处,“表示被检者的头皮表面的头皮表面形态图像”是通过如下而制作的3维形态图像:从由核磁共振图像诊断装置(以下简称作mri)或ct图像等制作出的被检者的影像数据中,抽出表示头皮表面的影像数据。而且,“表示被检者的脑表面的脑表面形态图像”是通过如下而制作的3维形态图像:从由mri或ct图像等制作的被检者的影像数据中,抽出表示脑表面的影像数据。
如以上所述,根据本发明的光生物测量装置,制作表示头皮表面或脑表面的3维形态图像,因而可无关于脑部的解剖学结构上的个人差异,而详细地研究脑活动。
附图说明
图1是表示作为本发明的一实施方式的光生物测量装置的构成的方框图。
图2是表示被插入8个送光探针、8个受光探针、及4个参考受光探针的支架的一例的平面图。
图3是表示显示由生体测量装置获得的图像的监控画面的一例的图。
图4是表示显示由生体测量装置获得的图像的监控画面的另一例的图。
图5是表示显示由生体测量装置获得的图像的监控画面的另一例的图。
图6是表示显示由生体测量装置获得的图像的监控画面的另一例的图。
图7(a)、图7(b)是表示一对送光探针及受光探针与测定部位的关系的图。
图8是表示设为与送光探针具有短距离r1的参考受光探针及设为与送光探针具有长距离r2的受光探针与测定部位的关系的剖面图。
图9是表示被插入8个送光探针与8个受光探针的支架的一例的平面图。
[符号的说明]
1:光生物测量装置
2:发光部
3:光检测部
12、12t1~12t8:送光探针
13、13r1~13r8:受光探针
14、14a~14d:参考受光探针
20:控制部(计算机)
21:中央处理器(cpu)
22:输入装置
22a:键盘
22b:鼠标
23:显示装置
23a:监控画面
24a:头皮表面图像
24b:脑表面图像
24c:3维形态图像
24d:测定数据
24e:皮肤血流数据
25:存储器
25a:受光量信息存储区域
25b:图像数据存储区域
30:支架(送受光部)
31:形态图像显示控制部
32:第二受光量信息获取部
33:第一受光量信息获取部
34:数据显示控制部
40:送受光部控制部
42:发光控制部
43:光检测控制部
50:mri
130:支架(送受光部)
m:中点
r、r1、r2:受光点
r1:第一设定距离
r2:第二设定距离
s:被检者的部位
t:送光点
具体实施方式
以下,使用附图来说明本发明的实施方式。另外,本发明不限定于以下说明的实施方式,在不脱离本发明的主旨的范围内包含各种形态。
图1是表示作为本发明的一实施方式的光生物测量装置的构成的方块图。而且,图2是表示被插入8个送光探针、8个受光探针、及4个参考受光探针的支架(送受光部)的一例的平面图。而且,图3是表示作为测量结果而进行图像显示的监控画面的一例的图。
光生物测量装置1由支架30、发光部2、光检测部3、以及执行光生物测量装置1整体的控制的控制部(计算机)20构成。
图3中,进行用以表示头皮表面图像24a与脑表面图像24b的位置关系的3维形态图像24c的图像显示。而且,在脑表面图像24b的24个规定位置上进行测定数据24d的图像显示,在头皮表面图像24a的4个规定位置上进行皮肤血流数据24e的图像显示。另外,测定数据24d与皮肤血流数据24e,由与某测量时间t时的氧合血红蛋白的浓度变化·光路长度的乘积[oxyhb]的数值对应的颜色来表现。而且,头皮表面图像24a与皮肤血流数据以半透明进行图像显示。
支架30具有8个送光探针12t1~送光探针12t8、8个受光探针13r1~受光探针13r8、及4个参考受光探针14a~参考受光探针14d。送光探针12t1~送光探针12t8出射光,另一方面,受光探针13r1~受光探针13r8与参考受光探针14a~参考受光探针14d对光量进行检测。
送光探针12t1~送光探针12t8与受光探针13r1~受光探针13r8以在行方向及列方向上交替的方式配置成正方格子状。此时,送光探针12t1~送光探针12t8与受光探针13r1~受光探针13r8间的间隔(通道)即第二设定距离r2为30mm。
而且,参考受光探针14a在送光探针12t1与受光探针13r3之间,配置于与送光探针12t1隔开第一设定距离r1的位置,送光探针12t1与参考受光探针14a之间的间隔即第一设定距离r1为10mm。而且,参考受光探针14b在送光探针12t4与受光探针13r2之间,配置于与送光探针12t4隔开第一设定距离r1的位置,参考受光探针14c在送光探针12t5与受光探针13r7之间,配置于与送光探针12t5隔开第一设定距离r1的位置,参考受光探针14d在送光探针12t8与受光探针13r6之间,配置于与送光探针12t8隔开第一设定距离r1的位置。
发光部2根据从计算机20输入的驱动信号而将光发送到选自8个送光探针12t1~送光探针12t8中的一个送光探针12。作为所述光,使用近红外光(例如,780nm、805nm及830nm这3种波长光)。
光检测部3个别地对由8个受光探针13r1~受光探针13r8接收的近红外光(例如,780nm、805nm及830nm这3种波长光)进行检测,由此将8个第二受光量信息δa2y(λ1)、δa2y(λ2)、δa2y(λ3)(y=1、2、…、8)输出到计算机20中,并且个别地对由4个参考受光探针14a~参考受光探针14d接收的近红外光(例如,780nm、805nm及830nm这3种波长光)进行检测,由此将4个第一受光量信息δa1m(λ1)、δa1m(λ2)、δa1m(λ3)(m=1、2、…、4)输出到计算机20中。
计算机20中具备cpu21及存储器25,且将具有监控画面23a等的显示装置23与具有键盘22a或鼠标22b等的输入装置22加以连结。而且,如果将cpu21处理的功能加以区块化来进行说明,则具有送受光部控制部40、形态图像显示控制部31、第二受光量信息获取部32、第一受光量信息获取部33、以及数据显示控制部34。进而,存储器25中,形成着存储受光量信息δa1m(λ1)、δa1m(λ2)、δa1m(λ3)、δa2y(λ1)、δa2y(λ2)、δa2y(λ3)的受光量信息存储区域25a,及存储图像数据的图像数据存储区域25b。
形态图像显示控制部31通过获取在测量前由mri50制作出的影像数据,而抽出表示头皮表面的影像数据,由此获取头皮表面形态图像数据,并且抽出表示脑表面的影像数据,由此获取脑表面形态图像数据,并将头皮表面形态图像数据与脑表面形态图像数据存储在图像数据存储区域25b。此处,mri50制作表示3个方向的2维图像的影像数据。另外,影像数据表示包括头皮表面与脑表面在内的被检者。而且,影像数据由具有mri信号的强度信息或相位信息等数值的多个像素构成。而且,作为所述抽出的方法,例如,可列举如下方法:通过使用具有mri信号的强度信息或相位信息等数值的多个像素,而利用区域扩张法、区域并合法、启发式方法等图像区域分割方法,将边界要素连结而抽出区域的方法,使闭曲线变形而抽出区域的方法等。
而且,形态图像显示控制部31进行如下控制:根据在测定后等从输入装置22输出的输入信号,将存储在图像数据存储区域25b的头皮表面形态图像数据与脑表面形态图像数据加以合成,从而制作出表示头皮表面图像24a与脑表面图像24b的位置关系的3维形态图像24c,并在监控画面23a进行3维形态图像24c的图像显示(参考图3)。
送受光部控制部40具有对发光部2输出驱动信号的发光控制部42,以及通过接受来自光检测部3的受光量信息δa1m(λ1)、δa1m(λ2)、δa1m(λ3)、δa2y(λ1)、δa2y(λ2)、δa2y(λ3)而将其存储于受光量信息存储区域25a的光检测控制部43。发光控制部42进行如下控制:将发送光到送光探针12的驱动信号输出至发光部2。光检测控制部43进行如下控制:使来自光检测部3的4个第一受光量信息δa1m(λ1)、δa1m(λ2)、δa1m(λ3)与8个第二受光量信息δa2y(λ1)、δa2y(λ2)、δa2y(λ3)存储于受光量信息存储区域25a。也就是,每当从1个送光探针12发送光时,将4个第一受光量信息δa1m(λ1)、δa1m(λ2)、δa1m(λ3)与8个第二受光量信息δa2y(λ1)、δa2y(λ2)、δa2y(λ3)存储于受光量信息存储区域25a。
第二受光量信息获取部32进行如下控制:从存储于受光量信息存储区域25a的第二受光量信息δa2y(λ1)、δa2y(λ2)、δa2y(λ3)中,获取由与送光探针12隔开第二设定距离r2的受光探针13检测到的第二受光量信息δa2x(λ1)、δa2x(λ2)、δa2x(λ3)(通道编号x=1、2、…、24)。也就是,获取24个第二受光量信息δa2x(λ1)、δa2x(λ2)、δa2x(λ3)(x=1、2、…、24)。
第一受光量信息获取部33进行下述控制:从存储于受光量信息存储区域25a的第一受光量信息δa1m(λ1)、δa1m(λ2)、δa1m(λ3)中,获取由与送光探针12相隔第一设定距离r1的参考受光探针14检测到的第一受光量信息δa1n(λ1)、δa1n(λ2)、δa1n(λ3)(通道编号n=1、2、…、4)。即,获取4个第一受光量信息δa1n(λ1)、δa1n(λ2)、δa1n(λ3)(n=1、2、…、4)。
数据显示控制部34进行如下控制:根据存储于受光量信息存储区域25a的第二受光量信息δa2x(λ1)、δa2x(λ2)、δa2x(λ3)(x=1、2、…、24),使用关系式(1)、关系式(2)、关系式(3),来求出氧合血红蛋白的浓度变化·光路长度的乘积[oxyhb]、脱氧血红蛋白的浓度变化·光路长度的乘积[deoxyhb]及总血红蛋白的浓度变化·光路长度的乘积([oxyhb]+[deoxyhb])并作为测定数据,并在脑表面图像24b的24个规定位置上进行测定数据24d的图像显示。此时,例如,根据表示数值与色彩的对应关系的颜色表,由颜色来表现某测量时间t时的24个规定位置的氧合血红蛋白的浓度变化·光路长度的乘积[oxyhb]。而且,脑表面图像24b的24个规定位置设为被检者的部位s,该被检者的部位s是从沿着被检者的头皮表面以最短距离连结送光点t与受光点r而得的线的中点m开始,到相当于沿着被检者的头皮表面以最短距离连结送光点t与受光点r而得的线的距离的一半的深度。
进而,数据显示控制部34进行如下控制:在脑表面图像24b的24个规定位置上进行测定数据24d的图像显示,并且根据存储于受光量信息存储区域25a的第一受光量信息δa1n(λ1)、δa1n(λ2)、δa1n(λ3)(n=1、2、…、4),使用关系式(1)、关系式(2)、关系式(3),来求出氧合血红蛋白的浓度变化·光路长度的乘积[oxyhb]、脱氧血红蛋白的浓度变化·光路长度的乘积[deoxyhb]及总血红蛋白的浓度变化·光路长度的乘积([oxyhb]+[deoxyhb])并作为皮肤血流数据,且在头皮表面图像24a的4个规定位置上进行皮肤血流数据24e的图像显示。此时,例如,根据表示数值与色彩的对应关系的颜色表,由颜色来表现某测量时间t时的4个规定位置的氧合血红蛋白的浓度变化·光路长度的乘积[oxyhb]。而且,头皮表面图像24a的4个规定位置设为沿着被检者的头皮表面以最短距离连结送光点t与受光点r而得的线的中点m。由此,在监控画面23a上显示如图3所示的图像。
如以上般,根据光生物测量装置1,医生或检查技师等可一边使用如图3般的图像参考皮肤血流数据24e与其测量位置,一边研究测定数据24d,因而可判断测定数据24d中是否产生假影,或可判断在哪一测定数据24d中产生哪一种假影。结果,医生或检查技师等可将某一测定数据24d废弃,从而可正确地诊断被检者的脑活动。而且,因制作头皮表面图像24a或脑表面图像24b,因而可无关于脑部的解剖学结构上的个人差异,而详细地研究脑活动。
〈其他实施方式〉
(1)所述光生物测量装置1中,表示了如下构成:数据显示控制部34在脑表面图像24b的24个规定位置上进行测定数据24d的图像显示,但也可设为如下构成:在脑表面图像24b的规定范围上进行测定数据24d的等高线映射图的图像显示。而且,表示了如下构成:数据显示控制部34在头皮表面图像24a的4个规定位置上进行皮肤血流数据24e的图像显示,但也可设为如下构成:在头皮表面图像24a的规定范围上进行皮肤血流数据24e的等高线映射图的图像显示。图4是表示进行图像显示的监控画面的另一例的图。
(2)所述光生物测量装置1中,表示了如下构成:数据显示控制部34在脑表面图像24b的24个规定位置上进行测定数据24d的图像显示,但也可设为如下构成:未使用脑表面图像24b而进行测定数据24d的等高线映射图的图像显示。而且,表示了如下构成:数据显示控制部34在头皮表面图像24a的4个规定位置上进行皮肤血流数据24e的图像显示,但也可设为如下构成:不使用头皮表面图像24a而进行皮肤血流数据24e的等高线映射图的图像显示。图5是表示进行图像显示的监控画面的另一例的图。
(3)所述光生物测量装置1中,表示了如下构成:数据显示控制部34在头皮表面图像24a的4个规定位置上进行皮肤血流数据24e的图像显示,但也可设为如下构成:不使用头皮表面图像24a,而在测定数据24d的等高线映射图中的被检者的头皮的规定位置附近进行皮肤血流数据24e的图像显示。图6是表示进行图像显示的监控画面的另一例的图。
产业上的可利用性
本发明可用于非侵扰地测定脑活动的光生物测量装置。
- 还没有人留言评论。精彩留言会获得点赞!