一种化合物在制备以组织蛋白酶K为靶标的疾病药中的应用的制作方法
本发明涉及组织蛋白酶抑制剂技术领域,具体地说,涉及一种具有高选择性的组织蛋白酶k非活性位点抑制剂在制备抑制以组织蛋白酶k为靶标的疾病药中的应用,所述疾病包括骨质疏松、牙龈病(牙龈炎和牙周炎)、佩吉特氏病、代谢性骨病、骨折、类风湿性关节炎、骨关节炎、假体周围骨质溶解、成骨不全、恶性高钙血症、多发性骨髓瘤、转移性骨病和疼痛。
背景技术:
涉及到异常骨吸收相关的病症很多,包括但不限于骨质疏松、牙龈病(牙龈炎和牙周炎)、佩吉特氏病、代谢性骨病、骨折、类风湿性关节炎、骨关节炎、假体周围骨质溶解、成骨不全、恶性高钙血症、多发性骨髓瘤、转移性骨病和疼痛。最常见之一是骨质疏松,其常见于老年人和绝经后妇女。中国50岁以上的人群中,有30%患有骨质疏松症,随着人均寿命延长,人口老龄化趋势严重,骨质疏松的发病率越来越高,由此引发的骨折导致老年患者的病死率和致残率增高[罗先正,骨质疏松症的流行病学概况,中国乡村医药,17(2):1651-1662,2010]。
骨质疏松是由破骨细胞的骨吸收和成骨细胞的骨形成之间的关系失衡引起的。组织蛋白酶k选择性地大量表达于破骨细胞,其生理作用底物正是在有机骨基质中含量达95%的ⅰ型胶原,它将完整的三股螺旋体结构胶原蛋白降解成不规则结构的纤维碎片,除ⅰ型胶原外,组织蛋白酶k还能降解骨基质中的骨桥接素和骨连接素,是破骨细胞中溶骨活性最强的关键酶。人体组织蛋白酶k基因表达的变异会导致致密性成骨不全症,最终导致骨质疏松和骨脆性增加。采用组织蛋白酶k基因缺失小鼠骨髓培养的离体破骨细胞不能形成骨吸收陷窝,不能有效降解i型胶原。
组织蛋白酶k是骨质疏松药物的关键靶标,临床前和临床研究数据表明组织蛋白酶k抑制剂对骨吸收的抑制作用可以达到80%,而不降低骨形成的生物指标。基于这种防治骨质疏松策略的4种组织蛋白酶k抑制剂中至少2种的临床试验失败,失败原因与导致非骨骼组织的纤维化有关。该类抑制剂是以组织蛋白酶k活性位点为靶点的,不仅抑制组织蛋白酶k与药效相关的胶原酶活性,同时也抑制酶的其他生理活性。研究发现组织蛋白酶k缺陷鼠除了表现骨骼系统预期的表型外,还表现肺气道损伤,易于使肺和皮肤发生纤维化,甲状腺球蛋白(tg)释放甲状腺素功能障碍,甚至导致学习记忆缺陷等,表明活性位点抑制剂可能引起副作用,这为开发新型的抗骨质疏松药物提出了挑战。
目前国内外catk抑制剂专利均为活性位点抑制剂,尚未有非活性位点抑制剂。
技术实现要素:
本发明一方面是针对现有技术中的不足,提供一种能特异性结合组织蛋白酶k非活性位点,选择性抑制组织蛋白酶k活性的物质在制备以组织蛋白酶k为靶标的疾病药中的应用。
为解决上述技术问题,本发明采取的技术方案如下:
一种组织蛋白酶k非活性位点抑制剂在制备以组织蛋白酶k为靶标的疾病药中的应用;所述组织蛋白酶k非活性位点抑制剂选自:化学式母核为i、ii或iii所示三环结构的化合物,所述化合物的可药用的酯、酰胺或盐,和包含所述酯或酰胺的盐或组合物;
其中:c环选自苯环和环己基环;a环存在对位和间位双酮、或五环和六环内酯类结构;a环1,2位取代基选自呋喃环、吡喃环、二氢取代呋喃环和二氢取代吡喃环。
作为本发明的一个优选例,c环选自甲基苯环和二甲基环己基环。
作为本发明的另一优选例,所述组织蛋白酶k非活性位点抑制剂选自a环或c环上取代基所形成的酯、酰胺和盐。
作为本发明的另一优选例,所述组织蛋白酶k非活性位点抑制剂为丹参酮iia磺酸钠。
作为本发明的另一优选例,所述以组织蛋白酶k为靶标的疾病选自骨质疏松、牙龈病、佩吉特氏病、代谢性骨病、骨折、类风湿性关节炎、骨关节炎、假体周围骨质溶解、成骨不全、恶性高钙血症、多发性骨髓瘤、转移性骨病和疼痛;所述牙龈病选自牙龈炎和牙周炎。
作为本发明的另一优选例,所述以组织蛋白酶k为靶标的疾病为骨吸收异常疾病。
作为本发明的另一优选例,所述骨吸收异常疾病为骨质疏松。
本发明另一方面提供了一种药物组合物在制备以组织蛋白酶k为靶标的疾病药中的应用,所述药物组合物包含组织蛋白酶k非活性位点抑制剂,所述组织蛋白酶k非活性位点抑制剂选自:化学式母核为i、ii或iii所示三环结构的化合物,所述化合物的可药用的酯、酰胺或盐,和包含所述酯或酰胺的盐或组合物;
其中:c环选自苯环和环己基环;a环存在对位和间位双酮、或五环和六环内酯类结构;a环1,2位取代基选自呋喃环、吡喃环、二氢取代呋喃环和二氢取代吡喃环。
作为本发明的一个优选例,所述药物组合物以所述组织蛋白酶k非活性位点抑制剂为唯一活性物质。
作为本发明的另一优选例,所述以组织蛋白酶k为靶标的疾病为骨吸收异常疾病。
本发明优点在于:
本发明的组织蛋白酶k非活性位点抑制剂作用于人体组织蛋白酶k氨基酸序列(1:位于氨基酸序列tyr87到gly102,2:gly108到glu118),药效学研究表明,能显著抑制人破骨细胞活性,改善雌激素缺失去卵巢骨质疏松小鼠骨结构特征和生理状态,包括提高骨密度、改善骨微细结构和提高骨组织的生物力学等,从而具有显著的抗骨质疏松作用,且对大脑学习记忆能力无影响。该类抑制剂为抗骨质疏松药物研发提供了新的思路。
附图说明
图1:t06作为非活性位点特征。(a)sds-page分析i型胶原降解,(b)胶原降解的ic50图,(c)sds-page分析明胶的降解活性,(d)sem观察t06存在和不存在下i型胶原纤维的电镜图,(e)i型胶原纤维消化后羟基脯氨酸定量测定,(f)分子对接鉴定t06的对接位点。
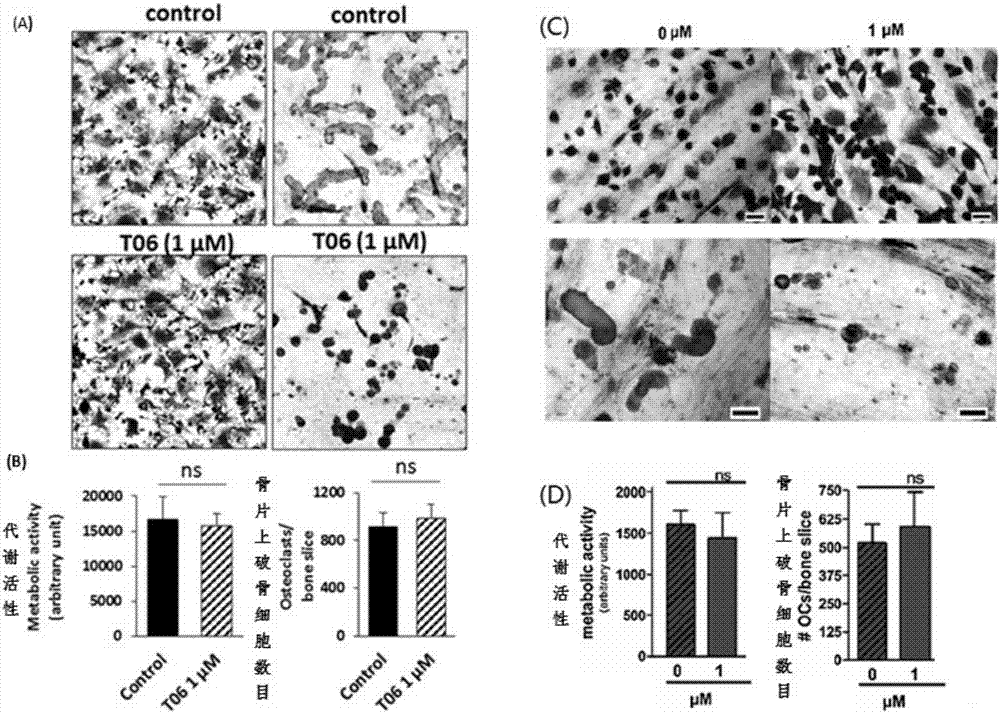
图2:t06和t02对破骨细胞tracp阳性细胞和破骨细胞骨吸收陷窝(a、c)以及破骨细胞代谢活性和细胞数目的影响(b、d)。
图3:小鼠造模10周的体重变化(a)和脏器系数(b)。
图4:t06对子宫系数(a)及子宫切片(b)包括对子宫面积(c),子宫腔面积(d),和子宫腔上皮细胞厚度(e)的影响。
图5:t06对去卵巢小鼠股骨(a)和脊椎骨l5(b)骨密度的影响。
图6:对小鼠骨吸收相关血清生化rankl和ctx-i的影响。
图7:t06对小鼠行为影响。(a)旷场实验,(b)高架十字迷宫,(c)水迷宫第2-5天训练,(d)水迷宫第6天测试。
具体实施方式
下面结合具体实施例,进一步阐述本发明。这些实施例应理解为仅用于说明本发明而不用于限制本发明的保护范围。在阅读了本发明记载的内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等效变化和修饰同样落入本发明权利要求所限定的范围。
骨质疏松的问题与破骨细胞中组织蛋白酶k活性有着密不可分的关系,因此能抑制组织蛋白酶k活性的化合物,也就意味着能改善骨质疏松所造成的骨质丢失和骨折现象。
本发明所述一种组织蛋白酶k非活性位点抑制剂(cathepsinkexositeinhibitor),该化合物母核结构选自下列中的一种:
较佳地:c环为甲基苯环或二甲基环己基环;a环存在对位或间位双酮,1,2位取代基为呋喃环和二氢取代呋喃环。上述a环和c环的选择可以同时或分开选择。本发明揭露较佳结构为丹参酮iia磺酸钠,但并不以此为限。其中丹参酮iia磺酸钠结构式为:
本发明揭露一种组织蛋白酶k非活性位点抑制剂的用途,应用于制备抗骨质疏松的药物。本发明揭露较佳结构为丹参酮iia磺酸钠,但并不以此为限。以下通过实验具体说明本发明应用于治疗骨质疏松的药效。
实施例1:新型组织蛋白酶k非活性位点抑制剂的筛选和确证
对丹参中7个单体化合物,i型结构丹参新醌d,ii型结构二氢丹参酮i,丹参酮i,丹参酮iia,隐丹参酮,丹参酮iia磺酸钠和iii型结构表丹参隐螺内酯进行了非活性位点抑制剂的筛选。结构如下:
1实验材料
1.1药材与试剂
单体化合物丹参新醌d,二氢丹参酮i,丹参酮i,丹参酮iia,隐丹参酮,丹参酮iia磺酸钠和表丹参隐螺内酯,购买自chemfaces公司;benzyloxycarbonyl-phe-arg-7-amido-4-methylcoumarin(z-fr-mca)购自日本wako公司;硫酸软骨素a(c4-s),e-64(l-3-carboxy-trans-2-3-epoxypropionyl-leucylamido-(4guanidino)-butane)和胃蛋白酶购自美国sigma公司;i型胶原购自美国affymetrix公司;微孔过滤滤膜离心管购自amicomillipore公司。
2实验方法
2.1胶原纤维降解活性
采用凝胶电泳法(sds-page),可溶性i型胶原溶解于100mm醋酸钠缓冲液(ph5.5,包含2.5mmdtt和2.5mmedta)中,最终浓度为0.6mg/ml,依次将catk(最终浓度400nm)、c4-s(最终浓度200nm)和化合物单体(不同浓度抑制剂)加入到含有i型胶原蛋白的反应液中,使总反应液容量为50μl。混匀,28℃孵育4小时,取出后加入1μl的100μme64终止反应。采用10%的sds-page凝胶电泳分离,卡马斯亮蓝染色20分钟,用乙酸-甲醇(4:1)脱色。i型胶原的α1条带的灰度用genesnap(syngeneinc.frederick,md)软件进行定量分析。非活性位点和活性位点抑制剂均能抑制i型胶原的α1条带降解。
2.2弹性纤维降解活性
称取1mg刚果红弹性纤维蛋白(congo-redelastin),置于100μl的100mm醋酸钠缓冲液中(ph5.5,包含2.5mmdtt和2.5mmedta),加入终浓度为1μm的catk和不同浓度抑制剂,37℃,200转/min摇床,孵育16小时。样品取出,8000转/min,离心5min,取上清液90μl,490nm波长下检测荧光信号。计算公式:抑制率%=100-(1-vi/v0)。vi和v0分别表示存在和不存在抑制剂情况下的荧光信号。
2.3z-fr-mca底物结合(活性位点)
抑制剂用100mm醋酸钠缓冲液(ph5.5,包含2.5mmdtt和2.5mmedta)稀释至浓度为25μm,加入96孔板,最终反应容量为1ml。加入终浓度为5nm的catk孵育5分钟,加入5μl底物1mm/ml的z-fr-mca溶液开始反应,检测荧光信号(发散光波长460nm,吸收光波长355nm)。实验设阴性对照组(无抑制剂),阳性对照组(e-64,活性位点抑制剂)。计算公式:抑制率%=100-(1-vi/v0)。vi和v0分别表示存在和不存在抑制剂情况下的荧光信号。
2.4明胶降解(活性位点)
采用凝胶电泳法(sds-page),可溶性i型胶原在95℃加热20分钟得到明胶,溶解在100mm醋酸钠缓冲液(ph5.5,包含2.5mmdtt和2.5mmedta),最终浓度为1.8mg/ml,将catk(最终浓度5nm)和单体化合物(最终浓度25μm)加入反应液中,使总反应液容量50μl。混匀,28℃孵育4小时,取出后加入1μl的100μme64终止反应。采用10%的sds-page凝胶电泳分离,卡马斯亮蓝染色20分钟,用乙酸-甲醇(4:1)脱色。明胶的α1条带的灰度用genesnap(syngeneinc.frederick,md)软件进行定量分析。活性位点抑制剂,明胶α1条带将被抑制,非活性位点抑制剂对明胶降解无抑制作用。
2.5分子对接
计算机模拟抑制剂与catk两个非活性位点对接,进一步确证结合位点及结合特性。
2.6胶原纤维降解(sem电镜)
sem电镜用来观察胶原纤维在catk干预前后的区别。1mg鼠i型胶原纤维和1μm的catk共同孵育在37℃摇床,震荡过夜。被降解的胶原纤维在sem扫描电镜(heliosnanolab650fei)下观察形态变化。
3实验结果
对选取的7个丹参化合物进行组织蛋白酶k活性筛选,组织蛋白酶k抑制剂具有抑制胶原纤维蛋白和弹性纤维蛋白降解活性,z-fr-mca和明胶降解活性是活性位点抑制剂的合成和生理底物,用于初期筛选活性位点抑制剂。
表1丹参中不同化合物的组织蛋白酶k活性
*二氢丹参酮i和丹参酮iia磺酸钠分别与odanacatib比较,p<0.05;#二氢丹参酮i与丹参酮iia磺酸钠比较,p<0.05。
结果发现(表1),丹参酮iia磺酸钠具有最强的胶原纤维降解活性(ic50为2.7±0.2μm)和弹性纤维降解活性(ic50为6.8±1.4μm),接近目前临床效果最佳的,处于iii期临床研究的组织蛋白酶k抑制剂odanacatib,同时丹参酮iia磺酸钠不显示z-fr-mca活性和明胶降解活性(表1和图1中a-c),表明丹参酮iia磺酸钠为非活性位点抑制剂。同时电镜下观察发现丹参酮iia磺酸钠抑制了catk对胶原纤维的消化,羟基脯氨酸定量测定验证了该结果(图1中d-e)。采用分子对接实验发现丹参酮iia磺酸钠与人组织蛋白酶k的结合,最佳的结合方式见图1中f,形成氢键结合位点为met97和glu94,tyr87与磺酸根基团结合。
ii型结构中二氢丹参酮i的胶原纤维降解活性仅次于丹参酮iia磺酸钠,弹性纤维降解活性与丹参酮iia磺酸钠无显著差异,但同时显示具有一定的z-fr-mca和明胶降解活性,与丹参酮iia磺酸钠有显著差异,有可能二氢丹参酮i同时与活性位点和非活性位点结合。丹参酮i和丹参酮iia的弹性纤维降解活性强于胶原降解活性,显示一定的z-fr-mca活性。i型结构的丹参新醌d和iii型结构的表丹参隐螺内酯胶原纤维降解和弹性纤维降解活性不显著,且同时显示一定的z-fr-mca和明胶降解活性。
实施例2:组织蛋白酶k抑制剂t06对破骨细胞骨吸收的影响
破骨细胞表达丰富的胞浆内酶系统,在破骨细胞前体细胞向成熟破骨细胞分化的过程中有一系列的标志性蛋白质产生,可以作为破骨细胞的识别及其分化阶段的标志。其中,分化后的破骨细胞前体细胞所表达的抗酒石酸酸性磷酸酶(tartrate-resistantacidphosphatase,trap)被认为是破骨细胞的标志酶。本实验采用骨髓诱导破骨细胞模型,考察t02,t06对破骨细胞分化,trap活性的影响。
1实验材料
1.1药材与试剂
动物:新生1-2天的同窝sd小鼠5只,雌雄不限,体重7-8g,由第二军医大学实验动物中心提供。
丹参酮iia磺酸钠:使用时以去离子水溶解稀释;rankl、m-scf购自美国sigma公司。
2实验方法
2.1破骨细胞培养
取新生3天的sd小鼠胫骨,培养基冲洗骨髓腔以收集骨髓细胞,加入等量ficoll试剂分离骨髓单核细胞,用含有25ng/mlm-csf、25ng/mlrankl的细胞因子和10%胎牛血清的α-mem培养基进行培养,每3天换液1次,6天后破骨细胞分化成熟。
2.2破骨细胞活性研究
(1)破骨细胞tracp活性;成熟破骨细胞以1×105/ml接种于96孔板内,换加不同浓度t06(0.1,.0.5,1.0,10.0μm),阴性对照组加不含药物的破骨细胞诱导培养基,培养48h后,取移出的培养基20μl,依据tracp试剂盒分光光度法测定破骨细胞活性。测定trap的活性,以对硝基苯酚溶液作标准曲线,trap活性用每孔的破骨细胞生成的对硝基苯酚的nmol数表示。
(2)破骨细胞活力;细胞成熟后,以1×105/ml接种于96孔板,提前置入牛股骨骨片,加入具有潜在抑制catk活性的1μmt06。继续培养48h后,取100μl培养基,加入20μlcelltriter-blue试剂,轻轻晃10s混匀,37℃孵育30min,荧光分光光度计检测(发散光波长560nm,吸收光波长590nm)。选择对细胞活力没有毒性的浓度范围进行破骨细胞活性测试。
(3)破骨细胞数目和tracp阳性细胞数目;成熟破骨细胞以1×105/ml接种于96孔板内,加入1μmt06的破骨细胞诱导培养基,提前培养48h后,移出培养基至另一孔板待测tracp活性。依据tracp染色试剂盒对破骨细胞细胞核染色,计算tracp阳性破骨细胞数目。
3实验结果
本实验采用骨髓细胞与成骨细胞共培养诱导破骨细胞模型,考察组织蛋白酶k抑制剂对破骨细胞分化和trap活性的作用,如表2所示。骨髓细胞经诱导培养8天后发育为成熟的破骨细胞,经1-10μm的t06和10μmt02药物作用48h后,抗酒石酸酸性磷酸酶(trap)活性被明显抑制(p<0.05)。
表2t06对骨髓源性破骨细胞的影响(n=10,
*p<0.05,**p<0.01vscontrol。
丹参酮iia磺酸钠在1μm时完全抑制破骨细胞的骨吸收,图2中a显示tracp染色的破骨细胞和甲苯胺蓝染色的骨吸收陷窝。在对照组中,可以发现较长和深的骨印迹和骨陷窝,1μmt06组只有较小和浅的骨陷窝,证明1μm丹参酮iia磺酸钠能显著减少骨吸收表面。然而,破骨细胞的代谢活力测定实验发现,药物对破骨细胞没有毒性作用,不能显著减少tracp染色阳性破骨细胞的数目(图2中b)。图2中c-d显示二氢丹参酮i对破骨细胞代谢活力无显著影响,对tracp阳性细胞数目无显著影响,但对骨吸收表面面积具有一定的抑制作用。细胞实验证明丹参酮iia磺酸钠是个理想的抗骨吸收药物。
实施例3:组织蛋白酶k抑制剂t06对去卵巢骨质疏松小鼠的影响
1实验材料
动物:c57bl6小鼠由加拿大英属哥伦比亚大学实验动物提供。动物分笼饲养(3~4只/笼)于空调温室内,温度21±2℃,湿度40~60%;用颗粒饲料喂养,自由饮水。
2实验方法
动物分组:将雌性c57bl6小鼠30只(18-22g),按体重随机分为3组,每组10只,包括假手术组(sham,灌胃生理盐水10ml/kg),骨质疏松模型组(ovx,给生理盐水10ml/kg)和t06(40mg/kg/d)3个组。恢复5天后,连续灌胃给药12周。
造模方法:手术台上异氟烷麻醉,在背部切开两个0.5cm大小的切口,分离肌肉,剪开后取出双侧卵巢。假手术组切开背部后将不做任何处理,缝合创口,消毒;手术组将双侧卵巢结扎后切除,缝合创口,消毒。
观察指标:
(1)体重:每周称量小鼠一次体重。
(2)脏器系数:小鼠处死后,迅速剥离其心、肝、脾、肺、肾和子宫的附属组织及脂肪,随即进行称重。脏器系数公式:脏器系数=脏器重量(mg)/体重(g),对子宫切片观察。
(3)血清tgf-β,ctx-i和rankl
眼眶取血,置于抗凝剂肝素钠管中,以3000转/min离心10分钟,分离血清,冻于-80℃备用。依据试剂盒方法检测。
(4)骨密度和骨组织形态计量学
小鼠处死后,剥离左侧股骨,剔除骨周围附属组织,用生理盐水擦洗干净,用锡箔纸包好,-80℃冻存,用于μct检测骨组织参数。
(5)行为学和记忆学习能力
小鼠在处死前,进行旷场实验,高架十字迷宫和水迷宫实验,用于评价小鼠的一般行为和学习记忆能力。
3实验结果
3.1对体重和主要脏器系数的影响
如表3所示,造模第一周后,ovx和ovx+t06的体重就显著高于正常sham组,造模结束后,去卵巢模型组小鼠体重增加值明显高于sham组,t06的体重增加量与模型组相比较无显著性差异。
如图3中b所示,去卵巢模型组小鼠各主要脏器系数(心、肝、脾、肺、肾)明显低于sham组,ovx和ovx+t06相比较主要脏器系数(心、肝、脾、肺、肾)无显著性变化。
3.2对子宫的影响
造模12周后,取出子宫称重,发现ovx和ovx+t06组的小鼠子宫萎缩,无显著差异,两组子宫系数显著低于sham组,显示了t06明显的子宫增生副作用。
对子宫切片观察发现,ovx和ovx+t06组小鼠子宫腔显著缩小,子宫面积显著减少,子宫腔上皮细胞厚度显著减少。去卵巢后,雌激素缺失导致子宫发育受阻,出现萎缩,子宫上皮细胞结构变得紧密,子宫腔上皮细胞不明显,出现断裂等。
3.3对骨密度和骨计量学指标影响
研究发现,经过μct扫描骨骼后,ovx组股骨和脊椎骨l5段的骨密度(bmd)均显著降低(p<0.05)。ovx+t06相比较ovx组,股骨骨密度有显著改善(p<0.05),l5骨密度有一定改善,无显著差异(图5)。
表3的结果显示,与正常组比较,ovx组显示,股骨bv/tv比例(bv/tv%)降低48%,骨小梁数目(tb.n)降低43%,骨小梁厚度(tb.th)降低8%,骨小梁间隙(tb.sp)增大50%,骨连接密度(conn.dn)降低至57%。脊椎骨l5,与股骨相似,bv/tv比例显著降低(p<0.001),骨小梁数目(tb.n)显著降低(p<0.05),骨小梁间隙(tb.sp)显著增大(p<0.05),骨连接密度(conn.dn)显著降低(p<0.01)。
相对于去卵巢模型组(ovx),ovx+t06的股骨指标,bv/tv比例显著增大(p<0.001),骨小梁数目(tb.n)显著增多(p<0.05),骨小梁厚度增大(p<0.05),骨小梁间隙(tb.sp)显著减小(p<0.05),骨连接密度(conn.dn)显著增大(p<0.01)。脊椎骨l5段各个指标无显著变化。
表3t06对股骨和脊椎骨l5去卵巢小鼠骨计量参数的影响
3.4对血清生化指标的影响
rankl参与破骨细胞形成、分化、融合、生存、激活、成熟的全过程,opg竞争性抑制rankl与前破骨细胞上的受体rank结合,opg/rankl比例降低,将抑制骨吸收。ctx-i为i型胶原最终降解产物,直接反映了骨胶原的降解状态。图6结果显示,与ovx组比较,ovx+t06中血清rankl(p<0.001)和磷ctx-i水平显著降低(p<0.05)。说明t06具有较强抑制骨吸收作用。
3.5对行为学和学习记忆能力的影响
三组小鼠进行旷场实验,5分钟的总活动距离、平均速度无显著差异,说明小鼠活动能力基本相同。与sham组比较,小鼠探索内部区域的时间显著较少(p<0.01)。高架十字迷宫显示,三组小鼠在造模前后,在开放手臂和密闭手臂的停留时间和出入次数均无显著差异。水迷宫实验显示,训练2-5天,ovx和ovx+t06小鼠每天寻找到水底平台所需要的时间减少,但游泳的距离越来越短,说明小鼠获得了一定的学习记忆能力。第6天,ovx和ovx+t06组小鼠通过阴性平台的次数和平台所在区间的时间均无显著差异。三种行为模型实验结果表明,ovx和ovx+t06均无差异,说明catk抑制剂t06对ovx小鼠学习记忆能力并无影响。
结论
我们通过高通量筛选得到非活性位点抑制剂丹参酮iia磺酸钠,考察了t02和t06对破骨细胞骨吸收活性(破骨细胞生长数量和trap活性)的作用,结果发现该抑制剂在体外具有较好的体外抑制骨吸收作用。同时,我们采用去卵巢骨质疏松小鼠模型来考察抗骨质疏松作用,结果该化合物对雌激素缺失骨质疏松具有较好的活性,且对小鼠体重和各器官系数无影响,对子宫系数和切片研究发现无雌激素样作用,未发现像雌激素治疗法导致体重降低、子宫增生等副作用,未出现catk缺失导致的学习记忆能力缺失的副作用。因此,我们相信非活性位点抑制剂丹参酮iia磺酸钠具有进一步开发为抗骨质疏松药物的潜力和应用前景。
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员,在不脱离本发明方法的前提下,还可以做出若干改进和补充,这些改进和补充也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!