去铁胺在制备用于治疗非酒精性脂肪肝的药物中的应用的制作方法
本发明涉及去铁胺的一种新用途,即去铁胺在制备用于治疗非酒精性脂肪肝的药物中的应用。
背景技术:
非酒精性脂肪性肝病(nafld)是指除外酒精和其他明确的损肝因素所致的肝细胞内脂肪过度沉积为主要特征的临床病理综合征,肝脏组织学病变和酒精性脂肪肝具有相似的临床症状和体征,可发展为肝硬化和肝癌。
近年来随着生活水平的提高,nafld的发病率逐年攀升,普通人群中约有14%至24%患有nafld,已成为最常见的肝脏疾患之一。
目前,限制热量摄取和运动是治疗nafld唯一有效的手段,但对于多数患者而言常难以坚持。因此,开发治疗nafld的有效药物十分必要。
现有技术中,去铁胺主要适用于治疗急性铁中毒和贫血治疗中输血产生的慢性铁过载。
技术实现要素:
本发明的目的是提供去铁胺的一种新用途,即去铁胺在制备用于治疗非酒精性脂肪肝的药物中的应用。
本发明首先保护物质甲或物质乙或物质丙在制备药物中的应用;所述物质甲为去铁胺;所述物质乙为去铁胺药物学可接受的盐;所述物质丙为去铁胺的溶剂合物;所述药物的用途为治疗和/或预防脂肪肝。
所述脂肪肝具体可为非酒精性脂肪肝。
所述脂肪肝具体可为高胆固醇引起的脂肪肝。
所述去铁胺药物学可接受的盐具体可为甲磺酸去铁胺。
本发明还保护一种药物,其活性成分为物质甲或物质乙或物质丙;所述物质甲为去铁胺;所述物质乙为去铁胺药物学可接受的盐;所述物质丙为去铁胺的溶剂合物;所述药物的用途为治疗和/或预防脂肪肝。
所述脂肪肝具体可为非酒精性脂肪肝。
所述脂肪肝具体可为高胆固醇引起的脂肪肝。
所述去铁胺药物学可接受的盐具体可为甲磺酸去铁胺。
本发明还保护物质甲或物质乙或物质丙在制备产品中的应用;所述物质甲为去铁胺;所述物质乙为去铁胺药物学可接受的盐;所述物质丙为去铁胺的溶剂合物;所述产品的用途为如下(1)至(14)中的至少一种:
(1)抑制肝脏内脂肪的积累;
(2)改善肝脏的脂肪变性;
(3)抑制肝脏体重比增加;
(4)抑制谷丙转氨酶升高;
(5)抑制肝细胞脂质蓄积;
(6)抑制脂肪酸合成相关基因的表达;
(7)抑制炎症相关因子基因的表达;
(8)抑制脂肪肝患者的肝脏内脂肪的积累;
(9)改善脂肪肝患者的肝脏的脂肪变性;
(10)抑制脂肪肝患者的肝脏体重比增加;
(11)抑制脂肪肝患者的谷丙转氨酶升高;
(12)抑制脂肪肝患者的肝细胞脂质蓄积;
(13)抑制脂肪肝患者的脂肪酸合成相关基因的表达;
(14)抑制脂肪肝患者的炎症相关因子基因的表达。
以上任一所述脂肪肝具体可为非酒精性脂肪肝。
以上任一所述脂肪肝具体可为高胆固醇引起的脂肪肝。
所述去铁胺药物学可接受的盐具体可为甲磺酸去铁胺。
所述产品可为药品或保健品。
所述脂肪酸合成相关基因具体可为srebp-1基因和/或fasn基因和/或scd5基因和/或scd1基因。
所述炎症相关因子基因具体可为tnfα基因和/或il-8基因和/或il-1β基因。
去铁胺作为治疗铁毒性和铁过载的药物已经在临床应用多年,药物的安全性好,毒副作用小。本发明公开了去铁胺在治疗非酒精性脂肪肝中的新用途。本发明的发明人通过建立高胆固醇动物模型证实了去铁胺可以明显改善高胆固醇诱导的肝组织病理学改变,减轻肝细胞的损伤,降低肝内脂质蓄积。本发明开发了去铁胺的新用途,又为治疗非酒精性脂肪肝提供了新途径。
附图说明
图1为实施例1中的肝脏表型比较、肝组织病理学分析、肝脏体重比和血浆谷丙转氨酶活性分析的结果。
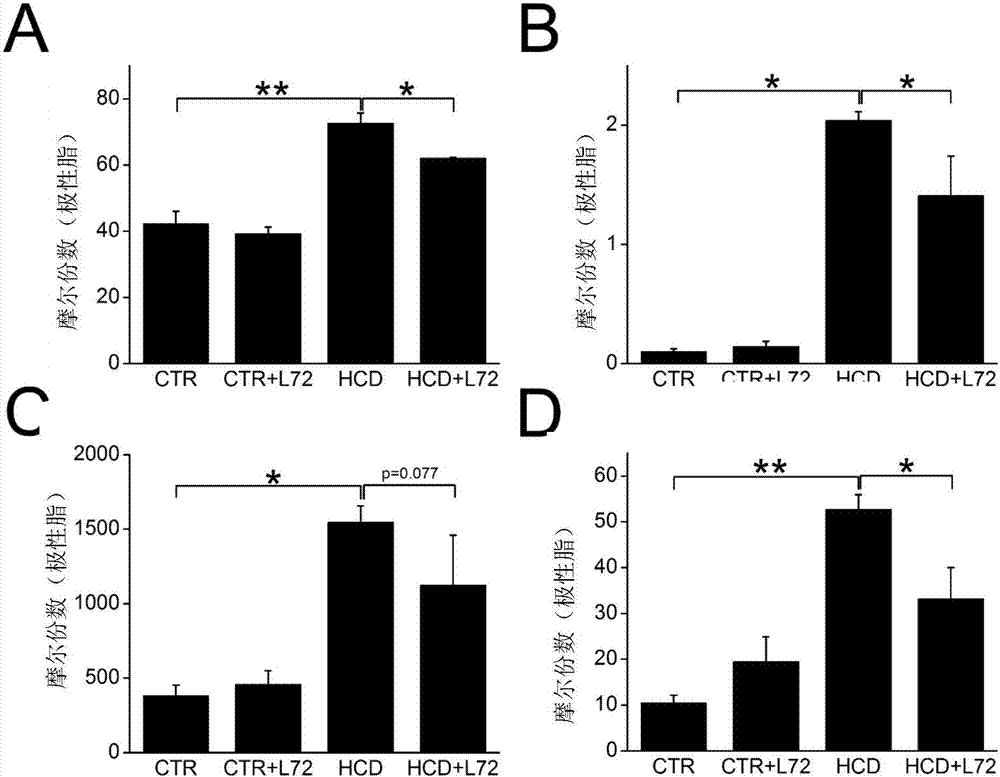
图2为实施例1中肝脏中的胆固醇和甘油三酯的含量的结果。
图3为实施例2中肝脏表型比较和肝组织病理学分析的结果。
图4为实施例2中肝脏体重比和血浆谷丙转氨酶活性的结果。
图5为实施例3中油红o染色的结果。
图6为实施例3中脂肪酸合成相关基因和炎症相关因子基因表达量分析的结果。
具体实施方式
以下的实施例便于更好地理解本发明,但并不限定本发明。下述实施例中的实验方法,如无特殊说明,均为常规方法。下述实施例中所用的试验材料,如无特殊说明,均为自常规生化试剂商店购买得到的。以下实施例中的定量试验,均设置三次重复实验,结果取平均值。图表数据均经过统计学分析,统计学分析使用ibmspssstatistics,version19进行双样本t-test和单因素方差分析检验,结果显示为平均值±标准误,p<0.05为有显著性差异。
c57bl/6小鼠:北京维通利华实验动物技术有限公司,品系代码213。胆固醇(饲料用):北京天启化工科技有限公司。普通饲料为ain-93m饲料。高胆固醇饲料:98.5质量份普通饲料和1.5质量份胆固醇混合。基础培养基为dmem高糖培养基:hyclone,sh30022.01。胆固醇(细胞实验):西格玛奥德里奇(上海)贸易有限公司,货号c3045。
实施例1和实施例2中所用的甲磺酸去铁胺为得斯芬(注射用甲磺酸去铁胺),为白色至类白色疏松块状物或粉末,novartispharmasteinag(瑞士诺华制药有限公司),进口药品注册证号h20140678。实施例3中所用的甲磺酸去铁胺为西格玛奥德里奇(上海)贸易有限公司生产,货号d9533。
甲磺酸去铁胺的结构式见式(ⅰ)。
甲磺酸去铁胺溶液:将甲磺酸去铁胺溶于灭菌后的0.9%生理盐水溶液,使甲磺酸去铁胺的浓度为0.00625g/ml。
hepg2细胞(人肝癌细胞):americantypeculturecollection。
实施例1、动物试验
一、分组处理
取17.5~23.3g、6-8周龄的雄性c57bl/6小鼠,适应性饲养2周,然后随机分为四组(每组8只),分别处理如下(分别处理的时间为22周,即第1周至第22周):
空白对照组(ctr):整个过程采用普通饲料饲喂;
药物对照组(ctr+l72):整个过程采用普通饲料饲喂;从第8周开始至第22周结束,每天注射甲磺酸去铁胺溶液一次,单次注射剂量为“72mg甲磺酸去铁胺/kg体重”;
模型组(hcd):整个过程采用高胆固醇饲料饲喂;
药物治疗组(hcd+l72):整个过程采用高胆固醇饲料饲喂;从第8周开始至第22周结束,每天注射甲磺酸去铁胺溶液一次,单次注射剂量为“72mg甲磺酸去铁胺/kg体重”。
二、相关检测
第22周结束后,动物禁食8小时,称重,通过戊巴比妥钠腹腔注射全麻后处死,心脏穿刺取血并离心获得血浆,肝脏灌注后取出称重,拍照,并在冰上完成组织切分,立即放于-80℃保存备用。
1、肝脏表型比较
肝脏灌注后的照片见图1a。空白对照组小鼠的肝脏的颜色较深,肝脏体积较小。模型组小鼠的肝脏颜色浅,偏黄,肝脏体积较大。与模型组小鼠相比,药物治疗组小鼠的肝脏的颜色和体积都有所恢复。结果表明,去铁胺可以抑制肝脏内脂肪的积累。
2、肝组织病理学分析(h&e染色)
取新鲜的肝组织,置于10%的中性福尔马林溶液中固定,然后进行常规的组织学处理,之后用石蜡对组织块进行包埋,石蜡切片(5μm)后用苏木素和伊红染色(h&e染色)进行组织病理学分析。
照片见图1b。空白对照组小鼠的肝脏具有中央静脉和辐射状肝细胞的正常肝小叶结构,且肝细胞中并无过多脂肪积累。模型组小鼠的肝脏中肝脏细胞膨胀呈气泡状,肝细胞中充满大量脂滴,细胞质疏松,细胞核呈固缩状,细胞内有较大的脂滴。与模型组小鼠相比,药物治疗组小鼠的细胞形态有所改善,细胞质变得较紧密,细胞排列更加规则。结果表明,去铁胺可以改善肝脏的脂肪变性。
3、计算各组小鼠的肝脏体重比(即肝脏重量与体重的比值)。
肝脏体重比是指示肝脏肿大、肝脏脂肪积累和非酒精性脂肪肝的一个重要指标。肝脏体重比的结果见图1c。与空白对照组小鼠相比,模型组小鼠的肝脏体重比显著增加。与模型组小鼠相比,药物治疗组小鼠的肝脏体重比显著降低。结果表明,去铁胺可以抑制肝脏体重比增加。
4、血浆谷丙转氨酶(alt)活性分析
血浆alt的活性反映了肝细胞损伤的程度。当肝细胞发生炎症、坏死等损伤时,转氨酶可释放到血液里,导致转氨酶升高,因此转氨酶水平是临床反应肝细胞损伤的敏感指标。血浆谷丙转氨酶活性的结果见图1d。与空白对照组小鼠相比,模型组小鼠血浆谷丙转氨酶活性显著升高(p<0.05),约为空白对照组小鼠的2.64倍。与模型组小鼠相比,药物治疗组小鼠的血浆谷丙转氨酶活性显著降低,降低幅度约为51.4%。结果表明,去铁胺可以抑制谷丙转氨酶升高。
5、肝脏中的胆固醇和甘油三酯的含量
取冷冻的肝脏组织,在液氮环境中研磨成粉,用“氯仿:甲醇(1:2,体积比)+h2o”进行脂质提取,然后采用lc-ms进行脂质的检测和分析。
肝脏组织中胆固醇(cho)、胆固醇酯(ce)、三酰甘油(tag)、二酰甘油(dag)的含量见图2。图2中,a为肝脏组织中的胆固醇含量,b为肝脏组织中的胆固醇酯含量,c为肝脏组织中的三酰甘油含量,d为肝脏组织中的二酰甘油含量。与空白对照组小鼠相比,模型组小鼠肝脏内的胆固醇、胆固醇酯、三酰甘油、二酰甘油均显著升高。与模型组小鼠相比,药物治疗组小鼠肝脏内的胆固醇、胆固醇酯、三酰甘油、二酰甘油均显著降低。由于脂质在肝细胞内沉积是非酒精性脂肪肝发生发展的必要条件。所以,一定程度上肝脏内脂质沉积反应了脂质在体内的蓄积水平。结果表明,去铁胺可以抑制肝细胞脂质蓄积。
实施例2、动物试验
一、分组处理
取16.7~21.3g、6周龄的雄性c57bl/6小鼠,适应性饲养2周,然后进行试验,试验分为连续进行的两个阶段。
第一阶段如下:
将所述小鼠随机分为二组,对照组(25只)和模型组(55只);
对照组(ctr):采用普通饲料饲喂18周;
模型组(hcd):采用高胆固醇饲料饲喂18周。
第一阶段的18周后(时间点1),每组随机取5只小鼠处死,采用实施例1的步骤二的方法进行相关检测。剩余的小鼠进行第二阶段。
第二阶段如下:
剩余的20只对照组小鼠随机分成两组,空白对照组和药物对照组,每组10只。
剩余的50只模型组小鼠随机分成五组,模型组、药物治疗低剂量组、药物治疗高剂量组、改变食物治疗方案组和改变食物配合药物治疗方案组,每组10只;
空白对照组(ctr):采用普通饲料饲喂18周;
药物对照组(ctr+l72):采用普通饲料饲喂18周;每天注射甲磺酸去铁胺溶液一次,单次注射剂量为“72mg甲磺酸去铁胺/kg体重”;
模型组(hcd):采用高胆固醇饲料饲喂18周;
药物治疗低剂量组(hcd+l36):采用高胆固醇饲料饲喂18周;每天注射甲磺酸去铁胺溶液一次,单次注射剂量为“36mg甲磺酸去铁胺/kg体重”;
药物治疗高剂量组(hcd+l72):采用高胆固醇饲料饲喂18周;每天注射甲磺酸去铁胺溶液一次,单次注射剂量为“72mg甲磺酸去铁胺/kg体重”;
改变食物治疗方案组(chow):采用普通饲料饲喂18周;
改变食物配合药物治疗方案组(chow+l72):采用普通饲料饲喂18周;每天注射甲磺酸去铁胺溶液一次,单次注射剂量为“72mg甲磺酸去铁胺/kg体重”。
第二阶段的9周后(时间点2),每组随机取5只小鼠处死,采用实施例1的步骤二的方法进行相关检测。
第二阶段的18周后(时间点3),每组剩余的5只小鼠处死,采用实施例1的步骤二的方法进行相关检测。
肝脏灌注后的照片见图3的a、b和c。肝组织病理学分析(h&e染色)的照片见图3的d、e和f。肝脏体重比的结果见图4的a、b和c。血浆谷丙转氨酶活性的结果见图4的d、e和f。结果与实施例1的结果一致。通过对比低剂量组和高剂量组的差异,显示了剂量效应关系。并且,去铁胺的治疗效果同已经验证的改变饮食治疗方案有高度的相似性趋势。
实施例3、细胞实验
hepg2细胞饥饿处理24h,然后分为三组,分别处理如下:
空白对照组:在含10g/100mlbsa的基础培养基中培养24h;
模型组:在含10g/100mlbsa和100μg/ml胆固醇的基础培养基中培养24h;
治疗组:在含10g/100mlbsa、100μg/ml胆固醇和50μm甲磺酸去铁胺的基础培养基中培养24h。
完成上述分组处理后,吸弃培养上清,用pbs缓冲液冲洗细胞,然后加入4%pfa溶液并37℃固定10min,然后用60%异丙醇溶液浸洗30s,然后用油红o工作液染色30min,然后加入60%异丙醇溶液冲洗,然后用pbs缓冲液冲洗3遍,然后在显微镜(nikoneclipseti)下观察染色。照片见图5。与空白对照组相比,模型组的脂质蓄积显著增多。与模型组相比,治疗组的脂质蓄积显著变少。
完成上述分组处理后,提取总rna,以gapdh基因为内参基因,采用rt-pcr检测srebp-1基因、fasn基因、scd5基因、scd1基因等脂肪酸合成基因以及tnfα基因、il-8基因、il-1β基因等细胞炎症因子基因的表达水平。结果见图6。
用于检测gapdh基因的引物如下:
上游引物(序列1):5’-accacagtccatgccatcac-3’;
下游引物(序列2):5’-tccaccaccctgttgctgta-3’。
用于检测srebp-1基因的引物如下:
上游引物:5’-ctggtctaccataagctgcac-3’;
下游引物:5’-gactggtcttcactctcaatg-3’。
用于检测fasn基因的引物如下:
上游引物:5’-gtgccttccaactggacgct-3’;
下游引物:5’-tgcctccggctcctccgcaa-3’。
用于检测scd5基因的引物如下:
上游引物:5’-tcgaaagctctgagggcggcggcggc-3’;
下游引物:5’-tctccccagatgtaccagggcacca-3’。
用于检测scd1基因的引物如下:
上游引物:5’-catgctccaagagatctccagttc-3’;
下游引物:5’-ttgcgcacaagcagccaacccacgt-3’。
用于检测tnfα基因的引物如下:
上游引物:5’-gaaagcatgatccgggacgtg-3’;
下游引物:5’-ctgatggtgtgggtgaggag-3’。
用于检测il-8基因的引物如下:
上游引物:5’-aagaaaccaccggaaggaacc-3’;
下游引物:5’-gtgttggcgcagtgtggtc-3’。
用于检测il-1β基因的引物如下:
上游引物:5’-agaagtacctgagctcgcca-3’;
下游引物:5’-caccacttgttgctccatatc-3’。
以上结果表明,去铁胺可以有效地降低由于胆固醇处理所引起的脂肪酸合成相关基因(srebp-1基因、fasn基因、scd5基因和scd1基因)以及炎症相关因子基因(tnfα基因、il-8基因和il-1β基因)的表达升高。
结果表明,去铁胺确实具有抑制脂质合成和炎症发生的作用。
序列表
<110>中国科学院遗传与发育生物学研究所
<120>去铁胺在制备用于治疗非酒精性脂肪肝的药物中的应用
<130>gncyx171064
<160>2
<170>patentinversion3.5
<210>1
<211>20
<212>dna
<213>人工序列
<400>1
accacagtccatgccatcac20
<210>2
<211>20
<212>dna
<213>人工序列
<400>2
tccaccaccctgttgctgta20
- 还没有人留言评论。精彩留言会获得点赞!