清石中药组合物及其制备方法与流程
本发明属于中药应用技术领域,涉及一种清石中药组合物及其制备方法。
背景技术:
尿石症是泌尿系统常见病和多发病,其中肾结石发病率最高,80%为草酸钙结石。中医学认为:肾结石属于“石淋”、“砂淋”、“血淋”、“腰痛”等病症的范畴。临床上多表现为尿液中钙、草酸、磷酸盐排出增加,镁离子、枸橼酸、柠檬酸等排出减少,且常伴有血钙升高。肾结石发病原因和机制比较复杂,是遗传因素和环境因素等共同作用的结果。目前研究认为,草酸钙的过饱和是肾结石形成的必要前提,而后经历成核、生长、聚集以及固相转化等一系列物理化学过程。因此,研制一种有效治疗肾结石的药物,是目前正在探索的一个问题。
技术实现要素:
本发明的一个目的是解决至少上述问题和/或缺陷,并提供至少后面将说明的优点。
本发明还有一个目的是提供一种清石中药组合物。
本发明另有一个目的是提供一种清石中药组合物的制备方法。
为此,本发明提供的技术方案为:
一种清石中药组合物,包括:
海金沙200-1600份和石韦150-1200份。
优选的是,所述的清石中药组合物,还包括如下重量份数的组分:
厚朴150-1200份,茯苓200-1600份,萹蓄150-1200份,茵陈150-1200份,泽泻200-1600份,瞿麦150-1200份和白茅根150-1200份。
优选的是,所述的清石中药组合物,还包括如下重量份数的组分:
大腹皮200-1600份,黄芪150-1200份,乌药200-1600份和炙甘草100-800份。
优选的是,所述的清石中药组合物中,所述清石中药组合物包含如下重量份数的组分:所述海金沙800份,石韦600份,厚朴600份,茯苓800份,萹蓄600份,茵陈600份,泽泻800份,瞿麦600份,白茅根600份,大腹皮800份,黄芪600份,乌药800份和炙甘草400份。
优选的是,所述的清石中药组合物中,该清石中药组合物包含如下重量份数的组分:
所述海金沙1600份,石韦1200份,厚朴1200份,茯苓1600份,萹蓄1200份,茵陈1200份,泽泻1600份,瞿麦1200份,白茅根1200份,大腹皮1600份,黄芪1200份,乌药1600份和炙甘草800份。
优选的是,所述的清石中药组合物中,所述清石中药组合物包含如下重量份数的组分:海金沙400-800份,石韦300-600份,厚朴300-600份,茯苓400-800份,萹蓄300-600份,茵陈300-600份,泽泻400-800份,瞿麦300-600份,白茅根300-600份,大腹皮400-800份,黄芪300-600份,乌药400-800份和炙甘草200-400份。
优选的是,所述的清石中药组合物中,所述清石中药组合物包含如下重量份数的组分:海金沙400份,石韦300份,厚朴300份,茯苓400份,萹蓄300份,茵陈300份,泽泻400份,瞿麦300份,白茅根300份,大腹皮400份,黄芪300份,乌药400份和炙甘草200份。
优选的是,所述的清石中药组合物中,所述清石中药组合物为颗粒制剂、合剂、胶囊制剂、丸剂或片剂,所述丸剂包括提取浸膏丸剂和原粉入药丸剂。
一种清石中药组合物的制备方法,包括如下步骤:
步骤一、以重量份数计,取厚朴、乌药和泽泻,加入乙醇回流提取2小时,滤过,滤液回收乙醇并浓缩至温度50℃~55℃下相对密度为1.20~1.25的浸膏;
步骤二、以重量份数计,步骤一中过滤得到的药渣与海金沙、石韦、茯苓、萹蓄、茵陈、瞿麦、白茅根、大腹皮、黄芪和炙甘草混合,加水浸泡2小时,煎煮二次,每次2小时,煎液滤过,与步骤一中的滤液合并,并浓缩,之后放冷,然后加乙醇使含醇量达60%,静置,滤过,滤液回收乙醇并浓缩至温度50℃~55℃下相对密度为1.20~1.25的浸膏,与上述厚朴、乌药和泽泻浸膏合并混匀,得到清石中药组合物;
其中,所述海金沙200-1600份,石韦150-1200份,厚朴150-1200份,茯苓200-1600份,萹蓄150-1200份,茵陈150-1200份,泽泻200-1600份,瞿麦150-1200份,白茅根150-1200份,大腹皮200-1600份,黄芪150-1200份,乌药200-1600份和炙甘草100-800份。
优选的是,所述的清石中药组合物的制备方法中,还包括如下步骤:
步骤三、向所述清石中药组合物中加糊精和矫味剂,混合,制粒,干燥,制成颗粒1000份,得到清石颗粒。
优选的是,所述的清石中药组合物的制备方法中,所述步骤一中,加入的乙醇的质量分数为40-80%,加入量为前述中药重量的5-10倍;
所述步骤二中,加入的乙醇的质量分数为50-95%。
优选的是,所述的清石中药组合物的制备方法中,所述步骤二中,加入的水量为前述中药重量的5-10倍。
本发明至少包括以下有益效果:
本发明的清石中药组合物由石韦、海金沙、茵陈、厚朴、泽泻等十三味中药提取精制而成,具有消石通淋,凉血止痛的功效。该制剂处方中,海金沙利尿通淋止痛,石韦利尿通淋,且能凉血止血,海金沙得石韦消石兼能止血,正对结石病常伴血尿之症,二者消石通淋,凉血止痛,共为君药。萹蓄利尿通淋兼有清热之功,茵陈清热利湿,泽泻渗湿利水泻热,三者使湿热从小便而出;厚朴燥湿行气,茯苓淡渗利湿兼能补益脾气,从而增强利湿功能,瞿麦、白茅根清热利尿,凉血止血,助石韦与萹蓄、茵陈、泽泻之功,共为臣药。大腹皮、黄芪行气利尿消肿,乌药行气止痛为佐药,三者行气助石以下,排石而出。甘草调和诸药,缓急止痛,兼能清热,为佐使药。
实验结果表明,清石颗粒各治疗组肾组织中钙、草酸含量显著降低,病理检验结果显示,肾内草酸钙结晶分布减少,肾小管扩张、脱落、坏死明显改善。提示清石颗粒可有效抑制草酸钙结石的形成及促进结石排出。同时,尿生化指标分析结果显示,清石颗粒可显著提高24h尿量,促进尿尿酸排泄,碱化尿液。增加尿量和碱化尿液可减少草酸钙过饱和析出,加强对尿路的冲刷作用,减少草酸钙晶体对肾小管上皮细胞的粘附作用,抑制结石的形成。尿酸可与草酸钙晶体结合,促进草酸钙晶体的生长。清石颗粒通过增加尿尿酸的排泄,减少尿酸对结石形成的促进作用,减少草酸钙结晶的形成。
清石颗粒可显著降低血清钙离子、肌酐、尿素含量,缓解肾功能受损症状,改善肾小球滤过功能,保护肾脏功能。高浓度的草酸会导致肾小管上皮细胞产生活性氧簇,导致细胞凋亡、坏死及细胞膜表面特性改变,促进结石形成。清石颗粒可提高肾组织内抗氧化物sod的水平,促进草酸排泄,降低肾小管上皮细胞的损伤,从而抑制草酸钙晶体的形成。
综上所述,清石颗粒可有效降低肾组织内钙、草酸含量,保护肾小管上皮细胞,,促进尿酸的排泄,碱化尿液,增加尿排量,从而抑制草酸钙结石的形成。
同时,本发明采用1%氯化铵联合1%乙二醇复制肾草酸钙结石模型。实验结果表明,模型对照组实验大鼠血清钙、肌酐、尿素显著增高,肾组织内草酸、钙含量及病理检验与空白组均有显著性差异。表示大鼠肾草酸钙结石模型复制成功。
本发明的其它优点、目标和特征将部分通过下面的说明体现,部分还将通过对本发明的研究和实践而为本领域的技术人员所理解。
附图说明
图1为本发明其中一个实施例中催化管和非催化管草酸的吸收光谱曲线;
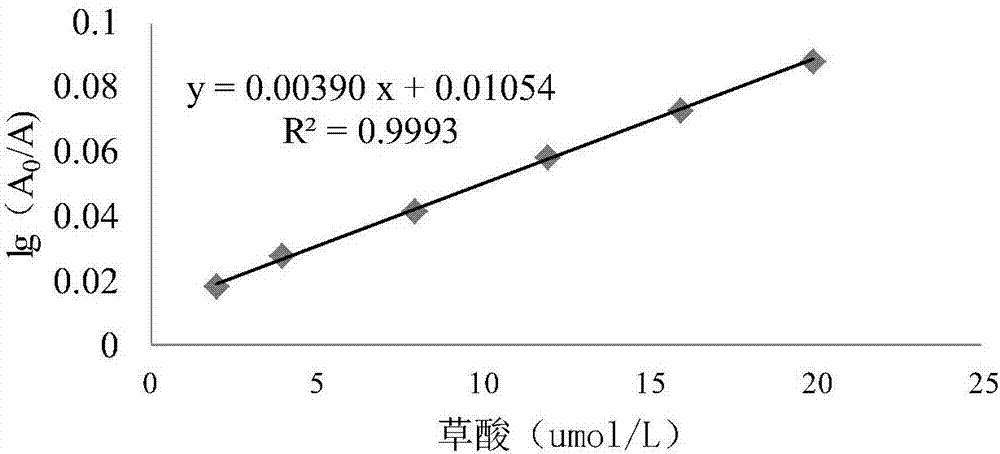
图2为本发明其中一个实施例中草酸标准曲线图;
图3为本发明其中一个实施例中钙离子标准曲线图;
图4为本发明其中一个实施例中400倍放大倍数下空白对照组he染色实验大鼠肾脏组织显微图像;
图5为本发明其中一个实施例中400倍放大倍数下模型对照组he染色实验大鼠肾脏组织显微图像;
图6为本发明其中一个实施例中400倍放大倍数下肾石通组he染色实验大鼠肾脏组织显微图像;
图7为本发明其中一个实施例中400倍放大倍数下清石颗粒低剂量组he染色实验大鼠肾脏组织显微图像;
图8为本发明其中一个实施例中400倍放大倍数下清石颗粒中剂量组he染色实验大鼠肾脏组织显微图像;
图9为本发明其中一个实施例中400倍放大倍数下清石颗粒高剂量组he染色实验大鼠肾脏组织显微图像;
图10为本发明其中一个实施例中清石颗粒对实验大鼠体重的影响柱状图;
图11为本发明其中一个实施例中清石颗粒对实验大鼠血钙的影响柱状图;
图12为本发明其中一个实施例中清石颗粒对实验大鼠肌酐的影响柱状图;
图13为本发明其中一个实施例中清石颗粒对实验大鼠尿素的影响柱状图;
图14为本发明其中一个实施例中清石颗粒对实验大鼠尿量的影响柱状图;
图15为本发明其中一个实施例中清石颗粒对实验大鼠尿ph值的影响柱状图;
图16为本发明其中一个实施例中清石颗粒对实验大鼠尿钙的影响柱状图;
图17为本发明其中一个实施例中清石颗粒对实验大鼠尿尿酸的影响柱状图;
图18为本发明其中一个实施例中清石颗粒对实验大鼠尿草酸的影响柱状图;
图19为本发明其中一个实施例中清石颗粒对实验大鼠肾钙的影响柱状图;
图20为本发明其中一个实施例中清石颗粒对实验大鼠肾草酸的影响柱状图;
图21为本发明其中一个实施例中清石颗粒对实验大鼠sod的影响柱状图;
图22为本发明其中一个实施例中清石颗粒对实验大鼠肾脏系数的影响柱状图。
具体实施方式
下面结合附图对本发明做进一步的详细说明,以令本领域技术人员参照说明书文字能够据以实施。
应当理解,本文所使用的诸如“具有”、“包含”以及“包括”术语并不配出一个或多个其它元件或其组合的存在或添加。
本发明提供一种清石中药组合物,包括如下重量份数的组分:
海金沙200-1600份和石韦150-1200份。
在上述方案中,作为优选,该清石中药组合物,还包括如下重量份数的组分:
厚朴150-1200份,茯苓200-1600份,萹蓄150-1200份,茵陈150-1200份,泽泻200-1600份,瞿麦150-1200份和白茅根150-1200份。
在上述方案中,作为优选,该清石中药组合物,还包括如下重量份数的组分:
200-1600份,黄芪150-1200份,乌药200-1600份和炙甘草100-800。
在一个优选的实施例中,该清石中药组合物包含如下重量份数的组分:
所述海金沙800份,石韦600份,厚朴600份,茯苓800份,萹蓄600份,茵陈600份,泽泻800份,瞿麦600份,白茅根600份,大腹皮800份,黄芪600份,乌药800份和炙甘草400份。
在一个优选的实施例中,该清石中药组合物包含如下重量份数的组分:
所述海金沙1600份,石韦1200份,厚朴1200份,茯苓1600份,萹蓄1200份,茵陈1200份,泽泻1600份,瞿麦1200份,白茅根1200份,大腹皮1600份,黄芪1200份,乌药1600份和炙甘草800份。
在一些优选的实施例中,所述清石中药组合物包含如下重量份数的组分:海金沙400-800份,石韦300-600份,厚朴300-600份,茯苓400-800份,萹蓄300-600份,茵陈300-600份,泽泻400-800份,瞿麦300-600份,白茅根300-600份,大腹皮400-800份,黄芪300-600份,乌药400-800份和炙甘草200-400份。
在一个优选的实施例中,所述清石中药组合物包含如下重量份数的组分:海金沙400份,石韦300份,厚朴300份,茯苓400份,萹蓄300份,茵陈300份,泽泻400份,瞿麦300份,白茅根300份,大腹皮400份,黄芪300份,乌药400份和炙甘草200份。
在一些优选的实施例中,该清石中药组合物为颗粒制剂、合剂、胶囊制剂、丸剂或片剂,所述丸剂包括提取浸膏丸剂和原粉入药丸剂。可以加糖也可以不加糖,制成颗粒制剂。
本发明还提供一种清石中药组合物的制备方法,包括如下步骤:
步骤一、以重量份数计,取厚朴、乌药和泽泻,加入乙醇回流提取2小时,滤过,滤液回收乙醇并浓缩至温度50℃~55℃下相对密度为1.20~1.25的浸膏;
步骤二、以重量份数计,步骤一中过滤得到的药渣与海金沙、石韦、茯苓、萹蓄、茵陈、瞿麦、白茅根、大腹皮、黄芪和炙甘草混合,加水浸泡2小时,煎煮二次,每次2小时,煎液滤过,与步骤一中的滤液合并,并浓缩,之后放冷,然后加乙醇使含醇量达60%,静置,滤过,滤液回收乙醇并浓缩至温度50℃~55℃下相对密度为1.20~1.25的浸膏,与上述厚朴、乌药和泽泻浸膏合并混匀,得到清石中药组合物;
其中,所述海金沙200-1600份,石韦150-1200份,厚朴150-1200份,茯苓200-1600份,萹蓄150-1200份,茵陈150-1200份,泽泻200-1600份,瞿麦150-1200份,白茅根150-1200份,大腹皮200-1600份,黄芪150-1200份,乌药200-1600份和炙甘草100-800份。
在一个优选的实施例中,该清石中药组合物的制备方法还包括如下步骤:
步骤三、向所述清石中药组合物中加糊精和矫味剂,混合,制粒,干燥,制成颗粒1000份,得到清石颗粒。
在一个优选的实施例中,所述步骤一中,加入的乙醇的质量分数为40-80%,加入量为前述中药重量的5-10倍;
所述步骤二中,加入的乙醇的质量分数为50-95%。
在一个优选的实施例中,所述步骤二中,加入的水量为前述中药重量的5-10倍。
为使本领域技术人员更好地理解本发明,现提供如下的实施例进行说明。
实施例1
【药效实验】
1.1实验材料
1.1.1实验动物
sd大鼠:清洁级,体重180-200g,雄性,健康,购于辽宁长生生物技术有限公司,合格证号:scxk(辽)2015-0001。
1.1.2药品和试剂
其中,清石颗粒的处方如下:
【低剂量处方】
【中剂量处方】
【高剂量处方】
1.1.3主要仪器
1.2实验方法
1.2.1大鼠模型的建立与分组
健康雄性sd大鼠48只,体重180-200g,适应性喂养1周后,采用随机数字法分为空白对照组、模型对照组、肾石通组、淸石颗粒低剂量组、中剂量组、高剂量组,每组8只。除空白对照组外其余各组均给予1%乙二醇自由饮水、1%氯化铵2ml/d灌胃。造模1周后,肾石通组、淸石颗粒低剂量组、中剂量组、高剂量组分别按照2.7g/kg、2.25g/kg、4.5g/kg、9.0g/kg灌胃给药,2次/日。模型对照组、空白对照组予以等量的蒸馏水灌胃,给药的同时给予造模药,连续灌胃3周。
1.2.2标本的收集与检测
1.2.2.1尿液标本的收集及指标分析:实验结束前一天收集大鼠24h尿液(加入防腐剂),用于测定24h尿量、尿ph值、尿草酸、尿ca2+。生化自动分析仪测定尿ca2+、比色法测定尿草酸。
1.2.2.2血清标本的收集及指标分析:造模4周后,大鼠腹腔注射10%水合氯醛(质量分数),待肌肉松弛后,腹腔静脉穿刺取血约5ml,注入离心管,静置30分钟,3000r/min离心15min,提取血清标本,-20℃保存待测。
1.2.2.3肾脏标本的收集及指标分析:大鼠取血后,立即完整切取双肾,分离肾被膜,生理盐水冲洗,拭干,称重,左肾放入10%中性甲醛(体积分数)溶液中固定,用于做he染色切片,光学显微镜下观察草酸钙结晶的形成情况及肾脏病理改变;将右肾放入-70℃低温冰箱中保存,用于测定肾脏系数、肾组织中ca2+、sod和草酸含量。
1.2.2.4指标检测分析方法
①一般状况观察:观察大鼠体重、精神状况、饮水量、进食量以及外观形态的变化等指标,并随时记录。
②血生化检测:用全自动生化分析仪测定血清尿素、肌酐、ca2+水平。
③尿生化检测:用全自动生化分析仪测定尿ca2+、尿酸。
④肾脏组织及尿液中草酸含量:采用催化光度法测定肾组织和尿液中草酸含量。
⑤肾脏组织中ca2+含量:采用甲基百里香酚蓝(mtb)比色法测定ca2+含量。
⑥肾脏组织中sod含量:sod试剂盒(wst-1法)。
⑦肾脏病理切片:光学显微镜下观察草酸钙结晶的形成情况及肾脏病理改变。
其中,肾脏组织和尿液中草酸含量均采用催化光度法测定,自配溶媒,摸索试验条件,建立稳定可行的草酸含量测定方法,具体试验内容如下:
1.2.2.4.1尿液中草酸及肾组织中草酸含量的测定
实验采用催化光度法测定尿液中草酸的含量。在酸性条件下,草酸可催化铬酸钾氧化甲基红,生成无色产物,反应方程式如下:
褪色速度可表示为:
采用固定时间法,在一定条件下,草酸的浓度与反应体系的吸光度改变成正比,此为催化光度法测定草酸的基础。
具体操作方法如下:
表1各管操作方法
用蒸馏水调零仪器,15min后,各管均加入1.0mmol/lzrocl2·8h2o1.0ml,摇匀,终止反应。测定吸光度,催化管为as,非催化管为a0。
1.2.2.4.1.1最大吸收波长的确定
取两个15ml具塞试管分别作为催化管(s)和非催化管(b),按照上述催化反应方法操作,在400nm-700nm进行波长扫描。结果见图1。结果表明,反应体系在519nm处有最大吸收,确定最大吸收波长为519nm。
1.2.2.4.1.2线性关系考察
精密称取草酸适量,制成浓度为1mmol/l的贮备液。精密量取贮备液适量,分别稀释至浓度为2,4,8,12,16,20μmol/l的溶液,按照催化反应方法操作,记录吸光度值,以浓度(μmol/l)为横坐标,lg(a0/a)为纵坐标,求得回归方程:y=0.00390x+0.01054,r2=0.9993。试验结果表明,草酸在0-20μmol/l范围内与lg(a0/a)有良好的线性关系。试验结果见表2,图2。
表2草酸标准曲线
1.2.2.4.1.3稳定性试验
取2支15ml具塞试管,作为催化管(s)和非催化管(b),按照催化反应方法操作,分别在制备后0、10、20、30、40、50、60min测定各管的吸光度,测得催化管吸光度的rsd为0.880%,非催化管吸光度的rsd为0.619%,说明反应体系在1小时内稳定,结果见表3。
表3催化管与非催化管显色稳定性考察
1.2.2.4.1.4精密度试验
取10μmol/l的草酸溶液,按照催化反应方法操作,连续测定6次,记录吸光度值,测得吸光度的rsd为0.611%(n=6),符合要求,结果见表4。
表4精密度试验
1.2.2.4.1.5回收率试验
取已测知草酸含量的尿样6份,精密量取0.50ml,分别加入草酸钠对照品溶液0.50ml,制成回收率用供试品溶液,参照催化反应方法,分别测定样品中草酸含量,计算回收率,结果草酸平均回收率为101.3%,rsd为0.858%(n=6),符合要求,结果见表5。
表5回收率数据
1.2.2.4.1.6尿液样本及肾组织中草酸测定
尿液前处理方法:取尿样1.5ml,加入活性炭0.25g,脱色,10000r/min离心10min,滤过,稀释100倍备用。按照催化反应操作方法对尿样中草酸含量进行测定。
肾脏组织前处理方法:取肾组织,精密称定,加入盐酸:乙醇:水(34:120:46)溶液8ml,匀浆,静置48h,3500r/min离心20min,吸取上清液备用。参照尿液中草酸含量测定方法,测定肾组织中草酸含量。
1.2.2.4.2肾组织中sod的测定
取肾组织,精密称定,按照重量(g):体积(ml)=1:9的比例加入9倍体积的生理盐水,剪碎组织,冰水浴制备组织匀浆液,3000r/min离心10min,取上清液。按照sod试剂盒方法操作,测定上清液中蛋白浓度、sod抑制率,计算sod活力。
1.2.2.4.3肾组织中钙离子含量的测定
1.2.2.4.3.1测定原理
组织中钙离子在碱性溶液中与甲基百里香酚蓝(mtb)结合,生成蓝色络合物。通过比色与同样处理的钙标准进行比较,可计算出钙的含量。
1.2.2.4.3.2操作方法,如表6所示。
表6钙测定操作方法
混匀,静置5min后,610nm,1cm光径,双蒸水调零,测定各管吸光度。
计算公式:
1.2.2.4.3.3线性范围
参照2.2.2.4.3.2操作方法,钙离子标准曲线图如图3所示,钙标准曲线数据如表7所示,分别加入不同浓度的钙溶液,测定其吸光度。结果表明在0-5mmol/l范围内,吸光度a与钙溶液浓度具有良好的线性关系。
表7钙标准曲线数据
1.3统计分析方法
实验数据以均数±标准差(±s)表示,采用spss22.0统计软件处理,组间采用t-检验进行比较,p<0.05表示差异具有统计学意义,p<0.01认为具有显著性差异。
1.4实验结果
1.4.1一般情况观察结果
实验过程中无动物死亡。模型对照组大鼠毛发不荣,无光泽,精神倦怠,活动量减少。肾石通组和清石颗粒低、中、高剂量组毛色白净,有光泽,精神状况,饮食活动基本正常。实验后,模型对照组体重较空白对照组体重显著性降低(p<0.01),肾石通组、清石颗粒低、中、高剂量组体重较模型对照组不同程度增加,差异具有统计学意义(p<0.05)。(见表8、图10)
表8清石颗粒对实验大鼠体重的影响
注:*表示与空白对照组比较p<0.05,**表示与空白对照组比较p<0.01,#表示与模型对照组比较p<0.05,##表示与模型对照组比较p<0.01。
1.4.2血生化分析结果
各组实验大鼠血生化分析结果见表9。与空白对照组相比,模型对照组尿素bu,cr,显著升高(p<0.01);与模型对照组相比,肾石通组大鼠血清尿素明显降低(p<0.05),血清肌酐下降不明显。清石颗粒低、中、高剂量组血清bu、cr较模型对照组均显著降低(p<0.01)。与空白对照组相比,模型对照组ca2+显著升高(p<0.01),肾石通组、清石颗粒低、中、高剂量组ca2+较模型对照组显著降低(p<0.01)。(见表9、图11~图13)
表9清石颗粒防治给药对结石大鼠血生化的影响
注:*表示与空白组比较p<0.05,**表示与空白组比较p<0.01,#表示与模型对照组比较p<0.05,##表示与模型组比较p<0.01。
1.4.3尿生化分析结果
各组实验大鼠尿生化分析结果见表10。与空白对照组相比,模型对照组24h尿量、尿钙、尿草酸显著升高(p<0.05),尿ph值、尿尿酸显著降低(p<0.01);与模型对照组相比,肾石通组大鼠24h尿量、尿ph值显著增加(p<0.05),尿尿酸增加不显著,尿草酸、尿钙显著降低(p<0.01)。清石颗粒低、中、高剂量组24h尿量、尿ph值、尿尿酸较模型对照组均显著增加,尿草酸、尿钙均降低。(p<0.05)。(见表10、图14~图18)
表10清石颗粒防治给药对结石大鼠尿生化的影响
注:*表示与空白组比较p<0.05,**表示与空白组比较p<0.01,#表示与模型对照组比较p<0.05,##表示与模型组比较p<0.01
1.4.4肾脏系数及肾组织中钙、草酸、sod测定结果
结果显示:模型对照组肾脏系数较空白对照组显著升高(p<0.01),肾石通组、清石颗粒低、中、高剂量组肾脏系数较模型对照组均有不同程度的降低(p<0.05)。肾组织超氧化物歧化酶测定结果表示,模型对照组sod较空白对照组显著降低(p<0.01),肾石通组、清石颗粒低、中、高剂量组sod较模型对照组均有不同程度的升高(p<0.05)。模型对照组肾组织内钙含、草酸含量与空白对照组相比显著升高(p<0.01),其余各治疗组肾组织内钙、草酸含量均有不同程度的降低。(见表11、图19~图22)
表11清石颗粒防治给药对结石大鼠肾组织的影响
注:*表示与空白组比较p<0.05,**表示与空白组比较p<0.01,#表示与模型对照组比较p<0.05,##表示与模型组比较p<0.01。
1.4.5肾脏病理检查结果
空白对照组实验大鼠肾脏组织结构正常,上皮细胞排列整齐,规则,未见扩张、变性水肿及草酸钙结晶分布。模型对照组大鼠肾脏组织皮质、髓质界限不清晰;上皮细胞呈现高度的肿胀、变性;管腔形状不规则,腔内可见散在或连接成片的草酸钙晶体聚集及坏死物质,间质内可见大量急性、慢性炎性细胞浸润。肾石通组大鼠肾脏组织内上皮细胞肿胀、坏死一定程度改善,草酸钙结晶分布减少,部分间质内出现急性、慢性炎性细胞浸润。清石颗粒各治疗组大鼠肾脏组织内偶见散在草酸钙结晶,皮质、髓质界限清晰;上皮细胞基本无肿胀,管腔排列整齐,间质内急性、慢性细胞浸润较模型对照组显著减轻。清石颗粒低、中、高剂量组未呈现明显的区别。(见图4~图9)
1.5结论与讨论
尿石症是泌尿系统常见病和多发病,其中肾结石发病率最高,80%为草酸钙结石。临床上多表现为尿液中钙、草酸、磷酸盐排出增加,镁离子、枸橼酸、柠檬酸等排出减少,且常伴有血钙升高。肾结石发病原因和机制比较复杂,是遗传因素和环境因素等共同作用的结果。建立符合人类肾结石发病过程的动物模型对阐明肾结石的发病机制和原因,寻找有效的治疗方案具有重要意义。目前研究认为,草酸钙的过饱和是肾结石形成的必要前提,而后经历成核、生长、聚集以及固相转化等一系列物理化学过程。通过增加乙二醇的摄入量,增加体内草酸的代谢生成及尿液中草酸的含量,促进草酸钙的过饱和。氯化铵具有肾脏毒性,能够损伤肾脏肾小管上皮细胞,致使其坏死、脱落,为结晶的形成提供晶核并为草酸钙晶体的粘附提供条件。同时,氯化铵能够酸化尿液,促进草酸钙的过饱和。本实验采用1%氯化铵联合1%乙二醇复制肾草酸钙结石模型。实验结果表明,模型对照组实验大鼠血清钙、肌酐、尿素显著增高,肾组织内草酸、钙含量及病理检验与空白组均有显著性差异。表示大鼠肾草酸钙结石模型复制成功。
中医学认为:肾结石属于“石淋”、“砂淋”、“血淋”、“腰痛”等病症的范畴。临床多表现为小便频短涩、滴沥刺痛、淋漓不尽,甚者排砂石等为主症,病程多缠绵反复。清石颗粒由石韦、海金沙、茵陈、厚朴、泽泻等十三味中药提取精制而成,具有消石通淋,凉血止痛的功效。该制剂处方中,海金沙利尿通淋止痛,石韦利尿通淋,且能凉血止血,海金沙得石韦消石兼能止血,正对结石病常伴血尿之症,二者消石通淋,凉血止痛,共为君药。萹蓄利尿通淋兼有清热之功,茵陈清热利湿,泽泻渗湿利水泻热,三者使湿热从小便而出;厚朴燥湿行气,茯苓淡渗利湿兼能补益脾气,从而增强利湿功能,瞿麦、白茅根清热利尿,凉血止血,助石韦与萹蓄、茵陈、泽泻之功,共为臣药。大腹皮、黄芪行气利尿消肿,乌药行气止痛为佐药,三者行气助石以下,排石而出。甘草调和诸药,缓急止痛,兼能清热,为佐使药。
实验结果表明,清石颗粒各治疗组肾组织中钙、草酸含量显著降低,病理检验结果显示,肾内草酸钙结晶分布减少,肾小管扩张、脱落、坏死明显改善。提示清石颗粒可有效抑制草酸钙结石的形成及促进结石排出。同时,尿生化指标分析结果显示,清石颗粒可显著提高24h尿量,促进尿尿酸排泄,碱化尿液。增加尿量和碱化尿液可减少草酸钙过饱和析出,加强对尿路的冲刷作用,减少草酸钙晶体对肾小管上皮细胞的粘附作用,抑制结石的形成。尿酸可与草酸钙晶体结合,促进草酸钙晶体的生长。清石颗粒通过增加尿尿酸的排泄,减少尿酸对结石形成的促进作用,减少草酸钙结晶的形成。
清石颗粒可显著降低血清钙离子、肌酐、尿素含量,缓解肾功能受损症状,改善肾小球滤过功能,保护肾脏功能。高浓度的草酸会导致肾小管上皮细胞产生活性氧簇,导致细胞凋亡、坏死及细胞膜表面特性改变,促进结石形成。清石颗粒可提高肾组织内抗氧化物sod的水平,促进草酸排泄,降低肾小管上皮细胞的损伤,从而抑制草酸钙晶体的形成。
综上所述,清石颗粒可有效降低肾组织内钙、草酸含量,保护肾小管上皮细胞,,促进尿酸的排泄,碱化尿液,增加尿排量,从而抑制草酸钙结石的形成。其作用机制可能与清石颗粒能增加尿中抑制物水平,减少结石形成促进因素,增加肾小管上皮细胞抗氧化应激水平有关。
实施例2
一种清石颗粒,包含如下重量份数的组分:海金沙320份,石韦240份,厚朴240份,茯苓320份,萹蓄240份,茵陈240份,泽泻320份,瞿麦240份,白茅根240份,大腹皮320份,黄芪240份,乌药320份和炙甘草160份。
一种清石中药组合物的制备方法,包括如下步骤:
步骤一、以重量份数计,取厚朴、乌药和泽泻,加入10倍量70%乙醇回流提取2小时,滤过,滤液回收乙醇并浓缩至温度50℃~55℃下相对密度为1.20~1.25的浸膏。
步骤二、以重量份数计,步骤一中过滤得到的药渣与海金沙、石韦、茯苓、萹蓄、茵陈、瞿麦、白茅根、大腹皮、黄芪和炙甘草混合,加10倍量水浸泡2小时,煎煮二次,每次2小时,煎液滤过,与步骤一中的滤液合并,并浓缩,之后放冷,然后加80%乙醇使含醇量达60%,静置,滤过,滤液回收乙醇并浓缩至温度50℃~55℃下相对密度为1.20~1.25的浸膏,与上述厚朴、乌药和泽泻浸膏合并混匀。
步骤三、向上述组合物中加糊精和矫味剂,混合,制粒,干燥,制成无糖颗粒1000份,得到清石颗粒。
实施例3
一种清石颗粒,包含如下重量份数的组分:海金沙480份,石韦360份,厚朴360份,茯苓480份,萹蓄360份,茵陈360份,泽泻480份,瞿麦360份,白茅根360份,大腹皮480份,黄芪360份,乌药480份和炙甘草240份。
一种清石中药组合物的制备方法,包括如下步骤:
步骤一、以重量份数计,取厚朴、乌药和泽泻,加入8倍量40%乙醇回流提取2小时,滤过,滤液回收乙醇并浓缩至温度50℃~55℃下相对密度为1.20~1.25的浸膏。
步骤二、以重量份数计,步骤一中过滤得到的药渣与海金沙、石韦、茯苓、萹蓄、茵陈、瞿麦、白茅根、大腹皮、黄芪和炙甘草混合,加8倍量水浸泡2小时,煎煮二次,每次2小时,煎液滤过,与步骤一中的滤液合并,并浓缩,之后放冷,然后加50%乙醇使含醇量达60%,静置,滤过,滤液回收乙醇并浓缩至温度50℃~55℃下相对密度为1.20~1.25的浸膏,与上述厚朴、乌药和泽泻浸膏合并混匀。
步骤三、向上述组合物中加糊精、糖和矫味剂,混合,制粒,干燥,制成含糖颗粒1000份,得到清石颗粒。
实施例4
一种清石颗粒,包含如下重量份数的组分:
海金沙200份,石韦150份,厚朴150份,茯苓200份,萹蓄150份,茵陈150份,泽泻200份,瞿麦150份,白茅根150份,大腹皮200份,黄芪150份,乌药200份和炙甘草100份。
一种清石中药组合物的制备方法,包括如下步骤:
步骤一、以重量份数计,取厚朴、乌药和泽泻,加入5倍量80%乙醇回流提取2小时,滤过,滤液回收乙醇并浓缩至温度50℃~55℃下相对密度为1.20~1.25的浸膏。
步骤二、以重量份数计,步骤一中过滤得到的药渣与海金沙、石韦、茯苓、萹蓄、茵陈、瞿麦、白茅根、大腹皮、黄芪和炙甘草混合,加5倍量水浸泡2小时,煎煮二次,每次2小时,煎液滤过,与步骤一中的滤液合并,并浓缩,之后放冷,然后加95%乙醇使含醇量达60%,静置,滤过,滤液回收乙醇并浓缩至温度50℃~55℃下相对密度为1.20~1.25的浸膏,与上述厚朴、乌药和泽泻浸膏合并混匀。
步骤三、向上述组合物中加糊精和矫味剂,混合,制粒,干燥,制成无糖颗粒1000份,得到清石颗粒。
尽管本发明的实施方案已公开如上,但其并不仅仅限于说明书和实施方式中所列运用,它完全可以被适用于各种适合本发明的领域,对于熟悉本领域的人员而言,可容易地实现另外的修改,因此在不背离权利要求及等同范围所限定的一般概念下,本发明并不限于特定的细节和这里示出与描述的图例。
- 还没有人留言评论。精彩留言会获得点赞!