霍山石斛提取物在调控血糖方面的应用的制作方法
本发明属于药学领域,涉及一种中药提取物的新用途,具体涉及一种霍山石斛提取物在调控血糖方面的应用。
背景技术:
霍山石斛(学名:dendrobiumhuoshanense),在国际上有“药界大熊猫”之称的野生霍山石斛,又名米斛,距今已有200多年的历史。霍山石斛原产于我国安徽霍山等地,是国家现代中药重大专项200多个濒危稀缺品种中首位保护品种,是药用石斛中的极品,也是霍山县独有的、拥有原产地地理标志的名贵中药材,历史上被誉为“中华九大仙草之首”、“健康软黄金”,《神农本草》、《本草纲目》均有记载。霍山石斛所含有的多糖能大幅度提高人体内sod(延缓衰老的主要物质),在增强免疫力、抗疲劳、延缓衰老和促进癌细胞凋亡等方面有明显作用,从而达到保健益寿的功效。除霍山石斛之外,其它药用石斛(霍山铁皮石斛和霍山铜皮石斛等)也有着相似的保健和药用价值。
目前,有关糖尿病的发病机制目前主要认为是由多基因诱导和环境相互作用所引起的机体代谢功能障碍而导致的,其中以高血糖为其最为显著的特点。常见的糖尿病主要包括ⅰ型和ⅱ型。
ⅰ型糖尿病主要是由于自身免疫介导的族岛b细胞严重受损或破坏所致自身不能分泌胰岛素,导致胰岛素绝对缺乏,必须长期依靠注射外源性胰岛素维持体内血糖值的稳定,故此t型糖尿病又称作胰岛素依赖型的糖尿病,由于ⅰ型糖尿病常常在35岁之前发病,又称作为青少年糖尿病。ⅰ型糖尿病起病急,代谢素乱症状明显,患者通常有醜症酸中毒的倾向;最终血糖控制不良的患者,易伴随肾病,严重者可能患有尿毒症。
ⅱ型糖尿病主要以胰岛素抵抗或胰岛素分泌相对不足而引起的高血糖症,患者不需要注射胰岛素治疗,因此又称为非胰岛素依赖型的糖尿病。ⅱ型糖尿病多见于成年人,患者多数伴有肥胖症状,其发病缓慢,患者早期无明显症状,通常无酮症酸中毒倾向。ⅱ型糖尿病占据糖尿病患者大约95%的比例,成为糖尿病患者的“主力军”。随年龄的增长病情可能会加重,并伴随多种并发症,严重影响患者身体健康。
糖尿病是多基因导致的代谢综合症状,所以对降血糖的机制不能从单一方向来分析。目前,对多糖降糖机制的探究主要包括通过改善胰岛细胞的损伤来调节血糖,通过促进胰岛素增敏作用来调控血糖,通过激活pparσ和pparγ来降血糖及降血脂,影响α-淀粉酶活性,増加糖储存并协同提高抗氧化来预防高血糖。
rna-seq测序技术从基因组学深层次来寻找效应靶基因和相关代谢信号通路,为研究疾病提供精准的基因定位,不同实验条件处理的样品在转录组中会反应出差异性基因(上调基因和下调基因)和信号通路的关键位点变化,这给研究者提供了更加精确的基因组学科研数据。
发明人通过不断的努力和研究,结合rna-seq测序技术,通过科学的实验发现,霍山石斛及其提取物在调控血糖方面的新的作用机理。
技术实现要素:
本发明的目的在于克服现有技术的不足,提供了一种基于新的作用机理的霍山石斛提取物在调控血糖方面的应用。
本发明是通过以下技术方案实现的:霍山石斛提取物在调控血糖方面的应用,具体为霍山石斛提取物在制备调控血糖药物中的应用,该药物用于缓解糖尿病病情;其中,所述霍山石斛提取物的获取方法为:
(1)取霍山石斛切片,50℃烘干后研磨成粉末;80%乙醇脱去色素,50℃水提5h;95%乙醇,过夜沉醇;60%蒸干,得霍山石斛粗多糖;
(2)采取sevage联合木瓜蛋白酶法脱蛋白,接着进行透析、真空冷冻干燥,得霍山石斛多糖;
(3)选择阴离子交换层析法对霍山石斛多糖进行分离纯化,收集目标洗脱液,浓缩至100-200mg生药/ml,滤过即得。
作为本发明的优选方式之一,所述霍山石斛提取物的获取步骤(2)中,采取sevage联合木瓜蛋白酶法脱蛋白的具体方法为:在获取的霍山石斛粗多糖中加入2%木瓜蛋白酶,50℃水浴2h,再按照霍山石斛粗多糖溶液:正丁醇:氯仿体积比例为25:1:5加入反应试剂,反复操作4-5次,直到无蛋白层。
作为本发明的优选方式之一,所述应用是通过促进p13k/akt信号通路,增强对葡萄糖的转运和利用途径起作用。
作为本发明的优选方式之一,所述霍山石斛提取物通过上调磷酸肌醇激酶来激活胰岛素受体下游的pi3k的表达,产生nadp,刺激ca2+依赖的蛋白激酶,促进葡萄糖转运蛋白对葡萄糖的转运,降低血糖值。
作为本发明的优选方式之一,所述霍山石斛提取物通过上调camp,启动信号级联反应,促进细胞内ca2+浓度上升,增加糖酵解和蛋白合成过程的进行。
作为本发明的优选方式之一,所述药物是以霍山石斛提取物为主要活性成分的药物组合物。
作为本发明的优选方式之一,所述药物组合物含药物活性物质10-100mg,其余为药学上可接受的载体。
作为本发明的优选方式之一,所述药学上可接受的载体具体包括:甘露醇、山梨醇、山梨酸、焦亚硫酸钠、亚硫酸氢钠、硫代硫酸钠、盐酸半胱氨酸、巯基乙酸、蛋氨酸、维生素a、维生素c、维生素e、维生素d、氮酮、edta二钠、edta钙钠,一价碱金属的碳酸盐、醋酸盐、磷酸盐、盐酸、醋酸、硫酸、磷酸、氨基酸、氯化钠、氯化钾、乳酸钠、木糖醇、麦芽糖、葡萄糖、果糖、右旋糖苷、甘氨酸、淀粉、蔗糖、乳糖、甘露糖醇、硅衍生物、纤维素、藻酸盐、明胶、聚乙烯吡咯烷酮、甘油、丙二醇、乙醇、土温60-80、司班-80、蜂蜡、羊毛脂、液体石蜡、十六醇、琼脂、三乙醇胺、碱性氨基酸、尿素、尿囊素、碳酸钙、碳酸氢钙、表面活性剂、聚乙二醇、环糊精、β-环糊精、磷脂类材料、高岭土、滑石粉、硬脂酸钙、硬脂酸镁、植物油、磷脂、聚乙二醇磷脂、油酸、edta。
作为本发明的优选方式之一,所述药物是任何药用剂型。
作为本发明的优选方式之一,所述药用剂型具体包括:片剂、糖衣片剂、薄膜衣片剂、肠溶衣片剂、胶囊剂、硬胶囊剂、软胶囊剂、口服液、口含剂、颗粒剂、冲剂、丸剂、散剂、膏剂、丹剂、混悬剂、溶液剂、注射剂、栓剂、软膏剂、硬膏剂、霜剂、喷雾剂、滴剂、贴剂。
本发明相比现有技术的优点在于:本发明针对现有技术对霍山石斛提取物药理作用机理研究的不足,对霍山石斛提取物在调控血糖方面的应用进行了研究分析,最终确认了基于转绿组学角度的霍山石斛多糖的调控血糖的分子机制:本发明的霍山石斛提取物通过上调磷酸肌醇激酶来激活胰岛素受体下游的pi3k的表达,产生nadp,刺激ca2+依赖的蛋白激酶,促进葡萄糖转运蛋白对葡萄糖的转运,降低血糖值;通过上调camp,启动信号级联反应,促进细胞内ca2+浓度上升,增加糖酵解和蛋白合成过程的进行。
附图说明
图1是实施例1中的deae-52离子柱分离纯化霍山石斛多糖过程中的洗脱曲线图;
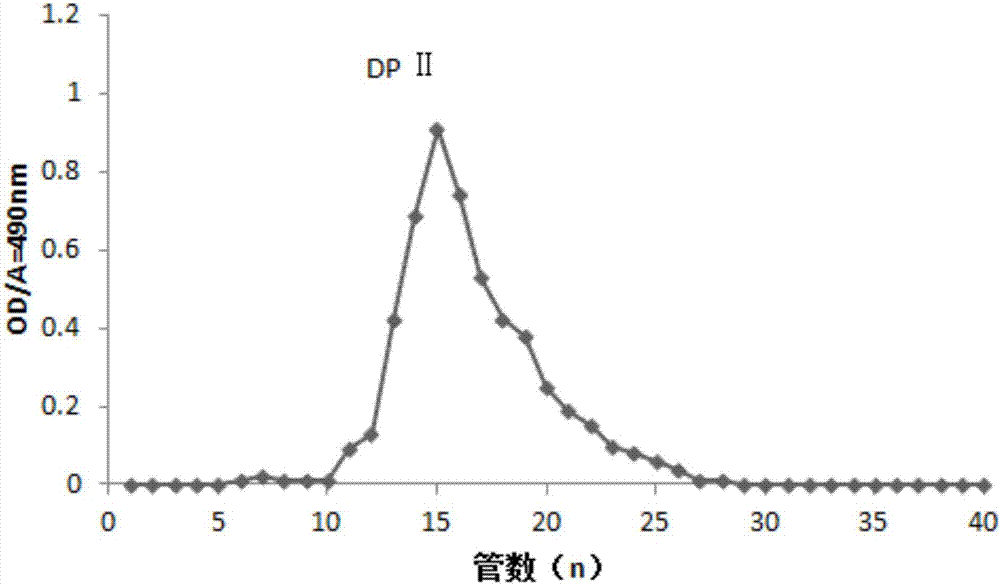
图2是实施例1中的sephadexg-100柱分离纯化dpii组分过程中的洗脱曲线图;
图3是实施例3中的rna文库的构建流程图。
具体实施方式
下面对本发明的实施例作详细说明,本实施例在以本发明技术方案为前提下进行实施,给出了详细的实施方式和具体的操作过程,但本发明的保护范围不限于下述的实施例。
实施例1
本实施例说明霍山石斛提取物。
霍山石斛提取物的获取过程如下:
(1)取霍山石斛切片,50℃烘干后研磨成粉末;80%乙醇脱去色素,50℃水提5h;95%乙醇,过夜沉醇;60%蒸干,得霍山石斛粗多糖。
(2)在获取的霍山石斛粗多糖中加入2%木瓜蛋白酶,50℃水浴2h,再按照霍山石斛粗多糖溶液:正丁醇:氯仿体积比例为25:1:5加入反应试剂,反复操作4-5次,直到无蛋白层;接着进行透析、真空冷冻干燥,得霍山石斛多糖。
(3)霍山石斛多糖的纯化
a、deae-52离子柱层析
选择阴离子交换层析法对霍山石斛多糖进行分离纯化,填充介质为deae-52;deae-52柱层析的流程如下:
①准备工作
霍山石斛多糖:称量0.1g的多糖,溶于50ml蒸溜水中,配制浓度为20mg/ml多糖溶液;
梯度洗脱液的配制:配制0.1mol/l、0.3mol/l、0.5mol/lnacl和0.5mol/lnaoh;
②梯度洗脱
deae-52进行预处理并填充至层析柱中,启动自动收集器,按设置好的程序运行(1ml/min,5min/管),洗脱液按照nacl溶液浓度从低到高依次进行,最后换用0.5mol/lnaoh;
③苯酷-硫酸跟踪检测每个试管中多糖的含量,绘制洗脱曲线,如图1所示,其中,纵坐标为od490nm,横坐标为洗脱管数;由图1可知,收集到三个峰值下的洗脱液,将其分别命名为dpi(试管6-16)、dpii(试管36-41)、dpiii(试管66-71);
④将三个组分dpi、dpii和dpiii分别进行细胞实验,检测其是否具有降血糖的活性,其中,dpii的活性最佳,将其用于后续实验。
b、sephadexg-100柱层析
对deae-52纯化后的dpii组分做进一步的分离纯化,此时填充介质为更改为sephadexg-100;参照deae-52柱层析操作步骤,配制0.05mol/lnacl为洗脱液,洗脱速度1ml/min,4min/管,绘制洗脱曲线,如图2所示,其中,纵坐标为od490nm,横坐标为洗脱管数;由图2可知,将dpii组分经sephadexg-100进一步的洗脱后,只得到一个洗脱峰;收集该洗脱峰下洗脱液,浓缩至100-200mg生药/ml,滤过,作为最终所需的霍山石斛提取物。
c、成分分析
对最终获得的霍山石斛提取物进行成分分析,根据gcms-qp2010气相色谱-质谱联用得出的离子峰碎片及单糖组成可得出:dpii组分主要链接方式由1,3,4-rha,1,4-p-glc,1,3,4-glc,还有一些阿拉伯糖和木糖组成的糖苷键,分子量为48365da。
实施例2
本实施例说明药物组合物。
药物组合物以霍山石斛提取物为主要活性成分,且根据需要加入药物可接受的载体制备成任何可药用的剂型,包括:片剂、糖衣片剂、薄膜衣片剂、肠溶衣片剂、胶囊剂、硬胶囊剂、软胶囊剂、口服液、口含剂、颗粒剂、冲剂、丸剂、散剂、膏剂、丹剂、混悬剂、溶液剂、注射剂、栓剂、软膏剂、硬膏剂、霜剂、喷雾剂、滴剂、贴剂。
其中,药学上可接受的载体包括但不限于:甘露醇、山梨醇、山梨酸、焦亚硫酸钠、亚硫酸氢钠、硫代硫酸钠、盐酸半胱氨酸、巯基乙酸、蛋氨酸、维生素a、维生素c、维生素e、维生素d、氮酮、edta二钠、edta钙钠,一价碱金属的碳酸盐、醋酸盐、磷酸盐、盐酸、醋酸、硫酸、磷酸、氨基酸、氯化钠、氯化钾、乳酸钠、木糖醇、麦芽糖、葡萄糖、果糖、右旋糖苷、甘氨酸、淀粉、蔗糖、乳糖、甘露糖醇、硅衍生物、纤维素、藻酸盐、明胶、聚乙烯吡咯烷酮、甘油、丙二醇、乙醇、土温60-80、司班-80、蜂蜡、羊毛脂、液体石蜡、十六醇、琼脂、三乙醇胺、碱性氨基酸、尿素、尿囊素、碳酸钙、碳酸氢钙、表面活性剂、聚乙二醇、环糊精、β-环糊精、磷脂类材料、高岭土、滑石粉、硬脂酸钙、硬脂酸镁、植物油、磷脂、聚乙二醇磷脂、油酸、edta。
本实施例的药物组合物,单位剂量的药剂含药物活性物质10-100mg,其余为药学上可接受的载体,并且,药学上可接受的载体以重量计是制剂总重量的0.1-99.9%。
本发明的药物组合物在使用时,根据病人的情况来确定用法用量,正常情况下,病人一天服用50-200mg/kg(自身体重)。
实施例3
本实施例通过ⅱ型糖尿病(t2dm)大鼠实验和转绿组学试验说明霍山石斛提取物在增强免疫、调控血糖和改善血脂代谢紊乱方面的应用。
一、ⅱ型糖尿病(t2dm)大鼠实验
(1)实验准备:56只sd雄性大鼠均为spf级(体重200-250g,8周鼠龄),在温度22℃、湿度50±10%、12h昼夜交替的环境中适应一周时间后进行试验。
(2)t2dm大鼠模型试验:
①将大鼠随机分为两组:a组(4只)饲喂普通饲料,b组(52只)饲喂高脂词料;8周后进行糖尿病模型的建立;
②建立糖尿病模型:两组空腹12h,b组腹腔注射25mg/kg/d的stz溶液,a组腹腔注射柠檬酸缓冲液;7d后测定空腹血糖值;当b组血糖值大于11.1mmol/l,则t2dm大鼠建模成功,可用于后续的试验研究。
(3)a组大鼠作为空白组,而b组建模成功的大鼠则随机分成3组(模型组,对照组和dpii组),试验处理情况如下;
nc(空白组):正常的sd大鼠,普通饲料,灌胃纯净水化;
dc(模型组):糖尿病sd大鼠,高脂饲料,灌胃纯净水/d;
ddpii(dpii组):糖尿病sd大鼠,高脂饲料,灌胃石斛多糖组分dpii(350mg/kg/d);
连续灌胃28天,每周在同一天检测各只大鼠的空腹血糖值并记录体重变化,28天后解剖。
二、转绿组学试验
(1)totalrna样品的制备与检测
提取解剖后的大鼠肝脏totalrna,提取参照试剂盒的详细操作进行,并采取0.8%琼脂糖凝胶电泳和agilentannlysis对totalrna样品进行检测。
(2)rna文库的构建
rna文库构建试验操作步骤按照neb建库试剂盒说明进行,文库构建流程如图3所示;对构建好的rna文库使用qubit准确定量,并进行质量检测。
(3)上机测序
文库构建成功后,根据测序深度(下机数据量)首先进行各样本文库混合(pooling)后,选择hiseq2500上机测序,本次试验测序服务和生物信息学分析均由华大基因公司提供。
(4)测序质量评估
评估检测主要涉及:错误率、a/t/g/c分布、数据过滤、数据质量、reads在染色体上的密度分布、重复样品相关性、重复样品基因表达等。
(5)测序结果质量
①构建的totalrna文库质量合格,进行上机测序;
②上机测序错误率低,a/t/g/c碱基含量分布均匀,无剪辑偏好性,符合试验样品性质;
③cleansreads占全部碱基分别为98.57%、98.50%、98.54%97.90%;各组亲q30(%)值均大于90%,数据较好;reads能比对到染色体上,并且在各区间均有表达;保证了测序的准确性;
④生物重复性检查dc组r2=0.977、ddpr2=0.975,数据具有严谨性。
三、差异基因表达分析
对转绿组学试验获得结果进行差异基因表达分析,发现霍山石斛提取物通过增强免疫应答和改善氧化损伤来缓解糖尿病代谢综合症症状;通过促进p13k/akt信号通路,增强对葡萄糖的转运和利用,来降血糖;通过影响脂质代谢信号通路来改善血脂代谢紊乱。具体分析如下:
(1)免疫应答和氧化还原反应分析
表1免疫应答和氧化还原反应中差异基因对比
表1为免疫应答和氧化还原反应中差异基因对比表,其显示的差异表达主要为免疫应答和氧化还原反应,同时还有对外源性物质代谢过程中的转运蛋白等。分析表1可知,霍山石斛提取物在控制糖尿病大鼠病情中的主要表现为:上调α-2免疫巨球蛋白、巨噬细胞活化因子以及快速应激反应来改善机体的免疫应答能力;通过上调谷胱甘肽合酶来增加谷胱甘肽(sod)的酶含量,减少糖尿病大鼠因肥胖和高血脂带来的氧化损伤,同时,协同免疫应答过程促进机体的免疫能力;此外,还存在一些对外源性物质代谢相关的因子,来调控高脂饲料带来的毒理作用。
由此可知,霍山石斛多糖可通过改善机体氧化损伤和免疫应答来调控和缓解糖尿病病情。
(2)糖酵解的代谢通路分析
表2p13k/akt信号通路中差异基因对比
表2为p13k/akt信号通路中差异基因对比表,分析表2可知,霍山石斛多糖可通过上调抗利尿激素来缓解糖尿病“多饮,多尿,多食”中的“多尿”症状;上调的胰岛素(in)与膀岛素样受体蛋白(inr)结合,通过上调磷酸肌醇激酶可激活pi3k的表达,产生nadp,刺激ca2+依赖的蛋白激酶,促进葡萄糖转运蛋白(glut)对葡萄糖的转运,减少多余葡萄糖的储存,降低血糖值;而表皮生长因子可通过与相应受体结合,上调camp,启动信号级联反应,促进细胞内ca2+浓度上升,增加糖酵解和蛋白合成过程的进行。
由此可知,霍山石斛多糖可通过激活胰岛素受体下游的pi3k及其他促进糖酵解的代谢通路来促进葡萄糖的转运和利用,达到降血糖的效果。
(3)脂质代谢信号通路分析
表3脂质代谢中差异基因对比
表3为脂质代谢中差异基因对比表,其显示的差异表达基因主要为脂质代谢信号通路的相关蛋白。分析表3可知,霍山石斛提取物通过上调载脂蛋白l、载脂蛋白ciii、脂质转运蛋白、abc转运蛋白-1来调控脂质的利用和去向;同时上调低密度脂蛋白(ldl)受体和β-乳球蛋白来改善血脂的水平,降低糖尿病高血脂的症状;通过影响脂肪羧酸化酶和脂肪酸去饱和酶的表达来调控脂质代谢紊乱,控制脂肪过度堆积造成的肥胖问题。
由此可知,霍山石斛多糖可通过调控脂质代谢来改善ⅱ型糖尿过度肥胖和血脂代谢素乱。
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!