药物球囊的制作方法
本实用新型属于医疗器械领域,尤其是涉及一种药物球囊。
背景技术:
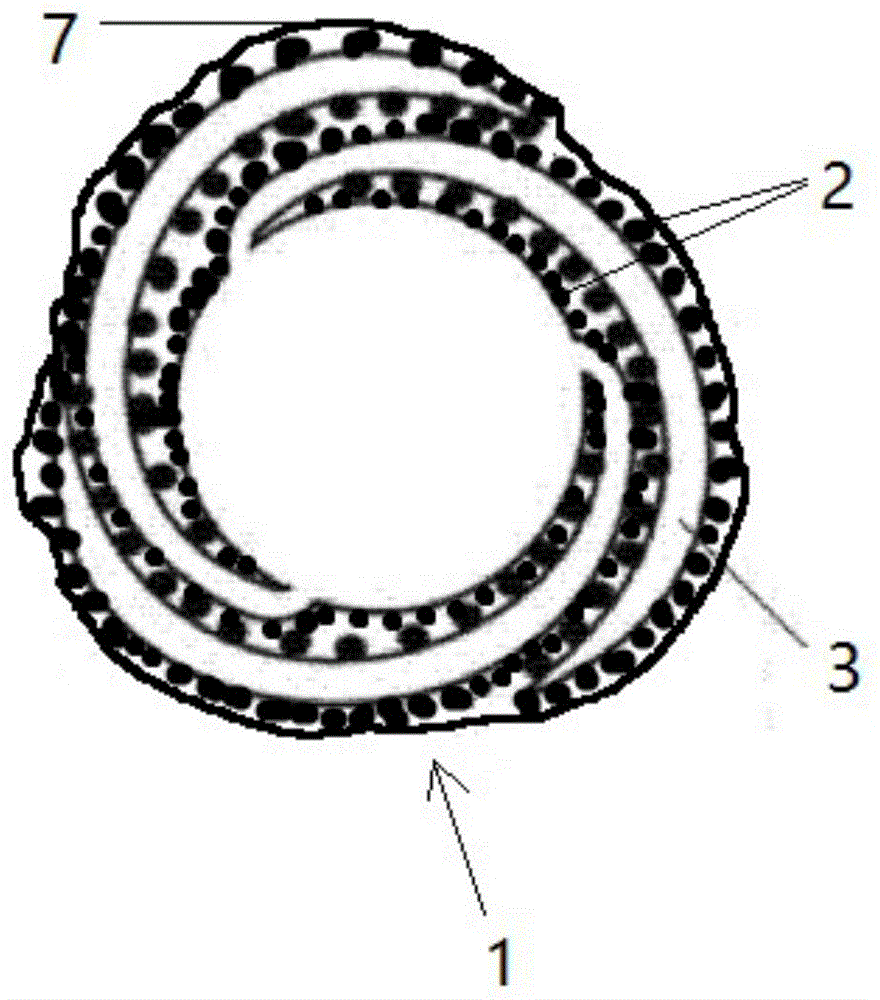
:心血管狭窄是造成冠心病的主要原因之一。介入治疗(PercutaneousCoronaryIntervention,PCI)是治疗心血管狭窄的重要手段。而随着支架使用数量的增加,支架内再狭窄(in-stentrestenosis,ISR)问题日益严重。经过治疗的病人5~60%在短、中期会发生血管再狭窄,严重限制了PCI的发展。近年来,出现了预防介入治疗手术后血管再狭窄的新技术——药物球囊。它是将抗血管内膜增生的药物涂置于球囊表面,当球囊达到病变血管壁并被撑开、充盈,与血管壁内膜接触,并加压快速释放、转移药物至局部血管壁内的技术。药物在局部起到抗血管内膜增生的作用,从而预防血管介入术后再狭窄。其临床应用方面的研究表明药物球囊处理ISR病变时显示良好的疗效,且可用于治疗小血管病变、分叉病变、部分管状动脉血管原发病变,以及不能耐受或不适合长期口服双联抗血小板药物的患者(《药物涂层球囊临床应用中国专家共识》专家组,药物涂层球囊临床应用中国专家共识,中国介入心脏病学杂志,2016,第24卷,第2期,61-67页)。由于当药物球囊处于被撑开、充盈的状态时,药物球囊会阻断血流,因此其持续充盈的时间最多只能在40秒左右,否则可能引起心肌缺血。这就要求药物能在短时间内迅速释放达到满足需要的剂量。技术实现要素:为了解决药物球囊释放足够的药物剂量的问题,本实用新型提供一种药物球囊,包括球囊本体和涂层,涂层包括药物层和保护层;药物层覆盖在球囊本体上;保护层覆盖在药物层外,用于保护药物层上的药物不被血液冲走。进一步地,球囊本体具有至少一个折翼,折翼具有内表面和外表面;球囊本体具有折叠状态和充盈状态;在折叠状态下,折翼的内表面被折叠在内,折翼的外表面显露于外,使得球囊本体的横截面缩小。进一步地,保护层仅覆盖在折翼的外表面的药物层外。作为优选,折翼为3至5个。在一个具体实施方式中,在充盈状态下,球囊本体的横截面呈圆形。在另一个具体实施方式中,在充盈状态下,球囊本体上呈现出凹陷结构,使得血液能够经凹陷结构流过球囊本体。进一步地,凹陷结构设置在折翼之间。作为优选,球囊本体上除凹陷结构外,全身均覆盖有药物。进一步地,凹陷结构平行于球囊本体的轴线。进一步地,凹陷结构的底部设置有显影线;显影线与凹陷结构的延伸方向相同。在一个具体实施方式中,球囊本体上设置有显影元件;显影元件为环状。进一步地,球囊本体的近端和远端均设置有显影元件。作为优选,在充盈状态下,凹陷结构位于球囊本体的横截面的表面。作为优选,在折叠状态下,一部分药物被折叠在内不与血管壁接触。作为优选,在充盈状态下,被折叠在内的药物展露出来。作为优选,球囊本体的全身均覆盖有药物层,即球囊本体的表面360°覆盖有药物。进一步地,保护层所用的原料包括保护剂和第一溶剂;保护剂选自碘普罗胺、聚乙烯吡咯烷酮、聚山梨酯和聚乙二醇中的至少一种。进一步地,保护剂与第一溶剂的配比关系是每毫升第一溶剂对应5-50毫克的保护剂。进一步地,第一溶剂选自水、甲醇、乙醇、丙酮、异丙醇、四氢呋喃、乙腈、乙酸乙酯和甲酸甲酯中的至少一种。进一步地,药物层所用的原料包括药物和第二溶剂。进一步地,药物选自紫杉烷类和大环内酯类中的至少一种。作为优选,药物选自紫杉醇、多西紫杉醇、白蛋白结合型紫杉醇、雷帕霉素、依维莫司、坦罗莫司、唑罗莫司、比奥莫司、他克莫司中的至少一种。进一步地,药物与第二溶剂的配比关系是每毫升第二溶剂对应5-50毫克的药物。进一步地,第二溶剂选自水、甲醇、乙醇、丙酮、异丙醇、四氢呋喃、乙腈、乙酸乙酯和甲酸甲酯中的至少一种。进一步地,药物层所用的原料还包括保护剂。进一步地,药物层所用的原料中含有的药物、保护剂、第二溶剂的配比关系是药物与保护剂的质量比为1:2到2:1,且每毫升第二溶剂对应5-50毫克的药物和保护剂之和。进一步地,药物层所用的原料包括重量份为5份所述药物、10份所述保护剂,且每毫升所述第二溶剂对应5毫克的所述药物和所述保护剂之和;或者7份所述药物、10份所述保护剂,且每毫升所述第二溶剂对应15毫克的所述药物和所述保护剂之和;或者10份所述药物、10份所述保护剂,且每毫升所述第二溶剂对应25毫克的所述药物和所述保护剂之和;或者15份所述药物、10份所述保护剂,且每毫升所述第二溶剂对应40毫克的所述药物和所述保护剂之和;或者20份所述药物、10份所述保护剂,且每毫升所述第二溶剂对应50毫克的所述药物和所述保护剂之和。进一步地,药物层所用的原料为紫杉醇、碘普罗胺和乙醇;或者雷帕霉素、碘普罗胺和乙醇。作为优选,药物层所用的原料为重量份为20份紫杉醇、10份碘普罗胺,且每毫升乙醇对应40毫克的紫杉醇和碘普罗胺之和;或者5份紫杉醇、10份碘普罗胺,且每毫升乙醇对应25毫克的紫杉醇和碘普罗胺之和;或者10份雷帕霉素、10份碘普罗胺,且每毫升乙醇对应10毫克的雷帕霉素和碘普罗胺之和。进一步地,球囊本体的材料为Pebax或者尼龙。进一步地,采用浸提和/或超声喷涂的方式将药物层覆盖到球囊本体上。进一步地,采用浸提和/或超声喷涂的方式将保护层覆盖到药物层外。本实用新型还提供一种如上所述药物球囊的制备方法,包括以下步骤:步骤一、按配比取药物和第二溶剂,混合均匀,得到药物层溶液;按配比取保护剂和第一溶剂,混合均匀,得到保护层溶液;步骤二、采用浸提和/或超声喷涂的方式将步骤一得到的药物层溶液涂覆到处于充盈状态的球囊本体的表面形成药物层;步骤三、将步骤二得到的表面覆盖有药物层的球囊本体折叠;步骤四、采用浸提和/或超声喷涂的方式将步骤一得到的保护层溶液涂覆到步骤三得到的处于折叠状态的球囊本体的表面形成保护层。进一步地,步骤一制备的药物层溶液中还包括按配比取的保护剂。进一步地,步骤三为待药物层干后,再将步骤二得到的表面覆盖有药物层的球囊本体折叠;干燥药物层的温度为室温到60℃。进一步地,干燥时间为3-30分钟。进一步地,步骤三具体为将步骤二得到的表面覆盖有药物层的球囊本体充气至内部压力为1-3atm,然后在40-60℃条件下将其折叠。进一步地,压制折痕的时间为60-600秒。有益效果:1、在血管中输送药物球囊的过程中,血液会对药物球囊的表面进行冲击,容易造成其上的药物脱落。保护层的存在能够较好地保护药物不被血液冲走,从而提高药物球囊到达指定位置后释放足量的药物到作用部位。由于保护层位于最外层,因此会率先受到血液冲击而部分或者全部脱落。当保护层脱落后,药物层显露出来,虽然也会受到血液冲击,但是延迟了其受到血液冲击的时间,因此避免或者减少了在输送过程中药物的丢失。再配合折叠的设计,本实用新型的药物球囊拥有避免药物在输送过程中脱落的双保险:一个来自保护层;另一个来自将部分药物覆盖在折翼的内表面。折翼有利于保护被折叠在内的药物不被血流冲走,从而避免药物损失。2、对球囊本体进行360°覆盖药物,使得血管全周都能接受到药物,治疗效果更佳,且生产更加方便。3、球囊本体的横截面呈圆形有利于与血管贴合。4、充盈状态下,球囊本体的横截面表现为折翼之间设置有凹陷,有利于血流通过,从而可以适当地延长持续充盈的时间,提升药物作用效果。5、材料为Pebax,半顺应性,贴壁性能好。适用于对于心脏支架堵塞,可以将球囊伸入,将堵塞部位撑大,球囊表面的药物可以涂上放内皮细胞生长的药物。6、材料为尼龙,比较硬,非顺应性,更适用于在支架植入前进行扩张。7、本实用新型的制备方法简便,尤其是当保护层和药物层的原料及其配比区别仅在于药物层加有药物,而保护层没有时,制备保护层时只需要在加入药物前取出部分溶液作为制备保护层的原料即可,没有增加额外制备保护层溶液的工序。附图说明图1是本实用新型所涉及的一种药物球囊在折叠状态下的结构示意图。图2是制备过程中,药物球囊尚未完全折叠的结构示意图。图3是实施例1中的药物球囊在充盈状态下的结构示意图。图4是实施例2中的药物球囊在充盈状态下的结构示意图。图5是实施例2中显影线与凹陷结构的局部的结构示意图。具体实施方式下面结合附图与具体实施例对本实用新型做进一步的描述,本实用新型的保护内容不局限于以下实施例。在不背离实用新型构思的精神和范围下,本领域技术人员能够想到的变化和优点都被包括在本实用新型中,并且以所附的权利要求书为保护范围。实施例1图1-3示出了本实用新型所涉及的药物球囊的一个具体实施例。其中,图2显示了制备过程中,药物球囊尚未完全折叠的时候的一个状态,此时保护层尚未覆盖在药物层上。在本实施例中,药物球囊包括球囊本体1和涂层。涂层分为保护层7和药物层2。球囊本体1的表面360°都覆盖有药物。球囊本体1具有三个折翼3。在本实用新型中折翼3的数量不限于三个。在折叠状态下,覆盖在折翼3内表面上的药物被折叠在内,因此不与血管壁接触,从而确保了这部分药物不会在球囊本体1穿越血管的过程中被损耗掉。在充盈状态下,如图3所示,覆盖在折翼3内表面上的药物展露出来,连同其余的药物(包括覆盖在折翼3外表面上的药物)一起与血管壁接触,发挥药效。在本实施例中,球囊本体1的横截面呈圆形,以便与血管贴合,使得更多的药物与血管发生作用。折翼3的折痕平行于球囊本体1的轴线。球囊本体1的轴线为穿过球囊本体1的导管。球囊本体1的近端和远端均设置有环状的显影元件。球囊本体1的材料为Pebax或者尼龙;药物选自紫杉烷类和大环内酯类中的至少一种,比如紫杉醇、多西紫杉醇、白蛋白结合型紫杉醇、雷帕霉素、依维莫司、坦罗莫司、唑罗莫司、比奥莫司或他克莫司。实施例2图4示出了本实用新型的另一种药物球囊,其充盈状态下,球囊本体1的横截面表现为相邻折翼间设置有凹陷4。凹陷4的作用是,使得药物球囊即使在充盈状态下也不会完全阻断血流,从而可以延长持续充盈的时间,为药物释放提供更多的时间,从而达到更好的效果。其余设计与实施例1同,均是360°覆盖药物,以及具备折翼3。凹陷4的数量与折翼3的数量相同。实施例3在充盈状态下,球囊本体的横截面的表面设置有凹陷,有利于血流通过。与实施例2不同的是,该凹陷并不限于是折翼之间的凹陷。其余同实施例2。实施例4如图5所示,本实施例中凹陷结构的底部41和侧面42均平行于球囊本体的轴线。球囊本体的轴线为穿过球囊本体轴心的导管5。显影线6设置在底部41上,也平行于导管5。其余与实施例2同。实施例5本实施例中,用球囊本体的近端和远端设置的环状的显影元件替换实施例4中的显影线,其余与实施例4同。实施例6药物球囊的制备实施例6.1步骤一、取紫杉醇和甲醇,混合均匀,配置成含紫杉醇5mg/ml的甲醇溶液,即药物层溶液;取碘普罗胺和乙醇,混合均匀,配置成含碘普罗胺5mg/ml的乙醇溶液,即保护层溶液;步骤二、采用超声喷涂的方式将步骤一得到的药物层溶液涂覆到处于充盈状态的球囊本体的表面形成药物层;步骤三、室温晾干药物层后,将步骤二得到的表面覆盖有药物层的球囊本体充气至内部压力为1atm,然后60℃下折叠60秒;步骤四、采用超声喷涂的方式将步骤一得到的保护层溶液涂覆到步骤三得到的处于折叠状态的球囊本体的表面形成覆盖在药物层外的保护层,得到实施例6.1制备的药物球囊。实施例6.2步骤一、取紫杉醇,溶于乙醇,混合均匀,配置成含紫杉醇为10mg/ml的乙醇溶液,即药物层溶液;取碘普罗胺和75%乙醇水溶液,混合均匀,配置成含碘普罗胺10mg/ml的乙醇水溶液,即保护层溶液;步骤二、采用浸提的方式将步骤一得到的药物层溶液涂覆到处于充盈状态的球囊本体的表面形成药物层;步骤三、60℃烘干药物层后,将步骤二得到的表面覆盖有药物层的球囊本体充气至内部压力为2atm,然后40℃下折叠600秒;步骤四、采用浸提的方式将步骤一得到的保护层溶液涂覆到步骤三得到的处于折叠状态的球囊本体的表面形成覆盖在药物层外的保护层,得到实施例6.2制备的药物球囊。实施例6.3步骤一、取碘普罗胺和乙醇,混合均匀,配置成含碘普罗胺15mg/ml的乙醇溶液,即保护层溶液;取一部分保护层溶液,向里面加入紫杉醇,使得紫杉醇和碘普罗胺的质量比为1:1,混合均匀,得到药物层溶液;步骤二、采用超声喷涂的方式将步骤一得到的药物层溶液涂覆到处于充盈状态的球囊本体的表面形成药物层;步骤三、室温晾干药物层后,将步骤二得到的表面覆盖有药物层的球囊本体充气至内部压力为2atm,然后50℃下折叠120秒;步骤四、采用超声喷涂的方式将步骤一得到的保护层溶液涂覆到步骤三得到的处于折叠状态的球囊本体的表面形成覆盖在药物层外的保护层,得到实施例6.3制备的药物球囊。实施例6.4步骤一、取碘普罗胺和四氢呋喃,混合均匀,配置成含碘普罗胺15mg/ml的四氢呋喃溶液,即保护层溶液;取一部分保护层溶液,向里面加入雷帕霉素,使得雷帕霉素和碘普罗胺的质量比为2:1,混合均匀,得到药物层溶液;步骤二、采用超声喷涂的方式将步骤一得到的药物层溶液涂覆到处于充盈状态的球囊本体的表面形成药物层;步骤三、50℃烘干药物层后,将步骤二得到的表面覆盖有药物层的球囊本体充气至内部压力为3atm,然后45℃下折叠400秒;步骤四、采用超声喷涂的方式将步骤一得到的保护层溶液涂覆到步骤三得到的处于折叠状态的球囊本体的表面形成覆盖在药物层外的保护层,得到实施例6.4制备的药物球囊。实施例6.5步骤一、取碘普罗胺和乙酸乙酯,混合均匀,配置成含碘普罗胺30mg/ml的乙酸乙酯溶液,即保护层溶液;取一部分保护层溶液,向里面加入他克莫司,使得他克莫司和碘普罗胺的质量比为2:1,混合均匀,得到药物层溶液;步骤二、采用超声喷涂的方式将步骤一得到的药物层溶液涂覆到处于充盈状态的球囊本体的表面形成药物层;步骤三、60℃烘干药物层后,将步骤二得到的表面覆盖有药物层的球囊本体充气至内部压力为2atm,然后45℃下折叠300秒;步骤四、采用超声喷涂的方式将步骤一得到的保护层溶液涂覆到步骤三得到的处于折叠状态的球囊本体的表面形成覆盖在药物层外的保护层,得到实施例6.5制备的药物球囊。对比例1不带保护层其余与实施例6相同,即包含了对比例1.1到1.5制备的药物球囊。实验例1脱落率实验1、实验目的研究本实用新型药物球囊的药物的脱落率,以及与保护剂的脱落率的关系。2、实验方法2.1药物脱落血管模型的准备选择符合《ASTMF2394–07(2013)安装在输送系统上的球囊扩张血管支架稳当性测量指南》标准中的血管模型,置于37℃水浴中,保持1h,将该模型的出口端用橡皮塞堵住,在入口端插入导引导管,在导引导管中插入到导引导丝,在模拟血管管路和导引导管中注入模拟血液,但不要让模拟液体流出。2.2药物球囊的模拟使用将导引导丝插入到药物球囊导管的导丝腔,沿导引导丝推送药物球囊导管,模拟手术应用,分别将实施例6.1到6.5、对比例1.1到1.5制备的药物球囊推送至目标位置,但不要扩张药物球囊,固定药物球囊导管,并保持90s。2.3剩余的药物量的计算撤回药物球囊,将该药物球囊上剩余的药物和保护剂洗脱,测定洗脱液的体积V1,使用HPLC分别测定洗脱液中药物和保护剂浓度,分别为c1和c2,计算球囊上剩余的药物的量:m1=V1·c1。2.4脱落率的计算按照如下公式计算药物的脱落率:药物的脱落率=(药物标称含量-m1)/药物标称含量·100%。3、实验结果具体实验结果如表1所示。表1实施例6.1到6.5及各对比例脱落率的实验结果由表1可知,与对比例1.1到1.5制备的药物球囊相比,实施例6.1到6.5制备的药物球囊的药物的脱落率分别显著低于对比例1.1到1.5,P>0.05。4、实验结论本实用新型制备的药物球囊的药物在保护层的保护下,药物的脱落率能够获得显著降低。实验例2释放率实验1、实验目的研究本实用新型药物球囊中药物的释放率,以及与保护层的脱落率的关系。2、实验方法2.1药物释放血管模型的准备选择两个符合《ASTMF2394–07(2013)安装在输送系统上的球囊扩张血管支架稳当性测量指南》标准中的血管模型,置于37℃水浴中,保持1h。选择猪冠脉血管作为目标位置,将其置于选中的两个血管模型之间,一端与其中一个模型(模型一)的出口端连接,另一端与另一个模型(模型二)的入口端连接,形成连通的模拟血管管路。将模型二的出口端用橡皮塞堵住,在模型一的入口端插入导引导管,在导引导管中插入到导引导丝,在模拟血管管路和导引导管中注入模拟血液,但不要让模拟液体流出。2.2药物球囊的模拟使用将导引导丝插入到药物球囊导管的导丝腔,沿导引导丝推送药物球囊导管,模拟手术应用,分别将实施例6.1到6.5和对比例1.1到1.5制备的药物球囊推送至目标位置,即猪冠脉血管,先不要扩张药物球囊,固定药物球囊导管,并保持90s。然后,使用液体扩张药物球囊,使药物球囊内部液压达到标称压力,药物球囊扩张过渡伸展率(即:药物球囊直径与血管直径的比例)约为1.10~1.20,以使药物球囊和猪冠脉血管保持贴壁,扩张保持30-60s,收缩并撤回药物球囊。在测试时,可以根据需要进行不超过3次的扩张和回缩,应记录扩张次数。2.3剩余的药物量的计算将该药物球囊上剩余的药物洗脱;测定洗脱液的体积V2,使用HPLC测定洗脱液中药物浓度c2,计算药物球囊上剩余的药物的量:m2=V2·c2。2.4药物释放率的计算按照如下公式计算药物释放率:药物释放率=[药物标称含量-(m1-m2)]/药物标称含量·100%。3、实验结果具体实验结果如表2所示。表2实施例6.1到6.5及各对比例药物释放率的实验结果扩张30s时药物释放率(%)扩张60s时药物释放率(%)实施例6.16880对比例1.15566实施例6.27088对比例1.25869实施例6.37490对比例1.35970实施例6.47188对比例1.45365实施例6.56985对比例1.55662由表2可知,扩张30s时和扩张60s时,与对比例1.1到15制备的药物球囊相比,实施例6.1到6.5制备的药物球囊中的药物释放率均较高。4、实验结论本实用新型制备的药物球囊中的药物释放率较高。这与本实用新型的药物脱落率较低有关。因为保护层的保护,使得药物脱落率降低,从而使得到达目标位置,开始工作(药物球囊被撑大,处于充盈状态)时,药物球囊上所保留的药物较多,从而提高了释放率。以上详细描述了本实用新型的较佳具体实施例,仅为了说明本实用新型的技术构思及特点,其目的在于让本领域技术人员能够了解本实用新型的内容并据以实施,并不能以此限制本实用新型的保护范围。应当理解,本领域的普通技术人员无需创造性劳动就可以根据本实用新型的构思作出诸多修改和变化。因此,凡本
技术领域:
中技术人员依本实用新型的构思在现有技术的基础上通过逻辑分析、推理或者有限的实验可以得到的技术方案,皆应在由权利要求书所确定的保护范围内。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1