迷走神经刺激患者选择的制作方法
本申请要求2016年4月1日提交的美国临时专利申请号62/317,352和2016年4月4日提交的美国临时专利申请号62/318,156的优先权和利益,这两个专利申请特此通过引用被全部并入。
背景
充血性心力衰竭(chf)是一种进行性和身体衰弱的慢性疾病,其中心脏不能够提供足够的血液流量来满足身体的需要。病理上,chf特征在于伴有受损的动脉和心肺压力反射功能和减少的迷走神经活动的升高的神经兴奋状态。chf由心功能不全引发,心功能不全触发交感肾上腺(交感)神经和肾素-血管紧张素-醛固酮荷尔蒙系统的代偿性激活。最初,这些机制帮助心脏补偿恶化的泵送功能,然而随着时间的推移,驱使过度的交感神经激活和增加的心率促进进行性左心室功能紊乱和有害的重塑。
慢性心功能不全源于交感和副交感神经系统的自主失衡,如果保持未治疗,该自主失衡导致心律失常发射,包括心动过缓、逐渐恶化的心功能和最终死亡。用于管理慢性心功能不全的当前护理标准要求药理剂——包括利尿剂、血管紧张素转换酶抑制剂、血管紧张素受体阻断剂、β-受体阻断剂和醛固酮拮抗剂——处方以及饮食和生活方式的改变。然而,这些措施的有效性仅仅是治标的,不是有治病效力的,而且患者常常由于疾病进展而遭受副作用和同病,例如肺水肿、睡眠呼吸暂停和心肌缺血。
心脏再同步化治疗(crt)最近已对具有受损的收缩功能的那些慢性心功能不全患者变得可用。crt通过协调的双心室起搏来恢复同步心跳,双心室起搏有助于改善收缩性心脏性能。然而,crt仅解决收缩功能不全,且限于展示宽qrs波群(机械不同步)和减小的左心室射血分数的患者。
神经刺激已经被提议作为对慢性心功能不全的补充治疗,其直接解决基础自主神经系统失衡,而不是缓解症状或直接起搏心肌。在交感神经系统和副交感神经系统的元件内和当中的活动通过对由越过细胞膜流动的离子电流介导的关键生物过程施加高分辨率控制来调节心血管功能。累积地,在健康人身上,这些生物过程的自主调节导致心率的稳定体内平衡和正常的收缩性能。然而,当疾病过程扰乱自主功能时,体内平衡丧失,且心血管功能退化;因此,收缩性能变得次优,且心率调节以产生正反馈回路的方式被扭曲,正反馈回路促进慢性心功能不全的发展并最终冒chf的风险。神经刺激可以通过电气地调节选择的迷走神经纤维凭借对过度神经激活的抑制来打破正反馈回路。电调节可能有助于改善心脏机械功能,并降低心脏的内在神经系统在慢性自主神经系统失衡期间诱发房性和室性心律失常(包括心动过缓)的倾向。
迷走神经刺激(vns)目前仅被批准用于耐药性癫痫和抑郁症的临床治疗,尽管vns已经被提议作为chf的长期治疗。然而,vns的功效可能从一个患者到另一患者改变,使得vns可能积极地影响一些患者,而最低限度地或甚至不利地影响其他患者。
概述
一个实施例涉及一种用于评估患者对接受迷走神经刺激治疗的适宜性的方法。该方法包括接收关于患者对接受迷走神经刺激治疗的适宜性的标准;控制刺激设备以向患者的迷走神经提供刺激;从传感器接收指示患者对迷走神经的刺激的生理反应的反应数据;以及基于标准和患者对刺激的生理反应来确定患者对接受迷走神经刺激治疗的适宜性。
另一实施例涉及一种用于评估患者对接受迷走神经刺激治疗的适宜性的方法。该方法包括接收关于患者对接受迷走神经刺激治疗的适宜性的标准;接收患者的特征;以及基于标准和患者的特征来确定患者对接受迷走神经刺激治疗的适宜性。
又一实施例涉及一种用于评估患者对接受迷走神经刺激治疗的适宜性的方法。该方法包括接收关于患者对接受迷走神经刺激治疗的适宜性的标准;接收患者的特征;基于该特征相对于标准来确定特征的值;以及基于相对于功效映射(efficacymapping)的值来确定患者对接受迷走神经刺激治疗的适宜性,其中功效映射包括阈值。
前述概述仅是说明性的,且并没有以任何方式被规定为限制性的。除了上述说明性方面、实施例和特征之外,通过参考附图和下面的详细描述,另外的方面、实施例和特征将变得明显。
附图简述
从参考附图做出的本发明的优选实施例的下面的详细描述中,本发明的另外的特征、特性和优点将对本领域中的普通技术人员变得明显,其中相似的参考符号表示相似的元件,以及其中:
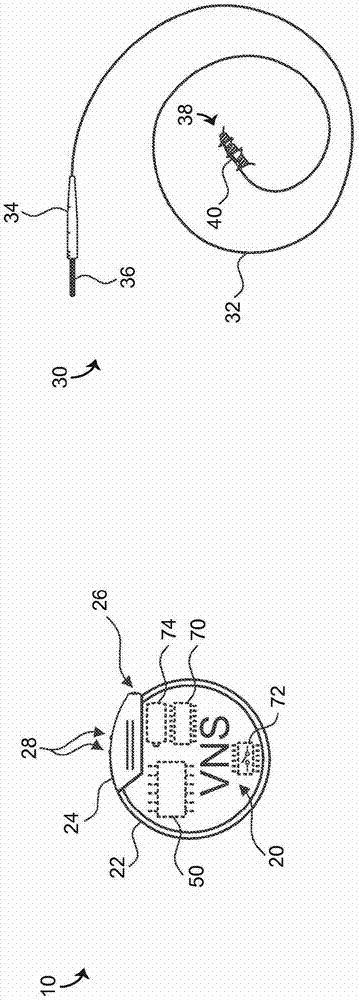
图1是根据示例性实施例的具有神经刺激器和引线的神经刺激设备的图示;
图2是根据示例性实施例的图1的神经刺激设备的示意性框图;
图3a是根据示例性实施例的植入患者体内以直接向迷走神经提供迷走神经刺激的图1的神经刺激设备的图示;
图3b是根据示例性实施例的植入患者体内以通过静脉系统在血管内向迷走神经提供迷走神经刺激的图1的神经刺激设备的图示;
图3c是根据示例性实施例的位于患者的身体外部以提供迷走神经刺激的图1的神经刺激设备的图示;
图4a是根据示例性实施例的迷走神经的图示;
图4b是根据示例性实施例的位于患者的静脉内以提供血管内迷走神经刺激的图1的引线的图示;
图5是示出根据示例性实施例的迷走神经刺激刺激分析系统的示意性框图;
图6是根据示例性实施例的用于评估患者对接受迷走神经刺激治疗的适宜性的方法的流程图;以及
图7是根据另一示例性实施例的用于评估患者对接受迷走神经刺激治疗的适宜性的方法的流程图。
详细描述
现在将参考某些示例和实施例描述本公开的各个方面,这些示例和实施例旨在说明而不是限制本公开。
在本公开中没有什么意欲暗示所公开的实施例的任何特定特征或特性是必要的。保护范围由跟随本描述的权利要求而不是由本文描述的任何特定实施例限定。在转到详细示出示例实施方式的附图之前,应当理解,本申请不限于在描述中阐述或在附图中示出的细节或方法。还应当理解,术语仅用于描述的目的,且不应被视为限制性的。
总体上参考附图,本公开涉及用于识别与vns的使用兼容和/或不兼容的患者以治疗和/或降低经历心力衰竭的可能性的装置、系统和方法。心力衰竭是一种具有暗示作为支持生理循环的泵的心脏的损伤的症状和体征的复杂的临床综合征,该损伤可能由心脏的结构和/或功能异常引起。心力衰竭的盛行很普遍,影响了大约1-2%的总人口。尽管有在治疗策略方面的最近进步,但进行性心力衰竭的管理继续保持是一项重大挑战。
心力衰竭的病理生理学特征在于血液动力学异常,其随着交感神经系统的交感神经活性的增加和副交感神经系统的迷走神经活动的退出而导致神经激素激活和自主失衡。交感神经系统涉及具有正性变力效应(例如心率增加以维持心输出量等)和正性肌力效应(例如通过去甲肾上腺素刺激的心肌收缩力增加等)的循环荷尔蒙。交感神经系统的增加的活动(例如能量成本等)可能导致心肌缺血(例如,因为心肌氧摄取也增加,等等)和/或室性心律失常的更高风险。增加的心率也可能对心室充盈时间消极地起作用,这可能进一步使心脏和/或其他器官暴露于局部缺血。
vns可用于心力衰竭的治疗,因为它包括激活副交感神经系统,以便补偿交感神经系统的过度活动。在vns期间,刺激可以通过使用具有由可植入神经刺激器供电的电极的引线直接和/或间接地施加到迷走神经。作为例子,电极(例如卡肤型电极、螺旋型电极等)可以附接到迷走神经的外部(例如,在迷走神经的颈部水平处等)以直接向迷走神经提供vns。作为另一个例子,引线(例如支架、猪尾引线、螺旋引线、预制引线等)可以在血管内位于静脉系统内。这种血管内引线可以具有定位成通过静脉系统(例如通过上腔静脉、肺动脉、奇静脉等的壁)经血管向迷走神经提供vns的电极。用于vns的输送的血管内方法可以被特征化为血管内迷走神经刺激(evns)。在本文件中,术语“evns”可以与术语“vns”可互换地使用,除非另有说明。关于一些实施例,evns可以被认为是vns的可选形式,而关于其他实施例,evns可以被认为是vns的子集。
据信,某些形式的vns治疗可能不能令人满意地治疗和/或可能不能降低一些患者的心力衰竭的风险或影响,可能给与一些患者无效的治疗,和/或可能使一些患者暴露于副作用或其他风险。特别是,在inovate-hf研究中的biocontrolmedical(clinicaltrials.gov标识符:nct01303718)评估了被命名为
根据示例性实施例,本公开的装置、系统和方法可用于识别作为对经由vns和/或evns设备和/或方法提供的vns治疗的适合或不适合的候选者的患者。这样的事可以通过确定哪些患者可能对vns和/或evns很好地做出反应以及哪些患者可能不能很好地做出反应来完成,从而提高治疗的功效。在一个实施例中,该确定基于患者的一个或更多个生理特征(例如,年龄、静息心率、心率变异性等)。在其他实施例中,该确定基于在使用vns和/或evns设备和/或方法来评估患者的评估期间的患者的生理反应。在还有其他实施例中,该确定基于在使用外部施加的刺激(例如,对耳朵、胸部、背部、颈部、耳廓vns等)的评估期间的患者的生理反应。在一些实施例中,该确定基于一个或更多个生理特征、在使用evns的评估期间的生理反应、在使用vns的评估期间的生理反应和/或在使用外部刺激的评估期间的生理反应的组合。这种确定可以减少被执行来将vns神经刺激器(其可能显示对evns和/或vns没有做出反应的指示)植入患者体内的不必要的侵入性医疗程序,从而防止可能从这种程序产生的不利的医疗影响和/或不必要的医疗费用,以及通过evns和/或vns增加art在心力衰竭中的功效。在特定实施例中,使用非侵入性或微创vns和/或evns设备和/或方法对患者进行的初步评估被用于筛选患者和/或生成相关信息,以确定患者是否能够或应该接受更侵入性的程序和/或植入的vns设备和/或系统。
现在参考图1-4b,被示为迷走神经刺激器10的刺激设备可以植入被示为患者100的人的体内,或者相对于患者100的身体位于外部,以向患者100的迷走神经提供evns和vns中的至少一个。根据图1-4b所示的示例性实施例,迷走神经刺激器10可以通过以电极终止的引线提供这种刺激。在一些实施例中,电极位于患者的迷走神经上。在一些实施例中,电极位于迷走神经的一部分附近,以从靠近迷走神经的血管输送刺激。在一些实施例中,电极位于患者100的身体外部在患者100的与迷走神经连通的周围神经上,刺激能量通过患者100的皮肤输送到例如耳朵附近。迷走神经刺激器10可适合于在通过治疗性双向迷走神经刺激来管理慢性心功能不全时使用。根据示例性实施例,迷走神经刺激器10在几种作用机制下操作。这些机制可包括增加副交感神经流出和通过凭借刺激阻断去甲肾上腺素释放来抑制交感神经效应。更重要的是,由迷走神经刺激器10提供的刺激可触发乙酰胆碱(ach)释放到突触间隙中,这可具有有益的抗心律失常、抗凋亡和减少异位的抗炎作用。如可以在下面描述的实施例中认识到的,应该理解,将迷走神经刺激器10呈现为内部迷走神经刺激器的实施例可以被修改以用向电极输送刺激能量的外部迷走神经刺激器代替向电极输送刺激能量的内部迷走神经刺激器,反之亦然。
如图3a-3b所示,迷走神经刺激器10可以包括被显示为可植入神经刺激器20的神经刺激器和被显示为引线30的治疗引线。如图3c所示,迷走神经刺激器10可以包括被显示为外部神经刺激器80的神经刺激器。根据示例性实施例,可植入神经刺激器20和/或外部神经刺激器80被配置成产生电信号,引线30将该电信号输送到期望的位置(例如迷走神经等)。如图1所示,可植入神经刺激器20包括被显示为气密密封壳体22的壳体。根据示例性实施例,气密密封壳体22由生物相容的、植入安全的材料(例如钛等)制成。可植入神经刺激器20包括耦合到气密密封壳体22的连接器盖,其被示为头部24。头部24被分成若干部分以围住被示为插座26的连接接口。
引线30包括被示为引接线32的接线。在一个实施例中,引接线32包括硅酮绝缘合金导体材料。引线30包括位于引接线32的近端的连接器,其被示为引线连接器34。如图1所示,引线连接器34从绝缘电引线主体过渡到被示为连接器插脚36(例如金属连接器插脚等)的连接接口。在一个实施例中,引线连接器34使用硅酮制造,并且连接器插脚36由不锈钢制造,尽管也可以使用其他合适的材料。根据示例性实施例,连接器插脚36被配置为由可植入神经刺激器20的插座26接纳,以将引线30耦合到其上。在植入期间,连接器插脚36被引导穿过插座26进入头部24内,并使用被示为定位螺钉28的紧固件牢固地固定在适当位置中,从而将引线30电耦合到可植入神经刺激器20。在一个实施例中,头部24包围插座26,引线30的单个连接器插脚36可以接纳在插座26中。在其他实施例中,也可以提供两个或更多个插座26,以将附加引线30耦合到可植入神经刺激器20。
如图1-3c所示,引线30包括被显示为电极38的模拟元件。如图1和3a-3c所示,电极38位于引接线32的远端上。根据图1和3a所示的示例性实施例,电极38包括卡肤型(cuff-type)电极40。在其他实施例中,电极38包括另一种类型的电极(例如,猪尾或螺旋电极等)。在一些实施例中,使用另一种类型的引线(例如支架、猪尾引线、预制引线等)。根据图3b所示的示例性实施例,电极38包括血管内电极42。根据图3c所示的示例性实施例,电极38可以包括卡肤型电极40、血管内电极42和/或外部电极44。根据示例性实施例,电极38被配置成将电信号从可植入神经刺激器20和/或外部神经刺激器80输送到期望的位置(例如迷走神经等)。
如图1-2所示,可植入神经刺激器20包括(例如,被包含在气密密封壳体22内等)被显示为控制电路50的电子电路、被显示为电源70的能量存储设备、被显示为通信接口72的通信接口以及被显示为电脉冲发生器74的脉冲发生器。电源70被配置为给可植入神经刺激器20(例如控制电路50、电脉冲发生器74、通信接口72等)供电。在一些实施例中,电源70包括锂碳单氟化物电池。在其他实施例中,电源70包括另一种类型的电池(例如锂离子电池、镍-金属氢化物电池等)。根据示例性实施例,通信接口72被配置为使用外部编程器、简单的患者磁体和/或电磁控制器来提供对可植入神经刺激器20的操作的远程访问。在一个实施例中,通信接口72包括簧片电路。在一些实施例中,通信接口72包括使用无线通信协议(例如射频信号、蓝牙等)与外部编程器远程通信的收发器以接收编程指令和/或向外部编程器或其他外部设备发送遥测信息。在一些实施例中,诸如集成心率传感器和/或加速度计的其他部件可以集成在可植入神经刺激器20内。
根据示例性实施例,控制电路50被配置成控制电脉冲发生器74以产生将由引线30(例如电极38等)输送的电脉冲以向期望的位置(例如迷走神经等)提供刺激。因此,可植入神经刺激器20可在控制电路50的控制下基于可编程(例如由医生、制造商等)的所存储的刺激参数来输送evns和/或vns。每个刺激参数可以独立地被编程,以定义治疗刺激和抑制的周期的特征,以确保对患者的最佳刺激。可编程刺激参数可以包括输出电流、信号频率、脉冲宽度、信号接通时间、信号断开时间、磁体激活(例如,对于由“磁体模式”特别触发的evns和/或vns等)和/或重置参数。刺激参数可以是同步的、异步的和/或脉冲的。其他可编程参数也是可能的。此外,重新选择的刺激参数的集合或“配置文件”可以利用外部编程器被提供给医生,并在被编程到可植入神经刺激器20中之前被针对患者的生理需求进行细调。
可植入神经刺激器20可以在植入前和在整个治疗期中用医疗保健提供者可操作的外部编程器和编程棒被询问,用于检查正确的操作、下载所记录的数据、诊断问题和对操作参数编程。在一些实施例中,外部编程器的使用限于医疗保健提供者,而更有限的手动控制通过“磁体模式”被提供给患者。在一个实施例中,外部编程器执行特别设计成询问可植入神经刺激器20的应用软件。编程计算机可以通过标准化或专有的有线或无线数据连接与编程棒通过接口连接。外部编程器、编程棒和/或应用软件的其他配置和组合是可能的。
如图2所示,迷走神经刺激器10的控制电路50包括处理电路52。处理电路52包括处理器54和存储器56。处理器54可以被实现为通用处理器、微处理器、专用集成电路(asic)、一个或更多个现场可编程门阵列(fpga)、数字信号处理器(dsp)、一组处理部件或其他合适的电子处理部件。存储器56(例如ram、rom、闪存、硬盘存储器等)可以存储用于便于这里描述的各种过程的数据和/或计算机代码。因此,存储器56可通信地连接到处理器54,并向处理器54提供用于执行在这里关于迷走神经刺激器10描述的过程的计算机代码或指令。存储器56可以是或包括有形的非临时易失性存储器或非易失性存储器。在一些实施例中,存储器56可包括数据库部件、对象代码部件、脚本部件或用于支持在本文所述的各种活动和信息结构的任何其他类型的信息结构。
存储器56可以包括用于完成这里描述的过程的各种模块。更特别地,存储器56包括被配置为控制迷走神经刺激器10的操作以经由vns和/或evns提供art的模块。存储器56可以存储控制程序,该控制程序根据所存储的刺激参数和定时周期(例如预定义的刺激协议等)来操作迷走神经刺激器10。例如,存储器56可以包括调节系统功率的电压模块、控制总脉冲发生器功能的刺激模块、接收和实现来自外部编程器或其他外部源的编程命令的输入模块、和/或收集和存储遥测信息的数据模块以及执行附加或可选的功能的其他可能的模块。虽然可以使用具有特定功能的各种模块,但是应当理解,存储器56可以包括用于完成这里描述的功能的任何数量的模块。例如,多个模块的活动可以组合为单个模块,并且具有附加功能的附加模块可以被包括。此外,应当理解,迷走神经刺激器10的处理电路52可以进一步控制超出本公开的范围的其他过程。
根据图3a-3b所示的示例性实施例,可植入神经刺激器20被植入患者100的右胸或左胸区域内。通常,可植入神经刺激器20被植入患者身体的与待刺激的迷走神经120(例如右或左迷走神经120等)相同的一侧(同侧)上。尽管包括对侧和双侧在内的其他神经刺激器-迷走神经配置是可能的。如图3a所示,卡肤型电极40被植入迷走神经120的主干122上大约在锁骨140a-b和乳突之间的一半处(例如,在颈部水平等处)。可以通过首先通过在患者100的颈部102的同侧上的侧颈切口暴露颈动脉鞘和所选择的迷走神经120来植入引线30和卡肤型电极40。然后将卡肤型电极40放置在暴露的神经鞘上并被栓系住。在可植入神经刺激器20的相应植入部位和卡肤型电极40之间形成皮下隧道,引线30通过该隧道被引导到可植入神经刺激器20并牢固连接。这种植入需要在全身麻醉下的侵入性外科手术来定位可植入神经刺激器20,以将刺激直接输送到迷走神经120并向患者提供vns治疗。
一旦迷走神经刺激器10的植入完成,可植入神经刺激器20就可以利用卡肤型电极40直接向迷走神经120的主干122提供vns。刺激在双向地传播的下伏神经中产生动作电位。交感和副交感神经纤维都通过迷走神经刺激器10的卡肤型电极40被刺激。颈部迷走神经120的刺激导致动作电位在传入和传出方向上从刺激的部位传播,以恢复自主平衡。传入动作电位向在疑核、孤束核和运动背核中的髓质中的副交感神经系统的起源以及向在脊髓的中间外侧细胞柱中的交感神经系统的起源传播。传出动作电位向心脏110传播以激活心脏的固有神经系统的成分。左或右迷走神经120可以由迷走神经刺激器10刺激,尽管在相同的参数水平处,右迷走神经120的刺激比左迷走神经120的刺激对心率有适度更强的影响(例如,在更强约20%的数量级)。
在颈部水平处,迷走神经120包含传入纤维,但还有传出纤维,其通过喉返神经支配大多数胸内和腹部器官以及喉区域,喉返神经与在颈部102中的迷走神经120包括在一起。刺激颈部区域中的迷走神经120可能导致与大的神经支配区域相关的不利影响,包括咳嗽、声音改变和嘶哑、疼痛、呼吸困难、恶心等。在心力衰竭中,刺激的预期影响可能主要是传出的(即指向心脏110)。因此,刺激部位可能离心脏110越近,期望的影响就越大,同时避免不利影响。然而,在胸部水平处的迷走神经120的直接接近也需要类似于在颈部水平处的侵入性手术。
现在参考图3b和4a-4b,在颈部水平处,每个迷走神经120(右和左)主要被组织在单个主干122周围,主干122具有布置在其中的主束124。然而,主干122分成支配器官的几个分支。在胸部水平处,被显示为心脏束126的一些分支或束离开主干122以将心脏组织作为目标。心脏束126的刺激不能通过传统的卡肤型电极来实现。然而,迷走神经120在胸部水平中沿着各种血管结构(例如,包括奇静脉等)行进。因此,可以通过血管壁来尝试刺激。在解剖学上,心脏束126与静脉系统的各种血管结构——包括奇静脉、上腔静脉和肺动脉的交叉——处于密切关系中。
作为例子,引线30(例如纵向引线、支架、预制引线、猪尾引线等)可以在血管内位于静脉系统内以提供evns。实际上,心脏束126由几个束组成,不是在所有人中都是相同的。因此,这样的血管内引线30可以具有沿着引接线32定位的一个或更多个电极,以通过静脉系统(例如通过上腔静脉、肺动脉、奇静脉等的壁)经血管向迷走神经120的心脏束126提供vns(即血管内迷走神经刺激(evns))。血管内或经静脉刺激可用于刺激一些神经,包括迷走神经120(例如,主干122、心脏束126等)。evns可以提供优于vns的各种优点(例如,与用卡肤型电极直接接近迷走神经120相比,等等),包括但不限于没有侵入性手术和没有对喉返神经的不希望有的刺激。血管内引线30的放置可以通过静脉的导管插入术(例如通过易于接近的静脉,与在起搏器程序中的类似、在荧光检查下等)来实现。
如图3b和4b所示,引线30的引接线32在血管内位于被示为静脉130(例如奇静脉等)的脉管结构(其被示为静脉腔134)的内部。作为例子,奇静脉可以容易从心脏110的腔静脉进入,这允许心脏束126的电刺激。引线30可以包括具有沿着引接线32(例如在其端部处等)的长度定位的一个或更多个电极38的血管内电极42,并且可以与静脉130的壁(其被显示为静脉壁132)接触。根据示例性实施例,多个电极38便于用引线30增加对小的和非均匀分散的心脏束126的刺激(例如,因为心脏束126的位置和数量从一个患者到另一患者改变,等等)。因此,位于静脉腔134内的图4b的引线30可以便于通过静脉130的静脉壁132经血管刺激心脏束126,从而向患者的迷走神经120提供evns。
现在参考图3c,外部神经刺激器80被配置成位于患者100的身体外部。在一个实施例中,外部神经刺激器80是配置成执行各种评估程序(例如,用于测试患者对接受可植入神经刺激器20的适宜性等)的静止设备。在其他实施例中,外部神经刺激器80被配置为可佩戴的或能够与患者100一起携带的便携式设备。如图3c所示,外部神经刺激器80包括用户接口82、控制电路50、电脉冲发生器74和引线接口84。用户接口82可以使外部神经刺激器80的用户能够与迷走神经刺激器10及其其他部件(例如电脉冲发生器74、控制电路50等)通信。用户接口82可以包括输入设备和/或显示设备。输入设备可以被配置成允许用户控制迷走神经刺激器10。输入设备可以包括但不限于键盘、鼠标、触摸屏设备、一个或更多个按钮和开关、语音命令接收器、所连接的便携式设备(例如智能电话、平板电脑、膝上型电脑等)等。显示设备可以被配置为向迷走神经刺激器的用户提供图形用户界面(gui)。显示设备可以包括但不限于触摸屏显示器、投影仪和投影屏幕、监视器或电视机(例如lcd、led、等离子体、dlp等)、增强现实眼镜、便携式设备(例如智能手机、平板电脑、笔记本电脑等)和/或可以提供gui的任何其他已知的显示设备。引线接口84可被配置成便于将一个或更多个引线30耦合到外部神经刺激器80(例如,类似于可植入神经刺激器20的插座26等)。
尽管在图3c中未示出,但是可以理解,外部神经刺激器80可以包括与可植入神经刺激器20一起使用的部件的全部或部分(例如,电源70、通信接口72等)。因为外部神经刺激器80可以被配置成在患者100的身体外部放置和使用,外部神经刺激器80的部件可以不需要气密密封壳体22,并且可以被合并到另一个外部医疗设备例如外部患者监测或外部治疗输送设备中,或者可以被配置成具有在外部神经刺激器80和接触人体的部件之间的可脱离的耦合。
如图3c所示,外部神经刺激器80可以耦合到一个或更多个引线30。一个或更多个引线30可以包括定位成向迷走神经120提供迷走神经刺激的各种电极38。在一些实施例中,引线30包括定位在迷走神经120上的卡肤型电极40,使得外部神经刺激器80可以直接向迷走神经120的主干122提供vns治疗。在一些实施例中,引线30包括位于静脉130内的血管内电极42,使得外部神经刺激器80可以通过静脉130(例如奇静脉等)经血管向迷走神经120提供vns治疗。在一些实施例中,引线30包括位于患者100的身体外部在患者100的周围神经上的外部电极44,周围神经与迷走神经120连通,刺激能量通过患者100的在例如耳朵附近的皮肤被输送(例如耳廓vns刺激等)。
在一个实施例中,可植入神经刺激器20和/或外部神经刺激器80包括具有传感器的一个或更多个心脏引线,所述传感器被配置成便于监测心脏110的活动(例如,心率、血压、心率变异性、射血分数、静息心率、夜间心率、舒张充盈时间等)。可以在图3a-3c所示和关于图3a-3c描述的任何前面提到的实施例中使用这种心脏引线。一个或更多个心脏引线可以位于心脏110内和/或附近(例如,植入的心脏引线)和/或在患者100的身体外部(例如,在靠近心脏110的患者的胸部上)。在一些实施例中,可植入神经刺激器20另外或可选地包括加速度计和/或被配置成收集心脏活动数据和/或患者活动数据(例如,关于患者100的活动,包括移动、行走、跑步、睡觉、休息等)的其他传感器(例如,定位在气密密封壳体22内)。迷走神经刺激器10的控制电路50可以接收和处理来自一个或更多个心脏引线和/或其他设备(例如加速度计)的信息(例如,心脏活动数据、身体活动数据等)。在一些实施例中,控制电路50被配置为使由引线30的电极38提供的迷走神经刺激与心脏110的心脏脉冲同步和/或基于心脏活动数据(例如,从一个或更多个心脏引线、加速度计等接收的)和/或患者活动数据(例如,从加速度计和/或其他设备接收的)控制迷走神经刺激。在一些实施例中,控制电路50被配置为存储心脏活动数据和/或身体活动数据用于将来使用(例如,以由医生下载、随时间的过去而跟踪心脏活动、构建直方图等)。
在另一个实施例中,迷走神经刺激器10包括(i)可植入神经刺激器20和(ii)外部神经刺激器80中的一个,并且可以与被配置成监测心脏110的活动的心脏监测设备结合来使用。心脏监测设备可以是可植入设备(例如,类似于可植入神经刺激器20)或外部设备(例如,类似于外部神经刺激器80)。心脏监测设备可以包括一个或更多个心脏引线、外部传感器、加速度计和/或被配置为监测心脏110的心脏活动(例如,获取心脏活动数据)和/或患者的身体活动(例如,获取身体活动数据)的又一设备。心脏监测设备可以包括独立的控制电路(例如,类似于迷走神经刺激器10的控制电路50),其被配置为存储心脏活动数据和/或身体活动数据用于将来使用(例如,以由医生下载、随时间的过去而跟踪心脏活动、构建直方图等)。在一些实施例中,心脏监测设备被配置成与迷走神经刺激器10通信(例如,经由有线通信协议、无线通信协议等),使得迷走神经刺激器10可以至少部分地基于心脏活动数据和/或身体活动数据来控制迷走神经刺激(例如,使由引线30的电极38提供的迷走神经刺激与由心脏监测设备监测的心脏110的心脏脉冲同步)。
然而,如上所述,通过迷走神经刺激的自主调节疗法(art)可能不适合于一些患者。因此,在植入迷走神经刺激器10的可植入神经刺激器20之前或者在植入外部神经刺激器80的引线30之前,可以针对各种特征和/或反应参数评估患者,以确定患者是否是通过vns和/或evns接受art的良好候选者(例如,基于纳入和/或排除标准等)。适当的患者选择可以增加art的成功以及vns和/或evns治疗的功效。
作为例子,确定哪些患者可能对vns和/或evns很好地做出反应以及哪些患者可能不能很好地做出反应可以基于使用非侵入性技术确定的患者的一个或更多个生理特征(例如,与纳入/排除标准等相比)。作为另一个例子,确定哪些患者可能对vns和/或evns很好地做出反应以及哪些患者可能不能很好地做出反应可以基于在刺激测试期间(例如,使用evns、外部vns方法,包括耳廓vns、直接vns等)的患者的生理反应(例如,与纳入/排除标准等相比)。在一些实施例中,确定哪些患者可以对vns和/或evns很好地做出反应基于一个或更多个生理特征和在刺激试验期间的患者的生理反应的组合。
因此,现在参考图5,vns分析系统200可用于便于评估患者对接受迷走神经刺激治疗的适宜性(例如,确定哪些患者可能对evns和/或vns积极地做出反应,以及哪些患者可能对evns和/或vns消极地做出反应;预测在手术植入前由迷走神经刺激器10提供的evns和/或vns的潜在功效;等等)。如图5所示,vns分析系统200包括用户输入/输出(i/o)设备210、刺激设备220、一个或更多个传感器230和处理电路252。
用户i/o设备210可以使vns分析系统200的用户能够与vns分析系统200及其其他部件(例如刺激设备220等)通信。在一些实施例中,用户i/o设备210经由无线通信协议(例如蓝牙、zigbee、wi-fi、无线电、蜂窝等)可通信地耦合到vns分析系统200。在一些实施例中,用户i/o设备210直接可通信地耦合到vns分析系统200(例如,通过有线连接等)。用户i/o设备210可以包括输入设备和/或显示设备。输入设备可以被配置成允许用户控制vns分析系统200和/或输入各种参数(例如,患者的特征、标准等)。输入设备可以包括但不限于键盘、鼠标、触摸屏设备、一个或更多个按钮和开关、语音命令接收器、便携式设备(例如智能电话、平板电脑、膝上型电脑等)等。显示设备可以被配置为向vns分析系统200的用户提供图形用户界面(gui)。显示设备可以包括但不限于触摸屏显示器、投影仪和投影屏幕、监视器或电视机(例如,lcd、led、等离子体、dlp等)、增强现实眼镜、便携式设备(例如智能手机、平板电脑、笔记本电脑等)和/或可以提供gui的任何其他已知的显示设备。
刺激设备220可以被配置为在用于评估患者对迷走神经刺激治疗的反应的预筛选评估期间提供刺激(例如,急性、暂时性等)。在一个实施例中,刺激设备220包括具有至少一个电极(例如电极38等)的引线(例如引线30等),电极配置成在血管内位于靠近迷走神经120的一部分(例如,从迷走神经20分支的心脏束126等)的静脉130(例如奇静脉等)的静脉腔134内。因此,刺激设备220可以通过静脉130的静脉壁132经血管向迷走神经120(例如,间接地、evns等)提供刺激。在另一个实施例中,刺激设备220包括外部刺激设备,该外部刺激设备被配置成位于患者的身体外部以通过患者的皮肤提供刺激。在一个实施例中,外部刺激设备包括耳廓刺激设备,该耳廓刺激设备被配置为在患者的耳朵周围和/或附近提供耳廓刺激。在其他实施例中,外部刺激设备包括被配置为向患者的另一外部区域(例如,胸部、背部、颈部等)提供刺激的另一类型的刺激设备。在还有其他实施例中,刺激设备220包括卡肤型电极(例如卡肤型电极40等)或临时植入到迷走神经120上并被配置成直接向迷走神经120(例如,vns等)提供刺激的另一类型的电极。作为例子,这种侵入性vns测试方法可以在患者已经经历手术过程时使用,该手术过程允许这种侵入性测试出现,而不需要额外或最低限度的手术操纵来接近迷走神经(例如,执行手术过程的原因不是被执行来便于vns测试,vns测试是被包括在另一个过程中的额外步骤,等等)。
传感器230可以被配置为获取正在经历植入前测试和评估的患者的反应数据,以便于监测患者对迷走神经刺激治疗的生理反应。反应数据可以包括指示患者对由刺激设备220提供给迷走神经120的刺激的生理反应的数据。传感器230可以便于监测患者的一个或更多个生理反应,包括心率变化、心率变异性、呼吸模式、诱发的疼痛和/或血压变化,以及由刺激引起的其他可能的反应。传感器230还可以被配置成监测电极38的刺激水平(例如,电流、电压、功率、信号频率、脉冲宽度、信号接通时间、信号断开时间、同步刺激、异步刺激、脉冲刺激等)。传感器230可以此外或可选地被配置成在刺激之前获取指示患者的一个或更多个生理特征的患者数据。由传感器230获取的一个或更多个生理特征可以包括静息心率、夜间心率、心率变异性(hrv)、炎症水平、左心室射血分数(ef)、脑利钠肽(bnp)水平、心力衰竭病因(即缺血性与非缺血性)、和/或自主神经功能障碍的存在以及其他可能的可测量的生理特征。
如图5所示,处理电路252包括处理器254和存储器256。处理器254可以被实现为通用处理器、专用集成电路(asic)、一个或更多个现场可编程门阵列(fpga)、数字信号处理器(dsp)、一组处理部件或其他合适的电子处理部件。存储器256(例如,ram、rom、闪存、硬盘存储器等)可以存储用于便于这里描述的各种过程的数据和/或计算机代码。因此,存储器256可以可通信地连接到处理器254并向处理器254提供用于执行在这里关于vns分析系统200描述的过程的计算机代码或指令。此外,存储器256可以是或包括有形的、非临时易失性存储器或非易失性存储器。在一些实施方式中,存储器256可包括数据库部件、对象代码部件、脚本部件或用于支持本文所述的各种活动和信息结构的任何其他类型的信息结构。
存储器256可以包括用于完成这里描述的过程的各种模块。更特别地,存储器256包括被配置成在迷走神经刺激器10的植入之前控制vns分析系统200的操作以评估患者对接受迷走神经刺激治疗的适宜性的模块。虽然可以使用具有特定功能的各种模块,但是应当理解,存储器256可以包括用于完成这里描述的功能的任何数量的模块。例如,多个模块的活动可以组合为单个模块,并且具有附加功能的附加模块可以被包括。在一些实施例中,存储器256的模块被集成和/或组合。此外将理解,vns分析设备的处理电路252可以进一步控制超出本公开范围的其他过程。
如图5所示,vns分析系统200包括特征模块258、刺激模块260、刺激分析模块262和功效模块264。特征模块258可以被配置为接收和存储指示正针对迷走神经刺激治疗的适宜性而被评估的患者的各种生理特征的患者数据。生理特征可以包括年龄、hrv、炎症、左心室ef、bnp水平、心力衰竭病因、静息心率、夜间心率、年龄、自主神经功能障碍的存在和/或心脏再同步治疗(crt)的存在以及患者的其他可能的生理特征(例如血压、体重、身高、性别等)的指示。在一些实施例中,特征模块258经由用户i/o设备210从vns分析系统200的操作者手动地输入和接收生理特征的至少一部分(例如,年龄、crt的存在、自主神经功能障碍的存在、静息心率等)。在一些实施例中,特征模块258从传感器230接收生理特征的至少一部分(例如,静息心率、夜间心率、左心室ef、hrv、自主神经功能障碍的存在等)。在一些实施例中,特征模块258从远程服务器或设备接收(例如从远程服务器或设备下载等)生理特征的至少一部分。如图5所示,特性模块258可通信地耦合到功效模块264。因此,特征模块258可以向功效模块264提供生理特征以执行进一步的分析。
功效模块264可以被配置为接收和存储关于患者对接受迷走神经刺激治疗的适宜性的一个或更多个标准(例如,筛选参数等)。一个或更多个标准可以在功效模块264内被预先定义和/或由vns分析系统200的操作者手动地输入。一个或更多个标准可以包括年龄范围或阈值、静息心率阈值、夜间心率阈值、缺血性心力衰竭与非缺血性心力衰竭、现有心脏再同步治疗、bnp阈值、左心室ef阈值或范围、hrv阈值、自主神经功能障碍和/或炎症阈值。功效模块264由此可以被配置为从特征模块258接收相应患者的生理特征,以基于一个或更多个标准和针对迷走神经刺激治疗而被评估的患者的一个或更多个生理特征来确定患者对接受迷走神经刺激治疗的适宜性。在一些实施例中,可以基于患者的各种特征——包括年龄、性别、身高、体重、血压和/或胆固醇水平(例如,标准可以是动态的,而不是静态的)——来设置或选择一个或更多个标准。
在一些实施例中,功效模块264被配置为将患者的年龄与年龄阈值和/或年龄范围进行比较。作为例子,年龄可能影响神经上的信号传导和/或脑可塑性,这可能降低迷走神经刺激治疗的功效。根据示例性实施例,功效模块264被配置为响应于患者的年龄小于最大年龄阈值而确定患者更适合于迷走神经刺激治疗。在一个实施例中,最大年龄阈值是90岁。在其他实施例中,最大年龄阈值是80岁。在还有其他实施例中,最大年龄阈值小于80岁(例如,75岁、65岁等)。根据另一示例性实施例,功效模块264被配置为响应于患者的年龄大于最小年龄阈值而确定患者更适合于迷走神经刺激治疗。在一个实施例中,最小年龄阈值是18岁。在其他实施例中,最小年龄阈值是30岁。在还有其他实施例中,最小年龄阈值大于30岁(例如,35岁、45岁等)。根据又一示例性实施例,功效模块264被配置为响应于患者的年龄在年龄范围内(例如,年龄范围的最小年龄可以是18、25、30、40等;年龄范围的最大年龄可以是65、70、75、80、85、90等)而确定患者更适合于迷走神经刺激治疗。功效模块264还可以被配置为向满足最小年龄阈值、最大年龄阈值和/或年龄范围的患者分配第一值或第一分类,并且向不满足最小年龄阈值、最大年龄阈值和/或年龄范围的患者分配第二值或第二分类。第一值或第一分类可以包括比第二值或第二分类更大的权重(例如,用于在确定复合加权分数时与其他特征的组合一起使用)。可选地,功效模块264可以基于患者的年龄相对于最小年龄阈值、最大年龄阈值和/或年龄范围从值的范围中分配值(例如,离最大年龄阈值越远则是较高的值,离最大年龄阈值较近则是较低的值,等等)。
在一些实施例中,功效模块264被配置为将患者的静息心率与静息心率阈值进行比较。作为例子,具有高静息心率(例如,尽管有omt)的患者可能处于高交感神经驱动下,并且可能对基于增强拮抗机制的迷走神经刺激治疗更敏感(例如,更适合于接受)。根据示例性实施例,功效模块264被配置为响应于患者的静息心率大于静息心率阈值而确定患者更适合于迷走神经刺激治疗。在一个实施例中,静息心率阈值约为每分钟七十次跳动。在其他实施例中,静息心率阈值大于或小于每分钟七十次跳动(例如,55、60、65、75、85等)。在可选的实施例中,功效模块264被配置为将患者的静息心率与静息心率范围(例如,55、60、65、70等的最小静息心率;60、65、70、75、80、85等的最大静息心率为)进行比较。功效模块264还可以被配置为将第一值或第一分类分配给满足静息心率阈值和/或静息心率范围的患者,并将第二值或第二分类分配给不满足静息心率阈值和/或静息心率范围的患者。第一值或第一分类可以包括比第二值或第二分类更大的权重(例如,用于在确定复合加权分数时与其他特征的组合一起使用)。可选地,功效模块264可以基于患者的静息心率相对于静息心率阈值和/或静息心率范围从一定范围的值中分配一个值。
在一些实施例中,功效模块264被配置成比较患者的夜间心率(例如睡眠心率等)与夜间心率阈值。作为例子,具有高夜间心率和心率不降的患者可能与心血管疾病和全因死亡率的增加的风险相关。根据示例性实施例,功效模块264被配置为响应于患者的夜间心率大于夜间心率阈值而确定患者更适合于迷走神经刺激治疗。在一个实施例中,夜间心率阈值约为每分钟五十五次跳动。在其他实施例中,静息心率阈值大于或小于每分钟五十五次跳动(例如,45、50、60、65、70、75等)。在可选的实施例中,功效模块264被配置为将患者的静息心率与静息心率范围(例如,45、50、55等的最小静息心率;50、55、60、65、70、75等的最大静息心率)进行比较。功效模块264还可以被配置为向满足夜间心率阈值和/或夜间心率范围的患者分配第一值或第一分类,并且向不满足夜间心率阈值和/或夜间心率范围的患者分配第二值或第二分类。第一值或第一分类可以包括比第二值或第二分类更大的权重(例如,用于在确定复合加权分数时与其他特征的组合一起使用)。可选地,功效模块264可以根据患者的夜间心率相对于夜间心率阈值和/或夜间心率范围从一定范围的值中分配一个值。
在一些实施例中,功效模块264被配置为确定患者的心力衰竭病因,包括缺血性心力衰竭或非缺血性心力衰竭的指示。作为例子,有非缺血性心力衰竭的患者可能不如有缺血性心力衰竭的患者对art很好地做出反应。因此,第一患者可能响应于第一患者患有非缺血性心力衰竭而不太适合于迷走神经刺激治疗,而第二患者可能响应于第二患者患有缺血性心力衰竭而更适合于迷走神经刺激治疗。
根据示例性实施例,功效模块264被配置为响应于患者的下列情况中的至少一个而确定患者更适合于迷走神经刺激治疗:(i)患有缺血性心力衰竭和(ii)不患有非缺血性心力衰竭。功效模块264还可以被配置为将第一值或第一分类分配给没有非缺血性心力衰竭(例如,有缺血性心力衰竭,两者都没有)的患者,并且将第二值或第二分类分配给确实有非缺血性心力衰竭的患者。第一值或第一分类可以包括比第二值或第二分类更大的权重(例如,用于在确定复合加权分数时与其他特征的组合一起使用)。
在一些实施例中,功效模块264被配置为确定患者是否正在经历现有crt。作为例子,具有现有crt的患者可能不如没有crt的患者对art很好地做出反应。因此,响应于第一患者具有现有crt,第一患者可能不太适合于迷走神经刺激治疗,而响应于第二患者没有crt,第二患者可能更适合于迷走神经刺激治疗。根据示例性实施例,功效模块264被配置为响应于患者没有现有crt而确定患者更适合于迷走神经刺激治疗。功效模块264还可以被配置为向没有现有crt的患者分配第一值或第一分类,并且向具有现有crt的患者分配第二值或第二分类。第一值或第一分类可以包括比第二值或第二分类更大的权重(例如,用于在确定复合加权分数时与其他特征的组合一起使用)。
在一些实施例中,功效模块264被配置为将bnp水平和/或前激素bnp(nt-probnp)的n端与bnp阈值进行比较。作为例子,如由高bnp水平所示的,有更糟的心力衰竭的患者可能对art更好地做出反应。例如,低于100pg/ml的bnp水平可以指示没有心力衰竭,在100-300pg/ml之间的bnp水平可以指示心力衰竭存在,高于300pg/ml的bnp水平可以指示轻度心力衰竭,高于600pg/ml的bnp水平可以指示中度心力衰竭,以及高于900pg/ml的bnp水平可以指示严重心力衰竭。根据示例性实施例,功效模块264被配置为响应于患者的bnp水平大于bnp阈值而确定患者更适合于迷走神经刺激治疗。在一个实施例中,bnp阈值约为100pg/ml。在其他实施例中,bnp阈值大于或小于100pg/ml(例如,90pg/ml、150pg/ml、300pg/ml等)。功效模块264还可以被配置为将第一值或第一分类分配给满足bnp阈值的患者,并将第二值或第二分类分配给不满足bnp阈值的患者。第一值或第一分类可以包括比第二值或第二分类更大的权重(例如,用于在确定复合加权分数时与其他特征的组合一起使用)。可选地,功效模块264可以基于患者的bnp水平相对于bnp阈值从一定范围的值分配一个值(例如,bnp水平更接近bnp阈值,则是较低值,bnp值更远离bnp阈值,则是较高值等等)。
在一些实施例中,功效模块264被配置为将患者的左心室ef与ef阈值和/或ef范围进行比较。作为例子,低的左心室ef可以指示患者可能患有心力衰竭,并且可能对art更好地做出反应。然而,太低的左心室ef可以指示心脏病可能过于严重,且对art的反应可能是很小的。根据示例性实施例,功效模块264被配置为响应于患者的左心室ef小于最大ef阈值而确定患者更适合于迷走神经刺激治疗。在一个实施例中,最大ef阈值是55%。在其他实施例中,最大ef阈值是40%。在还有其他实施例中,最大ef阈值小于40%(例如,35%、30%等)。
根据另一示例性实施例,功效模块264被配置为响应于患者的左心室ef大于最小ef阈值而确定患者更适合于迷走神经刺激治疗。在一个实施例中,最小ef阈值是15%。在其他实施例中,最小ef阈值是20%。在还有其他实施例中,最小ef阈值大于20%(例如,25%、30%等)。根据又一示例性实施例,功效模块264被配置成响应于患者的左心室ef在ef范围内(例如,ef范围的最小ef可以是15%、20%、25%等;ef范围的最大ef可以是30%、35%、40%、55%等)而确定患者更适合于迷走神经刺激治疗。功效模块264还可以被配置为向满足最大ef阈值、最小ef阈值和/或ef范围的患者分配第一值或第一分类,并且向不满足最大ef阈值、最小ef阈值和/或ef范围的患者分配第二值或第二分类。第一值或第一分类可以包括比第二值或第二分类更大的权重(例如,用于在确定复合加权分数时与其他特征的组合一起使用)。可选地,功效模块264可以根据患者的左心室ef相对于最小ef阈值、最大ef阈值和/或ef范围从一定范围的值分配一个值(例如,左心室ef更接近最大ef阈值,则是较高值,左心室ef更接近最小ef阈值,则是较低值,等等)。
在一些实施例中,功效模块264被配置为将患者的hrv与hrv阈值进行比较。作为例子,具有较低hrv的患者可能对art更好地做出反应,这增加了在心力衰竭患者中的hrv。可以使用各种时域测量(例如,avn、sdn、sdan、sdnidx、rmssd、pn50等)和/或频域测量(例如,vlf、lf、hf、lf/hf等)来测量hrv。根据示例性实施例,功效模块264被配置为响应于患者的hrv小于hrv阈值而确定患者更适合于迷走神经刺激治疗。功效模块264还可以被配置为将第一值或第一分类分配给满足hrv阈值的患者,并将第二值或第二分类分配给不满足hrv阈值的患者。第一值或第一分类可以包括比第二值或第二分类更大的权重(例如,用于在确定复合加权分数时与其他特征的组合一起使用)。可选地,功效模块264可以基于患者的hrv相对于hrv阈值从一定范围的值中分配一个值(例如,hrv更接近hrv阈值,则是较高值,hrv更远离hrv阈值,则是较低值,等等)。
在一些实施例中,功效模块264被配置成确定患者是否有自主神经功能障碍。可以使用压力反射敏感性(brs)、肌肉交感神经活性(msna)和/或血液生物标志物(例如去甲肾上腺素、乙酰胆碱等)来测量自主神经功能障碍。作为例子,有自主神经功能障碍的患者可能对art更好地做出反应,这可以恢复自主神经平衡。因此,响应于第一患者具有自主神经功能障碍,第一患者可能更适合于迷走神经刺激治疗,而响应于第二患者没有自主神经功能障碍,第二患者可能更不适合于迷走神经刺激治疗。根据示例性实施例,功效模块264被配置为响应于患者具有自主神经功能障碍而确定患者更适合于迷走神经刺激治疗。功效模块264还可以被配置为向确实有自主神经功能障碍的患者分配第一值或第一分类,并且向确实有自主神经功能障碍的患者分配第二值或第二分类。第一值或第一分类可以包括比第二值或第二分类更大的权重(例如,用于在确定复合加权分数时与其他特征的组合一起使用)。
在一些实施例中,功效模块264被配置为将炎症的水平和/或数量的指示与炎症阈值进行比较。可以使用血液生物标志物例如c反应蛋白(crp)、白细胞介素(il)-1、il-6、il-8、单核细胞趋化蛋白-1(mcp-1)、基质金属蛋白酶(mmp)等来测量炎症。作为例子,有较高水平的炎症的患者可能对art更好地做出反应,这具有抗炎作用。根据示例性实施例,功效模块264被配置为响应于患者的炎症水平大于炎症阈值而确定患者更适合于迷走神经刺激治疗。功效模块264还可以被配置为将第一值或第一分类分配给满足炎症阈值的患者,并将第二值或第二分类分配给不满足炎症阈值的患者。第一值或第一分类可以包括比第二值或第二分类更大的权重(例如,用于在确定复合加权分数时与其他特征的组合一起使用)。可选地,功效模块264可以基于患者的炎症水平相对于炎症阈值从一定范围的值中分配一个值(例如,炎症水平更接近炎症阈值则是较低值,炎症水平更远离炎症阈值则是较高值,等等)。
功效模块264还可以被配置为基于患者的一个或更多个生理特征与一个或更多个标准(例如,vns和/或evns的潜在功效)的比较来确定患者对接受迷走神经刺激的适宜性的度量。在一个实施例中,功效模块264被配置为基于患者的一个或更多个生理特征相对于一个或更多个标准(例如,第一值/第一分类、第二值/第二分类和/或来自值范围的值的聚集或其他汇编)来确定患者的复合分数。在一些实施例中,一个或更多个生理特征被加权(例如,使得一些特征比其他特征携带更多的权重,一些特征在评估患者时更重要或更有影响力,等等),使得功效模块264确定患者的加权复合分数。根据示例性实施例,功效模块264被配置为使用多个适宜性度量的加权组合来生成复合分数。每个适宜性度量可以基于相应特征相对于相关标准来生成,其中通过对每个度量应用权重来生成复合分数。在一些实施例中,将权重应用于患者的每个相应生理特征的值(例如,第一值/分类、第二值/分类、来自值范围的值等)以确定加权复合分数。将值应用于特征的这种过程可以允许特征的标准化,以便可以组合每一个特征来确定复合分数。
在一些实施例中,功效模块264被配置为将患者的一个或更多个特征与一个或更多个标准进行比较,并将患者分类为多个患者类别之一的成员。例如,在一些实施例中,可以将与一个或更多个特征相关联的值(例如,加权复合分数)与功效映射(例如,评级系统、评级指南等)例如一个或更多个标准的一个或更多个阈值进行比较,以使用比较的结果来将患者分类为多个患者类别之一。每个患者类别可能与对接受迷走神经刺激治疗的适宜性的不同水平相关联。在一个实施例中,功效映射包括单个阈值。作为例子,满足单个阈值(例如,大于等)的特征值(例如复合分数)可以指示处于第一患者类别中的患者,该第一患者类别包括被认为可能是被植入迷走神经刺激器以提供vns和/或evns的良好候选者(例如适合的)(例如,vns和/或evns可能成功的候选者,或者导致患者状况的改善的候选者),而不满足单个阈值(例如,小于等)的复合分数可以指示处于第二患者类别中的患者,该第二患者类别包括可能是被植入迷走神经刺激器以提供vns和/或evns的差的候选者(例如不适合的)(例如,vns和/或evns不太可能成功的候选者,或者不导致患者状况的实质性改善或导致患者状况的恶化的候选者)。在另一实施例中,功效映射包括两个阈值:第一阈值和小于第一阈值的第二阈值。作为例子,满足第一阈值(例如,大于等)的特征值(例如复合分数)可以指示处于第一类别或是良好候选者(例如合适的)的患者被植入迷走神经刺激器以提供vns和/或evns,满足第二阈值(例如,小于等)的特征值可以指示处于第二类别或是差的候选者(例如,不适合的)的患者被植入迷走神经刺激器以提供vns和/或evns,以及都不满足第一和第二阈值(例如,位于第一和第二阈值之间等)的特征值处于第三类别,其指示vns和/或evns可能或可能不对患者有效(例如,由医生的判断、潜在候选者等决定)。例如,不满足第一阈值但比第二阈值更接近第一阈值的特征值可以指示植入迷走神经刺激器以提供vns和/或evns将是成功的较大可能性。在另一个例子中,不满足第一阈值但比第一阈值更接近第二阈值的特征值可以指示植入迷走神经刺激器以提供vns和/或evns将是成功的较小可能性。在其他实施例中,功效映射包括多个阈值以对应于各种可能的复合分数(例如,指示95%潜在成功的第一阈值、指示80%潜在成功的第二阈值、指示70%潜在成功的第三阈值、指示60%潜在成功的第四阈值、指示50%潜在成功的第五阈值等)。
功效模块264还可以被配置为通过用户i/o设备210来提供患者对接受迷走神经刺激治疗的适宜性的指示。在一个实施例中,该指示包括复合分数和/或加权复合分数。在其他实施例中,该指示包括指示基于加权和/或复合分数的迷走神经刺激治疗对患者的潜在(例如,预测的等)功效的百分比、值和/或其他度量。在其他实施例中,该指示包括关于患者是否应该基于加权和/或复合分数来使迷走神经刺激器(例如迷走神经刺激器10等)被植入的推荐(例如,“通过”、“失败”“批准”、“不提供vns治疗”等)。
根据另一示例性实施例,功效模块264被配置为使用加权和/或复合分数作为是否应该由vns分析系统200的操作者对患者执行刺激测试和分析的前驱确定。在一些实施例中,患者对刺激测试的反应和患者的一个或更多个特征协作地用于确定患者对接受迷走神经刺激治疗的适宜性。在其他实施例中,独立于患者的一个或更多个生理特征而使用患者对刺激测试的反应(例如,可选地,为了验证目的等)。因此,可以基于患者的一个或更多个生理特征、患者对刺激测试的反应或其组合来确定患者对接受迷走神经刺激治疗的适宜性(例如,加权和/或复合分数基于患者的生理特征和/或生理反应)。
回来参考图5,刺激模块260可以被配置成控制刺激设备220(例如,电极38等)的操作以向患者的迷走神经提供刺激。刺激模块260还可以被配置成监测和/或控制由刺激设备220提供的刺激参数和/或水平(例如,电流、电压、功率、信号频率、脉冲宽度、信号接通时间、信号断开时间等)。在一些实施例中,刺激模块260被配置根据预定义的刺激协议来控制刺激设备220。在其他实施例中,刺激模块260被配置成基于由vns分析系统200的操作者提供的手动地输入的控制参数来控制刺激设备220。
刺激分析模块262可以被配置为接收由传感器230获取的反应数据,该反应数据指示患者对迷走神经刺激的生理反应。因此,刺激分析模块262可以被配置为监测患者对刺激的一个或更多个生理反应,包括心率变化、hrv变化、呼吸模式变化、所诱发的疼痛和/或血压变化以及由刺激引起的其他可能的反应。如图5所示,刺激分析模块262可通信地耦合到功效模块264。因此,刺激分析模块262可以向功效模块264提供关于患者的生理反应的信息以执行进一步的分析。
功效模块264可以被配置为接收和存储关于患者对接受迷走神经刺激治疗的适宜性的一个或更多个反应标准(例如,筛选参数等)。一个或更多个反应标准可以在功效模块264内被预先定义和/或由vns分析系统200的操作者手动地输入。一个或更多个反应标准可以包括心率变化阈值或心率变异性阈值以及其他可能性。阈值可以是幅度差和/或百分比差(例如,刺激后值相对于刺激前值的,等等)。功效模块264由此可以被配置为接收关于相应患者对所提供的刺激的生理反应的信息(例如,来自刺激分析模块262等)。功效模块264还可以基于一个或更多个反应标准和针对迷走神经刺激治疗而被评估的患者的一个或更多个生理反应来确定患者对接受迷走神经刺激治疗的适宜性。例如,如果患者的心率变化大于心率变化阈值(例如,响应于刺激等),则患者可能适合于接受迷走神经刺激治疗。
功效模块264还可以被配置为基于一个或更多个反应标准和患者对刺激的生理反应来确定患者对接受迷走神经刺激治疗的适宜性。如上所述,功效模块264可基于(i)一个或更多个特征与一个或更多个标准的比较、(ii)生理反应与一个或更多个反应标准的比较或者(i)和(ii)两者来确定患者对接受迷走神经刺激治疗的适宜性(例如,加权和/或复合分数等)。
现在参考图6,示出了根据示例性实施例的用于评估患者对接受迷走神经刺激治疗的适宜性的方法600。在一个示例实施例中,可以利用图5的vns分析系统200来实现方法600。因此,可以关于图5来描述方法600。
在步骤602,vns分析系统200被配置为接收关于患者对接受迷走神经刺激治疗的适宜性的一个或更多个标准。在一个实施例中,操作者通过输入设备(例如用户i/o设备210等)手动地输入一个或更多个标准。在其他实施例中,在vns分析系统200的存储器(例如存储器256等)内预定义一个或更多个标准。根据示例性实施例,一个或更多个标准包括年龄范围或阈值、静息心率阈值、夜间心率阈值、缺血性心力衰竭与非缺血性心力衰竭、现有心脏再同步治疗、脑利钠肽阈值、左心室射血分数范围或阈值、心率变异性阈值、自主神经功能障碍和/或炎症阈值。
在步骤604,vns分析系统200被配置为接收患者的一个或更多个特征(例如生理特征等)。根据示例性实施例,使用非侵入性方法来确定和/或测量患者的一个或更多个特征。在一些实施例中,患者的一个或更多个特征的至少一部分由操作者通过输入设备手动地输入(例如,一个或更多个特征在评估之前被确定,等等)。在一些实施例中,从一个或更多个传感器或外部设备接收患者的一个或更多个特征的至少一部分(例如,由传感器230获取、从远程服务器或数据库上的患者文件下载等)。根据示例性实施例,一个或更多个特征包括自主神经功能障碍、心率变异性、炎症量、左心室射血分数、脑利钠肽水平、现有心脏再同步治疗、心力衰竭病因(例如,缺血性心力衰竭与非缺血性心力衰竭等)、静息心率、夜间心率和/或患者的年龄的指示。
在步骤606,vns分析系统200被配置为将患者的一个或更多个特征与一个或更多个标准进行比较。在步骤608,vns分析系统200被配置为基于患者的一个或更多个特征与一个或更多个标准的比较来确定患者对接受迷走神经刺激的适宜性。在一个实施例中,vns分析系统200被配置为基于每个特征相对于相应标准来确定患者的复合分数。在一些实施例中,vns分析系统200被配置为基于每个特征相对于相应标准来确定患者的加权复合分数。
在步骤610,vns分析系统200被配置为在输出设备(例如用户i/o设备210等)上提供指示,其指示患者对接受迷走神经刺激治疗的适宜性(例如,vns的潜在功效等)。在一些实施例中,该指示包括加权和/或复合分数。在一些实施例中,该指示包括指示迷走神经刺激治疗对患者的潜在功效(例如,预测的等)的百分比、值和/或另一度量(例如,由vns分析系统200使用加权和/或复合分数等确定)。在其他实施例中,该指示包括关于患者是否应该(例如基于加权和/或复合分数等)使迷走神经刺激器(例如迷走神经刺激器10等)被植入的推荐(例如,“通过”、“失败”“批准”、“不提供vns治疗”等)。
现在参考图7,示出了根据另一示例性实施例的用于评估患者对接受迷走神经刺激治疗的适宜性的方法700。在一个示例实施例中,可以利用图5的vns分析系统200来实现方法700。因此,可以关于图5来描述方法700。
在步骤702,vns分析系统200被配置为接收关于患者对接受迷走神经刺激治疗的适宜性的反应标准。在一个实施例中,反应标准由操作者经由输入设备(例如用户i/o设备210等)手动地输入。在其他实施例中,反应标准在vns分析系统200的存储器(例如存储器256等)内被预定义。根据示例性实施例,反应标准包括由于刺激(例如对迷走神经等)而引起的患者的心率的反应(例如,心率的变化、心率变异性、心率的最小变化、心率的最大变化、心率的百分比变化等)。
在步骤704,vns分析系统200被配置成控制刺激设备(例如刺激设备220等)的操作以向患者的迷走神经提供刺激(例如,evns、直接vns、耳廓vns、急性刺激等)。
根据示例性实施例,vns分析系统200被配置为根据预定义的刺激协议来控制刺激设备的操作。在一个实施例中,刺激设备包括具有至少一个电极(例如电极38等)的引线(例如引线30等),电极在血管内位于靠近迷走神经的一部分(例如,从迷走神经分支的心脏束等)的静脉(例如奇静脉等)的腔内。因此,刺激设备可以通过静脉壁经血管向迷走神经提供刺激。在另一实施例中,刺激设备包括位于患者的身体外部的外部刺激设备,以通过患者的皮肤提供刺激。在一个实施例中,外部刺激设备包括耳廓刺激设备,该耳廓刺激设备被配置为在患者的耳朵周围提供耳廓刺激。在其他实施例中,外部刺激设备包括被配置为向患者的另一外部区域(例如胸部、背部、颈部等)提供刺激的另一类型的刺激设备。在还有其他实施例中,刺激设备包括卡肤型电极(例如卡肤型电极40等)或临时植入到迷走神经上并被配置成直接向迷走神经提供刺激的其他类型的电极。作为例子,这种侵入性vns测试方法可以在患者已经经历便于接近迷走神经的外科手术过程时使用(例如,执行外科手术过程的原因不是被执行来便于测试——被包括在另一个手术过程中的额外步骤等)。
在步骤706,vns分析系统200被配置为从传感器(例如传感器230等)接收反应数据,其指示患者对迷走神经的刺激的生理反应(例如,对迷走神经的血管内、外部和/或直接刺激等)。生理反应可以包括心率、心率的变化、心率变异性和/或由刺激引起的患者的其他生理反应。
在步骤708,vns分析系统200被配置为将患者的生理反应与反应标准进行比较。在步骤710,vns分析系统200被配置成基于患者的生理反应和反应标准的比较来确定患者对接受迷走神经刺激的适宜性。在步骤712,vns分析系统200被配置为在输出设备(例如用户i/o设备210等)上提供指示,其指示患者对接受迷走神经刺激治疗的适宜性。在一些实施例中,该指示包括指示迷走神经刺激治疗对患者的潜在功效(例如,预测的等)的百分比、值和/或其他度量(例如,由vns分析系统200基于生理反应等确定)。在其他实施例中,该指示包括关于患者是否应该使迷走神经刺激器(例如迷走神经刺激器10等)被植入(例如基于生理反应)的推荐(例如,“通过”、“失败”“批准”、“不提供vns治疗”等)。
在一些实施例中,方法600和方法700被组合。作为例子,vns分析系统200可以基于(i)一个或更多个特征与一个或更多个标准的比较和(ii)生理反应与反应标准的比较来确定患者对接受迷走神经刺激治疗的适宜性。在一个实施例中,vns分析系统200被配置为基于每个特征和生理反应相对于相应标准来确定患者的复合分数。在一些实施例中,vns分析系统200被配置为基于每个特征和生理反应相对于相应标准来确定患者的加权复合分数。在可选的实施例中,vns分析系统200首先实现方法600以确定执行任何刺激测试(即,方法700等)是否是值得(例如必要的等)。
鉴于以上所述,可以认识到,与耦合到与迷走神经直接接触的电极的完全植入的vns神经刺激器相比,evns提供了用于向迷走神经输送刺激能量的较小侵入性或微创设备、系统和方法。如也可以认识到的,evns方法可以用于评估患者对迷走神经刺激的反应,以便生成在确定候选者是否是对长期vns治疗的合适候选者的数据。如例如对由biocontrolmedical公司出售的
进一步参考由biocontrolmedical公司出售的
1.纽约心脏协会功能iii类中的慢性症状性心力衰竭。
2.至少18岁年龄。
3.受试者在加入时应占优势地处于窦性心律。
4.在作为心力衰竭治疗的护理标准的根据当前指南而推荐的稳定的最佳地强化的医学治疗上。
5.在加入前三个月内,每部位测量lvef≤40%。
6.每部位测量的左心室舒张末期内径应该在50和80毫米之间。
7.受试者是男性或绝经后女性。如果使用了可接受的避孕措施,则育龄女性可以被包括。
8.受试者必须签署批准的知情同意书。受试者同意参加所有随访评估。
9.拥有crt设备的受试者可以被包括在试验中,假定他们已经拥有crt设备至少12个月。
在inovate-hf研究中
1.可能导致在6个月内死亡的除了心力衰竭之外的威胁生命的状况或疾病的存在。
2.前一个月内的急性心肌梗死(mi)、变异型心绞痛、不稳定型心绞痛或急性冠脉综合症。
3.在前面3个月内的中风或tia的历史或将损害对迷走神经刺激做出反应或检测对迷走神经刺激的改善的能力的显著神经损伤。
4.在前3个月内的或者在6个月内计划/预期的冠状动脉旁路手术(cabg)、瓣膜置换或修复、主动脉手术或pci。
5.由于急性心肌炎、限制型心肌病、缩窄性心包炎或血流动力学显著的主动脉瓣关闭不全、主动脉瓣狭窄或二尖瓣狭窄导致的心力衰竭。
6.严重的肾衰竭(肌酸酐水平>3mg/dl(265微摩尔/升))。
7.严重的肝功能衰竭(转氨酶水平是uln的四倍,或总胆红素水平>1.8mmol/dl)。
8.不受控制的糖尿病在研究者看来将危害植入程序的安全性和/或对迷走神经刺激做出反应或检测对迷走神经刺激的改善的能力。
9.先前的右颈部手术,包括对脑血管疾病(cvd)、恶性肿瘤和先前的颈部放射治疗,其在植入外科医生看来将阻止迷走神经卡肤的安全植入。有在颈动脉超声上评估的多于70%右颈动脉狭窄的受试者被排除。
10.当前低血压(收缩压低于80mmhg)。
11.在6个月内的活动性消化性溃疡疾病或上消化道出血史或溃疡。
12.肺部疾病例如严重哮喘、copd(例如,fev1<1.5升)或持续氧依赖的历史。
13.第2度或第3度房室传导阻滞或未使用起搏器治疗的其他起搏器指示。
14.在前3个月内的慢性心房颤动或扑动,或由于在过去6个月内的临床表现而引起的af的住院治疗。
15.单极感测的使用
16.先天性或后天性长qt综合征。
17.以文件证明的所记录的或疑似血管迷走神经性晕厥或血管抑制性晕厥。
18.在过去3个月内通过试验药物或设备进行的治疗。
19.受试者必须在2个月内没有接受过变力治疗,或者被认为是最近的1个月内对变力治疗的可能候选者。
20.无法理解需要持续治疗且未被药物充分控制的重度情感障碍(例如,重度抑郁症或双相精神障碍或精神分裂症)的知情同意和/或先验诊断。
21.被移植有心脏或其他组织或器官或者在心脏移植等待名单上并预计在随机化的6个月内接受移植的受试者。
22.免疫抑制受试者;在全身类固醇治疗下的受试者。
23.hgb≤9.5g/l的贫血。如果用于保持hgb>9.5g/l,则允许使用促红细胞生成素或其他类似的试剂治疗。
24.具有15或更高的呼吸暂停低通气指数的未治疗的阻塞性睡眠呼吸暂停(“osa”);或被治疗少于3个月的osa。
如可从上面列出的纳入和排除标准认识到的,被考虑植入
据信,当考虑附加标准时,当评估患者对vns治疗的适宜性时由其他方使用的纳入和排除标准可以得到加强。例如,这些附加标准可以包括:
1.患者的自主神经功能障碍状态的评估。据信,患有自主神经功能障碍的患者可能对art更好地做出反应,art恢复自主神经平衡。自主神经功能障碍可以使用压力反射敏感性(brs)、肌肉交感神经活性(msna)或血液生物标志物(去甲肾上腺素、乙酰胆碱等)来测量。
2.患者的心率变异性(hrv)状态的评估。据信,具有较低的hrv的患者可能对art更好地做出反应,这增加了在心力衰竭中的心率变异性。可以使用各种时域测量(avnn、sdnn、sdann、sdnnidx、rmssd、pnn50)和频域测量(vlf、lf、hf、lf/hf)来测量hrv。
3.患者的炎症状态的评估。据信,具有较高的炎症程度的患者可能对art更好地做出反应,art具有抗炎作用。可以使用血液生物标志物例如c反应蛋白(crp)、白细胞介素(il)-1、il-6、il-8、单核细胞趋化蛋白-1(mcp-1)和基质金属蛋白酶(mmp)来测量炎症。
4.患者的射血分数(ef)状态的评估。据信,具有较低的左心室射血分数的患者可能对art更好地做出反应。这个截止可以在ef<40%、ef<35%或ef<30%处。
5.患者的ef范围状态的评估。据信,具有低的左心室射血分数的患者可能对art更好地做出反应;然而,如果ef过低,疾病可能太晚期,且反应可能更差。ef范围可以小于30%、35%或40%,并且大于15%、20%或25%。
6.患者的脑利钠肽(bnp)状态的评估。据信,具有如由高bnp或前激素bnp(nt-probnp)的n端指示的较差的心力衰竭的患者可能对art更好地做出反应。
7.患者的心脏再同步治疗(crt)状态的评估。据信,具有现有crt的一些患者不如没有crt的患者对art很好地做出反应。
8.患者的心力衰竭病因状态的评估。据信,具有非缺血性心力衰竭的一些患者不如具有缺血性心力衰竭的患者对art很好地做出反应。
9.患者的静息心率状态的评估。据信,尽管有omt,但具有高静息心率的患者可能处于高交感神经驱动下,且因此基于增强拮抗机制可能对迷走神经刺激更加敏感。高hr可被定义为hr>70bpm。
10.患者的夜间心率的评估。据信,高夜间hr可能是用于筛选的另一个目标,因为在有限的临床经验中,增加的睡眠心率和心率不降与cvd和全因死亡率的增加的风险相关,但清醒心率没有。
11.患者的年龄的评估。据信,年龄可以用作筛选参数,因为随着年龄而改变的在神经上的信号传导和大脑可塑性可阻止vns的功效。
12.患者的健康指数的评估。据信,能够达到某个水平的身体活动(例如,能够在六分钟步行测试期间行走150和450米之间)、具有小于30-35的体重指数(bmi)、具有在合适的ef范围内的ef、在合适的范围内的心输出量和/或具有少于五到十年的诊断出的心力衰竭状况的患者更适合于接受迷走神经刺激治疗。
13.患者的不同步性的评估。据信,具有较低的不同步性的患者更适合于接受迷走神经刺激治疗。作为例子,合适的患者可能具有低的心室电不同步性。例如,这样的患者可能没有接受crt治疗和/或可能有小于150毫秒的qrs波群。作为另一个例子,合适的患者可能具有低机械心室不同步性。例如,在合适的患者的左心室射血前间期(lvpei)和右心室射血前间期(rvpei)之间的差异可能小于四十毫秒。在另一个例子中,在合适的患者的后续lvpei之间的差异可能小于140毫秒。
14.患者的改善潜力的评估。据信,具有更大改善潜力的患者更适合于接受迷走神经刺激治疗。例如,具有高静息心率(例如大于70bpm等)、低hrv、低压力反射敏感性(例如,小于3ms/mmhg等)和/或低心率恢复(例如,小于11bpm/min等)的患者可能更适合于接受迷走神经刺激治疗。
15.患者的心力衰竭的严重程度的评估。据信,在某一心力衰竭严重程度范围内的患者可能更适合于接受迷走神经刺激治疗。心力衰竭严重程度范围可包括纽约心脏协会(nyha)心力衰竭症状分类中的ii类和iii类内的患者(i类和iv类可以或可以不被排除)。心力衰竭严重程度范围可以此外或可选地包括患者有诊断出的心力衰竭状况的持续时间(例如,在零和五年之间,少于八至十年,等等)和/或严重性增加的速率(例如,在分类中的变化之间的时间段、心力衰竭测试的测量参数的变化,包括例如在六分钟步行测试期间步行的距离的变化等)。
16.所有上述标准或者这些标准的子集的复合分数的评估。
如可从上面列出的附加标准认识到的,被考虑植入vns系统的患者可以由不直接测量或评估患者对迷走神经刺激的反应的多个附加标准评估。如还可以认识到的,一个、几个或所有上面列出的附加标准可以与当评估患者对vns治疗的适宜性时由其他方使用的一个或多个标准例如与
除了上述标准之外,上述实施例(且特别是描述可用于评估患者对vns刺激的反应的evns设备或方法的实施例)可用于在实施完全植入的系统的植入之前直接评估患者对迷走神经刺激的形式的反应。评估性vns系统例如evns的使用可以提供在确定患者是否是合适的候选者时有用的另外的附加标准。这些附加标准可以包括:
1.在急性evns过程期间患者的心率的评估。这可以包括当施加刺激时心率下降的指示。
2.在急性evns过程期间的患者的心率稳定性的评估。这可以包括在施加刺激时心率稳定性变化的指示。
3.在急性evns过程期间的患者的血压的评估。这可以包括在施加刺激时血压变化的指示。
4.在急性evns过程期间的患者的左心室舒张充盈时间的评估。这可以包括在施加刺激时患者的左心室舒张充盈时间的增加的指示。
5.患者对迷走神经刺激的耐受性的评估。这可以包括患者对较高电流刺激的耐受性和/或患者对滴定速率的较低敏感度的指示(例如,刺激事件随时间的增加、刺激电流随时间的增加等)。作为例子,能够接收较高刺激电流(例如,大于3.5ma、4ma等)的患者可能对迷走神经刺激有增加的积极反应。作为另一个例子,在一段时间内对增加的刺激速率和/或在一段时间内对刺激电流的增加的速率更耐受的患者可能更适合于接受迷走神经刺激。可以在刺激后调查期间确定患者的易感性,该调查用于指示从这种刺激引起的不适和/或疼痛的程度、在刺激期间一个或多个参数的测量(例如心率的变化等)和/或一种或多种生理副作用(例如咳嗽、声音丧失、不适等)的出现。
如还可以认识到的,一个、几个或所有上面列出的另外的附加标准可以与当评估患者对vns治疗的适宜性时由其他方使用的一个或多个标准例如与
包括附加标准和另外的附加标准的上面列出的标准可以呈现给医生或感兴趣的医疗保健提供者,以指示患者是否适合于vns治疗。标准可以是以网站或产品标签的形式,且可以呈现为纳入或排除标准。
在上述实施例中,且特别是关于描述可用于评估患者对vns刺激的反应的evns设备或方法的实施例,当确定患者是否是对由vns或evns系统提供的迷走神经刺激的合适候选者时,可识别和评估额外的纳入和排除标准。
本公开设想用于完成各个操作的方法、系统和在任何机器可读介质上的程序产品。可以运用现有计算机处理器、或通过为此目的或其他目的所引入的恰当系统的专用计算机处理器或通过硬接线的系统来实现本公开的实施例。本公开的范围之内的实施例包括程序产品,其包括用于携带或具有存储于其上的机器可执行指令或数据结构的机器可读介质。这种机器可读介质可以是任意可用介质,其可通过通用或专用计算机或具有处理器的其他机器访问。举例来讲,这种机器可读介质可包括ram、rom、eprom、eeprom、cd-rom或其他光盘储存器、磁盘储存器或其他磁储存设备、或可用于携带或存储以机器可执行指令或数据结构形式的所需程序代码的且可以通过通用或专用计算机或具有处理器的其他机器访问的任何其他介质。当信息通过网络或另一通信连接(硬接线的、无线的或硬接线或无线的组合)被传送或提供到机器时,该机器适当地将这个连接视为机器可读介质。因此,任意这种连接被适当地称之为机器可读介质。上面的组合也被包括在机器可读介质的范围内。机器可执行指令包括例如指令和数据,该指令和数据使得通用计算机、专用计算机或专用处理机器执行某一功能或一组功能。
尽管附图可能示出了方法步骤的特定顺序,但是该步骤的顺序可以不同于所描述的顺序。还可以同时或部分同时执行两个或多个步骤。这种变化将取决于所选择的软件和硬件系统以及设计人员的选择。所有这种变化在本公开的范围之内。同样地,软件实现可以用具有基于规则的逻辑和其他逻辑的标准编程技术来完成以完成各个连接步骤、处理步骤、比较步骤和决策步骤。
此外,术语“或”在其包括界限的意义上(而不是在其排他意义上)被使用,使得当用于例如连接元素的列表时,术语“或”意指列表中的一个、一些或所有元素。除非另有特别说明,否则诸如短语“x、y和z中的至少一个”的连接语言与上下文一起被理解为通常用于传达项目、术语等可以是x、y、z、x和y、x和z、y和z或者x、y和z。因此,这种连接语言通常不意欲暗示某些实施例需要x中的至少一个、y中的至少一个和z中的至少一个每个都存在。
虽然在这里公开了各种方面和实施例,但是其他方面和实施例对本领域中的技术人员将明显。在这里公开的各种方面和实施例是为了说明的目的,而没有被规定为限制性的,真实范围和精神由权利要求指示。
- 还没有人留言评论。精彩留言会获得点赞!