膜裂解嵌段共聚物的制作方法
本发明是在政府支持下根据美国国立卫生研究院(nationalinstitutesofhealth)授予的批准号r01ns064404进行。政府对本发明具有一定的权利。
背景技术:
细胞内药物诸如基于核酸的药物、肽和蛋白质的潜在变革性影响主要由于涉及大分子治疗剂的细胞内递送的相当大的递送挑战而尚未在临床上实现。m.e.davis等人.nature2010,464,1067-u1140;b)m.a.kay,natrevgenet2011,12,316-328;c)k.a.whitehead等人.natrevdrugdiscov2009,8,129-138。对于核酸,使用两种主要类别的递送媒介物、病毒系统和非病毒系统包装货物(cargo)并促进细胞吸收,但具有其对应的限制。病毒载体具有免疫原性和健康问题并且制造昂贵。c.e.thomas等人.naturereviewsgenetics2003,4,346-358。非病毒载体诸如合成聚合物与病毒相比具有改进的成本和安全性曲线,但是与其病毒对应物相比在基因转移方面的有效性低多个数量级。u.lachelt等人.chemrev2015,115,11043-11078。
探索聚合物载体的细胞内运输的多个研究已将核内体释放确定为细胞内递送的限制性步骤;如果没有发生外出,则核内体内容物通常被路送以用于溶酶体降解。j.m.bergen等人.thejournalofgenemedicine2008,10,187-197;b)c.m.varga等人.genether2005,12,1023-1032。因此,合成聚合物已被设计为通过诸如在酸性ph中缓冲(称为“质子海绵效应”)以及膜活性肽和烷基化羧酸结合的机制来增强核内体释放。j.-p.behr,chimiainternationaljournalforchemistry1997,51,34-36;b)e.wagner,advanceddrugdeliveryreviews1999,38,279-289;c)a.j.convertine等人.jcontrolrelease2009,133,221-229;d)e.j.adolph等人.journalofmaterialschemistryb2014,2,8154-8164。这些方法通常在培养的细胞中工作良好,但是可能不容易转译以用于体内应用。通过质子海绵效应进行核内体缓冲需要可能在体内难以实现的显著积累的聚合物浓度。同时,在到达核内体之前需要屏蔽膜活性肽,以使导致位点外毒性的细胞膜破坏最小化。
技术实现要素:
本公开提供一种合成聚合物,该合成聚合物模拟腺病毒(ad)所采用的有效核内体逃逸机制。
本公开的主要特征是一种嵌段共聚物,该嵌段共聚物包含第一亲水性嵌段,其在生理条件中提供溶解性;和第二嵌段,其是ph响应性的和可逆地疏水性的,膜裂解实体附接至该第二嵌段。在细胞外ph下,第二嵌段是疏水性的,从而使疏水性嵌段自组装,进而减小材料在内在化之前的裂解可能性。在某些酸性ph(在内在化到酸化核内体之后碰到)下,第二嵌段变成亲水性的并且膜裂解实体变得暴露出来以促进核内体释放。嵌段共聚物可以通过直接共价附接或通过非共价相互作用(诸如静电结合、范德华力、氢键结合、疏水性封装等)来与其大分子货物缔合。
在一方面,本公开提供嵌段共聚物,该嵌段共聚物包含:亲水性嵌段,该亲水性嵌段包含在约中性ph下为水溶性的重复单元;以及ph响应性嵌段,该响应性嵌段包含在约中性ph下为疏水性的重复单元,其中该ph响应性嵌段共价偶合至膜裂解实体。
在一方面,本公开提供嵌段共聚物,该嵌段共聚物包含:亲水性聚离子嵌段,该亲水性聚离子嵌段包含在约中性ph下为离子性的重复单元;以及ph响应性嵌段,该响应性嵌段包含在约中性ph下为疏水性的重复单元,其中该ph响应性嵌段共价偶合至膜裂解实体。
在某些实施方式中,聚离子嵌段包含选自在约中性ph下为阳离子的重复单元、在约中性ph下为阴离子的重复单元以及中性亲水性重复单元的重复单元。
在某些实施方式中,ph响应性嵌段在大于约6.8的ph下为疏水性的。
在某些实施方式中,膜裂解实体通过连接基共价连接至ph响应性嵌段。
在第二方面,本发明提供一种用于提供根据本文进一步描述的任何共聚物的共聚物的方法。
在第三方面,本发明提供胶束组装物,该胶束组装物包含:根据本文进一步描述的任何共聚物的多种共聚物。在某些实施方式中,胶束组装物具有约5nm至约100nm的直径。在某些实施方式中,胶束组装物在小于约6.5的ph下分解。
在第四个实施方式中,本发明提供一种药物组合物,该药物组合物包含根据本发明的任何方面的嵌段共聚物和根据本发明的方面的胶束组装物中的至少一种;以及与共聚物可逆地缔合的治疗剂。在某些实施方式中,治疗剂缀合至共聚物。在某些实施方式中,治疗剂与共聚物非共价缔合。在某些实施方式中,治疗剂是核酸分子。在某些实施方式中,治疗剂是蛋白质或肽。
在第五方面,本发明提供一种在细胞内递送核酸、肽或蛋白质的方法,该方法包括:向受试者给药根据本发明的药物组合物,其中该药物组合物被内吞到核内体中并且因此该药物组合物从核内体释放核酸、肽或蛋白质。
附图说明
本发明的上述方面和许多附带优点在结合附图时通过参考以下详细描述将变得更容易了解,也变得更好理解。
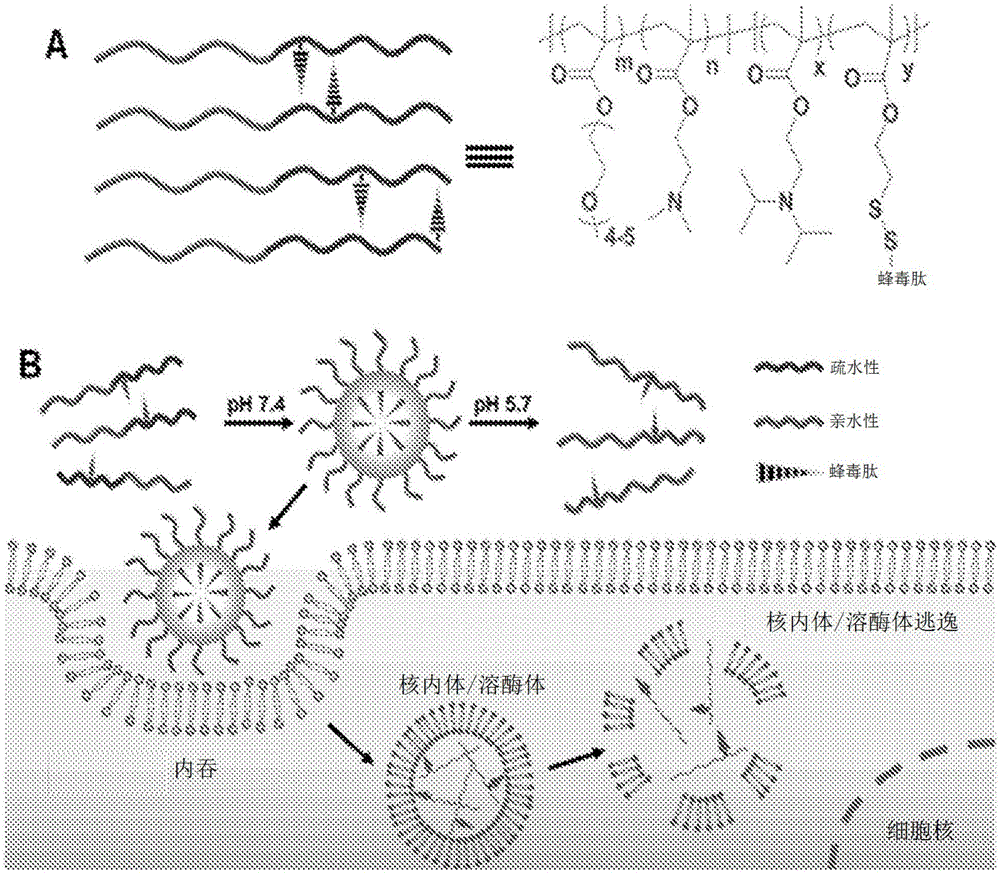
图1示出a).viper(用于核内体释放的病毒吸入型聚合物)的一个实施方式的化学结构。b).viper诱导的核内体/溶酶体逃逸的示意图。在中性ph下,viper自组装成纳米颗粒,其中膜裂解实体(在此实例中,肽蜂毒肽)被限制在ph敏感的结构域中。在由细胞内吞之后,酸性核内体/溶酶体环境诱导pdipama的亲水相变,从而实现蜂毒肽暴露、核内体/溶酶体膜破裂和核内体/溶酶体逃逸。
图2示出在各种酸性ph下经历疏水性至亲水性转变的viper的可替选实施方式的化学结构。
图3示出使用viper/质粒人工合成多聚物(polyplex)的优化配方进行的gfp质粒到各种永生化细胞系的体外转染。与viper相比进行所有统计分析。数据被示出为平均值±sd(n=3;student氏t检验,*p<0.05,***p<0.001)。
图4示出a).通过用各种人工合成多聚物瘤内注射进行治疗的携带kb肿瘤的小鼠的生物荧光图像。b).来自用人工合成多聚物治疗的小鼠的切下的kb肿瘤组织的荧光素酶活性。c).通过用各种人工合成多聚物瘤内注射进行治疗的携带a549肿瘤的小鼠的生物荧光图像。d).来自用人工合成多聚物治疗的小鼠的切下的a549肿瘤组织的荧光素酶活性。数据被示出为平均值±sd(n=4;student氏t检验,*p<0.05,**p<0.01,***p<0.001)。
图5示出p(oegma11-dmaema56)和p(oegma11-dmaema56)-b-p(dipama33-pdsema1)的1hnmr质谱。
图6示出聚合物/dna人工合成多聚物的表征。a).以不同n/p比率制备的聚合物/dna复合物的琼脂糖凝胶电泳。b)和c).以n/p=5形成的聚合物/dna复合物的tem图像(比例尺:200nm)。d).不同制剂的平均流体动力学直径。e).不同制剂的ζ电势。数据被示出为平均值±sd(n=3)。
图7示出在不同条件下由dna和viper(n/p=5)形成的人工合成多聚物的稳定性测试。数据被示出为平均值±sd(n=3)。
图8示出在不同聚合物浓度和ph下cp/dna和viper/dna人工合成多聚物的溶血活性。配方中使用的n/p比率是7。数据被示出为平均值±sd(n=3)。
图8示出在ph7.4和5.7下cp和viper人工合成多聚物的相对yoyo-1荧光强度。将荧光强度归一化至游离dna。数据被示出为平均值±sd(n=3)。
图9示出由cp和viper与dna(n/p=5)形成的人工合成多聚物的细胞摄取,用yoyo-1标记。数据被示出为平均值±sd(n=3)。
图10.用以不同n/p比率的各种人工合成多聚物对hela细胞进行的体外转染。a).转染效率。b).相对细胞活力。数据被示出为平均值±sd(n=3)。
图11示出用以不同n/p比率的各种人工合成多聚物对kb细胞进行的体外转染。a).转染效率。b).相对细胞活力。数据被示出为平均值±sd(n=3)。
图12示出用以不同n/p比率的各种人工合成多聚物对z310细胞进行的体外转染。a).转染效率。b).相对细胞活力。数据被示出为平均值±sd(n=3)。
图13示出用以不同n/p比率的各种人工合成多聚物对a549细胞进行的体外转染。a).转染效率。b).相对细胞活力。数据被示出为平均值±sd(n=3)。
图14示出用通过使viper、阳离子pdmaema向日葵(sunflower)聚合物和用于信使(mrna)递送的支链聚乙烯亚胺(bpei)静电络合形成的人工合成多聚物对hela细胞进行的体外转染。
具体实施方式
在一方面,本发明提供嵌段共聚物,该嵌段共聚物包含:亲水性嵌段,该亲水性嵌段在约中性ph下是水溶性的;以及ph响应性嵌段,该ph响应性嵌段包含在约中性ph下为疏水性的重复单元,其中该ph响应性嵌段共价联接至膜裂解肽。
在本说明书的不同位置处,以组或以范围公开了本公开的化合物的取代基。特别旨在的是,本公开包括此类组和范围的成员的各个和每个单个子组合。
应进一步了解的是,为了清楚而在单独实施方式的背景下描述的本公开的某些特征还可以按组合形式在单个实施方式中提供。
相反地,为了简洁而在单个实施方式的背景下描述的本公开的不同特征也可以单独地或以任何适合的子组合提供。
如本文所用,术语聚合物的“组成单元”是指聚合物中的原子或原子组,其包含链连同其侧接原子或原子组(如果有的话)的一部分。组成单元可以是指重复单元。组成单元还可以是指聚合物链上的末端基团。例如,聚乙二醇的组成单元可以是对应于重复单元的–ch2ch2o-或者对应于末端基团的–ch2ch2oh。
如本文所用,术语“重复单元”对应于最小组成单元,该最小组成单元的重复构成规则大分子(或寡聚物分子或嵌段)。
如本文所用,术语“疏水性”是指在生理ph和/或盐条件下具有显著非极性表面积的不会被吸引至水的部分。此相分离可以通过动态光散射和含水nmr测量的组合来观察。疏水性组成单元倾向于在含水条件下为非极性的。疏水性部分的实例包括烷基基团、芳基基团等。
如本文所用,术语“亲水性”是指被吸引至水并且倾向于被水溶解的部分。亲水性部分可与水相混溶。亲水性组成单元在含水条件下可为极性和/或可电离的。亲水性组成单元可在含水条件下为可电离的和/或含有极性官能团,诸如酰胺、羟基基团或乙二醇残基。亲水性部分的实例包括羧酸基团、氨基基团、羟基基团等。
如本文所用,术语“阳离子”是指带正电荷或者在生理条件下可电离成带正电荷部分的部分。阳离子部分的实例包括例如氨基、铵、吡啶鎓、亚胺基、锍、季鏻基团等。
如本文所用,术语“阴离子”是指带负电荷或者在生理条件下可电离成带负电荷部分的官能团。阴离子基团的实例包括羧酸根、硫酸根、磺酸根、磷酸根等。
在某些实施方式中,本发明的嵌段共聚物具有根据式(i)的结构:
其中
a1、a2、a3和a4选自由-c-c-、-c(o)(c)^c(o)o-、-o(c)ac(o)-和-o(c)bo-组成的组,其中a是1-4,b是2-4;
h是亲水性部分;
c在约7的ph下是带电荷部分;
q在大于约7的ph下为疏水性的。
l是连接基;
lp是膜裂解肽;
r1、r2、r3和r4独立地选自由氢、-cn、烷基、炔基、杂烷基、环烷基、杂环烷基、芳基和杂芳基组成的组;
m是在1-10,000之间;
n是在1-10,000之间;
p是在1-10,000之间;并且
q是在1-10,000之间。
在某些实施方式中,l是二硫桥。
如本文所用,术语“烷基”是指直链(例如线性)或支链的饱和烃基团。示例性烷基基团包括甲基(me)、乙基(et)、丙基(例如,正丙基和异丙基)、丁基(例如,正丁基、异丁基、叔丁基)、戊基(例如,正戊基、异戊基、新戊基)等。烷基基团可以含有1至约30、1至约24、2至约24、1至约20、2至约20、1至约10、1至约12、1至约8、1至约6、1至约4或1至约3个碳原子。
如本文所用,“亚烷基”是指连接的烷基基团。
如本文所用,“烯基”是指具有一个或多个双碳-碳键的烷基基团。烯基基团可以是线性或支链的。示例性烯基基团包括乙烯基、丙烯基等。烯基基团可以含有2至约30、2至约24、2至约20、2至约10、2至约8、2至约6或2至约4个碳原子。
如本文所用,“炔基”是指具有一个或多个三碳-碳键的烷基基团。炔基基团可以是线性或支链的。示例性炔基基团包括乙炔基、丙炔基等。炔基基团可以含有2至约30、2至约24、2至约20、2至约10、2至约8、2至约6或2至约4个碳原子。
如本文所用,“芳基”是指单环或多环(例如,具有2、3或4个稠合环)芳族烃,诸如苯基、萘基、蒽基(anthracenyl)、菲基(phenanthrenyl)、二氢茚基(indanyl)、茚基等。在一些实施方式中,芳基基团具有6至约20个碳原子。
如本文所用,“亚芳基”是指连接的芳基基团。
如本文所用,“环烷基”是指非芳族碳环,包括环状烷基、烯基和炔基基团。环烷基基团可以包括单环或多环(例如,具有2、3或4个稠合环)环体系,包括螺环。在一些实施方式中,环烷基基团可以具有3至约20个碳原子、3至约14个碳原子、3至约10个碳原子或3至7个碳原子。环烷基基团还可以具有0、1、2或3个双键和/或0、1或2个三键。在环烷基的定义中还包括具有一个或多个稠合(与其具有一个键)至环烷基环的芳族环的部分,例如戊烷、戊烯、己烷等的苯并衍生物。具有一个或多个稠合芳族环的环烷基基团可以通过芳族部分或非芳族部分附接。环烷基基团的碳原子的一个或多个成环碳原子可以被氧化,例如具有氧代或磺基取代基。示例性环烷基基团包括环丙基、环丁基、环戊基、环己基、环庚基、环戊烯基、环己烯基、环己二烯基、环庚三烯基、降冰片烯基(norbomyl)、降蒎烷基(norpinyl)、降莰基(norcamyl)、金刚烷基等。
如本文所用,“杂烷基”是指具有至少一个杂原子诸如硫、氧或氮的烷基基团。
如本文所用,“杂亚烷基”是指连接的杂烷基基团。
如本文所用,“杂芳基”是指具有至少一个杂原子环成员诸如硫、氧或氮的芳族杂环。杂芳基基团包括单环或多环(例如,具有2、3或4个稠合环)体系。杂芳基基团中的任何成环n原子可以被氧化以形成n-氧代部分。杂芳基基团的实例包括但不限于:吡啶基、n-氧代吡啶基、嘧啶基、吡嗪基、哒嗪基、三嗪基、呋喃基、喹啉基、异喹啉基、噻吩基、咪唑基、噻唑基、吲哚基、吡咯基、噁唑基、苯并呋喃基、苯并噻吩基、苯并噻唑基、异噁唑基、吡唑基、三唑基、四唑基、吲唑基、1,2,4-噻二唑基、异噻唑基、苯并噻吩基、嘌呤基、咔唑基、苯并咪唑基、吲哚啉基等。在一些实施方式中,杂芳基基团具有1至约20个碳原子,并且在另外的实施方式中具有约3至约20个碳原子。在一些实施方式中,杂芳基基团含有3至约14、3至约7或5至6个成环原子。在一些实施方式中,杂芳基基团具有1至约4、1至约3或1至2个杂原子。
如本文所用,后接有官能团的“烷基-”是指将官能团连接至取代的化合物的烷基基团。例如,“烷基-芳基”是指包括将芳基基团连接至取代的化合物的烷基基团的取代基。示例性“烷基-芳基”基团包括苄基或苯乙基。
在某些实施方式中,亲水性聚离子嵌段包含在约中性ph下为阳离子的重复单元。在某些其他实施方式中,此类阴离子重复单元选自由甲基丙烯酸2-(二甲基氨基)乙酯、丙烯酸2-二甲基氨基乙基酯、(3-丙烯酰氨基丙基)三甲基氯化铵、n-(3-氨基丙基)甲基丙烯酰胺、n,n-二乙基丙烯酰胺、n,n-二乙基甲基丙烯酰胺、n,n-二甲基丙烯酰胺、n-[3-(二甲基氨基)丙基]甲基丙烯酰胺、甲基丙烯酸2-氨基乙酯、甲基丙烯酸2-(二乙基氨基)乙酯、甲基丙烯酸2-(二甲基氨基)乙酯、甲基丙烯酸[2-羟基-3-(2-氨基乙基)氨基]丙酯、[3甲基丙烯酰胺基(methacryloylamino))丙基]三甲基氯化铵以及l-赖氨酸组成的组。
在某些实施方式中,亲水性聚离子嵌段包含在约中性ph下为阴离子的重复单元。在某些其他实施方式中,此类阴离子重复单元选自由甲基丙烯酸、丙烯酸、二甲基马来酸酐改性的n-(3-氨基丙基)甲基丙烯酰胺以及甲基丙烯酸2-氨基乙酯组成的组。
在某些实施方式中,亲水性聚离子嵌段包含中性亲水性重复单元。在某些其他实施方式中,中性亲水性重复单元是两性离子性的。在某些其他实施方式中,中性亲水性重复单元选自包含以下的重复单元:寡(乙二醇)、羟基丙基甲基丙烯酰胺、甲基丙烯酸2-羟基乙酯、n-异丙基丙烯酰胺、3-葡聚糖酰氨基丙基甲基丙烯酰胺、2-乳清蛋白酰氨基乙基甲基丙烯酰胺、甜菜碱、胆碱磷酸、磺基甜菜碱以及羧酸甜菜碱。
本公开的嵌段共聚物包括含有在约中性ph下为疏水性的重复单元的ph响应性嵌段。在某些实施方式中,ph响应性嵌段在大于约7.0的ph下为疏水性的。在其他实施方式中,ph响应性嵌段在超过范围为4至7.2的ph下变成疏水性的。在某些实施方式中,ph响应性嵌段包含选自由甲基丙烯酸2-二异丙基氨基乙酯、甲基丙烯酸2-(五亚甲基亚氨基)乙酯、甲基丙烯酸2-(六亚甲基亚氨基)乙基酯组成的组中的重复单元。
嵌段共聚物可以包含共价连接至ph响应性嵌段的膜裂解实体。在某些实施方式中,膜裂解实体通过连接基共价连接至ph响应性嵌段。在某些实施方式中,连接基选自碳-碳键、寡核苷酸、含酯片段、含酰胺片段、含二硫基的片段。
膜裂解实体能够在以临界浓度存在时裂解细胞膜。在某些实施方式中,膜裂解实体选自由蜂毒肽、来自腺病毒蛋白vi的肽、gala、kala、egla、jts1、短杆菌肽s、hgp肽(序列llgrrgwevlkywwnllqywsqel)、shgp肽(序列rgwevlkywwnllqy)、tat肽(序列grkkrrqrrrpq)、寡聚精氨酸以及血凝素组成的组。
在某些实施方式中,本发明的嵌段共聚物具有根据式(ii)的结构:
其中
每个a1是亲水性单体衍生单元;
每个a2是在ph10或更小值下独立地为中性或带电荷的单体衍生单元;
每个a3是包括治疗性肽、核酸或核酸衍生物单体衍生单元;
每个a4是pka范围为约ph4至约ph7的单体衍生单元;
每个a5是包括治疗性肽、核酸或核酸衍生物的单体衍生单元;
a6是包括膜裂解实体的单体衍生单元;
t1独立地是不存在的或是靶向基团;
t2独立地是不存在的、膜裂解实体、治疗性肽、核酸或核酸衍生物;
m是约1至约10,000;
n是约0至约10,000;
o是约0至约10,000;
p是约1至约10,000;
q是约0至约10,000;并且
r是约0至约10,000。
在某些实施方式中,本发明的嵌段共聚物具有根据式(iia)的结构:
其中
每个a1是亲水性单体衍生单元,
每个a2是在ph10.0或更小值下为中性或带电荷的单体衍生单元;
每个a4是pka范围为约ph4至约ph7的单体衍生单元;
每个a3’、a5’和a6’独立地是
其中
每个x独立地包括含有亚烷基、亚芳基、二硫基、环氧烷烃或丙烷-2,2-二醇的重复单元;
其中每个x可选地被-co2r1、l1-d1、l2-d2或l3-lp取代,其中r1是亲水性基团,
每个r独立地是氢、-co2r2、-cn、烷基、炔基、杂烷基、环烷基、杂环烷基、芳基或杂芳基,其中r2是亲水性基团、l1-d1、l2-d2或l3-lp,
a是1-4,并且
b是2-4;
l1、l2和l3各自独立地是不存在的或者是连接基;
每个lp是膜裂解实体;
d1和d2各自独立地是治疗性肽、核酸或核酸衍生物;
t1独立地是不存在的或是靶向基团;
t2独立地是不存在的、是膜裂解实体、治疗性肽、核酸或核酸衍生物;
m是约1至约10,000;
n是约0至约10,000;
o是约0至约10,000;
p是约1至约10,000;
q是约0至约10,000;并且
r是约0至约10,000。
在一些实施方式中,每个a1’、a2’、a3’、a4’、a5’和a6’独立地是
在一些实施方式中,每个x独立地包括含有亚烷基、亚芳基或环氧烷烃的重复单元。在一些实施方式中,环氧烷烃可以是聚(环氧乙烷)、聚(环氧丙烷)或聚(环氧丁烷)。在其他实施方式中,二硫基、环氧烷烃或丙烷-2,2-二醇。二硫基可包括结构
在x中的重复单元数量的范围可以是1至30、1至20、1至15、1至10、5至30、10至30或15至30。
在一些实施方式中,r1和r2的亲水性基团包括一个或多个氧化烯烃单元。例如,亲水性基团可以包括聚(环氧烷烃),诸如聚(环氧乙烷)、聚(环氧丙烷)或聚(环氧丁烷)。在一些实施方式中,r1和r2的亲水性基团包括氨基基团,诸如-烷基-nr’。
在一些实施方式中,a是2-4或1、2、3或4。在一些实施方式中,b是2、3或4。
在某些实施方式中,本发明的嵌段共聚物具有根据式(ii)的结构,其中l1、l2和l3各自独立地包含将d1、d2或lp分别连接至聚合物主链的共价键。在一些实施方式中,l是可逆键,诸如二硫桥、肼键、硼酸酯或肽。在一些实施方式中,l1、l2或l3是二硫桥。在一些实施方式中,l1、l2或l3是肽。在一些实施方式中,l1、l2或l3是例如通过点击化学或巯基-烯(thiol-ene)缀合形成的不可逆键。在一些实施方式中,其可为可逆的,像二硫桥或腙键或硼酸酯。在其他实施方式中,l1、l2或l3不存在。
在某些实施方式中,亲水性聚离子嵌段(即,包含a1、a2和a3的嵌段)包含在约中性ph下为阳离子的重复单元。在某些其他实施方式中,此类阴离子重复单元选自由甲基丙烯酸2-(二甲基氨基)乙酯、丙烯酸2-二甲基氨基乙酯、(3-丙烯酰氨基丙基)三甲基氯化铵、n-(3-氨基丙基)甲基丙烯酰胺、n,n-二乙基丙烯酰胺、n,n-二乙基甲基丙烯酰胺、n,n-二甲基丙烯酰胺、n-[3-(二甲基氨基)丙基]甲基丙烯酰胺、甲基丙烯酸2-氨基乙酯、甲基丙烯酸2-(二乙基氨基)乙酯、甲基丙烯酸2-(二甲基氨基)乙酯、甲基丙烯酸[2-羟基-3-(2-氨基乙基)氨基]丙酯、[3甲基丙烯酰胺基)丙基]三甲基氯化铵以及l-赖氨酸组成的组。
在某些实施方式中,亲水性聚离子嵌段包含在约中性ph下为阴离子的重复单元。在某些其他实施方式中,此类阴离子重复单元选自由甲基丙烯酸、丙烯酸、二甲基马来酸酐改性的n-(3-氨基丙基)甲基丙烯酰胺以及甲基丙烯酸2-氨基乙酯组成的组。
在某些实施方式中,亲水性聚离子嵌段包含中性亲水性重复单元。在某些其他实施方式中,中性亲水性重复单元是两性离子性的并且选自包含甜菜碱、胆碱磷酸、磺基甜菜碱和羧酸甜菜碱的重复单元。在某些其他实施方式中,中性亲水性重复单元选自包含以下的重复单元:寡(乙二醇)、羟基丙基甲基丙烯酰胺、甲基丙烯酸2-羟基乙酯、n-异丙基丙烯酰胺、3-葡聚糖酰氨基丙基甲基丙烯酰胺以及2-乳清蛋白酰氨基乙基甲基丙烯酰胺。
嵌段共聚物的每个a2是在ph10或更小值下为中性或带电荷的单体衍生单元。例如,单体衍生单元所来源的单体在ph10或更小值下为中性或带电荷的。在一些实施方式中,每个a2是在ph9.8或更小值、或9.6或更小值、或9.4或更小值、或9.2或更小值、或9.0或更小值、或8.8或更小值、或8.6或更小值、或8.4或更小值、或8.2或更小值、或8.0或更小值、或7.8或更小值、或7.6或更小值、或7.4或更小值、或7.2或更小值、或7.0下为中性或带电荷的单体衍生单元。
本发明的嵌段共聚物包含ph响应性嵌段(即,包含a4、a5和a6的嵌段)。ph响应性嵌段包含在约中性ph下为疏水性的重复单元(例如,a4)。例如,重复单元所来源的单体在约中性ph下为疏水性的。在某些实施方式中,ph响应性嵌段可在超过范围为4.0至7.0的ph下变成疏水性的。在一些实施方式中,ph响应性嵌段可以在超过范围为5.0至约7.0的ph、或超过范围为约6.0至约7.0的ph、或超过范围为约5.0至约6.5的ph、或超过范围为5.5至约7.0的ph、或超过范围为约5.5至约6.5的ph、或超过范围为约4.2至约6.8的ph、或超过范围为约4.8至约6.0的ph、或超过范围为约4.8至约6.8的ph、或超过范围为约5.8至约6.6的ph、或超过范围为约4.8至约6.4下变成疏水性的。
在其他实施方式中,每个a4是pka范围为约ph4.2至约ph7、或约ph4.4至约ph7、或约ph4.6至约ph7、或约ph4.8至约ph7、或约ph5至约ph7、或约ph5.2至约ph7、或约ph5.4至约ph7、或约ph5.6至约ph7、或约ph5.8至约ph7、或约ph6至约ph7、或约ph4至约ph6.8、或约ph4至约ph6.6、或约ph4至约ph6.6、或约ph4至约ph6.4、或约ph4至约ph6.2、或约ph4至约ph6的单体衍生单元。
例如,ph响应性嵌段可包含选自由甲基丙烯酸2-二异丙基氨基乙酯、甲基丙烯酸2-(五亚甲基亚氨基)乙酯、甲基丙烯酸2-(六亚甲基亚氨基)乙酯、甲基丙烯酸2-(二丙基氨基)乙酯、甲基丙烯酸2-(二丁基氨基)乙酯、甲基丙烯酸2-(二戊基氨基)乙酯以及甲基丙烯酸2-(乙基丙基氨基)乙酯组成的组中的重复单元。
在一些实施方式中,共聚物的亲水性聚离子嵌段和ph响应性嵌段可以彼此独立地共价联接至治疗性货物诸如核酸或肽。在某些实施方式中,治疗性货物诸如核酸或肽通过连接基共价连接至亲水性聚离子嵌段或ph响应性嵌段。连接基可以选自碳-碳键、寡核苷酸、由硼酸和二醇形成的硼酸酯键、亚胺键、含酯片段、硫醇酯、含酰胺片段、含二硫基的片段以及1,2,3-三唑诸如叠氮化物与炔烃的反应产物(“点击化学”)。在一些实施方式中,炔烃偶合配偶体是亲水性聚离子嵌段或ph响应性嵌段的一部分,并且叠氮化物偶合配偶体是膜裂解肽、治疗性肽或核酸的一部分。在其他实施方式中,叠氮化物偶合配偶体是亲水性聚离子嵌段或ph响应性嵌段的一部分,并且炔烃偶合配偶体是膜裂解肽、治疗性肽或核酸的一部分。
每个连接基(l1、l2或l3)可在每个单体衍生单元中独立地选择。例如,当o是2时,共聚物含有两个a3基团,其各自具有l1和d1。这两个基团可以是不同或相同的。类似地,每个a3单体衍生单元中的d1可以是不同或相同的。这同样适用于l2和d2以及l3和lp。
靶向基团可以是小分子、适配体、肽、蛋白质、抗体或抗体片段。
在一些实施方式中,t1和t2二者是不存在的,而在其他实施方式中,仅t1或t2之一不存在。在一些实施方式中,t1是靶向基团或治疗性货物并且t2是膜裂解实体或治疗性货物。
膜裂解实体可以是能够超过临界浓度裂解细胞膜的任何实体。在某些实施方式中,膜裂解实体是选自由蜂毒肽、来自腺病毒蛋白vi的肽、gala、kala、egla、jts1、gramicidins、hgp肽(序列llgrrgwevlkywwnllqywsqel)、shgp肽(序列rgwevlkywwnllqy)、tat肽(序列grkkrrqrrrpq)、寡聚精氨酸、call(kwklfkkifkrivqrikdflr)、墨蝎毒素(gildtiksiaskvwnsktvqdlkrkginwvanklgvspqaa)、红独角兽毒素(cupiennin)1a(gfgalfkflakkvaktvakqaakqgakyvvnkqme)、螃蟹毒素(crabolin)(fmoc-flalilrkivtal-conh2)、isct(ilgkiwegikslf-nh2)、hsap(sgtsekeresgrllgvvkrlivcfrspfp-nh2)、熊猫毒素(pandinin)2(fwgalakgalklipslfssfskkd)、猛蚁毒素(ponericin)(wlgsalkigakllpsvvglfkkkkq)、uyct5(iwsaiwsgikgll-nh2)以及血凝素组成的组中的肽。
治疗性肽可以是能够发挥生物效应的肽。实例包括用于免疫刺激、细胞凋亡或抑制血管收缩的肽(例如,kla肽、bh3肽、hsp-20肽等)。
核酸可以携带基因(例如,质粒、微环或纳米质粒)、mrna或寡核苷酸(例如,sirna、dna酶、反义寡核苷酸)。
在一个实施方式中,式(ii)的嵌段共聚物具有式(iiia)的结构:
其中m’是约1至约20。
在一个实施方式中,式(ii)的嵌段共聚物具有式(iiib)的结构:
其中m’是从约1至约20。
在一个实施方式中,式(ii)的嵌段共聚物具有式(iiic)的结构:
其中m’是约1至约20。
在一个实施方式中,式(ii)的嵌段共聚物具有式(iiid)的结构:
其中m’是约1至约20;并且每个r’独立地是氢、烷基、环烷基、杂环烷基、芳基、烷基-环烷基、烷基-杂环烷基或烷基-芳基。
在一个实施方式中,式(ii)的嵌段共聚物具有式(iiie)的结构:
其中m’是约1至约20;并且每个r’独立地是氢、烷基、环烷基、杂环烷基、芳基、烷基-环烷基、烷基-杂环烷基或烷基-芳基。
在一个实施方式中,式(ii)的嵌段共聚物具有式(iiif)的结构:
其中m’是约1至约20;并且每个r’独立地是氢、烷基、环烷基、杂环烷基、芳基、烷基-环烷基、烷基-杂环烷基或烷基-芳基。
在一个实施方式中,式(ii)的嵌段共聚物具有式(iiig)的结构:
其中m’是约1至约20。
在一个实施方式中,式(ii)的嵌段共聚物具有式(iva)的结构:
其中m’是约1至约20;并且每个r’独立地是氢、烷基、环烷基、杂环烷基、芳基、烷基-环烷基、烷基-杂环烷基或烷基-芳基。
在一个实施方式中,式(ii)的嵌段共聚物具有式(ivb)的结构:
其中m’是约1至约20;并且每个r’独立地是氢、烷基、环烷基、杂环烷基、芳基、烷基-环烷基、烷基-杂环烷基或烷基-芳基。
在一个实施方式中,式(ii)的嵌段共聚物具有式(ivc)的结构:
其中m’是从1至约20;并且每个r’独立地是氢、烷基、环烷基、杂环烷基、芳基、烷基-环烷基、烷基-杂环烷基或烷基-芳基。
在一个实施方式中,式(ii)的嵌段共聚物具有式(ivd)的结构:
其中m’是约1至约20。
在一些实施方式中,嵌段共聚物具有式(ii),其中m’是约1至约20。在一些实施方式中,是约1至约15、或约5至约20、或约5至15、或约10至约20、或约12至约20、或约1至约18、或约5至约18。
在一些实施方式中,嵌段共聚物具有式(ii),其中每个r’独立地是氢、烷基、环烷基、杂环烷基或芳基。在其他实施方式中,每个r’独立地是氢、烷基、烷基-环烷基、烷基-杂环烷基或烷基-芳基。在其他实施方式中,每个r’独立地是氢、烷基、环烷基、芳基、烷基-环烷基或烷基-芳基。在其他实施方式中,每个r’独立地是氢或烷基。在一些实施方式中,每个r’独立地是氢、甲基、乙基、正丙基、异丙基、正丁基、异丁基、叔丁基、正戊基、异戊基或己基。在一些实施方式中,每个r’独立地是甲基、乙基、正丙基、异丙基、正丁基、异丁基、叔丁基、正戊基、异戊基或己基。
在一些实施方式中,嵌段共聚物具有式(ii),其中
m是约1至约10,000;
n是约1至约10,000;
o是约0至约10,000;
p是约1至约10,000;
q是约0至约10,000;并且
r是约0至约10,000。
在一些实施方式中,嵌段共聚物具有式(ii),其中
m是约1至约10,000;
n是约0至约10,000;
o是约0至约10,000;
p是约1至约10,000;
q是约0至约10,000;并且
r是约0至约10,000。
在一些实施方式中,嵌段共聚物具有式(ii),其中
m是约1至约10,000;
n是约0至约10,000;
o是约0至约10,000;
p是约1至约10,000;
q是约0至约10,000;并且
r是约1至约10,000。
在一些实施方式中,嵌段共聚物具有式(ii),其中
m是约1至约10,000;
n是约1至约10,000;
o是约0至约10,000;
p是约1至约10,000;
q是约0至约10,000;并且
r是约0至约10,000。
在一些实施方式中,嵌段共聚物具有式(ii),其中
m是约1至约10,000;
n是约1至约10,000;
o是约0至约10,000;
p是约1至约10,000;
q是约0至约10,000;并且
r是约1至约10,000。
在一些实施方式中,嵌段共聚物具有式(ii),其中
m是约1至约10,000;
n是约0至约10,000;
o是约1至约10,000;
p是约1至约10,000;
q是约1至约10,000;并且
r是约0至约10,000。
在一些实施方式中,嵌段共聚物具有式(ii),其中
m是约1至约10,000;
n是约0至约10,000;
o是约0至约10,000;
p是约1至约10,000;
q是约0至约10,000;并且
r是约1至约10,000。
在一些实施方式中,嵌段共聚物具有式(ii),其中
m是约1至约10,000;
n是约1至约10,000;
o是约1至约10,000;
p是约1至约10,000;
q是约1至约10,000;并且
r是约0至约10,000。
在一些实施方式中,嵌段共聚物具有式(ii),其中
m是约1至约10,000;
n是约1至约10,000;
o是约0至约10,000;
p是约1至约10,000;
q是约0至约10,000;并且
r是约1至约10,000。
在一些实施方式中,嵌段共聚物具有式(ii),其中
m是约1至约10,000;
n是约0至约10,000;
o是约1至约10,000;
p是约1至约10,000;
q是约1至约10,000;并且
r是约0至约10,000。
在一些实施方式中,嵌段共聚物具有式(ii),其中
m是约1至约10,000;
n是约0至约10,000;
o是约0至约10,000;
p是约1至约10,000;
q是约0至约10,000;并且
r是约1至约10,000。
在一些实施方式中,嵌段共聚物具有式(ii),其中
m是约1至约10,000;
n是约1至约10,000;
o是约1至约10,000;
p是约1至约10,000;
q是约1至约10,000;并且
r是约0至约10,000。
在一些实施方式中,嵌段共聚物具有式(ii),其中
m是约1至约10,000;
n是约1至约10,000;
o是约1至约10,000;
p是约1至约10,000;
q是约0至约10,000;并且
r是约1至约10,000。
在一些实施方式中,嵌段共聚物具有式(ii),其中
m是约1至约10,000;
n是约1至约10,000;
o是约0至约10,000;
p是约1至约10,000;
q是约0至约10,000;并且
r是约1至约10,000。
在一些实施方式中,嵌段共聚物具有式(ii),其中
m是约1至约10,000;
n是约0至约10,000;
o是约1至约10,000;
p是约1至约10,000;
q是约0至约10,000;并且
r从约1至约10,000。
在一些实施方式中,如果r是0,那么t2是膜裂解肽、治疗性肽、核酸或核酸衍生物(即并非不存在)。在另一个实施方式中,如果r是0,那么膜裂解肽、治疗性肽、核酸或核酸衍生物可以结合到ph响应性嵌段中(即a4、a5或a6)。
在第二方面,本发明提供一种用于提供根据本文进一步描述的任何共聚物的共聚物的方法。该方法包括将对应于共聚物的单体衍生单元的单体组合并且开始聚合。聚合条件可以选自本领域已知使单体聚合的任何条件,以提供本发明的共聚物。在一些实施方式中,在raft条件下进行聚合。
在第三方面,本发明提供胶束组装物,该胶束组装物包含:根据本文描述的任何共聚物的多种共聚物。在某些实施方式中,胶束组装具有约5nm至约100nm的直径。在某些实施方式中,胶束组装在小于约6.5的ph下分解。
在第四个实施方式中,本发明提供一种药物组合物,该药物组合物包含根据本发明的任何方面的嵌段共聚物和根据本发明的方面的胶束组装中的至少一种;以及与亲水性聚离子嵌段可逆地缔合的治疗剂。在某些实施方式中,治疗剂是核酸分子。在某些实施方式中,治疗剂是蛋白质或肽。
在第五方面,本发明提供一种在细胞内递送治疗剂的方法,该方法包括:向受试者给药本文所述的药物组合物,其中该药物组合物被内吞到核内体中并且因此该药物组合物将治疗剂释放到核内体中。治疗剂可以是能够产生治疗效果以用于治疗疾病或病症的物质。在一些实施方式中,治疗剂是核酸。在一些实施方式中,给药是静脉内、气管内、心室内或肿瘤内皮下。
实施例
设计一种在中性ph下含有隐藏的膜裂解肽的自组装合成聚合物。此聚合物在酸性环境诸如早期核内体中经历构象改变,以显露用于选择性核内体膜破坏的肽。所采用的肽是可插入到脂质膜中并诱导孔形成的蜂毒肽。m.t.tosteson等人.biophysicaljournal,36,109-116。蜂毒肽已缀合至各种阳离子聚合物并且已显示通过促进载体的核内体释放来增强基因转移能力。m.ogris等人.journalofbiologicalchemistry2001,276,47550-47555。
已证实含有蜂毒肽的聚合物,viper,在酸性ph下具有选择性膜裂解能力。viper有效地包装质粒dna以用于递送到各种哺乳动物细胞中,其效率高于商业药剂。最后,显示viper可用于有效进行到肿瘤中的体内基因转移,从而克服对于许多聚阳离子基因递送体系观察到的体外/体内断开连接。
使用可逆添加-片段化链转移(raft)聚合(参见d.s.h.chu等人.accountschemres2012,45,1089-1099)合成viper,其由用于核酸装载的亲水性阳离子嵌段和用于膜裂解肽的触发显示的ph-响应性嵌段组成(图1a)。亲水性阳离子嵌段聚(寡聚(乙二醇)单甲基醚甲基丙烯酸酯)-共-聚(甲基丙烯酸2-(二甲基氨基)乙酯)(p(oegma-dmaema))包括在用于核酸递送的聚阳离子中广泛使用的dmaema以及提供胶体稳定性的亲水性单体oegma。p.vandewetering等人.jcontrolrelease1998,53,145-153;b)h.wei等人.angewchemintedit2013,52,5377-5381。ph-敏感性嵌段聚(甲基丙烯酸2-二异丙基氨基乙酯)-共-聚(甲基丙烯酸吡啶基二硫基乙酯)(p(dipama-pdsema))包括:特征在于在ph6.3下从疏水性到亲水性的急剧相变的ph敏感性聚合物p(dipama))(y.g.wang等人.natmater2014,13,204-212);和能够通过二硫交换反应用含硫醇肽进一步官能化的pdsema单体。共聚物p(oegma11-dmaema56)-b-p(dipama33-pdsema1)(用于进一步研究的对照聚合物,表示为cp)和viper(接枝有蜂毒肽的cp)的成功合成通过该1hnmr(图4)、gpc和uv光谱(图5)表征。
方案1
因此设计viper以在生理ph下与包埋在疏水性核内的蜂毒肽一起自组装成胶束结构。在内吞之后,酸性核内体环境触发了pdipama嵌段的亲水性转变,从而显露蜂毒肽,该肽然后可以通过破坏核内体/溶酶体膜来促进核内体释放(图1b)。
为了验证这种假设的机制,通过透射电子显微镜法(tem)成像和动态光散射(dls)分析来监测viper在ph7.4和ph5.7下的组装行为。viper在ph7.4下组装成直径约30nm的均匀球形纳米颗粒(对于tem和dls分别为图2a和图2c)。然而,在ph5.7下,通过任一种方法均未观察到组装,这表明纳米颗粒在核内体ph下完全解离(图2b和图2c)。此数据证实了viper的ph触发的相变。
接着,进行溶血研究以评价酸触发的蜂毒肽显示。在ph7.4下,在用人类红血细胞温育之后,甚至在高达240μg/ml的viper浓度下都未观察到显著的细胞裂解,证实了在纳米颗粒的疏水性结构域内蜂毒肽的包封和掩蔽(图2d)。在ph5.7下,使用浓度依赖性曲线观察到细胞裂解;用仅30μg/mlviper实现50%裂解并且用120μg/mlviper发生完全裂解。同时,在所有测试条件下对于cp未观察到显著膜裂解,表明膜裂解通过蜂毒肽而不是聚合物骨架引起。
然后使聚合物与质粒dna复合以形成用于基因递送的人工合成多聚物。viper和cp有效地包封质粒dna,在n/p(胺与磷酸)比率为2时完全缩合。viper和cp人工合成多聚物(n/p=5)的tem成像显示了具有相对均匀的球形状和直径<100nm的紧凑结构(图6b和图6c)。dls尺寸测量值与tem图像一致,并且显示在viper与cp复合物之间颗粒尺寸是类似的,并且随着n/p比率逐渐增加而减小(图6d、图7)。当以n/p≥3配制时,viper和cp复合物的表面电荷为正。最后,使用cp/dna和viper/dna人工合成多聚物的溶血研究证实在人工合成多聚物制剂中保持ph-敏感性膜裂解(图7)。在ph.5.7下使用viper/dna人工合成多聚物观察到细胞裂解但在ph74下最少,而cp/dna人工合成多聚物在任一ph下均不是膜活性的。
预期viper中的裂解肽蜂毒肽诱导人工合成多聚物的核内体/溶酶体逃逸。为了评价核内体释放,在确认人工合成多聚物中的yoyo-1荧光在酸性和中性ph下可以检测到之后通过三重荧光共聚焦显微镜追踪yoyo-1标记的viper和cp人工合成多聚物到hela细胞的递送(图8)。在4h温育之后,来自viper人工合成多聚物的大部分绿色荧光(yoyo-1dna)与红色荧光(lysotrackerred)分离,表明viper/dna人工合成多聚物的有效核内体/溶酶体逃逸。相反地,在用cp人工合成多聚物处理的细胞中观察到绿色荧光和红色荧光的几乎完全的共位(黄色)。与cp人工合成多聚物(72.2%)相比较,viper人工合成多聚物与溶酶体的共位比率仅为9.4%。我们先前的工作显示,bpei人工合成多聚物显示与cp人工合成多聚物类似的细胞内分布轮廓,表明核内体捕获。e.j.kwon,j.m.bergen,s.h.pun,bioconjugatechemistry2008,19,920-927。值得一提的是,在cp/dna与viper/dna复合物之间的细胞摄取效率方面未观察到显著差异,根据通过流式细胞术所测定的(图8)。因此,viper人工合成多聚物与cp相比提供核酸货物在哺乳动物细胞内的显著改进的核内体释放。
接着,在固定化哺乳动物细胞系(hela和kb宫颈癌、a549肺癌和z310脉络膜上皮细胞)小组中使用报告基因荧光素酶质粒测试cp和viper人工合成多聚物的体外基因递送效率。将聚阳离子标准物分支pei(bpei,25kda)和商业转染试剂脂质体转染胺(lipofectamine)2000(lf)用于比较。在所有测试的细胞系中,通过viper转染获得的荧光素酶活性的数量级高于通过cp和bpei获得的荧光素酶活性(图9)。在hela细胞、kb细胞和z310细胞中,与优化的lf制剂相比,viper还介导改进的转染效率。viper人工合成多聚物为良好耐受型的;在所有细胞类型中在所有测试的n/p比率下细胞活力保持>90%(图9)。然后使用携带绿色荧光蛋白基因(gfp)的报告基因质粒重复转染实验,以确定转染细胞百分比。对于所有细胞系观察到与荧光素酶实验相同的转染趋势。viper与cp相比转染13至60倍多的细胞并且与bpei相比转染11至46倍多的细胞,其效率范围为36%-77%gfp+细胞。
基因疗法被认为是一种治疗各种恶性肿瘤的强效方法,并且多个基于聚阳离子的基因载体已进入不同的临床阶段。h.yin,r.l.kanasty,a.a.eltoukhy,a.j.vegas,j.r.dorkin,d.g.anderson,natrevgenet2014,15,541-555。为了研究viper作为治疗癌症的基因载体的可能性,评价在kb和a549异种移植肿瘤模型中通过将含有人工合成多聚物的荧光素酶质粒直接递送至实体肿瘤来进行的体内基因转移。viper和bpei人工合成多聚物具有核内体逃逸的膜裂解肽(viper)和质子海绵(bpei)机制,其与cp相比将质粒有效地递送至kb肿瘤,这通过其在肿瘤部位中的强生物荧光来确认(图3a)。用viper人工合成多聚物治疗的肿瘤显示最高的荧光素酶活性,分别是bpei和cp人工合成多聚物治疗组的3.1倍和82.5倍(图3b)。viper人工合成多聚物还在肿瘤内基因转移至a549异种移植肿瘤方面分别胜过bpei和cp人工合成多聚物15.1倍和59.7倍(图3c和图3d)。这些结果证实,viper可以有效地介导到分裂细胞中的体外和体内基因转移。
捕获在核内体/溶酶体媒介物内是递送大部分具有细胞内靶标的大分子药物中的主要障碍。对于基因转移,溶酶体核酸酶诸如dna酶(脱氧核糖核酸酶)ii降解核酸,从而损害基因转移效率。d.pinto-gonzalezhowell等人.molther2003,8,957-963。为了解决此问题,已开发多种体系,诸如质子海绵效应和合成膜活性肽或病毒来源的膜活性肽的使用。然而,一些先前的工作已揭示单独的“质子海绵效应”对于核内体/溶酶体逃逸而言是不够的。y.y.won等人.jcontrolrelease2009,139,88-93。尽管裂解肽与聚阳离子载体的直接缀合改进了转染效率,但是显著细胞毒性通常与肽相关联。例如,我们先前的工作显示,将蜂毒肽或shgp肽结合到聚阳离子由于裂解肽在生理条件下的暴露和浆膜的去稳定性而导致细胞毒性。e.j.kwon等人.molecularpharmaceutics2010,7,1260-1265;j.g.schellinger等人.biomaterials2013,34,2318-2326。
为了解决细胞毒性对抗转染效率的困境,wolff和wagner组开发了掩蔽的蜂毒肽制剂,由此蜂毒肽通过马来酸酐衍生物被可逆地封阻,使得肽在中性ph下无活性并在酸性核内体ph下通过酸酐加帽基团的水解来活化。m.meyer等人.journaloftheamericanchemicalsociety2008,130,3272-3273;b)d.b.rozema等人.bioconjugatechemistry2003,14,51-57。掩蔽的蜂毒肽物质当与sirna胆固醇共注射时介导了有效的递送,c.i.wooddell等人.molther2013,21,973-985,但是缀合至蜂毒肽的聚阳离子和sirna当体内给药时显示肝毒性。m.meyer等人.molecularpharmaceutics2009,6,752-762。虽然有效,但酸酐保护基团容易水解,虽然以减小的速率,但即使在生理ph下就水解,这降低了该材料的稳定性和保质期。相比之下,viper中的膜裂解肽通过在胶束核心内疏水性包封来掩蔽,直到通过嵌段共聚物中ph触发的开关来暴露。因此,ph-敏感性聚合物充当响应鞘以遮蔽“蜂毒肽剑”。viper在ph7.4下展示最小的膜裂解活性,表明蜂毒肽在中性条件下的有效灭活,但是在酸性条件下变成膜裂解性的(图2d)。因此,viper人工合成多聚物也可以在内在化的4小时内有效地逃出核内体/溶酶体隔室(图3)。
viper也具有其他显著的优势。首先,oegma的共聚单体改进了人工合成多聚物的稳定性,从而预防了生理条件下盐诱导的絮凝,这对于在体内给药之后使毒性最小化是必需的(图6)。第二,pdipama嵌段不仅充当蜂毒肽灭活的遮蔽部分,而且还用作一种增强人工合成多聚物的稳定性的有效方法。聚阳离子的疏水性改性已证实与亲本聚阳离子相比改进了血液循环时间和转染效率,同时减小了细胞毒性并促进基因载体的总体生物可降解性。m.thomas等人.pnatlacadsciusa2002,99,14640-14645。viper/dna人工合成多聚物在血清减少的介质中与在蒸馏水中相比不会显示明显的尺寸改变,并且维持其尺寸达20h(图6)。另外,肿瘤内递送研究证实,viper人工合成多聚物在肿瘤部位中与bpei人工合成多聚物相比介导高得多的基因表达(图3)。因此,viper用于体内基因递送的可能性可以提供用于癌症治疗的有用平台。
总之,公开了促进核内体释放的模拟病毒的嵌段共聚物,称为viper。此聚合物有效地介导体外和体内基因转移。裂解肽蜂毒肽的酸触发的显示有效地介导了viper人工合成多聚物的核内体/溶酶体逃逸,同时在细胞外条件下遮蔽了蜂毒肽活性。viper因此展示了低细胞毒性和强效核内体逃逸特性并且具有作为用于大分子治疗剂的递送媒介物的强可能性。
实验部分
材料。甲基丙烯酸2-(二甲基氨基)乙酯(dmaema)和寡聚(乙二醇)单甲基醚甲基丙烯酸酯(oegma,mn=300和侧接eo单位dp4~5)购自sigma-aldrich,并且单体通过穿过用碱性氧化铝填充的柱来纯化以在聚合之前去除抑制剂。raftcta4-氰基戊酸二硫代-苯甲酸酯(cpadb)、n,n’-偶氮双异丁腈(aibn)、无水n,n’-二甲基乙酰胺(dmac,hplc,99.9%)和二噁烷购自sigma-aldrich并且未进一步纯化即使用。如先前所述地合成甲基丙烯酸吡啶基二硫基乙酯。meyer,c.等人.molecularpharmaceutics2009。甲基丙烯酸2-二异丙基氨基乙酯(dipama)购自scientificpolymerproductscompany并且通过穿过碱性氧化铝来纯化。半胱氨酸-蜂毒肽(mel-cys;nh2-gigavlkvlttglpaliswikrkrqqcconh2)已根据我们先前的工作来制备。16b无内毒素质粒pcmv-luc(在巨细胞病毒(cmv)增强子/启动子控制下的萤火虫荧光素酶)使用qiagenplasmidgiga试剂盒(qiagen,hilden,germany)根据制造商的建议来产生。yoyo-1碘化物和脂质体转染胺2000(lf)购自invitrogen(carlsbad,ca)。
细胞系。将hela细胞(atccccl-2tm)和kb细胞(atccccl-17)保持在最小必需培养基(mem)中,该培养基补充有10%胎牛血清(fbs)和抗生素/抗真菌剂(antibiotics/antimyotics,abam)(100iu青霉素、100ug/ml链霉素和0.25ug/ml两性霉素b)。将a549细胞(atccccl-185)保持在f-12k培养基中,该培养基补充有10%胎牛血清(fbs)和抗生素/抗真菌剂(abam)(100iu青霉素、100ug/ml链霉素和0.25ug/ml两性霉素b)。z310细胞由weizheng教授(purdue)捐赠并且在dulbecco氏最小必需培养基(dmem)中培养,该培养基补充有10%热灭活fbs、10%青霉素/链霉素、40mg/ml庆大霉素和10ng/ml神经生长因子(ngf)。
表征。在氘代氯仿(cdcl3)中在brukerav300(brukercorporation,billerica,ma)核磁共振(nmr)仪器上记录1hnmr质谱。通过尺寸排除色谱法确定聚合物的分子量和分子量分布(pdi)。为了制备用于分析的材料,将纯化的聚合物以10mg/ml溶解于运行缓冲液(用乙酸缓冲至ph4.4的0.15m乙酸钠)中,以用于通过sec进行分析。然后将样品施加于ohpaksb-804hq柱(shodex),该柱与minidawntreos光散射检测器(wyatt)和optilabrex折射率检测器(wyatt)联用。使用astra软件(wyatt)计算绝对分子量平均值(mw和mn)。
p(oegma-dmaema)的分析。通过raft聚合对oegma和dmaema进行聚合广泛可见。thomas等人.pnatlacadsciusa2002。简言之,将oegma(1.0g,3.44mmol)、maema(2.7g,17.2mmol)、aibn(9.5mg,0.058mmol)和cpadb(80mg,0.29mmol)溶解于5ml二噁烷中。在用氩气吹扫10min之后,将反应混合物在60℃油浴中搅拌18h。通过将反应烧瓶浸入在液氮中来淬灭该聚合。在解冻之后,使该溶液在醚中沉淀。通过离心来分离聚合物并且通过用dcm/醚重新溶解/重新沉淀三次来进一步纯化。
p(oegma-dmaema)-b-p(dipama-pdsema)的合成。使用p(oegma-dmaema)作为大分子cta制备嵌段共聚物p(oegma-dmaema)-b-p(dipama-pdsema)。首先将p(oegma11-dmaema56)(80mg,0.0066mmol)、dipama(282mg,1.32mmol)、pdsema(17mg,0.066mmol)和aibn(0.36mg,0.0022mmol)溶解于1.32mldmac中。在用氩气吹扫5min之后,将反应溶液浸入在60℃油浴中。在30min之后,使用液氮淬灭该聚合。通过针对甲醇的透析两天来纯化聚合物。
将cys-蜂毒肽缀合至p(oegma11-dmaema56)-b-p(dipama33-pdsema1)。通过根据我们先前的工作所述的二硫交换反应来将cys-蜂毒肽缀合至该嵌段共聚物。meyer,c.等人.molecularpharmaceutics2009。将p(oegma11-dmaema56)-b-p(dipama33-pdsema1)(20mg,0.001mmolpds基团)在10ml烧瓶中溶解于2mlpb缓冲液(0.2m,ph5.7)中。然后,将6.1mg(0.002mmol,相对于pds基团的2当量)的cys-蜂毒肽添加到烧瓶中并且允许在氩气下在室温下搅拌。通过在340nm下的uv监测反应的2-硫代-吡啶释放。在20h之后,使吸收饱和并且使反应混合物穿过pd-10柱以去除副产物和未反应的肽,之后冻干。共聚物的表征呈现于表1中。
表1
a通过1hnmr测定;b通过gpc获得。
聚合物溶血使用溶血测定评价合成的材料在ph7.4(细胞外ph)和5.7(核内体ph)下的酸触发的膜裂解活性。简言之,通过离心去除人类血液中的血浆。将红血细胞用150mmnacl洗涤三次,并且将其重悬浮到ph7.4或5.7的磷酸盐缓冲液(pb)中。将各种浓度(7.5-240μg/ml)的聚合物和作为对照物的1%tritonx-100添加到96孔锥形板中的rbc悬浮液中并且允许在37℃下温育1h。在离心之后,通过uv在541nm下测量上清液内释放的血红蛋白。相对于tritonx-100计算溶血百分比。将实验重复进行三次。
dna人工合成多聚物的制备和表征。通过将聚合物添加到dna溶液中随后在室温下温育30分钟来形成聚合物/dna人工合成多聚物。对于凝胶滞后研究,将具有不同n/p比率的人工合成多聚物装载到含有1%琼脂凝胶的tae缓冲液(40μmmtris-乙酸酯、1mmedta)和5mg/ml溴化乙锭中,在100v下经电泳40min。然后使用kodak(rochester,nk)uv透照器(激光激发荧光凝胶扫描仪)使pdna可视化。
在zetaplus仪器(brookhaveninstrumentscorporation,holtsvile,ny)上测试人工合成多聚物的尺寸和表面电荷。通过将人工合成多聚物(1μgdna,20μl溶液,n/p=5)与800μlddh2o混合来制备样品。将测量重复进行三次。
透射电子显微镜(tem)。在jeol1140tem上在100kv加速电压下对干燥状态下的聚合物和人工合成多聚物的形态进行成像。为了观察到在不同ph下聚合物组装物的形态,将聚合物溶液(1mg/ml,在蒸馏水中)用pb稀释至ph7.4和5.7。然后将所得溶液(10μl)沉积在400-目聚醋酸甲基乙烯酯/铜网格的顶部上并且在室温下温育30min。在用乙酸铀酰染色之后,使网格晾干过夜。人工合成多聚物样品的制备与聚合物样品相同。
体外细胞研究。
永生化细胞/癌细胞中的转染。将hela细胞、kb细胞、z310细胞和a549细胞以25,000个细胞/孔的密度接种在24孔板中的完全细胞培养基中。首先将细胞在37℃、5%co2下温育24h。在10μl总体积中使用0.5μgpcmv-luc2pdna制备不同n/p比率的人工合成多聚物。将每个样品用完全细胞培养基稀释至200μl。将细胞用pbs冲洗一次,接着添加转染溶液。在温育4h之后,将细胞用pbs洗涤两次并且将人工合成多聚物溶液用完全细胞培养基替换。在另外20h温育之后,根据制造商说明书使用荧光素酶测定试剂盒(promegacorp,fitchburg,wi)量化荧光素酶活性,不同之处在于,在添加裂解缓冲液以确保完全细胞裂解之后包括-80℃下的冷冻-解冻循环。在集成的板读取器上测量荧光强度1s。通过bca蛋白测定试剂盒(thermoscientific,rockford,il)根据制造商说明书测量每个孔中的总蛋白含量,使得荧光素酶活性被归一化至每个孔中的总蛋白含量。测试每个样品,其中样品大小(n)=3。用于bpei的n/p比率为5,其先前被确定为显示优化的转染效率。在无血清培养基中根据制造商说明书使用lf。
gfp转染。用gfp(绿色荧光质粒)对不同细胞系的转染与用荧光素酶质粒的转染相同。对于分析,将细胞用pbs洗涤,使其胰蛋白酶化并在4℃下在300×g下5min使其丸粒化。将丸粒重悬浮于0.3ml碘化丙啶(pi)溶液((1μg/ml,在pbs中的0.5%bsa中),将其保持在冰上并且使用流式细胞术、macsquant分析仪(miltenyibiotecinc.,auburn,ca)分析。使用正向和侧向散射数据鉴别完整细胞。基于绿色荧光和来自对照样品(没有聚合物转染但仅有dna的细胞)的pi强度,将所得细胞群门控成gfp+/pi+、gfp+/pi-、gfp-/pi+和gfp-/pi-,并且将其报告为gfp+/pi-细胞群的平均值百分比,包括标准偏差(sd)。将所有实验重复进行三次。
通过共聚焦显微镜获得的人工合成多聚物的核内体逃逸。为了评价基于蜂毒肽-聚合物的人工合成多聚物的核内体逃逸能力,首先将dna用yoyo-1标记。将细胞用人工合成多聚物温育4h。分别用lysotrackerred、dnd-99和4',6-双脒基-2-苯基吲哚(dapi)染色细胞的酸性囊泡和细胞核。为了量化人工合成多聚物的核内体逃逸比率,使用imagej软件如下量化dna与lysotrackerred之间的共位比率:
在yoyo-1像素共位表示与lysotrackerred共位的yoyo-1像素的数量,并且yoyo-1像素总和表示共聚焦显微镜图像中的全部yoyo-1像素的数量。结果呈现为15个单个细胞的平均值。
肿瘤内基因递送。使用华盛顿大学机构动物护理和使用委员会批准的方案进行所有动物程序。对于a549肿瘤接种,将100μla549细胞悬浮液(f12培养基中的2.0×106个细胞)皮下注射到雌性scid-beige(cb17)小鼠(4-5周龄)中。当肿瘤大小达到100mm3时,将5%葡萄糖溶液(含有10μg荧光素酶质粒)中的50μl人工合成多聚物(cp/dna、viper/dna、bpei/dna)注射到小鼠中。对每只小鼠重复给药三天。在第四天,将200μld-荧光素钾盐(15mg/ml)腹膜内注射到小鼠中。在注射后5min,将小鼠放置到体内成像系统(xenogenivis-200,caliperlifesciences,hopkinton)中,并且以2min的曝光时间记录肿瘤部位处的发光。从小鼠收获肿瘤组织并且收集在补充有蛋白酶抑制剂(roche,nutley,nj)的裂解缓冲液中并且在液氮中进行三次冷冻解冻循环。将组织机械均质化并且通过在4℃下在21,000g下旋转15min来清除裂解物。用100μl荧光素酶底物测定20μl裂解物的发光。测量发光并且通过三个大脑切片中的蛋白质含量进行归一化,使用bca蛋白测定试剂盒(pierce)测定,并且报告为每mg大脑的相对光单位(rlu)。
统计学分析。使用双尾student氏t检验进行所有统计学分析,具有不等方差。
示例性共聚物的合成
使用羧基官能化链转移剂,通过可逆加成-片段化链转移(raft)聚合来制备官能聚合物以用于进行靶向肽递送。亲水性嵌段聚(寡聚(乙二醇)单甲基醚甲基丙烯酸酯)-共-聚(甲基丙烯酸吡啶基二硫基乙酯)(p(oegma-pdsema))包括通过二硫交换反应用于含硫醇肽货物缀合的pdsema和提供胶体稳定性的亲水性单体oegma。ph-敏感性嵌段聚(甲基丙烯酸2-二异丙基氨基乙酯)-共-聚(甲基丙烯酸2-叠氮基乙酯)(p(dipama-aema))包括特征在于在ph6.3下从疏水性到亲水性的急剧相变的ph敏感性聚合物p(dipama))和能够通过点击化学用含炔基裂解肽进一步官能化的aema单体。末端羧基基团可以用于通过nhs化学进行靶向基团缀合(方案2)。
方案2
使用羧基官能化链转移剂,通过可逆加成-片段化链转移(raft)聚合来制备官能聚合物以用于进行靶向肽递送。亲水性嵌段聚(寡聚(乙二醇)单甲基醚甲基丙烯酸酯(p(oegma))包括提供胶体稳定性的亲水性单体oegma。ph-敏感性嵌段聚(甲基丙烯酸2-二异丙基氨基乙酯)-共-聚(甲基丙烯酸2-叠氮基乙酯)-共-聚(甲基丙烯酸吡啶基二硫基乙酯)(p(dipama-aema-pdsema))包括特征在于在ph6.3下从疏水性到亲水性的急剧相变的ph敏感性聚合物p(dipama))、能够通过点击化学用含炔基裂解肽进一步官能化的aema单体、以及用于通过二硫交换反应进行含硫醇肽货物缀合的pdsema。末端羧基基团可以用于通过nhs化学进行靶向基团缀合(方案3)。方案3
- 还没有人留言评论。精彩留言会获得点赞!