用于通过疗法在治疗人体的方法中使用的、包含物种姜花植物提取物的组合物与流程
姜花属(hedychium)是姜科(gingerfamily,zingiberaceae)开花植物的一个属。大约有七十到八十种已知物种,其原产于东南亚(泰国、马来西亚、印度尼西亚、菲律宾等)、中国南部、喜马拉雅山脉和马达加斯加岛。一些物种已在其他土地(南非,南美洲,中美洲,西印度群岛,以及太平洋、印度洋和大西洋的许多岛屿)广泛归化。属名姜花属(hedychium)来源于两个古希腊词,hedys意指“甜”,并且chios意指“雪(snow)”。这是指模式种姜花的芳香白花。俗名包括花环花(garlandflower)、野姜花(gingerlily)和蝴蝶姜(kahiliginger)。
姜花属的成员是多年生根茎植物,通常生长到从120cm至180cm高。有些物种是因为其异国情调的叶子以及白色、黄色和橙色色调花的芳香穗而栽培的。已经开发了用于花园用途的许多栽培品种。选择的物种包含例如橘黄姜花(hedychiumaurantiacum)、红姜花(hedychiumcoccineum)、姜花、密花姜花(hedychiumdensiflorum)、椭圆状姜花(hedychiumellipticum)(剃须刷姜(shavingbrushginger))、黄花钩藤(hedychiumflavescens)、金姜花(hedychiumgardnerianum)(野姜花(gingerlily))、hedychiumsamuiense、和在北印度称作kapurkachari的草果药(hedychiumspicatum)。
个体物种在他们的个体生物分类学中彼此不同,并且在一些情况下也与它们的起源有关。
物种姜花(也称为“姜蝴蝶(gingerbutterfly)”)于1783年由johanngerhardkoenig在andreajohanretzius“observationesbotanicae[植物观察]”一书第3章第73-74页中首次描述。
物种草果药(也称为“野头姜(wild-headedginger)”)由jamesedwardsmith(1811)首次记录,并且然后由francisbuchanan-hamilton于1819年在abrahamrees“thecyclopaedia;universaldictionaryarts,sciencesandliterature.”[百科全书;艺术、科学和文学通用字典]第17章第521-522页的作品中描述。
姜花属已被广泛描述用于传统医学,如描述于例如“ediblemedicinalandnonmedicinalplants[食用药用和非药用植物]”,第8卷flowers[花],第853-860页,或描述于“medicinalplantsusedbywomenfromagnalazahalittoralforest(south-easternmadagascar)[agnalazaha海岸林(马达加斯加东南部)妇女使用的药用植物]”,journalofethnobiologyandethnomedicine[民族生物学和民族医学杂志],2013,以及由x.yan,等人“traditionalchinesemedicines,molecularstructures,naturalsources,andapplications[传统中药、分子结构、天然来源和应用]”,1999或由sharma等人“phytochemistry[植物化学]”,14:578,1975中。
wo2002/056859a2披露了涉及包含姜花属提取物的组合物及其化妆品用途。然而,所述国际申请特别描述了物种草果药的用途,以及在一个方面,描述了草果药在调节皮肤紧致性、肤色或肌理方面的活性,以及在另一方面,描述了草果药基于抑制uv诱导的金属蛋白酶-1(mmp-1)分泌的潜在机制,在皮肤环境损害的治疗中的用途,防止烟雾诱导的硫醇损失以保护作为内源性细胞抗氧化剂防御系统的一部分的谷胱甘肽的用途,以及抑制作为有害活性氧簇(ros)形成的前体的一氧化氮产生的用途。
brpi0905586-0a2描述了来源于植物的花的姜花提取物用于保湿、活肤和再生皮肤的化妆品用途。此外,提到了由于花中高浓度的黄酮类产生的抗老化作用,连同抗炎和抗过氧化剂活性、和微小血管和毛细血管的强化、以及对抗水肿和光诱导的红斑形成的特性。
wo2006/053415a1提到了若干种植物提取物在化妆品应用中的适合性,包括利用抑制mmp-1、mmp-2、mmp-3、mmp-9、hle(人白细胞弹性蛋白酶)的机制的应用。然而,其中姜花属植物提取物仅在大量可能的植物清单中非常普遍地提及,并且没有描述或示出任何姜花属物种的特定效果。
根据第一实施例,本发明涉及包含物种姜花的植物提取物的组合物,用于通过疗法在人体的治疗方法中使用,例如特别用于防护和/或治疗皮肤的环境损害,并且更特别地,用于通过疗法在人体的治疗方法中使用以保护和/或活化至少一个细胞清除系统。
环境损害意指如来自毒素和/或污染(包括废气、工业污染、农业污染和香烟烟雾)的有害影响的任何有害的环境影响,以及有害辐射(如uv辐射(例如来自太阳或非天然来源,包括uv灯和太阳模拟器)),以及臭氧。
如本文使用的,“防护环境损害”意指预防和/或减少来源于有害环境影响的症状或有害影响。
如本文使用的,“环境损害的治疗”意指减少、缓解、改善和/或消除来源于有害环境影响的症状或损害。
如本文使用的,细胞清除系统包含细胞代谢的细胞系统(下文也称为“细胞代谢系统”)和胞内屏障系统的细胞系统,这对于提供活细胞和完整细胞是必需的,并且构成了活细胞和有活力的细胞的另一个关键要素,以及构成了抵御有害的环境影响的有效的细胞防御系统。其中,细胞代谢系统和胞内屏障系统的细胞系统特别地包含以下系统:
-产生大部分细胞的三磷酸腺苷(atp)供应的线粒体被用作化学能量的来源,并且因此代表细胞的所谓的能源供应。除了提供细胞能量外,线粒体还涉及一系列其他关键细胞过程,如信号传导,生热作用,细胞分化,细胞分裂周期和细胞生长的控制,细胞死亡(凋亡),氧化代谢,糖类、脂质、钙、铁(血红素合成)等的内稳态。
-溶酶体是细胞质的细胞器,其允许超过细胞材料寿命或不再有用的细胞材料的再循环。它们的主要功能是在所有真核细胞中消化内源或外源底物(所谓的自体吞噬或异体吞噬)。溶酶体将细胞废物、脂肪、碳水化合物、蛋白和其他大分子分解成简单的化合物,然后作为新的细胞构建材料转移回细胞质。实际上,它的脂质膜含有许多酶(约40种不同类型的水解酶)、质子泵和转运蛋白。调节酸性ph以允许酸性水解酶的最佳活性(因此溶酶体就像细胞的胃)。自体吞噬是一种重要的机制,该机制允许细胞动员其能量储备来防御和破坏其受损的细胞器,并且然后避免严重的效果。此过程允许蛋白和非功能性细胞器的消除和替换,然后以确保内稳态。它涉及寿命控制和如癌症或糖尿病等病理学的发展。
-特别地包含细胞跨膜系统的胞内屏障系统在细胞的细胞清除系统中起重要作用,因为细胞跨膜系统控制并影响来自线粒体的代谢能量产物和来自溶酶体的代谢废物的运输,并且因此在对于提供活细胞和完整细胞是必需的有效和功能性细胞代谢中起关键作用。强而完整的跨膜系统包含所谓的“紧密连接”,即在细胞之间建立的连接(细胞-细胞连接)。这些连接由若干个跨膜蛋白家族(如密蛋白(claudin)、闭合蛋白和粘附分子(zo-1、zo-2、zo-3……))构成。皮肤组织(包括表皮层)中存在紧密连接。密蛋白1和4是在表皮上层(角质化细胞分化的地方)中发现的蛋白。免疫染色研究表明这些标志的存在,并且这些蛋白通过控制上皮细胞的细胞之间细胞间隙中分子的流动、以及通过阻断小分子的进入和通过维持表皮的上层的完整性(角质细胞之间增强的内聚力),参与细胞旁路皮肤屏障。此外,密蛋白在角质层的内稳态和钙梯度的控制中起作用。紧密连接的损害导致由于增加的钙通量和扰乱的梯度而导致的皮肤屏障的损害,导致分化改变并最终导致皮肤屏障保护的损害。
-细胞代谢系统的另一个重要方面涉及白细胞介素8(il-8)的产生,白细胞介素8是由巨噬细胞和其他细胞类型如上皮细胞和内皮细胞产生的趋化因子。内皮细胞将il-8储存在它们的储存囊泡(weibel-palade小体)中。il-8最初作为99个氨基酸长的前体肽产生,该前体肽然后经历切割以产生若干种活性il-8同种型。il-8是分泌的,并且是先天免疫系统应答中免疫反应的重要介质。il-8(也称为中性粒细胞趋化因子)具有两个主要功能。它在靶细胞(主要是嗜中性粒细胞,还有其他的粒细胞)中诱导趋化性,导致它们向感染位点迁移。il-8一旦到达就会诱导吞噬作用。还已知il-8是血管生成的有效启动子。在靶细胞中,il-8诱导迁移和吞噬作用所需的一系列生理应答,如胞内ca2+的增加、胞吐作用(例如组胺释放)和呼吸爆发。il-8可由具有参与先天免疫应答的toll样受体的任何细胞分泌。通常,巨噬细胞首先看到抗原,并且因此是第一个释放il-8以招募其他细胞的细胞。据报道,单体和同二聚体形式的il-8两者都是趋化因子受体cxcr1和cxcr2的有效诱导物。
-细胞代谢系统的另一个重要方面涉及β-内啡肽的产生。β-内啡肽是神经介质(内源性类阿片),其来源于参与各种生物现象(如皮肤生理和内稳态、神经营养性活性、疼痛、免疫防御、内分泌、情绪和压力应答)的阿黑皮素原(pomc)。在皮肤中,β-内啡肽由角质化细胞分泌并且其受体存在于主要皮肤细胞(角质化细胞、成纤维细胞和黑素细胞)中。因此,据说β-内啡肽在各种皮肤代谢和皮肤防御过程中起重要作用,这些过程包括刺激角质化细胞迁移、参与伤口愈合和细胞分化、诱导表皮和滤泡黑素生成、以及控制毛发生长。此外,增加的β-内啡肽调节毛囊黑素细胞的树突状突起的数量。显而易见的是,功能性细胞代谢系统还需要功能性β-内啡肽产生系统在细胞的细胞清除系统中发挥进一步重要的作用,因此是用于提供活细胞和有活力的细胞以及针对有害的环境影响的功能性细胞防御系统的另一个重要方面。
-除了代谢系统的上述方面之外,另一方面涉及细胞的黑素生成,即通过黑素细胞在细胞中产生黑素。黑素是在皮肤、眼和毛发中发现的色素,因此负责皮肤颜色。黑素细胞位于表皮的基底层。黑素细胞是与角质化细胞连接的树突细胞,在角质化细胞中它们传递含有黑素的特定的细胞器、黑素体。黑素生成包括两个步骤:黑素合成并且然后转移到角质化细胞。黑素在黑素细胞的黑素体、来自高尔基体和粗面内质网的细胞器中合成。黑素的合成由酪氨酸酶催化的氨基酸酪氨酸产生。酪氨酸与二羟苯丙氨酸(dopa)反应,然后将其氧化成多巴醌。在若干个另外的化学反应步骤之后,最终形成黑素。在黑素细胞内,黑色素被捕获在“袋”中,然后黑素体被送到表面。黑素细胞具有树突延伸,这允许它们与若干种角质化细胞接触。黑素体从产生它们的细胞体运输到树突的末端(它们积聚在那里并转移到相邻的、其中分散有黑素的角质化细胞)。通常,黑素生成导致持久的色素淀积,这与源自已经存在的黑素的氧化的色素淀积形成对比。黑素生成有基底水平和活化的水平。通常,较浅肤色的人具有黑素生成的较低的基底水平。暴露于uv-b辐射导致黑素生成增加。黑素生成的目的是保护皮下组织(皮肤下的层)免受可能损害它的uv-b光(dna光损害)。黑素的颜色是深色的,允许它吸收大部分的uv-b光并且阻断它穿过该皮肤层。许多刺激能够通过培养的黑素细胞改变黑素生成或黑素的产生,尽管其工作方法尚不完全清楚。有害环境影响(如有毒污染物和uv辐射)也可能触发黑素生成,进而导致色素淀积。关于其保护功能,功能性黑素生成合意地提供了皮肤的恒定和均匀的色素淀积。由于有害的环境影响,有活力的细胞的黑素生成可能会恶化并导致形成不希望的斑点样色素淀积,并且还导致黑色素瘤(也称为恶性黑色素瘤)的形成,黑色素瘤是最危险的皮肤癌类型,并且是从含有色素的黑素细胞发展而来的。黑色素瘤的主要原因是具有低水平皮肤色素的那些人暴露于紫外线(uv)。显而易见的是功能性细胞代谢系统还需要有活力且具功能的黑素生成系统,导致皮肤的恒定和均匀的保护性色素淀积并且避免不希望的斑点样色素淀积,并且特别是黑色素瘤的形成。因此,功能性黑素生成在细胞的细胞清除系统中发挥进一步重要的作用,因此是用于提供活细胞和有活力的细胞以及针对有害的环境影响的功能性细胞防御系统的另一个重要方面。
从上述解释中特别明显的是,有活力且具功能的细胞需要用于有活力且具功能的细胞防御系统的强大的细胞清除系统,用于对抗有害环境影响,其中这种细胞清除系统特别基于有活力且具功能的细胞代谢系统,该系统具有功能性线粒体、溶酶体、il-8产生、β-内啡肽产生、黑素生成和强而完整的细胞跨膜系统的关键元件的最佳相互作用,根据本发明,它们一起形成细胞的细胞清除系统。
因此,本发明涉及如上所定义的组合物,其中所述清除系统选自线粒体保护和/或活化、溶酶体保护和/或活化、细胞il-8释放的抑制、β-内啡肽的细胞产生、不规律黑素释放的抑制、以及通过密蛋白修复进行的细胞跨膜系统的保护和/或活化。
在本发明的上下文中,术语“提取物”意指由物种姜花植物的植物相似或不同部分的提取获得的物质。根据本发明的提取物是从植物的一个或多个提取部分分离的化合物的共混物。
根据具体实施例,所述物种姜花的植物提取物来源于植物的花、种子、果实、叶、茎、根和/或根状茎;并且更特别地,来源于植物的根和/或根状茎。
本发明的组合物可进一步包含至少一种溶剂和/或至少一种局部可接受的辅助物质。
合适的溶剂的实例包括低级c1-c8-醇、c1-c8-烷基多元醇、c1-c8-烷基酮、c1-c8-烷基醚、乙酸、c1-c8-烷基酯、氯仿、和/或无机溶剂(如水、无机酸如盐酸、和无机碱如氢氧化钠)、及其混合物。
优选的溶剂包括乙醇、1-丙醇、异丙醇、乙酸乙酯、乙酸丁酯、甘油、丙二醇、液体聚乙二醇等、及其混合物。最优选的是乙醇、水、和甘油、及其混合物。
如上文所定义的物种姜花的植物提取物具有范围从0.05%至5.0%(重量/体积)、更优选的0.1%至3.0%(重量/体积)、甚至更优选的0.2%至2.0%(重量/体积)的浓度。
化妆品上可接受的辅助物质包括:
-ph调节剂,如缓冲物质;
-无机和有机酸或碱,包含所有化妆品上可接受的、本领域技术人员熟知的无机和有机酸;
-脂肪物质,如矿物油(例如石蜡油或凡士林油、硅油)、和植物来源的油(如椰子油、甜杏仁油、杏油、玉米油、荷荷巴油、橄榄油、鳄梨油、芝麻油、棕榈油、桉树油、迷迭香油、薰衣草油、松油、百里香油、薄荷油、小豆蔻油、橙花油、大豆油、糠油、米糠油、菜籽油和蓖麻油、小麦胚芽油和从其中分离的维生素e、月见草油);动物油或脂肪,如牛脂、羊毛脂、澄清奶油、以及中性油(miglycol812)、角鲨烷、脂肪酸酯、脂肪醇酯(如甘油三酯)、以及所谓的基础润露(basiccream,“basiscreme”)dac,dac是根据germancodexformedicaments(deutscherarzneimittelcodex)[德国医药法典(德国阿尔茨内密特法典)]的重要基础组合物,包含单硬脂酸甘油酯、鲸蜡醇、中链甘油三酯、白凡士林、聚乙二醇-1000-甘油单硬脂酸酯、丙二醇和纯化水,以及
-植物卵磷脂(例如豆磷脂),从植物中分离的鞘脂/神经酰胺,
-具有对应于皮肤温度的熔点的蜡质物质,如蜂蜡、巴西棕榈蜡和小烛树蜡、微晶蜡、聚乙烯或硅酮蜡、以及特别适用于局部应用的所有油和蜡,例如像在ctfapublicationcosmeticingredienthandbook[ctfa出版化妆品成分手册],第1版,1988,thecosmetic,toiletryandfragranceassociation,inc.[化妆品、化妆用具和香料协会公司],华盛顿中提及的那些;
表面活性剂,如分散剂、润湿剂、乳化剂等;
-填料;
-稳定剂;
-共溶剂;
-染料和色素;
-防腐剂;
-保湿剂;
-抗氧化剂;
-防uv剂;
-软化剂;
-润滑剂或增滑剂;
-皮肤调节剂。
优选的辅助剂选自下组,该组由以下组成:抗氧化剂、保湿剂、软化剂、皮肤调节剂、脂肪物质(如特别是化妆品脂肪和油),以及防uv剂。
通常,在本发明的上下文中将上述物质分类为辅助物质的分类并不排除这些辅助物质也可以展现出某种活性的事实,这在某种程度上特别适用于具有保湿和脂质补充效果的油和其他辅助剂。
本发明的组合物可进一步包含至少一种另外的化妆品活性剂。在本发明的上下文中,化妆品试剂或使用化妆品活性组合物制备的试剂基本上是德国食品和饲料代码[德语=lfgb]意义上的试剂,即旨在用于人皮肤护理剂、清洁、护理或用于影响外观或体臭、或用于赋予有气味的印象的外用物质或物质的配制品,它们主要旨在用于缓解或消除疾病、痛苦、身体损害或病理症状时除外。化妆品活性剂的实例通常包括:抗痤疮剂、抗微生物剂、止汗剂、收敛剂、除臭剂、脱毛剂、皮肤调节剂、皮肤平滑剂、用于增加皮肤水合作用的试剂(例如像甘油或脲)、防晒剂、角质软化剂、用于自由基的自由基清除剂、抗皮脂溢剂、去头屑剂、抗菌活性化合物、用于治疗皮肤老化迹象的活性化合物和/或调节皮肤分化和/或增殖和/或色素淀积的试剂、维生素(如维生素c(抗坏血酸))及其衍生物,例如像苷类(如抗坏血酸葡萄糖苷)、或抗坏血酸酯(如抗坏血酸磷酸钠或抗坏血酸磷酸镁或抗坏血酸棕榈酸酯和抗坏血酸硬脂酸酯、l-抗坏血酸磷酸酯)、l-抗坏血酸磷酸酯的碱金属盐(如钠盐和钾盐);l-抗坏血酸磷酸酯的碱土金属盐(如镁盐和钙盐);l-抗坏血酸磷酸酯的三价金属盐(如铝盐);l-抗坏血酸硫酸酯的碱金属盐(如l-抗坏血酸硫酸酯的钠盐和钾盐);l-抗坏血酸硫酸酯的碱土金属盐(如镁盐和钙盐);l-抗坏血酸硫酸酯的三价金属盐(如铝盐);l-抗坏血酸酯的碱金属盐(如钠盐和钾盐);l-抗坏血酸酯的碱土金属盐(如镁盐和钙盐);以及l-抗坏血酸酯的三价金属盐(如铝盐)、类视黄醇(视黄醇、视黄醛、网织红细胞酸)、地蒽酚(二羟蒽酚(dioxyanthranol))、蒽环类、过氧化物(特别是过氧化苯甲酰)、米诺地尔、锂盐、抗代谢物、维生素d及其衍生物;儿茶酚类,黄酮类,神经酰胺,多不饱和脂肪酸,必需脂肪酸(例如γ-亚麻酸),酶,辅酶,酶抑制剂,保湿剂,皮肤平滑剂,洗涤剂或泡沫形成剂,以及无机或合成消光填料,或装饰性物质(如用于粉底的颜料或染料和彩色颗粒),化妆配制品、以及用于眼、唇、面部等的化妆品装饰和着色造型的其他试剂,和摩擦剂。此外,可以提及植物来源的活性化合物提取物或由其获得的提取物或单独的物质(除了本发明的姜花属提取物之外)。通常,植物活性化合物提取物可选自下组,该组由以下组成:固体植物提取物、液体植物提取物、亲水性植物提取物、亲脂性植物提取物、单独的植物成分;及其混合物,如黄酮类及其糖苷配基:芦丁、槲皮素、洋芫荽苷、金丝桃苷、(新)橙皮苷、橙皮素、银杏(例如银杏叶类黄酮配糖体)、山楂提取物(例如低聚原花青素)、荞麦(例如芦丁)、槐木(如芦丁)、桦树叶(如槲皮酮糖苷类、金丝桃苷和芦丁)、接骨木花(如芦丁)、菩提花(例如含有槲皮素和法呢醇的精油)、圣约翰草油(例如橄榄油提取物)、金盏花、山金车(例如含有精油的花的油性提取物、含有黄酮类的极性提取物)、蜂花(例如黄酮类,精油);免疫刺激剂:紫锥菊(例如酒精提取物、新鲜树液、压榨汁)、刺五加(eleutherococcussenticosus);生物碱:萝芙木(例如普拉马林(prajmalin))、长春花(例如长春胺);另外的植物药物:芦荟、七叶树(例如七叶皂苷)、蒜(例如蒜油)、菠萝(例如菠萝蛋白酶)、人参(例如人参皂苷)、圣母蓟类水果(ourlady'sthistlefruit)(例如关于水飞蓟素标准化的提取物)、盒冬青根(例如螺可吉宁(ruscogenin))、缬草(例如缬草三酯、缬草酊(tct.valerianae))、醉椒根(例如卡瓦内酯)、啤酒花(例如苦味啤酒花)、西番莲、龙胆糖苷(例如乙醇提取物)、含蒽醌的药物提取物(例如含芦荟素的芦荟汁)、花粉提取物、藻类提取物、甘草提取物、棕榈提取物、银虎尾属(galphimia)(例如原始酊剂)、槲寄生(例如乙醇水溶液提取物)、植物甾醇(例如β-谷甾醇)、毛蕊花属(例如含水乙醇提取物)、茅膏菜属(drosera)(例如甜酒(vinumliquorosum)提取物)、沙棘果(例如从其中获得的果汁或沙棘油)、药蜀葵根、报春花根提取物、锦葵的新鲜植物提取物、紫草科植物、常春藤、木贼、蓍草、长叶车前(例如压榨汁)、荨麻、白屈菜、荷兰芹;来自norolaenalobata、大叶万寿菊、teeomasiems、苦瓜的植物提取物和芦荟提取物。
优选的化妆品活性化合物是在根据本发明的用途中具有活性的那些化合物,如特别是皮肤护理剂、皮肤调节剂、皮肤平滑剂、用于增加皮肤水合作用的试剂(例如像甘油或脲)、防晒剂、角质软化剂、用于自由基的自由基清除剂、抗皮脂溢剂、用于治疗皮肤老化迹象的活性化合物、和/或调节皮肤分化和/或增殖和/或色素淀积的试剂。
包含根据本发明的物种姜花提取物的植物提取物的化妆品组合物用于局部应用。因此,适合于局部应用于皮肤的配制品可以制成多种产品类型,包括但不限于洗剂、乳膏、凝胶、乳液、棒状物、喷雾、软膏剂、清洁洗涤液和固体棒、香波、糊剂、摩丝、擦拭巾、贴剂、化妆品敷料或面膜和胶布带、水凝胶、和薄膜或脂质体配制品。
在根据本发明的组合物中的物种姜花的植物提取物按重量计以从约0.001%至约20%的量、特别是以从约0.01%至约10%的量、优选地按重量计以从约0.1%至约5.0%的量、更优选地按重量计以从约0.15%至约3.0%的量、甚至更优选地按重量计以从约0.2%至约2.0%的量存在,在每一种情况下均基于组合物的总重量。
本发明进一步涉及根据权利要求5所述的用于制备姜花根和/或根状茎提取物的方法,该方法包括以下步骤:
-步骤a),该步骤包括提供待提取的姜花植物的一定量的根和/或根状茎的片;
-步骤b),在该步骤期间,用合适的溶剂或溶剂混合物提取姜花植物的所述根和/或根状茎的片;以获得姜花植物根和/或根状茎片提取混合物;
-步骤c),在该步骤期间,将步骤b)中获得的所述姜花植物根和/或根状茎片提取混合物过滤,以获得姜花植物根和/或根状茎片提取混合物的滤液;
-步骤d),在该步骤期间,将步骤c)中获得的所述姜花植物根和/或根状茎片提取混合物的滤液静置以从上清液中分离固体残余物;
-步骤e),在该步骤期间,将步骤d)中获得的所述上清液过滤,以获得呈澄清溶液的姜花植物根和/或根状茎提取物;
-步骤f),在该步骤期间,使用合适的溶剂或溶剂混合物将步骤e)中获得的所述澄清溶液调节至所希望的浓度,以获得所希望的姜花根和/或根状茎提取物。
在上文中定义的方法中,在步骤a)中,物种姜花的植物提取物的片优选地选自压碎的、切割的或研磨的根和/或根状茎;在步骤b)中,该溶剂或溶剂混合物优选是亲水性或水混溶性溶剂,如优选地选自如上所述的溶剂。优选地,将乙醇用于在步骤b)中姜花属片的提取。优选地进行一次或多次水醇提取(优选地使用乙醇)。优选地,使用以1/10比率的植物片和水醇溶剂(例如用10dm3的50%(w/w)乙醇提取1kg的植物片(如特别是根/根状茎片))比率进行提取。在步骤c)中,应用本领域技术人员熟知的常规的过滤技术;在步骤d)中,使用本领域技术人员熟知的常规技术进行固体残余物和上清液的分离;在步骤e)中,进行上清液的过滤以进一步澄清和纯化上清液,以获得澄清溶液形式的姜花属提取物;在步骤f)中,用合适的溶剂或溶剂混合物调节澄清溶液至所希望的浓度,该溶剂或溶剂混合物优选地选自如上所述的溶剂,并且更优选使用体积比率为从10/90至90/10、优选地从20/80至80/20的水和甘油的混合物。
根据具体实施例,在如上文所定义的方法的步骤f)中,用比率(体积/体积)等于30/70的水/甘油混合物实现将澄清溶液调节至所希望的浓度。
根据作为本发明主题的方法获得的姜花根和/或根状茎提取物可以引入另外可以口服地、局部地或肠胃外地给予的配制品中。
用于局部使用的配制品的特征在于其包含至少一种化妆品上可接受的赋形剂和有效量的根据本发明主题的方法获得的姜花根和/或根状茎提取物。
在如上所述的配制品定义中使用的表述“用于局部使用”意指所述配制品通过应用于皮肤上使用,无论是在直接应用还是间接应用的情况下,例如在呈纺织品或纸擦拭巾形式的身体护理产品或旨在与皮肤接触的卫生产品的情况下均如此。
在如上所述用于局部使用的配制品的定义中使用的表述“化妆品上可接受的”意指,根据通过1993年6月14日的指令号93/35/cee修订的1976年7月27日的欧洲经济共同体理事会指令号76/768/cee,该配制品包含任何旨在与人体各部位(表皮、毛发或多毛系统、指甲、嘴唇和生殖器)或者与牙齿和口腔粘膜接触(为了单独地且主要地清洗它们、使它们变香、改变其外观和/或矫正其体臭和/或保护它们或保持它们处于良好状态的目的)的任何物质或制剂。
用于局部使用的配制品包含至少一种化妆品上可接受的赋形剂和有效量的根据本发明主题的方法获得的姜花根和/或根状茎提取物,该配制品通常呈稀水溶液或水/醇溶液的形式,呈单一或多重乳液的形式,如油包水(w/o)、水包油(o/w)或水包油包水(w/o/w)乳液(其中油具有植物或矿物性质),或呈粉末形式。它们也可以分散或浸渍在纺织品或无纺材料上,无论是擦拭巾、纸巾或是服装均如此。
在一般情况下,根据本发明主题的方法获得的姜花根和/或根状茎提取物与如上定义的局部配制品中使用的多种类型的辅佐剂或活性成分相关,无论是在脂肪、有机溶剂、增稠剂、胶凝剂、软化剂、发泡表面活性剂和/或洗涤剂、富脂剂、增稠剂和/或胶凝表面活性剂、抗氧化剂、遮光剂、稳定剂、发泡剂、香料、乳化表面活性剂、水溶助剂、增塑剂、富脂剂、质地剂、颜料、掩蔽剂、螯合剂、防腐剂、精油、染料、亲水性或亲脂性活性剂、润湿剂、香料、矿物或有机防晒剂、矿物填料或化妆品中常用的任何其他成分的情况下均如此。
在用于局部使用的配制品中,可以与根据本发明主题的方法获得的姜花根和/或根状茎提取物相关联的油的实例包括矿物油(如石蜡油、凡士林油、异链烷烃或矿物白色油)、动物来源的油(如角鲨烯或角鲨烷)、植物油(如甜杏仁油、椰子仁油、蓖麻油、荷荷巴油、橄榄油、菜籽油、花生油、葵花籽油、小麦胚芽油、玉米胚芽油、大豆油、棉籽油、紫花苜蓿油、罂粟油、南瓜油、月见草油、小米油、大麦油、黑麦油、红花油、蜡杨梅油、西番莲油、榛子油、棕榈油、牛油树脂、杏仁油、红厚壳属油、水蒜芥油、鳄梨油、金盏花油;乙氧基化的植物油;合成油如脂肪酸酯(如肉豆蔻酸丁酯、肉豆蔻酸丙酯、肉豆蔻酸鲸蜡酯、棕榈酸异丙酯、硬脂酸丁酯、硬脂酸十六烷酯、硬脂酸异丙酯、硬脂酸辛酯、硬脂酸异鲸蜡酯、油酸十二烷基酯、月桂酸己酯、二辛酸丙二醇酯)、羊毛脂酸的酯衍生物(如,羊毛酸异丙酯、羊毛脂酸异鲸蜡酯)、脂肪酸甘油单酯、脂肪酸的甘油二酯和甘油三酯(如三庚酸甘油酯)、苯甲酸烷基酯、聚α烯烃(polyalfaolenfins)、聚烯烃(如聚异丁烯)、合成异烷烃(如异十六烷、异十二烷)、全氟化油和硅油。更特别地后者包括二甲基聚硅氧烷、甲基苯基聚硅氧烷、通过胺改性的硅酮、通过脂肪酸改性的硅酮、通过醇改性的硅酮、通过醇和脂肪酸改性的硅酮、通过聚醚基团改性的硅酮、改性的环氧硅酮、通过氟化的基团改性的硅酮、环状硅酮、以及通过烷基基团改性的硅酮。
在用于局部使用的配制品中,可以与根据本发明主题的方法获得的姜花根和/或根状茎提取物相关联的其他脂肪包括脂肪醇和脂肪酸。
在用于局部使用的配制品中,可以与根据本发明主题的方法获得的姜花根和/或根状茎提取物相关联的蜡的实例包括蜂蜡;巴西棕榈蜡;小烛树蜡;小冠巴西棕醋;日本蜡;软木纤维蜡或甘蔗蜡;石蜡、褐煤蜡;微晶蜡;羊毛脂蜡;地蜡;聚乙烯蜡;氢化油;硅酮蜡;植物蜡;在环境温度下的脂肪醇和脂肪酸固体;在环境温度下的甘油酯固体。
在用于局部使用的配制品中,可以与根据本发明主题的方法获得的姜花根和/或根状茎提取物相关联的增稠和/或乳化聚合物的实例包括丙烯酸的均聚物或共聚物或丙烯酸的衍生物、丙烯酰胺的均聚物或共聚物、丙烯酰胺衍生物的均聚物或共聚物、丙烯酰胺基甲基丙烷磺酸的均聚物或共聚物、乙烯基单体、三甲基氨乙基丙烯酰氯、植物或生物合成来源的水状胶体(例如黄原胶、刺梧桐树胶、角菜酸酯、海藻酸盐);硅酸盐;纤维素及其衍生物;淀粉及其亲水性衍生物;聚氨酯。
在用于局部使用的配制品中,可以与根据本发明主题的方法获得的姜花根和/或根状茎提取物相关联的聚电解质类型的聚合物包括例如丙烯酸和2-甲基-[(1-氧代-2-丙烯基)氨基]1-丙烷磺酸(mpsa)的共聚物、丙烯酰胺和2-甲基-[(1-氧代-2-丙烯基)氨基]1-丙烷磺酸的共聚物、2-甲基-[(1-氧代-2-丙烯基)氨基]1-丙烷磺酸和(2-羟乙基)丙烯酸酯的共聚物、2-甲基-[(1-氧代-2-丙烯基)氨基]1-丙烷磺酸的均聚物、丙烯酸的均聚物、丙烯酰乙基三甲基氯化铵和丙烯酰胺的共聚物、mpsa和乙烯基吡咯烷酮的共聚物、丙烯酸和丙烯酸烷基酯的共聚物(其碳链包含10和30个之间的碳原子)、mpsa和丙烯酸烷基酯的共聚物(其碳链包含10和30个之间的碳原子)。此类聚合物在名称simulgeltmeg、sepigeltm305、simulgeltmns、simulgeltmins100、simulgeltmfl、simulgeltm800、simulgeltma下由申请人分别出售。
在用于局部使用的配制品中,可以与根据本发明主题的方法获得的姜花根和/或根状茎提取物相关联的乳化剂的实例包括脂肪酸盐、乙氧基化脂肪酸、脂肪酸和山梨糖醇的酯、乙氧基化脂肪酸的酯、聚山梨醇酯、聚甘油酯、乙氧基化脂肪醇、蔗糖酯、烷基聚糖苷、硫酸化的和磷酸化的脂肪醇或烷基聚糖苷和脂肪醇的混合物,所述实例描述于法国专利申请2668080、2734496、2756195、2762317、2784680、2784904、2791565、2790977、2807435和2804432中。
在用于局部使用的配制品中,可以与根据本发明主题的方法获得的姜花根和/或根状茎提取物相关联的发泡表面活性剂和/或洗涤剂的实例包括在本活性领域中通常使用的局部可接受的阴离子、阳离子、两性或非离子的表面活性剂。
在用于局部使用的配制品中,可以与根据本发明主题的方法获得的姜花根和/或根状茎提取物相关联的阴离子表面活性剂特别地包括以下化合物的碱金属盐、碱土金属盐、铵盐、胺盐、氨基醇盐:烷基醚硫酸酯、烷基硫酸酯、烷基酰胺基醚硫酸酯、烷基芳基聚醚硫酸酯、单甘油酯硫酸酯、α-烯烃磺酸酯、石蜡磺酸酯、烷基磷酸酯、烷基醚磷酸酯、烷基磺酸酯、烷基酰胺磺酸酯、烷基芳基磺酸酯、烷基羧酸酯、烷基磺基琥珀酸酯、烷基醚磺基琥珀酸酯、烷基酰胺磺基琥珀酸酯、烷基磺基乙酸酯、烷基肌氨酸酯、酰化的硫代硫酸酯、n-酰基牛磺酸酯和酰基乳酸酯。
在用于局部使用的配制品中,可以与根据本发明主题的方法获得的姜花根和/或根状茎提取物相关联的阴离子表面活性剂还包括氨基酸、肽、蛋白的n-酰基化的衍生物(其酰基链包含8至16个碳原子);任选地氢化的脂肪酸盐、椰子仁油的酸盐。
在用于局部使用的配制品中,可以与根据本发明主题的方法获得的姜花根和/或根状茎提取物相关联的两性表面活性剂包括特别是烷基甜菜碱、烷基酰胺基甜菜碱、磺基甜菜碱、烷基酰胺基烷基磺基甜菜碱、咪唑啉衍生物、磷酸甜菜碱、两性聚乙酸酯以及两性丙酸酯。
在用于局部使用的配制品中,可以与根据本发明主题的方法获得的姜花根和/或根状茎提取物相关联的阳离子表面活性剂特别地包括季铵衍生物。
在用于局部使用的配制品中,可以与根据本发明主题的方法获得的姜花根和/或根状茎提取物相关联的非离子表面活性剂特别地包括烷基聚糖苷(其烷基链包含8至16个碳原子)、蓖麻油衍生物、聚山梨醇酯、椰子仁酰胺(coprahamide)、n-烷基胺和氧化胺。
在用于局部使用的配制品中,可以与根据本发明主题的方法获得的姜花根和/或根状茎提取物相关联的质地剂的实例包括氨基酸的n-酰化的衍生物(例如像由味之素公司(ajinomoto)在名称aminohopetmll下出售的月桂酰赖氨酸、由国民淀粉化学公司(nationalstarch)在名称dryflotm下出售的辛烯基淀粉琥珀酸酯、由seppic在名称montanov14下出售的肉豆蔻基聚葡糖苷、纤维素纤维、棉纤维、壳聚糖纤维、滑石、绢云母或云母。
在用于局部使用的配制品中,可以与根据本发明主题的方法获得的姜花根和/或根状茎提取物相关联的遮光剂和/或珠光剂的实例包括棕榈酸钠、硬脂酸钠、羟基硬脂酸钠、棕榈酸镁、硬脂酸镁、羟基硬脂酸镁、乙二醇单硬脂酸酯、乙二醇二硬脂酸酯、聚乙二醇单硬脂酸酯、聚乙二醇二硬脂酸酯、和脂肪醇。
在用于局部使用的配制品中,可以与根据本发明主题的方法获得的姜花根和/或根状茎提取物相关联的增稠和/或胶凝表面活性剂的实例包括:
-烷基聚糖苷的脂肪酯,任选地烷氧基化的,并且尤其是乙氧基化的甲基聚葡萄糖苷酯,如分别在名称glucamatetmlt和glumatetmdoe120下出售的peg120甲基葡萄糖三油酸酯和peg120甲基葡萄糖二油酸酯;
-烷氧基化的脂肪酸酯,如在名称crothixtmds53下出售的peg150季戊四醇四硬脂酸酯,在名称antiltm141下出售的peg55丙二醇油酸酯;
-脂肪链聚亚烷基二醇氨基甲酸酯,如在名称eflacostmt211下出售的ppg14月桂醇聚醚异佛尔基二氨基甲酸酯、在名称elfacostmgt2125下出售的ppg14棕榈油醇聚醚60己基二氨基甲酸酯。
在用于局部使用的配制品中,可以与根据本发明主题的方法获得的姜花根和/或根状茎提取物相关联的防晒剂的实例包括在修订的化妆品指令76/768/eec附件vii中出现的所有那些内容。
在用于局部使用的配制品中,可以与根据本发明主题的方法获得的姜花根和/或根状茎提取物相关联的活性成分的实例包括具有增亮或脱色作用的化合物例如像熊果苷,曲酸,氢醌,鞣花酸,维生素c,抗坏血酸磷酸镁,多酚的提取物,糖基化的多酚的衍生物(如迷迭香醯葡萄糖苷),葡萄提取物,松树提取物,葡萄酒提取物,橄榄提取物,池塘(pond)提取物,n-酰化的蛋白,n-酰化的肽,n-酰化的氨基酸,n-酰化的蛋白、氨基酸、肽的部分水解产物、蛋白的总水解产物,蛋白质的部分水解产物,多元醇(例如甘油或丁二醇),脲,吡咯烷酮羧酸或这种酸的衍生物,甘草次酸,甜没药醇(alpha-bisabolol),糖或糖衍生物,多糖或其衍生物,羟基酸(例如乳酸),维生素,维生素衍生物(如视黄醇),维生素e及其衍生物,矿物,酶,辅酶(如辅酶q10),激素类或激素样物质,大豆提取物(例如rafferminetm),小麦提取物(例如tensinetm或gliadinetm),植物提取物(如富含丹宁酸的提取物),富含异黄酮的提取物或富含萜烯的提取物,淡水或海水藻类的提取物,精华蜡,细菌提取物,矿物,一般脂类,脂类(如神经酰胺或磷脂),具有减肥作用的活性剂(如咖啡因或其衍生物、如在名称adipolesstm下出售的藜麦提取物、如在名称serenikstm207下出售的加拿大铁杉提取物、如包含在名称adiposlimtm下出售的月桂酰基脯氨酸的组合物),对于油性皮肤具有抗菌作用或纯化作用的活性剂如lipacidetmpvb,具有活肤或刺激特性的活性剂如sepitonictmm3或physiogenyltm,泛醇及其衍生物(如sepicaptmmp),抗老化活性剂(如sepilifttmdphp、lipicidetmpvb、sepivinoltm、sepivitaltm),水化活性剂(如sepicalmtms、sepicalmtmvg和sepilifttmdphp),“抗光老化”抗老化活性剂,保护真皮-表皮接合处的完整性的活性剂,提高胞外基质的组分的合成的活性剂,具有减肥活性的活性剂(如咖啡因、茶碱、ampc、绿茶、鼠尾草、银杏、常春藤、马栗树、竹、假叶树(ruscus)、假叶树(butcher'sbroom)、积雪草、帚石楠、旋果蚊草子、岩藻、迷迭香、柳树),在皮肤上产生“加热”感觉的活性剂(如皮肤微循环活化剂(例如烟酸盐)),或在皮肤上产生“凉爽”感觉的产品(例如薄荷醇及其衍生物)。
通过以下实例进一步展示本发明,这些实例涉及本发明的某些具体实施例。除非另有说明,否则实例使用本领域技术人员在常规范围内熟知的标准技术进行。以下实例仅用于说明目的,并不意图对本发明的条件或范围完全确定。因此,它们不应以任何方式解释为限制本发明的范围。
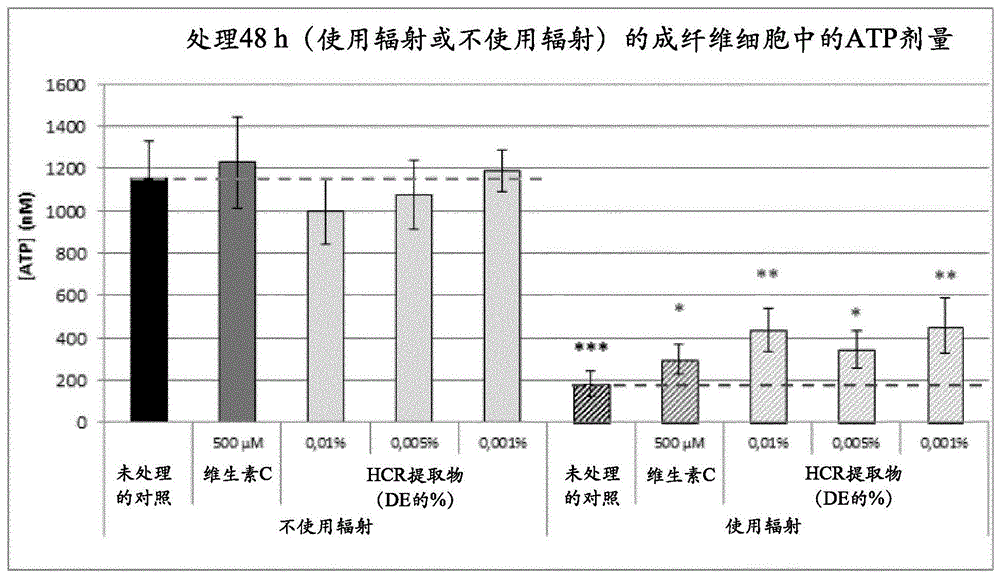
-图1示出了关于实例2的线粒体保护的结果,其中atp滴定在hcr提取物处理48h的成纤维细胞中进行(使用辐射或不使用辐射)。
-图2示出了关于实例2的线粒体保护的结果,其中nad+/nadh滴定在hcr提取物处理48h的成纤维细胞中进行(使用辐射或不使用辐射)。
-图3示出了关于实例3的溶酶体保护的结果,其中在用hcr提取物处理48h后定量lysotracker成纤维细胞染色(使用辐射或不使用辐射)。
-图4示出了用hcr提取物预处理24h或不处理,用实例4的bap污染并且再处理24h,关于由皮肤外植体释放的il-8的结果。
-图5示出了用实例5的hcr提取物处理40h后,关于由角质化细胞释放的β-内啡肽的滴定的结果。
-图6示出了用实例5的hcr提取物处理40h后,关于在角质化细胞中总蛋白量的滴定的结果。
-图7示出了用实例5的报道为总蛋白的hcr提取物处理40h后,关于由角质化细胞释放的β-内啡肽的滴定的结果。
-图8示出了用实例6的hcr提取物浓度0.001%、0.005%和0.01%的de处理72h后,关于由b16黑素细胞释放的黑素的滴定的结果。
-图9示出了用实例6的hcr提取物浓度0.01%、0.05%和0.1%的de处理72h后,关于由b16黑素细胞释放的黑素的滴定的结果。
-图10示出了用实例6的hcr提取物浓度0.001%、0.005%和0.01%的de处理72h后,关于b16黑素细胞中总蛋白量的滴定的结果。
-图11示出了用实例6的hcr提取物浓度0.01%、0.05%和0.1%的de处理72小时后,关于b16黑素细胞中总蛋白量的滴定的结果。
-图12示出了用实例6的报道为总蛋白的hcr提取物浓度0.001%、0.005%和0.01%的de处理72小时后,关于由b16黑素细胞释放的黑素的滴定的结果。
-图13示出了用实例6的报道为总蛋白的hcr提取物浓度0.01%、0.05%和0.1%的de处理72小时后,关于由b16黑素细胞释放的黑素的滴定的结果。
-图14示出了在没有实例7的ros产生刺激的情况下处理24小时后,关于hcr提取物对角质化细胞中ros放出的效果的结果。
-图15示出了在有实例7的ros产生刺激的情况下处理24小时后,关于hcr提取物对角质化细胞中ros放出的效果的结果。
实例1:姜花根提取物的制备
根据本发明的方法制备姜花根提取物。
在步骤(a)中,在合适的提取容器中提供尺寸长度达10cm的姜花的压碎的根(根状茎)。
在步骤(b)中,将水/乙醇[50/50(w/w)]的混合物作为提取溶剂添加至压碎的根中,并进行2次提取。
在步骤(c)中,使用常规过滤技术过滤提取混合物。
在步骤(d)中,通过沉降固体残余物浓缩步骤(c)的滤液,随后倾析上清液。
在步骤(e)中,使用常规过滤技术过滤步骤(d)的上清液。
在步骤(f)中,将步骤(e)的澄清溶液进行调节至在具有30/70(v/v)比率的水和甘油的混合物中20g/l的溶液,随后进行最终过滤用于进一步纯化,以获得所希望的浓度为2.0%(w/v)的最终提取物。
实例2:姜花根提取物(hcr提取物)对用uva辐射的成纤维细胞中线粒体网络的效果(mitotracker染色、atp和nad+/nadh滴定)的评估
1)-背景信息
a)-本研究的目的是评估hcr提取物对uva辐射的成纤维细胞的线粒体分布和细胞能量代谢的效果。
b)-将从41岁的供体(高加索女性)的乳腺皮肤真皮整形手术后提取的正常人成纤维细胞(nhf)作为原代单层培养;
c)-然后在24小时期间应用测试提取物,
d)-辐射细胞(未处理),并且在另外24小时期间再次应用测试化合物;
e)-对线粒体染色,或收集细胞以进行atp(三磷酸腺苷)和nad+/nadh(烟酰胺腺嘌呤二核苷酸)滴定。
2)-剂量确定(通过xtt测定的细胞毒性/活力检查)和评估的测试化合物
a)-在通过用xtt测定检查细胞活力/毒性评估工作剂量后,选择2%hcr干提取物(对应于培养基中1/20hcr的稀释度,以最终获得0.1%hcr)的测试浓度。
b)-在处理前24小时(在杜氏改良培养基(dulbecco'smodifiedeaglemedium)中或在含有抗生素(gibcotm15140)和10%的胎牛血清(fbs)(gibcotm10270)的dmem(gibcotm41966)中(在37℃孵育;5%co2)中),将细胞接种到96孔微板中(细胞密度为每孔5,000个细胞,即15,000nhf/cm2,该密度之后用于滴定)。处理在不含fbs的培养基中进行(48小时;37℃;5%co2)。
c)-处理48小时后,清空孔并用pbs(磷酸盐缓冲盐水)轻轻冲洗。然后将xtt溶液(0.3mg/ml)应用于细胞上,并且然后将板在黑暗中孵育(3小时;37℃;5%co2)。孵育3小时后,在450nm处与650nm参比处测量吸光度。还实现了空白(在没有细胞(但是有或没有产物)的孔中具有xtt溶液)以检查xtt分子和提取物之间不存在相互作用,这将在结果中引起偏差。使用试剂盒“细胞增殖试剂盒ii(xtt)(rochediagnosticstm11465015001)”进行xtt测试。xtt系统(比色方法)是量化线粒体活性的测定,并且用作活力测试。这种测试基于将黄色四唑盐xtt裂解成橙色甲臜,所述裂解是通过存在于细胞的线粒体呼吸链中的系统“琥珀酸-四唑还原酶”进行的。因此,这种转化仅发生在代谢活跃的细胞(即活细胞)中。通过分光光度法在450nm处与650nm参比处测量衍生物甲臜。
d)-在每种情况下计算光密度数据(od或吸光度)的平均值。处理的细胞的活力表示为未处理对照的百分比:
与未处理的对照相比,降低细胞活力,使其低于线粒体活性的80%极限的处理被认为对细胞有毒。相反,数据增加检测线粒体活性。
3)-线粒体网络保护的评估
a)-在处理前一天(在37℃;5%co2下孵育),在与前述相同的培养基中(完全培养基,即含有fbs),将成纤维细胞接种到皮氏培养皿(petridishes)中(细胞密度为直径为60mm的每个培养皿中150,000个细胞,即7,700nhf/cm2)。然后应用每种测试化合物浓度/剂量(在每个培养皿中)持续24小时(在没有血清的培养基中;在37℃/5%co2下孵育)。然后将细胞在盐水缓冲液(8j/cm2,在vilberlourmatrmx3wtm机中)中uva辐射或不uva辐射,并且最终再用测试化合物(在培养基中)再处理24小时。
b)-为了评估线粒体染色,将细胞与荧光探针(英杰公司(invitrogen)mitotrackertm)一起孵育。在有或没有合适的荧光滤光片下,观察细胞并用x40物镜(奥林巴斯公司(olympus)ck40tm显微镜和archimedmicrovision软件)拍摄照片。这些照片分别允许线粒体网络或整个细胞的可视化。
4)-对代谢活性的效果(atp&nad+/nadh滴定)的评估
a)-为了检查uv和测试的产物对细胞代谢的效果,进行atp和nad+/nadh滴定。
(i)-在处理前一天,在与前述相同的培养基中,将细胞接种到96孔板中(细胞密度为每孔中5,000个细胞,即15,000nhf/cm2)。然后处理和辐射时间相同:第一次应用24小时(在没有血清的培养基中),然后uva辐射或不uva辐射(相同剂量),并且最终第二次处理另外24小时。如前所述,从实验的开始到结束,将细胞在37℃/5%co2下孵育。在此,每个剂量以一式五份(对于atp)或以一式六份(对于nad+/nadh)进行测试。
(ii)-为了进行滴定,在处理结束时收集细胞裂解物或沉淀物。为了细胞atp总水平的滴定,在含有细胞和上清液(含有产物的培养基)的孔中添加洗涤剂以裂解细胞并且获得细胞裂解物。对于胞内nad+和nadh滴定,去除上清液并使细胞可渗透以获得可渗透的细胞沉淀。
(iii)-然后用商业试剂盒进行滴定:发光atp检测测定试剂盒(abcamtmab113849)和基于细胞的nad+/nadh测定试剂盒(caymanchemicaltm600480)。
(iv)-nad测定试剂盒以两种现有形式(氧化的nad+和还原的nadh)给药。首先,添加乙醇和醇脱氢酶允许将样品中发现的nad+还原为nadh,伴随着允许乙醇的氧化。然后在将四唑盐底物(wst-1)还原成有色甲臜的同时氧化总nadh。该产物的测量的量(吸光度)与每个样品中的总nad(nad+和nadh)成比例。
(v)-atp测定试剂盒是基于萤火虫(firefly,photinuspyralis)荧光素酶的atp监测系统。添加荧光素酶,并且d-荧光素与样品中的atp反应产生光,其量度(发光)与atp浓度成比例。
b)-将atp和nad+/nadh滴定两者的原始数据(即对各自标准获得的发光单位(rlu)或od测量值)绘制在图形上以确定标准曲线。然后,确定样品中测量的atp或nad+/nadh的浓度。将每种条件的定量值进行平均。数据以图形表示为浓度(nm,对于atp或nad+/nadh)。对于每种条件获得的结果也可以相对于有或没有辐射(设定为100%)的未处理的对照,或相对于没有辐射的相应的相同条件(uva效应的评估)来表示:
%“样品”=(平均rlu或od“样品”/平均rlu或od“辐射或未辐射的对照”)×100
使用与针对xtt测定所述相同的标准(与未辐射或辐射的对照比较,或与未辐射的相应的相同条件比较),通过学生t检验(student′st-test)确定结果的统计学上显著的效果。
5)-结果
a)-剂量确定(通过xtt测定的细胞毒性/活力检查)
对于成纤维细胞中0.0005%和0.01%hcr(干提取物(de))之间的测试浓度没有观察到细胞毒性:
b)-线粒体网络保护的评估
观察图像允许观察uv辐射对细胞形状和细胞中线粒体分布的效果。实际上,与没有uv辐射相比,一些uv辐射的成纤维细胞不再是纺锤形的,并且线粒体网络似乎不是那么有组织的。应用阳性对照(维生素c,500μm),uva的作用不太明显。用0.01%(的de)的hcr处理成纤维细胞保护受uv辐射损害的线粒体网络。在0.005%和0.001%的较低剂量下未观察到这种抗uv的效果。
c)-对代谢活性的效果(atp&nad+/nadh滴定)的评估
滴定的结果呈现于图1中。数据表示为报告为未辐射或辐射的对照、或未辐射的相应条件的浓度(nm)。与未辐射的对照或辐射的对照相比,计算统计p值。没有辐射,没有一种处理诱导atp产生的显著抑制或刺激。uv辐射诱导成纤维细胞对atp产生的强烈且非常高显著的抑制(-84%***,与基础水平(即没有辐射)相比的辐射的对照)。阳性参比(维生素c,500μm)允许显著抵消uva对这种能量合成的效果(与辐射的对照相比,+61%*)。通过hcr处理,观察到atp合成显著或高显著增加:+136%**、+86%*和+146%**分别地是0.01%、0.005%和0.001%。
d)-nad+/nadh滴定
(i)-在没有辐射的情况下,所有处理都倾向于抑制基础nad+/nadh成纤维细胞的产生。结果示出于图2中。
(ii)-通过uva辐射,nhf的这种辅酶合成被显著抑制(-21%*,与基础水平相比)。在此维生素c未显示uv辐射的细胞对nad+/nadh释放的预期的正面效果。在最高测试的剂量(0.01%)下的hcr应用允许恢复通过uva降低的nad+/nadh成纤维细胞产生(+19%*,与辐射的对照相比)。在另外两个测试的剂量下,效果不显著(+9%)。
e)-因此,本评估显示uva诱导线粒体网络的部分解构/崩解和atp和nad+/nadh产生的抑制。hcr提取物显示对培养的和uv辐射的成纤维细胞的效果,显著增加atp产生并刺激nad+/nadh合成。它可以保护线粒体网络对抗uv辐射。因此,hcr提取物有效地保护皮肤对抗线粒体的uv损害和能量代谢。
实例3:hcr提取物对用uva辐射的成纤维细胞中溶酶体网络的效果(lysotracker染色)的评估
1)-背景信息
a)-本研究的目的是评估hcr提取物对uva辐射的成纤维细胞中溶酶体分布的效果。
b)-将从41岁的供体(高加索女性)的乳腺皮肤真皮整形手术后提取的正常人成纤维细胞(nhf)作为原代单层培养;
c)-然后在24小时期间应用测试提取物,
d)-辐射细胞(未处理),并且在另外24小时期间再次应用测试化合物;
e)-然后用特定的测试化合物染色溶酶体。
2)-剂量确定(通过xtt测定的细胞毒性/活力检查)和评估的测试化合物
如实例2中所述进行用xtt测定的剂量确定。
3)-溶酶体网络保护的评估
a)-如实例2中所述进行成纤维细胞接种。
b)-然后将细胞与荧光探针(英杰公司lysotrackertm)一起孵育。在有或没有合适的荧光滤光片下,观察它们并用x40物镜(奥林巴斯公司ck40显微镜和archimedmicrovision软件)拍摄照片。这些照片允许溶酶体网络或整个细胞的分别地可视化。
c)-用columbus软件,通过hcs制药公司(hcspharma)(雷恩(rennes),法国)定量荧光作为平均强度(每种条件3个图像)。这是每个染色像素的强度的平均值,包含在用lysotracker染色的细胞区域中(考虑每个图像的细胞数,因为最终值是图像上所有细胞值的平均值)。
4)-结果
a)-剂量确定(通过xtt测定的细胞毒性/活力检查)
对于成纤维细胞中0.0005%和0.01%hcr(de)之间的测试浓度没有观察到细胞毒性:
b)-溶酶体网络保护的评估
(i)-观察uv辐射的对照图像允许观察辐射对细胞形状和细胞中溶酶体组织的效果。与未处理和未辐射的对照相比,一些uv辐射的成纤维细胞确实不再是纺锤形的并且溶酶体网络似乎没有那么有组织。
(ii)-荧光强度的测量证实了这种效果,因为它显著降低:-29%(显著*)。阳性对照(维生素c,500μm)的应用减少了uva的作用。结果示出于图3中。定量数据支持这一观察,因为荧光平均强度更高(高度显著效果**)。
(iii)-用0.01%的hcr提取物处理成纤维细胞保护被uv辐射损害的溶酶体网络。用0.005%和0.001%的提取物对抗uv的效果不那么明显。荧光定量的结果证实了这一点,因为用0.01%hcr增加了+36%(与辐射的对照相比显著*)。使用较低的测试剂量(0.005%和0.001%),效果不太明显且不显著(分别为+19%和+21%)。
c)-因此,本评估表明,uva辐射引起细胞溶酶体网络的部分损害。测试的hcr提取物显示对uv辐射的成纤维细胞的作用,并且允许保护溶酶体网络对抗uv辐射(特别是在最高测试剂量(0.01%)下)。因此,此评估允许得出结论,hcr提取物有效保护真皮细胞的溶酶体对抗uv损害。
实例4:hcr提取物在人皮肤外植体污染模型中的作用的评估
1)-背景信息
a)-本研究的目的是评估hcr提取物在人皮肤外植体污染模型中的潜在的保护作用。
b)-将该产品在人体皮肤外植体(8mm的直径)上全身应用24小时,该外植体由biopredictm国际(雷恩)提供,其来源于乳腺整形手术(高加索人来源的44岁女性);
c)-然后在污染期间再次应用该产品另外24小时。在此模型中通过应用环境污染物苯并芘(3,4-苯并芘/bap)作为全身处理,即在培养基中诱导所述污染。这种污染物诱导il-8释放(sephra结果)。
d)-通过在上清液(培养基)中滴定来分析通过外植体释放的炎性细胞因子il-8(白细胞介素8)。
e)-此外,保留皮肤外植体用于通过密蛋白1&4表达(cldn1和cldn4)的免疫染色进行分析。
2)-人皮肤外植体模型的污染
a)-将2%(de)hcr提取物稀释在培养基中以获得0.1%(de)hcr提取物,将其用作测试化合物。
b)-将所述hcr提取物全身应用于皮肤外植体上,作为24小时的预处理。
c)-然后在另外二十四小时期间用bap(西格玛公司(sigma)crm40071,40μm全身)污染或不污染皮肤外植体,同时将hcr提取物再次全身应用于未污染和污染的皮肤外植体上。每个非污染的条件一式三份进行测试(3个外植体:2个用于免疫染色,并且1个用于组织学),每个污染的条件一式四份进行测试(4个外植体:3个用于免疫染色,并且1个用于组织学)。
d)-上清液中的滴定(去除用于每种条件,对于3个未污染的外植体和4个污染的外植体)一式两份进行。
e)-为了验证il-8滴定,评估了另外的条件,即用1μg/ml的参比促炎分子pma(佛波醇-12-肉豆蔻酯13-乙酯,西格玛公司p8139)刺激。此产品在最后24小时期间在一个未用提取物处理过的也未污染的外植体上全身应用。
3)-皮肤外植体的处理
a)-然后将皮肤外植体置于24孔板中,该板填充有添加有5%胎牛/牛血清(fbs,invitrogentm10270)和300μl/孔抗生素(青霉素100u/ml和链霉素100μg/ml,invitrogentm15140)的dmem培养基(invitrogentm31053)。外植体在37℃/5%co2下稳定4小时。
b)-稳定化后,将提取物全身应用或不应用于外植体培养基中,在37℃/5%co2下培养24小时。然后使用的培养基是未添加fbs的dmem。然后在24小时期间全身应用bap(40μm)污染或不污染外植体,同时用hcr提取物再次处理(或不处理)(37℃/5%co2孵育)。
c)-在此时间段结束时,储存上清液(处理培养基)以给药il-8。将每种条件的一个外植体(污染的或未污染的)保存在4%甲醛中以进行组织学分析(h/e/s染色)。将其他外植体在液氮中冷冻保存,用于以后的免疫染色实验。
d)-然后用来自生物技术公司(bio-techne)/r&d系统公司(r&dsystems)(d8000c)的商业试剂盒测量炎性细胞因子il-8,这是elisa方法。在每种情况下,将该测量进行两次。以570nm作为参比,通过测量450nm波长处的吸光度或光密度(od)来获得滴定原始数据。
e)-通过使用il-8标准品的浓度范围确定样品中测量的il-8的浓度。将针对il-8标准品(pg/ml)获得的od数据绘制在横坐标轴为浓度且纵坐标轴为od的标准曲线中,并使用校准直线(calibrationstraightline)通过从每个数据中减去空白平均值从od数据确定il-8量(pg/ml或ng/ml)。
od《样品》=od原始数据-od平均值《空白》
将每种条件的定量值进行平均,并且将il-8浓度(ng/ml)示出于图4中。
4)-cldn1和4免疫染色
a)-通过荧光免疫染色观察这些蛋白的表达,荧光免疫染色是涉及用两种抗体检测靶蛋白的检测方法:第一个(一级抗体)对蛋白具有特异性,因此检测蛋白;然后,二级抗体,特异于一级抗体,允许检测蛋白-一级抗体络合物并发射荧光。以这种方式,可以观察到靶组织中的靶蛋白(在此是表皮皮肤)的表达谱。
b)-在免疫染色之前,用低温恒温器切割冷冻保存的外植体。将冷冻的横截面封装在载玻片上并冷冻保存。
c)-为了开始免疫染色,将载玻片解冻并用丙酮固定。然后用来自与二级抗体(圣克鲁斯公司(santacruz))相同物种的血清封闭(“blocked、blocking”)一级抗体的非特异性固定位点。在室温下用靶向密蛋白1或4(分别为圣克鲁斯公司sc-81796或sc-17664)的一级抗体孵育后,将横截面用偶联于荧光染料(alexa型,invitrogentm,488或546nm,绿色或红色)和dapi(rochetm,对dna特异的蓝色荧光标记)的二级抗体孵育,从而为细胞核着色。
d)-最后,用封片剂(达科公司(dako))“封装”载玻片,该封片剂提供荧光保护并且使盖玻片粘附到载玻片上。在荧光光学显微镜(奥林巴斯公司ck40)下用x40物镜观察载玻片,其中对荧光染料(fitc绿色或tritc红色)或对dapi(蓝色)使用适当的滤光片。使用archimedlogiciel(维视公司(microvision))完成图像采集。
e)-对于这两种染色中的每一种,进行一级抗体的特异性对照,即同种型对照。在一个补充横截面载玻片上,使用来自相同物种的一级抗体(igg,圣克鲁斯公司)的非特异性免疫球蛋白血清代替一级抗体。
f)-制作组织学对照以验证皮肤外植体的组织完整性、污染与否、处理与否(检查接受的组织质量和通过处理没有组织结构恶化)。将外植体固定并在处理结束时保存在4%甲醛中(每种条件一个)。然后将外植体包括在石蜡中,将横截面封装在载玻片上,并用苏木精/伊红/蕃红(或hes)着色。
5)-结果
a)-组织学分析
(i)-在全身应用bap污染物的情况下观察到密蛋白1的降解(抑制表达和啮合失效)。
(ii)-hcr提取物恢复了污染物引起的恶化。
(iii)-bap污染物的应用也降低了密蛋白4的表达(结构损害,荧光强度降低:更薄和不太厚的区域)。
(iv)-hcr提取物的全身应用恢复了由污染物引起的啮合失效。
b)-从皮肤外植体释放的il-8的滴定
(i)-污染与否后的il-8滴定结果示出于图4中。其中,数据表示为il-8浓度。与未污染的对照(黑色星)相比,或与污染的对照(红色星)相比,指示出了显著性。
(ii)-污染后,刺激细胞因子释放:+59%显著(*)(与未处理的/未污染的对照相比的污染的对照)。使用pma刺激(促炎参比分子),无污染,刺激细胞因子释放:+224%非常高显著的(***)(与未处理的/未污染的对照相比)。
(iii)-随着hcr提取物的全身应用,il-8释放在两种情况下均受到抑制:污染的或未污染的。没有污染,这种效果是-69%并且非常高显著的(***,与未处理的/未污染的对照相比)。有污染,由污染物诱导的il-8产生受到hcr提取物的应用的抑制:-69%,非常高显著的(***,与污染的对照相比)。
c)-结果证明了hcr提取物对抗由污染诱导的炎性应激介质的功效。因此,可以得出结论,hcr提取物有效地保护由污染物诱导的皮肤的炎症应激,以及参与维持组织完整性、内稳态和表皮屏障功能的蛋白经历的降解。
实例5:hcr提取物对正常人角质化细胞产生β-内啡肽的效果的评估
1)-背景信息
本研究的目的是评估四种hcr提取物对正常人角质化细胞(nhk)的β-内啡肽(或β-ep)的体外效果,该角质化细胞是从30岁的供体(高加索女性)的腹部皮肤表皮中提取的。β-内啡肽是在处理40小时后通过elisa技术在培养上清液中测量的神经肽。如实例2中所述,先前进行xtt测定以检查细胞活力,以确定待测试的浓度。
2)-剂量确定(通过xtt测定的细胞毒性/活力检查)和评估的测试化合物
a)-如实例2中所述进行用xtt测定的剂量确定,但是在处理24小时后[代替实例§c)中的48小时]。
b)-细胞接种和处理
在处理前24小时,在96孔微板中,在完全ksfm(含有抗生素和生长补充剂的角质化细胞无血清培养基)中,将细胞以12,500个角质化细胞/孔(相当于37,500个细胞/cm2,该细胞密度在研究后期使用)接种(在37℃孵育;5%co2)。在基础(即非补充)培养基(不含生长补充剂的ksfm)中,以一式三份对测试化合物的每种浓度进行测试。孵育时间为24小时(在37℃/5%co2下)。
3)-通过角质化细胞产生β-内啡肽
a)-将nhk接种在24孔板中,并且在40小时期间用不同浓度的测试化合物处理。通过来自uscn生命科学公司(uscnlifescience)(cea806hu)的elisa测定法在培养上清液中测量β-ep。还在细胞沉淀中测量总蛋白,以为了将β-ep滴定报告至总蛋白量。使用2mm的dbampc(n-6,2'-o-二丁酰基腺苷3',3'-环单磷酸,西格玛公司d0627)作为阳性对照。
b)-细胞处理和β-ep测定
在处理前48小时,将细胞以75000个细胞/孔(37500个细胞/cm2)在24孔板中,在完全ksfm中接种(在37℃/5%co2下孵育)。在基础ksfm中以一式三份测试每种测试化合物的浓度,该培养基添加了分子的抗蛋白酶混合物(亮抑酶肽、抑肽酶和苯甲基磺酰氟或pmsf,分别地是西格玛公司l8511、a1153和p7626)。这种混合物允许保护β-ep蛋白直至滴定。孵育时间为40小时(在37℃/5%co2下)。收集培养上清液和细胞沉淀物并在测试前储存在-20℃。
c)-在450nm下测量吸光度数据(或光密度,od)。以一式两份对每个样品进行测定,因此每个样品有六个值(未处理的对照和参比分子除外,其分别有8个值和2个值)。
d)-蛋白滴定(bca测定)
通过基于二辛可宁酸的比色方法平行进行细胞沉淀中的总蛋白滴定。二辛可宁酸(bca)测定的原理类似于lowry方法,因为两者都依赖于在碱性条件下形成蛋白-cu2+络合物,随后将cu2+还原为cu+。bca对cu+离子具有高度特异性,并且在碱性环境中与cu+形成紫蓝色络合物,从而为监测蛋白对碱性cu2+的还原提供了基础。bca-cu+络合物的还原量与存在的蛋白成比例,并且通过分光光度讲座(570nm长波)定量。使用的蛋白滴定试剂盒(西格玛公司bca1)由二辛可宁酸溶液(西格玛公司b9643)和五水合硫酸铜溶液(cuso4-西格玛公司c2284)组成。标准范围用bsa(牛血清白蛋白–西格玛公司a9418)制备。
e)-将细胞沉淀物在-20℃下干燥保存,等待细胞裂解和滴定。为了裂解细胞并使反应环境碱化,将细胞沉淀物在室温下平衡,并且然后在碱性溶液中裂解30分钟。通过将试剂(二辛可宁酸+cuso4)的混合物添加至裂解物(溶解的细胞沉淀物)的等分试样实现滴定。将板在37℃孵育,并且在停止反应后将板在4℃下放置几分钟,然后在570nm长波下进行讲座。
f)-结果的表示
对于β-ep和蛋白两者滴定,将各自的标准品获得的od数据绘制在图形上以确定标准曲线。然后,可以确定样品中测量的蛋白或β-ep的量/浓度。将每种条件的定量值进行平均。将量/浓度(对于β-ep的pg/ml和对于总蛋白的μg/孔)的结果示出于图5、6和7中。
4)-结果
a)-剂量确定(通过xtt测定的细胞毒性/活力检查)
对于成纤维细胞中0.0005%和0.01%hcr(de)之间的测试浓度没有观察到细胞毒性:
b)-β-内啡肽滴定
用hcr提取物处理对角质化细胞的β-ep释放产生有益效果,随着两种测试的浓度出现诱导:在0.001%时是+102%***以及在0.005%时是+259%**。结果示出于图5中。
c)-总蛋白滴定
报道为总蛋白量,证实了用hcr提取物处理后观察到的角质化细胞对β-ep释放的有益作用,因为用两种测试的浓度使刺激显著:在0.001%时是+120%***以及在0.005%时是+402%**。
正常人角质化细胞,β-内啡肽(β-ep)产生并且在进行滴定的培养上清液中释放。用hcr提取物(0.001%和0.005%)处理正常人角质化细胞诱导β-ep释放的刺激。
实例6:hcr提取物对b16细胞中黑素生成的效果(黑素滴定)的评估
1)-背景信息
本研究的目的是评估hcr提取物对鼠b16黑素细胞体外模型中黑素生成的效果。在此研究中使用的细胞是从鼠皮肤提取的鼠黑素细胞(b16-f0系,lgc标准,atcc-crl-6322)。此细胞系合成释放到培养基中的(所谓的上清液)大量黑素,因此通过分光光度法进行滴定很容易实现。将这些黑素细胞培养为单层细胞;在72小时期间应用测试化合物,并且然后释放合成的黑素并在上清液中测量。如实例2中所述,先前进行xtt测定以检查细胞活力,以确定待测试的浓度。
2)-剂量确定(通过xtt测定的细胞毒性/活力检查)和评估的测试化合物
a)-如实例2中所述进行用xtt测定的剂量确定,但是在处理72小时后[代替实例§c)中的48小时]。
b)-细胞接种和处理
在处理前24小时,将细胞接种到96孔微板(细胞密度为每孔10,500个细胞,即31,250b16/cm2,该细胞密度在研究后期使用)中(在37℃/5%co2下孵育)。以一式六份对测试化合物的每种浓度进行测试。孵育/处理时间为72小时(在37℃/5%co2下)。将细胞接种并在杜氏改良培养基中或在不含有酚红(gibco11880),含有抗生素(gibco15140)、l-谷氨酰胺(gibco25030)和补充有10%的胎牛血清或fbs(gibco10270)的dmem中处理。
3)-对黑素生成的效果的评估
a)-测定原理
将b16黑素细胞接种在24孔板中。然后用测试化合物(三种浓度)处理细胞72小时。最后,进行黑素和总蛋白滴定。每24小时培养的细胞的照片也允许在提取物应用中观察黑色素释放(72h)。在此研究中使用阳性对照:
-抑制黑素生成的参比分子(酪氨酸酶抑制剂),1mm的曲酸(西格玛公司k3125),以及相反的,
-刺激色素淀积的参比分子(camp刺激剂),100nm的αmsh类似物(即所谓的美拉诺坦(西格玛公司m8764,[nle4,d-phe7]-α-黑素细胞刺激性激素三氟乙酸盐))。
这些参比的效果是可见的,对于两者在刚处理48h时就可见,并且对于曲酸在处理72h时可见。测试三种提取物的浓度(干提取物或de的重量/体积%)。根据从xtt测定获得的结果测试这些非细胞毒性剂量。
b)-细胞处理和黑素滴定
在处理前一天,在与前述相同的培养基中,将细胞接种到24孔板(细胞密度为每孔中60,000个细胞,即31,250b16/cm2)中(在37℃/5%co2下孵育)。然后以一式三份持续72h测试每种测试化合物的浓度/剂量(在37℃/5%co2下孵育)。每24小时观察培养基的着色,并且与空白(具有处理培养基但没有细胞的孔)进行比较。处理48或72小时后,将上清液均化,并且将等分试样转移到96孔板中,在492nm波长下进行分光光度法读数(以一式两份读数)。此滴定允许相对于标准范围的合成黑素(m0418)来量化由b16细胞释放的黑素。
c)-总蛋白滴定(bca测定)
如实例5中所述,通过基于二辛可宁酸的比色方法平行进行细胞沉淀中的总蛋白滴定。
d)-结果的表示
对于黑素和蛋白两者滴定,将各自的标准品获得的od测量值绘制在图形上以确定标准曲线。然后,可以确定样品中测量的蛋白或黑素的量/浓度。将每种条件的定量值进行平均。不同浓度的hcr提取物的结果示出于图8至13中
4)-结果
a)-剂量确定(通过xtt测定的细胞毒性/活力检查)
对于成纤维细胞中0.0005%和0.01%hcr(de)之间的测试浓度没有观察到细胞毒性:
b)-黑素滴定
在这些实验中,脱色曲酸(1mm)的阳性参比诱导培养基中黑素释放的非常强和非常高显著(***)的抑制(超过90%)。处理48h后,促色素淀积美拉诺坦(100nm)的阳性参比诱导培养基中黑素释放的强且高显著(**)(超过两倍)的刺激(结果未详细示出)。在72h,黑素释放比在48h更明显(od超过20倍更高),这是正常的,并且允许在48h观察潜在的促色素淀积效果。在此模型中处理72h后,测试的hcr提取物显示出两种最高测试浓度的明显脱色效果。在此模型中应用72h后,hcr提取物抑制黑素释放,具有剂量效应:在统计学上非常高显著(***)的-86%和-45%,分别使用0.1%和0.05%的de(干提取物,相当于1mg/ml和0.5mg/ml)。在本评估中,表示了在72h期间通过处理b16黑素细胞的黑素生成的良好模型,hcr提取物允许抑制黑素合成。因此,发现hcr提取物有效减少黑素释放,因此能够防止阳光诱导的色素斑(即不规律和不均匀的色素淀积)。
实例7:hcr提取物在正常人角质化细胞中的抗氧化潜力的评估(使用h2dcfda探针进行ros检测)
1)-背景信息
本评估的目的是评估提取物hcr的抗氧化和抗污染作用,使用h2dcfda探针,对从腹部整形手术(62岁高加索女性供体)提取的正常人培养的角质化细胞中的氧化应激进行评估。二氯二氢荧光素二乙酸酯探针(h2dcfda/二氯荧光素二乙酸酯)是荧光素的化学还原形式,用作细胞中活性氧物类(ros)的指示物。它具有细胞渗透性和稳定性。当它穿透细胞时,乙酸酯基团被胞内酯酶切割。所得产物是非荧光的二氯二氢荧光素(或h2dcf)。在ros(o2-、oh、no、onoo……)存在下,即通过氧化,将其转化为高荧光产物二氯荧光素(或dcf)。探针氧化对一种类型的ros不具有特异性。在490nm(激发)和525nm(发射)的波长下检测荧光。氧化应激由环境污染物苯并芘(3,4-苯并芘/bap)或由活性氧物类(ros)(过氧化氢(含氧水/h2o2))的参比发生器诱导。如实例2中所述,先前进行xtt测定以检查细胞活力,以确定待测试的浓度。
2)-抗氧化效应(h2dcfda探针)的评估
a)-测定原理
将正常人角质化细胞接种在96孔微板中,并且然后用待测试的测试化合物处理24小时,然后添加荧光探针用于检测ros并通过污染物或过氧化氢刺激或不刺激。此测试基于检测系统(在与ros接触时降解并发出荧光的探针)的使用。此探针h2dcf-da通过细胞酯酶裂解两个ch3-cooh基团;然后探针遇到细胞中存在的ros,并且松落两个氢原子成为荧光dcf。
b)-细胞处理和黑素滴定
将细胞以10,000个角质化细胞/孔(30,000个细胞/cm2)接种于96孔微板中的完全ksfm培养基中,并使其在37℃/5%co2下粘附24小时。用3种非细胞毒性浓度的待测试提取物(以一式六份,在非补充培养基中)处理细胞24小时,并与对照条件(未处理的对照或抗氧化剂阳性参比)平行在37℃/5%co2下孵育。在此研究中使用内部抗氧化剂阳性参比,以10μm使用。
c)-探针掺入
洗涤细胞后,应用探针(英杰公司d399,在非补充ksfm中以50μm稀释),并将板在37℃/5%co2下孵育45分钟。空白孔在没有细胞的情况下进行(但是使用探针和测试的产品)。
d)-ros刺激
洗涤细胞后,将bap(西格玛公司crm40071)或过氧化氢溶液(西格玛公司h1009)应用于预期的孔中(刺激条件,最终分别在36μm和1mm,在非补充ksfm中)。对于其他孔(非刺激的条件),仅应用培养基。将板在37℃/5%co2下孵育20分钟。
e)-结果的表示
孵育后,在490nm(激发)和525nm(发射)波长读取荧光(tecansafireii酶标仪)。数据表示为rfu(荧光单位)。收集数据并减去平均空白数据。
rfu《样品》=rfu原始数据-rfu平均值《空白》
3)-结果
具有或不具有ros刺激(通过过氧化氢或bap)的抗氧化潜力测定的结果显示在图14和15中。其中,数据以荧光单位(rfu)表示。显著性(t-检验)表示相对于未刺激的对照(未处理的丙酮溶剂对照:黑色星),或相对于h2o2或bap刺激的对照(红色星)。空白对照(没有细胞但含有测试化合物)允许验证测试的提取物或阳性参比和h2dcf-da探针之间不存在相互作用。没有ros刺激,在任何不同的测试中都没有观察到效果。使用过氧化氢处理,细胞产生自由基,因为刺激了+808%的ros产生(相对于未刺激的对照)。应用bap,还观察到+141%的刺激(相对于未刺激的丙酮溶剂对照)。关于所使用的参比分子,通过ros刺激,观察到抗氧化效果并且其是显著的,因为ros产生降低-21%(*用h2o2)和-33%(*用bap)。测试的hcr提取物在0.01%的浓度下显示出功效,因为此最高测试浓度允许抑制由bap污染物刺激的ros产生(检测到ros的减少):-23%,几乎显著(p=0.122)。因此,本评估显示,在最高测试浓度(0.01%)下测试的hcr提取物显示出抗氧化和抗污染潜力。
实例8:姜花根提取物(hcr提取物)对用蓝光辐射的成纤维细胞自体吞噬活性的效果(mdc测定)的评估
1)-背景信息
该研究的目的是评估一种hcr提取物对用453纳米蓝光辐射的成纤维细胞的自体吞噬活性的效果。将细胞(正常人成纤维细胞或(nhf))作为原代单层培养。在辐射前24小时期间应用待测试的产品,并且然后在24小时期间应用待测试的产品,然后测量自体吞噬(mdc)。
溶酶体是胞质器,其允许超过其寿命或不再有用的细胞材料的再循环。它们的主要功能是在真核细胞中消化内源或外源底物(所谓的自体吞噬)。溶酶体将细胞废物、脂肪、碳水化合物、蛋白和其他大分子分解成小的化合物,作为新的细胞构建材料转移回细胞质。实际上,它的脂质膜含有许多酶、质子泵和转运蛋白。调节酸性ph以允许实现酸性水解酶的最佳活性[1]-[2]。荧光lysotracker探针的结构很容易插入活细胞(荧光团与在中性ph下仅部分质子化的弱碱连接)。此特征允许此标记/染色对酸性细胞器(即溶酶体)具有高选择性[3-5]。然后,可以评估在溶酶体水平上的辐射(例如像蓝光)的效果。实际上,这些辐射导致自由基形成并影响正常的溶酶体网络,其在细胞空间中的分布。这可以通过特定的荧光探针lysotracker进行可视化。自体吞噬是真核细胞过程,该过程允许细胞质物质在与溶酶体融合的液泡中消化。实际上,溶酶体可以直接(微自体吞噬)、或经由称为自噬体(巨自体吞噬,溶酶体和自噬体的融合是所谓的自溶体)的自体吞噬泡掺入细胞质片段。自体吞噬是一种重要的机制,该机制允许细胞动员其能量储备来防御和破坏其受损的细胞器,并且然后避免严重影响。此过程允许蛋白和非功能性细胞器的消除和替换,然后以确保内稳态。它是种必要的细胞保护机制,允许自适应细胞对不同类型的应激或损害(如营养缺乏(饥饿))作出应答。因此是细胞存活,还有其他基本的生理现象,如发育、免疫、细胞分化(包括表皮中的角质化细胞分化为角质细胞)所必需的。它涉及寿命控制、老化和病理学的发展,如癌症或糖尿病、感染、代谢或神经退行性疾病[6-7]。mdc探针对自噬体具有特异性,并且允许轻松和特异地量化自体吞噬活性[8]。
2)-测定原理
a)-为了评估提取物hcr对自体吞噬活性的效果,将成纤维细胞接种在96孔板中并用产物处理、辐射,再次处理,并且然后mdc探针允许测量自体吞噬活性。本研究中使用了两种阳性参比,已知抗氧化剂可防止uv辐射引起的氧化应激:维生素c(l-抗坏血酸,西格玛公司a4544)500μm(88μg/ml)和维生素e(α-醋酸生育酚,西格玛公司a1157)200μm(95μg/ml)。测试提取物hcr的三种浓度(干提取物或de的重量/体积%,因为它是液体提取物),每个剂量以一式五份评估(5个孔)。453nm蓝光的辐射剂量为40j/cm2(23mw/cm2,持续29分钟)。
b)-在处理前24小时,将细胞接种到96孔微板(细胞密度为每孔10,000个细胞,即30,000nhf/cm2)中(在37℃/5%co2下孵育)。
然后将细胞用提取物处理24小时(预防性的效果),然后辐射或不辐射(453nmbl,40j/cm2,23mw/cm2,持续29分钟)。然后用产物再次处理成纤维细胞(治愈作用)持续另外24h(因此总应用是48h)。将细胞接种于完全培养基中:杜氏改良培养基或dmem(gibco41966),含抗生素(gibco15140)和10%的胎牛血清或fbs(gibco10270)。在没有fbs的培养基中进行处理。在pbs(磷酸盐缓冲盐水)中进行辐射。所有次数的孵育/处理均在37℃/5%co2(辐射除外,在室温下进行)。
c)-自体吞噬活性评估(mdc测定)
在处理结束时,将孔精细冲洗(pbs)并在细胞上应用0,05mmmdc探针(西格玛公司30432)[17](37℃/5%co2)。在孵育(30分钟期间)并洗涤后,在380nm(激发)和525nm(发射)波长处测量荧光(tecansafireii机)。获得的数据表示为rfu(真实荧光单位)。完成空白(含有探针但没有细胞的孔)。
3)-结果表示
将所有数据减去空白平均值,然后针对每个条件计算rfu平均值。将数据与适当对照(未辐射的或辐射的)获得的数据进行比较,通过学生t检验(t-检验)计算显著性。
4)-结果
结果指示于下表1中:
表1:hcr提取物处理对由蓝光(435纳米)辐射的成纤维细胞的自体吞噬活性的效果。学生检验:(*):0,01<p≤0,05(**):0,001<p≤0,01(***):p≤0,001
5)分析和评论
结果显示,当由蓝光(波长为453纳米)辐射成纤维细胞时,自体吞噬活性增加。当用维生素c或维生素e处理并在453纳米处辐射时,用维生素c的成纤维细胞的自体吞噬活性下降14%,用维生素e的成纤维细胞的自体吞噬活性下降22%。当用不同重量浓度的hcr提取物(即0.001%、0.005%和0.01%)处理时,所述成纤维细胞的自体吞噬活性分别下降约13%、15%和35%。
参考文献
[1]:geneexpressionprofilingrevealsarylhydrocarbonreceptorasapossibletargetforphotobiomodulationwhenusingbluelight.beckera,klapczynskia,kuchn,arpinof,simon-kellerk,delatorrec,stichtc,vanabeelenfa,oversluizeng,gretzn.scirep.2016;6:33847.
[2]:animalcellstructure.lysosomes.davidsonmw.molecularexpressions[online].2015.urlhttp://micro.magnet.fsu.edu/cells/lysosomes/lysosomes.html
[3];real-timevisualizationofphotochemicallyinducedfluorescenceof8-halogenatedquinolones:lomefloxacin,clinafloxacinandbay3118inlivehumanhacatkeratinocytes.kokereb,bilskipj,mottenag,zhaob,chignellcf,heyy.photochemphotobiol.2010;86(4):792-797.
[4]:aninsightintothemechanismsofthephototoxicresponseinducedbycyamemazineinculturedfibroblastsandkeratinocytes.morlièrep,haiglej,aissanik,filipep,silvajn,santusr.photochemphotobiol.2004;79(2):163-71.
[5]:screeningofeffectivepharmacologicaltreatmentsformelassyndromeusingyeasts,fibroblastsandcybridmodelsofthedisease.garrido-maraverj,corderomd,
[6]:autophagyfightsdiseasethroughcellularself-digestion.mizushiman,levineb,cuervoam,klionskydj.nature.2008;451(7182):1069-75.
[7]:autophagyandhumandiseases.jiangp,mizushiman.cellres.2014;24(1):69-79.
[8]:monodansylcadaverine(mdc)isaspecificinvivomarkerforautophagicvacuoles.biederbicka,kernhf,
- 还没有人留言评论。精彩留言会获得点赞!