一种治疗疟疾的药物组合物的制作方法
本发明属于药学领域,涉及一种中药组合物,具体涉及一种治疗疟疾的药物组合物。
背景技术:
疟疾是严重威胁人类健康和生命安全的重大传染病,在全世界108个国家和地区传播流行,全球约半数人口受到疟疾的威胁,为世界三大公共卫生问题之一。根据who2016年世界疟疾报告,全球约有32亿人(占全世界总人口近一半)面临疟疾风险,2015年共有2.14亿疟疾新病例,大约43.8万人死于疟疾。同时疟原虫的抗药性也使疟疾药物治疗面临的严重挑战。为提高临床疗效,延缓抗药性的产生,who自2001年开始推广基于青蒿素类抗疟药的联合治疗方案(artemisinin-basedcombinationtherapies,acts),同时禁止单独使用青蒿素类抗疟。2006年who发布的第1版疟疾治疗指南中明确推荐了5种以青蒿素类药物为基础的acts药物组合。联合药物治疗是当今抗击疟疾的主要方式,2015年全球act采购量达到3.11亿份,但近年新型药物组合的研发进展缓慢,2015年发布的第3版疟疾治疗指南中仍然是10年前的5种acts药物组合。一旦疟原虫在大范围内对目前的acts产生抗药性,疟疾将面临无药可治的困境,新型复方抗疟药物研制面临重大挑战。
脑型疟(cerebralmalaria,cm)是恶性疟最严重的并发症之一,74%的脑型疟病例发生在五岁以下非洲儿童,死亡率为15-20%(who,worldmalariareport2015)。脑型疟临床可出现轻偏瘫、抽搐、共济失调、昏迷及意识障碍、脑膜刺激征等。大多数儿童脑型疟患者在中枢神经系统症状发作后一天内死亡,幸存儿童中有10-20%出现持续性神经功能缺损、认知功能障碍、行为障碍以及运动功能损伤等神经系统后遗症。目前认为,感染疟原虫红细胞堵塞脑血管所致脑组织局部微循环障碍及继发免疫病理损伤是脑型疟最主要发病机制。
青蒿琥酯被认为是治疗严重疟疾最有效的药物。静脉注射青蒿琥酯是who推荐的脑型疟首选治疗方案,作为目前一线治疗药物,除抗疟活性外,青蒿琥酯还具有抗炎作用,但青蒿琥酯单药治疗后再燃率可达10%-100%。
川芎嗪是川芎的主要活性成分,现代研究发现川芎嗪主要有治疗缺血性中风、头痛、高血压、冠状粥样硬化性心脏病(冠心病)、偏头痛、缺血性脑病等作用。
我们经过长时间的研究后,得到一种疗效更加显著的抗疟药物。
技术实现要素:
本发明的目的在于提供一种治疗疟疾的药物组合物。该药物具有疗效好、见效快、质量稳定、可改善神经损伤症状的特点。
本发明所述的药物组合物,含有青蒿琥酯,川芎嗪或其药用盐。
具体的,青蒿琥酯:川芎嗪或其药用盐的重量比为1-10:10-1;
优选的,青蒿琥酯:川芎嗪或其药用盐的重量比为1-2:2-1。
进一步优选的,青蒿琥酯:川芎嗪或其药用盐的重量比为2:1。
其中,所述川芎嗪的药用盐优选为盐酸川芎嗪。
其中,青蒿琥酯和川芎嗪或其药用盐都属于现有产品,可以在市场上购买到,也可以通过常规方法制备得到。
本发明的另一个目的在于提供药物组合物的制备方。
本发明的制备方法,包括以下步骤:
(1)青蒿琥酯粉末,加入5%碳酸氢钠溶液振摇,待完全溶解后,加0.9%氯化钠注射液稀释,
(2)川芎嗪或其药用盐加0.9%氯化钠注射液振摇,至完全溶解,
(3)将上述两个步骤所得的溶液,混合均匀。
优选的,本发明的制备方法,包括以下步骤:
(1)青蒿琥酯,加0.9%氯化钠注射液,完全溶解,加0.9%氯化钠注射液稀释,
(2)盐酸川芎嗪加0.9%氯化钠注射液振摇,至完全溶解,
(3)将上述两个步骤所得的溶液,混合均匀。
本发明另一个目的在于提供一种药物制剂。
本发明的药物制剂,包括药物组合物,和药学上可接受的载体。
其中,药学上可接受的载体以重量计可以是制剂总重量的0.1-99.9%。
本发明的药物制剂,可以制备成任何药用剂型,药用剂型包括:片剂、糖衣片剂、薄膜衣片剂、肠溶衣片剂、胶囊剂、硬胶囊剂、软胶囊剂、口服液、口含剂、颗粒剂、丸剂、散剂、膏剂、丹剂、混悬剂、溶液剂、注射剂、栓剂、软膏剂、硬膏剂、霜剂、喷雾剂、贴剂、经鼻给药的剂型。
优选剂型为滴鼻剂。
本发明的给药方式,包括:注射给药、口服给药和鼻腔给药,优选为鼻腔给药。
其中,所述药学上可接受的载体包括:甘露醇、山梨醇、山梨酸或钾盐、焦亚硫酸钠、亚硫酸氢钠、硫代硫酸钠、盐酸半胱氨酸、巯基乙酸、蛋氨酸、维生素a、维生素c、维生素e、维生素d、氮酮、edta二钠、edta钙钠,一价碱金属的碳酸盐、醋酸盐、磷酸盐或其水溶液、盐酸、醋酸、硫酸、磷酸、氨基酸、氯化钠、氯化钾、乳酸钠、木糖醇、麦芽糖、葡萄糖、果糖、右旋糖苷、甘氨酸、淀粉、蔗糖、乳糖、甘露糖醇、硅衍生物、纤维素及其衍生物、藻酸盐、明胶、聚乙烯吡咯烷酮、甘油、丙二醇、乙醇、土温60-80、司班-80、蜂蜡、羊毛脂、液体石蜡、十六醇、没食子酸酯类、琼脂、三乙醇胺、碱性氨基酸、尿素、尿囊素、碳酸钙、碳酸氢钙、表面活性剂、聚乙二醇、环糊精、β-环糊精、磷脂类材料、高岭土、滑石粉、硬脂酸钙、硬脂酸镁、微晶中一种或以上;优选所述的载体为微晶纤维素、乳糖、淀粉、羧甲基纤维素钠、低取代羟丙基纤维素、滑石粉中一种或以上。
本发明另一个目的在于提供该药物组合物的应用。
本发明的药物组合物在制备治疗疟疾的药物中的应用。
本发明的药物组合物在制备治疗脑型疟的药物中的应用。
本发明的药物组合物在制备治疗重症疟疾的药物中的应用。
本发明的药物组合物具有改善生存状态、降低脑血管堵塞及炎症细胞侵入,改善神经损伤症状等作用。
本发明还起到改善脑型疟过程中疟原虫在脑内蓄积引发的一系列脑缺血病变和神经功能损伤等兼变症状的作用。
本发明能够明显缓解伯氏疟原虫anka株感染导致的脑型疟的发生,延长生存时间,比单独使用更具优势。
本发明能够增加脑型疟小鼠脑部供血,减轻脑组织缺血缺氧性损伤。
本发明对小脑中微血管阻塞情况改善具有突出的作用。
青蒿琥酯在临床上用于脑型疟等重症疟疾的主要给药方法是静脉注射,但在非洲脑型疟高发地区,极端落后的医疗条件在很大程度上限制了青蒿琥酯的临床及时、有效应用。同时,青蒿琥酯具有青蒿素类药物共同的特点,即存在体内代谢快、首过效应明显、生物利用度低等问题,这些因素也在一定程度上限制了其抗疟药效的发挥,加重了治疗后的复燃问题。如果简单通过加大单次给药剂量或增加给药频次,则会促进耐药现象的发生、并可能增加药物的毒副作用。
本发明采用鼻腔给药后,有效解决现有技术中存在的问题。药物经鼻黏膜吸收可通过嗅神经通路、嗅黏膜上皮通路、血液循环通路这3条通路入脑,吸收后直接进入体循环,可免受胃肠道中酶的破坏和肝脏对药物的首过效应,平均生物利用度较高,非肽类药物的鼻腔吸收速度接近静注;且由于鼻腔与颅腔在解剖生理上的独特联系,使得药物可绕过血脑屏障进入大脑,实现脑靶向治疗;同时用药方便,患者顺应性好,适合自身给药。青蒿琥酯与川芎嗪从化学性质而言均适合鼻腔给药,且均已有文献报道,鼻腔给药吸收更快。故本发明将青蒿琥酯与川芎嗪配伍组合采用鼻腔给药的方式无论从针对脑型疟脑内靶向给药的需求、青蒿琥酯提高药物生物利用度的需求、用药方便角度的需求,两者组合后采用鼻腔给药治疗脑型疟均有很大意义。实验结果发现,青蒿琥酯与川芎嗪配伍组合鼻腔给药后在协同增效,改善动物生存状态、降低脑型疟小鼠脑血管堵塞及炎症细胞侵入,改善神经损伤症状等方面均优于腹腔给药。
附图说明
图1、模型小鼠生存时间
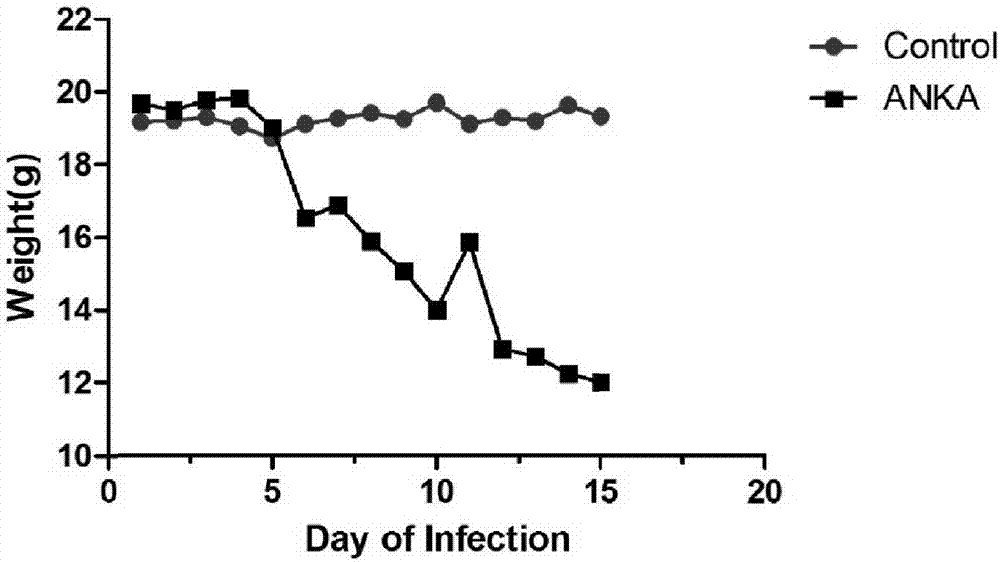
图2、模型小鼠体重增长
图3、模型小鼠虫血率
图4、模型小鼠行为学评分
图5a对照组脑微血管(he染色,20x)
图5b模型组脑微血管(he染色,20x)
图6、各组生长曲线
图7、各组体重增长曲线
图8、各组感染率
图9a、对血清炎症因子tnfa的作用,图9b对炎因子il-4的作用
图10a、模型组脑微血管(he染色,20x)
图10b、ars(ip)脑微血管(he染色,20x)
图10c、ars+cxq(ip)脑微血管(he染色,20x)
图11、各组生长曲线
图12、各组体重增长曲线
图13、各组感染率
图14、各组rmcbs评分
图15a、对血清炎症因子tnfa的作用,图15b对炎因子il-4的作用
图16a、模型组脑微血管(he染色,20x)
图16b、ars+cxq(ip)脑微血管(he染色,20x)
图16c、ars+cxq(in)脑微血管(he染色,20x)
具体实施方式
通过以下具体实施例对本发明作进一步的说明,但不作为本发明的限制。
实施例中的所有组分均可以在市场上购买到。
上述实施例只是用于对本发明的内容进行阐述,而不是限制,因此在与本发明的权利要求书相当的含义和范围内的任何改变,都应该认为是包括在权利要求书的范围内。
下述试验例中所用青蒿琥酯+川芎嗪为本发明实施例1,青蒿琥酯:川芎嗪=2:1。
试验例1、
实验性脑型疟模型建立:
6-8周龄雌性健康c57bl6小鼠,腹腔接种1×106个伯氏疟原虫anka株感染的红细胞(prbc),记为感染第0天。连续观察16天,观察脑型疟症状及死亡情况。
实验分组:
c57bl6小鼠分为2组,分别为①对照组(control),②模型组(anka),每只小鼠腹腔接种1×106个prbc。
评价指标:
1、生存曲线:逐日观察小鼠生存情况,12天后绘制生存曲线、体重变化。存活率=存活实验小鼠/总实验小鼠。
2、原虫率:实验小鼠感染3d后开始每天计算原虫率,方法为:取感染小鼠尾静脉血1小滴于洁净载玻片上制作薄血片,甲醇固定风干,giemsa染液染色15min后冲洗晾干,于100x油镜下进行计数.原虫率=prbc/总红细胞数;
3、脑微血管阻塞评价:感染后12天后取脑组织,用4%中性福尔马林固定将组织切成4μm切片,he染色,观察。根据梗阻的严重程度和微出血情况,使用半定量量表(0-5)对包含血管部位进行评分:0,无梗阻;1,部分阻塞;2,存在附着于内皮的白细胞;3,存在局部阻塞,白细胞和红细胞并存;4,完全阻塞,无出血;5,全身阻塞。数据表示为每个脑的平均分。
4、行为学评分将小鼠置于长×宽×高=31.8×19.8×10.5cm白盒内(底面方格),准备3mm直径的直杆用于触碰小鼠。采用下列标准进行评分。
rmcbs评分表:
根据rmcbs评分表对造模后的小鼠隔天对协调能力、探索行为、力量和骨骼、反射和自我保护和卫生行为五个方面共七项指标进行测试,并给予0~2分的评分。各项之和作为总评分,七项总分14分,分数越低表示神经功能损伤越严重。实验结果:
1、模型小鼠生存时间:
与对照组相比,anka组小鼠生存时间明显缩短,如图1所示,红色曲线为对照组,黑色曲线为anka。
2、模型小鼠体重增长:
与对照组相比,anka组小鼠体重明显减轻,如图2所示,红色曲线为对照组,黑色曲线为anka。
3、模型小鼠虫血率:
与对照组相比,anka组小鼠原虫血率显著增高,如图3所示,红色曲线为对照组,黑色曲线为anka。
4、模型脑微血管阻塞评价:
与对照组相比,anka组小鼠海马和小脑组织中脑微血管堵塞,如图4所示。
试验例2、
青蒿琥酯(art)与青蒿琥酯+川芎嗪(art+cxq)对实验性脑疟的保护作用
实验分组:
c57bl6小鼠分为3组,分别为①模型对照组(control)②青蒿琥酯腹腔注射组(artip)③青蒿琥酯+川芎嗪腹腔注射组(art+cxqip)。每只小鼠腹腔接种1×106个prbc建立脑型疟后,给药组小鼠分别在接种的前一天、第一天、第三天、第五天经腹腔注射给药4次。
评价指标:
1、逐日观察小鼠生存情况,12天后绘制生存曲线、体重变化
2、逐日取血涂血片,镜检计算感染率。
3、感染后12天后取血,离心取上清检测炎症因子。
4、感染后12天后取脑组织,用4%中性福尔马林固定。将组织切成4μm切片,he染色,观察脑微血管阻塞情况。
实验结果:
1、对小鼠生存时间的影响:
与模型对照组相比,青蒿琥酯腹腔注射组、青蒿琥酯+川芎嗪腹腔注射组均能够显著延长小鼠生存时间,青蒿琥酯+川芎嗪腹腔注射组优于青蒿琥酯单用组,如图6所示,黑色曲线为对照组,绿色曲线为青蒿琥酯腹腔注射组,蓝色曲线为青蒿琥酯+川芎嗪腹腔注射组。
2、对小鼠体重增长的影响:
与模型对照组相比,青蒿琥酯腹腔注射组、青蒿琥酯+川芎嗪腹腔注射组均能够显著增加小鼠体重,如图7所示,12d末青蒿琥酯+川芎嗪腹腔注射组体重增加显著。
3、对小鼠虫血率的影响:
与模型对照组相比,青蒿琥酯腹腔注射组、青蒿琥酯+川芎嗪腹腔注射组均能够降低小鼠原虫血率,如图8所示,2组作用相当。
4、对小鼠血清炎症因子的影响:
与模型对照组相比,青蒿琥酯+川芎嗪腹腔注射组能够降低小鼠血清炎症因子tnfa,对抗炎因子il-4有增高趋势。如图9所示。
5、对脑微血管阻塞的影响
与模型对照组相比,青蒿琥酯腹腔注射组、青蒿琥酯+川芎嗪腹腔注射组均能显著减轻小鼠海马和小脑组织中脑微血管堵塞,如图10所示,青蒿琥酯+川芎嗪腹腔注射组优于青蒿琥酯腹腔注射组。
试验例3、
青蒿琥酯+川芎嗪(art+cxq)不同给药途径对实验性脑疟的保护作用比较
实验分组:
c57bl6小鼠分为3组,分别为①模型对照组(control)②青蒿琥酯+川芎嗪腹腔注射组(art+cxqip)③青蒿琥酯+川芎嗪鼻腔给药组(art+cxqin)。每只小鼠腹腔接种1×106个prbc建立脑型疟后,给药组小鼠分别在接种的前一天、第一天、第三天、第五天经腹腔注射或鼻腔给药4次。
评价指标:
1、逐日观察小鼠生存情况,12天后绘制生存曲线、体重变化
2、逐日取血涂血片,镜检计算感染率。
3、4天后进行小鼠行为学评分。
4、感染后12天后取血,离心取上清检测炎症因子。
5、感染后12天后取脑组织,用4%中性福尔马林固定。将组织切成4μm切片,he染色,观察脑微血管阻塞情况。
实验结果:
1、对小鼠生存时间的影响:
与模型对照组相比,青蒿琥酯+川芎嗪鼻腔给药组均能够显著延长小鼠生存时间,如图11所示,黑色曲线为对照组,蓝色曲线为青蒿琥酯+川芎嗪腹腔注射组,红色曲线为青蒿琥酯+川芎嗪鼻腔给药组。
2、对小鼠体重增长的影响:
与模型对照组相比,青蒿琥酯+川芎嗪鼻腔给药组在染毒12天时的体重增加显著,如图12所示。
3、对小鼠虫血率的影响:
与模型对照组相比,青蒿琥酯+川芎嗪腹腔注射组、青蒿琥酯+川芎嗪鼻腔给药组均能够降低小鼠原虫血率,如图13所示,2组作用相当。
4、对小鼠行为学评分的影响
与模型对照组相比,青蒿琥酯+川芎嗪腹腔注射组、青蒿琥酯+川芎嗪鼻腔给药组均能显著增高小鼠行为学评分,其中给药10d后青蒿琥酯+川芎嗪鼻腔给药组优于青蒿琥酯+川芎嗪腹腔注射组,如图14所示。
5、对小鼠血清炎症因子的影响:
与模型对照组相比,青蒿琥酯+川芎嗪腹腔注射组、青蒿琥酯+川芎嗪鼻腔给药组均能够降低小鼠血清炎症因子tnfa,对抗炎因子il-4有增高趋势。如图15所示。
6、对微血管阻塞的影响
如图16示,与模型对照组相比,青蒿琥酯+川芎嗪鼻腔给药组对小脑中微血管阻塞及出血改善作用突出。
上述仅列举本发明部分药物的药效实验,实际上,本发明其他药物也具有相同或者相似的药物效果,在此不一一列举。
虽然,上文中已经用一般性说明及具体实施方案对本发明作了详尽的描述,但在本发明基础上,可以对之作一些修改或改进,这对本领域技术人员而言是显而易见的。因此,在不偏离本发明精神的基础上所做的这些修改或改进,均属于本发明要求保护的范围。
实施例1、本发明的药物组合物
青蒿琥酯40mg,盐酸川芎嗪20mg
(1)取40mg青蒿琥酯,加1ml0.9%氯化钠注射液,完全溶解,再加3ml0.9%氯化钠注射液稀释,
(2)取20mg盐酸川芎嗪,加0.9%氯化钠注射液4ml振摇,至完全溶解,
(3)将上述两个步骤所得的溶液,混合均匀,即可。
实施例2、本发明的药物组合物
青蒿琥酯20mg,盐酸川芎嗪20mg
(1)取20mg青蒿琥酯,加1ml0.9%氯化钠注射液,完全溶解,再加1ml0.9%氯化钠注射液稀释,
(2)取20mg盐酸川芎嗪,加0.9%氯化钠注射液4ml振摇,至完全溶解,
(3)将上述两个步骤所得的溶液,混合均匀,即可。
实施例3、本发明的药物组合物
青蒿琥酯20mg,盐酸川芎嗪40mg
(1)取20mg青蒿琥酯,加1ml0.9%氯化钠注射液,完全溶解,再加1ml0.9%氯化钠注射液稀释,
(2)取40mg盐酸川芎嗪,加0.9%氯化钠注射液8ml振摇,至完全溶解,
(3)将上述两个步骤所得的溶液,混合均匀,即可。
实施例4、本发明的药物组合物
青蒿琥酯20mg,盐酸川芎嗪200mg
(1)取20mg青蒿琥酯,加1ml0.9%氯化钠注射液,完全溶解,再加19ml0.9%氯化钠注射液稀释,
(2)取200mg盐酸川芎嗪,加0.9%氯化钠注射液20ml振摇,至完全溶解,
(3)将上述两个步骤所得的溶液,混合均匀,即可。
实施例5、本发明的药物组合物
青蒿琥酯200mg,盐酸川芎嗪20mg
(1)取200mg青蒿琥酯,加10ml0.9%氯化钠注射液,完全溶解,再加10ml0.9%氯化钠注射液稀释,
(2)取20mg盐酸川芎嗪,加0.9%氯化钠注射液20ml振摇,至完全溶解,
(3)将上述两个步骤所得的溶液,混合均匀,即可。
- 还没有人留言评论。精彩留言会获得点赞!