千伏辐射治疗的制作方法
本申请要求在2017年6月2日提交的发明名称为“systemforkilovoltageradiationtherapy”的共同未决的美国临时专利申请no.62/514,466依据35u.s.c.§119(e)获得的优先权利益。以上提到的申请的公开内容以引用方式并入本文中。
背景
本公开的领域
本公开涉及将x射线辐射递送到靶病损,并且更具体地说,涉及使用治疗阳极和多个成像阳极来递送x射线辐射。
背景
艰难的经济几乎没有机会来填平大的基础设施缺口并且缺少熟练的专业人员来进行医疗服务。尽管医疗技术和数据分析迅猛增长,但许多最常见的致命疾病一直缺少定向和成本划算的治疗。在这个背景下,癌症仍是全球健康护理服务的主要负担和挑战。虽然用于癌症的标准辐射治疗系统可能对治疗大多数癌症有效,但是辐射治疗系统是昂贵且复杂的。因此,辐射治疗系统的使用在发展中国家受到严重限制,并且甚至在发达国家,辐射治疗系统的分布都通常是不均的。因此,减少用于辐射治疗的资本设备成本可能是重要的。
概要
本公开涉及递送x射线辐射。在一个实现方式中,使用治疗阳极和多个成像阳极将x射线辐射递送到靶病损。部件安装于台架上,所述台架绕所述靶病损旋转以使所递送的剂量分布在大量的健康组织上,同时基本上最大化递送到所述靶病损的剂量。
在一个实现方式中,公开一种用于朝向身体内的靶病损递送kvx射线的设备。所述设备包括:治疗阳极,所述治疗阳极被配置成接收电子束并输出所述kvx射线;电子束源,所述电子束源被配置成产生所述电子束并朝向所述治疗阳极引导所述电子束;以及一个或多个磁体,所述一个或多个磁体被配置成沿着所述治疗阳极操纵并扫描所述电子束,用水冷却所述阳极以防止所述治疗阳极过热。
在另一个实现方式中,公开一种用于朝向身体内的靶病损递送千伏(kv)x射线的方法。所述方法包括:产生电子束并朝向治疗阳极引导所述电子束;使用一个或多个磁体沿着所述治疗阳极操纵和扫描所述电子束,使得所述治疗阳极产生所述kvx射线;使用专门设计的准直器来阻挡未被引导到会聚点的所有所述kvx射线,所述会聚点的中心位于所述靶病损处;以及使所述电子束源、所述一个或多个磁体、所述治疗阳极和所述准直器绕所述靶病损旋转。
从本说明书中将显而易见其它特征和优点,本说明书举例说明了本公开的方面。
图式简单说明
可以通过查看附图来部分地了解本公开的、关于其结构和操作的细节,在附图中,相同的元件符号指代相同的部分,并且其中:
图1a是根据本公开的一个实现方式的kv辐射治疗系统的框图;
图1b是根据本公开的一个实现方式的kvx射线源的详细框图;
图1c是阳极的详细框图,所述阳极包括治疗阳极(所述治疗阳极产生治疗束)和成像阳极(所述成像阳极实现了实时成像和追踪);
图2是根据本公开的一个实现方式的kv辐射治疗系统的透视图;
图3是根据本公开的一个实现方式的包括x射线管的x射线源的详细透视图;
图4是根据本公开的一个实现方式的x射线管的剖切透视图;
图5a示出被配置成朝向会聚点引导x射线的准直器;
图5b示出准直器的正视图,在顶部具有两个缩放视图;
图6a示出使用200kvp、200makv弧形治疗(kvat)的蒙特卡罗模型病人剂量分布;
图6b示出使用15兆伏(mv)线性加速器(线性加速器)体积调控弧形治疗(vmat)的蒙特卡罗模型病人剂量分布;
图7a示出在准直器出口处的隔膜厚度固定(t=0.2mm)时准直器效率和全宽半高(fwhm)随准直器孔大小(d)而变;
图7b示出在具有适当倾斜(相对于电子束路径的平面成30°)的阳极的平面上使用大小为75×2cm2的x射线源的剂量分布,其中(d,t)=(2.3mm,0.2mm);
图8是示出根据本公开的一个实现方式的用于朝向身体内的靶病损递送kvx射线的方法800的流程图。
详细描述
过去,由于千伏(kv)x射线穿过靶病损上游的健康组织(尤其是表层皮肤)的高衰减而使kvx射线的医疗使用限于表层辐射治疗。明确地说,kvx射线的常规使用目前仅可用于表层治疗,原因是:(1)难以通过单个焦点将剂量分布于大面积上;以及(2)大多数x射线管和电源供应器用于成像目的(~120kvp)并且由于过热而无法在高功率下长时间运行的事实。虽然mv系统通常用于治疗深层病损,但是使用mv系统的成本可能非常高。mv系统还是体积大的并且可能需要大量空间来容纳所述系统。另外,来自mv系统的对靶病损的高能量辐射可能会对周围健康组织造成很多损害。
为了解决常规辐射系统和使用的上述问题,本公开的若干实现方式涉及一种kv辐射治疗系统,所述kv辐射治疗系统采用具有被设计用于实现组合的治疗与成像的准直器和检测器的扫描电子束技术。本公开的kv辐射治疗系统被配置成使用安装于台架上的扫描电子束x射线管和用水冷却的阳极来防止钨阳极损坏而克服常规辐射系统的上述问题中的两者。
实验表明,通过具有1×8mm2的焦点的130kv、600ma源,钨在0.7毫秒时开始起泡并且在暴露1.0毫秒时熔化。由于使电子束停留在钨阳极上可能会易于破坏所述阳极,因此在一个实现方式中,使钨阳极保持为冷的,并且使用一个或多个磁体使电子束一直保持移动(“扫描”)。另外,使电子束散焦以增加焦点大小并且因此防止钨熔化。因此,本公开的kv辐射治疗系统被配置成(1)用水冷却所述阳极(铜块上的钨),(2)使电子束散焦(例如,散焦到1cm2),和(3)不断地移动所述束。
在一个实现方式中,本公开的kv辐射治疗系统包括具有3-d轨迹的强度调控型kvx射线源,所述3-d轨迹是通过用台架和以磁力操纵的不断扫描的电子束来调整旋转治疗来实现。因此,电子束以电子方式沿着治疗阳极的长轴扫掠并且通过机械运动而基本上垂直于所述长轴移动。结果是由光子组成的倒置金字塔形状,其中顶点是在靶病损上。这与具有停留在预定数目个准直器上的电子束的常规x射线源大不相同。对于本系统,在通过操纵磁体来操纵电子束时,可以调整阳极上的扫描速度和束电流以实时地调控剂量率。此外,较缓慢地移动电子束会递送更多剂量(在当前束位置处)。
本公开的实现方式在对现有基础设施进行微小修改的情况下以相对较低的成本来提供优于常规系统的优势。由于kv部件的成本和屏蔽要求(例如,具有两米厚水泥墙的数百万美金的地下堡垒通常用于mv辐射屏蔽)低于常规部件的成本和要求,因此kv辐射治疗系统的总成本较低。本公开的kv辐射治疗系统的成本估计不到常规mv线性加速器系统的成本的20%。用于200kvpx射线的屏蔽将仅要求壁中有3mm的铅,使得普通的房间也能容易地进行屏蔽。
在阅读了这些描述之后,将明白在各种实现方式和应用中如何实施本公开。然而,虽然将在本文中描述本公开的各种实现方式,但是应理解,这些实现方式仅举例呈现并且并非限制性的。因而,对各种实现方式的此详细描述不应被理解为限制本公开的范围或宽度。
在一个实现方式中,本公开的kv辐射治疗系统提供组合的治疗与成像以使得能够实时追踪病损以便将治疗束精确地递送到靶病损。已发现所提出的能量范围(130-220ma时分别为180-300kv)的剂量测定(所述剂量测定是人体吸收的离子化辐射剂量的测量、计算和评定)与常规辐射治疗系统中通常使用的mv束相当。
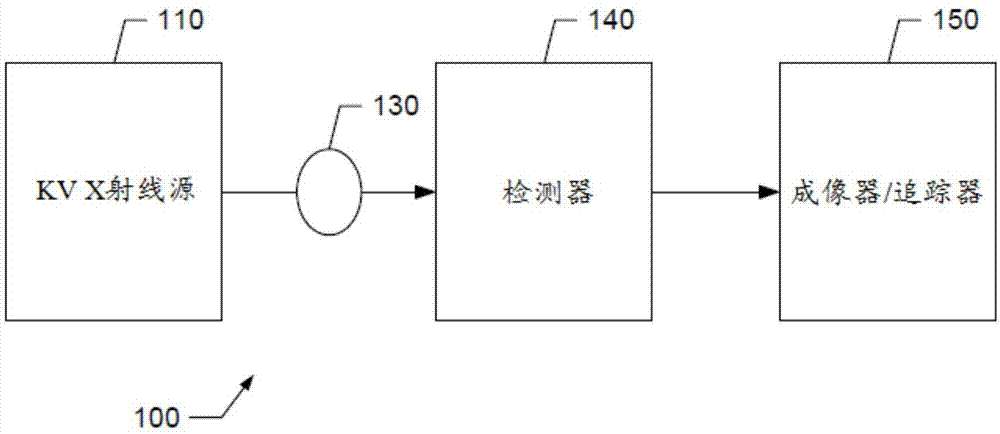
图1a是根据本公开的一个实现方式的kv辐射治疗系统100的框图。在图1a的所示实现方式中,kv辐射治疗系统100包括kvx射线源110、检测器140和成像器/追踪器150。kvx射线源110将x射线递送到预定靶病损和周围的组织130。成像器/追踪器150确定靶病损的确切位置。kvx射线源110和检测器140大体上安置于台架上。
图1b是根据本公开的一个实现方式的kvx射线源110的详细框图。在图1b的所示实现方式中,kvx射线源110包括电子束源(例如,x射线管)112、阳极120和准直器114。在一个实现方式中,准直器可移动以使准直器能够调整会聚点。
图1c是阳极120的详细框图,所述阳极包括治疗阳极122(所述治疗阳极产生治疗束)和成像阳极124(所述成像阳极实现了规划成像、实时成像和追踪)。
在一个实现方式中,使用扫描电子束和台架旋转通过3-d轨迹来对kvx射线源110进行强度调控,这使得治疗束能够在大得多的皮肤面积和组织体积上进入身体。如上文所述,使扫描电子束在治疗阳极122上不断地扫掠,所述治疗阳极允许用制冷机进行冷却。在一个实现方式中,使用一个或多个操纵磁体(容纳在离开电子束源112的束的四周)来“扫描”(或操纵)电子束以在阳极122上扫掠。操纵磁体包括并且可以是偶极磁体、四极磁体和螺线管磁体中的一者或多者。
当电子束撞击阳极122时,阳极产生近各向同性的x射线,使得x射线在所有方向上传播。因此,准直器114被配置成通过阻挡不朝向“会聚点”传播的x射线来将x射线引导到靶病损和周围组织130,所述会聚点是以所述靶病损为中心。成像阳极124被配置成提供对周围组织130内的靶病损的规划成像、实时成像和追踪以使得能够将治疗束精确地瞄准周围组织130内的靶病损。
在一个示例性实现方式中,kv辐射治疗系统100包括电子束源112(例如,在x射线源110内),所述电子束源在高达30分钟的治疗时间内绕位于等中心点处的、具有癌性病损的患者旋转。电子束源112通过阻挡不朝向“会聚点”传播的所有x射线来将治疗x射线束引导到预定的靶病损(例如,等中心点处的1cm球体)(详情请参见图5a和图5b)。因此,通过充分的冷却和热管理,x射线管(详情请参见图4)可以容纳200kvp、200ma(40kw)、1-cm直径的电子束,所述电子束在高达30分钟内在75×3cm2钨阳极上不断地扫描。大阳极面积上的扫描电子束允许充分冷却到400℃以下,400℃是x射线管/源烘烤温度,如此确保进行操作而不会发生损坏或出气。1-cm直径的电子束焦点大小是上述“散焦的电子束”的一个实例,所述散焦的电子束最大化通量并且将热分布在相对较大的面积上。然而,光点大小可以根据病损的大小和距病损的距离而变化。
使用以上示例性实现方式(所述实现方式包括含有辐射变色薄膜或法莫型电离室的适当体模),可以在少于30分钟内递送(例如)用于肺癌的3-d剂量分布以证实与预计值偏差在5%之内的剂量递送。可以将此剂量分布与现有技术的标准线性加速器mv治疗系统的那些剂量分布直接进行比较。在复杂的病损形状或较大体积的情况下,源与病人检查台可以在治疗期间移动,由此将适当剂量分布在整个几何形状上。
对于深层病损,常规kvx射线治疗的较高组织衰减会对靶病损上游的皮肤和组织用药过量。因此,非常希望治疗x射线的进入点分布在尽可能大的区域上。具有3-d轨迹(使用扫描电子束和台架旋转)的强度调控型kvx射线源使得治疗x射线的进入点分布在大区域上。
在具有3-d轨迹的强度调控型kvx射线源的一个实现方式中,x射线管安装在台架上,在将电子束以磁力操纵(使用磁体的操纵线圈)到与台架的圆形轨迹正交的治疗阳极(例如,钨阳极)上的同时,所述台架使所述管旋转。因此,源位置的轨迹变成圆柱体的表面(对于360°治疗计划)。此几何形状使治疗x射线的进入点分布在大的皮肤区域上,由此增加靶病损到皮肤的剂量。因此,可以通过改变电子束电流(被定义为每秒安培或库伦,其中1库伦=6.25×1018个电子)或改变电子束在治疗阳极上扫掠的速度来“调控”x射线的强度。这与mv系统大不相同,在mv系统中,通过改变约5微秒的脉冲的脉冲重复频率来执行调控。
使用诊断检查的容易获得的ct扫描器剂量率数据,可以通过假设对kvp的二次相关和对电流-时间乘积(mas)的线性相关来估计由kv辐射治疗系统递送的剂量。对于25岁和更老的成人,具有120kv、240ma源的腹部ct递送约15mgy。假设花了大约一秒钟来进行检查(情况通常是这样),kv辐射治疗系统将每秒递送35mgy(=15×200/240×(200/120)2)。这对应于2gy/min(=35×60),这是在由典型mv系统递送的1gy/min至6gy/min的邻区内。在10cm深度处,对于kv系统和mv系统,剂量率分别将减少到约0.2和0.5。因此,200kvp、200makv辐射治疗的剂量率可以是一gy/min到几gy/min并且将与基于mv系统的治疗相当。实际上,本公开的kv辐射治疗系统甚至可能优于mv系统,因为kvx射线可以在快速剂量下降的情况下进行准直,而mv多叶准直器系统由于(通常是)钨叶的厚度和钝缘而产生具有弱剂量下降的剂量分布。也就是说,较高能量的mvx射线较难以阻挡,因为阻挡材料需要为厚的(通常是约1cm或更厚的钨),而较低能量的kvx射线通常用薄铅板就能容易地阻挡。
图2是根据本公开的一个实现方式的kv辐射治疗系统100的透视图。在图2的所示实现方式中,kv辐射治疗系统100包括kvx射线源110和检测器140。如上所述,kvx射线源110将x射线递送到靶病损和周围的组织130。在一个实现方式中,kvx射线源110和检测器140安置于台架210上。另外,台架210可被配置成绕躺在平坦表面220上的患者旋转以使x射线源110能够从各种角度照亮靶病损。
图3是根据本公开的一个实现方式的包括x射线管300的x射线源110的详细透视图。在一个实现方式中,x射线源110被配置成通过阻挡不朝向会聚点340传播的所有x射线(使用阳极330和准直器240)来将x射线230(经由扫描电子束312产生)递送到预定的靶病损350(例如,等中心点处的1cm球体)。在一个实现方式中,x射线管300包括电子枪310和被配置有一个或多个磁体的操纵线圈320。
在图3的所示实现方式中,x射线管300的电子枪310产生电子束312并朝向治疗阳极330引导所述电子束。由于使电子束312停留在钨阳极330上可能会易于破坏所述阳极,因此使钨阳极330保持为冷的(例如,如图4中所示,为水冷却的)。使用所述一个或多个磁体(即,操纵线圈320)使电子束312一直保持移动(“扫描”和/或“操纵”),使得每一束落在钨阳极330的不同部分上。因此,通过调整以磁力操纵的不断扫描的电子束312(所述电子束是以磁力沿着阳极330的长轴来扫掠)使之适应旋转治疗,强度调控型kvx射线源110实现3-d轨迹,所述旋转治疗通过图2中所示的台架210的机械运动使所得光子基本上垂直于所述长轴来移动。结果是由光子组成的倒置金字塔形状,其中顶点340是在靶病损350上。另外,在一个实现方式中,电子枪310包括散焦单元,所述散焦单元使每一电子束散焦以增加焦点314的大小并且因此防止阳极330熔化。在一个实现方式中,扫描电子束和台架旋转的上述使用使得治疗束230能够在大得多的皮肤面积和组织体积上进入身体。
如上所述,当电子束312撞击阳极330时,阳极330产生各向同性的x射线以在所有方向上传播。因此,准直器240被配置成通过阻挡不朝向“会聚点”340传播的x射线来将x射线230引导到靶病损350,所述会聚点是以所述靶病损350为中心。
图4是根据本公开的一个实现方式的在治疗阳极442附近的x射线源400的剖切透视图(无图3中所示的梯形准直器)。在图4的所示实现方式中,在电子束420(例如,束大小=1×1cm2)以倾角(例如,60°)撞击水冷却的钨治疗阳极442(例如,大小=75×3cm2)时,x射线422经由水冷却的窗452离开源400。治疗阳极442上的大电子束光点(例如,大小=1×2cm2)会降低阳极冷却要求。在一个实现方式中,通过从外部的40kw制冷机经由冷却水通道450泵抽出的4gal/min的水,对40kw(=200kv×200ma)x射线源冷却使之持续工作是足够的。在图4的所示实现方式中,准直器(示出于图5a和图5b中)(例如,大小=75×2×6cm3)通过阻挡未朝向“会聚点”(例如,图3中的点340)引导的所有x射线来将x射线422引导到靶病损,所述会聚点是以所述靶为中心。x射线源400进一步包括成像阳极440。在另一个实现方式中,准直器通过阻挡未朝向“会聚区”引导的所有x射线来将x射线422引导到靶病损。会聚区是3-d空间中的小体积,例如,一厘米至几厘米的球体。
图5a和图5b是示出根据本公开的一个实现方式的准直器500的图。图5a示出被配置成将x射线510朝向会聚点520引导的准直器500。图5b示出准直器500的正视图,在顶部具有两个缩放视图530、540。
在图5b的所示实现方式中,准直器500由缩放视图530中所示的六角形孔532(和相关联的隔膜)建构。所述六角形孔被配置成将x射线引导到会聚点520处的点。也就是说,在本公开的一个实现方式中,在将x射线510朝向会聚点520向下游引导时,六角形孔532和相关联隔膜的截面变小且变薄。在另一个实现方式中,所述截面是矩形的。
在查看了在会聚点处通过虚拟光源取得的第一缩放视图530之后,可以在视觉上验证图5b的准直器设计。请注意,光源在中间是最明显的,表明到会聚点520的清楚视线。在准直器入口处从别处朝向会聚点的其它视图将示出类似呈现。
在图5a和图5b中所示的一个特定实现方式中,准直器500被配置为六角形孔的阵列,所述六角形孔具有直径d=2mm542(在入口处)、隔膜厚度t=0.2mm544(在入口处)和在距准直器500的出口40cm处的会聚点520。距会聚点520的距离(即,焦距)指示直径和隔膜厚度的大小改变的速率。
为了进行治疗,可以使用具有不同会聚点和具有不同治疗区的若干准直器。因此,可以取决于特定治疗计划来选择准直器。可以针对不同的靶病损大小(例如,大小s=1、2、3、4cm)和焦距(例如,焦距f=26、36、46cm)建构若干可附接准直器。
往回参看图4,通过成像阳极440(例如,可以使用19个成像阳极)来实现kv辐射治疗系统的实时成像和追踪能力。在治疗期间,电子束420可以周期性地循环遍历所述成像阳极440。在一个实现方式中,电子束420聚焦到成像阳极440中的一者上达1毫秒至10毫秒(并且类似地循环遍历所有成像阳极),并且通过检测器(例如,图2的平板检测器140)来俘获投影图像。之后使用投影图像(例如,由检测器140俘获的投影图像)来重建构3-d体积图像(使用(例如)断层融合算法来检测和显示靶病损的图像)。靶病损的准确位置允许准确定位以进行准确且精确的剂量递送。断层融合算法的使用实现了使用19个投影图像对靶病损的准确3-d重建构(以呈现癌性病损(例如,在肺部中,所述癌性病损在治疗期间会移动)的足够细节以允许进行检测和追踪)。
图6a示出使用200kvp、200makv弧形治疗(kvat)的蒙特卡罗模型病人剂量分布600。图6b示出使用15mv线性加速器体积调控弧形治疗(vmat)的蒙特卡罗模型病人剂量分布610。
图6a和图6b示出对深层病损的治疗展现出同样出色的剂量分布的kvat与vmat。因此,如果可以解决对阳极的冷却,那么使用kvat的治疗系统可以与vmat系统相当。
图7a和图7b是示出在kv辐射治疗系统中使用的准直器(例如,准直器500)的性能的图。
图7a示出在准直器出口处的固定隔膜厚度(t=0.2mm)时准直器效率和全宽半高(fwhm)随准直器孔大小(d)而变。图7a提供了选择隔膜厚度(t)和准直器孔大小(d)的重要的设计指导方针。举例来说,在fwhm为1.0cm时,可以实现55%的效率。
图7b示出在d和t的特定设置时的实际递送的剂量分布。图7b示出在具有适当倾斜(相对于电子束路径的平面成30°)的阳极的平面上使用大小为75×2cm2的x射线源的剂量分布,其中(d,t)=(2.3mm,0.2mm)。检测器为中心的射线投射与位于距准直器的出射面40cm处的检测平面一起使用。
图7a和图7b中示出的结果表明,剂量分布的形状不是太依赖于隔膜厚度(t),而是依赖于准直器孔大小(d)。
图8是示出根据本公开的一个实现方式的用于朝向身体内的靶病损递送kvx射线的方法800的流程图。在框810处,产生电子束并朝向治疗阳极引导所述电子束。在框820处,接着使用一个或多个磁体沿着治疗阳极操纵和扫描所述电子束,使得所述治疗阳极产生kvx辐射。在框830处,使用准直器来阻挡未朝向中心位于靶病损处的会聚点引导的所有kvx射线。在框840处,接着使电子束源、一个或多个磁体、治疗阳极和准直器绕靶病损旋转。
在一个实现方式中,方法800进一步包括调整操纵和扫描所述电子束的速度以调控kvx射线到靶病损的剂量率。在另一个实现方式中,所述操纵和扫描包括沿着治疗阳极的纵轴不断地移动电子束。在另一个实现方式中,方法800进一步包括调控kvx射线的强度。在另一个实现方式中,所述调控包括改变电子束电流。在另一个实现方式中,所述调控包括改变沿着治疗阳极操纵和扫描电子束的速度。在另一个实现方式中,方法800进一步包括使朝向治疗阳极引导的电子束散焦,使得电子束的光点大小增加。在另一个实现方式中,阻挡x射线进一步包括在基本上垂直于被操纵和扫描到治疗阳极上的电子束的平面中从准直器输出kvx射线。在另一个实现方式中,所述准直器是可移动的,并且所述方法进一步包括使用多个成像阳极对靶病损实时成像以使得能够调整所述可移动准直器,使得会聚点跟随移动(例如,随着呼吸移动)的靶病损。在另一个实现方式中,方法800进一步包括使用水冷却单元来冷却治疗阳极。
对这些实现方式的各种修改将是本领域的技术人员易于显而易见的,并且在不脱离本公开的精神或范围的情况下,本文中描述的一般原理可以应用于其它实现方式。因此,所述技术不限于上文描述的特定实例。因此,将理解,本文中呈现的描述和图式表示本公开的当前可能的实现方式并且因此代表在广义上被本公开涵盖的标的。进一步理解,本公开的范围完全涵盖可能变成本领域的技术人员显而易见的其它实现方式,并且本公开的范围相应地仅受所附权利要求书限制。
- 还没有人留言评论。精彩留言会获得点赞!