一种全层皮肤新型支架和构建方法与流程
本发明属于组织工程技术领域,尤其涉及一种全层皮肤新型支架和构建方法。
背景技术:
在细胞和组织培养领域,从上世纪70年代起二维(2d)培养科学家已经看到其局限性,开始更多地关注三维(3d)培养的优点,目前越来越多的研究从细胞培养的平面环境中转变到三维培养。细胞增殖,分化和代谢等生理活动都严重受到微环境的影响。当前细胞生物学研究大多还是在二维平面培养进行,这种平面培养、生长方式与机体内立体环境差别很大,导致细胞形态、分化、细胞与基质间的相互作用以及细胞与细胞间的相互作用与体内生理条件下细胞的行为存在明显差异。2d和3d环境下培养的细胞相比较,诸多生理指标都显著不同,例如原代小鼠乳腺管腔上皮细胞(mammaryluminalepithelialcells,mec)在3d基底膜基质中增殖的时间明显长于2d培养环境;更有甚者,有时药物作用于2d培养的细胞呈现的效应与3d细胞相反。3d培养可以设计模拟体内的生理环境,让细胞在生理行为上与机体实际的生理环境更接近。随着在生物相关性,通量,产出量等方面的改进,伴随3d培养成本的降低,3d培养在再生医学,基础研究和药物研发中的应用将越来越广泛,一场细胞由2d培养走向3d的变革正在发生。组织工程皮肤在临床皮肤再生修复、化学品安全毒理与功效测试以及皮肤疾病研究等领域均有重要的应用。特别是欧美动物替代测试的推广,已造成贸易壁垒,严重影响我国经济发展,迫切需要有效且简便的方法构建组织结构与功能与人体皮肤更加相近的组织工程皮肤。
因此,制备一种组织培养周期短,可较快构建细胞共培养体系、生物相容性好、成本低和力学性能较强,更接近人体真实环境的全层皮肤构建支架是本领域的技术人员亟待解决的技术问题。
技术实现要素:
有鉴于此,本发明一种全层皮肤新型支架和构建方法能有效解决目前三维细胞支架的力学性能及细胞在支架上贴合扩增问题,以及全层皮肤培养营养供问题的技术缺陷。
本发明公开了一种全层皮肤新型支架和构建方法,包括:
步骤一、将可降解淀粉进行酶降解后,制备成多孔淀粉;
步骤二、将多孔淀粉与胶原蛋白肽交联,冷冻干燥,制备成多孔支架;
步骤三、将成纤维细胞外泌液和tgf-β混合液装载到多孔支架,再冷冻干燥,制得用于构建全层皮肤新型支架;
步骤四、采用微流控装置模拟血液进行细胞培养液微循环,构建全层皮肤培养装置。
作为优选,所述的可降解淀粉包括玉米淀粉、大米淀粉、马铃薯淀粉及木薯淀粉中的一种或多种。
更为优选,所述步骤一具体为称取可降解淀粉溶解于去离子水中,搅拌均匀后,加入α-淀粉酶和葡萄糖淀粉酶为1:10-10:1(w:w),复合酶用量为2.4%,反应温度50℃,体系ph值为6.0,反应时间为24h。
更为优选,所述胶原蛋白肽的分子量在1000道尔顿以下。
具体的,将淀粉多孔和胶原蛋白肽放入模具中,放入-20℃冰箱,冷冻干燥后,置于140℃烘箱热交联2-4h。
作为优选,成纤维细胞外泌液和tgf-b混合液装载多孔支架中。
作为优选,所述步骤三的交联处理具体为高温热交联处理或/和化学交联处理。
作为优选,所述步骤四的微流控为pegda皮肤细胞组织培养小室。
具体的,所述聚二甲基硅氧烷的固化模具为中间镂空的pdms模具,优选为环形pdms模具。
具体的,聚二甲基硅氧烷的固化模具的具体制备方法如下:将液态聚二甲基硅氧烷(pdms)和固化剂以5:1的质量比例混合,搅拌混匀得到pdms混合液,称取10g的pdms混合液完全覆盖于底面积为125cm2的圆形皿中,真空抽去气泡后放入80℃烘箱固化聚二甲基硅氧烷(pdms),再用12cm直径的圆形打孔器打孔,再用8cm直径的圆形打孔器打孔,获得环状pdms模具,最后用最后用等离子表面处理器进行表面改性处理备用。
需要说明的是,环状pdms模具不是唯一的铸模方式,环状pdms模具是为了提高制备过程中的可操作性,以及有利于对多孔海绵支架厚度进行定量,而且较为便宜。环状pdms模具可换为无细胞毒性的所有固状材料,中间镂空的形状也无任何要求。
具体的,多孔支架设置在环状pdms模具上。
具体的,多孔淀粉是多孔淀粉是一种新型变性淀粉,作为吸附剂,具有高效、无毒、安全、可生物降解;
具体的,胶原蛋白肽是是由胶原或明胶经蛋白酶降解处理后制成的一种胶原蛋白前体产品,分子量在3000道尔顿,比普通胶原蛋白分子量小,一般认为更易消化吸收。针对于人体衰老细胞分裂、衰竭、萎缩,微整形术后损伤、新细胞再生受阻、细胞生长变异、增生等多项细胞修复功能障碍问题研发的医生营养。
本发明发现,现有的全层皮肤组织构建材料大多为多孔结构支架,因此,现有的多孔结构支架进行皮肤组织构建需要真皮层细胞增殖生长,分泌细胞外基质填充孔洞,形成一定的屏障后,才能再接种表皮细胞,使得多孔结构支架构建全层皮肤模型的培养周期较长,如在传统的多孔结构支架同时接种真皮层细胞和表皮细胞,这会容易造成表皮细胞与真皮细胞混合与多孔结构上,且表皮细胞容易团状增殖生长,与体内表皮细胞增殖生长、分化情况不一致。
本发明的目的针对现有技术多孔结构支架的力学性能较差,且在组织培养过程中多孔结构支架容易被酶解,以及多孔结构支架构建全层皮肤模型的培养周期较长的技术缺陷。
因此,本发明提供的一种全层皮肤新型支架和构建方法,包括:包括:一、将可降解淀粉进行酶解,制备成多孔淀粉,二、将多孔淀粉与胶原蛋白肽进行交联,冷冻干燥、制备成多孔支架,三、将成纤维细胞外泌液和tgf-b混合液装载到多孔支架,再冷冻干燥,制得用于构建全层皮肤的复合支架,四、采用微流控装置模拟血液进行细胞培养液微循环,构建全层皮肤培养装置。
综上所述,本发明的用于构建全层皮肤新型支架能让表皮层与真皮层细胞短时间内接种,组织培养周期短,可较快构建细胞共培养体系,解决三维细胞支架的力学性能及细胞在支架上贴合扩增问题,以及全层皮肤培养营养供问题的技术缺本发明用于制备与人体皮肤组织结构和功能相近的全层皮肤,应用于人体皮肤修复、化学品安全毒理功效检测和皮肤疾病模型研究等领域。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍。
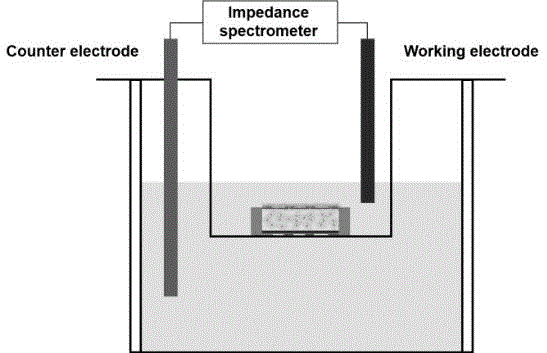
图1为采用微流控装置模拟血液进行细胞培养液微循环,构建全层皮肤培养装置图;
图2为本发明提供的用于全层皮肤新型支架的截面结构图;
图3为人角质细胞接种于本发明提供的全层皮肤新型支架7天后的扫面电镜图像;
图4为人角质细胞接种于现有技术的明胶支架7天后的扫面电镜图像。
具体实施方式
本发明提供了一种全层皮肤新型支架和构建方法,用于解决现有的胶原凝胶支架的力学性能较差,且在组织培养过程中胶原凝胶支架容易酶解,以及多孔海绵结构支架构建全层皮肤模型的培养周期较长的技术缺陷。
下面将对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
本具体实施例公开了一种全层皮肤新型支架和构建方法,包括:
步骤一、将可降解淀粉进行酶降解后,制备成多孔淀粉;
步骤二、将多孔淀粉与胶原蛋白肽交联,冷冻干燥,制备成多孔支架;
步骤三、将成纤维细胞外泌液和tgf-β混合液装载到多孔支架,再冷冻干燥,制得用于构建全层皮肤新型支架;
步骤四、采用微流控装置模拟血液进行细胞培养液微循环,构建全层皮肤培养装置。
作为优选,所述的可降解淀粉包括玉米淀粉、大米淀粉、马铃薯淀粉及木薯淀粉中的一种或多种。
更为优选,所述步骤一具体为称取可降解淀粉溶解于去离子水中,搅拌均匀后,加入α-淀粉酶和葡萄糖淀粉酶为1:10-10:1(w:w),复合酶用量为2.4%,反应温度50℃,体系ph值为6.0,反应时间为24h。
更为优选,所述胶原蛋白肽的分子量在1000道尔顿以下。
具体的,将淀粉多孔和胶原蛋白肽放入模具中,放入-20℃冰箱,冷冻干燥后,置于140℃烘箱热交联2-4h。
作为优选,成纤维细胞外泌液和tgf-β混合液装载多孔支架中。
作为优选,所述步骤三的交联处理具体为高温热交联处理或/和化学交联处理。
作为优选,所述步骤四的微流控为pegda皮肤细胞组织培养小室。
具体的,所述聚二甲基硅氧烷的固化模具为中间镂空的pdms模具,优选为环形pdms模具。
其中,以下实施例的原料为市售或自制。
实施例1
本发明实施例的用于一种全层皮肤新型支架和构建方法具体如下:
(1)将液态聚二甲基硅氧烷(pdms)和固化剂以5:1的质量比例混合,搅拌混匀,称取10g完全覆盖于底面积为125cm2的圆形皿中,真空抽去气泡后放入80℃烘箱固化聚二甲基硅氧烷(pdms),再用12cm直径的圆形打孔器打孔,再用8cm直径的圆形打孔器打孔,获得环状pdms,最后用等离子体表面处理器进行表面改性备用,形成模具。
(2)称取一定质量的玉米淀粉溶解于去离子水中,搅拌均匀后,加入α-淀粉酶和葡萄糖淀粉酶为1:10(w:w),复合酶用量为2.4%,反应温度50℃,体系ph值为6.0,反应时间为24h,得到多孔淀粉。
(3)将(2)中的多孔淀粉与胶原蛋白肽进行交联,在-20℃条件下,冷冻24h后进行冷冻干燥24h,形成多孔前体,接着多孔前体放入140℃烘箱中进行4h的交联,制得多孔支架。
(4)将成纤维细胞外泌液和tgf-β混合液装载到多孔支架,再冷冻干燥,制得用于构建全层皮肤新型支架。
(5)采用微流控装置模拟血液进行细胞培养液微循环,构建全层皮肤培养装置(装置图见图1)。
图2为实施例1的全层皮肤新型支架的扫描电镜图。从扫描电镜图可知,多孔支架的厚度为300-550μm,其孔径为108±18μm,具有高孔隙率,多孔结构均匀的三维支架。全层皮肤新型支架的总厚度为388μm~588μm,其孔隙率不低于90.0%。
实施例2
本发明实施例的用于一种全层皮肤新型支架和构建方法具体如下:
(1)将液态聚二甲基硅氧烷(pdms)和固化剂以5:1的质量比例混合,搅拌混匀,称取10g完全覆盖于底面积为125cm2的圆形皿中,真空抽去气泡后放入80℃烘箱固化聚二甲基硅氧烷(pdms),再用12cm直径的圆形打孔器打孔,再用8cm直径的圆形打孔器打孔,获得环状pdms,最后用等离子体表面处理器进行表面改性备用,形成模具。
(2)称取一定质量的大米淀粉溶解于去离子水中,搅拌均匀后,加入α-淀粉酶和葡萄糖淀粉酶为1:8(w:w),复合酶用量为2.0%,反应温度50℃,体系ph值为6.0,反应时间为18h,得到多孔淀粉。
(5)将(2)中的多孔淀粉与胶原蛋白肽进行交联,在-20℃条件下,冷冻24h后进行冷冻干燥24h,形成多孔前体,接着多孔前体放入140℃烘箱中进行4h的交联,制得多孔支架。
(6)将成纤维细胞外泌液和tgf-β混合液装载到多孔支架,再冷冻干燥,制得用于构建全层皮肤新型支架。
(5)采用微流控装置模拟血液进行细胞培养液微循环,构建全层皮肤培养装置。
实施例3
本发明实施例的用于一种全层皮肤新型支架和构建方法具体如下:
(1)将液态聚二甲基硅氧烷(pdms)和固化剂以5:1的质量比例混合,搅拌混匀,称取10g完全覆盖于底面积为125cm2的圆形皿中,真空抽去气泡后放入80℃烘箱固化聚二甲基硅氧烷(pdms),再用12cm直径的圆形打孔器打孔,再用8cm直径的圆形打孔器打孔,获得环状pdms,最后用等离子体表面处理器进行表面改性备用,形成模具。
(2)称取一定质量的玉米淀粉、木薯淀粉溶解于去离子水中,搅拌均匀后,加入α-淀粉酶和葡萄糖淀粉酶为1:10(w:w),复合酶用量为3.0%,反应温度45℃,体系ph值为6.0,反应时间为24h,得到多孔淀粉。
(3)将(2)中的多孔淀粉与胶原蛋白肽进行交联,在-20℃条件下,冷冻24h后进行冷冻干燥24h,形成多孔前体,接着多孔前体放入140℃烘箱中进行4h的交联,制得多孔支架。
(4)将成纤维细胞外泌液和tgf-β混合液装载到多孔支架,再冷冻干燥,制得用于构建全层皮肤新型支架。
(5)采用微流控装置模拟血液进行细胞培养液微循环,构建全层皮肤培养装置。
实施例4
本实施例为利用实施例1制备得到的全层皮肤新型支架,添加人角质细胞构建全层皮肤,图3、图4为人角质细胞接种于全层皮肤新型支架、现有技术的明胶多孔支架7天后的扫面电镜图像。由图可以看出,新型支架的厚度在570-625μm之间,人角质细胞很好地粘附在表面,形成一层细胞层,支架在150μm深的空间里,人角质细胞可较均匀地分散开粘附生长。现有技术明胶支架的厚度只有50-70μm,多孔结构少,仅有少量的人角质细胞在支架表面粘附增殖。
以上实验说明,人角质细胞接种于实施例1的全层皮肤新型支架和现有技术明胶支架7天后的扫面电镜图像,可以清晰的看出人角质细胞粘附在新型支架的效果更佳,人角质细胞粘附得更好更快,其细胞较容易伸展开,形态与体内更相近,且细胞增殖也较快,十分有利于表皮层的快速构建。
综上所述,本发明全层皮肤新型支架的生物相容性好、成本低、力学性能较强,允许表皮层与真皮层细胞短时间内完成接种,可缩短组织培养周期,较快构建细胞共培养体系,建立真表皮层细胞间通讯,快速构建全层皮肤。
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!