一种包载多种金属离子的聚乙烯醇纺丝纳米纤维膜敷料及制备方法与流程
本发明属于医用敷料技术领域,具体涉及一种包载多种金属离子的聚乙烯醇纺丝纳米纤维膜敷料及制备方法。
背景技术:
临床上应用于创口愈合的药物,其中部分会带有金属离子,因为各种金属离子在创口愈合过程中会起到各种效果。常见的有银离子、铜离子、钙离子、锌离子,具体在创口愈合过程中所起到的效果如下:
银离子:银的化学结构决定了银具有较高的催化能力,高氧化态银的还原势极高,足以使其周围空间产生氧自由基。氧自由基具有强氧化性可以灭菌,银离子可以强烈地吸引细菌体中蛋白酶上的巯基(-sh),迅速与其结合在一起,使蛋白酶丧失活性,导致细菌死亡。当细菌被银离子杀后,银离子又由细菌尸体中游离出来,再与其它菌落接触,周而复始地进行上述过程,具有杀菌持久性。据测定,水中含银离子为0.01ppm时,就能完全杀死水中的大杆菌,能保持长达90天内不繁衍出新的菌丛。
铜离子:铜在各种细胞中扮演着复杂的角色,调节多种细胞因子和生长因子的作用机制,它基本上参与了伤口愈合过程的各个阶段。铜离子刺激血管生成,促进胶原沉积和再上皮化,并增加伤口闭合。然而,伤口床上使用铜盐或氧化铜,会有一定毒性,增加了对病人产生铜中毒的风险。如果离子缓慢释放,铜离子毒性的风险就会降低。
钙离子:1.细胞内的钙调节蛋白与钙离子结合,形成的一种复合物,可激活体内多种酶的活性。比如凝血酶,所以钙离子是凝血因子,参与凝血过程;
2.参与肌肉(包括骨骼肌、平滑肌)收缩过程;
3.参与神经递质合成与释放、激素合成与分泌;
4.是骨骼构成的重要物质。
锌离子:锌离子的释放可以刺激免疫功能产生大量白细胞和中性粒细胞(2-4倍于对照组),从而产生协同抗菌作用,加速伤口愈合。锌离子可以促进成纤维细胞的增殖,尤其是在皮肤再生过程中,在真皮和皮下组织中对细胞的增殖和分化非常重要。
现在含有金属离子的抗菌药物存在无法缓释的问题,通常需要频繁给药,且浓度不易控制,太高则有细胞毒性,太低则抗菌效果不好的缺点。
技术实现要素:
本发明的目的是为了克服现有技术存在的缺点和不足,而提供一种包载多种金属离子的聚乙烯醇纺丝纳米纤维膜敷料及制备方法。
本发明所采取的技术方案如下:一种包载多种金属离子的聚乙烯醇纺丝纳米纤维膜敷料,包括由含银离子和钙离子的聚乙烯醇溶液通过纺丝法形成的第一纤维层、由含锌离子的聚乙烯醇溶液通过纺丝法形成的第二纤维层、由含铜离子的聚乙烯醇溶液通过纺丝法形成的第三纤维层,所述第一纤维层、第二纤维层、第三纤维层先后叠加。
聚乙烯醇,是一种极安全的高分子有机物,对人体无毒,无副作用,具有良好的生物相容性,尤其在医疗中的如其水性凝胶在眼科、伤口敷料和人工关节方面的有广泛应用,同时在聚乙烯醇薄膜在药用膜,人工肾膜等方面也有使用。其安全性可以从用于伤口皮肤修复,和眼部滴眼液产品可见一斑。其中一些型号也常被用在化妆品中的面膜、洁面膏、化妆水及乳液中,是一种常用的安全性成膜剂。聚乙烯醇的物理性质受化学结构、醇解度、聚合度的影响。在聚乙烯醇分子中存在着两种化学结构,即1,3和1,2乙二醇结构,但主要的结构是1,3乙二醇结构,即“头•尾”结构。聚乙烯醇的聚合度分为超高聚合度(分子量25~30万)、高聚合度(分子量17-22万)、中聚合度(分子量12~15万)和低聚合度〔2.5~3.5万〕。本发明中所选择的聚乙烯醇分子量为2.5~5万。
所述聚乙烯醇溶液所采用的的溶剂为水、甘油、二甲亚砜、硼酸溶液、n,n-二甲基甲酰胺中的一种或多种。其中,溶剂优选水,绿色环保,制成敷料时,对人体无害。
所述含银离子和钙离子的聚乙烯醇溶液为硝酸银、葡萄糖酸钙、聚乙烯醇溶解于水中。其中,硝酸银也可以用硫化银,磺胺嘧啶银、氯酸银、氟化银、高氯酸银,氯化银,次氯酸银,草酸银,醋酸银等银盐替代,葡萄糖酸钙也可以用碳酸钙、溴化钙,氯化钙,硫化钙,氟化钙,硝酸钙,次氯酸钙,高氯酸该,草酸钙,醋酸钙等钙盐替代。所述含锌离子的聚乙烯醇溶液为葡萄糖酸锌、聚乙烯醇溶解于水中。葡萄糖酸锌也可以用硫化锌,氯酸锌、氟化锌、高氯酸锌,氯化锌,次氯酸锌,草酸锌,醋酸锌等锌盐替代。含铜离子的聚乙烯醇溶液为葡萄糖酸铜、聚乙烯醇溶解于水中,葡萄糖酸铜也可用硫化铜,氯酸铜、氟化铜、高氯酸铜,氯化铜,次氯酸铜,草酸铜,醋酸铜等铜盐替代。替换的盐需要考虑降低对人体的危害性,以及可溶性,如果替换的盐无法完全溶于水中而导致配置的含金属离子的聚乙烯醇溶液中金属离子的浓度低于预期浓度,则替换为其它溶剂或加入其它辅料使金属离子的浓度达到目标。
在本发明在一些优选实施方案中,所述金属离子的负载浓度为0.0025~0.01mol/l;例如含有多重金属离子溶液时,各个金属离子的负载浓度为0.0025mol/l或者0.005mol/l,含有一种金属离子时,其金属离子的负载浓度为0.01mol/l,根据本发明的教导以及结合医学常识,负载离子的浓度可做多种替换。
本发明的另一个目的在于提供一种包载多种金属离子的聚乙烯醇静电纺丝纳米纤维膜敷料的制备方法,包括以下步骤:
(1)制备含银离子和钙离子的聚乙烯醇溶液、含锌离子的聚乙烯醇溶液、含铜离子的聚乙烯醇溶液;
(2)将步骤(1)得到的含银离子和钙离子的聚乙烯醇溶液通过纺丝法形成第一纤维层;
(3)将步骤(1)得到的含锌离子的聚乙烯醇溶液在步骤(2)得到的第一纤维层上通过纺丝法形成第二纤维层;
(4)将步骤(1)得到的含铜离子的聚乙烯醇溶液在步骤(3)得到的第二纤维层上通过纺丝法形成第三纤维层。
所述纺丝法选择静电纺丝法,步骤(1)得到的聚乙烯醇溶液均通过静电纺丝机纺丝成纤维层。
静电纺丝机工作时,针头距离电纺丝接收器的距离为14cm,推进速度为0.0007mm/s,正极电压为20kv,负极电压为1kv。
本发明的有益效果如下:本发明通过纺丝法纺成纳米纤维膜作为伤口敷料,作为一张多层的亲水性固体纤维薄膜,每一层包载了不同的金属离子,每种金属离子有不同的效果,作用于伤口愈合的不同阶段,可保存放置,使用方便,性质稳定。操作简单,材料易得,利用率高,通过改变纺丝时间或金属离子和聚乙烯醇的相对浓度即可调节负载量。金属离子均匀分布在制成的纤维膜上,纤维除了有稍微吸湿性以外,性质稳定,因此可长期保存使用。且本方法得到的敷料可直接应用于创面,或先制成负载单重金属离子的纳米纤维膜,通过层层叠放,控制金属离子依次释放,从而在创面愈合的不同时期起到相应的作用。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动性的前提下,根据这些附图获得其他的附图仍属于本发明的范畴。
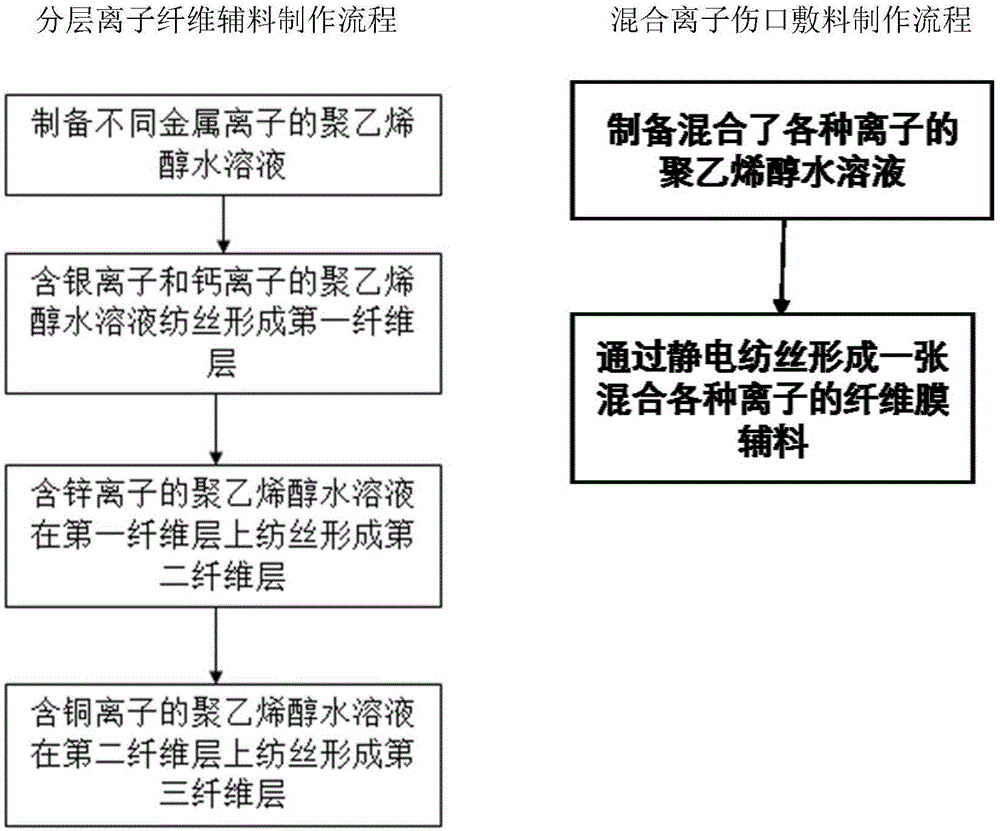
图1为分层离子组(lbl)和混合给药组(mix)所用敷料制备过程的流程示意图;
图2为分层离子组(lbl)、聚乙烯醇纤维组(pv),control组,分时间给药组(timelydosin),混合给药组(mix)对创口愈合影响对比的试验结果;图3为分层离子组(lbl)、聚乙烯醇纤维组(pv),control组,分时间给药组(timelydosin),混合给药组(mix)对创口愈合影响对比的试验结果;
图4为金属离子释放测试装置的结构示意图,(a)为剖视图,(b)为俯视图;
图5为混合给药组的金属离子释放结果;
图6为实施例一的金属离子释放结果;
图7为实施例二的金属离子释放结果;
图8为实施例三的金属离子释放结果;
图9为实施例四的金属离子释放结果。
具体实施方式
为使本发明的目的、技术方案和优点更加清楚,下面将结合附图对本发明作进一步地详细描述。
实施例一:
第一步:
将3g聚乙烯醇(购买自麦克林,cas号:9002-89-5),0.43g硝酸银,1g葡萄糖酸钙溶解在10ml水中,先室温搅拌半小时使其分散溶胀,再67℃油浴加热搅拌1.5h,溶解完成。
将3g聚乙烯醇(购买自麦克林,cas号:9002-89-5),1g葡萄糖酸锌溶解在10ml水中,先室温搅拌半小时使其分散溶胀,再67℃油浴加热搅拌1.5h,溶解完成。
将3g聚乙烯醇(购买自麦克林,cas号:9002-89-5),1g葡萄糖酸铜溶解在10ml水中,先室温搅拌半小时使其分散溶胀,再67℃油浴加热搅拌1.5h,溶解完成。
第二步:
聚合物溶液冷却到室温后,装进10ml注射器(购买自kdl)中,安装在静电纺丝机(型号:天津云帆科技天津云帆科技yfsp-giii静电纺丝机),针头距离电纺丝接收器的距离为14cm,上在静电纺丝平面接收器上覆盖一层锡箔纸,用于接收电纺纤维。先纺一层银离子和钙离子的纤维,再在原纤维上纺一层锌离子的纤维,最后纺铜离子纤维。注射器推进速度为0.0007mm/s,正极电压为20kv,负极电压为1kv。
实施例二:
第一步:
将3g聚乙烯醇(购买自麦克林,cas号:9002-89-5),0.43g硝酸银,1g葡萄糖酸钙溶解在10ml水中,先室温搅拌半小时使其分散溶胀,再67℃油浴加热搅拌1.5h,溶解完成。
将3g聚乙烯醇(购买自麦克林,cas号:9002-89-5),1.24g葡萄糖酸锌溶解在10ml水中,先室温搅拌半小时使其分散溶胀,再67℃油浴加热搅拌1.5h,溶解完成。
将3g聚乙烯醇(购买自麦克林,cas号:9002-89-5),0.87g葡萄糖酸铜溶解在10ml水中,先室温搅拌半小时使其分散溶胀,再67℃油浴加热搅拌1.5h,溶解完成。
第二步:
聚合物溶液冷却到室温后,装进10ml注射器(购买自kdl)中,安装在静电纺丝机(型号:天津云帆科技天津云帆科技yfsp-giii静电纺丝机),针头距离电纺丝接收器的距离为14cm,上在静电纺丝平面接收器上覆盖一层锡箔纸,用于接收电纺纤维。先纺一层银离子和钙离子的纤维,注射器推进速度为0.0005mm/s,正极电压为20kv,负极电压为1kv。再在原纤维上纺一层锌离子的纤维,注射器推进速度为0.0007mm/s,正极电压为20kv,负极电压为1kv。最后纺铜离子的纤维,注射器推进速度为0.0006mm/s,正极电压为20kv,负极电压为1kv。
实施例三:
第一步:
将3g聚乙烯醇(购买自麦克林,cas号:9002-89-5),0.86g硝酸银,1.5g葡萄糖酸钙溶解在10ml水中,先室温搅拌半小时使其分散溶胀,再67℃油浴加热搅拌1.5h,溶解完成。
将3g聚乙烯醇(购买自麦克林,cas号:9002-89-5),1.5g葡萄糖酸锌溶解在10ml水中,先室温搅拌半小时使其分散溶胀,再67℃油浴加热搅拌1.5h,溶解完成。
将3g聚乙烯醇(购买自麦克林,cas号:9002-89-5),1.5g葡萄糖酸铜溶解在10ml水中,先室温搅拌半小时使其分散溶胀,再67℃油浴加热搅拌1.5h,溶解完成。
第二步:
聚合物溶液冷却到室温后,装进10ml注射器(购买自kdl)中,安装在静电纺丝机(型号:天津云帆科技天津云帆科技yfsp-giii静电纺丝机),针头距离电纺丝接收器的距离为14cm,上在静电纺丝平面接收器上覆盖一层锡箔纸,用于接收电纺纤维。先纺一层银离子和钙离子的纤维,注射器推进速度为0.00085mm/s,正极电压为20kv,负极电压为1kv。再在原纤维上纺一层锌离子的纤维,注射器推进速度为0.0008mm/s,正极电压为20kv,负极电压为1kv。最后纺铜离子的纤维,注射器推进速度为0.0008mm/s,正极电压为20kv,负极电压为1kv。
实施例四:
第一步:
将3g聚乙烯醇(购买自麦克林,cas号:9002-89-5),0.43g硝酸银,1g葡萄糖酸钙溶解在10ml水中,先室温搅拌半小时使其分散溶胀,再67℃油浴加热搅拌1.5h,溶解完成。
将3g聚乙烯醇(购买自麦克林,cas号:9002-89-5),1g葡萄糖酸锌溶解在10ml水中,先室温搅拌半小时使其分散溶胀,再67℃油浴加热搅拌1.5h,溶解完成。
将3g聚乙烯醇(购买自麦克林,cas号:9002-89-5),1g葡萄糖酸铜溶解在10ml水中,先室温搅拌半小时使其分散溶胀,再67℃油浴加热搅拌1.5h,溶解完成。
第二步:
聚合物溶液冷却到室温后,装进10ml注射器(购买自kdl)中,安装在静电纺丝机(型号:天津云帆科技天津云帆科技yfsp-giii静电纺丝机),针头距离电纺丝接收器的距离为14cm,上在静电纺丝平面接收器上覆盖一层锡箔纸,用于接收电纺纤维。先纺一层银离子和钙离子的纤维,注射器推进速度为0.0005mm/s,正极电压为20kv,负极电压为1kv。再在原纤维上纺一层锌离子的纤维,注射器推进速度为0.0006mm/s,正极电压为20kv,负极电压为1kv。最后纺铜离子的纤维,注射器推进速度为0.0008mm/s,正极电压为20kv,负极电压为1kv。
测试一:
将实施例一所得到的纺在锡箔纸上的纤维膜中间厚度均匀处,打下一块圆,贴在b6小鼠感染伤口处,为分层离子组(lbl)。
除了分层离子组,同时间还有另外四组进行试验,为聚乙烯醇纤维组(pv),control组,分时间给药组(timelydosin),混合给药组(mix);
聚乙烯醇纤维组(pv)为不含金属离子的聚乙烯醇溶液纺丝成型的敷料;
分时间给药组(timelydosin)为现有临床上含有金属离子的抗菌药物的给药方式,给药量与分层离子组(lbl)相同;
混合给药组(mix)为混合有银离子、钙离子、锌离子、铜离子的聚乙烯醇溶液纺丝成型的敷料,其中银离子、钙离子、锌离子、铜离子的浓度与分层离子组(lbl)相同;
每组7只老鼠,
-2天:punch,拍照,造成创面,加菌液形成感染
0天:拍照+给药;
2天:取菌涂菌;
4天:拍照+取菌涂菌+给药;
7天:拍照+取菌涂菌+每组杀三只取组织+剩下的4只给药;
10天:拍照;
14天:拍照;
17天:拍照+杀老鼠取组织;
(每次拍照均进行称重),试验结果如图2所示,分层离子组(lbl)的愈合效果是最佳的,其次是混合给药组(mix),最差的是聚乙烯醇纤维组(pv),说明了本发明的包载多种金属离子的聚乙烯醇纺丝纳米纤维膜敷料具有很好的疗效,相比其它同时试验的四组试验组疗效更佳。
测试二:
对创面给药后第17天的创面愈合情况进行描述,在小鼠给药第2,4,7天时,分别用无菌棉签擦取每组小鼠创面上的分泌液,用生理盐水稀释后将其于涂布于琼脂板上,结果如图3所示,参考表1所示,可知第2.3组的创面在第二天菌量即明显减少,而第1组的创面中的菌量一直保持最高。
由以上创面愈合试验可知,分层离子组(lbl)和混合给药组(mix)获得的敷料,其抗菌性明显大于现有的单纯pva纱布敷料,且如图3可以看出,分层离子组(lbl)得到的层层释放金属离子的敷料抗菌性明显优于混合给药组(mix)获得混合离子敷料。
测试三:
将滴加了单纯pva的纱布,上述实施例一、实施例二及实施例三中的敷料分别应用于小鼠创面上。在创面给药后第17天对各组小鼠的创面进行评估。
测试四:
如图4所示的金属离子释放测试装置,包括圆柱形的容器1、敷料架2,容器1上端边缘等间距设有四个开槽101,敷料架2对应设有四个凸起的支撑部201,支撑部201设置在开槽101从而放置敷料架2,敷料架2主体为网格,厚度为1mm左右,测试时,在容器内倒入ph=7.40的磷酸盐缓冲溶液直到缓冲溶液从开槽101处流出,将测试的敷料3放置在敷料架2上。
将实施例一所得到的纤维膜,与混合给药组两组敷料取中间厚度均匀处进行金属离子释放测试,试验结果如图5、图6所示,从释放结果可以看出,各种离子确实是在不同时间段先后释放的,实施例一所得到的纤维膜确实达到了预期想要达到的分层释放效果。
测试五:
将实施例一、实施例二、实施例三、实施例四所制得的敷料取中间厚度均匀处进行金属离子释放测试,试验结果如图6-9所示,电纺丝过程中注射器推进速度回影响纤维层的厚度,进而影响各种离子先后释放的速度,其中,实施例四中,各离子释放的速度更符合临床上创口愈合过程中对不同金属离子的需要。
以上所揭露的仅为本发明实施例而已,当然不能以此来限定本发明之权利范围,因此依本发明权利要求所作的等同变化,仍属本发明所涵盖的范围。
- 还没有人留言评论。精彩留言会获得点赞!