一种盐酸美金刚缓释胶囊及其制备方法与流程
本发明涉及制药领域,尤其涉及一种盐酸美金刚缓释胶囊及其制备方法。
背景技术:
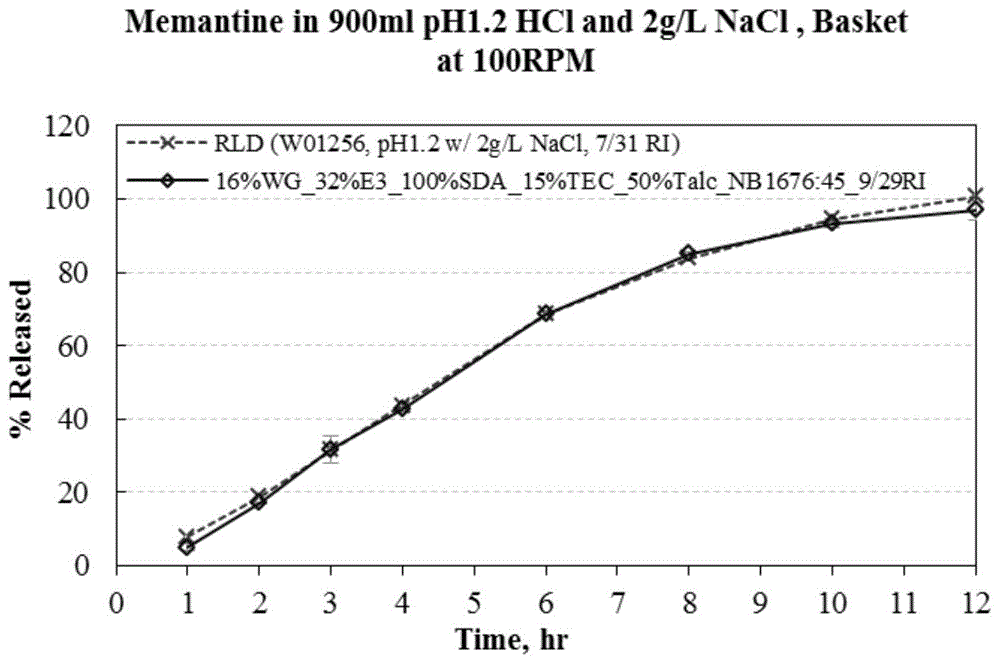
:阿尔兹海默症(alzheimer’sdisease,ad)是一种中枢神经系统退行性疾病,是老年期痴呆最常见的一种类型。一种脑细胞(神经元)恶化的不可逆进行性紊乱,其导致认知功能、主要记忆、判断和推理、运动协调性和图形识别的丧失。在该疾病的晚期,所有的记忆和智力功能都可能丧失。患有阿尔茨海默症的人在记忆、判断和思考方面存在问题,从而使其难以工作或参与日常生活。它和老年性痴呆,即与老龄有关的智力退化(智能丧失)有关联。老年性痴呆被定义为两种主要类型:由广义的萎缩症引起的阿尔茨海默型和由血管问题引起的,主要是中风等。在80岁以上的人中,20%患有阿尔茨海默症。尽管有能改善症状的药物,但阿尔茨海默症目前不能被治愈。据who在2012年4月公布数据显示,全世界有近3560万ad患者,预计人数到2030年翻一番(6570万),到2050年将达到现在的三倍。我国ad患者有600万左右,预计到2025年我国将有1000万ad患者。1982年,德国梅尔兹公司(merz)发现了美金刚的中枢神经系统活性后,对其进行了深入的研究。1986年,美金刚作为一种痴呆症治疗药物进入临床试验,1989年正式在德国上市,商品名为随后美金刚的nmda受体抑制作用得到了确认,2000年6月,德国merz公司和美国森林制药公司(forestlab)在美国启动了治疗阿尔茨海默病及其他中枢神经系统疾病的临床试验。同时,丹麦灵北制药公司(lundbeck)获得了产品转让。2002年2月20日,欧洲专利药品委员会(cpmp)批准了lundbeck公司的盐酸美金刚用于治疗中度至重度ad症,商品名为namenda。同年8月美金刚在德国上市,2003年10月以商品名namenda在美国上市。2010年,fda批准了forestlab和merz公司联合开发的盐酸美金刚缓释胶囊namendaxr用于一日1次口服治疗中度至重度ad患者。美金刚目前在欧洲被批准用于中重度到重度ad的治疗,并且在美国被用于中度到重度ad的治疗。专利cn201410830047公开了一种用于治疗阿尔茨海默症的缓释制剂及其制备方法,所述缓释制剂由缓释片芯和速释外层组成,所述速释外层包裹缓释片芯;按每片的重量计,所述缓释片芯主要由下述重量的原辅料制备而成:盐酸美金刚4.5-30mg,缓释材料45-160mg,润滑剂0.5-10mg,所述速释外层主要由下述重量的原辅料制备而成:盐酸美金刚0.5-20mg,填充剂330-370mg,润滑剂2-15mg,崩解剂13-17mg。该发明所制得的缓释制剂起效快、作用时间持久、稳定的效果,提高病人的依从性。但是此专利剂型为缓释片剂,与原研制剂剂型不同,因此在一致性上无法比较。专利cn201410073178公开了一种盐酸美金刚缓释制剂,包括盐酸美金刚缓释迷你片,所述盐酸美金刚缓释迷你片由片芯和包衣膜组成,所述包衣膜的重量是片芯重量的0-30%。该发明缓释迷你片的生产设备简单,与普通片相似,仅需改变冲头直径大小,容易实现工业生产。迷你片在工艺参数确定后,压制出片剂的大小基本一致,基本不存在批内或批间差异的问题,质量更易控。同样地,但是该专利剂型为缓释片剂,与原研制剂剂型不同,因此在一致性上无法比较。专利cn201410254808公开了一种盐酸美金刚缓释药丸。该胶囊内填充物为盐酸美金刚缓释小丸,所述盐酸美金刚缓释小丸从里至外依次包括空白丸芯、含盐酸美金刚的主药层、隔离包衣层和缓释包衣层。该发明稳定性好、无突释现象,确保药物持续、均匀缓慢地释放药物,提高了产品的疗效。但是此产品为了解决盐酸美金刚缓释胶囊的突释问题,加入了隔离包衣层。工艺较繁琐。专利cn201110446337公开了一种盐酸美金刚缓释制剂的制备方法。本发明是将含盐酸美金刚的含药小丸进行缓释包衣得到缓释微丸。通过挤出滚圆或者是溶液上药或是混悬液上药得到的含药小丸,该小丸在形状上接近圆形,对形状粒度可控的含药小丸进行缓释包衣,使得包衣形成的膜的厚薄也可控。本发明实现了包衣膜和微丸球状的可控,确保盐酸美金刚晶型不发生转化的情况下,对盐酸美金刚释放的稳定性重现性进行可控。本发明制剂以单剂量形式在24小时的范围内提供持续释放,药物通过膜孔渗透扩散至释放介质中,且因体积小,药物服用时不易受食物的影响,提高疗效。本发明生产方法简单易行,宜于工业化生产,有较大的应用价值。但是该产品在24小时内的范围内释放,且12小时的释放程度与参比制剂(原研药制剂)一致性低,参比制剂在12小试内释放程度达到85%以上。由上可知,上述专利的美金刚制剂与forestlab和merz公司联合开发的盐酸美金刚缓释胶囊namendaxr在药效一致性上相去甚远,目前市场上还未有符合要求的盐酸美金刚缓释胶囊namendaxr仿制药制剂。因此,有必要研发出一款以盐酸美金刚缓释胶囊namendaxr为原研药制剂且具有高度一致性的仿制药制剂。技术实现要素:为了解决上述技术问题,本发明提供了一种盐酸美金刚缓释胶囊及其制备方法,本发明的盐酸美金刚缓释胶囊,在配方以及工艺不同的情况下,其与原研药制剂盐酸美金刚缓释胶囊namendaxr在药效上能够保持高度的一致性,并且本发明的释放曲线对乙醇的抗干扰能力更强。本发明的具体技术方案为:一种盐酸美金刚缓释胶囊,包括胶囊和填充于所述胶囊内的盐酸美金刚缓释微丸,所述盐酸美金刚缓释微丸由里至外依次包括空白丸芯、主药层、缓释包衣层。所述主药层中包括盐酸美金刚和粘合剂,所述粘合剂为水溶性粘合剂或醇溶性粘合剂;所述缓释包衣层中包括缓释材料、抗粘剂、致孔剂和增塑剂,所述缓释材料为醇溶性材料。所述盐酸美金刚缓释胶囊中包括以下重量份的原料:空白丸芯100-150份,盐酸美金刚28份,粘合剂11-17份,缓释材料5-14份,抗粘剂4-10.1份,致孔剂2.5-6.5份,增塑剂1.2-3.1份。本发明在配方以及工艺与原研药制剂盐酸美金刚缓释胶囊namendaxr均不同的情况下,在药效上能够保持高度的一致性,与原研药制剂对比在5种溶出介质下的溶出曲线f2均大于50。在本发明的配方中,虽然各种主辅料均为本领域中的常用原料,但是这并不代表本发明的配方就能够简单地通过本领域的常规技术手段获得。并且,与其他领域不同,在制药药领域,任何原料要作为药用主辅料都需要通过相关部门严格的层层批准,因此目前所选用的辅料肯定都是现有技术中公开的,在辅料中很难有新材料,因此目前绝大多数对于药物制剂的创新都集中于如何从已有的原料库中复配出具有突出技术效果的组合。虽然采用的都是现有原料,但是这并不代表本领域技术人员就能够通过常规试验就轻易地获得优化的配方。原因在于药用原料有成千上万种,本领域技术人员很难发现其中的某几种按特定比例复配后会具有特别好的效果,虽然理论上也是可以通过有限次试验试错后获得,但是这工作量显然是巨大的。在上述背景下,本发明成功研制出了在药效上与原研药制剂具有高度一致性的盐酸美金刚缓释胶囊,填补了目前市场上该类药物无高质量仿制药制剂的空白。作为优选,所述空白丸芯为蔗糖丸芯;优选卡乐康成品蔗糖丸芯。所述粘合剂选自聚乙烯吡咯烷酮、羟丙基纤维素、羟丙甲基纤维素中的至少一种;所述缓释材料为乙基纤维素、丙烯酸树脂、醋酸纤维素、丙烯酸树脂、聚乙烯中的至少一种;所述抗粘剂选自滑石粉、胶态二氧化硅、硬脂酸镁、硅酸镁、单硬脂酸甘油酯中的至少一种。所述致孔剂选自聚乙烯吡咯烷酮、羟丙基纤维素、羟丙甲基纤维素中的至少一种;所述增塑剂选自邻苯二甲酸二乙酯、邻苯二甲酸二甲酯、柠檬酸三乙酯、邻苯二甲酸丁苄酯中的至少一种。作为进一步的优选,所述粘合剂为羟丙甲基纤维素;所述缓释材料为乙基纤维素;所述致孔剂为羟丙甲基纤维素;所述增塑剂为柠檬酸三乙酯;所述抗粘剂为滑石粉。本发明团队在经过大量试验后,发现上述选择的辅料效果最佳。作为优选,所述蔗糖丸芯的粒径为15~30目。作为进一步的优选,所述蔗糖丸芯的粒径为20~25目。本发明团队对微丸平均粒径进行评估,经过大量试验后将蔗糖丸芯的大小确定为20/25目(710-850μm)。此粒径的蔗糖丸芯经过本处方上药和缓释层包衣后,得到的微丸直径约900μm。微丸的粒径大小会影响缓释层的厚度,微丸过小导致释放变慢,微丸过大导致释放变快。作为优选,所述胶囊为硬明胶。上述盐酸美金刚缓释胶囊的制备方法,包括以下步骤:1)向乙醇水溶液中加入粘合剂搅拌至溶解,然后加入盐酸美金刚搅拌至溶解,制得上药包衣液。2)安装b型气流分布板,倒入空白丸芯,开机预热空白丸芯,当空白丸芯温度达到35-40℃后开始喷雾,空白丸芯温度控制范围35-40℃;上药包衣液喷完后,关闭喷雾,关闭加热,继续干燥,关闭进风,出料,制得上药微丸;3)在容器中依次加入乙醇、缓释材料、增塑剂、致孔剂,期间当前一物料搅拌溶解后再加入后一种物料,添加完毕后密封,静置;静置后边搅拌边加入抗粘剂并搅拌使其充分混悬,以抗粘剂不沉底为宜,制得缓释层包衣液。4)安装b型气流分布板,倒入上药微丸,开机上药微丸,当上药微丸温度达到30-34℃后开始喷雾,上药微丸温度控制范围30-34℃;喷雾过程中对缓释包衣液持续进行搅拌;缓释层包衣液喷完后,关闭喷雾,关闭加热,继续干燥,关闭进风,出料,制得盐酸美金刚缓释微丸。5)将盐酸美金刚缓释微丸与抗粘剂混合均匀后将其装入胶囊中,制成盐酸美金刚缓释胶囊。作为优选,步骤1)中,上药包衣液中盐酸美金刚的占比为5-20wt%。作为进一步的优选,步骤1)中,上药包衣液中盐酸美金刚的占比为8-15wt%。主药和粘合剂的溶剂既不能太粘又不能太稀,否则无法保证药物层的成功包裹。浓度过低会导致上药时间过长,且微丸上药时间过长会导致包裹上去的api被微丸之间的互相摩擦而磨损下来,导致微丸含量偏低。浓度过高会导致粘合剂浓度变大,影响雾化效果,对上药过程带来一定难度。上药包衣液中盐酸美金刚的占比为8-15wt%也是基于盐酸美金刚的溶解度考虑,浓度过高会导致部分盐酸美金刚不溶解或溶解后析出。作为优选,步骤2)和步骤4)中,继续干燥的时间为5-10min。作为优选,步骤5)中,所述抗粘剂占盐酸美金刚缓释微丸质量的0.1-0.3%。与现有技术对比,本发明的有益效果是:1、本发明的盐酸美金刚缓释胶囊在ph=1.2hcl和2g/lnacl溶出介质900ml,100转条件下满足:时间(h)溶出释放(%)1不多于20435-55872-9212不少于85本发明在配方以及工艺不同的情况下,其与原研药制剂盐酸美金刚缓释胶囊namendaxr在药效上能够保持高度的一致性,与原研药制剂对比在5种溶出介质下的溶出曲线f2均大于50。2、空白丸芯通过包衣液上药制得的上药小丸,该小丸在形状上接近圆形、大小相近。对形状粒度可控的上药小丸进行缓释包衣,使得包衣形成的膜的厚薄也可控。在药物的释放过程中药物的释放速度主要由包衣膜的厚薄来决定,膜的厚度均匀可控,保证了药物制剂工艺的重现性和药物制剂的稳定性。同时为了增加小颗粒之间的润滑和抗粘效果,将缓释层包衣后的微丸与滑石粉混合。3、本发明采用多颗粒系统,药物通过膜孔渗透扩散至释放介质中,多颗粒系统的优点在于如果有少数几颗颗粒包衣膜有破损突释,不会影响整个剂量单元的释放速度,从而将药物突释的风险降到最低,确保药物持续、均匀缓慢地释放药物,且因体积小,药物服用时不易受食物的影响,提高疗效。本发明生产方法简单易行,宜于工业化生产,有较大的应用价值。4、本发明的盐酸美金刚缓释胶囊,相较于原研药制剂在各种溶出介质中,其释放曲线对乙醇的抗干扰能力更强。附图说明图1为实施例3(处方号nb1676:45)批次ph1.2,hcland2g/lnacl溶出度曲线与原研制剂对比图;图2为实施例3(处方号nb1676:45)批次ph1.2hcl溶出度曲线与原研制剂对比图;图3为实施例3(处方号nb1676:45)批次ph4.5缓冲液溶出度曲线与原研制剂对比图;图4为实施例3(处方号nb1676:45)批次ph6.8缓冲液溶出度曲线与原研制剂对比图;图5为实施例3(处方号nb1676:45)批次水中溶出度曲线与原研制剂对比图6.nb1676.63批次溶出度曲线图(16%增重);图7为nb1676.66批次溶出度曲线(16%增重);图8为乙醇诱导的剂量倾泻研究图,5%(v/v)乙醇;图9为乙醇诱导的剂量倾泻研究图,20%(v/v)乙醇;图10.乙醇诱导的剂量倾泻研究图,40%(v/v)乙醇;图11为7mg和28mg的溶出度对比图,ph4.5,f2=57.1(nb1676∶45为28mg);图12为7mg和28mg的溶出度对比图,ph6.8,f2=66.5(nb1676∶45为28mg);图13为7mg和28mg的溶出度对比图,水,f2=70.2(nb1676∶45为28mg);图14为7mg溶出度对比图,f2=57.0;图15为14mg溶出度对比图,f2=58.3;图16.为21mg溶出度对比图,f2=59.6。具体实施方式下面结合实施例对本发明作进一步的描述。总实施例一种盐酸美金刚缓释胶囊,包括胶囊和填充于所述胶囊内的盐酸美金刚缓释微丸,所述盐酸美金刚缓释微丸由里至外依次包括空白丸芯、主药层、缓释包衣层。所述主药层中包括盐酸美金刚和粘合剂,所述粘合剂为水溶性粘合剂或醇溶性粘合剂;所述缓释包衣层中包括缓释材料、抗粘剂、致孔剂和增塑剂,所述缓释材料为醇溶性材料。所述盐酸美金刚缓释胶囊中包括以下重量份的原料:空白丸芯100-150份,盐酸美金刚28份,粘合剂11-17份,缓释材料5-14份,抗粘剂4-10.1份,致孔剂2.5-6.5份,增塑剂1.2-3.1份。优选地,所述空白丸芯为卡乐康成品蔗糖丸芯(优选15~30目,最优选20~25目);所述粘合剂选自聚乙烯吡咯烷酮、羟丙基纤维素、羟丙甲基纤维素中的至少一种;所述缓释材料为乙基纤维素、丙烯酸树脂、醋酸纤维素、丙烯酸树脂、聚乙烯中的至少一种;所述抗粘剂选自滑石粉、胶态二氧化硅、硬脂酸镁、硅酸镁、单硬脂酸甘油酯中的至少一种。所述致孔剂选自聚乙烯吡咯烷酮、羟丙基纤维素、羟丙甲基纤维素中的至少一种;所述增塑剂选自邻苯二甲酸二乙酯、邻苯二甲酸二甲酯、柠檬酸三乙酯、邻苯二甲酸丁苄酯中的至少一种。最优选地,所述粘合剂为羟丙甲基纤维素;所述缓释材料为乙基纤维素;所述致孔剂为羟丙甲基纤维素;所述增塑剂为柠檬酸三乙酯;所述抗粘剂为滑石粉。上述盐酸美金刚缓释胶囊的制备方法,包括以下步骤:1)向乙醇水溶液中加入粘合剂搅拌至溶解,然后加入盐酸美金刚搅拌至溶解,制得上药包衣液,上药包衣液中盐酸美金刚的占比为5-20wt%(优选8-15wt%)。2)安装b型气流分布板,倒入空白丸芯,开机预热空白丸芯,当空白丸芯温度达到35-40℃后开始喷雾,空白丸芯温度控制范围35-40℃;上药包衣液喷完后,关闭喷雾,关闭加热,继续干燥5-10min,关闭进风,出料,制得上药微丸。3)在容器中依次加入乙醇、缓释材料、增塑剂、致孔剂,期间当前一物料搅拌溶解后再加入后一种物料,添加完毕后密封,静置;静置后边搅拌边加入抗粘剂并搅拌使其充分混悬,以抗粘剂不沉底为宜,制得缓释层包衣液。4)安装b型气流分布板,倒入上药微丸,开机上药微丸,当上药微丸温度达到30-34℃后开始喷雾,上药微丸温度控制范围30-34℃;喷雾过程中对缓释包衣液持续进行搅拌;缓释层包衣液喷完后,关闭喷雾,关闭加热,继续干燥5-10min,关闭进风,出料,制得盐酸美金刚缓释微丸。5)将盐酸美金刚缓释微丸与抗粘剂(占盐酸美金刚缓释微丸质量的0.1-0.3%)混合均匀后将其装入胶囊(优选硬明胶)中,制成盐酸美金刚缓释胶囊。实施例1一、上药微丸处方:名称单位用量mg百分比%批处方(kg)卡乐康成品蔗糖丸芯(20-25目)12073.1712盐酸美金刚2817.072.8羟丙甲基纤维素169.761.695%乙醇150/15纯化水100/10合计(除去挥发溶剂)164100.0016.4在50l配液罐中加入95%乙醇15kg与纯化水10kg搅拌5min配制成乙醇溶液25kg(溶解剂),加入羟丙甲基纤维素(1.6kg)搅拌至溶解,然后加入原料2.8kg搅拌溶解10min。安装b型气流分布板,调节喷枪喷雾角度,倒入空白丸芯,开机预热空白丸芯。当空白丸芯温度达到36℃后开始喷雾,物料温度控制范围35-40℃。上药包衣液喷完后,关闭喷雾,关闭加热,继续干燥8min,关闭进风,出料,制得上药微丸。二、缓释处方:名称单位用量mg百分比%批处方(kg)上药微丸16482.9516.4乙基纤维素147.081.4羟丙甲基纤维素6.53.290.65柠檬酸三乙酯3.11.570.31滑石粉10.15.111.0195%乙醇50050合计(除去挥发溶剂)197.7100.0019.77在100l容器中加入物料。加料顺序为:乙醇50kg(溶剂)→乙基纤维素1.4kg→柠檬酸三乙酯0.31kg(搅拌至少30min)→羟丙甲基纤维素(0.65kg),一种物料搅拌溶解后再加入另一种物料,密封,静置过夜。次日边搅拌边加入滑石粉,搅拌至少30min,使其充分混悬,以滑石粉不沉底为宜。安装b型气流分布板,调节喷枪喷雾角度,倒入上药微丸,开机预热微丸,当物料温度达到33℃后开始喷雾。物料温度控制范围32-34℃。喷雾过程中包衣液持续进行搅拌。缓释层包衣液喷完后,关闭喷雾,关闭加热,继续干燥8min,关闭进风,出料。将19.77kg缓释小丸加入0.2%的滑石粉的以常规方式装入硬明胶胶囊中,每粒胶囊中盐酸美金刚的含量为28mg。实施例2一、上药微丸处方:名称单位用量mg百分比%批处方(kg)卡乐康成品蔗糖丸芯(20-25目)12574.4012.5盐酸美金刚2816.672.8羟丙甲基纤维素158.931.595%乙醇160/16纯化水90/9合计(除去挥发溶剂)168100.0016.8在50l配液罐中加入95%乙醇16kg与纯化水9kg搅拌5min配制成乙醇溶液25kg(溶解剂)。加入羟丙甲基纤维素e5(1.5kg)搅拌至溶解,然后加入原料2.8kg搅拌溶解10min。安装b型气流分布板,调节喷枪喷雾角度,倒入空白丸芯,开机预热空白丸芯。当空白丸芯温度达到35℃后开始喷雾,空白丸芯温度控制范围35-39℃。上药包衣液喷完后,关闭喷雾,关闭加热,继续干燥5min,关闭进风,出料,制得上药微丸。二、缓释处方:名称单位用量mg百分比%批处方(kg)上药微丸16892.9716.8乙基纤维素52.770.5羟丙甲基纤维素2.51.380.25柠檬酸三乙酯1.20.660.12滑石粉42.210.495%乙醇25025合计(除去挥发溶剂)180.7100.0018.07在50l容器中加入物料。加料顺序为:乙醇25kg(溶剂)→乙基纤维素0.5kg→柠檬酸三乙酯0.12kg(搅拌至少30min)→羟丙甲基纤维素(0.25kg),一种物料搅拌溶解后再加入另一种物料,密封,静置过夜。次日边搅拌边加入滑石粉,搅拌至少30min,使其充分混悬,以滑石粉不沉底为宜。安装气流分布板b,调节喷枪喷雾角度,倒入上药微丸,开机预热上药微丸,当上药微丸温度达到31.5℃后开始喷雾。上药微丸温度控制范围30-33℃。喷雾过程中包衣液持续进行搅拌。缓释层包衣液喷完后,关闭喷雾,关闭加热,继续干燥5-10min,关闭进风,出料。将18.07kg缓释小丸加入0.2%的滑石粉的以常规方式装入硬明胶胶囊中,每粒胶囊中盐酸美金刚的含量为28mg。实施例3一、上药微丸处方:在50l配液罐中加入95%乙醇14kg与纯化水10kg搅拌5min配制成乙醇溶液24kg(溶解剂),加入羟丙甲基纤维素e5(1.4kg)搅拌至溶解,然后加入原料2.8kg搅拌溶解10min。安装b型气流分布板,调节喷枪喷雾角度,倒入空白丸芯,开机预热空白丸芯。当空白丸芯温度达到35℃后开始喷雾,空白丸芯温度控制范围35-39℃。上药包衣液喷完后,关闭喷雾,关闭加热,继续干燥5-10min,关闭进风,出料,制得上药微丸。二、缓释处方:名称单位用量mg百分比%批处方(kg)上药微丸16686.2316.6乙基纤维素115.711.1羟丙甲基纤维素52.600.5柠檬酸三乙酯2.51.300.25滑石粉84.160.895%乙醇380/38合计(除去挥发溶剂)192.5100.0019.25在容器中加入物料。加料顺序为:乙醇38kg(溶剂)→乙基纤维素1.1kg→柠檬酸三乙酯0.25kg(搅拌至少30min)→羟丙甲基纤维素0.5kg,一种物料搅拌溶解后再加入另一种物料,密封,静置过夜。次日边搅拌边加入滑石粉,搅拌至少30min,使其充分混悬,以滑石粉不沉底为宜。安装b型气流分布板,调节喷枪喷雾角度,倒入上药微丸,开机预热上药微丸,当上药微丸温度达到31.5℃后开始喷雾,喷雾过程中包衣液持续进行搅拌。上药微丸温度控制范围30-33℃。缓释层包衣液喷完后,关闭喷雾,关闭加热,继续干燥5-10min,关闭进风,出料。将19.25kg缓释小丸加入0.2%的滑石粉的以常规方式装入硬明胶胶囊中,每粒胶囊中盐酸美金刚的含量为28mg。本发明团队进行对比溶出曲线后发现实施例3(处方号nb1676:45)与原研药制剂namendaxr(厂家forestlabsllc)拟合度最佳。实施例3(处方号nb1676∶45)处方工艺的产品与原研制剂进行5条溶出曲线的对比结果附图所示,其中:图1为实施例3(处方号nb1676∶45)批次ph1.2,hcland2g/lnacl溶出度曲线与原研制剂对比图;图2为实施例3(处方号nb1676:45)批次ph1.2,hcl溶出度曲线与原研制剂对比图;图3为实施例3(处方号nb1676:45)批次ph4.5缓冲液溶出度曲线与原研制剂对比图;图4为实施例3(处方号nb1676:45)批次ph6.8缓冲液溶出度曲线与原研制剂对比图;图5为实施例3(处方号nb1676:45)批次水中溶出度曲线与原研制剂对比图。该处方的样品在五种溶出介质中进行检测:ph1.2(nacl)、ph1.2(无nacl)、ph4.5、ph6.8和水。其溶出度检测结果如图1、图2、图3、图4、图5所示。这些缓冲液中的溶出度相似因子均超过50,因此,实施例3(处方号nb1676:45)处方被确定为主导处方。重现性测试:为了确认实例3处方的工艺重现性,本发明团队另外制作了两个处方相同的批次(nb1676:63和nb1676:66)。其溶出度曲线如图6和图7所示。这两次批次的溶出度曲线与rld也基本一致。f2因子分别为79.7和78.0,均超过50。药物释放-乙醇诱导的剂量倾泻研究目的:药物在乙醇溶液中的释放度曲线影响安全性。该项的意义在于避免药物在乙醇的作用下改变其生物利用度,进而提高患者的用药风险。本发明团队进行了一项体内乙醇诱导的剂量倾泻研究,试液为0.1nhcl和5%,20%,40%(v/v)乙醇的混合溶液。总实验时间为2小时,每隔15分钟取样一次。在各试液中,根据先导处方生产的胶囊其溶出相似与rld(数据如图8,图9,图10所示)。结果显示,相较于rld,先导处方在各种溶出介质中,其释放曲线更不容易受乙醇所干扰。对不同规格(装量)的研究盐酸美金刚缓释胶囊有4种不同剂量7mg,14mg,21mg和28mg。胶囊中填充7mg,14mg,21mg和28mg含量的微丸,这些微丸上药层和缓释层成分均相同,仅填充量不同,该方式与rld一致。例如,7mg胶囊的填充量只有28mg胶囊的四分之一。依照先导处方,28mg胶囊的缓释微丸(和滑石粉混合后)理论填充量为192.5mg,那7mg胶囊为48.13mg,14mg胶囊为96.25mg,21mg胶囊为144.38mg。很明显,7mg剂量的溶出曲线应该与14mg,21mg和28mg相似。为了证明这个,本发明团队在不同溶出介质中对7mg和28mg的溶出度进行了对比,溶出曲线和f2如图11,图12和图13所示。所有相似因子均>50,证明最低剂量与28mg拥有相似的体外溶出度。其中,图11为7mg和28mg的溶出度对比,ph4.5,f2=57.1(nb1676:45为28mg);图12为7mg和28mg的溶出度对比,ph6.8,f2=66.5(nb1676:45为28mg);图13为7mg和28mg的溶出度对比,水,f2=70.2(nb1676:45为28mg)7mg,14mg,21mg与rld的溶出度对比为了证明7mg,14mg和21mg与rld有相似的溶出度,在官方介质中,将三种剂量的产品分别与对应剂量的rld进行对比。溶出曲线如图14,图15和图16所示。三种剂量的f2均>50,证明其与rld拥有相似的体外溶出度。其中,图14为7mg溶出度对比,f2=57.0;图15为14mg溶出度对比,f2=58.3;图16为21mg溶出度对比,f2=59.6。本发明盐酸美金刚缓释胶囊在ph1.2,hcl和2g/lnacl溶出介质900ml,100转条件下满足:时间(h)溶出释放(%)1不多于20435-55872-9212不少于85本发明的盐酸美金刚缓释胶囊处方与原研厂家forestlabsllc的参比制剂namendaxr不同,但本发明团队开发的处方经过3批10万粒的车间中试放大批生产,对比5种溶出介质其溶出曲线与rld相似度均在50以上。3批次间处方重现性好,批间差异小。此产品不同规格仅灌装量不同,在不同规格下与原研制剂均能保持溶出曲线f2大于50。本发明团队进行了一项体内乙醇诱导的剂量倾泻研究,试液为0.1nhcl和5%,20%,40%(v/v)乙醇的混合溶液。总实验时间为2小时,每隔15分钟取样一次。结果显示,相较于rld,自研处方在各种溶出介质中,其释放曲线更不容易受乙醇所干扰。上述结果证明本发明所设计的盐酸美金刚缓释胶囊的处方和工艺具有其创新性,且产品质量能与原研厂家forestlabsllc的参比制剂namendaxr保持高度相同。本发明中所用原料、设备,若无特别说明,均为本领域的常用原料、设备;本发明中所用方法,若无特别说明,均为本领域的常规方法。以上所述,仅是本发明的较佳实施例,并非对本发明作任何限制,凡是根据本发明技术实质对以上实施例所作的任何简单修改、变更以及等效变换,均仍属于本发明技术方案的保护范围。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1