基于皮肤菌群分析的定制化护肤产品和个人护理产品的制作方法
交叉引用
本申请要求于2017年3月10日提交的美国临时专利申请号62/469,655的优先权,所述申请通过引用整体并入本文。
发明背景
约100万亿个微生物生存在人体内和人体表上,远远超过了人体的大约10万亿个人细胞。这些通常无害的病毒、细菌和真菌被称为共生或互生生物体。
技术实现要素:
共生和互生的生物体可以以多种方式帮助我们的身体健康:它们帮助我们消化食物并获取诸如维生素b和k等营养物,促进免疫系统的发育并通过与例如引起疾病的细菌病原体竞争而防止其定植。将在个体体内和体表上生存的所有微生物,即共生微生物、互生微生物和致病性微生物,统称为微生物组。将构成个体身体的微生物组的生物体的代谢过程和/或代谢过程产物称为代谢组。微生物组内生物体的平衡以及与构成微生物组的这些生物体相关的代谢组与个体的健康状态密切相关,反之亦然。
本文描述了系统和方法,用于生成供人和动物使用的定制化护肤和个人护理产品,更特别地但非限制性地用于基于对栖息在皮肤和皮下组织的菌群和/或菌群的代谢活性的初步评价来开发个人护理产品。
本文描述了系统和方法,其用于分析皮肤和皮下组织菌群例如微生物组及其相关代谢组,将皮肤和皮下组织菌群和代谢组的所得谱和健康谱进行比较(表示为落入由一组健康皮肤类型和/或不健康皮肤类型确定的范围内的菌群的量和多样性),以及随后定制护肤和个人护理产品,所述产品将增加驻留于测试受试者的皮肤和皮下组织上的菌群及其相关的代谢组或将健康的菌群谱复制到测试受试者的皮肤和皮下组织上。
下一代测序(ngs)为快速并准确地对栖息在皮肤和皮下组织的微生物组进行鉴别和谱分析创造了机会,继而为创建定制化或个性化的护肤和个人护理产品创造了机会,这些产品维持健康的微生物组,或通过混合特别创建以建立健康谱的共生和/或互生生物体的混合物将谱向健康的平衡或谱转变。最佳菌群还以协同方式与宿主免疫系统相互作用,进一步传播其健康益处。个体的相关代谢组还可以通过基于质谱法的系统或使用基于基因组学的代谢组建模和流量平衡分析来进行谱分析,并用于建立健康的代谢组谱。也可以补充任何有益代谢物的不足。
某些皮肤病学状况的传统治疗包括对包括共生和互生细菌在内的微生物组产生巨大影响的抗生素。某些皮肤病学状况的其他传统治疗包括对免疫反应具有局部和全身作用的抗炎药,如类固醇。如果皮肤状况是由于共生或互生微生物的失衡或缺乏、机会性或致病性细菌过多,或必需或有益代谢物的缺乏引起的,则这两种传统治疗即基于抗生素和类固醇的疗法都可能无法解决皮肤状况的根本原因。
本文描述了表征受试者的皮肤或皮下组织的微生物组的方法。所述方法包括:a)从所述受试者的所述皮肤或皮下组织获得包含多种微生物的样品;以及b)对所述多种微生物进行分析和分类以表征所述受试者的所述微生物组,从而表征所述受试者的所述微生物组。在一些实施方案中,所述方法进一步包括将所述受试者的所述微生物组与参考微生物组进行比较,或生成所述受试者的微生物组谱,或鉴别所述受试者患有或有风险发展出的疾病或病症,或为所述受试者提供个性化的治疗方案。在各个实施方案中,所述参考微生物组被分类为具有健康谱,并且所述受试者的所述微生物组与所述参考微生物组之间的相似性将所述受试者的所述微生物组鉴别为具有健康谱。备选地,所述参考微生物组被分类为患有疾病或病症或处于患疾病或病症的风险中,并且所述受试者的所述微生物组与所述参考微生物组之间的相似性将所述受试者的所述微生物组鉴别为患有所述疾病或病症或处于患所述疾病或病症的风险中。
在另一方面,本发明提供了表征多个受试者的皮肤或皮下组织的微生物组的方法。所述方法包括:a)从所述多个受试者的所述皮肤或皮下组织获得多个样品,每个样品包含多种微生物;以及b)对所述多个样品中的每个样品的所述多种微生物进行分析和分类,以鉴别所述多个样品中每一个的微生物组,从而生成包括所述多个受试者的所述微生物组的表征的分析结果。在一些实施方案中,所述方法进一步包括对所述分析结果进行聚类以鉴别所述多个样品的单独队列。在一些实施方案中,每个单独的队列表现出特定的表型或谱。在一些实施方案中,每个单独的队列包括具有相似微生物组的样品、来自患有常见皮肤疾病或病症的受试者的样品或来自具有相似代谢物谱的受试者的样品。
在另一方面,本发明提供了一种诊断受试者的疾病或病症的方法。所述方法包括:a)从所述受试者的所述皮肤或皮下组织获得包含多种微生物的样品;b)对所述多种微生物进行分析和分类以鉴别所述受试者的微生物组;以及c)将所述受试者的所述微生物组与代表患有所述疾病或病症或处于所述疾病或病症的风险中的受试者的微生物组的参考微生物组进行比较,其中所述受试者的所述微生物组与所述参照微生物组之间的相似性指示所述受试者患有所述疾病或病症或处于患有所述疾病或病症的风险中,从而诊断出所述受试者的疾病或病症。在一些实施方案中,所述方法进一步包括向所述受试者提供个性化的治疗方案。在一些实施方案中,所述方法进一步包括配制定制化治疗制剂并将其施用于所述受试者。
在另一方面,本发明提供了为患有疾病或病症或处于疾病或病症的风险中的受试者配制定制化治疗制剂的方法。所述方法包括:a)从所述受试者的所述皮肤或皮下组织获得包含多种微生物的样品;b)对所述多种微生物进行分析和分类以鉴别所述受试者的微生物组;c)将所述受试者的所述微生物组与代表患有所述疾病或病症或处于所述疾病或病症的风险中的受试者微生物组的参考微生物组进行比较,其中所述受试者的所述微生物组与所述参考微生物组之间的相似性指示所述受试者处于所述疾病或病症的风险中,或患有所述疾病或病症;以及d)基于所述受试者的所述微生物组与代表患有所述疾病或病症或处于所述疾病或病症的风险中的受试者微生物组的参考微生物组的比较,配制定制化治疗制剂,从而配制定制化治疗制剂。在另一方面,向所述受试者提供经由所述方法配制的治疗制剂。
本文描述了表征受试者组织的微生物组以评估体味的方法。所述方法包括:a)从所述受试者获得包含多种微生物的样品;b)对所述多种微生物进行分析和分类以表征所述受试者的所述微生物组;c)将所述受试者分类为低体味或高体味;以及d)任选地向所述受试者施用组合物,如治疗制剂,从而表征所述受试者的所述微生物组。在实施方案中,所述细菌是丙酸杆菌(propionibacteria)属、葡萄球菌(staphylococci)属或棒杆菌(corynebacteria)属。在一个实施方案中,分类包括确定细菌菌株的不同种如痤疮丙酸杆菌(propionibacteriumacnes)的不同种的比例。
本文描述了一种评估和治疗受试者的体味的方法。所述方法包括:a)从所述受试者获得包含细菌的样品;b)对所述细菌进行分析和分类以表征所述受试者的微生物组,其中分析和分类包括确定痤疮丙酸杆菌的不同种的丰度;c)基于痤疮丙酸杆菌的不同种的丰度提供对所述受试者的体味评估;以及d)任选地向所述受试者施用组合物,如治疗制剂,从而评估和治疗所述受试者的体味。
本文描述了一种用于表征提供微生物组的个体的方法,其包括:生成包含与所述微生物组相关的核苷酸序列的序列谱;生成代谢组谱,所述代谢组谱选自与所述微生物组相关的细胞生长率、与所述微生物组相关的营养摄取率和与所述微生物组相关的副产物分泌率;将所述序列谱和所述代谢组谱与参考谱进行比较,从而生成比较结果;以及基于所述比较结果生成所述个体的表征。在一些实施方案中,所述样品包括皮肤或毛发。在一些实施方案中,使用全基因组测序生成多个核苷酸序列,在一些实施方案中,使用下一代测序生成所述多个核苷酸序列。在一些实施方案中,使用sanger测序生成所述多个核苷酸序列。在一些实施方案中,使用16srdna测序生成所述多个核苷酸序列。在一些实施方案中,使用16srrna测序生成所述多个核苷酸序列。在一些实施方案中,所述多种微生物中的一种或多种包括来自丙酸杆菌属、葡萄球菌属或棒杆菌属的细菌。在一些实施方案中,使用质谱法生成所述代谢谱。在一些实施方案中,通过机器学习算法生成所述一个或多个参考谱,所述机器学习算法采用来自未患有与组织样品相关的病症的个体的微生物组和代谢组数据来训练。在一些实施方案中,通过机器学习算法生成所述比较结果,所述机器学习算法采用来自患有与所述组织样品相关的病症的个体和未患有所述病症的个体的微生物组和代谢组数据来训练。在一些实施方案中,所述病症包括寻常痤疮。在一些实施方案中,所述病症包括体味。在一些实施方案中,所述组织样品的所述表征包括确定所述组织样品内病症的存在和所述病症的相对存在程度。在一些实施方案中,所述比较结果、所述序列谱和所述代谢组谱中的一个或多个用于确定定制治疗方式。在一些实施方案中,所述定制治疗方式包括一种或多种促进所述多种微生物中的一种或多种生长的药剂。
本文描述了一种用于表征提供微生物组的个体的系统,其包括:处理器;以及非暂时性计算机可读存储介质,所述非暂时性计算机可读存储介质编码有所述处理器可执行的指令,所述指令使所述处理器:生成包含与所述微生物组相关的序列的序列谱;生成代谢组谱,所述代谢组谱选自与所述微生物组相关的细胞生长率、与所述微生物组相关的营养摄取率和与所述微生物组相关的副产物分泌率;将所述序列谱和所述代谢组谱与一个或多个参考谱进行比较,从而产生比较结果;以及基于所述比较结果生成所述个体的表征。在一些实施方案中,所述样品包括皮肤或毛发。在一些实施方案中,使用全基因组测序生成所述多个核苷酸序列,在一些实施方案中,使用下一代测序生成所述多个核苷酸序列。在一些实施方案中,使用sanger测序生成所述多个核苷酸序列。在一些实施方案中,使用16srdna测序生成所述多个核苷酸序列。在一些实施方案中,使用16srrna测序生成所述多个核苷酸序列。在一些实施方案中,所述多种微生物中的一种或多种包括来自丙酸杆菌属、葡萄球菌属或棒杆菌属的细菌。在一些实施方案中,使用质谱法生成所述代谢谱。在一些实施方案中,通过机器学习算法生成所述一个或多个参考谱,所述机器学习算法采用来自未患有与所述组织样品相关的病症的个体的微生物组和代谢组数据来训练。在一些实施方案中,通过机器学习算法生成所述比较结果,所述机器学习算法采用来自患有与所述组织样品相关的病症的个体和未患有所述病症的个体的微生物组和代谢组数据来训练。在一些实施方案中,所述病症包括寻常痤疮。在一些实施方案中,所述病症包括体味。在一些实施方案中,所述组织样品的所述表征包括确定所述组织样品内病症的存在和所述病症的相对存在程度。在一些实施方案中,所述比较结果、所述序列谱和所述代谢组谱中的一个或多个用于确定定制治疗方式。在一些实施方案中,所述定制治疗方式包括一种或多种促进所述多种微生物中的一种或多种生长的药剂。
附图说明
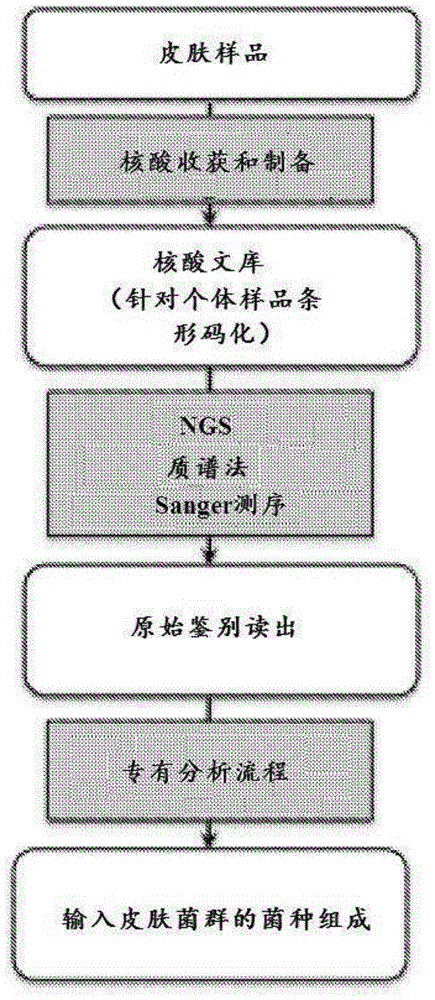
图1示出了用于对皮肤和皮下组织菌群进行谱分析的示例性实验和分析流程。
图2示出了生成健康共有谱或参考谱的示例性示意图。
图3示出了一个或多个样品与一个或多个参考谱的比较的示例性示意图。
图4示出了如本文所述的系统和方法的实施方案中使用的,用于对基因组规模代谢重建或gsm进行建模的算法的示意图。
图5示出了用于对从个体获取的样品进行分类并向该个体提供定制疗法的方法的示意图。
图6示出了如本文所述的系统的示例性实施方案。
图7示出了示出本发明的一个实施方案中的平均微生物组成的图。
图8示出了示出本发明的一个实施方案中的微生物组成的图。
图9示出了示出本发明的一个实施方案中的微生物组成的图。
图10示出了示出本发明的一个实施方案中的微生物组成的图。
图11示出了示出本发明的一个实施方案中的不同微生物组成的图。
图12示出了描绘本发明的一个实施方案中的实验数据的图。
图13示出了描绘本发明的一个实施方案中的实验数据的图。
图14示出了描绘本发明的一个实施方案中的差异映射的图。
图15示出了描绘本发明的一个实施方案中的差异映射的图。
图16示出了呈现与生成的体味模型有关的结果的表。
图17示出了呈现与生成的体味模型有关的结果的图。
具体实施方式
如本文所用,术语“个体”是指任何人或动物。
构成微生物组的生物体的实例包括原核生物和真核生物,其可以在体外、离体和/或体内定植(即在人皮肤上生存和繁殖)或暂时栖息在人皮肤上。示例性的皮肤共生微生物包括但不限于α变形杆菌纲(alphaproteobacteria)、β变形杆菌纲(betaproteobacteria)、γ变形杆菌纲(gammaproteobacteria)、丙酸杆菌、棒杆菌、放线菌(actinobacteria)、梭菌目(clostridiales)、乳杆菌目(lactobacillales)、葡萄球菌属(staphylococcus)、芽孢杆菌属(bacillus)、微球菌属(micrococcus)、链球菌属(streptococcus)、拟杆菌目(bacteroidales)、黄杆菌目(flavobacteriales)、肠球菌属(enterococcus)、假单胞菌属(pseudomonas)、鳞斑霉属(malassezia)、maydida、德巴利酵母属(debaroyomyces)和隐球菌属(cryptococcus)。
用于表征微生物组和/或代谢组数据的系统和方法
本文描述了表征个体组织的系统和方法。在系统和方法的一些实施方案中,待表征的组织包括皮肤。本文所述的表征过程包括对取自例如个体皮肤的样品的微生物菌群和/或相关代谢组的分析。在一些实施方案中,表征过程包括确定组织的状况(例如,疾病或病症)是否是共生或互生微生物失衡或缺乏和/或相关代谢组的失衡或不足的结果。
本文描述了用于分析取自患有某些病症和疾病的个体的样品以便表征样品的系统和方法,并且在一些实施方案中,基于该表征为个体提供定制疗法。更具体地,对样品进行分析以根据以下方面来表征与样品相关的微生物组和/或代谢组数据:(a)构成微生物组的微生物的分类学,(b)与微生物组相关的代谢组谱,和/或(c)个体中微生物组和/或代谢组的物理表达。
例如,在本文所述的系统和方法的一些实施方案中,在样品内鉴别出不同细菌的百分比,并且以某种微生物过度生长的形式检测个体微生物组的失衡,该种微生物通常在正常个体(或处于未患病状态的个体)的微生物组中少量存在。
例如,在本文所述的系统和方法的一些实施方案中,根据鉴别取自个体的样品中存在的代谢物的百分比并在某代谢物的过度产生方面检测失衡来确定代谢组谱,该微生物通常在正常个体(或处于未患病状态的个体)中少量存在。
例如,在本文所述的系统和方法的一些实施方案中,通过将个体的微生物组和/或代谢组特征与正常个体(或处于未患病状态的同一个体)的微生物组和/或代谢组特征进行比较,来鉴别个体中的微生物组和/或代谢组的物理表达。即,在一些实施方案中,基于个体的微生物组和/或代谢组与其他个体的微生物组和/或代谢组的特征比较,个体的微生物组和/或代谢组的物理表达指示个体具有大量的体味。以这种方式,对个体进行分类。在该特定实例中,将个体分类为具有大量的体味。
在一些实施方案中,取自个体的样品的表征是基于一个个体的样品分析结果与一个或多个健康个体的样品分析结果的比较。健康个体提供被确定具有健康微生物组的样品或样品分析数据,例如,没有疾病或病症或其风险和/或没有特定疾病或病症。这样,在一些实施方案中,参考微生物组取自从一个或多个未患有皮肤病和/或不具有特定不良表型的健康个体获得的一个或多个细胞样品。同样地,健康谱包括落入由一组健康皮肤类型确定的范围内的菌群的量和多样性。术语“健康皮肤”包括没有皮肤状况、疾病或病症的皮肤,该皮肤状况、疾病或病症包括但不限于炎症、皮疹、皮炎、特应性皮炎、湿疹、银屑病、头皮屑、痤疮、蜂窝组织炎、酒渣鼻、疣、脂溢性角化病、光化性角化病、花斑癣、病毒疹、带状疱疹、癣和癌症,如基底细胞癌、鳞状细胞癌和黑素瘤。在基于样品分析对个体进行分类中,本文所述的系统和方法还提供对某些个体的疾病和病症的诊断。通过本文所述的系统和方法的实施方案诊断的疾病和病症的非限制性实例包括炎症、皮疹、皮炎、特应性皮炎、湿疹、银屑病、头皮屑、痤疮、蜂窝组织炎、酒渣鼻、疣、脂溢性角化病、光化性角化病、花斑癣、病毒疹、带状疱疹、癣和癌症,如基底细胞癌、鳞状细胞癌、黑素瘤、癌和肉瘤。
适用于本文所述的系统和方法的样品包括通过非侵入性技术如胶带剥离、刮擦、擦拭,或更具侵入性的技术如对受试者的活检获得的皮肤或皮下组织样品。应理解,适用于本文所述的系统和方法的样品包括衍生自个体皮肤或皮下组织的任何制品。同样,在一些实施方案中,适用于本文所述的系统和方法的样品取自显示表现出疑似由疾病或病理或生理状态如银屑病或皮炎造成的疾病或病症的皮肤区域,或周围边缘或组织。同样,取自周围边缘或周围组织的样品是指与显示表现出疾病或病症的皮肤相邻但看起来正常的受试者组织,并且这些类型的样品也适用于本文所述的系统和方法。皮肤和皮下组织构成身体的外部保护层,并包含表皮(包括角质层)和下面的真皮,并且应理解为包括汗腺和皮脂腺以及毛囊结构和指甲。在整个本申请中,可以使用形容词“皮肤”和“皮下”,并且其应被理解为通常指皮肤的属性,适合其所用于的上下文。人皮肤的表皮包括几层不同的皮肤组织。最深的一层是基底层,由柱状细胞组成。上覆层是棘层,由多角细胞组成。从棘皮层推上来的细胞是扁平化的并且合成透明角蛋颗粒以形成颗粒层。当这些细胞向外移动时,它们失去细胞核,并且透明角蛋颗粒与张力原纤维融合并混合。这形成称为透明层的透明的层。透明层的细胞紧密堆积。随着细胞从透明层中移出,它们变得压缩成许多层不透明的鳞。这些细胞都是细胞的扁平化残迹,已经完全充满角蛋白并且失去了包括细胞核在内的所有其他内部结构。这些鳞构成表皮的外层,即角质层。在角质层的底部,细胞被紧密地压紧并牢固地相互粘附,但是在较高的层中,它们变得松散地堆积,并最终在表面剥落。
使用例如本文所述的非侵入性样品采集方法获得的细胞样品用于分离在样品中、样品上或与样品相关的核酸分子或蛋白质。更具体地,分离的核酸分子包括来自微生物的dna和rna,该微生物包含与样品相关的微生物组。
图1示出了用于对皮肤和皮下组织菌群进行谱分析的示例性方法。在第一步中,用设计用于捕获各种细菌物种的最大多样性的通用引物序列扩增从皮肤或皮下组织样品收集的混合群体中微生物基因组的形成区域。在第二步中,对扩增区域进行唯一索引,以允许对来自各种来源的样品进行多路复用处理(核酸收获和制备)。在第三步中,可以将来自不同来源的扩增区域组合在一起,并在ngs平台上以配对末端(pe)模式进行测序,或者备选地可以在sanger测序、质谱法、定量pcr、免疫荧光、原位杂交或基于微生物染色的平台上进行分析。在第四步中,将鉴别平台的原始输出分配给不同的分类学组。类似的工作流程将用于映射与任何给定样品相关的代谢物。
图2示出了示例性示意图,该示意图是关于如何从健康个体队列采集数据,然后使用图1中所示的方法对其进行处理以建立健康群体的共有谱,从而捕获菌群的组成优势种和/或其相关代谢组。健康共有谱被当作用于比较任何受影响的组、群体或个体的参考。
图3示出了来自个体的队列的多个样品,他们的一种特征性皮肤状况将被收集并且他们的皮肤菌群及其相关代谢组如本文所述地进行谱分析。物种元数据谱用于鉴别导致该皮肤状况或与其相关的标志性微生物或代谢物。与之前鉴别的健康谱相反,新客户的皮肤和皮下组织菌群或代谢组组成中的任何异常(图中用问号示出)都可以甚至在早期阶段发现,并且可以用定制化或个性化的护肤产品进行固定或修复,该产品将受影响的谱向健康平衡转变,该健康平衡通过混合特别预期用于建立健康谱的共生生物体或代谢物的混合物而建立。
如本文进一步讨论的,下一代测序或“ngs”是一种强大的dna测序技术,其允许对细胞或生物体进行快速和准确的测序,并能够评价复杂的细菌群落,该细菌群落的一个很好的实例是微生物组。在一些实施方案中,在这样的ngs平台上进行每个个体的栖息菌群的鉴别。这样的平台允许以相对较短的周转时间和可扩展的通量以及足够高的灵敏度和特异性快速且准确地生成栖息在个体皮肤上的微生物组的谱。
或者,可以使用sanger测序、质谱法、定量pcr、免疫荧光、原位杂交或基于微生物染色的平台来表征个体谱。类似地,可以通过基于质谱法的系统或使用基于基因组学的代谢组建模和流量平衡分析来对微生物组或代谢组进行谱分析。所有上述鉴别方法都可以在没有任何增殖步骤的情况下在直接收集自个体的样品上实施。以这样的方式,向可培养和不可培养微生物或其相关代谢组的混合物的鉴别引入的偏差最小。
通过利用ngs的高通量能力或质谱法或sanger测序等其他微生物鉴别方法,将同时鉴别个体皮下组织上的微生物及其相关的微生物组和代谢组,并且可将所得的谱与皮肤和皮下组织谱数据库中的健康谱进行比较。与采用哪个平台进行谱分析无关,可以将上述平台作为测试提供给任何客户,并且与健康谱相比,输出可以用于确定受试者皮肤和皮下组织上哪些共生微生物、致病性微生物或互生微生物或其相关代谢物被耗尽或过度表现。
适用于本文所述的系统和方法的探针包含核酸分子,该核酸分子至少部分是单链的并且与感兴趣序列至少部分互补或至少部分基本互补。探针可以是rna、dna或rna与dna的组合。合适的探针还包含这样的核酸分子,该核酸分子包含其中主链糖不是核糖或脱氧核糖的核酸。合适的探针还包含包括肽核酸的核酸。在一些实施方案中,探针包含抗溶核活性的连接或可检测的标记,并且可以可操作地连接至其他部分,例如肽。
杂交反应可以是敏感的和选择性的,使得感兴趣的特定序列即使在其以低浓度存在的样品中也可以得到鉴别。在体外情况下,合适的严格条件可以通过例如预杂交和杂交溶液中盐或甲酰胺的浓度,或通过杂交温度来定义。特别地,可以通过降低盐的浓度、提高甲酰胺的浓度或提高杂交温度来提高严格性。例如,在高严格条件下的杂交可以于约37℃至42℃下在约50%甲酰胺中发生。杂交可以在降低的严格性条件下于约30℃至35℃下在约35%至25%的甲酰胺中发生。特别地,杂交可以在高严格条件下于42℃下在50%甲酰胺、5xsspe、0.3%sds和200mg/ml剪切和变性的鲑鱼精子dna中发生。杂交可以在如上所述的降低的严格性条件下但是于35℃的降低温度下在35%甲酰胺中发生。通过计算感兴趣核酸的嘌呤与嘧啶之比并相应调整温度,可以进一步缩小与特定严格性水平相对应的温度范围。也可以设想上述范围和条件的变化。
这样,本文所述的方法和平台可以利用核酸分子的分析,如对核酸分子进行测序。测序方法可以包括全基因组测序、下一代测序、sanger测序、16srdna测序和16srrna测序。此外,本文所述的这样的方法和平台可以利用质谱法、定量pcr、免疫荧光、原位杂交、基于微生物染色的平台或其组合。
在一些实施方案中,鉴别平台的输入可以是任何核酸,包括dna、rna、cdna、mirna、mtdna、单链或双链。该核酸可以具有任何长度,短如约5bp的寡核苷酸,长如兆碱基或更长。如本文所用,术语“核酸分子”是指dna、rna、单链、双链或三链及其任何化学修饰。实际上,考虑核酸的任何修饰。“核酸分子”可以具有几乎任何长度,从10、20、30、40、50、60、75、100、125、150、175、200、225、250、275、300、400、500、600、700、800、900、1000、1500、2000、2500、3000、3500、4000、4500、5000、6000、7000、8000、9000、10,000、15,000、20,000、30,000、40,000、50,000、75,000、100,000、150,000、200,000、500,000、1,000,000、1,500,000、2,000,000、5,000,000个甚至更多个碱基到一个全长染色体dna分子。对于分析基因表达的方法,从样品中分离的核酸通常是rna。
微小rna(mirna)是小的单链rna分子,平均长22个核苷酸,其参与调节包括人在内的多种物种的mrna表达(在bartel2004中进行了综述)。对mirna的第一个报道是在线虫秀丽隐杆线虫(c.elegans)中发现的lin-4基因的mirna(lee,feinbaum等人1993)。从此以后,在蝇、植物和哺乳动物中发现了数百种mirna。mirna通过与mrna的3’-非翻译区结合来调节基因表达,并催化i)mrna的切割;或2)翻译的抑制。mirna对基因表达的调节对于许多生物学过程(例如,细胞发育、分化、通讯和凋亡)至关重要(reinhart,slack等人2000;baehrecke2003;brennecke,hipfner等人2003;chen,li等人2004)。已经表明,mirna在小鼠上皮的胚胎发生期间具有活性,并在皮肤形态发生中起重要作用(yi,o'carroll等人2006)。
鉴于mirna在基因表达中的作用,很明显,mirna将影响(如果未完全指定)特定细胞类型中mrna的相对量,并从而确定不同细胞类型中的特定基因表达谱(即,特定mrna群体)。此外,细胞中特定mirna的特定分布在不同细胞类型中也可能将是独特的。因此,确定组织的mirna谱可以用作对该组织中的实际mrna群体进行表达谱分析的工具。因此,mirna水平和/或mirna突变的检测对于疾病检测、诊断、预后或与治疗有关的决定(即,在开始治疗方案之前或之后指示反应)或受试者中特定疾病的表征是有用的。
在实施方案中,核酸分子还可以通过经由用本领域技术人员公知的许多方法裂解收集自皮肤样品的细胞和细胞材料来分离。例如,可以使用许多可用于分离多核苷酸的许多商业产品,包括但不限于rneasytm(qiagen,valencia,ca)和trireagenttm(molecularresearchcenter,inc,cincinnati,oh)。然后可以测试或测定分离的多核苷酸的特定核酸序列,包括编码细胞因子的多核苷酸。回收核酸样品内的靶核酸分子的方法是本领域公知的,并且可以包括微阵列分析。
如本文中进一步讨论的,可以以本领域已知的许多方式分析核酸分子,这些方式可以帮助确定与个体皮肤相关的微生物组和/或代谢组。例如,可以使用特定核酸分子的探针或片段通过dna-dna或dna-rna杂交或扩增来检测核酸分子的存在。基于核酸扩增的测定涉及基于核酸序列使用寡核苷酸或寡聚物来检测含有特定dna或rna的转化体。
在另一实施方案中,可以使用特异性结合微生物组和/或代谢组的核酸分子的表达产物的抗体来表征受试者的皮肤损伤。抗体可以以修饰或不修饰的方式使用,并且可以通过将其与报道分子共价或非共价接合来标记。
多种标记和缀合技术是本领域技术人员已知的,并且可以用于各种核酸和氨基酸测定中。产生用于检测序列的经标记杂交或pcr探针的方法包括寡聚物标记、切口平移、末端标记或使用标记核苷酸的pcr扩增。备选地,可以将核酸分子或其任何片段克隆到用于产生mrna探针的载体中。这样的载体是可商购的,并且可以用于通过添加适当的rna聚合酶如t7、t3或sp6和标记的核苷酸在体外合成rna探针。可以使用多种可商购的试剂盒(pharmacia&upjohn(kalamazoo,mich.);promega(madisonwis.);以及u.s.biochemicalcorp.,cleveland,ohio)进行这些程序。可以使用以方便检测的合适的报道分子或标记包括放射性核素、酶、荧光、化学发光或生色剂以及底物、辅因子、抑制剂、磁性颗粒等。
pcr系统通常使用两个扩增引物和额外的扩增子特异的荧光杂交探针,该探针与扩增子内的位点特异性结合。探针可以包括一个或多个荧光标记部分。例如,探针可以用以下两种荧光染料标记:1)位于5’端的作为报告分子的6-羧基荧光素(fam),以及2)位于3’端的作为淬灭剂的6-羧基-四甲基罗丹明(tamra)。当发生扩增时,taqdna聚合酶的5’-3’核酸外切酶活性在延伸阶段中从探针上切割报告分子,从而将其从淬灭剂释放。所造成的报告分子染料的荧光发射的增加在pcr过程中监测,并代表所生成的dna片段的数目。原位pcr可以用于靶核酸分子的直接定位和可视化,并且可能在使表达与组织病理学发现相关中有进一步作用。
产生用于本发明核酸分子的特异性杂交探针的手段包括将核酸序列克隆到用于产生mrna探针的载体中。这样的载体是可商购的,并且可以用于通过添加适当的rna聚合酶和适当的标记的核苷酸在体外合成rna探针。杂交探针可以由多种报告分子基团标记,例如放射性核素如32p或35s或酶标记如经由亲和素/生物素偶联系统耦合到探针的碱性磷酸酶等。
痤疮丙酸杆菌是一种共生的、非孢子形成的、杆菌状(杆状)的、革兰氏阳性细菌,见于人体的多个位置,包括皮肤、口腔、泌尿道和大肠区域。痤疮丙酸杆菌可以消耗皮肤油脂并产生诸如短链脂肪酸和丙酸等副产物,已知这有助于维持健康的皮肤屏障。丙酸杆菌如痤疮丙酸杆菌还产生细菌素和类细菌素化合物(例如丙酸菌素p1g-1、詹氏杆菌素g、丙酸菌素sm1、sm2t1和痤疮菌素(acnecin)),它们抑制不期望的产乳酸细菌、革兰氏阴性细菌、酵母和霉菌。在一些实施方案中,可以用被设计用于抑制痤疮丙酸杆菌的生长和增殖的个人护理产品来治疗具有被鉴别为患有痤疮丙酸杆菌的皮肤的受试者。
在一些实施方案中,通过捕获皮肤菌群的多样性及其显著性(eminence)来协助配制个人护理产品,将个体的皮肤谱转换为个性化的skiniqtm指数,该指数是皮肤健康的整体快照。对显著性有贡献的主要因素是益生菌平衡——互生微生物和共生微生物与(机会性)病原体的比率。然而,显著性也可以包括其他可以积极影响皮肤健康的因素。这些因素可以包括负责促进或维持健康宿主皮肤的关键生物合成微生物基因、基因产物或蛋白质的存在。所有这些因素将通过但不限于皮肤炎症的减少、病原体相对量的减少以及维生素原、抗菌肽、维生素和脂肪酸的生物合成而对皮肤的整体健康有贡献。skiniqtm指数所代表的多样性和显著性的结合也可以作为皮肤健康的预测指标。例如,痤疮丙酸杆菌的某些亚种的优势可能与痤疮爆发的风险密切相关。同样,skiniqtm可以预测其他皮肤状况的发作,包括但不限于湿疹、银屑病、特应性皮炎和酒渣鼻。
skiniqtm指数是在皮肤健康测量系统下定义的,该系统将任何个体谱与皮肤谱(微生物组和/或代谢组)数据库中的“共有健康谱”进行对比,并将每个谱置于健康人群的环境中。针对每种细菌物种分别定义共有健康谱。来自健康群体的数据用于定义预期在健康个体中发现任何给定细菌物种的范围。所有这些范围为将来的比较定义了参考。skinhealthmeasurementsystemtm进一步用作强大的发现工具,其可以用于挖掘新颖微生物的丰富数据集,这些新颖微生物可以用于护肤配方中,以积极影响不同的皮肤状况,包括但不限于痤疮、特应性皮炎、银屑病和湿疹。它还可以用于挖掘不同细菌物种之间的更高水平的相互作用,这具有潜在的治疗意义。
这样,本发明设想生成参考数据库,该参考数据库包含从具有已知状态(例如正常或健康皮肤)以及各种皮肤疾病状态的受试者的皮肤样品创建的多个参考投影谱。可以将个体谱与包含参考资料的参考数据库进行比较。如果受试者的谱与数据库中特定疾病状态的谱最佳匹配,则诊断该受试者具有这样的疾病状态。多种计算机系统和软件可以用于实施本发明的分析方法,并且对于本领域技术人员而言是显而易见的。示例性软件程序包括但不限于cluster&treeview(stanford,urls:rana.lbl.govormicroarray.org)、genecluster(mit/whiteheadinstitute,url:mpr/genecluster/genecluster.html)、arrayexplorer(spotfireinc,url:spotfire.com/products/scicomp.asp#sae)以及genespring(silicongeneticsinc,url:sigenetics.com/products/genespring/index.html)(对于计算机系统和软件,还参见美国专利号6,203,987,其通过引用并入本文)。
在一些实施方案中,本发明提供了表征皮肤和/或皮下组织的方法,其包括从受试者收集含有皮肤或皮下组织菌群的样品。可以使用刷扫、刮擦、擦拭、使用胶带条或任何其他有效的微生物收集方法来收集健康个体的皮肤和皮下组织菌群。可以在ngs、sanger测序、质谱法、定量pcr、免疫荧光、原位杂交或基于微生物染色的平台上对收获的样品进行谱分析。对于基于测序的平台,这可以使用全基因组测序方法来完成,或经由针对性应用来完成,其中最突出的实例是16srdna测序。所有上述鉴别方法都可以在没有任何增殖步骤的情况下在直接收集自个体的样品上实施。以这样的方式,向可培养和不可培养微生物的混合物的鉴别引入的偏差最小。专有的分析算法可以用于鉴别每个个体的物种组成。可以从健康队列建立共有健康谱。当随着时间的推移收集更多样品时,健康谱可以实时更新。健康谱将用作用于比较所有个体样品(即,谱)的参考。所鉴别细菌的实例属于任何门,包括放线菌门、厚壁菌门、变形菌门、拟杆菌门。其通常将包括常见种,如丙酸杆菌属的种、葡萄球菌属的种、棒杆菌属的种和拟杆菌属的种。
在一些实施方案中,本发明提供了用于表征具有皮肤状况的个体的皮肤和皮下组织微生物菌群的平台或方法。具有被认为是次优的皮肤状况的个体的皮肤和皮下组织菌群可以使用刷扫、擦拭、胶带剥离或任何其他有效的微生物收集方法进行收集。可以在ngs、sanger测序、质谱法、定量pcr、免疫荧光、原位杂交或基于微生物染色的平台上对收集的微生物样品进行谱分析。对于基于测序的平台,这可以使用全基因组测序方法来完成,或经由针对性应用来完成,其中最突出的实例是16srdna测序。所有的鉴别方法都可以在没有任何增殖步骤的情况下在直接收集自个体的样品上实施。以这样的方式,向可培养和不可培养微生物的混合物的鉴别引入的偏差最小。可以为每个个体生成个人皮肤和皮下组织菌群谱。个体也可以基于其表型特征而置于特定的皮肤状况类别下。这样的聚类工作将有助于鉴别每个队列特征性的生物学显著模式。受影响队列的微生物组成与健康谱不同。与任何给定的皮肤状况相关的微生物物种可以用作尚未发展出视觉皮肤状况但可能容易出现这种状况的个体的早期诊断标志物。所鉴别细菌的实例属于任何门,包括放线菌门、厚壁菌门、变形菌门、拟杆菌门。其通常将包括常见种,如丙酸杆菌属的种、葡萄球菌属的种、棒状杆属的种和拟杆菌属的种。受损的皮肤可能影响细菌菌群的组成或可能导致非致病性细菌变得致病。
在一些实施方案中,本发明提供了用于表征共有健康皮肤和皮下组织代谢物谱的平台或方法。还可以通过基于质谱法的系统或使用基于基因组学的代谢组建模和流量平衡分析来对与皮肤和皮下组织菌群相关的代谢组进行谱分析。可以对通过使用刷扫、擦拭、胶带剥离或任何其他有效的微生物收集方法收集的样品进行提取。备选地,这些代谢物和生化物质,特别是细胞外的代谢物和生化物质,可以不经过任何细胞收获而直接从任何个体分离。表征可以在整个代谢组上进行,或者可以仅针对代谢物的子集,这些代谢物是已知的或可能在特定疾病病理学中显示出重要意义。所有上述鉴别方法都可以在没有任何增殖步骤的情况下在直接收集自个体的样品上实施。以这样的方式,在群体组成中引入的偏差最小。专有的分析算法可以用于鉴别每个个体皮肤菌群的代谢物组成。可以从健康队列建立共有健康谱。当随着时间的推移收集更多样品时,健康谱可以实时更新。健康谱将用作用于比较所有个体样品(即,谱)的参考。
在一些实施方案中,本发明提供了用于表征具有皮肤状况的个体的皮肤和皮下组织微生物菌群的平台或方法。可以通过基于质谱法的系统或使用基于基因组学的代谢组建模和流量平衡分析来对具有被认为是次优的皮肤状况的个体的皮肤和皮下组织菌群的代谢物组成进行谱分析。可以对通过使用刷扫、擦拭、胶带剥离或任何其他有效的微生物收集方法收集的样品进行提取。备选地,这些代谢物和生化物质,特别是细胞外的代谢物和生化物质,可以不经过任何细胞收获而直接从任何个体分离。表征可以在整个代谢组上进行,或者可以仅针对代谢物的子集,这些代谢物是已知的或可能显示出重要意义。所有上述鉴别方法都可以在没有任何增殖步骤的情况下在直接收集自个体的样品上实施。以这样的方式,在群体组成中引入的偏差最小。可以为每个个体生成反映皮肤和皮下组织菌群的代谢物组成的个人谱。个体也可以基于其表型特征而置于特定的皮肤状况类别下。这样的聚类工作将有助于鉴别每个队列特征性的生物学显著模式。受影响队列的代谢物组成与健康谱不同。与任何给定的皮肤状况相关的代谢物可以用作尚未发展出视觉皮肤状况但可能容易出现这种状况的个体的早期诊断标志物。
图4示出了如本文所述的系统和方法的实施方案中使用的,用于对基因组规模代谢重建或gsm进行建模的算法的示意图。在一些实施方案中,机器学习算法接收从样品提取的数据,该数据包括与特定样品(例如,皮肤或毛发样品)相关的微生物组和代谢组数据。首先训练机器学习算法以生成参考数据库,该参考数据库包括与从已知未患病和/或患有疾病的个体获取的样品相关的各种微生物和微生物代谢物的阈值。机器学习算法针对诸如营养摄取率、细胞生长率和副产物分泌率等因素对该参考数据进行建模。机器学习算法接收包括微生物组和/或代谢组数据在内的新样品数据,并将新样品数据与阈值进行比较,以确定样品的表征。下面的表1示出了用于针对健康个体的微生物组和代谢组来训练机器学习算法的实施方案的示例性数据,该微生物组和代谢组取自这些个体的皮肤和/或毛发样品。
表1
图5示出了用于对从个体获取的样品进行分类并向该个体提供定制疗法的方法的示意图。在第一步中,如本文所述对样品如皮肤或毛发样品进行测序。在第二步中,鉴别某些生物标志物,包括例如指示健康皮肤的生物标志物和指示存在痤疮的生物标志物。在第三步中,确定代谢组,并然后在第四步中,使用例如图4的算法进行代谢建模。在第五步中,确定每种生物标志物的效应量或相对表示。在第六步中,以模拟每种生物标志物在各种成分存在下的生长的方式对每种生物标志物菌株进行建模,并基于模型结果和刺激或抑制某些生物标志物生长的目标,鉴别定制疗法的潜在成分。在第七步中,确定每种潜在成分的丰度加权的度量计算。在第八步中,基于第一步到第七步的结果,推荐(或生成)定制疗法。在可选的第九步中,使用第一到第九步骤中的一个或多个来分析新样品。应理解,在该方法的某些实施方案中省略这些步骤中的一个或多个,并且在该方法的某些实施方案中,以不同的顺序执行该方法的一个或多个步骤。
因此,在一方面,本发明提供了表征受试者的皮肤或皮下组织的微生物组的方法。方法包括:a)从受试者的皮肤或皮下组织获得包含多种微生物的样品;以及b)对多种微生物进行分析和分类以表征受试者的微生物组,从而表征受试者的微生物组。在一些实施方案中,方法进一步包括将受试者的微生物组与参考微生物组进行比较或生成受试者的微生物组谱,或鉴别受试者患有或有发展风险的疾病或病症,或为受试者提供个性化的治疗方案。在各个实施方案中,参考微生物组被分类为具有健康谱,并且受试者的微生物组与参考微生物组之间的相似性将受试者的微生物组鉴别为具有健康谱。备选地,参考微生物组被分类为患有疾病或病症或处于患疾病或病症的风险中,并且受试者的微生物组与参考微生物组之间的相似性将受试者的微生物组鉴别为患有疾病或病症或处于患疾病或病症的风险中。
用于提供定制化治疗的系统和方法
皮肤病学状况的传统治疗包括使用抗生素和/或抗炎剂。抗生素(并且尤其是过于广谱的抗生素)的不良副作用往往会以相较于益处更有害的方式改变个体的微生物组。即,抗生素最适合用于治疗细菌感染,而许多皮肤病学疾病过程与细菌过度生长相关或由细菌过度生长引起,细菌过度生长导致细菌/微生物失衡。感染在许多方面不同于微生物失衡。从根本上说,通过根除传染性微生物来治疗感染,而微生物失衡通常最好通过调整或重新平衡存在失衡的皮肤区域中的微生物平衡来治疗,而不是通过根除受影响区域的微生物。这样,对罹患某些皮肤病学病症的个体进行抗生素治疗往往会根除包括微生物组的正常组分在内的细菌,而不是重新平衡微生物组的微生物,且这样的抗生素治疗往往会引起某些不良影响和失衡。抗炎剂,并且尤其是基于类固醇的抗炎剂,往往会减弱人体的免疫反应,从而减弱表皮细胞对病原体的反应,并因此往往会产生某些不良影响。同样,传统的抗生素和抗炎治疗往往无法解决某些皮肤病学病症的潜在病理生理学,因为例如,这些传统疗法的作用方式往往过于广泛,这在许多情况下会导致个体的微生物组和免疫系统的有害失衡。
本文描述了供人和动物使用的定制化护肤和个人护理产品,以及更特别地但非限制性地,基于对栖息在皮肤和皮下组织的菌群的初步评价来开发个人护理产品。本文描述了系统和方法,用于分析皮肤和皮下组织菌群及其相关代谢组,将皮肤和皮下组织菌群和代谢组的所得谱与表示为落入从一组健康皮肤类型确定的范围内的菌群量和多样性的健康谱进行比较,并且随后定制护肤和个人护理产品,所述产品将增加驻留于测试受试者的皮肤和皮下组织上的菌群及其相关的代谢组或将健康的菌群谱复制到测试受试者的皮肤和皮下组织上。
个体化皮肤测试结果用作开发个体化护肤和个人护理产品的基础,这些产品被定制成通过添加一种或多种共生和/或互生生物体和/或促进皮肤上的共生和互生生物体生长的底物来维持健康的皮肤微生物组和代谢组或使谱向健康平衡或状态转变。
在将任何个体的皮肤和皮下组织菌群和代谢组的所得谱与健康谱进行比较后,可以确定护肤产品混合物的确切组成,并且然后定制使受试者的皮肤和皮下组织菌群和代谢组最佳地朝着健康谱转变的护肤和个人护理产品。最佳的菌群和底物和代谢组也可以与宿主的免疫系统协同作用,并从这个角度来看有助于皮肤健康。
此外,可以将受试者的菌群和代谢组的组成与先前汇编的不同皮肤状况的数据库进行比较,以查看他或她将来是否容易出现任何这些皮肤状况。基于定制化或个性化的测试结果,可以通过在具有或不具有有利于共生和互生生物体增殖的必要底物和营养物的情况下将在该个体的菌落或代谢组中耗尽的共生和互生微生物或其相关代谢物的混合物混合,为该个体配制定制化或个性化的护肤或个人护理混合物。该定制化或个性化的护肤或个人护理产品是以通过维持健康的微生物组或将次优谱向健康平衡转变来建立最佳谱的方式特别创建的。最佳微生物菌群及其相关代谢组与宿主免疫系统之间的协同作用还将进一步促进皮肤健康保健。
在一些实施方案中,适用于本文所述的系统和方法的护肤产品或个人护理产品包括护肤产品,并且包括但不限于清洁产品、洗发水、护发素、爽肤水或乳霜、外用软膏和凝胶以及局部(例如,眼下)凝胶,所有这些都可以被配制为包含特别设计用于在有或没有处于活跃或休眠状态下的共生或互生生物体或共生或互生生物体的混合物的情况下将微生物群体向健康谱转变的成分。这样的护肤产品可以进一步包括治疗剂、维生素、抗氧化剂、矿物质、皮肤调理剂、聚合物、赋形剂、表面活性剂、益生菌或其部分、微生物或来自其培养物的产物,如存活的、休眠的或不活动的细菌、真菌等。
在一些实施方案中,本文所述的平台或方法可以被提供为用于对健康或具有皮肤状况的任何个体的皮肤菌群以及其相关代谢组进行谱分析的测试。这样的测试对于表征任何个体的优势皮肤菌群和代谢物将很敏感。可以对任何个体的菌群进行定制化或个性化评价,并将确定的皮肤和皮下组织菌群和代谢物与健康皮肤谱和受影响的皮肤谱进行比较。可以生成定制化或个性化的报告,该报告将指定个体皮肤和皮下组织菌群的物种组成及其相关代谢物。这份报告将征集在每个个体中被耗尽或过度表现的有益和共生物种。它还将包括在每个个体中耗尽或过度表现的有益或不期望的代谢物的列表。这可以用于配制定制化或个性化的护肤或个人护理产品。备选地,可以施用该测试以评估其他护肤和个人护理产品、疗法的表现,或者评价正常皮肤菌群或代谢物的任何破坏。该测试可以在任何皮肤治疗之前、期间和之后进行,以监测该治疗方案对皮肤菌群或其相关代谢物的功效。该测试还可以用于与特征性微生物谱或其伴随代谢物相关的皮肤状况的早期诊断。测试的敏感性允许这样的皮肤状况在其表型爆发之前及早被诊断。在一方面,本发明提供了一种用于生成为特定个体配制的定制化或个性化的护肤或个人护理产品的方法。定制化或个性化的产品包含可能在任何给定的个体中被耗尽的一种或多种有益或共生的微生物或一组化学物质和代谢物。定期施用这样的护肤产品和个人护理产品应该会将次优的谱向健康平衡转变。可以在使用专有洗剂清洁现有菌群后应用护肤产品,这将增强护肤产品微生物或其组成代谢物定植的功效。任何定制化或个性化的护肤或个人护理产品都可以包含一种或多种可培养或不可培养的微生物。备选地,定制化或个性化的产品可以是有利于互生或共生生物体的建立或增殖和/或致病生物体抑制的底物和营养物。可以在体外合成或从微生物纯化这些化学物质和代谢物。
图6示出了如本文所述的系统的示例性实施方案。在一些实施方案中,系统包括数字处理设备601。数字处理设备601包括软件应用,该软件应用被配置用于表征获取自个体的样品,并且在一些实施方案中进一步确定针对个体的定制疗法。数字处理设备601可以包括中央处理单元(cpu,本文中也称为“处理器”和“计算机处理器”)605,其可以是单核或多核处理器,或者是用于并行处理的多个处理器。数字处理设备601还包括存储器或存储位置610(例如,随机存取存储器、只读存储器、闪速存储器)、电子存储单元615(例如,硬盘)、用于与一个或多个其他系统通信的通信接口619(例如,网络适配器、网络接口)以及外围设备,诸如高速缓冲存储器。外围设备可以包括存储设备或存储介质665,其经由存储接口670与设备的其余部分通信。存储器610、存储单元615、接口619和外围设备被配置用于通过通信总线1925如主板与cpu605通信。数字处理设备601可以借助于通信接口619可操作地耦合至计算机网络(“网络”)630。网络630可以包括互联网。网络630可以是电信和/或数据网络。
数字处理设备601包括用于从用户接收信息的输入设备645,该输入设备经由输入接口650与该设备的其他元件通信。数字处理设备601可以包括经由输出接口660与设备的其他元件通信的输出设备655。
cpu605被配置用于执行体现在软件应用或模块中的机器可读指令。指令可以存储在存储器位置如存储器610中。存储器610可以包括多种组件(例如,机器可读介质),包括但不限于随机存取存储器组件(例如,ram)(例如,静态ram“sram”、动态ram“dram等”)或只读组件(例如,rom)。存储器110还可以包括基本输入/输出系统(bios),该基本输入/输出系统包括诸如在设备启动期间帮助在数字处理设备内的元件之间传递信息的可以存储在存储器610中的基本例程。
存储单元615可以被配置用于存储文件。存储单元615还可以用于存储操作系统、应用程序等。任选地,存储单元615可以(例如,经由外部端口连接器(未示出))和/或经由存储单元接口与数字处理设备可移除地接口。软件可以全部或部分地驻留在存储单元615之内或之外的计算机可读存储介质中。在另一实例中,软件可以全部或部分地驻留在处理器605中。
可以通过显示器635向用户显示信息和数据。显示器经由接口640连接到总线625,并且可以经由接口640控制设备601的显示器与其他元件之间的数据传输。
如本文所述的方法可以通过机器(例如,计算机处理器)可执行代码的方式来实现,该机器可执行代码存储在数字处理设备601的电子存储位置上,例如存储器610或电子存储单元615上。机器可执行代码或机器可读代码可以以软件应用或软件模块的形式提供。在使用期间,代码可以由处理器605执行。在一些情况下,可以从存储单元615检索该代码并将其存储于存储器610上以备由处理器605存取。在一些情况下,可以排除电子存储单元615,而将机器可执行指令存储于存储器610上。
在一些实施方案中,远程设备602被配置用于与数字处理设备601通信,并且可以包括任何移动计算设备,其非限制性示例包括平板计算机、膝上型计算机、智能电话或智能手表。
提供以下实施例以进一步说明本发明的实施方案,但并不意图限制本发明的范围。尽管它们是可能使用的典型实施例,但也可以备选地使用本领域技术人员已知的其他程序、方法或技术。
实施例1
评估体味的微生物组特征
一般描述
皮肤拭子收集自从以下两个个体队列:腋下体味高和低。从腋下、腋下毛囊和颈后收集来自每个个体的样品。通过本文所述的微生物组谱分析工作流程处理拭子。
涵盖的概念
对于腋下,表皮微生物组可以以非常显著的一致性反映出与毛囊相关的更深层的真皮微生物组。
腋下的微生物组组成极大地影响腋下体味状态。
低气味个体中葡萄球菌属的种较丰富,而高气味个体中棒杆菌和丙酸杆菌属的种较常见。
比较高气味和低气味个体的功能谱,以下这些功能类别在高气味个体中更活跃:次生代谢物的生物合成;转运和分解代谢;以及膜转运调节。
不同的痤疮丙酸杆菌菌株在高体味和低体味个体中具有不同的丰度。
可以使用机器学习来建立预测性表征模型,以基于微生物组组成将个体分类为高体味或低体味。
结果
平均组成(微生物组)
比较了三个部位的平均微生物组成。
对于颈后,优势细菌是痤疮丙酸杆菌。
对于腋下和毛囊,葡萄球菌属的种是最普遍的细菌。
腋下和毛囊的平均谱显示出显著的相似性(见图7)。图7表现出收集自腋下(“表皮”)的皮肤拭子中的微生物组组成与收集自腋下毛囊(“毛囊”)的皮肤拭子中的微生物组组成之间的相关性。每个黑点对应于腋下表皮微生物组(x轴)和腋下毛囊(y轴)中突出细菌的盛行性。点示出拔下的毛相对于腋下的最突出细菌的平均频率。
这种相似性证明,对于腋下、表皮微生物组可以很好地反映与毛囊相关的更深层的真皮微生物组。
图8描绘了从收集自颈后的皮肤拭子获得的样品中的平均微生物组成的示例性说明。
图9描绘了从收集自受试者腋下区域的皮肤拭子获得的样品中的平均微生物组成的示例性说明。
图10描绘了从收集自受试者腋下毛囊的皮肤拭子获得的样品中的平均微生物组成的示例性说明。
差异组成
腋下的差异组成
在高气味和低气味个体之间比较腋下样品的微生物组组成。使用welch’st检验和sotry’sfdr校正方法进行了两组分析。效应过滤量设置为=0.2。
低气味个体中葡萄球菌属的种较丰富,而高气味个体中棒杆菌和丙酸杆菌属的种较常见。
结果示于图11中。图11示出了高气味和低气味受试者的腋下皮肤拭子中微生物组物种丰度的差异。
接下来将进行物种水平分析以评价差异。
功能推论
功能预测,腋下
使用welch’st检验和sotry’sfdr校正方法进行了两组分析。效应过滤量设置为=0.2。
比较高气味和低气味个体的功能谱,以下这些功能类别在高气味个体中更活跃:次生代谢物的生物合成;转运和分解代谢;以及膜转运调节。
在高气味个体中更高活性的转运和分解代谢以及膜转运调节是有道理的,因为据信气味是由于汗液组分通过细菌分解而引起的,而这需要激活的膜活性。
次要代谢物如二乙酰基2,3-丁二酮、异戊酸和丙酸也通常与体味相关。
结果示于图12中。图12将微生物组组成分类为功能类别,并且示,“其他次级代谢物的生物合成”;“转运和分解代谢”;以及“膜转运调节”是在具有高体味的个体的腋下区域中升高的三类。
功能预测,腋下,通路水平
使用welch’st检验和sotry’sfdr校正方法进行了两组分析。效应过滤量设置为=0.2。
卟啉代谢在高气味个体中更活跃。卟啉可以通过其细胞毒性作用和通过刺激角质形成细胞衍生的il-8的表达来促进毛囊周炎性反应。
基于对tca循环的比较分析,高气味个体中的细菌似乎具有更高的代谢活性。
值得注意的是,由于丁酸盐具有强烈的气味,因此高气味个体中丁酸酯的代谢较高。
结果示于图13中。图13扩展了图9中进行的表征,并将微生物组组成分解为通路。图10中的结果示出,在高气味个体的腋下区域中,卟啉代谢、tca循环和丁酸酯代谢更活跃。
痤疮丙酸杆菌分型
拔下的毛中的痤疮丙酸杆菌slst差异映射示于图14中。图14描绘了单基因座单性状(slst)差异映射,并且基于腋下毛囊的微生物组组成分析,示出了在高气味和低气味受试者中各种痤疮丙酸杆菌类型的盛行性。
痤疮丙酸杆菌f1和c1几乎仅在低体味个体中发现,而f5主要在高体味个体中发现。
腋下的痤疮丙酸杆菌slst差异映射示于图15中。图15示出了单基因座单性状(slst)差异映射,并且基于腋下的微生物组组成分析,示出了在高气味和低气味受试者中各种痤疮丙酸杆菌类型的盛行性。
在腋下,a6和b1在高体味个体中较为丰富,而f1则相反。
体味模型
数据被用来建立可以预测个体的体味是高还是低的模型。
表征模型使用气味状态低或高的样品,并将其与otu丰度相关联。创建的模型将预测测试组的气味状态并将其分类为“高”或“低”。
如图16所示,该模型的精度为55/60=0.92。图16示出,该模型准确地预测了实际上是高气味个体的15个高气味个体,并且准确地预测了实际上是低气味个体的40个低气味个体。
图17示出了不同的操作分类单位(otu)对模型的预测能力的贡献。
尽管已经参考以上实施例描述了本发明,但是应理解,在本发明的精神和范围内包括修改和变化。
- 还没有人留言评论。精彩留言会获得点赞!