纤连蛋白结合结构域嵌合抗原受体及其使用方法与流程
相关申请
本申请要求2017年6月16日提交的美国临时专利申请序列号62/521,095的优先权,其内容通过引用并入本文。
背景技术:
基于支架的结合蛋白在其结合特定配体靶标的能力方面是抗体的合法替代品。基于支架的结合蛋白包括衍生自完整的人类纤连蛋白iii型(fn3)结构域的那些。fn3结构域首先被识别为是纤连蛋白蛋白中的重复结构域之一。fn3结构域构成小的(~94个氨基酸)单体β三明治蛋白,其由具有三个连接环的7条β链组成。fn3的n端附近的三个环在功能上类似于免疫球蛋白结构域的互补决定区。衍生自完整人fn3结构域的基于支架的结合蛋白质是小的(常规单克隆抗体的1/15的大小),具有高稳定性,并具有对靶抗原的高亲和力和选择性。参见例如cappuccilli等(美国专利号8,680,019)。
嵌合抗原受体(car)已被广泛研究用于治疗多种癌症。使用表达car的细胞(例如car-t细胞)的免疫疗法是非常有前途的治疗方法,具有根除肿瘤细胞的潜力。尽管在特定的实施方式中细胞疗法是用于癌症,包括涉及实体瘤和血液恶性肿瘤的癌症,但是这样的疗法可以适用于任何医学状况。当前的car分子是基于scfv的使用,scfv是具有免疫原性问题的大蛋白。另外,由于scfv结构的不稳定性和灵活性,vh/vl结构域通过框架区域相互作用而交换和多聚体形成的可能性,不正确的折叠问题,和由聚集引起的问题,scfv的使用与异常信号传导相关。这样,当前的car-t策略受到诸如严重患者副作用和响应持久性不良的困扰。例如,使用基于car的免疫疗法的某些临床试验的失败已被归因于scfv免疫原性,参见,例如,turtle等,j.clin.invest.(2016)126(6):2134-2138。
因此,仍然需要具有高稳定性,亲和力,和选择性的通用型car分子,和有效、稳健且毒性较低的car-t癌症疗法,导致更低的患者副作用和更高的响应持久性。
技术实现要素:
在本发明的一个方面,提供了一种用于与靶抗原结合的嵌合抗原受体(car),其包含:i)包含纤连蛋白3型(fn3)结构域多肽的至少一个抗原特异性靶向区;和ii)跨膜结构域;iii)胞内信号传导结构域。
在某些示例性实施方式中,所述fn3结构域多肽包含:a)具有选定的天然纤连蛋白3型多肽的野生型氨基酸序列的区域a,ab,b,c,cd,d,e,ef,f和g,和b)具有选定的氨基酸长度的环区域bc,de和fg。
在某些示例性实施方式中,bc环的长度为11、14或15个氨基酸。
在某些示例性实施方式中,de环的长度为6个氨基酸。
在某些示例性实施方式中,fg环的长度为8或11个氨基酸。
在某些示例性实施方式中,所述fn3结构域多肽包含人纤连蛋白的第14纤连蛋白3型模块。
在某些示例性实施方式中,所述fn3结构域多肽包含人纤连蛋白的第10纤连蛋白3型模块。
在某些示例性实施方式中,所述car进一步包含胞外间隔结构域。
在某些示例性实施方式中,所述胞外间隔结构域选自抗体的fc片段,抗体的铰链区,抗体的ch2区,抗体的ch3区,人工间隔序列,包含cd8的氨基酸序列的铰链,及其任何组合。
在某些示例性实施方式中,所述至少一个抗原特异性靶向区演化自野生型抗原特异性靶向区,并且具有以下中的至少一者:a)与所述野生型抗原特异性靶向区相比,在正常生理条件下在测定中与所述靶抗原结合的活性降低;和b)与所述野生型抗原特异性靶向区相比,在异常生理条件下在测定中与所述靶抗原结合的活性增加。
在某些示例性实施方式中,与所述野生型抗原特异性靶向区相比,所述至少一个抗原特异性靶向区在正常生理条件下在测定中与所述靶抗原结合的活性降低。
在某些示例性实施方式中,与所述野生型抗原特异性靶向区相比,所述至少一个抗原特异性靶向区在异常生理条件下在测定中与所述靶抗原结合的活性增加。
在某些示例性实施方式中,所述至少一个抗原特异性靶向区具有以下两者:a)与所述野生型抗原特异性靶向区相比,在正常生理条件下在测定中与所述靶抗原结合的活性降低,和b)与所述野生型抗原特异性靶向区相比,在异常生理条件下在测定中与所述靶抗原结合的活性增加。
在某些示例性实施方式中,与包含所述野生型抗原特异性靶向区的相同嵌合抗原受体相比,所述嵌合抗原受体的表达水平增加。
在某些示例性实施方式中,与在正常生理条件下相比,所述胞外间隔结构域在异常生理条件下具有增强的泛素化抗性水平。
在某些示例性实施方式中,所述生理条件选自:温度;ph;渗透压;渗透度(osmolality);氧化应激;电解质浓度;葡萄糖、乳酸、丙酮酸盐、营养组分、代谢物、氧、碳酸盐、磷酸盐、或二氧化碳的浓度;细胞类型;和营养可得性。
在某些示例性实施方式中,所述生理条件是温度,并且其中所述抗原特异性靶向区在正常生理温度下基本上无活性,并且在低于所述正常生理温度的异常生理温度下有活性。
在某些示例性实施方式中,所述跨膜结构域选自人工疏水序列和以下中的跨膜结构域:i型跨膜蛋白,t细胞受体的α、β或ζ链,cd28,cd3ε,cd45,cd4,cd5,cd8,cd9,cd16,cd22,cd33,cd37,cd64,cd80,cd86,cd134,cd137和cd154。
在某些示例性实施方式中,所述car进一步包含至少一个共刺激结构域。
在某些示例性实施方式中,所述至少一个共刺激结构域选自以下中的共刺激结构域:tnfr超家族中的蛋白,cd28,4-1bb(cd137),ox40(cd134),pd-1,cd7,light,cd83l,dap10,dap12,cd27,cd2,cd5,icam-1,lfa-1,lck,tnfr-i,tnfr-ii,fas,cd30,cd40,icos,nkg2c和b7-h3。
在某些示例性实施方式中,所述胞内信号传导结构域选自以下中的胞质信号传导结构域:人cd3ζ链,fcγriii,fcsri,fc受体的细胞质尾,具有基于免疫受体酪氨酸的激活基序(itam)的胞质受体,tcrζ,fcrγ,fcrβ,cd3γ,cd3δ,cd3ε,cd5,cd22,cd79a,cd79b,和cd66d。
在某些示例性实施方式中,所述至少一个抗原特异性靶向区结合选自以下的靶抗原:agr2,aig1,akap1,akap2,angpt1,angpt2,angptl3,angptl4,anpep,apc,apoc1,ar,azgp1(锌-α-糖蛋白),bad,bag1,bai1,bcl2,bmp6,bpag1,brc1a,brca1,cant1,cav1,ccl11,ccl2,ccna1,ccna2,ccnd1,ccne1,ccne2,cd138,cd164,cd19,cd20,cd22,cd3,cd4,cd44,cd52,cd8,cdh1(e-钙黏蛋白),cdh10,cdh12,cdh13,cdh18,cdh19,cdh20,cdh5,cdh7,cdh8,cdh9,cdk2,cdk3,cdk4,cdk5,cdk6,cdk7,cdk9,cdkn1a(p21wap1/cip1),cdkn1b(p27kip1),cdkn1c,cdkn2a(p16ink4a),cdkn2b,cdkn2c,cdkn3,cea,chga,chgb,cldn3,cldn7(claudin-7),cln3,clu(簇集素),col18a1,col1a1,col4a3,col6a1,ctnnb1(β-连环蛋白),ctsb(组织蛋白酶),cxcl1,cxcl10,cxcl3,cxcl5,cxcl6,cxcl9,cyb5,cyc1,dap2ip,des,dncl1,e2f1,ecgf1,edg1,efna1,efna3,efnb2,egf,egfr,egfrviii,elac2,eng,eno1,eno2,eno3,ephb4,erbb2(her-2),ereg,erk8,esr1,esr2,f3(tf),fap,fasn,fgf1,fgf10,fgf11,fgf12,fgf13,fgf14,fgf16,fgf17,fgf18,fgf19,fgf2,fgf20,fgf21,fgf22,fgf23,fgf3,fgf4,fgf5,fgf6,fgf7,fgf8,fgf9,fgfr3,figf,flj12584,flj25530,flrt1(纤连蛋白),flt1,fosl1(fra-1),gabrp(gaba-a),gageb1,gagec1,gata3,gd2,ggt1,gnas1,gnrh1,gpc3,grp,gsn(凝溶胶蛋白),gstp1,hgf,hgfr(met),hip1,humcyt2a,id2,ifna1,ifnb1,ifng,igf1,igf1r,igf2,igfbp2,igfbp3,igfbp6,igκ轻链,il12a,il13ra2,il1a,il1b,il2,il24,il29,il2ra,il3ra(cd123),il6,il6r,il6st(糖蛋白130),il8,ilk,inha,insl3,insl4,itga1,itga6(α6整联蛋白),itgav,itgb3,itgb4(β4整联蛋白),jag1,jun,k6hf,kaii,kdr,klf5(gcboxbp),klk10,klk12,klk13,klk14,klk15,klk3,klk4,klk5,klk6,klk9,krt1,krt19,krt2a,krthb6(毛发特异性ii型角蛋白),lama5,lewis-y,macmarcks,map2k7(c-jun),mdk,mib1,mki67(ki-67),mmp2,mmp9,msln(间皮素),msmb,mt3(金属硫蛋白-3),mtss1,muc1(黏蛋白),muc16,myc,ngfb(ngf),ngfr,nkg2d配体,nme1(nm23a),nox5,nr0b1,nr0b2,nr1d1,nr1d2,nr1h2,nr1h3,nr1h4,nr1i2,nr1i3,nr2c1,nr2c2,nr2e1,nr2e3,nr2f1,nr2f2,nr2f6,nr3c1,nr3c2,nr4a1,nr4a2,nr4a3,nr5a1,nr5a2,nr6a1,nrp1,nrp2,ntn4,odz1,p1as2,p1k3cg,pap,part1,pate,pawr,pca3,pcna,pdgfa,pecam1,pf4,pgf,pgr,plau(upa),网蛋白,plg,plxdc1,ppid,pr1,prkcq,prkd1,prl,prok2,psap,psca,psma,pten,ptgs2(cox-2),rac2(p21-rac2),rarb,robo2,ror-1,s100a2,scgb1d2(亲脂素b),scgb2a1(乳腺珠蛋白-2),scgb2a2(乳腺珠蛋白-1),serpina3,serpinb5(乳腺丝抑蛋白(maspin)),serpine1(pai-1),serpinf1,shbg,shbq,slc2a2,slc33a1,slc43a1,sprr1b(spr1),stab1,steap,steap2,tek,tgfa,tgfb1,tgfb111,tgfb1i1,tgfb2,tgfb3,tgfbr1,tgra,thbs1(血小板反应蛋白-1),thbs2,thbs4,tie(tie-1),timp3,tnf,tnfaip2(b94),tnfrsf6(fas),tnfrsf7(bcma),tnfrsf8(cd30),tnfsf10,tnfsf6(fasl),top2a(拓扑异构酶-2α),tp53,tpm1,tpm2,trpc6,vegf,vegfc,及其任何组合。
在某些示例性实施方式中,所述至少一个抗原特异性靶向区结合选自以下的靶抗原:cd19,cd20,cd22,igκ轻链,tnfrsf8(cd30),cd138,tnfrsf7(bcma),cd33,il3ra(cd123),nkg2d配体,ror1,egfr,egfrviii,gd2,il13ra2,erbb2(her-2),msln(间皮素),psma,fap,gpc3,hgfr(met),muc16,cea,lewis-y,muc1及其任何组合。
在本发明的另一方面,提供了一种用于与靶抗原结合的多特异性嵌合抗原受体(car),其包含:i)至少两个抗原特异性靶向区,其中所述抗原特异性靶向区中的一个或多个包括fn3结构域多肽;ii)跨膜结构域;和iii)胞内信号传导结构域。
在某些示例性实施方式中,每个fn3结构域多肽包含:a)具有选定的天然纤连蛋白3型多肽的野生型氨基酸序列的区域a,ab,b,c,cd,d,e,ef,f和g,和b)具有选定的氨基酸长度的环区域bc,de和fg。
在某些示例性实施方式中,每个fn3结构域多肽的bc环的长度为11、14或15个氨基酸。
在某些示例性实施方式中,每个fn3结构域多肽的de环的长度为6个氨基酸。
在某些示例性实施方式中,每个fn3结构域多肽的fg环的长度为8或11个氨基酸。
在某些示例性实施方式中,所述fn3结构域多肽包含人纤连蛋白的第14纤连蛋白3型模块。
在某些示例性实施方式中,所述fn3结构域多肽包含人纤连蛋白的第10纤连蛋白3型模块。
在某些示例性实施方式中,所述多特异性car进一步包含胞外间隔结构域。
在某些示例性实施方式中,与在正常生理条件下相比,所述胞外间隔结构域在异常生理条件下具有增强的泛素化抗性水平。
在某些示例性实施方式中,所述至少两个抗原特异性靶向区通过接头连接。
在某些示例性实施方式中,所述接头是条件性接头,所述条件性接头在异常生理条件下具有第一构象用于所述至少两个抗原特异性靶向区以比所述条件性接头在正常生理条件下的第二构象的结合活性更高的结合活性结合所述靶抗原。
在某些示例性实施方式中,所述至少两个抗原特异性靶向区中的至少一个演化自野生型抗原特异性靶向区,并且具有以下中的至少一者:a)与所述野生型抗原特异性靶向区相比,在正常生理条件下在测定中与所述靶抗原结合的活性降低;和b)与所述野生型抗原特异性靶向区相比,在异常生理条件下在测定中与所述靶抗原结合的活性增加。
在某些示例性实施方式中,与所述野生型抗原特异性靶向区相比,所述至少两个抗原特异性靶向区中的至少一个在正常生理条件下在测定中与所述靶抗原结合的活性降低。
在某些示例性实施方式中,与所述野生型抗原特异性靶向区相比,所述至少两个抗原特异性靶向区中的至少一个在异常生理条件下在测定中与所述靶抗原结合的活性增加。
在某些示例性实施方式中,所述至少两个抗原特异性靶向区中的至少一个具有以下两者:a)与所述野生型抗原特异性靶向区相比,在正常生理条件下在测定中与所述靶抗原结合的活性降低,和b)与所述野生型抗原特异性靶向区相比,在异常生理条件下在测定中与所述靶抗原结合的活性增加。
在某些示例性实施方式中,与包含所述野生型抗原特异性靶向区的相同嵌合抗原受体相比,所述嵌合抗原受体的表达水平增加。
在某些示例性实施方式中,所述生理条件选自:温度;ph;渗透压;渗透度;氧化应激;电解质浓度;葡萄糖、乳酸、丙酮酸盐、营养组分、代谢物、氧、碳酸盐、磷酸盐、或二氧化碳的浓度;细胞类型;和营养可得性。
在某些示例性实施方式中,所述生理条件是温度,并且其中所述抗原特异性靶向区在正常生理温度下基本上无活性,并且在低于所述正常生理温度的异常生理温度下有活性。
在某些示例性实施方式中,所述胞内信号传导结构域选自以下中的胞质信号传导结构域:人cd3ζ链,fcγriii,fcsri,fc受体的细胞质尾,具有基于免疫受体酪氨酸的激活基序(itam)的胞质受体,tcrζ,fcrγ,fcrβ,cd3γ,cd3δ,cd3ε,cd5,cd22,cd79a,cd79b,和cd66d。
在某些示例性实施方式中,所述至少一个抗原特异性靶向区结合选自以下的靶抗原:agr2,aig1,akap1,akap2,angpt1,angpt2,angptl3,angptl4,anpep,apc,apoc1,ar,azgp1(锌-α-糖蛋白),bad,bag1,bai1,bcl2,bmp6,bpag1,brc1a,brca1,cant1,cav1,ccl11,ccl2,ccna1,ccna2,ccnd1,ccne1,ccne2,cd138,cd164,cd19,cd20,cd22,cd3,cd4,cd44,cd52,cd8,cdh1(e-钙黏蛋白),cdh10,cdh12,cdh13,cdh18,cdh19,cdh20,cdh5,cdh7,cdh8,cdh9,cdk2,cdk3,cdk4,cdk5,cdk6,cdk7,cdk9,cdkn1a(p21wap1/cip1),cdkn1b(p27kip1),cdkn1c,cdkn2a(p16ink4a),cdkn2b,cdkn2c,cdkn3,cea,chga,chgb,cldn3,cldn7(claudin-7),cln3,clu(簇集素),col18a1,col1a1,col4a3,col6a1,ctnnb1(β-连环蛋白),ctsb(组织蛋白酶),cxcl1,cxcl10,cxcl3,cxcl5,cxcl6,cxcl9,cyb5,cyc1,dap2ip,des,dncl1,e2f1,ecgf1,edg1,efna1,efna3,efnb2,egf,egfr,egfrviii,elac2,eng,eno1,eno2,eno3,ephb4,erbb2(her-2),ereg,erk8,esr1,esr2,f3(tf),fap,fasn,fgf1,fgf10,fgf11,fgf12,fgf13,fgf14,fgf16,fgf17,fgf18,fgf19,fgf2,fgf20,fgf21,fgf22,fgf23,fgf3,fgf4,fgf5,fgf6,fgf7,fgf8,fgf9,fgfr3,figf,flj12584,flj25530,flrt1(纤连蛋白),flt1,fosl1(fra-1),gabrp(gaba-a),gageb1,gagec1,gata3,gd2,ggt1,gnas1,gnrh1,gpc3,grp,gsn(凝溶胶蛋白),gstp1,hgf,hgfr(met),hip1,humcyt2a,id2,ifna1,ifnb1,ifng,igf1,igf1r,igf2,igfbp2,igfbp3,igfbp6,igκ轻链,il12a,il13ra2,il1a,il1b,il2,il24,il29,il2ra,il3ra(cd123),il6,il6r,il6st(糖蛋白130),il8,ilk,inha,insl3,insl4,itga1,itga6(α6整联蛋白),itgav,itgb3,itgb4(β4整联蛋白),jag1,jun,k6hf,kaii,kdr,klf5(gcboxbp),klk10,klk12,klk13,klk14,klk15,klk3,klk4,klk5,klk6,klk9,krt1,krt19,krt2a,krthb6(毛发特异性ii型角蛋白),lama5,lewis-y,macmarcks,map2k7(c-jun),mdk,mib1,mki67(ki-67),mmp2,mmp9,msln(间皮素),msmb,mt3(金属硫蛋白-3),mtss1,muc1(黏蛋白),muc16,myc,ngfb(ngf),ngfr,nkg2d配体,nme1(nm23a),nox5,nr0b1,nr0b2,nr1d1,nr1d2,nr1h2,nr1h3,nr1h4,nr1i2,nr1i3,nr2c1,nr2c2,nr2e1,nr2e3,nr2f1,nr2f2,nr2f6,nr3c1,nr3c2,nr4a1,nr4a2,nr4a3,nr5a1,nr5a2,nr6a1,nrp1,nrp2,ntn4,odz1,p1as2,p1k3cg,pap,part1,pate,pawr,pca3,pcna,pdgfa,pecam1,pf4,pgf,pgr,plau(upa),网蛋白,plg,plxdc1,ppid,pr1,prkcq,prkd1,prl,prok2,psap,psca,psma,pten,ptgs2(cox-2),rac2(p21-rac2),rarb,robo2,ror-1,s100a2,scgb1d2(亲脂素b),scgb2a1(乳腺珠蛋白-2),scgb2a2(乳腺珠蛋白-1),serpina3,serpinb5(乳腺丝抑蛋白),serpine1(pai-1),serpinf1,shbg,shbq,slc2a2,slc33a1,slc43a1,sprr1b(spr1),stab1,steap,steap2,tek,tgfa,tgfb1,tgfb111,tgfb1i1,tgfb2,tgfb3,tgfbr1,tgra,thbs1(血小板反应蛋白-1),thbs2,thbs4,tie(tie-1),timp3,tnf,tnfaip2(b94),tnfrsf6(fas),tnfrsf7(bcma),tnfrsf8(cd30),tnfsf10,tnfsf6(fasl),top2a(拓扑异构酶-2α),tp53,tpm1,tpm2,trpc6,vegf,vegfc,及其任何组合。
在某些示例性实施方式中,所述一种或多种抗原是不同的。
在某些示例性实施方式中,所述一种或多种抗原在同一细胞上。
在某些示例性实施方式中,所述一种或多种抗原在至少两个细胞上。
在某些示例性实施方式中,所述至少两个细胞各自具有相同的细胞类型。
在某些示例性实施方式中,所述至少两个细胞各自具有不同的细胞类型。
在某些示例性实施方式中,所述细胞类型选自细胞毒性细胞和癌细胞。
在某些示例性实施方式中,所述细胞毒性细胞是选自幼稚t细胞,中央记忆t细胞和效应记忆t细胞的t细胞。
在某些示例性实施方式中,所述细胞毒性细胞选自自然杀伤(nk)细胞,激活的nk细胞,嗜中性粒细胞,嗜酸性粒细胞,嗜碱性粒细胞,b细胞,巨噬细胞和淋巴因子激活杀伤细胞。
在某些示例性实施方式中,所述至少两个细胞之一是癌细胞。
在另一个方面,提供了一种核酸序列,其编码本公开的car或多特异性car。
在某些示例性实施方式中,表达载体包含所述核酸序列。
在某些示例性实施方式中,所述表达载体进一步包含编码可操作地连接至t细胞激活响应性启动子的细胞因子的核酸序列。
在某些示例性实施方式中,所述细胞因子是il-12。
在某些示例性实施方式中,所述表达载体选自慢病毒载体,γ逆转录病毒载体,泡沫病毒载体,腺相关病毒载体,腺病毒载体,痘病毒载体,疱疹病毒载体,工程化杂交病毒载体,和转座子介导载体。
在另一方面,提供了一种产生工程化细胞的方法,所述方法包括将本公开的表达载体引入细胞中以产生所述工程化细胞。
在另一方面,提供了一种工程化细胞,其包含本公开的核酸序列,或本公开的表达载体。
在某些示例性实施方式中,所述细胞是t细胞。
在某些示例性实施方式中,所述t细胞选自幼稚t细胞,中央记忆t细胞和效应记忆t细胞。
在某些示例性实施方式中,所述细胞选自自然杀伤(nk)细胞,激活的nk细胞,嗜中性粒细胞,嗜酸性粒细胞,嗜碱性粒细胞,b细胞,巨噬细胞,和淋巴因子激活杀伤细胞。
在某些示例性实施方式中,所述核酸序列被整合到所述细胞的基因组中。
在某些示例性实施方式中,所述工程化细胞产生用于治疗用途的足够量的car或多特异性car。
在另一方面,提供了一种药物组合物,其包含:i)本公开的一种或多种car或多特异性car,本公开的表达载体,或本公开的工程化细胞;和ii)药学上可接受的载体或赋形剂。
在另一方面,提供了一种在有需要的受试者中治疗癌症的方法,所述方法包括:i)将本公开的car或多特异性car,或本公开的表达载体,引入从所述受试者获得的细胞中以产生工程化细胞;和ii)向所述受试者施用所述工程化细胞,从而治疗所述癌症。
在某些示例性实施方式中,所述表达载体选自慢病毒载体,γ逆转录病毒载体,泡沫病毒载体,腺相关病毒载体,腺病毒载体,痘病毒载体,疱疹病毒载体,工程化杂交病毒载体,和转座子介导载体。
在某些示例性实施方式中,所述细胞是选自幼稚t细胞,中央记忆t细胞和效应记忆t细胞的t细胞。
在某些示例性实施方式中,所述细胞选自自然杀伤(nk)细胞,激活的nk细胞,嗜中性粒细胞,嗜酸性粒细胞,嗜碱性粒细胞,b细胞,巨噬细胞,和淋巴因子激活杀伤细胞。
在某些示例性实施方式中,所述核酸序列被整合到所述细胞的基因组中。
在某些示例性实施方式中,所述工程化细胞产生用于治疗用途的足够量的car或多特异性car。
在某些示例性实施方式中,所述癌症是实体瘤或血液肿瘤。
在某些示例性实施方式中,所述实体瘤选自纤维肉瘤,粘液肉瘤,脂肪肉瘤,软骨肉瘤,骨肉瘤,和其它肉瘤,滑膜瘤,间皮瘤,尤因氏瘤,平滑肌肉瘤,横纹肌肉瘤,结肠癌,淋巴恶性肿瘤,胰腺癌,乳腺癌,肺癌,卵巢癌,前列腺癌,肝细胞癌,鳞状细胞癌,基底细胞癌,腺癌,汗腺癌,甲状腺髓样癌,甲状腺乳头状癌,嗜铬细胞瘤、皮脂腺癌,乳头状癌,乳头状腺癌,髓样癌,支气管癌,肾细胞癌,肝癌,胆管癌,绒毛膜癌,威尔姆斯氏肿瘤,宫颈癌,睾丸肿瘤,精原细胞瘤,膀胱癌,黑素瘤,神经胶质瘤,成胶质细胞瘤,星形细胞瘤,cns淋巴瘤,生殖细胞瘤,髓母细胞瘤,神经鞘瘤,颅咽管瘤,室管膜瘤,松果体瘤,血管母细胞瘤,听神经瘤,少突神经胶质瘤,脑膜瘤,神经母细胞瘤,视网膜母细胞瘤,和脑转移瘤。
在某些示例性实施方式中,所述血液肿瘤选自白血病,真性红细胞增多症,淋巴瘤,霍奇金淋巴瘤,非霍奇金淋巴瘤,多发性骨髓瘤,华氏巨球蛋白血症,重链疾病相关肿瘤,骨髓增生异常综合症(myelodysplasticsyndrome)相关肿瘤,毛细胞白血病和骨髓增生异常。
在另一方面,提供了一种t细胞激活性双特异性抗原结合分子,其包含与单链fv(scfv)融合的含有fn3结构域的多肽,其中fn3结构域多肽能够特异性结合靶抗原,并且所述scfv能够特异性结合激活性t细胞抗原。
在某些示例性实施方式中,所述含有fn3结构域的多肽包含fn3结构域,所述fn3结构域包含:
a)具有选定的天然纤连蛋白3型多肽的野生型氨基酸序列的区域a,ab,b,c,cd,d,e,ef,f和g,和
b)具有选定的氨基酸长度的环区域bc,de和fg。
在某些示例性实施方式中,bc环的长度为11、14或15个氨基酸。
在某些示例性实施方式中,de环的长度为6个氨基酸。
在某些示例性实施方式中,fg环的长度为8或11个氨基酸。
在某些示例性实施方式中,所述fn3结构域多肽包含人纤连蛋白的第14纤连蛋白3型模块。
在某些示例性实施方式中,所述fn3结构域多肽包含人纤连蛋白的第10纤连蛋白3型模块。
在某些示例性实施方式中,所述fc结构域是iggfc结构域,特别是igg1或igg4fc结构域。
在某些示例性实施方式中,所述fc结构域是人fc结构域。
在某些示例性实施方式中,与天然igg1fc结构域相比,所述fc结构域表现出对fc受体的结合亲和力降低和/或效应功能降低。
在某些示例性实施方式中,所述fc结构域包含减少与fc受体的结合和/或效应功能的一个或多个氨基酸置换。
在某些示例性实施方式中,存在不多于一个能够特异性结合激活性t细胞抗原的抗原结合部分。
在某些示例性实施方式中,所述含有fn3结构域的多肽包含一个或多个fn3结构域单体。
在某些示例性实施方式中,所述含有fn3结构域的多肽包含两个fn3结构域单体。
在某些示例性实施方式中,所述含有fn3结构域的多肽包含三个fn3结构域单体。
在某些示例性实施方式中,所述一个或多个fn3结构域单体各自通过接头序列连接在一起。
在某些示例性实施方式中,所述一个或多个fn3结构域单体各自能够特异性结合所述靶抗原的不同表位。
在某些示例性实施方式中,所述一个或多个fn3结构域单体各自能够特异性结合所述靶抗原的重叠表位。
在某些示例性实施方式中,所述靶抗原是axl。
在某些示例性实施方式中,所述激活性t细胞抗原是cd3。
在某些示例性实施方式中,能够结合axl的所述含有fn3结构域的多肽包含选自seqidno:33-36的氨基酸序列。
在某些示例性实施方式中,所述结合分子包含选自seqidno:37-39的氨基酸序列。
在某些示例性实施方式中,提供了一种核酸序列,其编码上述方面中任一项所述的t细胞激活性双特异性抗原结合分子。
在某些示例性实施方式中,提供了一种表达载体,其包含上述方面中任一项所述的核酸序列。
在某些示例性实施方式中,提供了一种宿主细胞,其包含上述方面中任一项所述的核酸。
在另一方面,提供了一种产生上述方面中任一项所述的t细胞激活性双特异性抗原结合分子的方法,其包括以下步骤:a)在适合于表达所述t细胞激活性双特异性抗原结合分子的条件下培养上述方面中任一项的权利要求的宿主细胞;和b)回收所述t细胞激活性双特异性抗原结合分子。
在某些示例性实施方式中,提供了一种通过上述方面中任一项所述的方法产生的t细胞激活性双特异性抗原结合分子。
在某些示例性实施方式中,提供了一种药物组合物,其包含上述方面中任一项所述的t细胞激活性双特异性抗原结合分子,和药学上可接受的载体。
在某些示例性实施方式中,提供了上述方面中任一项所述的t细胞激活性双特异性抗原结合分子,或上述方面中任一项所述的药物组合物,其用作药物。
在某些示例性实施方式中,提供了上述方面中任一项所述的t细胞激活性双特异性抗原结合分子,或上述方面中任一项所述的药物组合物,其用于治疗有需要的个体的疾病。
在某些示例性实施方式中,所述疾病是癌症。
在某些示例性实施方式中,提供了一种诱导靶细胞裂解的方法,其包括在t细胞存在下使靶细胞与上述方面中任一项所述的t细胞激活性双特异性抗原结合分子或上述方面中任一项所述的药物组合物接触。
在另一方面,提供了一种t细胞激活性双特异性抗原结合分子,其包含与单链fv(scfv)融合的含有fn3结构域的多肽,其中所述含有fn3结构域的多肽能够特异性结合axl,并且所述scfv能够特异性结合cd3。
在某些示例性实施方式中,所述t细胞激活性双特异性抗原结合分子包含seqidno:37-39中任一项所述的氨基酸序列。
在另一方面,提供了一种t细胞激活性双特异性抗原结合分子,其包含与单链fv(scfv)融合的含有fn3结构域的多肽,其中所述含有fn3结构域的多肽包含各自能够特异性结合axl的fn3结构域单体的二聚体,并且其中所述scfv能够特异性结合cd3。
在某些示例性实施方式中,所述t细胞激活性双特异性抗原结合分子包含seqidno:40所述的氨基酸序列。
在另一方面,提供了一种t细胞激活性双特异性抗原结合分子,其包含与单链fv(scfv)融合的含有fn3结构域的多肽,其中所述含有fn3结构域的多肽包含各自能够特异性结合axl的fn3结构域单体的三聚体,并且其中所述scfv能够特异性结合cd3。
在某些示例性实施方式中,所述t细胞激活性双特异性抗原结合分子包含seqidno:41所述的氨基酸序列。
附图说明
通过示意性实施方式的以下详细描述结合附图,将更充分地理解本发明的前述和其他特征和优点。
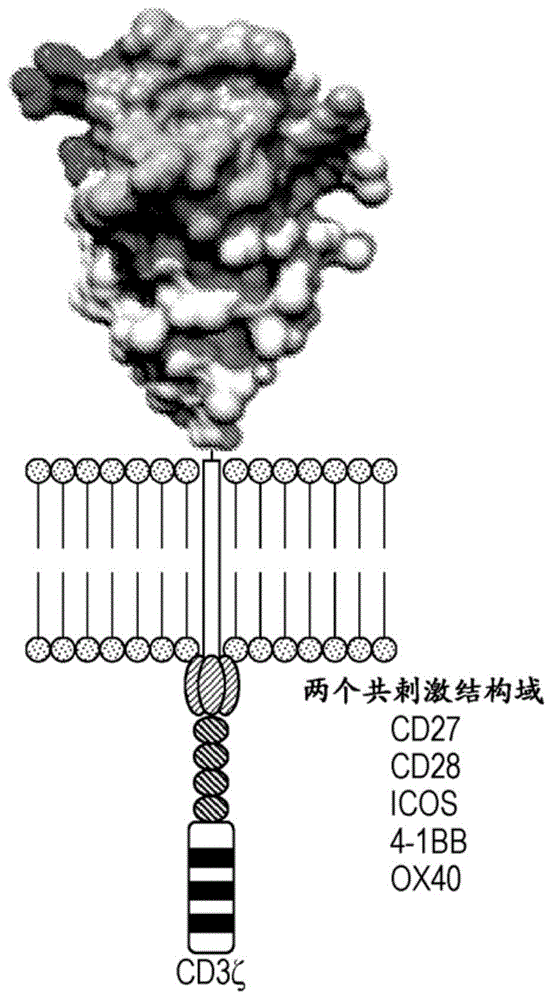
图1描绘了包含两个共刺激结构域的本公开的主题fn3car的示意图。
图2描绘了包含编码本公开的主题fn3car的序列的多核苷酸结构的示意图。
图3描绘了本公开的主题多特异性fn3car的示意图。
图4描绘了亲和力筛选的facs分析。
图5描绘了特异性筛选的facs分析。
图6描绘了通过生物层干涉术(bli)测量的对于各种axl特异性fn3结合物的结合亲和力的表。
图7a和7b描绘了特异性筛选的facs分析。
图8描绘了根据本公开的各种蛋白的考马斯染色凝胶。
图9描绘了fn3结构域-scfv融合体的facs分析。
图10a和10b分别描绘了针对fn3结构域-scfv融合体的t细胞依赖性细胞毒性(tdcc)测定杀伤曲线,和ec50值。
图11a和11b分别描绘了显示t细胞激活的facs分析,及其定量。
图12描绘了显示在tdcc测定中与axl-fc蛋白竞争测量的axl-cd3fn3结构域-scfv融合体的特异性的图。
具体实施方式
本公开提供了用于与靶抗原结合的car,其包含包含fn3结构域多肽的至少一个抗原特异性靶向区。本公开还提供了用于与两种或更多种靶抗原结合的多特异性fn3car,其包含包含fn3结构域多肽的至少一个或多个抗原特异性靶向区。本公开还提供了与本发明的主题fn3car的用途有关的组合物和治疗方法。本发明可以解决的合适疾病包括但不限于各种实体瘤和血液癌症。
本文所述的发明主要基于对改善包含单链可变片段(scfv)的当前car的局限性的需要。这样的局限性包括,例如,scfv是具有免疫原性问题的大蛋白,由于其结构的不稳定性和灵活性,当前car与强直(tunic)信号传导相关,vh/vl结构域交换以及通过框架区相互作用形成多聚体的可能性,不正确折叠的可能性,聚集的可能性,以及car-t细胞的耗竭的可能性。
应理解,本公开描述的组合物和方法不限于本文公开的特定组合物、方法或实验条件,这样,方法和条件可以变化。还应理解,本文所使用的术语仅出于描述特定实施方式的目的,而不旨在是限制性的。
此外,除非另有说明,否则本文所述的实验使用本领域技术范围内的常规分子和细胞生物学及免疫学技术。这样的技术对于技术人员是众所周知的,并且在文献中有充分的解释。参见例如ausubel,等,ed.,currentprotocolsinmolecularbiology,johnwiley&sons,inc.,ny,n.y.(1987-2008),包括所有补充,molecularcloning:alaboratorymanual(fourthedition)bymrgreenandj.sambrookandharlow等,antibodies:alaboratorymanual,chapter14,coldspringharborlaboratory,coldspringharbor(2013,2ndedition)。
本文中提及或引用的文章、专利和专利申请的内容以及所有其他文件和电子可用信息的全部内容通过引用并入本文,其程度如同具体地和单独地指出每份单独的出版物通过引用并入本文一样。申请人保留将来自任何这样的文章、专利、专利申请或其他物理和电子文档的任何和所有材料和信息以物理方式并入本申请的权利。
除非本文另外定义,否则本文所使用的科学和技术术语具有本领域普通技术人员通常理解的含义。在存在任何潜在歧义的情况下,本文提供的定义优先于任何字典或外部定义。除非上下文另有要求,否则单数形式应包括复数,复数形式应包括单数。除非另有说明,否则“或”的使用表示“和/或”。术语“包括/包含(includes)”以及其他形式(例如“包括/包含(includes)”和“包括/包含(included)”)的使用不是限制性的。
通常,与本文所述的细胞和组织培养、分子生物学、免疫学、微生物学、遗传学以及蛋白质和核酸化学结合使用的命名法是本领域众所周知的和常用的那些。除非另外指出,否则本文中提供的方法和技术通常根据本领域众所周知的常规方法进行,并且如本说明书通篇所引用和讨论的各种一般性和更具体的参考文献中所述。本文描述的与分析化学、合成有机化学以及药物和药物化学结合使用的命名法及其实验室程序和技术是本领域众所周知的和常用的那些。标准技术用于化学合成、化学分析、药物制备、制剂、递送和患者治疗。
首先定义了某些术语,使得可以更容易理解本发明。应当理解,本文使用的术语仅出于描述特定实施方式的目的,而非旨在是限制性的。
术语“氨基酸”或“氨基酸残基”通常是指具有其本领域公认的定义的氨基酸,例如选自以下的氨基酸:丙氨酸(ala,a);精氨酸(arg,r);天冬酰胺(asn,n);天冬氨酸(asp,d);半胱氨酸(cys,c);谷氨酰胺(gln,q);谷氨酸(glu,e);甘氨酸(gly,g);组氨酸(his,h);异亮氨酸(ile,i);亮氨酸(leu,l);赖氨酸(lys,k);蛋氨酸(met,m);苯丙氨酸(phe,f);脯氨酸(pro,p);丝氨酸(ser,s);苏氨酸(thr,t);色氨酸(trp,w);酪氨酸(tyr,y);和缬氨酸(val,v),尽管可以根据需要使用修饰的、合成的或稀有的氨基酸。
“化学等效氨基酸”是指具有相似的空间、电荷和溶解度特性的氨基酸。一种常见的方案通过以下方式对氨基酸进行分组:(1)具有氢侧链的甘氨酸;(2)具有氢或未取代的脂肪族侧链的丙氨酸(ala,a)、缬氨酸(val,v)、亮氨酸(leu,l)和异亮氨酸(iso,i);(3)具有带有羟基的脂肪族侧链的丝氨酸(ser,s)和苏氨酸(thr,t);(4)具有含羧基的侧链的天冬氨酸(asp,d)和谷氨酸(glu,e);(5)具有终止于酰胺基的脂肪族侧链的天冬酰胺(asn,n)和谷氨酰胺(glu,q);(6)具有终止于碱性氨基的脂肪族侧链的精氨酸(arg,r)、赖氨酸(lys,l)和组氨酸(his,h);(7)具有含硫的脂肪族侧链的半胱氨酸(cys,c)和蛋氨酸(met,m);(8)具有芳香族侧链的酪氨酸(tyr,y)和苯丙氨酸(phe,f);(9)具有杂环侧链的色氨酸(trp,w)、脯氨酸(pro,p)和组氨酸(his,h)。
术语“保守氨基酸残基”或“固定氨基酸”是指对于给定残基位置,被确定以高频率出现的氨基酸残基,所述频率通常为至少50%或更高(例如,约60%、70%、80%、90%、95%或100%)。当确定给定残基以如此高的频率(即高于约50%的阈值)发生时,可以确定其是保守的,因此在本发明的文库中表示为“固定的”或“恒定的”残基,至少是对于所分析的环区域中的氨基酸残基位置而言。
“纤连蛋白3型(fn3)蛋白”是指一组由具有由具有三个连接环的七个β链组成的纤连蛋白3型(fn3)结构或基序的单体亚基组成的蛋白质。β-链a、b和e形成r-三明治的一半,β-链c、d、f和g形成另一半,且分子量为约94个氨基酸和分子量为约10kda。fn3结构域的整体折叠与免疫球蛋白结构域的整体折叠密切相关,fn3的n端附近的三个环(称为bc、de和fg)可以分别在结构上视为类似于抗体可变重链(vh)结构域互补决定区cdr1、cdr2和cdr3。纤连蛋白本身由16个不同的模块或结构域组成。fn3蛋白的给定模块通过模块编号和蛋白名称来标识,例如,人纤连蛋白的第14fn3模块(14/fn或14/fn3),人纤连蛋白的第10fn3模块(10/fn或10/fn3),生腱蛋白(tenascin)的第1fn3模块(1/tenascin),依此类推。
“纤连蛋白3型(fn3)结构域多肽”或“fn3多肽”是指具有本文讨论的纤连蛋白3型结构域或模块的多肽,其中一个或多个模块将构成纤连蛋白型蛋白(fn3蛋白),例如构成人纤连蛋白(fn)的16个不同的fn3模块,和构成生腱蛋白的15个不同的fn3模块。个体fn3结构域多肽用模块编号和蛋白质名称来指代,例如人纤连蛋白的第10模块或第14模块(10/fn或14/fn)或生腱蛋白的第1模块(1/tenascin)。
术语“框架区”是指纤连蛋白β-链支架的本领域公认的部分,其存在于差异更大的环区域之间。这样的框架区域通常被称为β链a至g,其共同提供了支架,在那里六个限定的环可以延伸以形成一个或多个配体接触表面。在纤连蛋白中,7个β链将它们自己定向为两个β褶(pleat)以形成β三明治。框架区还可以分别在链a和b、c和d以及e和f之间包含环ab、cd和ef。
术语“环区”是指未分配给β链褶的肽序列。在纤连蛋白结合支架中,有六个环区域,已知其中三个与支架的结合结构域有关(bc、de和fg),其中三个位于多肽的相反侧(ab、ef和cd)。在本发明中,序列多样性在bc、de和fg环中的一个或多个中建立,而ab、cd和ef环通常被分配fn3多肽的野生型氨基序列,从其衍生所述多肽的其他框架区。
fn3多肽的bc、de或fg环中的“共有”氨基酸是保守氨基酸,或者半保守氨基酸中的选定一者。
术语“配体”或“抗原”是指就其基本组成而言在结构/化学上相似的化合物。典型的配体类别是蛋白质(多肽)、肽、多糖、多核苷酸和小分子。当被特异性抗体识别时,配体可以等同于“抗原”。
如本文所用,术语“抗原”或“ag”定义为引起免疫应答的分子。这种免疫应答可涉及抗体产生,或特定的有免疫学能力的细胞的激活,或两者。本领域技术人员将理解,任何大分子,包括实际上所有的蛋白质或肽,可以用作抗原。此外,抗原可以衍生自重组dna或基因组dna。本领域技术人员将理解,任何dna,包括编码引起免疫应答的蛋白质的核苷酸序列或部分核苷酸序列,因此编码如本文所用的术语“抗原”。此外,本领域技术人员将理解抗原不需要仅由基因的全长核苷酸序列编码。此外,技术人员将理解,抗原根本不需要由“基因”编码。显而易见的是,抗原可以产生、合成或可以衍生自生物样品。这样的生物样品可以包括但不限于组织样品、肿瘤样品、细胞或生物流体。
如本文所用,术语“抗体”是指完整的免疫球蛋白分子,以及能够结合抗原的表位的免疫球蛋白分子的片段。
术语“嵌合抗原受体(car)”是指包含能够结合抗原的细胞外结构域,衍生自与从其衍生细胞外结构域的多肽不同的多肽的跨膜结构域,以及至少一个细胞内结构域的蛋白。“能够结合抗原的细胞外结构域”是指可以结合某种抗原的任何寡肽或多肽。“细胞内结构域”是指已知充当传递信号以引起细胞中的生物学过程的激活或抑制的结构域的任何寡肽或多肽。
术语“条件性活性嵌合抗原受体”是指野生型蛋白的变体或突变体,其在一种或多种正常生理条件下比亲本(parent)野生型蛋白具有更多或更少的活性。该条件性活性蛋白还在身体的选择区域中表现出活性和/或在异常或允许的生理条件下表现出增加或降低的活性。
如本文所用,术语“正常生理条件”是指温度、ph、渗透压、渗透度(osmolality),氧化应激,电解质浓度,小有机分子例如葡萄糖、乳酸、丙酮酸盐、营养组分、其他代谢物等等的浓度,另一分子例如氧、碳酸盐、磷酸盐和二氧化碳的浓度,以及细胞类型和营养可得性,其在受试者的施用部位或者在作用部位的组织或器官的正常范围内考虑。
术语“约”或“大约”是指在给定值或范围的20%之内,例如10%之内,5%之内或1%内或更少。
如本文所用,“施用(administer/administration)”是指在物质存在于体外时将其注射或以其他方式物理递送至患者中的行为,例如但不限于肺、粘膜、皮内、静脉内、肌内递送和/或本文所述或本领域已知的任何其他物理递送方法。当管理或治疗疾病或其症状时,通常在疾病或其症状发作之后进行物质的施用。
如本文所用,术语“组合物”旨在涵盖含有任选地指定量的指定成分的产品,以及直接或间接地由任选地指定量的指定成分的组合产生的任何产品。
“有效量”是指足以在需要试剂的个体中实现期望生理结果的活性药剂的量。有效量可以在个体之间不同,这取决于被治疗个体的健康和身体状况,被治疗个体的分类组,组合物的制剂,对个体医疗状况的评估以及其他相关因素。
如本文所用,术语“受试者”和“患者”可互换使用。如本文所用,受试者可以是哺乳动物,例如非灵长类动物(例如,牛,猪,马,猫,狗,大鼠等)或灵长类动物(例如,猴和人)。在某些实施方式中,本文所用的术语“受试者”是指脊椎动物,例如哺乳动物。哺乳动物包括但不限于人、非人灵长类、野生动物、凶猛(feral)动物、农场动物、运动动物和宠物。在一个实施方式中,受试者是患有疾病(例如实体瘤或血液癌)的哺乳动物,例如人。
如本文所用,术语“疗法”是指可用于预防、管理、治疗和/或改善疾病或与其相关的症状的任何方案、方法和/或药剂,例如实体瘤或血液癌症。在一些实施方式中,术语“疗法”是指可用于调节对受试者中的感染或与其相关的症状的免疫应答的任何方案、方法和/或试剂。在一些实施方式中,术语“疗法”是指本领域技术人员例如医务人员已知的可用于预防、管理、治疗和/或改善疾病或与其相关的症状(例如实体瘤或血液癌症)的生物疗法、支持性疗法和/或其他疗法。在其他实施方式中,术语“疗法”是指本领域技术人员例如医务人员已知的可用于调节对受试者中的感染或与其相关的症状的免疫应答的生物疗法、支持性疗法和/或其他疗法。
如本文所用,术语“治疗”(treat/treatment/treating)是指施用一种或多种疗法(包括但不限于施用一种或多种预防剂或治疗剂,例如本文提供的组合物)引起的疾病或与其相关的症状的进展、严重程度和/或持续时间的减少或改善,例如实体瘤或血液癌症。如本文所用,术语“治疗”还可以指改变被治疗的受试者的病程。治疗的治疗性作用包括但不限于预防疾病的发生或复发,减轻症状,减轻疾病的直接或间接病理后果,降低疾病进展的速度,改善或减轻疾病状态,以及缓解或预后改善。
纤连蛋白3型结构域多肽
纤连蛋白型蛋白是指一组由具有由具有三个连接环的七个β链组成的fn3结构或基序的单体亚基组成的蛋白质。β-链a、b和e形成r-三明治的一半,β-链c、d,f和g形成另一半,且分子量为约94个氨基酸和分子量为约10kda。fn3结构域的整体折叠与免疫球蛋白结构域的整体折叠密切相关,fn3的n端附近的三个环(称为bc、de和fg)可以分别在结构上视为类似于抗体可变重链(vh)结构域互补决定区cdr1、cdr2和cdr3。
代表性的fn3蛋白包括血管生成素1受体(angiopoietin1receptor)、接触蛋白(contactinprotein)、细胞因子受体共同β链、唐氏综合症细胞粘附蛋白、纤连蛋白和其他本领域已知的。纤连蛋白本身由16个不同的模块或结构域组成。fn3蛋白的给定模块通过模块编号和蛋白名称来标识,例如,人纤连蛋白的第14fn3模块(14/fn或14/fn3)、人纤连蛋白的第10fn3模块(10/fn或10/fn3)、腱生蛋白的第1fn3模块(1/tenascin),依此类推。
纤连蛋白通过充当将细胞锚定至整联蛋白、胶原蛋白或其他蛋白聚糖底物的一般细胞粘附分子而参与许多细胞过程,包括组织修复、胚胎发生和血液凝结。此外,纤连蛋白可用于组织(organize)结合不同组分(如肝素)的细胞外基质至细胞表面上的膜结合受体。纤连蛋白的氨基酸序列揭示了被(通常)短连接序列分隔的三种类型的内部同源重复序列或模块。有12个i型模块、2个ii型模块和16个iii型模块,分别称为fni(fn1)、fnii(fn2)和fniii(fn3)。每个fn模块构成独立折叠单元,通常称为结构域。如上所述,在其他蛋白中也发现了与纤连蛋白中的那些同源的模块,特别是fn3基序,其是所有模块中的最普遍存在的之一,发现于细胞外受体激酶、磷酸酶、腱生蛋白等等。自其发现以来,该fn3结构域已在许多动物蛋白中发现,据估计在迄今测序的蛋白中占2%。在纤连蛋白本身内,有十六个具有非常相似的三级结构的fn3结构域。尽管fn3构象高度保守,但在给定的纤连蛋白中,具有相同类型的不同模块之间的相似性非常低,通常小于20%。相比之下,跨多个物种的相同fn3模块的氨基酸序列同源性明显更高,约为80%-90%。
纤连蛋白模块独立折叠,因此可以与其邻居孤立地存在。已经确定了每种类型的纤连蛋白模块的多个实例的三维结构。如从氨基酸序列和3d结构之间的众所周知的关系所预期的,相同类型的模块具有相似的折叠。所有三种类型的模块几乎排他地由反平行r片层(sheet)和转角(turn)组成,几乎没有或没有α螺旋。在fn3模块中,顶部片层包含四条反平行β链,底部片层是三链的。二硫桥并不使fn3结构稳定。相反,这仅通过模块核心中的疏水相互作用发生。
本发明提供了用于与靶抗原结合的car,其包含包含fn3结构域多肽的至少一个抗原特异性靶向区。
在一个实施方式中,如美国专利号8,680,019中所述,通过走查(walk-through)诱变产生fn3结构域多肽,该专利的全部内容通过引用并入本文。
在另一个实施方式中,fn3结构域多肽选自fn3结构域多肽的天然变体组合文库,其在美国专利号8,680,019中进一步描述。
在一些实施方式中,每个fn3结构域多肽可以对抗原具有特异性。在一些实施方式中,每个fn3结构域多肽可以对不同的抗原具有特异性。在一些实施方式中,含有fn3结构域的多肽对单个抗原具有特异性。在一些实施方式中,含有fn3结构域的多肽包含两个或更多个各自对抗原具有特异性的fn3结构域。在一些实施方式中,含有双特异性fn3结构域的多肽包含两个fn3结构域,其中第一fn3结构域对抗原具有特异性,并且其中第二fn3结构域对不同抗原具有特异性。在一些实施方式中,含有多特异性fn3结构域的多肽包含两个或更多个fn3结构域,其中第一fn3结构域对抗原具有特异性,其中第二fn3结构域对不同抗原具有特异性,并且其中后续fn3结构域对后续抗原具有特异性。
在一些实施方式中,一个或多个fn3结构域多肽可对抗原具有重叠的特异性。例如,含有fn3结构域的多肽可以包含fn3结构域的二聚体,其各自结合相同的抗原(例如,相同抗原的不同表位)。在一些实施方式中,含有fn3结构域的多肽可以包含fn3结构域的三聚体,其各自结合相同的抗原(例如,相同抗原的不同表位)。
在一些实施方式中,含fn3结构域的多肽可以进一步包含单链可变片段(scfv),在本文中称为fn3结构域-scfv融合体。如本文所用,“fn3结构域-scfv融合体”是指包含对抗原具有特异性的fn3结构域多肽和对抗原具有特异性的scfv的多肽。在一些实施方式中,本公开的fn3结构域-scfv融合体包含对一种或多种靶抗原具有特异性的一个或多个fn3结构域,以及对一种或多种靶抗原具有特异性的一个或多个scfv。例如,axl-cd3fn3结构域-scfv融合体包含对酪氨酸-蛋白激酶axl具有特异性的一个或多个fn3结构域,并且包含对细胞表面cd3蛋白具有特异性的一个或多个scfv。在这样的实施方式中,axl-cd3fn3结构域-scfv融合体也可以称为axl-cd3fn3结构域-scfv双特异性t细胞衔接子(engager)(bite)。在这样的实施方式中,axl-cd3fn3结构域-scfv融合体包含对axl的结合亲和力(例如,通过axl特异性fn3结构域)和对cd3的结合亲和力(例如,通过cd3特异性scfv)。对于包含对t细胞受体组分(例如cd3)的结合亲和力的fn3结构域-scfv融合体,那些fn3结构域-scfv融合体可以称为fn3结构域-scfvt细胞衔接子。
在一些情况下,fn3结构域-scfv融合体的fn3结构域部分可以包含靶特异性fn3结构域的单体。在一些实施方式中,fn3结构域部分可以包含靶特异性fn3结构域的二聚体、三聚体或更多单体。在一个实施方式中,二聚体或三聚体等中的每个单体可以对单个抗原(例如,相同抗原的不同表位)具有特异性。例如,axl-cd3fn3结构域-scfv融合体可包含各自对axl(例如,axl的不同表位)具有特异性的fn3结构域的二聚体,并且还包含对cd3具有特异性的scfv。在另一个实例中,axl-cd3fn3结构域-scfv融合体可以包含各自对axl(例如,axl的不同表位)具有特异性的fn3结构域的三聚体,并且还包含对cd3具有特异性的scfv。在一个实施方式中,二聚体或三聚体等中的每个单体可以对不同抗原具有特异性。
由本公开的fn3结构域靶向的抗原存在于为了去除而靶向的组织中的细胞的表面或内部,例如肿瘤、腺体(例如前列腺)增生和血液恶性肿瘤。虽然表面抗原被一个或多个fn3结构域更有效地识别和结合,但是胞内抗原也可以被fn3结构域靶向。在一些实施方式中,靶抗原优选对癌症具有特异性。靶抗原的实例包括由各种免疫细胞、癌、肉瘤、淋巴瘤、白血病、生殖细胞肿瘤、母细胞瘤和与各种血液疾病相关的细胞所表达的抗原。
可被一个或多个fn3结构域靶向的癌症特异性的抗原包括4-ibb、5t4、腺癌抗原、α-甲胎蛋白、baff、b淋巴瘤细胞、c242抗原、ca-125、碳酸酐酶9(ca-ix)、c-met、ccr4、cd152、cd19、cd20、cd200、cd22、cd221、cd23(ige受体)、cd28、cd30(tnfrsf8)、cd33、cd4、cd40、cd44v6、cd51、cd52、cd56、cd74、cd80、cea、cnt0888、ctla-4、dr5、egfr、epcam、cd3、fap、纤连蛋白额外结构域b(fibronectinextradomain-b)、叶酸受体1、gd2、gd3神经节苷脂、糖蛋白75、gpnmb、her2/neu、hgf、人散射因子受体激酶、igf-1受体、igf-i、igg1、li-cam、il-13、il-6、胰岛素样生长因子i受体、整联蛋白α5β1、整联蛋白ανβ3、morab-009、ms4a1、muc1、粘蛋白canag、n-羟乙酰基(glycolyl)神经氨酸、npc-ic、pdgf-ra、pdl192、磷脂酰丝氨酸、前列腺癌细胞、rankl、ron、ror1、sch900105、sdc1、slamf7、tag-72、腱生蛋白c、tgfβ2、tgf-β、trail-r1、trail-r2、肿瘤抗原ctaa16.88、vegf-a、vegfr-1、vegfr2或波形蛋白中的一种或多种。
可被一个或多个fn3结构域靶向的炎性疾病特异性的抗原包括aoc3(vap-1)、cam-3001、ccl11(嗜酸粒细胞趋化因子(eotaxin)-1)、cd125、cd147(basigin)、cd154(cd40l)、cd2、cd20、cd23(ige受体)、cd25(il-2受体链)、cd3、cd4、cd5、ifn-α、ifn-γ、ige、igefc区、il-1、il-12、il-23、il-13、il-17、il-17a、il-22、il-4、il-5、il-5、il-6、il-6受体、整联蛋白α4、整联蛋白α4β7,lfa-1(cd11a)、medi-528、肌生长抑制素、ox-40、rhumabβ7、硬化蛋白(scleroscin)、sost、tgfβ1、tnf-α或vegf-a中的一种或多种。
癌症特异性的抗原包括以特异性或扩增方式在癌细胞上发现的表面蛋白,例如il-14受体,对于b细胞淋巴瘤为cd19、cd20和cd40,对于多种癌为lewisy和cea抗原,对于乳腺癌和结直肠癌为tag72抗原,对于肺癌为egf-r,叶酸结合蛋白和her-2蛋白(通常在人乳腺癌和卵巢癌中扩增),或病毒蛋白,例如hiv的gp120和gp41包膜蛋白,乙型和丙型肝炎病毒的包膜蛋白,人巨细胞病毒的糖蛋白b和其他包膜糖蛋白,以及来自癌病毒(例如卡波西氏肉瘤相关疱疹病毒)的包膜蛋白。其他潜在的靶抗原包括cd4(其中配体为hivgp120包膜糖蛋白)和其他病毒受体,例如icam(其是人鼻病毒的受体),和脊髓灰质炎病毒的相关受体分子。
在一个实施方式中,fn3结构域可以靶向接合(engage)癌症治疗细胞(例如nk细胞和本文提及的其他细胞)的抗原,以通过充当免疫效应细胞来激活癌症治疗细胞。这方面的一个例子是靶向cd16a抗原以接合nk细胞以对抗表达cd30的恶性肿瘤的fn3结构域。双特异性四价afm13抗体是可以发挥这种作用的抗体的实例。这种类型的实施方式的更多细节可见于例如rothe等,blood(2015)125(26):4024-4031。
在一个实施方式中,fn3结构域可以靶向抗原,例如axl受体酪氨酸激酶(axl),mer受体酪氨酸激酶(mer),b细胞成熟蛋白(bcma;也称为tnf受体超家族成员17(tnfrsf17)),程序性细胞死亡1配体1(pdl1;也称为cd274),程序性细胞死亡蛋白1(pd-1;也称为cd279),cd3t细胞共受体(cd3),细胞毒性t淋巴细胞相关蛋白4(ctla-4;也称为cd152),血管内皮生长因子受体2(vegfr2),卷曲的类受体(frizzledclassreceptor)2(fzd2),卷曲的类受体4(fzd4),上皮细胞粘附分子(epcam),siglec-3(也称为cd33),前列腺特异性膜抗原(psma),分化簇28(cd28),4-1bb(也称为cd137或肿瘤坏死因子受体超家族成员9(tnfrsf9)),fc-γ受体iiia(cd16a),抑制性nk细胞受体cd94/nkg2a,mhci类链相关蛋白a(mica),mhci类链相关蛋白b(micb),分化簇38(cd38;也称为环状adp核糖水解酶),和激活受体nkp46(也称为cd335)。
因此,可以产生各种类型的走查诱变和天然变体组合fn3结构域多肽文库,并且这样的文库可用于筛选具有选定的结合或酶活性的一个或多个fn3结构域多肽的存在。
例如,fn3结构域多肽的文库可以包括(a)具有选定的天然fn3结构域多肽的野生型氨基酸序列的区域a、ab、b、c、cd、d、e、ef、f和g,和(b)具有选定的长度的环区bc、de和fg。具有选定的长度的至少一个选定的环区包含由编码序列的文库所编码的自然变体组合序列或走查诱变序列的文库,所述编码序列在各个环位置处编码保守或选定的半保守共有氨基酸,和如果共有氨基酸的出现频率等于或小于至少50%的所选阈值频率,在该位置处出现率高于选定的最小阈值出现率的其他天然变异氨基酸(包括半保守氨基酸和可变氨基酸)或其化学等效物。
在一些实施方式中,本发明的fn3结构域多肽包含具有选定的长度的环区bc、de和fg。本发明的fn3结构域多肽的选定的环长度包括具有11个氨基酸的环长度的bc、具有14个氨基酸的环长度的bc、具有15个氨基酸的环长度的bc、具有6个氨基酸的环长度的de、具有8个氨基酸的环长度的fg、和/或具有11个氨基酸的环长度的fg。
在一些实施方式中,本发明的fn3结构域多肽包含具有选择的天然fn3结构域多肽的野生型氨基酸序列的区域a、ab、b、c、cd、d、e、ef、f和g。在一个实施方式中,选定的天然fn3结构域多肽是人纤连蛋白的第14fn3模块。在一个实施方式中,选定的天然fn3结构域多肽是人纤连蛋白的第10fn3模块。
在某些实施方式中,筛选fn3结构域多肽的文库中具有选定的结合或酶活性的一种或多种fn3结构域多肽。筛选可以包括例如使fn3结构域多肽的文库与靶抗原/底物接触,其中每个fn3结构域多肽包含纤连蛋白结合结构域,和鉴定包含结合靶抗原/底物的纤连蛋白结合结构域的fn3结构域多肽。筛选可以通过例如通过facs进行的阳性物理克隆选择、噬菌体淘选(panning),或选择性配体保留来进行。
在一些实施方式中,在鉴定靶特异性fn3结构域多肽后,可以通过将靶特异性fn3结构域多肽序列与编码嵌合抗原受体的个体结构域的序列连接在一起来装配嵌合抗原受体。
嵌合抗原受体
本发明提供了用于与靶抗原结合的car,其包含包含fn3结构域多肽的至少一个抗原特异性靶向区,即“fn3car”。在一些实施方式中,fn3car是包含至少两个抗原特异性靶向区的多特异性car,其中所述抗原特异性靶向区中的一个或多个包含fn3结构域多肽。在一个实施方式中,fn3car是包含至少两个抗原特异性靶向区的多特异性car,其中每个抗原特异性靶向区包含fn3结构域多肽。在一些实施方式中,一旦靶特异性fn3结构域多肽被鉴定,就可以通过将靶特异性fn3结构域多肽序列与编码嵌合抗原受体的个体结构域的序列连接在一起来装配嵌合抗原受体。
在一些实施方式中,本发明的嵌合抗原受体是包含至少一个抗原特异性靶向区(astr)、跨膜结构域(tm)和胞内信号传导结构域(isd)的嵌合人工蛋白。在一些实施方式中,fn3car可以进一步包含胞外间隔结构域(esd)和/或共刺激结构域(csd)。
astr是car的胞外区域,用于与包括蛋白质、碳水化合物和糖脂的特定靶抗原结合。在一些实施方式中,astr包含具有靶特异性纤连蛋白结合结构域的fn3结构域多肽。astr还可以包含另一个蛋白质功能结构域,以识别并结合靶抗原。因为靶抗原可以具有其他生物学功能,例如充当受体或配体,所以astr可以替代地包含用于特异性结合抗原的功能结构域。具有功能结构域的蛋白的一些实例包括连接的细胞因子(其导致识别带有细胞因子受体的细胞),亲和体(affibody),来自天然存在的受体的配体结合结构域,受体的可溶性蛋白质/肽配体,例如在肿瘤细胞上。如本领域技术人员将理解的,能够以高亲和力结合给定抗原的几乎任何分子可以用于astr。
在一个实施方式中,本发明的fn3car包含靶向至少两个不同抗原或同一抗原上的两个表位的至少两个astr。在一个实施方式中,fn3car包含靶向至少三个或更多个不同抗原或表位的三个或更多个astr。当fn3car中存在多个astr时,所述astr可以串联排列并且可以被接头肽分开。当fn3car中存在两个或更多个astr时,所述astr通过寡肽或多肽接头、fc铰链或膜铰链区,在单一多肽链上彼此共价连接。在一个实施方式中,连接两个或更多个astr的接头是寡肽接头。在一个实施方式中,连接两个或更多个astr的接头是fc铰链区。在一个实施方式中,连接两个或更多个astr的接头是膜铰链区。
在一些实施方式中,fn3car的跨膜结构域(tm)是能够跨越细胞(例如细胞毒性细胞)的质膜的区域。跨膜结构域用于插入细胞膜中,例如真核细胞膜。在一些实施方式中,跨膜结构域插入在fn3car的一个或多个astr与细胞内部分之间。跨膜结构域可以选自跨膜蛋白的跨膜区,例如i型跨膜蛋白的跨膜区,人工疏水序列或其组合。跨膜结构域的实例包括但不限于t细胞受体的α、β或ζ链,cd28,cd3ε,cd45,cd4,cd5,cd7,cd8,cd9,cd16,cd22,cd33,cd37,cd64,cd80,cd86,cd134(ox-40),cd137,cd154的跨膜区。在一些实施方式中,合成跨膜结构域可以包含苯丙氨酸、色氨酸和缬氨酸的三联体。在一些实施方式中,短寡肽接头或多肽接头,优选长度在2至10个氨基酸之间,可形成fn3car的跨膜结构域和胞内信号传导结构域之间的连接。甘氨酸-丝氨酸二联体提供了在fn3car的跨膜结构域和胞内信号传导结构域之间特别合适的接头。
本发明的fn3car还包含胞内信号传导结构域。胞内信号传导结构域转导效应子功能信号并指导细胞(例如细胞毒性细胞)执行其专门功能,例如伤害和/或破坏靶细胞。胞内信号传导结构域的实例包括但不限于t细胞受体复合物的ζ链或任何其同源物,例如η链、fcεriγ和β链、mb1(iga)链、b29(ig)链等,人cd3ζ链,cd3多肽(δ,δ和ε),syk家族酪氨酸激酶(syk、zap70等),src家族酪氨酸激酶(lck、fyn、lyn等),以及其他涉及t细胞转导的分子,例如cd2、cd5和cd28。在一个实施方式中,胞内信号传导结构域可以是人cd3ζ链,fcγriii,fcεri,fc受体的细胞质尾巴,具有基于免疫受体酪氨酸的激活基序(itam)的细胞质受体,及其组合。
在一些实施方式中,在fn3car中使用的胞内信号传导结构域可以包含多种其他免疫信号传导受体的多种类型的胞内信号传导结构域,包括但不限于第一代、第二代和第三代t细胞信号传导蛋白,包括cd3、b7家族共刺激,和肿瘤坏死因子受体(tnfr)超家族受体(参见例如parkandbrentjens,j.clin.oncol.(2015)33(6):651-653)。另外,胞内信号传导结构域包含nk和nkt细胞使用的信号传导结构域(参见例如hermansonandkaufman,front.immunol.(2015)6:195),例如nkp30(b7-h6)(参见例如,zhang等,j.immunol.(2012)189(5):2290-2299)和dap12(参见例如topfer等,j.immunol.(2015)194(7):3201-3212),nkg2d,nkp44,nkp46,dap10和cd3z的信号传导结构域。
适用于本公开的fn3car的胞内信号传导结构域包括响应于car的激活(即,被抗原和二聚剂激活),提供独特且可检测的信号(例如,通过细胞进行的一种或多种细胞因子的产生增加;靶基因转录改变;蛋白质活性变化;细胞行为变化,例如细胞死亡;细胞增殖;细胞分化;细胞存活;细胞信号传导响应的调节等)的任何期望的信号传导结构域。在一些实施方式中,胞内信号传导结构域包含至少一个(例如,一个、两个、三个、四个、五个、六个等)如下所述的itam基序。在一些实施方式中,胞内信号传导结构域包含dap10/cd28型信号传导链。在一些实施方式中,胞内信号传导结构域不共价附于膜结合的fn3car,而是分散在细胞质中。
适用于本公开的fn3car的胞内信号传导结构域包括含有基于免疫受体酪氨酸的激活基序(itam)的细胞内信号传导多肽。在一些实施方式中,itam基序在胞内信号传导结构域中重复两次,其中itam基序的第一实例和第二实例彼此间隔6至8个氨基酸。在一个实施方式中,主题fn3car的胞内信号传导结构域包含3个itam基序。
在一些实施方式中,胞内信号传导结构域包含人免疫球蛋白受体的信号传导结构域,其包含基于免疫受体酪氨酸的激活基序(itam),例如但不限于fcγri,fcγriia,fcγriic,fcγriiia,fcrl5(参见例如gillis等,front.immunol.(2014)5:254)。
合适的胞内信号传导结构域可以是衍生自包含itam基序的多肽的包含itam基序的部分。例如,合适的胞内信号传导结构域可以是来自任何包含itam基序的蛋白质的包含itam基序的结构域。因此,合适的胞内信号传导结构域不需要包含从其衍生的整个蛋白质的整个序列。合适的含itam基序的多肽的实例包括但不限于:dap12,fcer1g(fcε受体iγ链),cd3d(cd3δ),cd3e(cd3ε),cd3g(cd3γ),cd3z(cd3ζ)和cd79a(抗原受体复合物相关的蛋白质α链)。
在一个实施方式中,胞内信号传导结构域衍生自dap12(也称为tyrobp;tyro蛋白酪氨酸激酶结合蛋白;karap;plosl;dnax激活蛋白12;kar相关蛋白;tyro蛋白酪氨酸激酶结合蛋白;杀伤激活受体相关蛋白;杀伤激活受体相关蛋白等)。在一个实施方式中,胞内信号传导结构域衍生自fcer1g(也称为fcrg;fcε受体iγ链;fc受体γ链;fc-εri-γ;fcrγ;fcer1γ;高亲和力免疫球蛋白ε受体亚单位γ;免疫球蛋白e受体,高亲和力,γ链等)。在一个实施方式中,胞内信号传导结构域衍生自t细胞表面糖蛋白cd3δ链(也称为cd3d;cd3-delta;t3d;cd3抗原,δ亚基;cd3δ;cd3d抗原,δ多肽(tit3复合物);okt3,δ链;t细胞受体t3δ链;t细胞表面糖蛋白cd3δ链;等)。在一个实施方式中,胞内信号传导结构域衍生自t细胞表面糖蛋白cd3ε链(也称为cd3e,t细胞表面抗原t3/leu-4ε链,t细胞表面糖蛋白cd3ε链,ai504783,cd3,cd3ε,t3e等)。在一个实施方式中,胞内信号传导结构域衍生自t细胞表面糖蛋白cd3γ链(也称为cd3g,t细胞受体t3γ链,cd3-gamma,t3g,γ多肽(tit3复合物)等)。在一个实施方式中,胞内信号传导结构域衍生自t细胞表面糖蛋白cd3ζ链(也称为cd3z,t细胞受体t3ζ链,cd247,cd3-zeta,cd3h,cd3q,t3z,tcrz等)。在一个实施方式中,胞内信号传导结构域衍生自cd79a(也称为b细胞抗原受体复合物相关蛋白α链;cd79a抗原(免疫球蛋白相关α);mb-1膜糖蛋白;ig-α;膜结合免疫球蛋白相关蛋白;表面igm相关蛋白等)。在一个实施方式中,适用于本公开的fn3car的胞内信号传导结构域包括dap10/cd28型信号传导链。在一个实施方式中,适用于本公开的fn3car的胞内信号传导结构域包括zap70多肽。在一些实施方式中,胞内信号传导结构域包括tcrζ,fcrγ,fcrβ,cd3γ,cd3δ,cd3ε,cd5,cd22,cd79a,cd79b或cd66d的胞质信号传导结构域。在一个实施方式中,fn3car中的胞内信号传导结构域包括人cd3ζ的胞质信号传导结构域。
本发明的fn3car可以包含共刺激结构域,其具有为表达fn3car的细胞毒性细胞增强细胞增殖、细胞存活和记忆细胞发育的功能。本发明的fn3car可以包含一个或多个共刺激结构域,其选自以下中的共刺激结构域:tnfr超家族的蛋白,cd28,cd137(4-1bb),cd134(ox40),dap10,cd27,cd2,cd7,cd5,icam-1,lfa-1(cd11a/cd18),lck,tnfr-i,pd-1,tnfr-ii,fas,cd30,cd40,icoslight,nkg2c,b7-h3或其任何组合。如果fn3car包含一个以上的共刺激结构域,则这些结构域可以串联排列,任选地由接头分隔。共刺激结构域是细胞内结构域,其可以位于fn3car中的跨膜结构域和胞内信号传导结构域之间。
适用于本公开的fn3car的共刺激结构域通常是衍生自受体的多肽。主题共刺激结构域可以是跨膜蛋白的细胞内部分(即共刺激结构域可以衍生自跨膜蛋白)。合适的共刺激多肽的非限制性实例包括但不限于4-1bb(cd137),cd28,icos,ox-40,btla,cd27,cd30,gitr和hvem。
在一个实施方式中,共刺激结构域衍生自跨膜蛋白4-1bb(也称为tnfrsf9;cd137;4-1bb;cdw137;ila等)的细胞内部分。在一个实施方式中,共刺激结构域衍生自跨膜蛋白cd28(也称为tp44)的细胞内部分。在一个实施方式中,共刺激结构域衍生自跨膜蛋白icos(也称为ailim、cd278和cvid1)的细胞内部分。在一个实施方式中,共刺激结构域衍生自跨膜蛋白ox-40(也称为tnfrsf4、rp5-902p8.3、act35、cd134、ox40、txgp1l)的细胞内部分。在一个实施方式中,共刺激结构域衍生自跨膜蛋白btla(也称为btla1和cd272)的细胞内部分。在一个实施方式中,共刺激结构域衍生自跨膜蛋白cd27(也称为s152、t14、tnfrsf7和tp55)的细胞内部分。在一个实施方式中,共刺激结构域衍生自跨膜蛋白cd30(也称为tnfrsf8、d1s166e和ki-1)的细胞内部分。在一个实施方式中,共刺激结构域衍生自跨膜蛋白gitr(也称为tnfrsf18、rp5-902p8.2、aitr、cd357和gitr-d)的细胞内部分。在一个实施方式中,共刺激结构域衍生自跨膜蛋白hvem(也称为tnfrsf14、rp3-395m20.6、atar、cd270、hvea、hvem、lightr和tr2)的细胞内部分。
fn3car的胞外间隔结构域是位于astr和跨膜结构域之间的亲水区域。在一些实施方式中,该结构域促进fn3car的适当的蛋白质折叠。胞外间隔结构域是fn3car的任选组分。胞外间隔结构域可以包含选自以下的结构域:抗体的fc片段,抗体的铰链区,抗体的ch2区,抗体的ch3区,人工间隔子序列或其组合。胞外间隔结构域的实例包括cd8a铰链,由可小至三个甘氨酸(gly)的多肽制成的人工间隔子,以及igg(例如人igg4)的ch1和ch3结构域。
在一些实施方式中,本公开的fn3car分子包含将两个抗原特异性靶向区与跨膜结构域连接的胞外间隔结构域,所述跨膜结构域又连接至t细胞内部的共刺激结构域和胞内信号传导结构域。胞外间隔结构域优选地能够支持抗原特异性靶向区以识别并结合靶细胞上的靶抗原(hudecek等,cancerimmunol.res.(2015)3(2):125-135)。在一些实施方式中,胞外间隔结构域是柔性结构域,因此允许抗原特异性靶向区具有最佳识别细胞例如肿瘤细胞上靶抗原的特异性结构和密度的结构(hudecek等,如上)。胞外间隔结构域的灵活性允许胞外间隔结构域采用许多不同的构象。
在一些实施方式中,胞外间隔结构域是免疫球蛋白重链铰链区。在一些实施方式中,胞外间隔结构域是衍生自受体的铰链区多肽(例如,cd8衍生的铰链区)。
胞外间隔结构域的长度可为约4个氨基酸至约50个氨基酸,例如约4个氨基酸至约10个氨基酸,约10个氨基酸至约15个氨基酸,约15个氨基酸至约20个氨基酸,约20个氨基酸至约25个氨基酸,约25个氨基酸至约30个氨基酸,约30个氨基酸至约40个氨基酸,或约40个氨基酸至约50个氨基酸。
合适的胞外间隔结构域可以容易地选择并且可以具有许多合适长度中的任一个,例如从1个氨基酸(例如gly)至20个氨基酸,从2个氨基酸至15个氨基酸,从3个氨基酸氨基酸至12个氨基酸,包括4个氨基酸至10个氨基酸,5个氨基酸至9个氨基酸,6个氨基酸至8个氨基酸,或7个氨基酸至8个氨基酸,并且可以是1、2、3、4、5、6或7个氨基酸。
例如,胞外间隔结构域包括甘氨酸聚合物(g)n,甘氨酸-丝氨酸聚合物(包括例如(gs)n,(gsggs)n(seqidno:1)和(gggs)n(seqidno:2),其中n是至少一的整数,甘氨酸-丙氨酸聚合物,丙氨酸-丝氨酸聚合物和本领域已知的其他柔性接头。可以使用甘氨酸和甘氨酸-丝氨酸聚合物;gly和ser两者是相对非结构化的,因此可以充当组件之间的中性纽带。可以使用甘氨酸聚合物;甘氨酸获得比甚至丙氨酸显著更多的phi-psi空间,并且比具有更长侧链的残基更不受限制(参见,例如,scheraga,rev.computational.chem.(1992)2:73-142)。示例性间隔子可包含氨基酸序列,包括但不限于ggsg(seqidno:3),ggsgg(seqidno:4),gsgsg(seqidno:5),gsggg(seqidno:6),gggsg(seqidno:7),gsssg(seqidno:8)等。
在一些实施方式中,胞外间隔结构域是免疫球蛋白重链铰链区。免疫球蛋白铰链区的氨基酸序列是本领域已知的。参见,例如,tan等,proc.natl.acad.sci.usa(1990)87(1):162-166;和huck等,nucleicacidsres.(1986)14(4):1779-1789。作为非限制性实例,免疫球蛋白铰链区可包含以下氨基酸序列之一:dktht(seqidno:9);cppc(seqidno:10);cpepkscdtpppcpr(seqidno:11)(参见例如glaser等,j.biol.chem.(2005)280:41494-41503);elktplgdttht(seqidno:12);kscdkthtcp(seqidno:13);kccvdcp(seqidno:14);kygppcp(seqidno:15);epkscdkthtcppcp(seqidno:16)(人igg1铰链);erkccvecppcp(seqidno:17)(人igg2铰链);elktplgdtthtcprcp(seqidno:18)(人igg3铰链);spnmvphahhaq(seqidno:19)(人igg4铰链);等。
胞外间隔结构域可以包含人igg1,igg2,igg3或igg4铰链区的氨基酸序列。在一个实施方式中,与野生型(天然存在的)铰链区相比,胞外间隔结构域可以包含一个或多个氨基酸置换和/或插入和/或缺失。例如,人igg1铰链的his229可以被tyr置换,使得铰链区包含序列epkscdktytcppcp(seqidno:20);参见例如,yan等,j.biol.chem.(2012)287:5891-5897。在一个实施方式中,胞外间隔结构域可以包含衍生自人cd8或其变体的氨基酸序列。
fn3car靶向的抗原存在于为去除而靶向的组织中的细胞的表面上或内部,例如肿瘤,腺体(例如前列腺)增生,和血液恶性肿瘤。尽管表面抗原被主题fn3car的一个或多个astr更有效地识别和结合,但是胞内抗原也可以被fn3car靶向。在一些实施方式中,靶抗原优选对癌症具有特异性。靶抗原的实例包括由各种免疫细胞,癌,肉瘤,淋巴瘤,白血病,生殖细胞肿瘤,母细胞瘤和各种血液疾病相关的细胞表达的抗原。
可被主题fn3car的一个或多个astr靶向的癌症特异性的抗原包括4-ibb,5t4,腺癌抗原,α-甲胎蛋白,baff,b淋巴瘤细胞,c242抗原,ca-125,碳酸酐酶9(ca-ix),c-met,ccr4,cd152,cd19,cd20,cd200,cd22,cd221,cd23(ige受体),cd28,cd30(tnfrsf8),cd33,cd4,cd40,cd44v6,cd51,cd52,cd56,cd74,cd80,cea,cnt0888,ctla-4,dr5,egfr,epcam,cd3,fap,纤连蛋白额外结构域b,叶酸受体1,gd2,gd3神经节苷脂,糖蛋白75,gpnmb,her2/neu,hgf,人分散因子受体激酶,igf-1受体,igf-i,igg1,li-cam,il-13,il-6,胰岛素样生长因子i受体,整联蛋白α5β1,整联蛋白ανβ3,morab-009,ms4a1,muc1,粘蛋白canag,n-羟乙酰神经氨酸,npc-ic,pdgf-ra,pdl192,磷脂酰丝氨酸,前列腺癌细胞,rankl,ron,ror1,sch900105,sdc1,slamf7,tag-72,腱生蛋白c,tgfβ2,tgf-β,trail-r1,trail-r2,肿瘤抗原ctaa16.88,vegf-a,vegfr-1,vegfr2或波形蛋白中的一种或多种。
可被主题fn3car的一种或多种astr靶向的炎性疾病特异性的抗原包括aoc3(vap-1),cam-3001,ccl11(嗜酸粒细胞趋化因子-1),cd125,cd147(basigin),cd154(cd40l),cd2,cd20,cd23(ige受体),cd25(il-2受体链),cd3,cd4,cd5,ifn-α,ifn-γ,ige,igefc区,il-1,il-12,il-23,il-13,il-17,il-17a,il-22,il-4,il-5,il-5,il-6,il-6受体,整联蛋白α4,整联蛋白α4β7,lfa-1(cd1la),medi-528,肌生长抑制素,ox-40,rhumabβ7,硬化蛋白,sost,tgfβ1,tnf-α或vegf-a的一种或多种。
癌症特异性抗原包括以特异性或扩增方式在癌细胞上发现的表面蛋白,例如il-14受体,对于b细胞淋巴瘤为cd19、cd20和cd40,对于多种癌症为lewisy和cea抗原,对于乳腺癌和结直肠癌为tag72抗原,对于肺癌为egf-r,叶酸结合蛋白和her-2蛋白(通常在人乳腺癌和卵巢癌中扩增),或病毒蛋白,例如hiv的gp120和gp41包膜蛋白,乙型和丙型肝炎病毒的包膜蛋白,人巨细胞病毒的糖蛋白b和其他包膜糖蛋白,以及来自癌病毒(例如卡波西氏肉瘤相关疱疹病毒)的包膜蛋白。其他潜在的靶抗原包括cd4(其中配体为hivgp120包膜糖蛋白)和其他病毒受体,例如icam(其是人鼻病毒的受体),和脊髓灰质炎病毒的相关受体分子。
在一个实施方式中,fn3car可以靶向接合癌症治疗细胞(例如nk细胞和本文提及的其他细胞)的抗原,以通过充当免疫效应细胞来激活癌症治疗细胞。这方面的一个例子是靶向cd16a抗原以接合nk细胞以对抗表达cd30的恶性肿瘤的fn3car。双特异性四价afm13抗体是可以发挥这种作用的抗体的实例。这种类型的实施方式的更多细节可见于例如rothe等,blood(2015)125(26):4024-4031。
在一个实施方式中,fn3car可以靶向抗原,例如axl受体酪氨酸激酶(axl),mer受体酪氨酸激酶(mer),b细胞成熟蛋白(bcma;也称为tnf受体超家族成员17(tnfrsf17)),程序性细胞死亡1配体1(pdl1;也称为cd274),程序性细胞死亡蛋白1(pd-1;也称为cd279),cd3t细胞共受体(cd3),细胞毒性t淋巴细胞相关蛋白4(ctla-4;也称为cd152),血管内皮生长因子受体2(vegfr2),卷曲的类受体2(fzd2),卷曲的类受体4(fzd4),上皮细胞粘附分子(epcam),siglec-3(也称为cd33),前列腺特异性膜抗原(psma),分化簇28(cd28),4-1bb(也称为cd137或肿瘤坏死因子受体超家族成员9(tnfrsf9)),fc-γ受体iiia(cd16a),抑制性nk细胞受体cd94/nkg2a,mhci类链相关蛋白a(mica),mhci类链相关蛋白b(micb),分化簇38(cd38;也称为环状adp核糖水解酶),和激活受体nkp46(也称为cd335)。
在一些实施方式中,本公开的fn3car是多特异性fn3car。多特异性fn3car包含两个或更多个astr,例如三个或更多个,四个或更多个,五个或更多个,六个或更多个等,每个astr结合两个或更多个靶抗原,例如三个或更多个,四个或更多个,五个或更多个,六个或更多个等。在一个实施方式中,两个或更多个靶抗原是相同靶抗原的不同表位。在一个实施方式中,两个或更多个靶抗原是不同的。
在一些实施方式中,本公开的多特异性fn3car包含结合两个或更多个靶抗原的两个或更多个astr,其中所述两个或更多个靶抗原在同一细胞上。在一个实施方式中,两个或更多个靶抗原在至少两个细胞上。在一个实施方式中,两个或更多个靶抗原在至少两个细胞上,其中至少两个细胞各自具有相同的细胞类型。在一个实施方式中,两个或更多个靶抗原在至少两个细胞上,其中至少两个细胞各自具有不同的细胞类型。例如,两个或更多个靶抗原中的至少一个可以在癌细胞上,而两个或更多个靶抗原中的另一个可以在细胞毒性细胞(例如t细胞)上。
在一些实施方式中,两个或更多个astr可以独立地起作用,例如,包含两个或更多个fn3结构域多肽并且没有其他另外的组分(例如,car组分)的分子结合两个或更多个靶抗原。在一个实施方式中,两个或更多个靶抗原在同一细胞上。在一实施方式中,两个或更多个靶抗原在至少两个细胞上。在一个实施方式中,两个或更多个靶抗原在至少两个细胞上,其中至少两个细胞各自具有相同的细胞类型。在一个实施方式中,两个或更多个靶抗原在至少两个细胞上,其中至少两个细胞中各自具有不同的细胞类型。例如,两个或更多个靶抗原中的至少一个可以在癌细胞上,而两个或更多个靶抗原中的另一个可以在细胞毒性细胞(例如t细胞)上。
在一些实施方式中,两个或更多个astr通过接头连接。可用于连接两个或更多个astr的本公开的接头可以具有任何长度,例如2个或更多个氨基酸,3个或更多个氨基酸,4个或更多个氨基酸,5个或更多个氨基酸,6个或更多个氨基酸,7个或更多个氨基酸,8或更多个氨基酸,9或更多个氨基酸,10或更多个氨基酸,11或更多个氨基酸,12或更多个氨基酸,13或更多个氨基酸,14或更多个氨基酸,15或更多个氨基酸,16或更多个氨基酸,17或更多个氨基酸,18或更多个氨基酸,19或更多个氨基酸,20或更多个氨基酸,21或更多个氨基酸,22或更多个氨基酸,23或更多个氨基酸,24或更多个氨基酸,25或更多个氨基酸,等等。在一个实施方式中,接头是具有20个氨基酸(aa)的长度的接头。在一个实施方式中,接头是具有14个氨基酸的长度的接头。在一个实施方式中,接头衍生自天然纤连蛋白序列。在一个实施方式中,天然纤连蛋白序列是天然纤连蛋白例如人纤连蛋白的第14fn3结构域的末端与第15fn3结构域的bc环之间的序列。在一个实施方式中,接头包含序列aidapsnlrflattpnsllv(seqidno:21)。在一个实施方式中,接头是衍生自第14fn3结构域的末端与第15fn3结构域的bc环之间的序列的长度为20个氨基酸的接头,例如具有序列aidapsnlrflattpnsllv(seqidno:21)的接头。在一个实施方式中,接头包含序列aidapsnlrflatt(seqidno:22)。在一个实施方式中,接头是衍生自第14fn3结构域的末端和第15fn3结构域的bc环之间的序列的长度为14个氨基酸的接头,例如具有序列aidapsnlrflatt(seqidno:22)的接头。天然纤连蛋白的第14fn3结构域和第15fn3结构域之间的示例性序列如下所示:
nvspprrarvtdatettitiswrtktetitgfqvdavpangqtpiqrtikpdvrsytitglqpgtdykiylytlndnarsspvvidastaidapsnlrflattpnsllvswqppraritgyiikyekpgspprevvprprpgvteatitglepgteytiyvialknnqksepligrkkt(seqidno:23)。
靶抗原的另外实例包括但不限于agr2,aig1,akap1,akap2,angpt1,angpt2,angptl3,angptl4,anpep,apc,apoc1,ar,azgp1(锌-α-糖蛋白),bad,bag1,bai1,bcl2,bmp6,bpag1,brc1a,brca1,cant1,cav1,ccl11,ccl2,ccna1,ccna2,ccnd1,ccne1,ccne2,cd138,cd164,cd19,cd20,cd22,cd3,cd4,cd44,cd52,cd8,cdh1(e-钙黏蛋白),cdh10,cdh12,cdh13,cdh18,cdh19,cdh20,cdh5,cdh7,cdh8,cdh9,cdk2,cdk3,cdk4,cdk5,cdk6,cdk7,cdk9,cdkn1a(p21wap1/cip1),cdkn1b(p27kip1),cdkn1c,cdkn2a(p16ink4a),cdkn2b,cdkn2c,cdkn3,cea,chga,chgb,cldn3,cldn7(claudin-7),cln3,clu(簇集素),col18a1,col1a1,col4a3,col6a1,ctnnb1(β-连环蛋白),ctsb(组织蛋白酶),cxcl1,cxcl10,cxcl3,cxcl5,cxcl6,cxcl9,cyb5,cyc1,dap2ip,des,dncl1,e2f1,ecgf1,edg1,efna1,efna3,efnb2,egf,egfr,egfrviii,elac2,eng,eno1,eno2,eno3,ephb4,erbb2(her-2),ereg,erk8,esr1,esr2,f3(tf),fap,fasn,fgf1,fgf10,fgf11,fgf12,fgf13,fgf14,fgf16,fgf17,fgf18,fgf19,fgf2,fgf20,fgf21,fgf22,fgf23,fgf3,fgf4,fgf5,fgf6,fgf7,fgf8,fgf9,fgfr3,figf,flj12584,flj25530,flrt1(纤连蛋白),flt1,fosl1(fra-1),gabrp(gaba-a),gageb1,gagec1,gata3,gd2,ggt1,gnas1,gnrh1,gpc3,grp,gsn(凝溶胶蛋白),gstp1,hgf,hgfr(met),hip1,humcyt2a,id2,ifna1,ifnb1,ifng,igf1,igf1r,igf2,igfbp2,igfbp3,igfbp6,igκ轻链,il12a,il13ra2,il1a,il1b,il2,il24,il29,il2ra,il3ra(cd123),il6,il6r,il6st(糖蛋白130),il8,ilk,inha,insl3,insl4,itga1,itga6(α6整联蛋白),itgav,itgb3,itgb4(β4整联蛋白),jag1,jun,k6hf,kaii,kdr,klf5(gcboxbp),klk10,klk12,klk13,klk14,klk15,klk3,klk4,klk5,klk6,klk9,krt1,krt19,krt2a,krthb6(毛发特异性ii型角蛋白),lama5,lewis-y,macmarcks,map2k7(c-jun),mdk,mib1,mki67(ki-67),mmp2,mmp9,msln(间皮素),msmb,mt3(金属硫蛋白-3),mtss1,muc1(黏蛋白),muc16,myc,ngfb(ngf),ngfr,nkg2d配体,nme1(nm23a),nox5,nr0b1,nr0b2,nr1d1,nr1d2,nr1h2,nr1h3,nr1h4,nr1i2,nr1i3,nr2c1,nr2c2,nr2e1,nr2e3,nr2f1,nr2f2,nr2f6,nr3c1,nr3c2,nr4a1,nr4a2,nr4a3,nr5a1,nr5a2,nr6a1,nrp1,nrp2,ntn4,odz1,p1as2,p1k3cg,pap,part1,pate,pawr,pca3,pcna,pdgfa,pecam1,pf4,pgf,pgr,plau(upa),网蛋白,plg,plxdc1,ppid,pr1,prkcq,prkd1,prl,prok2,psap,psca,psma,pten,ptgs2(cox-2),rac2(p21-rac2),rarb,robo2,ror-1,s100a2,scgb1d2(亲脂素b),scgb2a1(乳腺珠蛋白-2),scgb2a2(乳腺珠蛋白-1),serpina3,serpinb5(乳腺丝抑蛋白,maspin),serpine1(pai-1),serpinf1,shbg,shbq,slc2a2,slc33a1,slc43a1,sprr1b(spr1),stab1,steap,steap2,tek,tgfa,tgfb1,tgfb111,tgfb1i1,tgfb2,tgfb3,tgfbr1,tgra,thbs1(血小板反应蛋白-1),thbs2,thbs4,tie(tie-1),timp3,tnf,tnfaip2(b94),tnfrsf6(fas),tnfrsf7(bcma),tnfrsf8(cd30),tnfsf10,tnfsf6(fasl),top2a(拓扑异构酶-2α),tp53,tpm1,tpm2,trpc6,vegf和vegfc。
条件性活性嵌合抗原受体
本发明提供了用于与靶抗原结合的条件性活性fn3car,其包含包含fn3结构域多肽的至少一个抗原特异性靶向区,其中所述至少一个抗原特异性靶向区演化自野生型蛋白或其结构域,并具有以下中的至少一者:(a)与所述野生型蛋白或其结构域的抗原特异性靶向区相比,在正常生理条件下在测定中活性降低;和(b)与所述野生型蛋白或其结构域的抗原特异性靶向区相比,在异常条件下在测定中活性增加。在一些实施方式中,本发明的嵌合抗原受体还包含跨膜结构域(tm)和胞内信号传导结构域(isd)。在一些实施方式中,fn3car可以进一步包含胞外间隔结构域(esd)和/或共刺激结构域(csd)。本文描述了本发明的fn3car的非astr组分。
与没有条件性活性抗原特异性靶向区的相同fn3car相比,本发明的条件性活性fn3car具有以下中的至少一者:(1)其在正常生理条件下对靶抗原的亲和力可逆或不可逆地降低,和(2)亲和力增加。这些条件性活性fn3car可以例如将细胞毒性细胞引导到存在异常条件的疾病部位,例如肿瘤微环境或滑液。作为这些特性的结果,由于其对正常组织的低亲和力,条件性活性fn3car可以优先将细胞毒性细胞引导至疾病部位。这样的条件性活性fn3car可以显著减少副作用,并允许使用更高剂量的治疗剂来提高治疗效果。本公开的条件性活性fn3car对于开发在受试者内短时间段或有限时间段所需的新型疗法特别有价值。有益应用的实例包括高剂量的全身性治疗,以及高浓度的局部治疗。
在一个实施方式中,条件性活性嵌合抗原受体可包含抗原特异性靶向区,其与野生型蛋白或其结构域的抗原特异性靶向区相比,在正常生理条件下与靶抗原结合的亲和力降低。
在一个实施方式中,条件性活性嵌合抗原受体可包含抗原特异性靶向区,其与野生型蛋白或其结构域的抗原特异性靶向区相比,在异常条件下在测定中活性增加,且与野生型蛋白或其结构域的抗原特异性靶向区相比,在正常生理条件下与靶抗原结合的亲和力降低。
在一些实施方式中,条件性活性嵌合抗原受体可以包含抗原特异性靶向区,其与野生型蛋白或其结构域的抗原特异性靶向区相比,在异常条件下在测定中选择性增加。
在一些实施方式中,本公开的条件性活性fn3car包含连接一个或多个抗原特异性靶向区的接头。接头以使fn3car上的两个抗原特异性靶向区表现出改善的或最佳的结合靶抗原的活性的方式来定向两个抗原特异性靶向区(jensenandriddell,immunol.rev.(2014)257(1):127-144)。因此,接头能够采用特定构象,所述构象能够使得两个抗原特异性靶向区与靶抗原的结合改善或达到最佳,从而提高了fn3car-t细胞的效力。
在一些实施方式中,接头可以是长度为18-25个氨基酸的gly-ser串联重复序列(grada等,mol.ther.nucleicacids(2013)2:e105)。该柔性接头能够采用用于用于结合靶抗原的两个抗原特异性靶向区改善或优化的呈现的许多不同的构象。
在一些实施方式中,接头能够在正常生理条件和异常条件下采用不同的构象。特别地,接头在异常条件下具有第一构象,所述第一构象对于呈现用于结合靶抗原的两个抗原特异性靶向区是改善的或最佳的,而相同的接头在正常生理条件下具有第二构象,所述第二构象相比于接头在异常条件下的第一构象对于呈现用于结合靶抗原的两个抗原特异性靶向区是更不有效的。这样的接头可以称为“条件性接头”,其允许两个抗原特异性靶向区在异常条件下以比在正常生理条件下更高的结合活性结合靶抗原。因此,包括这样的条件性接头的fn3car-t细胞在异常条件下比在正常生理条件下的相同fn3car-t细胞具有更高的活性。
在不同ph下改变构象的蛋白质是本领域已知的,例如参见dirusso等,ploscomput.biol.(2012)8(11):e1002761。在不同温度下具有不同构象的蛋白质是本领域已知的,参见例如caldwell,plantphysiol.(1987)84(3):924-929。受ph和/或温度影响的抗体的构象已经在例如gandhi,universityofrhodeislandmaster’sthesis,u.s.(2002)中讨论。
在一些实施方式中,选择条件性接头以用于本公开的条件性活性car分子。条件性接头可以在异常条件下采用第一构象,所述第一构象对于呈现用于结合靶抗原的一个或多个抗原特异性靶向区是改善的或最佳的,并且在正常生理条件下采用第二构象,所述第二构象对于呈现用于结合靶抗原的一个或多个抗原特异性靶向区是次优的。在一些实施方式中,接头在正常生理条件下的次优构象产生条件性活性fn3car分子,其与靶抗原的结合活性小于具有接头在异常条件下改善的或最佳的构象的条件性活性fn3car分子的结合活性的约90%、或约80%、或约70%、或约60%、或约50%、或约40%、或约30%、或约20%、或约10%、或约5%。
条件性接头可从选自以下的起始接头产生:2a接头,2a样接头,细小核糖核酸病毒2a样接头,猪捷申病毒(p2a)的2a肽,和thoseaasigna病毒(t2a)的2a肽,及其变体和功能等同物。起始接头演化产生突变蛋白。然后将突变蛋白在正常生理条件下进行测定和在异常条件下进行测定。
从突变蛋白质基于以下选择具有条件性接头的蛋白质:选择的蛋白质表现出:(a)在异常条件下具有第一构象的条件性接头,其对于呈现用于结合靶抗原的两个抗原特异性靶向区是改善的或最佳的,和(b)条件性接头在正常生理条件下的第二构象,其对于呈现用于结合靶抗原的两个抗原特异性靶向区是次优的。
在一些实施方式中,胞外间隔结构域能够在正常生理条件和异常条件下采用不同的构象。特别地,胞外间隔结构域在异常条件下具有第一构象,所述第一构象对于呈现用于结合靶抗原的一个或多个与抗原特异性靶向区是改善的或最佳的,而相同的胞外间隔结构域在正常生理条件下具有第二构象,所述第二构象对于呈现用于结合靶抗原的一个或多个抗原特异性靶向区是次优的。这样的胞外间隔结构域可以被称为“条件性胞外间隔结构域”,因为它使一个或多个抗原特异性靶向区能够在异常条件下以比在正常生理条件下更高的结合活性结合靶抗原。因此,利用条件性胞外间隔结构域,fn3car-t细胞可以在异常条件下比相同fn3car-t细胞在正常生理条件下具有更大的活性。
在一些实施方式中,选择条件性细胞外间隔结构域以用于本公开的条件性活性的fn3car分子。在一些实施方式中,在正常生理条件下胞外间隔结构域的次优构象产生条件性活性fn3car分子,其与靶抗原的结合活性小于具有相同胞外间隔结构域在异常条件下的最佳构象的fn3car分子的约90%、或约80%、或约70%、或约60%、或约50%、或约40%、或约30%、或约20%、或约10%、或约5%。
已经发现,包含胞外间隔结构域和跨膜结构域的区域的泛素化抗性形式可以增强fn3car-t细胞信号传导并因此增强抗肿瘤活性(参见例如kunii等,hum.genether.(2013)24(1):27-37)。在该区域内,胞外间隔结构域位于fn3car-t细胞外部,因此暴露于不同条件下,并可以潜在地被使得具有条件性泛素化抗性。在一些实施方式中,胞外间隔结构域具有条件性泛素化抗性。在一个实施方式中,本公开的条件性活性fn3car分子的胞外间隔结构域在异常条件下比在正常生理条件下具有更大的泛素化抗性。因此,相对于其在正常生理条件下的细胞毒性,具有条件性泛素化抗性的胞外间隔结构域的fn3car-t细胞在异常条件下将具有增强的细胞毒性。
可以选择具有条件性泛素化抗性的胞外间隔结构域是在异常ph或异常温度下具有更大的泛素化抗性,而在正常生理ph或正常生理温度下具有更小的泛素化抗性。在一个实施方式中,具有条件性泛素化抗性的胞外间隔结构域在肿瘤微环境的ph下具有更大的泛素化抗性,而在正常生理ph(例如人血浆中的ph7.2-7.6)下具有更小的泛素化抗性。
为了产生条件性胞外间隔结构域,演化选自抗体的fc片段、抗体的铰链区、抗体的ch2区和抗体的ch3区的起始蛋白片段以产生突变蛋白。对突变蛋白进行正常生理条件下的测定和异常条件下的测定。条件性胞外间隔结构域选自:表现出以下的突变蛋白:(a)条件性胞外间隔结构域,其在异常条件下具有第一构象,所述第一构象用于使抗原特异性靶向区以更高的结合活性结合靶抗原,且条件性细胞外结合结构域在正常生理条件下具有第二构象,所述第二构象用于使抗原特异性靶向区以比在异常条件下更低的结合活性结合靶抗原;或蛋白,其(b)在异常条件下比在正常生理条件下具有更大的泛素化抗性。参见例如,pct公开号wo2017034615a1,其全部内容通过引用并入本文。
另外,本公开的嵌合抗原受体可以被配置为使得含有抗原受体的蛋白相比于野生型蛋白或其结构域表达水平增加。
在一个实施方式中,本发明提供了一种用于结合靶抗原的嵌合抗原受体,所述嵌合抗原受体包含演化自野生型蛋白或其结构域且相比于野生型蛋白或其结构域的抗原特异性靶向区在异常条件下在测定中选择性增加的至少一个抗原特异性靶向区;跨膜结构域;和胞内信号传导结构域。在一些实施方式中,嵌合抗原受体还包含胞外间隔结构域或至少一个共刺激结构域。
本公开还涉及演化野生型蛋白或其结构域(例如纤连蛋白3型结构域多肽)以产生具有以下中的至少一者的条件性活性蛋白的方法:(a)与所述野生型蛋白或其结构域的抗原特异性靶向区相比,在正常生理条件下在测定中活性减少;和(b)与所述野生型蛋白或其结构域的抗原特异性靶向区相比,在异常条件下在测定中活性增加。可以将条件性活性蛋白(例如,条件性活性纤连蛋白3型结构域多肽)工程化到car中。
通过所述方法产生的嵌合抗原受体可以包含至少一个抗原特异性靶向区,其与野生型蛋白或其结构域的抗原特异性靶向区相比在正常生理条件下与靶抗原结合的亲和力降低。
通过所述方法产生的嵌合抗原受体可以包含抗原特异性靶向区,其与野生型蛋白或其结构域的抗原特异性靶向区相比在异常条件下在测定中活性增加,而与野生型蛋白或其结构域的抗原特异性靶向区相比在正常生理条件下与靶抗原结合的亲和力降低。
在通过所述方法产生的任何嵌合抗原受体中,抗原特异性靶向区相比于野生型蛋白或其结构域的抗原特异性靶向区在异常条件下在测定中的选择性也可增加。
在通过所述方法产生的任何嵌合抗原受体中,可以配置fn3car使得包含抗原受体的蛋白与野生型蛋白质或其结构域相比表达水平增加。
在一个实施方式中,通过所述方法产生的用于结合靶抗原的嵌合抗原受体包含演化自野生型蛋白或其结构域且相比于所述野生型蛋白或其结构域的抗原特异性靶向区在异常条件下在测定中选择性增加的至少一个抗原特异性靶向区;跨膜结构域;和胞内信号传导结构域。在一些实施方式中,嵌合抗原受体还包含胞外间隔结构域或至少一个共刺激结构域。
修饰
本公开的fn3car可以用修饰的接头合成,使得另外的功能性部分可以连接至该fn3car。修饰的接头允许例如任何巯基反应性部分的连接。在一个实施方式中,将n-琥珀酰亚胺基-s-乙酰基硫代乙酸酯(sata)连接至双马来酰亚胺以形成双马来酰亚胺基-乙酰基硫代乙酸酯(bmata)。在对被掩蔽的巯基进行脱保护之后,可以将具有巯基反应性(或硫醇基反应性)部分的任何官能团连接至fn3car。
示例性的硫醇反应性试剂包括多功能接头试剂、捕获剂(即亲和性标记试剂(例如生物素接头试剂)、检测标记(例如荧光团试剂)、固相固定试剂(例如sepharosetmtm、聚苯乙烯或玻璃)或药物-接头中间体。硫醇反应性试剂的一个实例是n-乙基马来酰亚胺(nem)。这样的具有修饰的接头的fn3car可以进一步与药物部分试剂或其他标记反应。fn3car与药物-接头中间体的反应可提供fn3car-药物缀合物。
本公开的fn3car可以进一步包含一个或多个另外的多肽结构域,其中这样的结构域包括但不限于信号序列;表位标签;亲和结构域;以及产生可检测信号的多肽。
在一些实施方式中,主题fn3car可以包含信号序列。适用于主题fn3car中的信号序列包括任何真核信号序列,包括天然存在的信号序列、合成(例如人造)信号序列等。
在一些实施方式中,主题fn3car可包含表位标签。合适的表位标签包括但不限于血凝素(ha;例如,ypydvpdya(seqidno:24);flag(例如,dykddddk(seqidno:25);c-myc(例如,eqkliseedl;seqidno:26)等。
在一些实施方式中,主题fn3car可包含亲和结构域。亲和结构域包括可与结合伴体(partner)相互作用的肽序列,例如,诸如固定在固体支持物上的结合伴体,可用于鉴定或纯化。当与表达的蛋白质融合时,编码多个连续的单氨基酸(如组氨酸)的dna序列可用于通过与树脂柱(如镍琼脂糖)的高亲和力结合一步纯化重组蛋白。示例性亲和结构域包括his5(hhhhh)(seqidno:27)、hisx6(hhhhhh)(seqidno:28)、c-myc(eqkliseedl)(seqidno:26)、flag(dykddddk)(seqidno:25)、streptag(wshpqfek)(seqidno:29)、血凝素,例如ha标签(ypydvpdya)(seqidno:24)、gst、硫氧还蛋白、纤维素结合结构域、ryirs(seqidno:30)、phe-his-his-thr(seqidno:31)、几丁质结合结构域、s-肽、t7肽、sh2结构域、c端rna标签、weaaareaccreccara(seqidno:32)、金属结合结构域,例如锌结合结构域或钙结合结构域,如来自钙结合蛋白的那些(例如钙调蛋白、肌钙蛋白c、钙调神经磷酸酶b、肌球蛋白轻链、恢复蛋白、s-调节蛋白、视锥蛋白、vilip、神经钙蛋白、河马钙结合蛋白、聚集蛋白、钙牵蛋白、钙蛋白酶大亚基、s100蛋白、小白蛋白、钙结合蛋白d9k、钙结合蛋白d28k和钙网膜蛋白)、内含额肽类、生物素、链霉亲和素、myod、id、亮氨酸拉链序列和麦芽糖结合蛋白,等。
在一些实施方式中,主题fn3car可包含产生可检测信号的多肽。合适的产生可检测信号的蛋白包括,例如荧光蛋白;催化产生可检测信号作为产物的反应的酶;等等。合适的荧光蛋白包括但不限于绿色荧光蛋白(gfp)或其变体、gfp的蓝色荧光变体(bfp)、gfp的青色荧光变体(cfp)、gfp的黄色荧光变体(yfp)、增强的gfp(egfp)、增强的cfp(ecfp)、增强的yfp(eyfp)、gfps65t、emerald、topaz(tyfp)、venus、citrine、mcitrine、gfpuv、去稳定的egfp(degfp)、去稳定的ecfp(decfp)、去稳定的eyfp(deyfp)、mcfpm、cerulean、t-sapphire、cypet、ypet、mko、hcred、t-hcred、dsred、dsred2、dsred-单体、j-red、dimer2、t-dimer2(12)、mrfp1、pocilloporin、renillagfp、monstergfp、pagfp、kaede蛋白和kindling蛋白、藻胆蛋白和藻胆蛋白缀合物,包括b-藻红蛋白、r-藻红蛋白和别藻蓝蛋白。荧光蛋白的其他实例包括mhoneydew、mbanana、morange、dtomato、tdtomato、mtangerine、mstrawberry、mcherry、mgrape1、mraspberry、mgrape2、mplum(shaner等,naturemethods(2005)2:905-909)等。如例如matz等,naturebiotechnol.(1999)17:969-973中所描述的多种荧光和彩色蛋白中的任一种。合适的酶包括但不限于辣根过氧化物酶(hrp)、碱性磷酸酶(ap)、β-半乳糖苷酶(gal)、葡萄糖-6-磷酸脱氢酶、β-n-乙酰基氨基葡糖苷酶、β-葡萄糖醛酸酶、蔗糖酶、黄嘌呤氧化酶、萤火虫荧光素酶、葡萄糖氧化酶(go)等。
核酸
本公开提供了编码用于与靶抗原结合的嵌合抗原受体的核酸,所述嵌合抗原受体包含包含纤连蛋白3型结构域多肽的至少一个抗原特异性靶向区。
在一些实施方式中,主题核酸用于例如在哺乳动物细胞中产生本公开的fn3car。在一些实施方式中,主题核酸用于编码fn3car的核酸的扩增。
在一些实施方式中,可以将编码本公开的fn3car的主题核酸可操作地连接至转录控制元件,例如启动子和增强子等。合适的启动子和增强子元件是本领域已知的。为了在细菌细胞中表达,合适的启动子包括但不限于laci、lacz、t3、t7、gpt、λp和trc。为了在真核细胞中表达,合适的启动子包括但不限于轻链和/或重链免疫球蛋白基因启动子和增强子元件;巨细胞病毒立即早期启动子;单纯疱疹病毒胸苷激酶启动子;早期和晚期sv40启动子;存在于逆转录病毒长末端重复序列中的启动子;小鼠金属硫蛋白-i启动子;和各种本领域已知的组织特异性启动子。合适的可逆启动子(包括可逆诱导型启动子)是本领域已知的。这样的可逆启动子可以从许多生物体分离和衍生,例如真核生物和原核生物。用于第二生物体的衍生自第一生物体的可逆启动子修饰,例如第一原核生物和第二真核生物,第一真核生物和第二真核生物等,是本领域众所周知的。这样的可逆启动子以及基于这样的可逆启动子但还包含另外的控制蛋白的系统包括但不限于醇调控启动子(例如,醇脱氢酶i(alca)基因启动子、对醇反式激活蛋白(a1cr)有响应的启动子等)、四环素调控的启动子(例如,包括tetactivators、teton、tetoff等的启动子系统)、类固醇调控的启动子(例如,大鼠糖皮质激素受体启动子系统、人雌激素受体启动子系统、类视黄醇启动子系统、甲状腺启动子系统、蜕皮激素启动子系统、米非司酮启动子系统等)、金属调控的启动子(例如金属硫蛋白启动子系统等)、疾病发生相关调控的启动子(例如水杨酸调控的启动子、乙烯调控的启动子、苯并噻二唑调控的启动子等)、温度调控的启动子(例如,热休克诱导型启动子(例如,hsp-70、hsp-90、大豆热休克启动子等)、光调控的启动子、合成诱导型启动子,等。
在一些实施方式中,含有合适启动子的基因座或构建体或转基因通过诱导型系统的诱导不可逆地切换。用于不可逆切换的诱导的合适系统是本领域众所周知的,例如,不可逆切换的诱导可利用cre-lox介导的重组(参见,例如,fuhrmann-benzakein等,proc.natl.acad.sci.usa(2000)28:e99,其公开内容通过引用并入本文)。本领域已知的重组酶、核酸内切酶、连接酶、重组位点等的任何合适的组合可用于产生可不可逆切换的启动子。本文其他地方描述的用于进行位点特异性重组的方法/机制和要求可用于产生不可逆切换的启动子并且是本领域众所周知的,参见例如grindley等,annualreviewofbiochemistry(2006)567-605;和tropp,molecularbiology(2012)(jones&bartlettpublishers,sudbury,mass.),其公开内容通过引用并入本文。
在一些实施方式中,启动子是cd8细胞特异性启动子、cd4细胞特异性启动子、嗜中性粒细胞特异性启动子或nk特异性启动子。例如,可以使用cd4基因启动子。参见,例如,salmon等,proc.natl.acad.sci.usa(1993)90:7739;和marodon等,(2003)blood101:3416。作为另一个实例,可以使用cd8基因启动子。nk细胞特异性表达可通过使用ncri(p46)启动子来实现;参见例如,eckelhart等,blood(2011)117:1565。
在一些实施方式中,例如,为了在酵母细胞中表达,合适的启动子是组成型启动子,例如adh1启动子、pgk1启动子、eno启动子、pyk1启动子等;或可调节的启动子,例如gal1启动子、gal10启动子、adh2启动子、phos启动子、cup1启动子、galt启动子、met25启动子、met3启动子、cyc1启动子、his3启动子、adh1启动子、pgk启动子、gapdh启动子、adc1启动子、trp1启动子、ura3启动子、leu2启动子、eno启动子、tp1启动子和aox1(例如,用于毕赤酵母)。合适的载体和启动子的选择完全在本领域普通技术人员的水平内。适用于原核宿主细胞的启动子包括但不限于噬菌体t7rna聚合酶启动子;trp启动子;lac操纵子启动子;杂合启动子,例如lac/tac杂合启动子、tac/trc杂合启动子、trp/lac启动子、t7/lac启动子;trc启动子;tac启动子等;arabad启动子;体内调控的启动子,如ssag启动子或相关启动子(参见例如,美国专利公开号20040131637)、pagc启动子(pulkkinen和miller,j.bacteriol.(1991)173(1):86-93;alpuche-aranda等,proc.natl.acad.sci.usa(1992)89(21):10079-83)、nirb启动子(harborne等,mol.micro.(1992)6:2805-2813)等(参见例如,dunstan等,infect.immun.(1999)67:5133-5141;mckelvie等,vaccine(2004)22:3243-3255;和chatfield等,biotechnol.(1992)10:888-892);σ70启动子,例如共有σ70启动子(参见,例如genbank登录号ax798980、ax798961和ax798183);固定相启动子,例如dps启动子、spv启动子等;衍生自致病岛spi-2的启动子(参见例如wo96/17951);acta启动子(参见例如shetron-rama等,infect.immun.(2002)70:1087-1096);rpsm启动子(参见例如valdivia和falkow,mol.microbiol.(1996)22:367);tet启动子(参见例如hillen,w.和wissmann,a.(1989),saenger,w.和heinemann,u.(eds),topicsinmolecularandstructuralbiology,protein--nucleicacidinteraction.macmillan,英国伦敦,第10卷,第143-162页);sp6启动子(参见例如,melton等,nucl.acidsres.(1984)12:7035);等等。用于原核生物如大肠杆菌的合适的强启动子包括但不限于trc、tac、t5、t7和plambda。用于细菌宿主细胞的操纵子(operator)的非限制性例子包括乳糖启动子操纵子(当与乳糖接触时,laci阻遏蛋白改变构象,从而防止lad阻遏蛋白与操纵子结合)、色氨酸启动子操纵子(与色氨酸复合时,trpr阻遏蛋白具有结合该操纵子的构象;在不存在色氨酸的情况下,trpr阻遏蛋白具有不结合该操纵子的构象)和tac启动子操纵子(参见例如,deboer等,proc.natl.acad.sci.usa(1983)80:21-25)。
在一些实施方式中,编码主题fn3car的多核苷酸序列进一步包含编码fn3car诱导表达盒的多核苷酸序列。在一个实施方式中,fn3car诱导表达盒用于产生在car信号传导时释放的转基因多肽产物。参见例如chmielewski和abken的expertopin.biol.ther.(2015)15(8):1145-1154;和abken,immunotherapy(2015)7(5):535-544。在一些实施方式中,编码主题fn3car的多核苷酸序列进一步包含编码与t细胞激活响应性启动子可操作地连接的细胞因子的多核苷酸序列。在一些实施方式中,与t细胞激活响应性启动子可操作地连接的细胞因子存在于单独的多核苷酸序列上。在一个实施方式中,细胞因子是il-12。
编码主题fn3car的核苷酸序列可以存在于表达载体和/或克隆载体中。表达载体可以包括可选择标志物、复制起点和用于载体复制和/或维持的其他特征。合适的表达载体包括例如质粒、病毒载体等。大量合适的载体和启动子是本领域技术人员已知的;许多可商购用于产生主题重组构建体。以下载体通过举例提供:细菌:pbs、phagescript、psix174、pbluescriptsk、pbsks、pnh8a、pnh16a、pnh18a、pnh46a(stratagene,lajolla,calif.,usa);ptrc99a、pkk223-3、pkk233-3、pdr540和prit5(pharmacia,uppsala,sweden)。真核生物:pwlneo、psv2cat、pog44、pxr1、psg(stratagene)psvk3、pbpv、pmsg和psvl(pharmacia)。
表达载体通常具有位于启动子序列附近的便利的限制性位点以用于编码异源蛋白的核酸序列的插入。可以存在在表达宿主中有效的可选择标志物。合适的表达载体包括但不限于病毒载体(例如基于以下的病毒载体:痘苗病毒;脊髓灰质炎病毒;腺病毒(参见,例如,li等,invest.opthalmol.vis.sci.(1994)35:2543-2549;borras等,genether.(1999)6:515-524;li和davidson,proc.natl.acad.sci.usa(1995)92:7700-7704;sakamoto等,h.genether.(1999)5:1088-1097;wo94/12649、wo93/03769;wo93/19191;wo94/28938;wo95/11984和wo95/00655);腺相关病毒(参见例如,ali等,hum.genether.(1998)9:81-86,flannery等,proc.natl.acad.sci.usa(1997)94:6916-6921;bennett等,invest.opthalmol.vis.sci.(1997)38:2857-2863;jomary等,genether.(1997)4:683-690,rolling等,hum.genether.(1999)10:641-648;ali.等,hum.mol.genet.(1996)5:591-594;srivastava,wo93/09239,samulski等,j.vir.(1989)63:3822-3828;mendelson等,virol.(1988)166:154-165;和flotte等,proc.natl.acad.sci.usa(1993)90:10613-10617);sv40;单纯疱疹病毒;人免疫缺陷病毒(参见例如,miyoshi等,proc.natl.acad.sci.usa(1997)94:10319-23;takahashi等,j.virol.(1999)73:7812-7816);逆转录病毒载体(例如鼠白血病病毒、脾坏死病毒以及衍生自逆转录病毒如劳斯肉瘤病毒、哈维肉瘤病毒、禽白血病病毒、人免疫缺陷病毒、骨髓增生性肉瘤病毒和乳腺肿瘤病毒的载体),等等。
适用的另外的表达载体是,例如但不限于,慢病毒载体、γ逆转录病毒载体、泡沫病毒载体、腺相关病毒载体、腺病毒载体、痘病毒载体、疱疹病毒载体、工程化杂交病毒载体、转座子介导的载体等。
在一些实施方式中,编码本公开的主题fn3car的核酸在一些实施方式中是rna,例如体外合成的rna。rna的体外合成方法是本领域已知的;可以使用任何已知方法来合成包含编码本发明的fn3car的序列的rna。用于将rna引入宿主细胞中的方法是本领域已知的。参见例如,zhao等,cancerres.(2010)15:9053。可以在体外或离体或在体内将包含编码本公开的fn3car的核苷酸序列的rna引入宿主细胞。例如,宿主细胞(例如,nk细胞、细胞毒性t淋巴细胞等)可以用包含编码本公开的fn3car的核苷酸序列的rna在体外或离体电穿孔。
工程化细胞
本公开的嵌合抗原受体可以通过连接编码个体结构域的多核苷酸序列来组装以形成单个多核苷酸序列(fn3car基因,其编码本公开的fn3car)。个体结构域包括包含纤连蛋白3型结构域多肽、tm和isd的至少一个astr。在一些实施方式中,其他结构域也可以引入fn3car中,包括esd和csd。如果fn3car是多特异性car,则fn3car基因可以例如沿n端至c端方向处于以下构型中:n端信号序列-astr1-接头-astr2-胞外间隔结构域-跨膜结构域-共刺激结构域-胞内信号传导结构域。在一个实施方式中,这样的fn3car基因可以包含两个或更多个共刺激结构域。
在一些实施方式中,编码fn3car的多核苷酸序列可以沿n端至c端方向处于以下构型中:n端信号序列-astr1-接头-astr2-跨膜结构域-共刺激结构域-胞内信号传导结构域。在一个实施方式中,这样的fn3car可以包含两个或更多个共刺激结构域。如果fn3car包含多于两个astr,则编码fn3car的多核苷酸序列沿n端至c端方向可以处于以下构型中:n端信号序列-astr1-接头-astr2-接头-(抗原特异性靶向区)n-跨膜结构域-共刺激结构域-胞内信号传导结构域,其中n是至少1的整数。这样的fn3car可以进一步包含胞外间隔结构域。每个astr可以由接头分隔。在一个实施方式中,这样fn3car可以包含两个或更多个共刺激结构域。
在一些实施方式中,条件性活性的fn3car通过表达载体引入细胞(例如,细胞毒性细胞)中。本文提供了包括编码本发明的条件性活性fn3car的多核苷酸序列的表达载体。合适的表达载体包括慢病毒载体、γ逆转录病毒载体、泡沫病毒载体、腺相关病毒(aav)载体、腺病毒载体、工程化杂交病毒、裸dna,包括但不限于转座子介导的载体,如sleepingbeauty、piggybak和integrases如phi31。一些其他合适的表达载体包括单纯疱疹病毒(hsv)和逆转录病毒表达载体。
腺病毒表达载体基于腺病毒,其具有低的用于整合到基因组dna中的能力,但具有高的用于转染宿主细胞的效率。腺病毒表达载体包含足以实现以下的腺病毒序列:(a)支持表达载体的包装和(b)最终在宿主细胞中表达fn3car基因。在一些实施方式中,腺病毒基因组是36kb的线性双链dna,其中外源dna序列(例如fn3car基因)可插入以替代大的腺病毒dna片段,以制备本发明的表达载体(参见例如danthinne和imperiale,genetherapy(2000)7(20):1707-1714)。
另一种表达载体是基于腺相关病毒,其利用了腺病毒偶联系统。这种aav表达载体具有高的整合到宿主基因组中的频率。它可以感染非分裂的细胞,因此使得其可用于将基因递送到哺乳动物细胞中,例如在组织培养物中或在体内。aav载体具有广泛的感染宿主范围。关于aav载体的产生和使用的细节在美国专利号5,139,941和4,797,368中描述。
逆转录病毒表达载体能够整合到宿主基因组中、递送大量外来遗传物质、感染广谱的物种和细胞类型和包装在特殊的细胞系中。逆转录病毒载体通过将核酸(例如,编码fn3car的核酸)在某些位置处插入病毒基因组中以产生复制缺陷病毒来构建。尽管逆转录病毒载体能够感染广泛多样的细胞类型,但fn3car基因的整合和稳定表达需要宿主细胞的分裂。
慢病毒载体源自复杂的逆转录病毒的慢病毒,除了常见的逆转录病毒基因gag、pol和env之外,还包含具有调节或结构性功能的其他基因(参见例如,美国专利号6,013,516和5,994,136)。慢病毒的一些实例包括人类免疫缺陷病毒(hiv-1、hiv-2)和猿猴免疫缺陷病毒(siv)。慢病毒载体是通过多重减弱hiv毒力基因产生的,例如,缺失env、vif、vpr、vpu和nef基因,使得载体具有生物学上的安全性。慢病毒载体能够感染非分裂的细胞,并且可以用于体内和离体基因转移以及fn3car基因的表达(参见例如,美国专利号5,994,136)。
可以通过本领域技术人员已知的任何方式将包含条件性活性的fn3car基因的表达载体引入宿主细胞。如果需要,表达载体可以包括用于转染的病毒序列。或者,表达载体可以通过融合、电穿孔、基因枪、转染、脂转染等引入。在引入表达载体之前,可以使宿主细胞在培养中生长和扩增,然后进行适当的处理用于引入和整合载体。宿主细胞然后扩增和借助载体中存在的标志物进行筛选。可以使用的各种标志物是本领域已知的,并且可以包括hprt、新霉素抗性、胸苷激酶、潮霉素抗性等。如本文所用,术语“细胞”、“细胞系”和“细胞培养物”可以是可互换使用的。在一些实施方式中,宿主细胞是t细胞、nk细胞或nkt细胞。
本发明还提供了基因工程化细胞(例如,细胞毒性细胞),其包含并稳定表达本公开的嵌合抗原受体。在一些实施方式中,基因工程化细胞是基因工程化t淋巴细胞(t细胞)、幼稚t细胞(tn)、记忆t细胞(例如,中央记忆t细胞(tcm)、效应记忆细胞(tem))、自然杀伤细胞(nk细胞)和能够产生治疗相关后代的巨噬细胞。在一个实施方式中,基因工程化细胞是自体细胞。
合适的t细胞的非限制性实例包括cd4+/cd8"、cd47cd8+、cd47cd8"或cd4+/cd8+t细胞。t细胞可以是例如cd4+/cd8"和cd47cd8"1"细胞的混合群体或者单克隆的群体。本发明的cd4+t细胞也可以在与表达靶抗原的细胞(例如cd20+和/或cd19+肿瘤细胞)在体外共培养时产生il-2、ifn-γ、tnf-α和其他t细胞效应细胞因子。本发明的cd8+t细胞可以裂解表达靶抗原的细胞。在一些实施方式中,t细胞可以是cd45ra+cd62l+幼稚细胞、cd45rocd62i7中央记忆细胞、cd62l效应记忆细胞或其组合中的任何一种或多种(berger等,curr.opin.immunol.(2009)21(2):224-232)。
基因工程化的细胞毒性细胞可以通过用本发明的包含fn3car基因的表达载体稳定转染宿主细胞来产生。使用表达载体对细胞毒性细胞进行基因工程改造的其他方法包括化学转化方法(例如,使用磷酸钙、树状聚合物、脂质体和/或阳离子聚合物)、非化学转化方法(例如,电穿孔、光学转化、基因电转移和/或流体动力学递送)和/或基于颗粒的方法(例如,穿刺转染(impalefection)、使用基因枪和/或磁转染)。证明存在单整合的未重排载体并表达fn3car的转染细胞可以离体扩增。
用于将表达载体引入宿主细胞中的物理方法包括磷酸钙沉淀、脂转染、粒子轰击、显微注射、电穿孔等。产生包含载体和/或外源核酸的细胞的方法是本领域众所周知的。参见,例如,sambrook等.(2001),molecularcloning:alaboratorymanual,coldspringharborlaboratory,newyork。用于将表达载体引入宿主细胞中的化学方法包括胶体分散系统,例如大分子复合物、纳米胶囊、微球、珠和基于脂质的系统,包括水包油乳液、胶束、混合胶束和脂质体。
在一些实施方式中,包含编码主题fn3car的多核苷酸序列的表达载体还包含编码用于在car信号转导时产生和释放的转基因多肽产物的car诱导型表达盒的多核苷酸序列。在一些实施方式中,包含编码主题fn3car的多核苷酸序列的表达载体还包含编码与t细胞激活响应性启动子可操作地连接的细胞因子的多核苷酸序列。在一些实施方式中,将包含编码与t细胞激活响应性启动子可操作地连接的细胞因子的核酸序列的表达载体进一步引入本公开的工程化细胞毒性细胞(例如,包含主题fn3car分子)中。在一个实施方式中,细胞因子是il-12。在这样的实施方式中,表达本公开的fn3car的工程化t细胞能够诱导性或组成性地释放细胞因子(例如,il-12)。在一个实施方式中,t细胞激活响应性启动子是激活的t细胞的核因子(nfat)响应性启动子。在能够诱导性或组成性释放il-12的表达本公开的fn3car的工程化t细胞中,il-12可以累积在例如肿瘤病变中,其在此处至少通过以下方式促进肿瘤破坏:(a)诱导对肿瘤细胞的固有免疫细胞应答,该肿瘤细胞对于重定向的t细胞是不可见的,和(b)触发免疫抑制细胞的程序性变化。这提供了涉及使用fn3car工程化t细胞的另一层策略。参见例如chmielewski和abken,expertopin.biol.ther.(2015)15(8):1145-1154;和abken,immunotherapy(2015)7(5):535-544。
在将包含fn3car基因的表达载体引入宿主细胞中后,表达fn3car基因从而产生可以结合靶抗原的fn3car分子。所产生的fn3car分子至少由于具有跨膜结构域而成为跨膜蛋白。宿主细胞然后转化为fn3car细胞如fn3car-t细胞。例如,在(cartellieri等,j.biomed.biotechnol.(2010)articleid:956304;和ma等,proc.natl.acad.sci.usa(2016)113(4):e450-458)中描述了用于产生具有fn3car分子的工程化细胞毒性细胞,例如fn3car-t细胞的方法。
无论是在对细胞毒性细胞进行遗传修饰以表达所期望的fn3car之前还是之后,细胞都可以使用例如在美国专利号6,352,694;6,534,055;6,905,680;6,692,964;5,858,358;6,887,466;6,905,681;7,144,575;7,067,318;7,172,869;7,232,566;7,175,843;5,883,223;6,905,874;6,797,514;6,867,041;和美国公开号20060121005中所描述的方法激活和数量扩增。例如,本发明的t细胞可以通过与在其上附着有刺激cd3/tcr复合物相关信号的试剂和刺激t细胞表面上的共刺激分子的配体的表面接触而扩增。特别地,t细胞群体可以通过与抗cd3抗体或其抗原结合片段或者固定在表面上的抗cd2抗体接触,或者通过结合钙离子载体与蛋白激酶c激活剂(例如,苔藓抑素)接触来刺激。对于t细胞表面上的辅助分子的共刺激,使用结合辅助分子的配体。例如,可以在适于刺激t细胞增殖的条件下使t细胞与抗cd3抗体和抗cd28抗体接触。为了刺激cd4+t细胞或cd8+t细胞的增殖,抗cd3抗体和抗cd28抗体。抗cd28抗体的实例包括9.3、b-t3、xr-cd28(diaclone,besancon,france),并且这些可以用于本发明中,本领域中已知的其他方法也一样(参见例如tenberge等,transplantproc.(1998)30(8):3975-3977;haanen等,j.exp.med.(1999)190(9):1319-1328;和garland等,j.immunol.methods(1999)227(1-2):53-63)。
组合物
本发明提供了药物组合物,其包含药学上可接受的赋形剂和治疗有效量的本发明的fn3car。组合物中的fn3car可以是编码fn3car的多核苷酸、包含fn3car的蛋白或表达fn3car蛋白的遗传修饰细胞中的任一种或多种。
药学上可接受的赋形剂可以包括可用于制备通常安全、无毒且期望的药物组合物的任何赋形剂,并且包括兽医学使用以及人类药用可接受的赋形剂。一种类型的赋形剂包括药学上可接受的载体,其可以加入以增强或稳定组合物,或便于组合物的制备。
药学上可接受的载体部分地取决于所施用的特定组合物以及用于施用该组合物的特定方法。因此,存在本发明药物组合物的多种多样的合适制剂。可以使用多种水性载体,例如缓冲盐水等。这些溶液是无菌的,并且通常不含不期望的物质。这些组合物可以通过常规的、众所周知的灭菌技术进行灭菌。组合物可以包含模拟生理条件所需的药学上可接受的辅助物质,例如ph调节剂和缓冲剂、毒性调节剂等,例如乙酸钠、氯化钠、氯化钾、氯化钙、乳酸钠等。这些制剂中fn3car的浓度可以广泛变化,并且根据所选择的特定施用方式和患者的需要,主要基于流体体积、粘度和体重进行选择。
药物组合物可以配制用于肠胃外施用,例如通过关节内(在关节中)、静脉内、肌肉内、真皮内、腹膜内和皮下途径,包括水性和非水性的、等渗的无菌注射溶液,其可以包含抗氧化剂、缓冲剂、抑菌剂和使制剂与预期受体的血液等渗的溶质;以及水性和非水性无菌混悬液,其可以包含悬浮剂、增溶剂、增稠剂、稳定剂和防腐剂,在本发明的实践中,组合物可以例如通过静脉内输注、口服、局部、腹膜内、膀胱内或鞘内方式施用。在一个实施方式中,肠胃外施用方式是用于施用包含fn3car蛋白或基因工程细胞毒性细胞的组合物的优选施用方法。组合物可以方便地以单位剂型施用,并且可以通过药学领域公知的任何方法制备,例如,如remington'spharmaceuticalsciences,mackpublishingco.eastonpa.,第18版,1990中所述的。用于静脉内施用的制剂可以包含药学上可接受的载体,例如无菌水或盐水、聚亚烷基二醇如聚乙二醇、植物来源的油、氢化萘等。
药物组合物可以通过选自肠胃外、皮下、肌内、静脉内、关节内(intrarticular)、支气管内、腹内、囊内、软骨内、腔内、体腔内、小脑内(intracelebellar)、脑室内、结肠内、宫颈内、胃内、肝内、心肌内、骨内、骨盆内、心包内、腹膜内、胸膜内、前列腺内、肺内、直肠内、肾脏内、视网膜内、脊柱内、滑膜腔内、胸内、子宫内、膀胱内、浓注(bolus)、阴道、直肠、颊、舌下、鼻内或经皮。该方法可以任选地进一步包括在主题car之前、同时或之后施用至少一种包含有效量的至少一种选自以下的化合物或蛋白的组合物:可检测标记或报告子、tnf拮抗剂、抗风湿药、肌肉松弛药、麻醉药、非类固醇抗炎药(nsak)、镇痛药、麻醉剂、镇静药、局部麻醉剂、神经肌肉阻断剂、抗微生物药、抗牛皮癣药、皮质类固醇、合成代谢类固醇、促红细胞生成素、免疫、免疫球蛋白、免疫抑制剂、生长激素、激素替代药物、放射性药物、抗抑郁药、抗精神病药、兴奋剂、哮喘药物、β激动剂、吸入类固醇、肾上腺素或其类似物、细胞毒性或其他抗癌药、抗代谢物(如甲氨蝶呤)或抗增殖剂。
治疗方法
当存在于t淋巴细胞或nk细胞中时,本公开的fn3car可以介导对靶细胞的细胞毒性。本公开的fn3car与存在于靶细胞上的抗原结合,从而介导遗传修饰以产生fn3car的t淋巴细胞或nk细胞对靶细胞的杀伤。fn3car的抗原结合结构域与靶细胞表面上存在的抗原结合。靶细胞包括但不限于癌细胞,例如血液癌细胞、实体肿瘤细胞等。因此,本公开提供了杀死靶癌细胞或抑制其生长的方法,所述方法包括接触经遗传修饰以产生主题fn3car的细胞毒性免疫效应细胞(例如,细胞毒性t细胞或nk细胞),使得该t淋巴细胞或nk细胞识别靶癌细胞表面上存在的抗原,并介导靶细胞的杀伤。
本公开提供了一种在患有癌症的受试者中治疗癌症的方法,所述方法包括:i)将本公开的嵌合抗原受体引入或者将本公开的表达载体引入细胞中,以产生工程化细胞;和ii)将所述工程化细胞施用于受试者。在一些实施方式中,细胞从受试者获得,离体工程化并施用于相同受试者。在一些实施方式中,细胞从一个受试者获得,离体工程化并施用于第二个合适的受试者。
在一些实施方式中,本发明提供了一种方法,所述方法包括从受试者获取细胞毒性细胞,通过将本发明的fn3car基因引入所述细胞毒性细胞中而对所述细胞毒性细胞进行基因工程化,以及将基因工程化的细胞毒性细胞施用于受试者。在一些实施方式中,细胞毒性细胞选自t细胞、幼稚t细胞、记忆t细胞、效应t细胞、自然杀伤细胞和巨噬细胞。在一个实施方式中,细胞毒性细胞是t细胞。
在一个实施方式中,t细胞获自受试者。t细胞可从多个来源获得,包括外周血单核细胞、骨髓、淋巴结组织、脐带血、胸腺组织、来自感染部位的组织、腹水、胸腔积液、脾脏组织和肿瘤。在本发明的一些实施方式中,可以使用本领域可获得的任何数量的t细胞系。在本发明的一些实施方式中,可以使用本领域技术人员已知的多种技术,例如ficolltm分离,从自受试者收集的血液中获得t细胞。
在一个实施方式中,通过单采血液分离术(apheresis)获得来自个体循环血液的细胞。单采血液分离术产物通常包含淋巴细胞,包括t细胞、单核细胞、粒细胞、b细胞、其他有核白细胞、红细胞和血小板。在一个实施方式中,可以洗涤通过单采血液分离术收集的细胞以除去血浆级分和将细胞置于适当的缓冲液或培养基中用于后续处理步骤。在本发明的一个实施方式中,细胞用磷酸盐缓冲盐水(pbs)洗涤。在一个实施方式中,洗涤溶液缺乏钙并且可以缺乏镁或可以缺乏许多(如果不是全部的话)二价阳离子。如本领域普通技术人员容易理解的,洗涤步骤可以通过本领域技术人员已知的方法来完成,如通过按照制造商的说明使用半自动“流通式”离心机(例如cobe2991细胞处理器、baxtercytomate或haemoneticscellsaver5)。洗涤后,可将细胞重悬于多种生物相容的缓冲液中,例如无ca2+、无mg2+的pbs、plasmalytea或另一种含或不含缓冲剂的盐水溶液。在一些实施方式中,可以去除单采血液分离术样品的不期望的成分,并将细胞直接重悬浮在培养基中。
在一个实施方式中,t细胞通过裂解红细胞并耗尽单核细胞从外周血中分离,例如通过percolltm梯度的离心或通过逆流离心淘析。可以通过正向或负向选择技术进一步分离t细胞的特定亚群,如cd3+、cd28+、cd4+、cd8+、cd45ra+和cd45ro+t细胞。例如,通过负向选择富集t细胞群体可以通过针对负向选择细胞特有的表面标志物的抗体的组合来完成。一种方法是通过负磁性免疫粘附的细胞分选和/或选择或者使用针对存在于负向选择的细胞上存在的细胞表面标志物的单克隆抗体的混合物进行的流式细胞术。为了通过负向选择富集cd4+细胞,单克隆抗体混合物通常包括针对cd14、cd20、cd11b、cd16、hla-dr和cd8的抗体。在一些实施方式中,可能希望富集或正向选择通常表达cd4+、cd25+、cd62lhi、gitr+和foxp3+的调节性t细胞。
例如,在一个实施方式中,t细胞通过与抗cd3/抗cd28(即,3x28)缀合的珠(如
然后如本文所述对获得的细胞进行基因工程化。将通常位于表达载体中的编码fn3car的多核苷酸引入细胞毒性细胞中,以使得细胞毒性细胞表达(优选稳定地表达)fn3car。通常将编码fn3car的多核苷酸整合到细胞毒性细胞的宿主基因组中。在一些实施方式中,编码fn3car的多核苷酸也编码用于在car信号转导时产生和释放的转基因多肽产物的fn3car诱导表达盒。在一些实施方式中,编码fn3car的多核苷酸也编码可操作地连接至t细胞激活响应性启动子的细胞因子(例如il-12)。在一些实施方式中,表达载体包含编码fn3car的多核苷酸和包含编码与t细胞激活响应性启动子可操作连接的细胞因子的多核苷酸两者。参见例如chmielewski和abken,expertopin.biol.ther.(2015)15(8):1145-1154;和abken,immunotherapy(2015)7(5):535-544。在一些实施方式中,用包含编码fn3car的多核苷酸的表达载体和包含编码与t细胞激活响应性启动子可操作地连接的细胞因子(例如il-12)的多核苷酸的表达载体对细胞进行基因工程化。在一些实施方式中,多核苷酸的引入不需要导致整合,而是引入的多核苷酸的仅短暂维持可以是足够的。以此方式,可以具有短期效应,其中细胞毒性细胞可以引入宿主中和然后在预定时间后,例如在细胞能够迁移到特定治疗部位后发动。
取决于细胞毒性细胞的性质和待治疗的疾病,可以以多种方式将基因工程化的细胞毒性细胞引入受试者,例如哺乳动物中。基因工程化的细胞毒性细胞可以在肿瘤部位引入。在一个实施方式中,基因工程化的细胞毒性细胞引导至癌症或经修饰以引导至癌症。所使用的基因工程化细胞毒性细胞的数量将取决于许多因素,例如环境、引入的目的、细胞寿命、待使用的方案。例如,施用次数、细胞增殖的能力以及重组构建体的稳定性。基因工程化的细胞毒性细胞可以作为感兴趣的位点处或附近注射的分散体应用。在一个实施方式中,细胞可以处于生理可接受的培养基中。
应当理解的是,治疗方法受到许多变量的影响,例如对fn3car的细胞响应、细胞毒性细胞表达fn3car的效率和(在适当时)分泌水平、表达的fn3car的活性、受试者的特殊需要(其可能随时间和环境而变化)、由于基因工程化细胞毒性细胞的损失而导致的细胞活性的损失率或个体细胞的表达活性,等等。因此,预期对于每个个体患者,即使存在可以施用于整个群体的通用细胞,也监测每个患者的个体合适剂量,并且这种监测患者的实践是本领域中常规的。
实体肿瘤的当前fn3car靶标(其也适合作为本公开的fn3car的靶标)的非限制性实例包括egfr(egfr+实体肿瘤)、egfrviii(胶质母细胞瘤)、gd2(神经母细胞瘤、尤因肉瘤、骨肉瘤、黑素瘤)、il13rα2(神经胶质瘤)、her2(her2+实体肿瘤)、间皮素(间皮瘤、胰腺癌、卵巢癌)、psma(前列腺癌)、fap(恶性胸膜间皮瘤)、gpc3(肝细胞癌)、met(乳腺癌)、muc16(卵巢癌)、cea(各种实体肿瘤)、lewis-y(实体肿瘤、骨髓恶性肿瘤)、muc1(肝细胞癌、非小细胞肺癌(nsclc)、胰腺癌、三阴性侵入性乳腺癌)。参见例如fesnak等,naturerev.cancer(2016)16:566-581。
血液恶性肿瘤的当前fn3car靶标(其也适合作为本公开的fn3car的靶标)的非限制性实例包括cd19或cd20(白血病、淋巴瘤、多发性骨髓瘤)、cd22(b细胞恶性肿瘤)、igκ轻链(b细胞恶性肿瘤)、cd30(淋巴瘤)、cd138(多发性骨髓瘤)、bcma(多发性骨髓瘤)、cd33(骨髓恶性肿瘤)、cd123(骨髓恶性肿瘤)、nkg2d配体(各种血液恶性肿瘤)、ror1(白血病)。参见,例如,fesnak等,同上。
待用本发明的基因工程化细胞毒性细胞或药物组合物治疗的癌症类型包括癌瘤(carcinomas)、胚细胞瘤和肉瘤,以及某些白血病或淋巴恶性肿瘤、良性和恶性的肿瘤,以及恶性肿瘤(malignancies),例如肉瘤、癌瘤和黑素瘤。癌症可以是非实体肿瘤(例如血液肿瘤)或实体肿瘤。成人肿瘤/癌症和儿科肿瘤/癌症也包括在内。在一个实施方式中,癌症是实体肿瘤或血液肿瘤。在一个实施方式中,癌症是癌瘤。在一个实施方式中,癌症是肉瘤。在一个实施方式中,癌症是白血病。在一个实施方式中,癌症是实体肿瘤。
实体肿瘤是通常不包含囊肿或液体区域的异常组织团块。实体肿瘤可以是良性或恶性的。不同类型的实体肿瘤因形成它们的细胞类型而命名(例如肉瘤、癌瘤和淋巴瘤)。实体肿瘤如肉瘤和癌瘤的实例包括纤维肉瘤、粘液肉瘤、脂肪肉瘤、软骨肉瘤、骨肉瘤和其他肉瘤、滑膜瘤、间皮瘤、尤因氏瘤、平滑肌肉瘤、横纹肌肉瘤、结肠癌、淋巴性恶性肿瘤、胰腺癌、乳腺癌、肺癌、卵巢癌、前列腺癌、肝细胞癌、鳞状细胞癌、基底细胞癌、腺癌、汗腺癌、甲状腺髓样癌、甲状腺乳头状癌、嗜铬细胞瘤、皮脂腺癌、乳头状癌、乳头状腺癌、髓样癌、支气管癌、肾细胞癌、肝癌、胆管癌、绒毛膜癌、威尔姆斯氏肿瘤、宫颈癌、睾丸肿瘤、精原细胞瘤、膀胱癌、黑素瘤和cns肿瘤(如神经胶质瘤(例如脑干神经胶质瘤和混合神经胶质瘤)、成胶质细胞瘤(也称为多形性成胶质细胞瘤)、星形细胞瘤、cns淋巴瘤、生殖细胞瘤、髓母细胞瘤、神经鞘瘤、颅咽管瘤(craniopharyogioma)、室管膜瘤、松果体瘤、血管母细胞瘤、听神经瘤、少突胶质细胞瘤、脑膜瘤(menangioma)、神经母细胞瘤、视网膜母细胞瘤和脑转移瘤)。
可以通过本文公开的方法进行治疗的癌瘤包括但不限于食道癌、肝细胞癌、基底细胞癌(皮肤癌的形式)、鳞状细胞癌(各种组织)、膀胱癌包括移行细胞癌(膀胱的恶性肿瘤)、支气管癌、结肠癌、结肠直肠癌、胃癌、肺癌(包括小细胞肺癌和非小细胞肺癌)、肾上腺皮质癌、甲状腺癌、胰腺癌、乳腺癌、卵巢癌、前列腺癌、腺癌、汗腺癌、皮脂腺癌、乳头状癌、乳头状腺癌、囊腺癌、髓样癌、肾细胞癌、导管原位癌或胆管癌、绒毛膜癌、精原细胞瘤、胚胎性癌、威尔姆斯氏肿瘤、宫颈癌、子宫癌、睾丸癌、骨原癌、上皮癌和鼻咽癌。
可能适用于通过本文公开的方法进行治疗的肉瘤包括但不限于纤维肉瘤、粘液肉瘤、脂肪肉瘤、软骨肉瘤、脊索瘤、成骨肉瘤、骨肉瘤、血管肉瘤、内皮肉瘤、淋巴管肉瘤、淋巴管内皮肉瘤、滑膜瘤、间皮瘤、尤因氏肉瘤、平滑肌肉瘤、横纹肌肉瘤和其他软组织肉瘤。
可能适用于通过本文公开的方法进行治疗的其他实体肿瘤包括但不限于神经胶质瘤、星形细胞瘤、髓母细胞瘤、颅咽管瘤、室管膜瘤、松果体瘤、血管母细胞瘤、听神经瘤、少突神经胶质瘤、脑膜瘤、黑色素瘤、神经母细胞瘤和视网膜母细胞瘤。
在一些实施方式中,实体肿瘤选自纤维肉瘤、粘液肉瘤、脂肪肉瘤、软骨肉瘤、骨肉瘤和其他肉瘤、滑膜瘤、间皮瘤、尤因氏瘤、平滑肌肉瘤、横纹肌肉瘤、结肠癌、淋巴恶性肿瘤、胰腺癌、乳腺癌、肺癌、卵巢癌、前列腺癌、肝细胞癌、鳞状细胞癌、基底细胞癌、腺癌、汗腺癌、甲状腺髓样癌、甲状腺乳头状癌、嗜铬细胞瘤、皮脂腺癌、乳头状癌、乳头状腺癌、髓样癌、支气管癌、肾细胞癌、肝癌、胆管癌、绒毛膜癌、威尔姆斯氏肿瘤、宫颈癌、睾丸肿瘤、精原细胞瘤、膀胱癌、黑色素瘤、神经胶质瘤、成胶质细胞瘤、星形细胞瘤、cns淋巴瘤、生殖细胞瘤、髓母细胞瘤、神经鞘瘤、颅咽管瘤、室管膜瘤、松果体瘤、血管母细胞瘤、听神经瘤、少突胶质细胞瘤、脑膜瘤、神经母细胞瘤、视网膜母细胞瘤和脑转移瘤。
血液癌症是血液或骨髓的癌症。血液(或血源性)癌症的实例包括白血病,包括急性白血病(例如急性淋巴细胞性白血病、急性髓细胞性白血病、急性髓性白血病和成髓细胞性、早幼粒细胞性、髓单核细胞性、单核细胞性和红细胞白血病)、慢性白血病(如慢性髓细胞性(粒细胞性)白血病、慢性髓性白血病和慢性淋巴细胞性白血病)、真性红细胞增多症、淋巴瘤、霍奇金病、非霍奇金淋巴瘤(惰性和高等级形式)、多发性骨髓瘤、华氏巨球蛋白血症、重链疾病、骨髓增生异常综合症、毛细胞白血病和骨髓增生异常。
在一些实施方式中,血液肿瘤选自白血病、真性红细胞增多症、淋巴瘤、霍奇金淋巴瘤、非霍奇金淋巴瘤、多发性骨髓瘤、华氏巨球蛋白血症、重链疾病相关肿瘤、骨髓增生异常综合症相关肿瘤、毛细胞白血病和骨髓增生异常。
可能适用于通过本文公开的方法进行治疗的白血病包括但不限于:a)慢性骨髓增生综合症(多能造血干细胞的肿瘤性疾病);b)急性髓性白血病(多能性造血干细胞或受限谱系潜能的造血细胞的肿瘤转化);c)慢性淋巴细胞性白血病(cll;未免疫成熟且功能不健全的小淋巴细胞的克隆增殖),包括b细胞cll、t-细胞cll前淋巴细胞性白血病和毛细胞白血病;和d)急性淋巴母细胞性白血病(以淋巴母细胞的累积为特征)。可以使用所述方法治疗的淋巴瘤包括但不限于b细胞淋巴瘤(例如burkitt淋巴瘤);霍奇金淋巴瘤;非霍奇金淋巴瘤等。
可能适用于根据本文公开的方法进行治疗的其他癌症包括非典型脑膜瘤(脑)、胰岛细胞癌(胰腺)、髓样癌(甲状腺)、间皮瘤(肠)、肝细胞癌(肝脏)、肝母细胞瘤(肝脏)、透明细胞癌(肾脏)和纵隔神经纤维瘤。
本公开的方法也可以用于治疗炎性病症和自身免疫疾病。所述fn3car在t辅助细胞或tregs中表达用于免疫调节方法。免疫调节方法包括,例如,增强哺乳动物受试者对病原体的免疫应答;在免疫受损的受试者中增强免疫应答;减轻炎症应答;降低哺乳动物受试者中对自身抗原的免疫应答,例如治疗自身免疫疾病;以及降低哺乳动物受试者中对移植的器官或组织的免疫应答以减少器官或组织排斥。
当所述方法涉及降低对自身抗原的免疫应答时,用于激活fn3car的抗原是自身抗原。在所述方法涉及降低对移植的器官或组织的免疫应答的情况下,用于激活fn3car的抗原是对移植的器官具有特异性的抗原。
本文中提及或引用的文章、专利和专利申请以及所有其他文件和电子可得信息的全部内容以引用的方式并入本文,其程度与具体地和单独地指示每个单独的出版物以引用的方式并入一样。申请人保留将来自任何此类文章、专利、专利申请或其他物理和电子文档的任何和所有材料和信息实际并入本申请中的权利。
虽然已经参考本发明的特定实施方式描述了本发明,但是本领域技术人员应当理解,在不脱离本发明的真实精神和范围的情况下,可以进行各种改变并且可以用等同物代替。对于本领域技术人员而言清楚的是,在不脱离本文公开的实施方式的范围的情况下,可以使用适当的等同物对本文所述的方法进行其他适当的修改和改造。另外,可以做出许多修改以使特定情况、材料、物质组成、工艺、一个或多个工艺步骤适应于本发明的目的、精神和范围。所有这些修改旨在落入所附权利要求的范围内。现在已经详细描述了某些实施方式,通过参考以下实施例将更清楚地理解它们,这些实施例仅出于说明的目的而被包括,并且不旨在进行限制。
实施例
实施例1:bcma-特异性fn3结构域多肽的鉴定
在m13噬菌体的表面上表达两个fn3结构域文库总计250亿个变体,并作为噬菌体原液于4℃储存在1xpbs中。每个文库原液的滴度为1.5x1013cfu/ml。
靶蛋白bcma-fc嵌合体(r&dsystems)以下列浓度结合蛋白adynabeads(invitrogen):第1轮:500nm;第2轮:200nm;第三轮:40nm。iggfc蛋白(r&dsystems)作为差减筛选对于所有轮以500nm结合蛋白a珠。每个文库作为单独的反应处理,因此进行了三个选择。将含有fc清除的结合物的上清液转移至bcma蛋白a珠。对于第1轮,对于每个文库添加1x1013cfu/ml的噬菌体,且对于随后的每一轮,使用1x1012cfu/ml的噬菌体。珠洗涤6次,并用低ph缓冲液洗脱bcma结合的fn3结构域噬菌体颗粒。噬菌体在tg1细胞上滴定并扩增以制备第1轮噬菌体原液。进行三轮噬菌体选择。
在噬菌体elisa中测试第2轮和第3轮噬菌体以测试fn3结构域在噬菌体颗粒上的功能展示。单个克隆挑入96孔深孔模块的孔中并添加m13k07辅助噬菌体,扩增fn3结构域噬菌体颗粒。在仅bcma和fc涂覆的maxisorp平板上测试噬菌体。对具有bcma结合信号与fc结合信号的高比率的克隆进行测序。
酵母展示用于分选出最高bcma亲和力结合物。将第3轮结合bcma的fn3结构域噬菌体克隆到修饰的pyd1载体(invitrogen)中,其将aga2蛋白展示为c端融合蛋白。首先,噬菌粒dna在tg1中扩增,并且dna进行大量制备(maxi-prepped)(qiagen)。fn3结构域序列通过bamhi和xhoi从噬菌粒载体切下,并通过电穿孔用线性化的修饰pyd1载体将dna转化到eby100酵母中。fn3结构域在半乳糖培养基中表达。第一次分选分离与bcma的前0.5%-1%结合物作为群体。对于第二次分选,对于bcma结合噬菌体的前0.1%将单个酵母细胞的八个96孔板进行分选。dna通过酵母微量制备(mini-prep)(zymoresearch)分离并测序。
将结合bcma的fn3结构域克隆到pet-24a载体(novagen)中以进行可溶性表达。通过c端6xhis标签纯化结合bcma的fn3结构域。
使用octet生物层干涉测量系统(pallfortebio)测定bcma特异性fn3结构域的结合亲和力。将bcma-fc嵌合体靶蛋白以25μg/ml固定在proteina传感器尖端上。bcma特异性fn3结构域结合以10μg/ml测试。解离在仅1x动力学缓冲液中监测。通过fortebio软件确定ka、kd和kd值。bcma特异性fn3结构域按照对bcma的最高至最低结合亲和力排序。
示例性的结合bcma的fn3结构域序列如下所示:
nvspprrarvtdatettitipwalagspvvrfqvdavpangqtpiqrtiqpskrgytitglqpgtdykiylytlngpvvidast
实施例2:对癌抗原具有特异性的嵌合抗原受体的克隆
如美国专利号8,680,019所述生成天然变体组合的fn3结构域文库。纤连蛋白结合结构域的文库将在噬菌粒载体中构建。噬菌体将与生物素化的癌症抗原(例如vegf(121))一起孵育,该抗原在室温下在pbs-2.5%脱脂奶粉中与链霉亲和素涂覆的磁珠预结合1小时。用pbs-0.1%tween-20洗涤后,结合的噬菌体用0.1nhcl洗脱,并在tg1细胞中繁殖用于下一轮选择。在第1轮中,使用的vegf浓度为1μm,且每轮降低5倍以使得最后一轮选择包含20nmvegf。为了测量相对富集,由非展示性对照噬菌粒(pbc)制备的噬菌体(其赋予氯霉素抗性)也包括在选择反应中。在每一轮中,与非展示性对照噬菌体相比,预期文库噬菌体富集2至5倍。
选择后,通过噬菌体elisa筛选单个克隆与vegf的结合。阳性克隆通过噬菌体elisa再筛选针对vegf、tnfα或空白平板的结合特异性,以鉴定vegf特异性变体。vegf特异性变体进一步开发为包含fn3结构域多肽的候选vegf特异性靶向区。
使用本领域已知的标准分子生物学技术,vegf特异性靶向区用于构建fn3car分子。t细胞用fn3car分子转导,使得t细胞表达fn3car分子(fn3car-t细胞)。表达靶vegf的cho细胞或不表达靶vegf的常规cho细胞分别用fn3car-t细胞处理。非转导的t细胞(无fn3car分子)用作对照。
使用类似的实验程序,可以将axl特异性靶向区用于构建fn3car分子(即,axl特异性fn3car分子)。合适的axl特异性fn3结构域多肽在本文其他地方描述。
图1和图2描绘了显示fn3car分子的一般结构的示意图。
实施例3:双功能fn3结构域多肽car-t
可以构建包含fn3结构域多肽的双特异性car-t,其表达:i.结合肿瘤抗原的fn3结构域多肽,ii.结合t细胞表面受体的fn3结构域多肽,和iii.接头。潜在的肿瘤抗原靶标是bcma和cd-19。bcma涉及血液癌症,例如多发性骨髓瘤和白血病,并可能导致细胞存活和细胞增殖。cd19在b细胞癌症上发现。可以用fn3结构域多肽靶向的两种t细胞受体是pd-1和ctla-4。这两种受体均在激活的t细胞上表达,并传递抑制性信号和共刺激性信号两者。
可以构建包含fn3结构域多肽的双特异性car-t的另一个实例,其包括:i.结合axl的fn3结构域多肽,ii.结合t细胞表面受体的fn3结构域多肽或t细胞表面受体结合scfv(例如,抗cd3scfv),和iii.接头。合适的结合axl的fn3结构域多肽序列在本文其他地方描述。
使用本领域已知的标准分子生物学技术,双特异性靶向区用于构建fn3car分子。t细胞用fn3car或fn3/scfvcar分子转导,以使得t细胞表达fn3car或fn3/scfvcar分子(fn3car-t细胞或fn3/scfvcar-t细胞)。表达靶抗原的cho细胞或不表达靶抗原的常规cho细胞分别用fn3car-t或fn3/scfvcar-t细胞处理。非转导的t细胞(无fn3car或fn3/scfvcar分子)用作对照。
图3描绘了显示双特异性fn3car分子的一般结构的示意图。
两个fn3结构域多肽(i.和ii.的)之间的接头可以是衍生自天然纤连蛋白序列的20碱基对或14碱基对的序列。示例性的20碱基对和14碱基对的接头如下所示:
20碱基对接头:aidapsnlrflattpnsllv(seqidno:21)
14碱基对接头:aidapsnlrflatt(seqidno:22)
这一接头序列衍生自第14fn3结构域的末端与第15fn3结构域的bc环之间的天然纤连蛋白序列。使用这一内源序列降低对接头序列的免疫应答的可能性。
天然纤连蛋白的第14fn3结构域和第15fn3结构域之间的示例性序列如下所示:
nvspprrarvtdatettitiswrtktetitgfqvdavpangqtpiqrtikpdvrsytitglqpgtdykiylytlndnarsspvvidastaidapsnlrflattpnsllvswqppraritgyiikyekpgspprevvprprpgvteatitglepgteytiyvialknnqksepligrkkt(seqidno:23).
实施例4:fn3结构域双特异性t细胞衔接子
筛选
噬菌体展示:通过噬菌体展示筛选fn3结构域文库以发现与酪氨酸激酶受体axl(r&dsystemscat#154-al)结合的fn3结构域多肽。用以下靶标浓度完成三轮选择:第一轮:500nm和噬菌体文库1013;第二轮:200nm和噬菌体文库1012;和第三轮:40nm和噬菌体文库1012。
噬菌体筛选和针对axl结合活性的fn3文库的分析:通过噬菌体elisa验证单个克隆(1732个),并对576个进行测序,得到157个独特克隆。
酵母展示:将第3轮噬菌体原液克隆到酵母展示载体pyd1中,并完成两轮分选。第一次酵母分选使用25nm的axl靶蛋白,并且将前0.1-0.5%的结合物分选为富集群体。第二次酵母分选使用2.5nm的可溶性靶蛋白,并产生代表67个独特序列的192个个体克隆。
酵母筛选和使用facs针对axl结合活性分析fn3文库:根据以下所述使用axl可溶性靶标进行单克隆的酵母结合亲和力筛选:酵母单克隆(10μlod=0.1-0.2)针对1和0.01nm的axl-fc进行测试,并在facs染色培养基(pbs-bsa0.1%)中使用1:25抗fc-pe(109116098jacksonimmunoresearch)进行染色(图4)。
使用mda-mb-231癌细胞系和komda-mb-231细胞系通过facs对单克隆的酵母特异性筛选根据以下所述进行:粘附的靶细胞(axl表达和axlko细胞)在实验前一天接种(sided)在6wp上。按照建议的实验方案,细胞用vybranttmdid细胞标记溶液(thermofischerscientific目录号:v22887)标记。细胞相继与100ul酵母fn3结构域单克隆孵育。充分洗涤后,使用抗histag(r&dref)每6wp3ul检测酵母与细胞的结合(在4℃下30分钟)。洗涤后,从平板刮下细胞并通过facs分析。如果仅在mda231细胞系中而不在ko中观察到双色群体(did-红色和488-绿色),则鉴定出特异性克隆(图5)。
克隆axl特异性fn3结构域
总共,通过噬菌体展示和酵母展示发现的对axl具有特异性的59个fn3结构域被克隆到大肠杆菌载体pet-24a中用于表达可溶性蛋白。通过蛋白elisa和通过在octet(fortebiosystems)上的spr测试了axlfn3结构域的axl结合。观察到结合亲和力达到低至2nm的值(图6)。
在mda-mb-231上的特异性
针对具有高axl受体表达的mda-mb-231细胞和axl敲除(ko)mda-mb-231细胞系筛选axlfn3结构域结合物(图7a和7b)。四个fn3结构域(axl#44、axl#53、axl#54和axl#56)显示无非特异性结合。它们以高亲和力结合mda-mb-231细胞,且与敲除细胞不结合(图9a和9b)。
axl#44
nvspprrarvtdatettitirwegrgvigfqvdavpangqtpiqrtikpdvrsytitglqpgtdykiylytlpnigtghfssspvvidast(seqidno:33).
axl#53
nvspprrarvtdatettitiswegspstfigfqvdavpangqtpiqrtikpdvrsytitglqpgtdykiylytlpdfgrghftsspvvidast(seqidno:34).
axl#54
nvspprrarvtdatettitirwegrgvigfqvdavpangqtpiqrtikpdvrsytitglqpgtdykiylytlpdfgrghftsspvvidast(seqidno:35).
axl#56
nvspprrarvtdatettitiswrvspstvvglqvdavpangqtpiqrtikpdvrsytitglqpgtdykiylytlnviggsahasspvvidast(seqidno:36).
axl-cd3pronectins
通过ecorv位点将fn3结构域axl#54和scfvsp34cd3克隆到载体pmaxcloning(lonza)中。fn3结构域通过gibsonassembly克隆为g-block(idt),并进行序列验证。通过pei将质粒dna转染到293-t中,并收获含有axl#54-cd3fn3结构域-scfv融合体的上清液。蛋白通过his-重力柱(gehealthcare)纯化。fn3结构域axl#44和axl#56也克隆为与scfvsp34cd3的融合体。预测的大小为37.3kda(图8)。
44cd3
mdmrvpaqllgllllwlsgarcnvspprrarvtdatettitirwegrgvigfqvdavpangqtpiqrtikpdvrsytitglqpgtdykiylytlpnigtghfssspvvidastggggselvvtqepsltvspggtvtltcrsstgavttsnyanwvqqkpgqaprgliggtnkrapgtparfsgsllggkaaltlsgvqpedeaeyycalwysnlwvfgggtkltvlggggsggggsggggsevqllesggglvqpggslklscaasgftfntyamnwvrqapgkglewvarirskynnyatyyadsvkdrftisrddskntaylqmnnlktedtavyycvrhgnfgnsyvswfaywgqgtlvtvsshhhhhh(seqidno:37).
54cd3
mdmrvpaqllgllllwlsgarcnvspprrarvtdatettitirwegrgvigfqvdavpangqtpiqrtikpdvrsytitglqpgtdykiylytlpdfgrghftsspvvidastggggselvvtqepsltvspggtvtltcrsstgavttsnyanwvqqkpgqaprgliggtnkrapgtparfsgsllggkaaltlsgvqpedeaeyycalwysnlwvfgggtkltvlggggsggggsggggsevqllesggglvqpggslklscaasgftfntyamnwvrqapgkglewvarirskynnyatyyadsvkdrftisrddskntaylqmnnlktedtavyycvrhgnfgnsyvswfaywgqgtlvtvsshhhhhh(seqidno:38).
56cd3
mdmrvpaqllgllllwlsgarcnvspprrarvtdatettitiswrvspstvvglqvdavpangqtpiqrtikpdvrsytitglqpgtdykiylytlnviggsahasspvvidastggggselvvtqepsltvspggtvtltcrsstgavttsnyanwvqqkpgqaprgliggtnkrapgtparfsgsllggkaaltlsgvqpedeaeyycalwysnlwvfgggtkltvlggggsggggsggggsevqllesggglvqpggslklscaasgftfntyamnwvrqapgkglewvarirskynnyatyyadsvkdrftisrddskntaylqmnnlktedtavyycvrhgnfgnsyvswfaywgqgtlvtvsshhhhhh(seqidno:39).
t细胞依赖性细胞毒性(tdcc)测定
axl-cd3fn3结构域-scfv融合体在mda-mb-231和mda-mb-231ko细胞系上以500nm开始以1:4滴定,且结果显示它们是axl的特异性结合物。在caspace-glo3/7细胞毒性测定(promega)中测试axl-cd3fn3结构域-scfv融合体。axl-cd3fn3结构域-scfv融合体的起始浓度为500nm,且滴定为1:4,8个点。mda-mb-231细胞以10,000个细胞/孔接种,然后pbmc从含超过70%淋巴细胞的血液中分离,并以100,000个细胞/孔添加。因此,靶标:效应子的比率为1:10。孵育48小时后,添加caspace-glo试剂并测量发光(图10)。
绘制杀伤曲线并计算ec50(图10a和10b)。
t细胞激活测定
t细胞激活通过在axl-cd3fn3结构域-scfv融合体和表达axl受体的靶细胞的存在下cd69表达的增加来证实。在mda-mb-231细胞和pbmc(cd8+)上滴定(0.03-500nm)fn3结构域-scfv融合体axl#54-cd3。细胞用cd8和cd69抗体染色,且测量cd8+群体中cd69表达的增加为与仅pbmc相比41%的cd69增加。发现scfvcd3是功能性的(图11a和11b)。
axl-fc竞争/tdcc测定
为了测试axl-cd3fn3结构域-scfv融合体的靶标特异性,进行了具有axl-fc竞争的细胞毒性测定。该测定以500nm的axl-fc浓度设置和500nm的对照人fc进行设置。用pbmc、mda-mb-231细胞和axl#54-cd3滴定进行相同的测定。由于与axl-cd3fn3结构域-scfv融合体的结合竞争,axl-fc在测定中降低了细胞毒性。在细胞毒性测定中发现axl#54是靶标特异性的(图12)。
实施例5:axl二聚体和三聚体双特异性t细胞衔接子
通过gibsonassembly使用g-blocks将二聚体构建体和一个三聚体构建体克隆到pmaxcloning载体中。二聚体融合构建体是axl#44-axl54-cd3,和三聚体融合构建体是axl#44-axl54-axl56-cd3。两种构建体在293-t细胞中表达,并使用6xhis-标签进行纯化。
axl#44-axl#54-cd3
mdmrvpaqllgllllwlsgarcnvspprrarvtdatettitirwegrgvigfqvdavpangqtpiqrtikpdvrsytitglqpgtdykiylytlpnigtghfssspvvidastggggsggggsggggsnvspprrarvtdatettitirwegrgvigfqvdavpangqtpiqrtikpdvrsytitglqpgtdykiylytlpdfgrghftsspvvidastggggselvvtqepsltvspggtvtltcrsstgavttsnyanwvqqkpgqaprgliggtnkrapgtparfsgsllggkaaltlsgvqpedeaeyycalwysnlwvfgggtkltvlggggsggggsggggsevqllesggglvqpggslklscaasgftfntyamnwvrqapgkglewvarirskynnyatyyadsvkdrftisrddskntaylqmnnlktedtavyycvrhgnfgnsyvswfaywgqgtlvtvsshhhhhh(seqidno:40)
axl#44-axl#54-axl#56-cd3
mdmrvpaqllgllllwlsgarcnvspprrarvtdatettitirwegrgvigfqvdavpangqtpiqrtikpdvrsytitglqpgtdykiylytlpnigtghfssspvvidastggggsggggsggggsnvspprrarvtdatettitirwegrgvigfqvdavpangqtpiqrtikpdvrsytitglqpgtdykiylytlpdfgrghftsspvvidastggggsggggsggggnvspprrarvtdatettitiswrvspstvvglqvdavpangqtpiqrtikpdvrsytitglqpgtdykiylytlnviggsahasspvvidastggggselvvtqepsltvspggtvtltcrsstgavttsnyanwvqqkpgqaprgliggtnkrapgtparfsgsllggkaaltlsgvqpedeaeyycalwysnlwvfgggtkltvlggggsggggsggggsevqllesggglvqpggslklscaasgftfntyamnwvrqapgkglewvarirskynnyatyyadsvkdrftisrddskntaylqmnnlktedtavyycvrhgnfgnsyvswfaywgqgtlvtvsshhhhhh(seqidno:41)
- 还没有人留言评论。精彩留言会获得点赞!