通过超声治疗血管的血栓形成的装置的制作方法
本发明涉及一种通过超声,更具体地说通过组织摧毁法治疗血管的血栓形成的装置。
背景技术:
通过急性血栓形成过程(凝块形成或血栓形成)形成的血管、静脉或动脉阻塞是导致世界上大多数死亡发生的常见且严重的机制。在动脉中,血栓形成是大多数中风和心肌梗塞的根源。在静脉网络中发生血栓形成时,会导致疼痛、水肿以及凝块脱落的风险,凝块脱落会导致肺栓塞。通过血栓形成的静脉的持续性阻塞可能最终导致慢性静脉功能不全,表现为疼痛、水肿和溃疡,这些会导致生活质量的大幅下降。
动脉或静脉血栓形成的治疗原则是以全身抗凝为基础,从而避免血栓的扩大和栓塞并发症。然而,在深静脉血栓形成的情况下,这种治疗方法对慢性静脉功能不全是无效的,因为大多数情况下,其不能使形成血栓的静脉再通。使用溶栓治疗可以使阻塞的静脉再通,但是由于可能会诱发出血,全身给药是危险的。因此,在没有严重肺栓塞的静脉血栓形成的情况下,不建议使用这种治疗方法。借由导管局部给药,原位溶栓的使用可以限制全身效应。这些技术是侵入性的,并且通常需要植入外部装置(通常是支架)。因此,由于血管内装置的持续存在,局部存在风险(出血、感染),并且存在进一步阻塞的风险。另一种治疗方法是单独或与药物联合使用超声波。具体地,众所周知的是,采用被称为组织摧毁的技术来分解凝块,从而重建通过阻塞血管的循环;然后,人们提出了“血栓摧毁”。组织摧毁术是利用强烈并聚焦的超声脉冲来诱导产生局部空化效应,从而机械性地分解靶向软组织。
文献us5,827,204描述了一种基于超声的治疗装置,该装置可以特别地用于血栓摧毁治疗。该装置包括与成像换能器联用的治疗换能器,这两个换能器连接到致动器,使得它们沿轴向移动。
国际专利申请wo2009/094554以及以下文章:
-xizhang等人发表的“histotripsythrombolysisonretractedclots”,ultrasoundinmed.&biol.,第42卷,第8期,2016年8月,第1903-1918页;
-xizhang等人发表的“non-invasivethrombolysisusinghistotripsyinaporcinedeepveinthrombosismodel”,ultrasoundinmed.&biol.,第43卷,第7期,2017年7月;以及
公开了已经通过在体外进行的以及2017年的文章中在猪体内进行的研究所验证的血栓摧毁技术。
在这些情况下,通过设定焦距的多元件“治疗性”换能器的方式来应用频率为1mhz的治疗性超声波,多元件“治疗性”换能器的中心布置有利用超声波成像的换能器(超声回波描记术)。在体外研究中,换能器和模拟待治疗静脉的毛细管均浸没在声学耦合液体中。在活体研究中,换能器浸没在由无底碗状物和塑料制成的板所限制的声学耦合液体中,塑料制成的板与动物的皮肤接触。成像换能器使得等待治疗的静脉和治疗换能器的焦点被定位,由于产生空穴气泡云,能够看到所述焦点。然后,机械地移动由治疗换能器和成像换能器组成的组件,直到焦点与静脉重合。
由k.b.bader等人的文章“efficacyofhistotripsycombinedwithrt-painvitro”(phys.med.biol.,2016年7月21日)研究了结合组织摧毁术和溶栓药物的给药来治疗静脉血栓形成的方法的最佳操作条件。仅仅提供了使用多环治疗换能器、成像换能器(与前一换能器分离)以及模拟静脉的毛细管(这些全部浸没在耦合液体中)的体外研究。
通过浸没在液体中的换能器实现声学耦合是不现实的。此外,成像换能器必须与患者的皮肤保持一定距离,这会降低采集到的图像的质量。此外,这一距离并不是恒定不变的,因此图像的质量是变化的。这降低了治疗的精确度,因此降低了治疗的有效性,并且增加了利用聚焦的超声波治疗时损伤血管壁的风险。
技术实现要素:
本发明旨在克服现有技术的上述缺点。更具体地说,本发明旨在提供一种成像辅助的血栓摧毁方法,该方法更易于实施,能够实现更高的治疗精度,特别是降低血管壁损伤的风险。
根据本发明,通过机械和/或电子装置使治疗超声换能器的焦点沿着发射轴相对于成像超声换能器移动来实现该目的。这使得在扫描待治疗区域期间,成像换能器能够与待治疗的人体或动物体的表面保持接触,或者更一般地,与后者保持基本恒定的距离,因此获得更高质量的图像。反过来,更高质量的图像可以更精确地定位待治疗的血管壁,因此避免了对血管壁的意外损伤。
根据本发明的一个有利的实施方案,通过使用以高于或等于2mhz的频率工作的治疗超声换能器(而不是如现有技术中的以大约1mhz的频率工作的治疗超声换能器)也可以实现该目的。这可以获得更小、更稳定的焦点,可以充分利用对血管壁位置的更好了解,以避免对血管壁造成损伤。
因此,本发明的主题是利用超声治疗血管的血栓形成的装置,其包括:
-治疗超声换能器,其适于产生沿着发射轴传播的聚焦的超声波;
-成像超声换能器,其与治疗超声换能器联用,适于获取人体或动物体的待治疗区域的二维或三维图像,所述待治疗区域包括治疗超声换能器的焦点;
-用于使治疗超声换能器的焦点移动的装置,其用于使治疗超声换能器的焦点沿着发射轴相对于成像超声换能器移动;
-机动化机械系统,其适于使治疗超声换能器和成像超声换能器至少沿着平行于所述发射轴的第一运动轴平移地移动,并且沿着不平行于第一运动轴的第二运动轴平移地移动或围绕不平行于第一运动轴的第二运动轴旋转地移动;以及
-电子控制系统,其配置为:
-驱动机动化机械系统,以对待治疗区域进行扫描,同时以预定义的公差使成像超声换能器与人体或动物体的表面之间保持恒定距离;
-驱动用于使治疗超声换能器的焦点移动的装置,以在所述扫描期间控制焦点沿着发射轴的位置。
根据本发明的具体实施方案:
-所述装置还可以包括:受力传感器,其适于产生指示在平行于所述发射轴的方向上施加在成像超声换能器上的力的信号;电子控制系统配置为获取该信号并且使用该信号驱动机动化机械系统,以在扫描期间使所述成像超声换能器与人体或动物体的所述表面保持接触。
-所述电子控制系统还可以配置为:在扫描期间以恒定的力将所述成像超声换能器应用于人体或动物体的所述表面。
-所述电子控制系统还可以配置为:分析由治疗超声换能器获取的图像以检测所述人体或动物体的表面,以在所述扫描期间驱动机动化机械系统。
-所述电子控制系统还可以配置为:以如下方式来驱动将用于使治疗超声换能器的焦点移动的装置驱动为:在扫描期间,使得所述焦点在所述人体或动物体内部遵循预定义的路径。
-所述电子控制系统还可以配置为:
a)驱动机动化机械系统以进行待治疗区域的第一次扫描;
b)在该第一次扫描期间,获取所述区域的多个图像,同时保持治疗超声换能器不激活;
c)驱动机动化机械系统以进行待治疗区域的第二次扫描;
d)在该第二次扫描期间,激活治疗超声换能器并且将用于使治疗超声换能器的焦点移动的装置驱动为:使得所述焦点在所述人体内部遵循预定义的路径,所述预定义的路径是从第一次扫描期间所获取的图像中识别的。
-更具体地说,所述电子控制系统还可以配置为:
b1)分析第一次扫描期间所获取的图像,以识别所述人体或动物体的待治疗区域内的血管;
b2)将所述人体内部的所述预定义的路径确定为:使得所述预定义的路径与所述血管相对应。
-此外,所述电子控制系统还可以配置为:将机动化机械系统驱动为:在第二次扫描期间,使得所述血管位于成像超声换能器的视场的中心部分。
-所述电子控制系统还可以配置为:在第二次扫描期间,获取待治疗区域的多个图像,并且利用这些图像驱动机动化机械系统。
-所述治疗超声换能器可以是多元件换能器,并且用于使治疗超声换能器的焦点移动的装置包括:电子束成形器,其配置为以可变延迟来驱动所述换能器的元件,从而以可调焦距发射聚焦的超声波。更具体地说,它可以是同心多环换能器。
-所述用于使治疗超声换能器的焦点移动的装置可以包括:机械系统,其允许治疗超声换能器和成像超声换能器沿着所述发射轴相对移动。
-所述成像超声换能器可以在平行于所述发射轴的方向上延伸超过治疗超声换能器。
-所述成像超声换能器可以布置在治疗超声换能器的中心。
-所述装置还可以包括:声学界面装置,其适于将治疗超声换能器产生的聚焦的超声波耦合到人体或动物体的所述表面。
-所述机动化机械系统可以具有三个平移自由度和三个旋转自由度。
-所述治疗超声换能器可以适于产生频率大于或等于2mhz的聚焦的超声波。
-所述电子控制系统和成像超声换能器还可以配置为通过多普勒成像监测被治疗的血管的再通。
附图说明
本发明的其它特征、细节和优点将在阅读参照附图给出的描述时变得更加清楚,附图分别以示例的方式提供和示出:
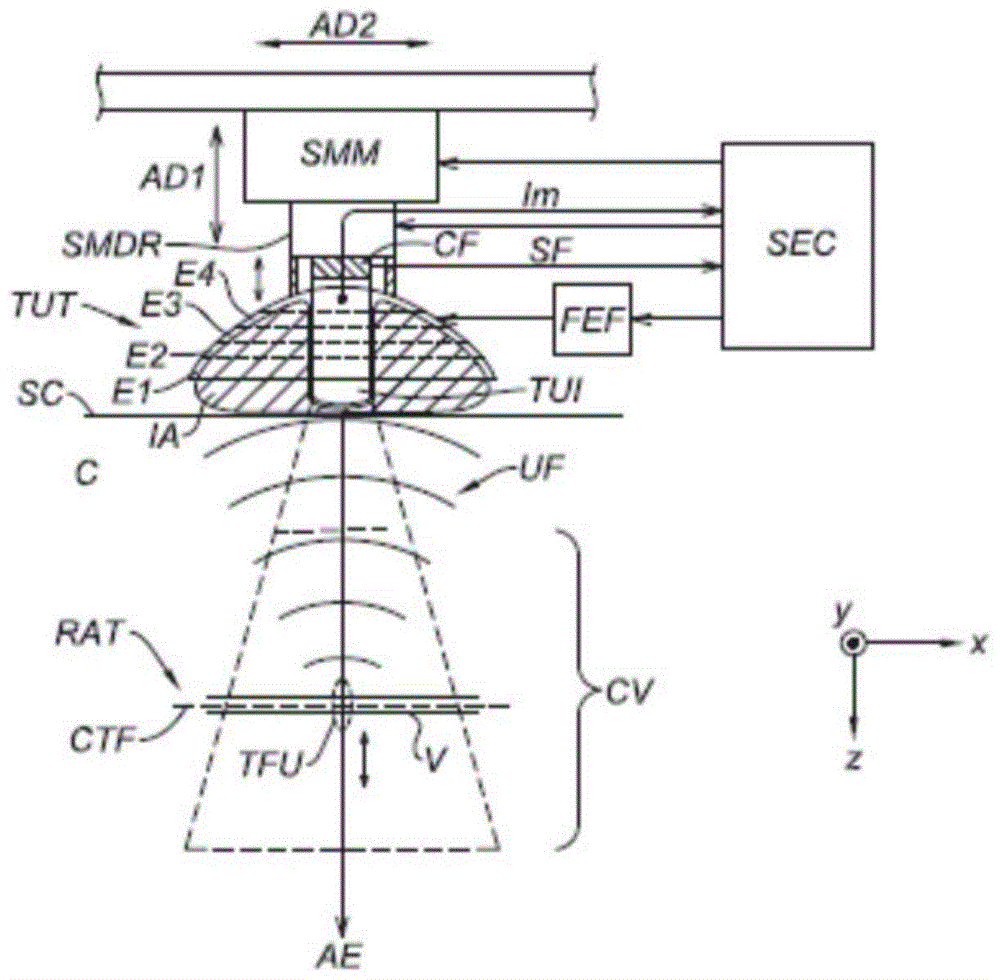
-图1是根据本发明一个实施方案的装置的示意图;
-图2是使用这种装置的治疗方法的流程图。
具体实施方式
在图1的装置中,治疗超声换能器tut是同心布置的半径逐渐减小的多元件环形换能器(即,它包括一组环形超声换能器)或元件(附图标记为e1、e2、e3、e4),以形成球形,或者更一般地,形成凹形(例如抛物面形)帽状。例如,在文献us5,520,188中描述了这种换能器。
当然,换能器的数量不一定等于4;优选地,该数量将包含在4到20之间,以避免过于复杂。
环形元件优选是圆形的;更准确地说,它们可以具有圆形底座的截头圆锥形形状,但是可以预想为其它形状。它们可以是连续的,或者由分离的部段组成。
由治疗换能器tut的元件e1-e4产生的超声波uf聚焦到通常具有椭圆形状的焦点tfu。超声波的主发射轴由“z”表示。为了简单起见,虽然不是必需的,但该轴将被视为垂直于待治疗的人体或动物体c的表面sc(即,皮肤)。超声波通过声学界面ia耦合到身体,声学界面ia例如由充有凝胶或脱气水的柔性塑料制成的口袋形成。该口袋具有与换能器的元件接触的凸面和旨在与表面sc接触的大体上平坦的面。在使用中,该平坦的面可以依次涂覆声学耦合凝胶。
换能器的凹面形状确保超声波uf沿着z轴聚焦在“自然”或“几何”焦距处。通过在元件的驱动信号之间引入相移而获得的电子聚焦能够精细地修改该焦距。在图1的实施方案中,这些驱动信号是通过电子控制系统sec产生的,相移是通过由系统sec驱动的波束成形电路fef引入的。
有利地,治疗换能器配置为例如以高于或等于2mhz、等于2.25mhz的频率工作,而在上述现有技术中,治疗超声波的频率则是大约1mhz。特别地,对于换能器的给定几何形状和给定焦距,焦点的宽度(垂直于传播方向)和长度(平行于该长度)与频率成反比。数值仿真已经证实了这一理论结果。因此,通过以2mhz而不是1mhz工作,可以将焦点的体积除以因子8。这可以更好的瞄准待分解的凝块并且使血管壁受损的风险最小化。
体外试验已经证实了2.25mhz的超声波在血栓摧毁治疗中的有效性。在这些试验中,将人血放置在模拟人的股静脉的硅胶制成的6mm内径的管中,并且所述管保持竖直位置。通过加入20nm氯化钙而诱使血液凝结,导致形成2.5cm长度的凝块。接下来,将试管放置在水平位置并且在30cmh2o的压力下加载盐溶液(0.9%的nacl)。仅保留含有阻塞性凝块的试管并接受血栓摧毁治疗。通过两个以2.25mhz工作、焦距为38mm并且直径也为38mm的超声换能器来进行这种治疗。将管、血栓摧毁换能器和成像换能器放置在脱气水浴中。测试三种治疗方案:以1mm/s、2mm/s和3mm/s的速度通过3次。在每种情况下,以2.5kw的8个周期的脉冲来驱动两个换能器,产生-15mpa的峰值负压。第一个方案被证明是最佳方案,在90秒的治疗时间内,通过3次之后导致有效的再通(最大流量的80±7%)。检测到极少数量的尺寸大于100μm的碎屑颗粒(每个血栓1.6±1.7),但没有尺寸大于200μm的碎屑颗粒:这可以被认为是表示栓塞没有危险了。
超声成像换能器tui(例如二维或三维超声探测器)设置在治疗换能器的中心(最小半径的元件e4内部)。该换能器具有主要沿着z轴延伸的视场cv并且包括通常能够找到焦点tfu的区域。更确切地说,在图1的实施方案中,成像超声换能器tui是二维类型并且视场位于xz平面中。成像控制系统sec驱动成像换能器、接收由后者获取的信号im并且对这些信号进行处理,以重建身体c的待治疗区域rat的图像。
有利地,成像换能器轴向地(即在z方向上)延伸超过治疗换能器的外边缘。例如,可以延伸超过10-50mm,优选为10-25mm。声学界面ia可以具有允许由成像换能器通过的孔径,或者,如图1所示的情况,具有与成像换能器相称的凹槽。这使得成像换能器的活动面与身体c的表面sc进行“直接”接触(事实上,通过声学耦合凝胶薄层接触),或者进行“间接”接触(通过声学界面ia的口袋以及同样的凝胶薄层的双重厚度)而治疗换能器的边缘可以与该表面间隔开。
在图1的实施方案中,治疗换能器tut和成像换能器tui通过机械系统smdr相连,允许在z方向上平移地相对运动。例如,成像换能器可以固定到该机械系统的基座,并且治疗换能器通过沿着z轴定向的三个致动缸(图中仅示出其中两个)连接到该基座。利用电子控制系统sec同步地驱动三个致动缸,使得治疗换能器在z方向上移动,并且因此使得聚焦的超声波的焦点tfu在z方向上移动,而无需同时移动成像换能器。用于实现相对运动的机械系统smdr也可以采用其它形式:例如,可以基于齿条和小齿轮系统。
机械系统smdr的存在不是必要的:具体地,治疗换能器的多元件结构和波束成形电路fef也允许聚焦的超声波的焦点tfu在z方向上相对于成像换能器移动。反过来,在无需设置多元件换能器和电子聚焦系统的情况下,机械系统smdr可以满足需求。在任何情况下,在根据本发明的装置中,无需移动成像换能器就可以在轴向上定位焦点tfu。相比之下,这在国际专利申请wo2009/094554和xizhang等人的上述文章中描述的装置中是不可能的,在这些装置中,只有通过将治疗换能器和成像换能器一起移动才可以定位焦点。
在图1的实施方案中,成像换能器tui通过受力传感器cf(其例如为压电的)连接到机械系统smdr的基座,或者更一般地连接到保持部件,从而测量施加到换能器的z方向上的力。将传感器获取的受力测量信号sf发送到电子控制系统sec。这具有双重功能:一方面,检测到非零的受力可以确保成像换能器确实与身体c的表面sc直接或间接的接触;另一方面,对该受力的定量测量可以防止成像换能器过分地压向表面sc并且挤压身体c的组织。
受力传感器cf的存在不是必要的。具体地,还可以使用用于分析由电子控制系统重建的图像的技术来检测表面sc并确定其相对于换能器tui的位置。
包括治疗换能器tut、成像换能器tui,以及在适当情况下还包括用于实现相对运动的机械系统smdr和/或受力传感器cf的组件固定到由电子控制系统sec驱动的机动化机械系统smm,从而允许以至少两个自由度相对于底座(并且因此相对于身体c)运动:
-沿着平行于z轴的第一轴ad1的平移;以及
-沿着第二轴ad2的平移或围绕第二轴ad2的旋转,第二轴ad2不平行于并且通常垂直于第一轴。
在图1的实施方案中,第二自由度是沿着平行于x方向的第二轴ad2的平移。更确切地说,在该实施方案中,机动化机械系统smm包括沿着轨道滑动并且承载致动缸的托架,所述轨道沿着轴ad2(x)定向,所述致动缸确保沿着轴ad1(z)的平移。在更复杂的实施方案中,可以提供多个自由度,例如三个平移和三个旋转,更具体地为沿着正交轴x、y和z的三个平移以及围绕这些轴的三个旋转。尤其可以通过机械臂来实现。
如上所述,电子控制系统sec执行多个功能:驱动用于实现相对运动的机械系统smdr和机动化机械系统smm、驱动治疗换能器和成像换能器、获取成像信号、重建并分析图像、获取受力测量信号等等。该系统可以包括一个或更多个计算装置和/或专用数字电子板。这些元件不一定要位于一处,而是具体地可以通过总线、局域网或者甚至因特网来连接。
根据本发明的装置可以用于实现根据图2的治疗血栓形成的方法。
首先,步骤a)-通过电子控制系统sec驱动电动化机械系统smm,以根据待治疗区域rat对身体c的表面sc进行第一次扫描。同时,步骤b)-使用成像超声换能器tui获取区域rat的多个图像,优选地,允许后者的三维重建。机动化机械系统smm被驱动为使得成像换能器以通常小于或等于10%并且优选为小于1%的预定义的公差与表面sc保持恒定距离。该距离通常在0(直接或间接接触,这是优选的实施方案)至40mm之间,以确保扫描期间令人满意和稳定的图像质量。如上面提到的,此外,当成像换能器与表面sc保持接触时,受力测量信号sf可以用于使换能器施加在所述表面上的压力保持恒定(也具有通常小于或等于10%并且优选为小于1%的公差)。
在该第一次扫描期间,治疗换能器保持不激活。
接下来,步骤b1)电子控制系统sec分析第一次扫描期间所获取的图像,以自动识别区域rat中的待治疗血管(图1中的附图标记v)。可以通过选择或重建使得血管呈现为圆或椭圆的近似垂直于待检测血管的轴线的平面(图1的情况中为平面yz)的截面图,并且通过应用圆检测算法来执行这一步骤,所述圆检测算法例如可以基于hough变换或与累加器联用的canny-dériche边缘检测,所述累加器利用投票机制确定圆的中心位置。也可以使用其他已知算法。作为变体形式,在适当的情况下,可以由操作者利用所获取图像的阈值和/或边缘检测来检测血管。接下来,步骤b2)-确定身体c内部并沿着识别出的血管v的路径或轨迹。这一操作可以由电子控制系统sec自动执行,或者由操作者手动执行。
一旦这些准备操作结束,实际的治疗就可以开始了。
步骤c)-再次通过电子控制系统sec驱动电动化机械系统smm,以对身体c的表面sc进行第二次扫描。与第一次扫描一样,驱动使得成像换能器与表面sc保持恒定距离(该距离优选在0(优选的情况)至40mm之间,公差不高于10%甚至不高于1%)。还与第一次扫描一样,当成像换能器与表面sc保持接触时,受力测量信号sf可以用于使换能器施加在所述表面上的压力保持恒定(也具有通常小于或等于10%并且优选小于1%的公差)。
第二次扫描通常与第一次扫描不同。具体地,第一次扫描的目的是对包含待治疗血管v的待治疗区域实现详细的探查,而在第二次扫描期间,机动化机械系统smm被驱动为使得血管v位于成像换能器的视场cv的中心区域(例如,在沿着z轴和沿着垂直于z的轴的中心的三分之一处)。有利地,在第二次扫描期间所获取的图像被用于闭环驱动机动化机械系统。
在第二次扫描期间,激活治疗超声换能器tut,并且用于实现相对运动的机械系统smdr和/或波束生成电路fef被驱动为使得换能器tut发射的聚焦的超声波的焦点tfu遵循步骤b2)中定义的路径。这是图2的方法的最后一个步骤d)。
此外,在第二次扫描期间或之后,可以在电子系统sec的控制下使用成像超声换能器来获取多普勒超声图像,以通过多普勒成像来监测被治疗的血管的再通。
- 还没有人留言评论。精彩留言会获得点赞!