炎症性肠病的治疗药的制作方法
本申请涉及包含高迁移率族蛋白1(highmobilitygroupbox1,hmgb1)的片段肽的用于预防和/或治疗炎症性肠病的药物组合物。
背景技术:
炎症性肠病(inflammatoryboweldisease;ibd)是在肠道的粘膜中发生慢性炎症和/或溃疡的难治性疾病,作为其代表例,可举出溃疡性结肠炎及克隆氏病。炎症性肠病的原因尚未完全阐明,但认为其原因是由于遗传因素和各种环境因素复杂参与而引起免疫系统的异常。但是,对于炎症性肠病,目前尚没有根治性疗法,大多反复发生缓解和复发,因此需要长期的医学管理。
作为炎症性肠病的治疗药,现使用5-氨基水杨酸制剂、皮质类固醇制剂、免疫抑制剂、生物学制剂(例如抗tnf-α抗体、抗α4β7整合素抗体)等,但存在无法获得充分效果的病例。此外,在副作用方面,也有由5-氨基水杨酸制剂引起的恶心、发热、腹痛、贫血、间质性肾炎及肝功能障碍;由皮质类固醇制剂引起的失眠、骨质疏松症、肾上腺皮质功能障碍、葡萄糖耐量异常和血压上升;以及由免疫抑制剂引起的肾功能障碍、肝功能障碍、白细胞减少及血压上升等问题,还存在改善的余地。因此,期望开发出与现有的治疗药不同类型的、更有效且安全性高的炎症性肠病的治疗药。
现有技术文献
专利文献
专利文献1:wo2012/147470
专利文献2:wo2014/065347
专利文献3:wo2014/065348
技术实现要素:
发明所要解决的课题
本申请的目的在于提供一种对炎症性肠病的治疗有效的新药物。
用于解决课题的手段
本发明者们研究了对炎症性肠病的治疗有效的物质,其结果发现,具有特定的氨基酸序列的hmgb1片段肽在炎症性肠病的动物模型中显示出抑制体重减少的效果以及抑制结肠缩短和粘膜损伤的效果。因此,本申请提供一种用于预防和/或治疗炎症性肠病的药物组合物,其含有该特定的hmgb1片段肽。
即,本申请提供以下方案。
〔1〕一种用于预防和/或治疗炎症性肠病的药物组合物,其含有以下的(a)~(c)中任一项所述的物质(以下称为物质a):
(a)包含序列号1所记载的氨基酸序列的hmgb1片段肽;
(b)包含在序列号1所记载的氨基酸序列中1个或多个氨基酸被替换、缺失、插入或添加而成的氨基酸序列的肽;以及
(c)包含与序列号1所记载的氨基酸序列具有约80%以上的序列同源性的氨基酸序列的肽。
〔2〕根据〔1〕所述的药物组合物,其中,炎症性肠病是非特异性炎症性肠病。
〔3〕根据〔2〕所述的药物组合物,其中,非特异性炎症性肠病是溃疡性结肠炎。
〔4〕根据〔2〕所述的药物组合物,其中,非特异性炎症性肠病是克隆氏病。
〔5〕一种用于在炎症性肠病的患者中抑制体重减少或肠道粘膜损伤的药物组合物,其含有物质a。
〔6〕根据〔5〕所述的药物组合物,其中,炎症性肠病是非特异性炎症性肠病。
〔a1〕一种预防和/或治疗炎症性肠病的方法,其包含将物质a的有效量给药至对象的工序。
〔a2〕根据〔a1〕所述的方法,其中,炎症性肠病是非特异性炎症性肠病。
〔a3〕根据〔a2〕所述的方法,其中,非特异性炎症性肠病是溃疡性结肠炎。
〔a4〕根据〔a2〕所述的方法,其中,非特异性炎症性肠病是克隆氏病。
〔a5〕一种在炎症性肠病的患者中抑制体重减少或肠道粘膜损伤的方法,其包含将物质a的有效量给药至所述患者的工序。
〔a6〕根据〔a5〕所述的方法,其中,炎症性肠病是非特异性炎症性肠病。
〔b1〕一种用于预防和/或治疗炎症性肠病的物质a。
〔b2〕根据〔b1〕所述的物质a,其中,炎症性肠病是非特异性炎症性肠病。
〔b3〕根据〔b2〕所述的物质a,其中,非特异性炎症性肠病是溃疡性结肠炎。
〔b4〕根据〔b2〕所述的物质a,其中,非特异性炎症性肠病是克隆氏病。
〔b5〕一种用于在炎症性肠病的患者中抑制体重减少或肠道粘膜损伤的物质a。
〔b6〕根据〔b5〕所述的物质a,其中,炎症性肠病是非特异性炎症性肠病。
〔c1〕物质a在用于制造预防和/或治疗炎症性肠病的药物中的用途。
〔c2〕根据〔c1〕所述的用途,其中,炎症性肠病是非特异性炎症性肠病。
〔c3〕根据〔c2〕所述的用途,其中,非特异性炎症性肠病是溃疡性结肠炎。
〔c4〕根据〔c2〕所述的用途,其中,非特异性炎症性肠病是克隆氏病。
〔c5〕物质a在用于制造在炎症性肠病的患者中抑制体重减少或肠道粘膜损伤的药物中的用途。
〔c6〕根据〔c5〕所述的用途,其中,炎症性肠病是非特异性炎症性肠病。
附图说明
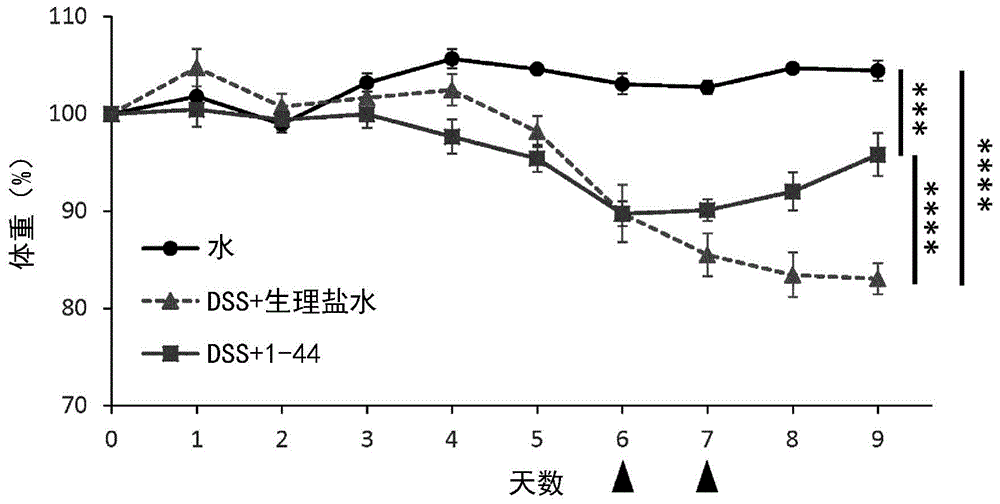
图1是表示小鼠的体重变化的图表(***p<0.001、****p<0.0001)。图表中,“水”表示正常小鼠,“dss+生理盐水”表示对照组,“dss+1-44”表示hmgb1肽(1-44)给药组。横轴中,天数是葡聚糖硫酸钠(dextransulfatesodium;dss)水溶液的饮水开始后的天数,三角标记表示对照组及hmgb1肽(1-44)给药组的给药日。
图2是从dss水溶液的饮水开始后第9天的小鼠摘出的结肠的照片和表示结肠长度的图表(*p<0.05,**p<0.01)。
图3是表示dss水溶液的饮水开始后第9天的结肠中的炎症性细胞因子的表达量的图表(*p<0.05、**p<0.01、***p<0.001、****p<0.0001)。
图4是表示小鼠的体重变化的图表(****p<0.0001)。图表中,“水”表示正常小鼠,“dss+生理盐水”表示对照组,“dss+1-44”表示hmgb1肽(1-44)给药组。横轴中,天数表示dss水溶液的饮水开始后的天数,三角标记表示对照组及hmgb1肽(1-44)给药组的给药日。
图5是从dss水溶液的饮水开始后第10天的小鼠摘出的结肠的照片和表示结肠长度的图表(*p<0.05、**p<0.01)。
图6是表示dss水溶液的饮水开始后第10天的结肠组织的he染色结果的图像。
图7是表示小鼠的体重变化的图表(****p<0.0001)。图表中,“水”表示正常小鼠,“dss+pi5生理盐水”表示对照组,“dss+pi51-44”表示hmgb1肽(1-44)给药组。横轴中,天数表示dss水溶液的饮水开始后的天数。
图8是从dss水溶液的饮水开始后第10天的小鼠摘出的结肠的照片和表示结肠长度的图表(*p<0.05、**p<0.01、***p<0.001)。
图9是表示小鼠的体重变化的图表(****p<0.0001)。图表中,“水”表示正常小鼠,“dss+pbs”表示对照组,“dss+mscs”表示msc给药组。横轴中,天数表示dss水溶液的饮水开始后的天数,三角标记表示对照组及msc给药组的给药日。
具体实施方式
本申请提供一种用于预防和/或治疗炎症性肠病的药物组合物,其含有包含序列号1所记载的氨基酸序列的hmgb1片段肽。
本申请的炎症性肠病(以下也称为ibd)中包括原因不明的疾病(非特异性炎症性肠病)和与原因的关系明确的疾病(特异性炎症性肠病)。作为非特异性炎症性肠病,可举出溃疡性结肠炎、克隆氏病及肠型白塞病(intestinalbehcetdisease),但并不限定于这些。作为特异性炎症性肠病,可举出感染性肠炎、药剂性肠炎、缺血性肠炎、肠结核等,但并不限定于这些。在一个方式中,本申请的炎症性肠病是非特异性炎症性肠病。在进一步的方式中,本申请的非特异性炎症性肠病是溃疡性结肠炎或克隆氏病。在另一方式中,本申请的非特异性炎症性肠病是溃疡性结肠炎。在又一方式中,本申请的非特异性炎症性肠病是克隆氏病。
溃疡性结肠炎是指在结肠粘膜上发生糜烂或溃疡的原因不明的炎症性疾病。作为主要症状,呈现出血便、粘血便、腹泻或血性腹泻、腹痛等症状,多伴有发热或体重减少。
克隆氏病是指在消化道发生伴有溃疡或纤维化的肉芽肿性炎症性病变的原因不明的慢性炎症性疾病。作为主要症状,除了呈现腹痛、腹泻、体重减少、发热等之外,有时也会发生瘘、狭窄等肠道并发症、或贫血、关节炎、虹膜炎、结节性红斑、肛门部病变等肠道外并发症。
本申请中,“药物组合物”这一用语与“药物”、“药剂”或“药学组合物”互换使用。
另外,本发明提供一种用于在炎症性肠病的患者中抑制体重减少或肠道粘膜损伤的药物组合物,其含有包含序列号1所记载的氨基酸序列的hmgb1片段肽。在一个方式中,本申请的药物组合物用于在炎症性肠病的患者中抑制结肠的粘膜损伤。
本申请中,包含序列号1所记载的氨基酸序列的hmgb1片段肽是指由hmgb1蛋白的一部分构成的肽,即是指包含序列号1所记载的氨基酸序列的肽。这样的肽可以通过将编码该肽的dna整合到适当的表达系统中而作为基因重组体(recombinant)得到,或者也可以人工合成。
本申请中,作为hmgb1蛋白,可例示出包含序列号2所记载的氨基酸序列的蛋白、以及由包含序列号3所记载的碱基序列的dna编码的蛋白,但并不限定于这些。
作为本申请的包含序列号1所记载的氨基酸序列的hmgb1片段肽,可例示出由序列号1所记载的氨基酸序列构成的hmgb1片段肽,但并不限定于此。
本申请的药物组合物中,代替包含序列号1所记载的氨基酸序列的hmgb1片段肽,还可以使用或与其一起使用包含在序列号1所记载的氨基酸序列中1个以上的氨基酸残基被改变(替换、缺失、插入或添加)而成的氨基酸序列的肽,即与包含序列号1所记载的氨基酸序列的hmgb1片段肽在功能上同等的肽。作为所述肽的例子,可例示出以下的肽,但并不限定于这些:
i)包含在序列号1所记载的氨基酸序列中1个或多个(例如1个~10个、1个~9个、1个~8个、1个~7个、1个~6个、1个~5个、1个~4个、1个~3个、或者1个或2个)氨基酸被替换、缺失、插入或添加而成的氨基酸序列的肽;
ii)由在序列号1所记载的氨基酸序列中1个或多个(例如1个~10个、1个~9个、1个~8个、1个~7个、1个~6个、1个~5个、1个~4个、1个~3个、或者1个或2个)氨基酸被替换、缺失、插入或添加而成的氨基酸序列构成的肽;
iii)包含与序列号1所记载的氨基酸序列具有约80%以上、例如约85%以上、约90%以上、约91%以上、约92%以上、约93%以上、约94%以上、约95%以上、约96%以上、约97%以上、约98%以上或约99%以上的序列同源性的氨基酸序列的肽;
iv)由与序列号1所记载的氨基酸序列具有约80%以上、例如约85%以上、约90%以上、约91%以上、约92%以上、约93%以上、约94%以上、约95%以上、约96%以上、约97%以上、约98%以上或约99%以上的序列同源性的氨基酸序列构成的肽。
本申请中的肽或含有其的药物组合物(以下称为肽等)的有效量以治疗或预防本说明书中记载的疾病或症状为目的而被给药至对象。
本申请中的有效量是指治疗或预防本说明书中记载的疾病或症状所需的足够的量。本申请中的治疗包括减轻、延迟、阻止、改善、缓解、治愈、根治等,但并不限定于这些。另外,本申请中的预防包括减轻、延迟、阻止等,但并不限定于这些。
作为本申请中的对象,没有特别限制,可举出哺乳类、鸟类、鱼类等。作为哺乳类,可举出人或非人动物,例如可例示出人、小鼠、大鼠、猴子、猪、狗、兔子、仓鼠、豚鼠、马、羊、鲸等,但并不限定于这些。本申请中,“对象”这一用语与“患者”、“个体”以及“动物”互换使用。
本申请的肽等的给药部位没有限制,即使是向出现炎症性肠病的症状的部位或其附近、与这些不同的部位(除这些以外的部位)、与出现炎症性肠病的症状的部位分开的部位、位于出现炎症性肠病的症状的部位的远离处的部位、或相对于出现炎症性肠病的症状的部位为远离处且不同处的部位等任意部位给药,本申请的肽等也能够发挥其效果。
另外,本申请的肽等即使是向与出现炎症性肠病的症状的组织(例如消化道)不同的组织、与出现炎症性肠病的症状的组织分开的组织、位于出现炎症性肠病的症状的组织的远离处的组织、或相对于出现炎症性肠病的症状的组织为远离处且不同处的组织等任意组织给药,也能够发挥其效果。
作为本申请的肽等的给药方法,可举出经口给药或非经口给药,作为非经口给药方法,可举出血管内给药(动脉内给药、静脉内给药等)、肌肉内给药、皮下给药、皮内给药、腹腔内给药、经鼻给药、经肺给药、经皮给药等,但不限定于这些。另外,可以通过将本申请的肽等注射给药、例如静脉内注射、肌肉内注射、腹腔内注射、皮下注射等向全身或局部(例如皮下、皮内、皮肤表面、眼球或者眼睑结膜、鼻腔粘膜、口腔内以及消化道粘膜、阴道-子宫内粘膜、或损伤部位等)给药。
另外,代替本申请的肽等,还可以使用分泌本申请的肽的细胞、插入有编码该肽的dna的基因治疗用载体、以及含有它们的药物组合物。
另外,可以根据患者的年龄、症状适当地选择给药方法。在给药本申请的肽的情况下,例如对于一次给药,每1kg体重可以在0.0000001mg至1000mg的范围内选择给药量。或者,例如可以每位患者在0.00001~100000mg/body的范围内选择给药量。在给药分泌本申请的肽的细胞或插入有编码该肽的dna的基因治疗用载体的情况下,也可以按照该肽的量达到上述范围内的方式进行给药。但是,本申请中的药物组合物并不限定于这些给药量。
本申请的药物组合物可以按照常规方法进行制剂化(例如remington'spharmaceuticalscience,latestedition,markpublishingcompany,easton,u.s.a),可以一起含有药物上可容许的载体、添加物。例如表面活性剂、赋形剂、着色剂、着香料、防腐剂、稳定剂、缓冲剂、悬浮剂、等渗剂、粘合剂、崩解剂、润滑剂、流动性促进剂、矫味剂等,但并不限定于这些,其他常用的载体也可以适当使用。具体而言,可举出轻质硅酸酐、乳糖、结晶纤维素、甘露醇、淀粉、羧甲基纤维素钙、羧甲基纤维素钠、羟丙基纤维素、羟丙基甲基纤维素、聚乙烯醇缩醛二乙基氨基乙酸酯、聚乙烯基吡咯烷酮、明胶、中链脂肪酸甘油三酯、聚氧乙烯氢化蓖麻油60、白糖、羧甲基纤维素、玉米淀粉、无机盐类等。
需要说明的是,本说明书中引用的所有现有技术文献作为参照引入本说明书中。
本发明通过下述实施例进一步进行例示,但本发明并不限定于这些。
实施例
实施例1
hmgb1片段肽对炎症性肠病的有效性的评价(1)
(1)材料和方法
i)药剂制备
将葡聚糖硫酸钠(dss)(分子量为5000~6000、nacalaitesque公司制、商品目录编号为10930-94)溶解在水中,制备3%(w/v)的dss水溶液。另外,通过固相法化学合成由来自人的hmgb1蛋白的氨基酸残基1-44(序列号1)构成的肽。以下,将该hmgb1片段肽称为hmgb1肽(1-44),在与实施例对应的附图中省略地记为“1-44”。
ii)炎症性肠病(ibd)小鼠模型的制作
代替精制水(ro水),通过使c57bl/6小鼠(8~10周龄、雄性、体重为约20g)自由饮用3%dss水溶液来诱发结肠炎(dss水溶液的饮水持续至结肠摘出时为止)。另外,使用自由饮用精制水(ro水)的小鼠(以下称为“正常小鼠”)作为比较对象。
iii)肽的给药
将如上制作的ibd小鼠模型分成hmgb1肽(1-44)给药组(n=3)和对照组(n=3)。受试物质的给药通过如下来进行:在dss水溶液的饮水开始后第6天和第7天,以200μl/只的量(以肽的给药量计为5mg/kg)向静脉注入以生理盐水为溶剂调整为0.5mg/ml的浓度的hmgb1肽(1-44)溶液。对照组在dss水溶液的饮水开始后第6天和第7天,以200μl/只的量向静脉注入生理盐水。不对正常小鼠(n=3)进行物质的给药。另外,下文中,将“dss水溶液的饮水开始后第x天”省略地记为“dss饮水第x天”。
iv)肽给药带来的效果的评价
从dss水溶液的饮水开始至结肠摘出时为止,每天测定小鼠的体重。在dss饮水第9天从小鼠摘出结肠,测定结肠长度。从摘出的结肠中靠近肛门的末端部分提取mrna,通过定量pcr分析炎症性细胞因子(tnf-α、il-1β、il-6)的表达量。
(2)结果
i)体重变化
将试验期间中的小鼠的体重变化示于图1(正常小鼠参照“水”,对照组参照“dss+生理盐水”,hmgb1肽(1-44)给药组参照“dss+1-44”)。对照组的ibd小鼠模型的体重随着天数的经过而减少,dss饮水第9天时与正常小鼠相比显著地变小。与此相对,在hmgb1肽(1-44)给药组中,暂时减少的体重在肽给药后恢复,在dss饮水第9天时与对照组相比显著地变大。
ii)结肠长度
如图2所示,在对照组的ibd小鼠模型的结肠长度与正常小鼠相比显著性地变短的条件下,hmgb1肽(1-44)给药组的结肠长度与对照组相比显著性地长(正常小鼠参照“水”,对照组参照“dss+生理盐水”,hmgb1肽(1-44)给药组参照“dss+1-44”)。该结果表明,作为ibd模型的dss诱发肠炎中的结肠的缩短通过给药hmgb1肽(1-44)而被抑制。
iii)炎症性细胞因子
将dss饮水第9天的结肠中的炎症性细胞因子的表达量示于图3(正常小鼠参照“水”,对照组参照“dss+生理盐水”,hmgb1肽(1-44)给药组参照“dss+1-44”)。在对照组的ibd小鼠模型中,tnf-α、il-1β和il-6与正常小鼠相比显著地高。另一方面,hmgb1肽(1-44)给药组中的tnf-α、il-1β和il-6的表达与对照组相比显著性地低。该结果表明,作为ibd模型的dss诱发肠炎中的炎症性细胞因子的表达通过给药hmgb1肽(1-44)而被抑制。
实施例2
hmgb1片段肽对炎症性肠病的有效性的评价(2)
(1)材料和方法
i)药剂及小鼠
dss水溶液和hmgb1肽(1-44)的制备以及炎症性肠病小鼠模型的制作与实施例1相同。
ii)肽的给药
将如实施例1中记载那样制成的ibd小鼠模型分成hmgb1肽(1-44)给药组(n=3)和对照组(n=3)。受试物质的给药通过如下来进行:在dss饮水第1、3、5和7天,以200μl/只的量(以肽的给药量计为5mg/kg)向静脉注入以生理盐水为溶剂调整为0.5mg/ml的浓度的hmgb1肽(1-44)溶液。对照组在dss饮水第1、3、5和7天、以200μl/只的量向静脉注入生理盐水。不对正常小鼠(n=3)进行物质的给药。
iii)肽给药带来的效果的评价
从dss水溶液的饮水开始至结肠摘出时为止,每天测定小鼠的体重。在dss饮水第10天从小鼠摘出结肠,测定结肠长度。使用摘出的结肠中靠近肛门的末端部分制作肠道截面的组织切片,进行苏木精-伊红(he)染色。
(2)结果
i)体重变化
将试验期间中的小鼠的体重变化示于图4(正常小鼠参照“水”,对照组参照“dss+生理盐水”,hmgb1肽(1-44)给药组参照“dss+1-44”)。ibd小鼠模型(对照组和hmgb1肽(1-44)给药组)的体重随着天数的经过而减少,dss饮水第10天时与正常小鼠相比显著地变小。在hmgb1肽(1-44)给药组中,与对照组相比,体重减少得到抑制,dss饮水第10天的体重与对照组相比显著地大。
ii)结肠长度
如图5所示,在对照组的ibd小鼠模型的结肠长度与正常小鼠相比显著性地变短的条件下,hmgb1肽(1-44)给药组的结肠长度与对照组相比显著性地长(正常小鼠参照“水”,对照组参照“dss+生理盐水”,hmgb1肽(1-44)给药组参照“dss+1-44”)。该结果表明,作为ibd模型的dss诱发肠炎中的结肠的缩短通过给药hmgb1肽(1-44)而被抑制。
iii)粘膜组织
将dss饮水第10天的结肠组织的he染色图像示于图6(正常小鼠参照“水”,对照组参照“dss+生理盐水”,hmgb1肽(1-44)给药组参照“dss+1-44”)。对照组的ibd小鼠模型中粘膜组织损伤,而hmgb1肽(1-44)给药组中粘膜组织的损伤被抑制。该结果表明,作为ibd模型的dss诱发肠炎中的结肠粘膜组织的损伤通过给药hmgb1肽(1-44)而被抑制。
实施例3
hmgb1片段肽对炎症性肠病的有效性的评价(3)
(1)材料和方法
i)药剂及小鼠
dss水溶液和hmgb1肽(1-44)的制备以及炎症性肠病小鼠模型的制作与实施例1相同。
ii)含肽水凝胶的制备
向切成约5mm×5mm大小的生物体吸收性水凝胶(medgel(注册商标)pi5、株式会社medgel制)中滴加20μl以生理盐水为溶剂调整为5μg/μl的浓度的hmgb1肽(1-44)溶液而使其含有,将冰冷下静置30分钟后的水凝胶用于对hmgb1肽(1-44)给药组的小鼠的埋入。另外,按照与此相同的步骤,将含有生理盐水以代替hmgb1肽(1-44)溶液的水凝胶用于对对照组的小鼠的埋入。
iii)肽的给药
将如实施例1中记载那样制成的ibd小鼠模型分成hmgb1肽(1-44)给药组(n=3)和对照组(n=3)。受试物质的给药通过如下来进行:在dss水溶液的饮水开始的1天前,将如上制备的含有hmgb1肽(1-44)溶液的水凝胶埋入到小鼠的背部。在对照组的小鼠的背部在dss水溶液的饮水开始的1日前,埋入如上制备的含有生理盐水的水凝胶。不对正常小鼠(n=3)进行物质的给药。
iv)肽给药带来的效果的评价
从dss水溶液的饮水开始至结肠摘出时为止,每天测定小鼠的体重。在dss饮水第10天从小鼠摘出结肠,测定结肠长度。
(2)结果
i)体重变化
将试验期间中的小鼠的体重变化示于图7(正常小鼠参照“水”,对照组参照“dss+pi5生理盐水”,hmgb1肽(1-44)给药组参照“dss+pi51-44”)。ibd小鼠模型(对照组和hmgb1肽(1-44)给药组)的体重随着天数的经过而减少,dss饮水第10天时与正常小鼠相比变小。在hmgb1肽(1-44)给药组中,与对照组相比,体重减少得到抑制,dss饮水第10天的体重与对照组相比较大。
ii)结肠长度
如图8所示,在对照组的ibd小鼠模型的结肠长度与正常小鼠相比变短的条件下,hmgb1肽(1-44)给药组的结肠长度与对照组相比较长(正常小鼠参照“水”,对照组参照“dss+pi5生理盐水”,hmgb1肽(1-44)给药组参照“dss+pi51-44”)。该结果表明,作为ibd模型的dss诱发肠炎中的结肠的缩短通过给药hmgb1肽(1-44)而被抑制。
比较例1
炎症性肠病模型中间充质干细胞(mscs)的给药
近年来,尝试了将从生物体取出的间充质干细胞用于炎症性肠病的治疗。另一方面,本发明者们到目前为止,发现hmgb1肽(1-44)具有将骨髓内的间充质干细胞动员到末梢血中的作用。因此,为了比较给药间充质干细胞与给药hmgb1肽(1-44)的效果,进行了以下的实验。
(1)材料和方法
i)药剂及小鼠
dss水溶液和hmgb1肽(1-44)的制备以及炎症性肠病小鼠模型的制作与实施例1相同。
ii)间充质干细胞的给药
将如实施例1中记载那样制成的ibd小鼠模型分成间充质干细胞(msc)给药组(n=3)和对照组(n=3)。从c57bl/6小鼠(6~8周龄、雄性)的大腿骨采集骨髓,作为培养基使用mesencult(商标)mscbasalmedium(mouse)(stemcelltechnologies公司制、包含10nmrockinhibitor和mesenpure),在塑料板上进行培养,由此得到作为附着性菌落的间充质干细胞。在dss饮水第5天,将传代3次后的上述间充质干细胞悬浮在pbs中并调整为1×106个/ml,向msc给药组的小鼠的腹腔内给药100μl。对照组的小鼠在dss饮水第5天,向腹腔内给药100μl的pbs。不对正常小鼠(n=3)进行物质的给药。
iii)间充质干细胞给药带来的效果的评价
至dss水溶液的饮水开始后第9天为止,每天测定小鼠的体重。
(2)结果
将试验期间中的小鼠的体重变化示于图9(正常小鼠参照“水”,对照组参照“dss+pbs”,msc给药组参照“dss+mscs”)。ibd小鼠模型(对照组和msc给药组)的体重随着天数的经过而减少。在msc给药组与对照组之间,体重变化没有差异,未观察到由msc给药带来的改善效果。
在本比较例的条件下,给药间充质干细胞并没有抑制炎症性肠病小鼠模型的体重减少,但hmgb1肽(1-44)对于在与此相同的条件下制作的炎症性肠病小鼠模型显示出改善体重减少等症状的效果。由此可期待,对于通过给药间充质干细胞无法获得效果的炎症性肠病的患者,本申请的肽也有效。
产业上的可利用性
可期待含有本申请的肽的药物组合物会对通过现有的治疗药无法获得充分的效果的炎症性肠病的患者带来巨大的好处。
序列表
<110>斯特姆里姆有限公司
国立大学法人大阪大学
<120>炎症性肠病的治疗药
<130>g6-a1801p
<150>us62/593,310
<151>2017-12-01
<150>jp2018-020686
<151>2018-02-08
<160>3
<170>patentinversion3.5
<210>1
<211>44
<212>prt
<213>人工序列
<220>
<223>人工合成的肽序列
<400>1
metglylysglyaspprolyslysproargglylysmetsersertyr
151015
alaphephevalglnthrcysargglugluhislyslyslyshispro
202530
aspalaservalasnpheserglupheserlyslys
3540
<210>2
<211>215
<212>prt
<213>智人
<400>2
metglylysglyaspprolyslysproargglylysmetsersertyr
151015
alaphephevalglnthrcysargglugluhislyslyslyshispro
202530
aspalaservalasnpheserglupheserlyslyscyssergluarg
354045
trplysthrmetseralalysglulysglylysphegluaspmetala
505560
lysalaasplysalaargtyrgluargglumetlysthrtyrilepro
65707580
prolysglygluthrlyslyslysphelysaspproasnalaprolys
859095
argproproseralaphepheleuphecysserglutyrargprolys
100105110
ilelysglygluhisproglyleuserileglyaspvalalalyslys
115120125
leuglyglumettrpasnasnthralaalaaspasplysglnprotyr
130135140
glulyslysalaalalysleulysglulystyrglulysaspileala
145150155160
alatyrargalalysglylysproaspalaalalyslysglyvalval
165170175
lysalaglulysserlyslyslyslysglugluglugluaspgluglu
180185190
aspglugluaspgluglugluglugluaspglugluaspgluaspglu
195200205
glugluaspaspaspaspglu
210215
<210>3
<211>648
<212>dna
<213>智人
<400>3
atgggcaaaggagatcctaagaagccgagaggcaaaatgtcatcatatgcattttttgtg60
caaacttgtcgggaggagcataagaagaagcacccagatgcttcagtcaacttctcagag120
ttttctaagaagtgctcagagaggtggaagaccatgtctgctaaagagaaaggaaaattt180
gaagatatggcaaaagcggacaaggcccgttatgaaagagaaatgaaaacctatatccct240
cccaaaggggagacaaaaaagaagttcaaggatcccaatgcacccaagaggcctccttcg300
gccttcttcctcttctgctctgagtatcgcccaaaaatcaaaggagaacatcctggcctg360
tccattggtgatgttgcgaagaaactgggagagatgtggaataacactgctgcagatgac420
aagcagccttatgaaaagaaggctgcgaagctgaaggaaaaatacgaaaaggatattgct480
gcatatcgagctaaaggaaagcctgatgcagcaaaaaagggagttgtcaaggctgaaaaa540
agcaagaaaaagaaggaagaggaggaagatgaggaagatgaagaggatgaggaggaggag600
gaagatgaagaagatgaagatgaagaagaagatgatgatgatgaataa648
- 还没有人留言评论。精彩留言会获得点赞!