麻醉管理的系统及方法与流程
本文公开的实施例整体上涉及系统、方法及设备,以评估及管理麻醉与镇静对于患者的认知作用的系统、方法及设备。
技术实现要素:
公开的实施例包括使用一脑电波(eeg)监控设备以进行麻醉管理的系统及方法。更具体地,所述公开的实施例涉及使用脑电波以即时确定系统性及/或局灶性脑功能障碍的系统、方法及设备。所述公开的实施例亦可用于监控所述患者的一麻醉深度及/或识别一潜在的脑中风、术中脑中风、脑震荡或脑外伤。
美国麻醉医师学会(asa)已知手术后的认知改变及妄想症是所需解决的主要健康挑战。因各种包括年龄的增加、经历手术后妄想症(pod)的风险因素,估计约12%-50%的外科手术患者会产生手术后的认知改变及妄想症。经报告的手术后认知功能障碍(pocd)的发生率亦有所不同。例如,据报道,心脏手术后pocd的发生率为30-80%,而在主要的非心脏手术中,在所有年龄层的成年人中有30-40%被诊断为pocd。美国目前超过三分之一的住院手术是针对65岁或65岁以上的患者进行,由于在未来的数十年,美国65岁以上人口的比例持续急剧地增加,因此,预期此数字将被提高。每年pocd的医院系统的直接成本在于18至200亿美元之间。估计表明,每年照顾pod及pocd的患者的花费超过1500亿美元。
过度麻醉与pod及pocd的风险增加有关,但是麻醉不足与在一手术过程中患者回忆或意识的风险有关。双谱指数(bis)用于检测麻醉患者的麻醉深度。此指数取决于患者的脑电波及肌电波。用于计算所述双谱指数的装置(bis装置)已被广泛采用于麻醉学。通常,对于失去意识的高风险患者或过度地深度麻醉的高风险患者,建议在全麻期间使用基于eeg的麻醉深度监控仪。
然而,bis不一定提供所述麻醉深度的准确测量。例如,bis值可为药物依赖性的。服用引起神经肌肉阻滞的药物的患者可能具有异常的bis值。当实际上仅对彼等进行轻度麻醉时,此等患者可能根据其bis值而呈现深度的麻醉。结果,此患者可能在手术期间麻醉不足,从而使她记住所述手术,或者在所述手术期间经历焦虑、意识或疼痛。
所公开的实施例包括用于治疗麻醉患者的一第一方法。所述第一方法可包括一连串的操作。所述操作包括确定所述患者是否在麻醉期间冒着意识的风险。此确定可至少部分地通过在向所述患者呈现一刺激的期间,自所述被麻醉患者的头部上的多个eeg电极接收至少一信号,而实现确定患者是否在麻醉期间冒着意识。所述多个eeg电极可包括一前电极及一后电极。产生多个分段后验指数值可包括使用至少一信号产生多个经滤波的eeg信号历元;以及使用所述多个经滤波的eeg信号历元以产生多个历元值;以及使用所述多个历元值以产生所述多个分段后验指数值。倘若多个分段后验指数值满足在麻醉期间意识的一风险标准,则可增加所述麻醉患者的一麻醉深度。倘若多个分段后验指数值不满足对于所述麻醉并发症的所述风险标准,则可保持所述麻醉患者的一麻醉深度。
增加所述麻醉患者的所述麻醉深度可包括:施用一麻醉剂,提高一麻醉剂的一给药速率,或施用一麻醉激动剂。产生所述多个经滤波的eeg信号历元可包括:使用一滤波器,所述滤波器具有5-9hz的一较低截止频率及11-15hz的一较高截止频率中的至少一者,以对所述至少一信号进行滤波。使用所述多个经滤波的eeg信号历元以产生所述多个历元值可包括使用多个有效历元,以识别多个有效历元以及产生多个历元值。识别多个有效历元可进一步包括识别多个有效片段。确定所述患者是否在麻醉期间冒着意识的风险,可进一步包括基于所述多个分段后验指数值以产生一整体后验指数值。所述风险标准的满足可取决于所述整体后验指数值。使用所述多个经滤波的eeg信号历元以产生所述多个历元值包括:识别多个无效的历元及/或多个无效的片段。当在所述历元其间的一经滤波的eeg信号无法满足一相对的波幅标准时,多个历元可为无效的。当一定比例的包含多个片段的所述多个历元是无效时,所述多个片段是无效的。所述多个历元值可包括基于所述至少一前电极的多个eeg信号的多个前值,以及基于所述至少一后电极的多个eeg信号的多个后值。
所公开的实施例包括第一诊断设备。所述第二诊断设备可包括至少一处理器;以及至少一计算机可读介质存储指令。所述计算机可读介质存储指令可存储指令,当所述计算机可读介质所存储的多个指令由所述至少一处理器执行时,会使所述诊断设备执行多个操作。所述多个操作可包括在向一患者呈现一刺激的期间,自所述患者的头部上的多个eeg电极接收至少一信号。所述多个eeg电极可包括至少一前电极以及至少一后电极。所述多个操作可进一步包括使用使用所述至少一信号产生多个滤波后的eeg信号历元;使用所述多个经滤波的eeg信号历元以产生多个历元值;以及基于所述多个分段后验指数值显示一指示。
产生所述多个经滤波的eeg信号历元可包括:使用一滤波器,所述滤波器具有5-9hz的一较低截止频率及11-15hz的一较高截止频率中的至少一者,以对所述至少一信号进行滤波。使用所述多个经滤波的eeg信号历元以产生所述多个历元值可包括:使用多个有效历元,以识别多个有效历元以及产生多个历元值。所述多个操作可进一步包括:基于所述多个分段后验指数值以产生一整体后验指数值。所述指示是基于此整体后验指数值。使用所述多个经滤波的eeg信号历元以产生所述多个历元值可包括:识别多个无效的历元及/或多个无效的片段。当在所述历元其间的一经滤波的eeg信号无法满足一相对的波幅标准时,多个历元可为无效的。当一定比例的包含多个片段的所述多个历元是无效时,所述多个片段是无效的。所述多个历元的持续时间可介于大约500毫秒与3秒之间。多个片段可包括大约介于5至20个连续的多个历元。所述多个历元值可包括基于所述至少一前电极的多个eeg信号的多个前值,以及基于所述至少一后电极的多个eeg信号的多个后值。使用所述多个历元值以产生多个分段后验指数值可包括:确定在一片段中满足一相对的历元值标准的多个有效历元的一计准。
所公开的实施例包括用于治疗一麻醉患者的一第二方法。所述第二方法可包括一连续的多个操作。所述多个操作可包括确定所述患者是否冒着一麻醉并发症的风险。至少部分可通过以下方式进行此确定:在向所述患者呈现一刺激的期间,自所述被麻醉患者的头部上的一成对eeg电极接收至少一信号,并产生一同步值,以确定所述患者在麻醉期间是否冒着意识的风险。所述成对电极可包括一左半球电极及一右半球电极。所述产生可包括使用所述至少一信号产生多个经滤波的eeg信号历元;使用所述多个经滤波的eeg信号历元以产生多个历元值;使用所述多个历元值计算一同步值;以及根据所述同步值显示一指示。倘若所述多个同步值满足对于所述麻醉并发症的一风险标准,则可降低所述麻醉患者的一麻醉深度或者执行一手术干预。倘若所述多个同步值不满足对于所述麻醉并发症的所述风险标准,则可保持所述麻醉患者的所述麻醉深度。
所述麻醉并发症可包括术后妄想症、术后认知能力退化、相对低血压、相对低氧或相对低血糖。降低所述麻醉患者的所述麻醉深度可包括延迟一麻醉剂量的施用、降低一麻醉剂的一给药速率,或施用一逆转剂;且其中所述手术干预包括一血栓切除术。所述手术干预可包括一血栓切除术。所述多个操作可进一步包括:倘若所述多个同步值满足术中脑中风风险标准,则提供术中脑中风的一指示。
产生所述多个经滤波的eeg信号历元可包括使用一滤波器,所述滤波器具有至少一0.5-2hz的一较低截止频率及3-5hz的一较高截止频率,以对所述至少一信号进行滤波。所述多个历元值可包括针对所述第一电极及所述第二电极的多个经滤波的eeg信号的多个统计量度。所述多个历元值可包括针对所述左半球电极的一组多个历元值及针对所述右半球电极的一组多个历元值。所述同步值可包括在与所述左半球电极相关的所述一组多个历元值以及与右半球电极相关的所述一组多个历元值之间所计算的一皮尔逊相关系数或一斯皮尔曼相关系数。计算所述同步值可包括识别一组多个连续有效历元,所述一组多个连续有效历元具有大于5个连续历元的一预定最小尺寸及/或小于60个连续历元的一预定最大尺寸。多个有效历元可满足一相对的波幅标准。
所公开的实施例包括一第二诊断设备。所述第二设备可包括至少一处理器及至少一个计算机可读介质。所述计算机可读介质可存储多个指令,当所述多个指令由所述至少一处理器执行时,会使所述诊断设备执行多个操作。所述多个操作可包括在向所述患者呈现一刺激的期间,自所述被麻醉患者的头部上的一成对eeg电极接收至少一信号。所述成对可包括一左半球电极及一右半球电极。所述多个操作可进一步包括使用所述至少一信号以产生多个经滤波的eeg信号历元;使用所述多个经滤波的eeg信号历元以产生多个历元值;使用所述多个历元值计算一同步值;以及根据所述同步值显示一指示。
所述指示可涉及所述患者是否正在经历或已经历过一脑震荡或一脑中风。该指示可涉及所述患者是否患有局灶性脑损伤。产生所述多个经滤波的eeg信号历元可包括使用一滤波器,所述滤波器具有至少一0.5-2hz的一较低截止频率及3-5hz的一较高截止频率,以对所述至少一信号进行滤波。所述多个历元值可包括针对所述第一电极及所述第二电极的多个经滤波的eeg信号的多个统计量度。所述多个历元值可包括针对所述左半球电极的一组多个历元值及针对所述右半球电极的一组多个历元值。所述同步值可包括在针对所述左半球电极的所述一组多个历元值以及针对所述右半球电极的所述一组多个历元值之间所计算的一皮尔逊相关系数或一斯皮尔曼相关系数。计算所述同步值可包括识别一组多个连续有效历元,所述一组多个连续有效历元具有大于5个连续历元的一预定最小尺寸及/或小于60个连续历元的一预定最大尺寸。所述左半球电极及所述右半球电极可对称放置于所述患者的头部。所述左半球电极及所述右半球电极可为多个额部电极。所述刺激是一听觉畸变试验。
应当理解,前述普通的描述及以下详细的描述皆仅是示例性及说明性的,并不限制如所要求保护的公开实施例。
附图说明
附图并非按比例或详尽。取而代之,强调的重点一般是在于本文所述的实施例的原理上。结合于本说明书中且构成本说明书的一部分的附图示出与本公开一致的数个实施例,并与说明书一起用于解释本公开的原理。在图式中:
图1a至图1e示出各种示例性事件相关电位的组成;
图2a示出在三种临床状态下的多个bis值的一示例性比较;
图2b示出根据设想的系统及方法对于四种临床状态所生成的指数的示一例性比较;
图3示出bis对规范化emg的依赖关系与预期索引的示例性比较;
图4说明一局部的功能障碍指数及一扩散功能障碍指数的诊断意义。
图5示出多个eeg信号的一示例性分析。
图6示出用于获取多个eeg信号的一示例性设备。
图7示出用于调整置放一患者上的图6的所述示例性装置在的一示例性方法。
图8示出用于检测系统性脑功能障碍的方法。
图9示出用于检测局灶性脑功能障碍的方法。
图10a至图10f示出一项研究的结果,所述研究证实多个同步指数值可识别冒着pocd风险的麻醉患者。
图11至图12d示出一项研究的结果,所述研究证实多个后验指数值可识别在麻醉期间冒着意识风险的麻醉患者。
图13示出一示例性标准,所述示例性标准用于确定适当的镇静剂量,以避免妄想症及回忆二者。
图14示出一项研究的结果,所述研究证实多个同步指数值可识别可能已经历术中脑中风的麻醉患者。
图15示出一种用于治疗冒着一麻醉并发症风险的麻醉患者的方法。
图16示出一种用于治疗在麻醉期间冒着意识风险的一麻醉患者的方法。
图17示出一项研究的结果,所述研究证实多个同步指数值可识别患有脑震荡的患者。
具体实施方式
参考说明将详细记载于示例性实施例,且与附图进行讨论。在某些情况下,于整个附图及以下的描述中将使用相同的参考标号,以代表相同或相似的部分。除非另有定义,否则技术的及/或科学的术语具有本领域普通技术人员一般理解的含义。所公开的实施例已被详细描述,使本领域技术人员能够实践所公开的实施例。应当理解,在不背离所公开的实施例的范围的情况下,可利用其他实施例,且可进行改变。因此,材料、方法及实例仅是说明性的,并不意图是限制性的。
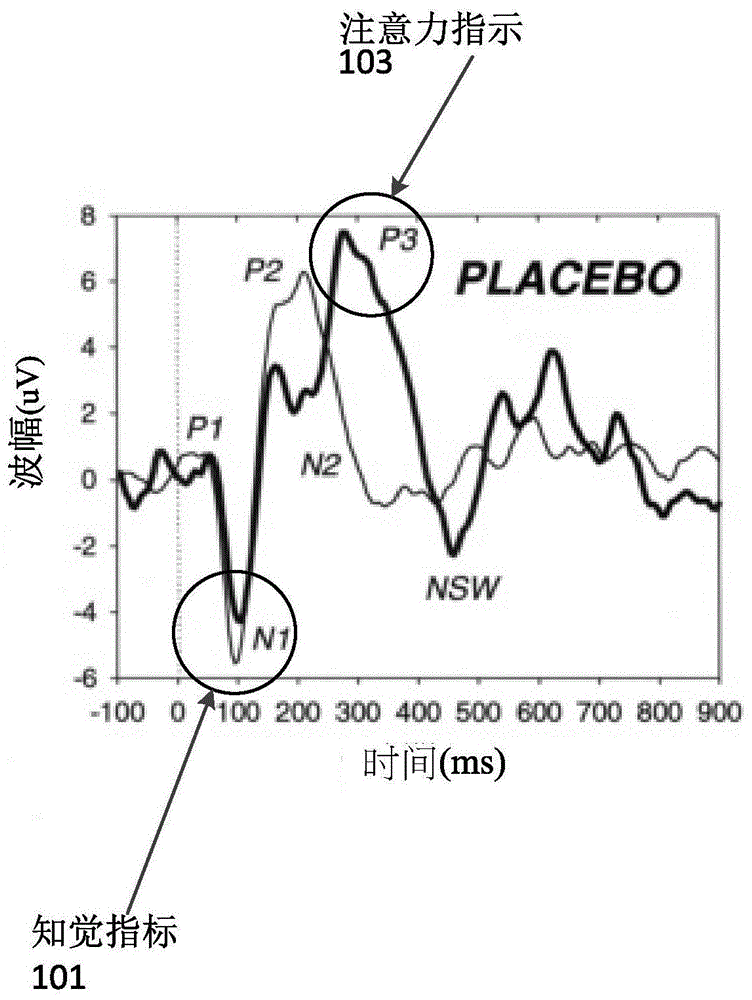
某些公开的实施例可使用多个事件相关电位(erp)以改善用于检测患者脑功能障碍及检测患者的麻醉深度的习知方法。如本领域已知一erp是对于一刺激的一定型电生理反应。例如,多个erp可使用视觉、听觉或触觉刺激以触发。图1a示出与所公开的实施例一致的一示例性erp的组成。所述示例性erp中所示出的组成包括数个正向峰值(p1、p2及p3)及数个负向峰值或波纹(n1、n2及nsw)。此等峰及波纹反映大量神经元的协调作用,并局限于某些神经解剖结构。此等神经解剖结构亦与某些金属过程相关,例如记忆、注意力及知觉。多个药物会影响此等神经解剖结构的活动,从而对多个erp产生可衡量的影响。因此,一药物对于erp的影响可与所述药物对于在一神经解剖结构内的活动的作用有关。对于所述神经解剖结构的影响可造成对于所述患者的临床参数的影响的结果,例如记忆、注意力或知觉。因此,多个erp提供一机制,所述机制用于估计一特定药物对于一特定神经生物学过程的影响。
如图1a至1d所示,一听觉erp的n1及p3峰可与一患者的麻醉程度和镇静程度相关。所述n1峰与知觉(知觉指标101)相关,所述知觉是多个刺激进入中枢神经系统的门控。所述p3峰与刺激处理的注意力(注意力指标103)相关。使用芬太尼而达镇静的一患者显示所述p3峰降低(注意力),而n1峰并未显示降低(知觉)。相反的,使用异丙酚而达麻醉的一患者显示所述n1峰降低(知觉)且p3峰并不存在(注意力)。在erp中的此等变化是剂量依赖性的。例如,如图1d所示,n1峰随着血液中丙泊酚的浓度的增加而降低。此外,听觉erp的组成显示一空间依赖性。使用多个后电极以进行eeg检测可在多个erp中显示一更明显的n1峰,而使用多个前电极以进行eeg检测可在多个erp中显示一个更显着的p3峰。如同原始的eeg数据,经滤波的eeg数据在一听觉erp期间显示变化,所述听觉erp表明知觉及注意力。例如,如图1e所示,一患者在一听觉erp期间可展现重复的早期alpha活动及重复的持久delta活动。在一些方面,使用一听觉畸变试验触发的不同电极(例如,后电极及前电极)的周围刺激α或δ活动可用于评估注意力及知觉。以此种方式,一erp(诸如一听觉erp)可提供所施用药物对于一患者的中枢神经系统功能的影响的即时检测。
如图所示,镇静催眠药物可在多个erp波形(诸如听觉erp波形)中产生全然的变化。增加麻醉可减低注意力,其可通过使用多个前电极以检测p3并进行量化。进一步增加麻醉可降低知觉,其可通过使用多个后电极检测n1并进行量化。相反地,bis设备仰赖多个前电极,以限制n1的检测,且基于eeg/emg,可能会混淆eeg和emg的检测。
所公开的系统及方法可使用自多个erp波形所衍生的注意力及知觉的检测,以监测麻醉深度。通过确定特定的多个erp波形模式可衍生出此等检测结果。可使用多个模板识别此等模式。在一些实施例中,所公开的系统及方法可使用多个电极。例如,所公开的系统及方法可具有多个顶电极(例如,在10至20个电极设置中的所述p3及p4电极位置)。额外地或替代地,所公开的系统及方法可使用多个额部电极(例如,在10至20个电极设置中的所述f3及f4电极位置)。
在一些实施例中,所公开的系统及方法可计算一系统性脑功能障碍指数,所述系统性脑功能障碍指数代表一临床状态,例如,麻醉深度。可使用erp模式计算此指数。在一些方面,可在较短的采样周期内计算此指数,从而可对麻醉深度进行时间轴特定的检测。此指数可独立于emg。在一些方面,此指数能够区分临床状态(例如,具有回忆的轻度镇静及无回忆的轻度镇静)。因此,此系统性脑功能障碍指数可协助临床医师,以确定当前的麻醉水平是否足以在镇静期间内避免回忆。以此种方式,设想的系统性脑功能障碍指数可防止不必要的高麻醉剂量,所述剂量可能会使一患者处于pocd或pod的风险中。
图2a及2b示出通过所述设想的指数对多个bis指数进行改善。评估三组患者:全身麻醉、轻度镇静及深度镇静的患者。术中使用标准asa监测仪对患者进行监测,所述监测包括一脉搏血氧仪、心电图、无创血压仪及一温度监测仪;bis监测仪;以及根据所公开的系统及方法所配置的一eeg监测器(一emotivepoc)。在此研究中,所述bis监测器使用多个前(额)电极,而所述eeg监测器则使用前(额)及后(顶)电极二者。在麻醉后护理单位,患者完成一brice问卷,以评估术中意识。根据回忆的评估对患者进行分类。图2a示出在三种临床状态下的bis的一示例性比较。如图所示,在具有回忆的镇静(轻度镇静)及无回忆的镇静(深度镇静)的患者之间,bis并未显示显着差异。图2b示出根据设想的系统及方法,针对四种临床状态所产生的指数的一示例性比较。相较于bis,通过根据所公开的系统及方法配置的所述eeg监测仪所计算的所述设想指数,可区分具有回忆的镇静与无回忆的镇静。如本领域技术人员所理解,在某些情况下,深度镇静与全身麻醉之间可能不具临床相关的差异。
图3示出对于bis的归一化emg的依赖性及所述设想的指数的一示例性比较。如图所示,bis是归一化emg的一增加函数(p值约为0.01)。相反地,所述设想的指数显示独立于归一化emg(p值约为0.26)。如本领域技术人员所理解,bis对于归一化eeg的依赖性可导致麻醉不足的患者施用引起神经肌肉阻滞的药物的结果。
图4示出一局部功能障碍指数及一扩散功能障碍指数的所述诊断意义。如图4所示,多个神经信号可用于确定一局部功能障碍指数(ldi)或一扩散功能障碍指数(sdi)。
所述sdi可表明脑功能的一整体水平。一麻醉患者的sdi可受麻醉水平的影响,且可为术后妄想症的一预测指标。低的sdi值表明存在整体功能障碍。所述sdi值可取决于后知觉的活动。可基于额部活动而将此后知觉活动归一化。可使用脑电波确定后部和额部活动。例如,后部及额部活动可从所述患者的脑波图的α含量(例如,在大约7-13hz的频率范围内的脑波图的含量)而得到。可从两侧确定后知觉活动及额不活动(例如,使用来自于两个额部电极及两个后电极的多个信号)。所述sdi值的确定可在停止测试时或在测试之后的测试过程中进行。可使用一经记录的脑波图进行确定。
ldi可以指示局灶性脑损伤。麻醉患者的ldi可能会受到海马网络功能障碍或中风的影响。ldi可以预测术后认知功能障碍。ldi的低值表示局灶性损伤。ldi可以取决于额叶活动水平的左右半球之间的同步程度。针对ldi的目的,此等活动水平可从所述患者的一脑波图的所述δ增量含量中得到(例如,所述脑波图的含量小于约4hz)。可将其他的患者的ldi值变化与先前确定的其他患者的ldi值变化进行比较。一ldi值变化的诊断意义可取决于具体情况-相较于脑震荡患者,大脑中风患者展现较大的ldi值变化。因此,先前确定的其他患者的ldi值变化可用于评估于当前患者中检测ldi变化的一诊断意义。
根据所述设想的系统及方法,整体功能障碍相对于局灶性损伤的差异诊断可涉及计算所述ldi及sdi。在一些实施方式中,此计算可包括将所述ldi及sdi归一化为临床人群。所述差异诊断可取决于ldi及sdi中较低的一者。例如,在一手术室的环境中,低于ldi的一sdi可表明麻醉药的过度使用(可能导致术后妄想症),而低于sdi的一ldi则可表明低氧、低血压、低血糖、栓塞或局灶性损伤(可能导致慢性术后认知能力降低)。作为另一实例,在手术室的环境中,低于ldi的一sdi可表明一药物过量或多个系统性疾病,而低于sdi的一ldi则可表明一脑中风、脑炎或一癫痫发作。作为一进一步的实例,当诊断可疑的头部创伤时,低于ldi的一sdi可表明严重的疼痛或焦虑,而低于sdi的一ldi则可表明一脑震荡或脑出血。通常,正常的脑功能可由大于一阈值的sdi以及大于一阈值的ldi表示。
图5示出多个eeg信号的一示例性sdi分析。如图5所示,可向一患者提供一连串的刺激(例如,刺激501a及刺激501b)。在一些实施例中,所述刺激可为听觉刺激。例如,如本领域的技术人员所熟悉,所述一连串的刺激可构成一听觉畸变试验。在此一连串的刺激中,所述刺激的大约70%至90%可处于一第一音调(例如,10000hz),且在此一连串的刺激中,其余的刺激物可处于一第二音调(例如,2000hz)。在一些实施例中,所述sdi分析可限于以单一音调(例如,所述第二音调)所提供的刺激。在各种实施例中,所述sdi分析可包括在第一和第二音调两者处提供的刺激。在一些实施例中,一连串的刺激可包括2-20或5-15个刺激(或在一连串的刺激中的此种数量的畸变刺激,包括额外的非畸变刺激)。替代地或额外地,可向患者呈现视觉或触觉的畸变刺激。
在一些实施例中,对于一连串刺激中的各个刺激,所述sdi分析可被限制为一周围刺激间隔。此刺激周围间隔可包括一刺激前间隔(例如,刺激前间隔503a、刺激前间隔503b)及一刺激后间隔(例如,刺激后间隔505a、刺激后间隔505b)。所述刺激前间隔的持续时间范围可自100毫秒至500毫秒。刺激前间隔可在刺激发生时或在刺激发生之前结束。例如,所述刺激前间隔可在刺激发生之前的0-100毫秒结束。刺激后间隔的持续时间范围可为自100毫秒至500毫秒。所述刺激后间隔可在刺激发生时或刺激发生后开始。例如,所述刺激后间隔可在刺激发生后0-100毫秒开始。
在一些实施例中,所述sdi分析可包括计算周围刺激间隔的至少一活动水平。作为一额外的实例,所述sdi分析可包括计算一刺激前活动水平及一刺激后活动水平。可自一eeg信号的功率,或者自一特定的频带中的所述eeg信号的功率,例如在所述α频带(例如,大约7-13hz)的所述功率计算多个活动水平。所述刺激前活动水平可自在刺激前间隔期间的所述eeg信号的功率计算。所述刺激后活动水平可自在刺激后间隔期间的所述eeg信号功率计算。在一些实施例中,所述信号的功率可取决于所述eeg信号的一函数的积分或平均。此函数可包括所述eeg信号的所述绝对值。替代地或额外地,此函数可包括所述eeg信号的幂(例如,所述eeg信号的平方)。例如,所述刺激前活动水平可取决于在在所述刺激前间隔期间,所述eeg信号的绝对值的积分。类似地,所述刺激后活动水平可取决于,在所述刺激后间隔期间,所述eeg信号的绝对值的积分。
在一些实施例中,所述sdi分析可包括计算在所述刺激前活动水平与所述刺激后活动水平之间的活动水平的变化。例如,所述sdi分析可包括计算在所述刺激前活动水平与所述刺激后活动水平之间的差,或者在所述刺激前活动水平与所述刺激后活动水平之间的差的绝对值。
在一些实施例中,所述sdi分析可包括针对在所述刺激前活动水平与所述刺激后活动水平之间的活动水平的变化进行阈值化。例如,所述sdi分析可包括识别所述周围刺激间隔,所述周围刺激间隔的变化的幅度超过一个数值。作为一额外的非限制性实例,给定一连串的刺激中的一第一组刺激(或一连串的刺激中的畸变的第一组刺激包括额外的的非畸变刺激),所述sdi分析可包括确定一第二组相应的周围刺激间隔,所述第二组相应的周围刺激间隔的活动水平的变化的幅度超过一个数值。
在一些实施例中,所述sdi分析可排除无法满足某些标准的多个周围刺激间隔。例如,所述sdi分析可排除多个“嘈杂的”周围刺激间隔。排除来自于所述sdi分析中诸如多个“嘈杂的”周围刺激间隔可减低在电极电导内的变化的影响。在一些方面,多个“嘈杂的”周围刺激间隔包括可自所述分析中排除活动水平超过一最大阈值或无法超过一最小阈值的多个周围刺激间隔。作为一额外的实例,所述sdi分析可排除多个“未受影响”的周边刺激间隔。在一些方面,多个“未受影响的”周围刺激间隔包括周围刺激间隔,对于多个周围刺激间隔,在所述刺激前活动水平与所述刺激后活动水平之间的活动水平的变化超过一阈值。在一些实施例中,在识别多个“未受影响的”的周围刺激间隔之前,可排除多个“嘈杂的”周围刺激间隔。在各种实施例中,所述sdi分析可首先排除多个“嘈杂的”周围刺激间隔,且之后自多个其余的周围刺激间隔中排除多个“未受影响的”周围刺激间隔。在各种实施例中,所述sdi分析可首先排除多个“未受影响”的周围刺激间隔,且之后自多个其余的周围刺激间隔中排除多个“嘈杂的”周围刺激间隔。
在一些实施例中,所述sdi分析可包括基于所述未排除的周围刺激间隔以确定sdi。在一些方面,sdi可取决于一后活动水平与一前活动水平的比例。所述后活动水平可为针对多个电极所检测的后活动水平的最大值(例如,针对p3及p4上的电极所检测的活动水平的最大值)。前活动水平可为针对多个电极所检测的前活动水平的最大值(例如,针对f3及f4上的电极所检测的活动水平的最大值)。
在一些实施例中,所述sdi分析可包括将所述患者的sdi的变化与针对其他患者所计算的sdi的变化进行比较。在某些方面,所述其他患者可包括一相关的患者群体。例如,当评估麻醉深度时,可将在麻醉期间所述患者的sdi的变化与在麻醉期间其他患者的sdi的变化进行比较。相似地,当监控处于妄想症危险中的一患者时,可在此监控期间将所述患者的sdi的变化与其他患者的sdi的变化进行比较。所述sdi分析可包括基于比较所述患者的sdi的变化以及针对其他患者所计算的sdi变化,以确定所述患者是否表现出状况。
在一些实施例中,类似于上述的sdi分析,可执行ldi分析。如上关于图5所述,可向一患者提供一连串的刺激(例如,刺激501a及刺激501b)。此一连串的刺激可具有如上关于sdi分析所描述的相同的特征。在一些实施例中,相似于上述的sdi分析,所述ldi分析可包括所述计算周围刺激间隔的至少一种活动水平。所述ldi分析的活动水平可自一eeg信号的功率或在一特定频带中的所述eeg信号的功率中计算而得,所述特定频带诸如在所述β频带的功率(例如,小于约4hz)。可针对多个前电极(例如,电极f3及f4)以及多个后电极(例如,电极p3及p4)计算活动水平。
在一些实施例中,所述ldi分析可仅包括满足某些标准的刺激周围间隔。例如,所述ldi分析可仅包括周围刺激间隔,其中针对所述多个前电极的一活动水平(例如,针对所述多个前电极的多个活动水平的一最大值或所述多个前电极的多个活动水平的一平均值)大于所述后电极的一活动水平(例如,针对所述多个后电极的多个活动水平的一最大值或针对所述多个后电极的多个活动水平的一平均值)。有时在意识减弱的情况下呈现强烈的后活动(例如,睡眠纺锤)。此活动可在多个前电极中不对称地表现出来。排除多个周围刺激间隔可减低此后活动对于ldi计算的影响,所述多个周围刺激间隔为其中所述多个前电极的一活动水平小于所述后电极的一活动水平。
图6示出用于获取多个eeg信号的一示例性设备。在一些实施例中,此设备可包括符合一患者的头部的一柔性部件(例如,头带)。如图6所示,可将所述柔性部件配置为围绕所述患者的头部放置,且所述柔性部件的前中部设置为自所述患者的鼻根至头顶的距离的50%-70%。多个信号电极可设置于所述柔性部件的内部。例如,多个信号电极可设置在所述柔性部件内,使得当如图6所示的一患者佩戴所述柔性部件时,多个信号电极大约置于所述10-20个电极放置系统的所述f3、f4、p3及p4电极位置。至少一额外的参考电极可被附接至所述柔性部件。
一计算设备可连接至所述柔性部件。多个导线可将所述计算设备与所述信号电极及所述参考电极相连接。在一些实施例中,所述计算设备可被配置为使用所述多个信号电极以获取多个eeg信号(且在一些方面额外使用至少一参考电极)。所述计算设备可被配置为执行信号隔离、信号调节、数字或模拟滤波或模数转换中的至少一项。在一些实施例中,所述计算设备可被配置为处理所获取的多个eeg信号。例如,所述计算设备可被配置为执行以上关于图5所描述的至少一些所述sdi分析。另一计算设备,诸如移动设备、膝上型计算机、桌上型计算机、工作站、服务器或集群可被配置为:执行以上关于图5所述的所述sdi分析的其余部分(如果有的话)。在一些实施例中,所述计算设备可配置为将获取的所述多个eeg信号提供予另一计算机设备,之后,所述另一计算机设备随后可执行以上关于图5所述的所述sdi分析的至少一部分的操作。在一些实施例中,所述柔性部件搭配所述计算设备可包括设置于所述患者头部上的头戴式耳机。
图7示出用于调整图6的所述示例性装置置放于一患的一示例性方法。在步骤701开始之后,所述方法可包括在步骤703中确定所述前电极及后电极的多个活动水平。例如,可向所述患者提供一连串的刺激。如上所述,此等刺激可包括听觉、视觉或触觉刺激。如上关于图5所述,可在一连串的至少一刺激的周围刺激间隔期间内确定所述前电极及所述后电极的多个活动水平。例如,可确定在一连串的各个刺激(或各个“畸变”刺激)的一活动水平。
可在步骤705中确定一前/后比例。在一些实施例中,可使用一连串的至少一刺激以确定所述前/后比例。例如,可使用一连串的各个刺激(或各个“畸变”刺激)以确定比例。可自多个刺激的所述个别的比例中确定所述比例(例如,通过平均此等个别的比例)。个别的比率可与一第一阈值相比较。当个别的比例小于所述第一阈值时,所述调整过程可终止于步骤711。当所述比率大于所述第一阈值时,所述调整过程可前进至步骤707。所述第一阈值可介于1与2之间,或者介于1.2与1.6之间。
可在步骤707中使用多个刺激以确定后比例。此等刺激可包括一连串的至少一所述刺激(或一连串的至少一“畸变”刺激)。所述后比例可为此刺激数量中所述后活动水平超过所述前部活动水平的比例。例如,当所述一连串的刺激包括10个刺激时,可使用8个刺激以确定后比例。当此等8个刺激中的2个刺激的后活动水平超过所述前部活动水平时,所述后比例可为0.25。可将所述后比例与一第二阈值进行比较。当所述后比例小于所述第二阈值时,所述调整过程可终止于步骤711。当所述后比例大于所述第二阈值时,所述调整过程可前进至步骤709。所述第二阈值可介于0.1与0.9之间,或介于0.3与0.5之间。
可在步骤709中调整所述设备置放于所述患者身上的位置。在一些实施例中,应调整所述柔性部件,以降低所述后电极置放于所述患者的位置。在步骤709之后,所述调整过程可终止于步骤711。倘若所述示例性设备需要进一步的调整,则可重复图7中所示的方法。
图8示出检测系统性脑功能障碍的方法800。方法800可基于所述大脑的不同区域之间的大脑活动的比较。例如,方法800可包括将多个前脑活动水平与多个后脑活动水平进行比较。方法800可包括以下步骤:一在分析期间引起一脑反应、产生经滤波后的多个eeg信号片段及/或多个历元、针对多个有效历元产生成多个历元值、生成一分段后验指数,以及产生一整体后验指数。
在一些实施例中,方法800的所述多个步骤可至少部分同时地运行。例如,当在步骤801中引起脑反应时,可在步骤803中产生多个经滤波的eeg信号历元、当在步骤803中产生多个经滤波的eeg信号历元时,可在步骤805中产生多个有效历元的多个历元值、当在步骤805中产生多个有效历元的多个历元值时,可在步骤807中产生多个分段后验指数,及/或当在步骤807中产生多个分段后验指数,可在步骤809中产生多个整体后验指数。以此种方式,方法800的步骤可形成一处理管道,所述处理管道自经诱发的脑反应中产生多个分段后验指数。可选地,方法800的一或多个步骤可在方法800的一先前步骤完成时执行。
在起始之后,方法800可前进至步骤801。在步骤801中,可在一分析期间内诱发一患者的脑反应。如以上关于图5所述,可使用一听觉的、视觉的或触觉畸变试验,以诱发所述脑反应,或者能够在一患者中诱发一erp的另一试验。尽管被描述为一第一步,但在整个所述分析期间,此种激发一大脑反应的过程仍可继续进行。
步骤803中,可将记录系统配置为产生经滤波的多个eeg信号片段及/或历多个元。所述记录系统可包括多个电极,其可设置在一头戴式耳机的内部。例如,多个电极可设置在用于获取图6的多个eeg信号的所述示例性设备的内部,或者一类似的设备内部。在一些方面,所述记录系统可被配置为检测多个eeg信号、针对所述多个eeg信号进行滤波,以及将所述经滤波的eeg信号划分为多个片段及多个历元。
检测所述多个eeg信号可包括自附接至所述患者的多个电极接收多个eeg信号。在一些实施例中,具有四个电极。所述多个电极可在一标准位置连接至所述患者。所述多个电极可对称地连接于所述患者的中线的两侧。例如,所述多个电极可包括两个前电极。可以将所述多个前电极置放于与所述10-20个eeg电极的f3及f4所相对应的位置。作为一额外的实例,所述多个电极可包括两个后电极。可将所述多个后电极置放于与10-20个eeg电极的o1和o2所相对应的位置。在一些方面,可使用额外的多个电极,或者可将所述前电极及/或后电极放置在不同的位置。在各个方面,可使用一单个前电极及/或一单个后电极。
过滤所述eeg信号可包括对来自所述多个电极所接收的所述多个eeg信号进行带通滤波。此带通滤波可通过一单个滤波器或多个滤波器而实现。例如,所述记录系统可包括分开的多个低通及多个高通滤波器,彼等一起对于所接收的所述多个eeg信号进行带通滤波。在一些方面,可使用具有5-9hz的一较低的截止频率的一滤波器对于所述多个eeg信号进行滤波。在各个方面,可使用具有11-15hz的更高截止频率的滤波器对eeg信号进行滤波。在一些方面,所述单个滤波器或多个滤波器可被配置为选择所述αeeg频率范围。
可使用所述记录系统或另一计算系统以将所述分析期间划分为多个片段及/或多个历元。在一些实施例中,可以即时地实施划分(例如,当所述eeg信号被所述患者接收时)。在一些实施例中,所述eeg信号的所述分析可与事件无关。例如,将所述分析期间划分为多个历元可能与erp不同步。在此种方式中,关于图8所述的所述分析可与关于图5及图7所述的所述分析不同。作为一非限制性的实例,所述eeg信号的所述分析可与试验相关。在一些实施例中,将所述分析期间划分为多个历元可取决于分析何时开始及所述多个历元的长度。例如,所述记录系统可被配置为将所述eeg信号划分为相等或近似相等的多个片段。此等片段反过来又可划分为多个历元。在一些方面,所述多个历元的持续时间可为大约500毫秒至3秒长。在各种实施例中,一片段可包括5至20个连续的多个历元。或者,可将所述分析期间划分为与一连串刺激同步的多个历元,以使各历元皆包含相同或相似次数的刺激(例如,连续的多个历元可能在次数上相差少于三个刺激,或者少于刺激次数的10%)。
在步骤805中,所述记录系统可产生对于多个有效历元的多个历元值。此步骤可包括识别多个无效历元、识别多个无效片段以及生成多个历元值,所述历元值包括多个前值及多个后值。所述记录设备可使用来自所述电极的所述经滤波的eeg信号,以识别各电极的多个无效历元(例如,包括噪声信号、伪像、测量误差、混淆的emg信号等等的多个历元)。在一些方面,识别可取决于波幅标准及所述经滤波的eeg信号的波幅。所述波幅标准可为绝对或相对的标准。例如,当所述过滤的eeg超过一预定的波幅或未能超过一预定波幅时,所述记录设备可将来自一电极的一经过滤的eeg信号识别为无效。作为一额外的实例,当经所述经滤波的eeg超过或未能超过一相对的阈值时,所述相对的阈值是取决于在所述历元内的所述经滤波的eeg信号的一数值,则所述记录设备可将来自一电极的一经滤波的eeg信号识别为无效。此述值可为在所述历元内的所述经滤波的eeg信号的平均波幅。所述相对的阈值可为该数值的倍数。例如,所述相对的阈值可为在所述历元内的所述经滤波的eeg信号的平均波幅的倍数。在某些方面,识别可取决于可变性标准。例如,当所述历元内的所述经滤波的eeg信号的波幅的变化(或变化系数)超过预定阈值时,所述记录设备可将来自一电极的一经滤波的eeg信号识别为无效。
所述记录设备亦可被配置为在步骤805中进行分段。在一些实施例中,所述记录设备可被配置为,针对各段,当针对所述历元的多个所述经滤波的eeg信号中的任何一个无效时,自后续的分析中将所述历元排除为无效。时代无效。在不同的实施例中,所述记录设备可被配置为当一定比例的的多个历元无效时,自后续分析中排除所述片段。在一些实施例中,此比例可介于40%与60%之间。所述记录设备可被配置为使用所述剩余的多个历元以处理所述剩余的片段。
在步骤805中,所述记录设备可配置为产生成所述历元的前值及后值。在一些实施例中,可将所述记录设备配置为计算各电极的一电极值(例如,置放于10-20个标准电极的f3、f4、o1及o2位置)。在一些方面,在一位置中的一电极的所述电极值可为在针对所述电极的所述历元期间,所述经滤波的eeg信号的波幅的一函数。例如,所述电极值可为针对所述历元的所述电极的所述信号的功率。在不同的实施例中,所述记录设备可被配置为基于针对所述历元的多个所述电极值,以计算前值及后值。所述记录装置可被配置为通过使所述电极值的前值及/或后值作用,以避免多个半球之间的多个电极值的差异(例如,多个侧向效应)。例如,所述前值可为针对前放置的多个电极的所述多个电极值的一平均值,及/或后值可为针对后放置的多个电极的所述电极值的一平均值。作为一额外的实例,所述前值可为针对所述前放置的多个电极的所述多个电极值的最大值(或最小值),及/或后值可为针对后放置的多个电极的所述多个电极值的最大值(或最小值)。
在步骤807中,所述记录系统可产生多个片段后验指数。在一些实施例中,对于一有效片段,所述记录设备可被配置为确定片段中满足相对的历元值标准的多个有效历元的计数。在一些实施方式中,计数满足所述相对的历元值标准的多个有效历元可相较于多个经平均的后历元值及经平均的前历元值的多个函数较少的嘈杂。在一些方面,所述相对的历元值标准可为所述后历元值(所述后α检测)是否大于所述前历元值(所述前α检测)。在各个方面中,所述记录系统可被配置为计算一后历元值/前历元值比例的计算,且将此比例与一相对的历元值标准(例如,1.0)进行比较。在一些实施例中,所述记录系统可被配置为基于在所述多个片段中有效历元的计数及数量,以产生满足一相对的历元值标准的多个分段后验指数,如同满足所述相对的历元值标准的多个有效历元的比例。
在步骤809中,所述记录系统可产生作为多个有效分段的两个或更多个分段后验指数的一函数的整体后验指数。例如,所述记录系统可产生所述整体后验指数,以作为多个有效分段的多个分段后验指数的一中值、平均值或加权平均。可以在多个分段的一窗口上执行此生成,例如,eeg数据的最后3-10分段。
图9示出检测局灶性脑功能障碍的方法900。方法900可包括所述大脑的不同区域之间的大脑活动的一比较。例如,方法900可包括比较多个大脑半球之间的同步水平。同步水平的异常可表明pocd、pod、相对低血压、相对低氧或相对低血糖的风险增加。在一些方面,方法900可用于脑震荡或脑中风病例的分类(例如,识别指示脑导管需求的可行的一脑中风后半影区)。方法900可包括以下步骤:在一分析期间内诱发一大脑反应、产生多个经滤波的eeg信号片段及/或多个历元、针对一组多个有效历元产生多个历元值;以及针对所述多个有效历元组计算一同步值。
相似于上述方法800的所述多个步骤,如上所述,方法900的所述多个步骤可形成一处理管道,所述处理管道自经诱发的多个脑反应中产生整体后验指数。或者,方法900的一或多个步骤可在方法900的一先前步骤完成时执行。
在起始之后,方法900可前进至步骤901。在步骤901中,所述记录系统可配置为以相似于上文关于方法800的步骤801所述的方式而诱发一大脑反应。
在步骤903中,可将所述记录系统配置为以相似于上文关于方法800的步骤801所述的方式以产生多个经滤波的eeg信号段及/多个或历元。在方法900中,可使用置放于所述患者身上的一对或多对eeg电极(例如,两对eeg电极、四对eeg电极等)。此等电极可对称的放置。在一些方面,所述多个电极可为额部电极(例如,将多个电极置放于一标准10-20个eeg电极的f3及f4处)。在一些实施例中,所述记录系统亦可使用置放于所述患者身上的一参考电极。在一些实施例中,根据方法900,所述记录系统可使用0.5-2hz的较低截止频率及/或3-5hz的较高截止频率以滤波来自所述多个电极的多个eeg信号。在各个方面,根据方法900,所述记录系统可滤波来自所述多个电极的所述多个eeg信号,以选择所述δeeg频率范围。相似于根据方法800所执行的划分,所述记录系统可被配置为将所述分析期间划分为多个片段及/或多个历元。
在步骤905中,所述记录系统可产生用于多个有效历元的多个历元值。以与以上关于方法800的步骤805所述的方式相似的方式,所述记录系统可被配置为识别多个无效历元。在步骤905中,所述记录系统可被配置为识别一组连续的有效历元。所述组可具有大于5个连续的历元的一预定最小尺寸及/或小于60个连续历元的一预定最大尺寸。
所述记录系统可被配置为计算多个连续有效历元组中的各个有效历元的多个代表值。在一些方面,可为各个电极计算所述多个代表值(例如,可为在设置于一标准的10-20个电极的f3及f4处的各个电极计算多个代表值)。在一些实施例中,所述多个代表值可为在所述历元期间内,一经滤波的eeg信号的波幅的函数。例如,在历元期间内,来自一电极的一经滤波的eeg信号的所述代表值可为一统计量度,诸如在所述历元期间内的所述经滤波的eeg信号的所述波幅的平均值、中值或模式。
在步骤907中,所述记录系统可计算多个有效历元的组的一同步值。所数同步值可表明在患者的脑半球内的活动之间的一同步程度。在一些实施例中,所数同步值可为一皮尔逊相关系数,斯皮尔曼相关系数或一相似的相关性度量。可使用多个连续历元的组中多个历元的所述代表值以计算所述相关性度量。可使用所述第一电极的一组代表值及所述第二电极的一组代表值以计算相关度量。相关性增加意味着相关的同侧及对侧活动之间的同步性更高,反之亦然,相关性降低。
实例1:pocd研究
在以色列海法市的兰巴姆医学中心正在进行的2组100位患者研究获得初步的结果。第i组包括接受全膝关节置换术(tkr)及全髋关节置换术(thr)的骨科患者。此等程序大多数是在镇静及局部麻醉下进行的。第ii组药物包括接受全身麻醉(ga)手术的心脏病患者。研究设计包括术前认知测试,在过程中进行eeg监控,以及针对pocd的术后认知测试(术后约1周、3周及3个月)。
如图10a所示,初步结果(n=20及1周后的术后认知评估)证实根据方法900(半球间同步)所计算的指标水平与患者释放时的pocd之间具有统计学上显着的相关性。在完成三个月认知测试的患者中,进行随访,发现在第一周中约有50%的认知能力降低的患者在3个月后仍表现出术后认知能力降低。图10a中的条形图表示在此过程中同步最低时的10分钟内的平均同步值。pocd条是术后被识别为认知功能降低的患者的平均值。正常条是指认知功能未降低的患者的平均值。
如图10b至10d所示,额外的结果(总共n=48,包括25名骨科患者和23名心脏病患者)持续证明,根据方法900(半球间同步)所计算的指标水平与患者释放时的pocd之间存在一统计学上的显着相关性。维持高半球间同步指数的患者(如图10e所示)相较于在半球间同步的索引中(如图10f所示)经历持续(大于15分钟)降低的患者,发生认知功能持续降低的并发症的可能性显著地低(p<0.0001)。图10e及10f亦示出pocd的风险标准,其中指标值超过阈值0.8表明pocd的可能性较低,而指标值低于阈值0.7表明pocd的可能性较高。在一些实施例中,此种风险标准可取决于一幅波标准(例如,一阈值)及一持续期间或比例标准(例如,指标满足波幅标准多低或多频繁)。使用持续时间为10秒的连续历元的组产生如图10e及图10f中所示出的半球间同步值。
实例2:镇静安全性研究
在以色列海法市的兰巴姆医学中心进行51位参与者的研究。所述研究具有三组。第i组包括26例在镇静下接受手术的患者(其中18例使用咪达唑仑且8例使用异丙酚),第ii组包括12例在全身麻醉下接受手术的患者,以及第iii组包括13个清醒对照组。研究设计包括在手术过程中使用bis(medtronic)以及epoc(emotive)进行eeg监控,包括听觉刺激,之后进行术后回忆测试(经改良的brice问卷)。
在术后评估具有回忆的意识,并将其与根据方法800所计算的整体后验指数值以及麻醉的黄金标准深度监控仪(bed,来自medtronic)的结果进行比较。图11总结对于不同组别的患者的整体后验指数值(清醒、镇静(咪达唑仑)回忆、镇静(咪达唑仑)无回忆、镇静异丙酚及全身麻醉)。tukey事后检验显示,清醒患者及具有回忆的经镇静的患者(咪达唑仑)的平均整体总体后验指数值高于无回忆的经镇静的患者、使用异丙酚的经镇静的患者及全身麻醉的患者(p<0.01)。
可基于后验指数而非bis指数,将经历具有回忆的使用咪达唑仑镇静的患者与经历无回忆的使用咪达唑仑镇静的患者予以区分。详细分析的结果显示,bis无法识别具有回忆的意识的原因为eog/emg噪声。如图12c所示,增加的eog/emg活性与bis指数所增加的值相关联,从而损害确定麻醉深度的bis指数的使用。然而,如图12d所示,由于所述指标并不明确地依赖于emg,因此,此种噪声不会影响根据方法800所计算的指标。
图12a及图12b总结第i组(使用咪达唑仑镇静,18位患者)的术中监控结果与具回忆的术后意识之间的关联性。图12a及12b的条表示bis的平均整体后验指数值(图12a,p<0.001)及bis(图12b,p=0.48)。确定患者在术后具有回忆(回忆条)或无回忆(无回忆条)。此等结果证实后验指数值可用以作为麻醉下认知安全性的量度。此指标可提高术中镇静的安全性,其目的为尽可能投予最低剂量。
图13显示医师如何可使用后验指标值,通过评估较高的剂量水平避免妄想症及较低的剂量水平避免回忆,以提供患者最佳的剂量。此等图表显示两位不同的患者在手术过程中的后验指数值。一位患者(灰色线)在手术过程中具有回忆,另一位患者(黑色线)则无回忆。红色虚线是一阈值,在此实例中,所述阈值表明与无回忆相关的一最大后验指数值。倘若后验指数值在阈值线以下,则在此实例中,无需额外的镇静剂量。
实例3:脑中风导管研究
一项针对23位患者的研究(17位患者具有有效的术前样本、20位患者具有有效的术后样本)已证实,在镇静状态下使用根据方法900所计算的指标水平(半球间同步)检测脑中风动态。在进行急性脑中风的血栓切除术的前五分钟及后五分钟,计算麻醉患者的指标值。根据使用nih脑中风量表进行的随访患者评估的结果,所述血栓切除术之后被分类为成功或失败。如图14所示,由于半影状组织仍然可以存活,因此在血栓切除术之前,具有高的所述指标水平,且与一先前的研究中所获得的对照值相当。在成功干预之后,仍维持高的指数值,且可与对照及干预前值相媲美。在不成功的干预之后,指数值显着地降低(p<0.0001),且与一先前的研究中所获得的脑中风患者的指数值相当。如发明人所认知及理解的,所述公开的系统及方法可在一麻醉的患者术后检测出不成功的血栓切除术。如发明人进一步认知及理解的,所述公开的系统及方法可检测一麻醉患者的中风。
实例4:脑震荡研究
一项针对15位患有脑震荡(n=9)或局部肢体损伤(n=6,作为一对照组)的患者进行的研究证实,如上述关于图9所计算的一同步指数可用于确定脑震荡。如图17所示,脑震荡患者的同步指数值显著地低于局部肢体损伤的患者的同步指数值(p~0.01)。如发明人所认知及理解,所述同步指数可用于诊断脑震荡及/或脑外伤。
示例性治疗方法:
图15示出与所公开的实施例一致的用于治疗麻醉患者的方法1500。可在执行一外科手术的过程中执行方法1500。例如,可以在一患者正在进行一心脏手术、整形外科手术或另一种医学手术的同时执行方法1500。
在步骤1501中,一计算设备可接收一eeg信号。可自置放于患者身上的一对或多对eeg电极接收eeg信号。所述计算设备可通过一物理连接(例如,电线)及/或无线地可操作地连接至所述多个eeg电极。所述eeg信号可直接自eeg电极接收,亦可通过前置放大器或其他的信号调节设备而间接地接收。
在步骤1503中,所述计算设备可产生一同步值。所述同步值可代表患者大脑左右半球之间的同步程度。所述同步值可取决于前脑活动。可根据以上关于图9所述的方法900以计算所述同步值。所述计算设备可被配置为提供所述同步值的指示(例如,一视觉指示或一听觉指示中的至少一者)。
在步骤1505中,人员(例如,诸如医生或护士的从业人员)可确定同步值是否满足麻醉并发症的一个或多个风险标准(例如,术后妄想症、术后认知能力退化、相对低血压、相对低氧或相对低血糖)或术中脑中风。在一些实施例中,人员可基于所述同步值(或针对患者的同步值的一时间历史)以确定所述同步值是否满足一或多个风险标准。在一些实施例中,此确定可额外地取决于其他患者参数(例如,血压、血液氧合等等)。在各种实施例中,所述计算设备可配置用于一麻醉并发症或术中脑中风的一种或多种风险标准。当同步值满足一或多个风险标准中的至少一者时,所述计算设备可被配置为提供一指示(例如,一视觉指示或一听觉指示中的至少一者)。
在一些实施例中,风险标准可表达为预定的指标值阈值。例如,一预定的指标值阈值可表明pocd的风险(或术后妄想症、术后认知能力退化、相对低血压、相对低氧或相对低血糖)。在一些实施例中,此阈值可介于0.65与0.75之间。在各种实施例中,一预定的指数值阈值可表明术中脑中风的风险。在一些实施例中,此阈值可介于0.55与0.65之间。在一些实施例中,风险标准可取决于指标值的变化或变化率。例如,更大的降低或更快速的降低可能表明术中脑中风的风险更大。
在步骤1505中,可基于对一或多个风险标准的满足而对患者进行一干预。所述干预可由一人或另一人(例如,另一个从业者)执行。例如,当满足风险标准表明存在pocd风险(或术后妄想症、术后认知能力退化、相对低血压、相对低氧或相对低血糖)时,可降低麻醉患者的一麻醉深度。作为一非限制性实例,此降低可通过延迟一麻醉剂量的施用、降低一麻醉剂的施用速率或施用一逆转剂而实现。作为额外的例子,当满足风险标准表明术中脑中风的风险时,可进行干预以确认术中脑中风的存在(例如,使用医学影像),以解决任何术中脑中风(例如,通过执行一血栓形成术),及/或减轻任何术中脑中风的影响(例如,通过施用保护剂或血液稀释剂)。如本领域技术人员所理解,此干预的列表并非意图为详尽无遗的或限制性的。
图16示出与所公开的实施例一致的用于治疗一麻醉患者的方法1600。方法1600可在执行一外科手术过程的期间内执行。例如,方法1600可在患者正在进行一心脏手术、一整形外科手术或另一种医学手术的同时执行。
在步骤1601中,一计算设备可接收eeg信号。可自置放于患者身上的一对或多对eeg电极接收eeg信号。所述计算设备可通过一物理连接(例如,电线)及/或无线地可操作地连接至eeg电极。无线地eeg信号可直接自eeg电极接收,亦可通过前置放大器或其他信号调节设备间接地接收。
在步骤1603中,无线地计算设备可产生一整体局后验指数值。所述整体后验指数值可取决于前脑活动及后脑活动的一相对程度。可根据以上关于图8所描述的方法800以计算同步值。所述计算设备可被配置为提供所述同步值的指示(例如,一视觉指示或一听觉指示中的至少一者)。
在步骤1605中,人员(例如,诸如医生或护士的从业人员)可确定整体后验指标值是否满足在麻醉期间的意识的风险标准。在一些实施例中,所述人员可基于整体后验指数值(或针对患者的整体后验指数值的一时间历史)以确定所述整体后验指数值是否满足一或多个风险标准。在一些实施例中,此确定可额外地取决于其他患者参数(例如,血压、血液氧合等等)。在各种实施方式中,所述计算设备可配置用于在麻醉期间的意识的风险标准。当所述整体后验指数值满足风险标准时,所述计算设备可被配置为提供一指示(例如,一视觉指示或一听觉指示中的至少一者)。
在一些实施例中,所述风险标准可表达为预定的指标值阈值。例如,一预定的指标值阈值可表明在麻醉期间的意识的风险。在一些实施例中,此阈值可介于0.5与0.8之间(例如,阈值可为0.7)。在一些实施例中,所述风险标准可取决于指标值的变化或变化率。例如,更大的上升或更快速的上升可能表明在麻醉期间更大的意识的风险。
在步骤1605中,可基于对一或多个风险标准的满足而对患者进行一干预。所述干预可以由一人或另一人(例如,另一从业者)执行。例如,当满足风险标准表明在麻醉期间的意识的风险时,可增加麻醉患者的一麻醉深度。作为一非限制性实例,此增加可通过施用一麻醉剂、增加一麻醉剂的施用速率或施用一麻醉的激动剂而实现。
通过考虑本文所公开的实施例的说明书及实施,其他实施例对于本领域技术人员将是显而易见的。说明书及实例旨在仅被认为是示例性的,所公开的实施例的真实范围与精神由所附的权利要求书表明。此外,尽管将所公开的实施例的方面描述为与储存在记忆体及其他有形的计算机可读存储介质中的数据相关联,然而本领域技术人员将理解,此等方面亦可储存在许多类型的有形的计算机上并执行,所述有形的计算机诸如辅助的储存设备,例如硬盘、软盘或cd-rom,或其他形式的ram或rom。因此,所公开的实施例不限于上述实例,而是由所附的权利要求书,根据其等效物的全部范围而定义。
此外,尽管本文已经描述说明性实施例,然而范围包括具有基于本公开的等同要素、修改、省略、组合(例如,各种实施例中的方面)、改编或变更的任何及所有的实施例。权利要求中的元件将基于权利要求中所使用的语言而被广泛地解释,且不限于在本说明书中或在本申请的申请过程中所描述的实例,此等实例应被解释为非排他性的。此外,可依任何方式修改所公开的方法的步骤,包括通过重新排序步骤或插入或删除步骤。因此,本说明书及实施例仅被认为是示例,真正的范围及精神由所附的权利要求及其等同物的全部范围所表明。
- 还没有人留言评论。精彩留言会获得点赞!