一种基于水溶性小分子的可快速溶解微针及其制备与应用的制作方法
本发明属于给药器械技术领域,更具体地,涉及一种基于水溶性小分子的可快速溶解微针及其制备与应用。
背景技术:
透皮给药是指药物涂布或敷贴于皮肤表面的一种给药方式,具有操作简单方便、药效持久和无药物首过效应等优点。但由于皮肤角质层的屏障作用,透皮给药的给药效率有限,在很多情况下不能满足实际应用的需要。微针给药是一种新型的微侵袭透皮给药方式,它克服了皮肤角质层的屏障作用,大大提高了透皮给药的给药效率和生物利用率。微针长度一般为25-2000微米,足够刺穿皮肤角质层,但基本不会触及神经和血管,因此不会出现出血和疼痛现象,对病人的损害程度较小。而且,与传统的透皮注射方式不同,微针给药只需病人把微针扎入患处,操作简单,患者可自行给药,无需专业的医护人员进行操作,因此患者依从性高。因此,微针给药方式在药物递送领域受到了广泛关注,是当前透皮给药领域的研究热点之一。
其中,可溶性微针因其生物安全性高、制备简单、载药量大等优点,是微针中最具有研究前景的一种微针类型。可溶性微针一般由生物相容性好的可溶性或可降解的高分子材料制备而成,如用透明质酸、壳聚糖、羧甲基纤维素、软骨硫磺素、支链淀粉等聚合物来制备可溶性微针。包覆在可溶性微针内的药物随着可溶性材料在皮肤中的溶解而逐渐释放出来,可溶性材料的溶解速率越快,药物释放速度越快,微针施加时间越短。然而,现有的大多数可溶性高分子微针需要十几甚至几十分钟才能使微针完全溶解并释放其中包覆的药物,微针施加时间过长,给患者带来了极大的不便。另外,可溶性高分子微针难以负载疏水性药物,且在配制分子量较大的高分子微针基质水溶液时,高分子在水中的溶解需要耗费较长时间,且形成的高分子水溶液中存在大量气泡,需要一定时间待气泡消除后才能使用,生产效率低,不利于大规模工业化生产。因此,亟需开发一种制备过程简单快速、溶解速度快、施加作用时间短以及具有高效负载疏水性药物的可溶性微针。
技术实现要素:
针对现有技术的以上缺陷或改进需求,本发明的目的在于提供一种基于水溶性小分子的可快速溶解微针及其制备与应用,其中通过对该制备方法的整体工艺流程设计,以及各个步骤所涉及的条件及参数(如小分子种类及其水溶液浓度等)进行改进,能够制备出溶解速度极快、机械性能好的小分子可溶性微针,与现有技术相比,能够有效地解决目前高分子可溶性微针制备过程耗时长、微针溶解速度慢等问题。本发明与现有技术相比,制备的小分子可溶性微针所采用的微针基质材料为小分子,刺入皮肤后溶解速度极快,能快速释放其中包覆的药物,且制备出的微针机械性能好,易于刺穿皮肤,解决了现有通过高分子材料制备的可溶性微针溶解速度较慢、微针施加时间长等问题,能够给患者带来极大的便利。并且,本发明中小分子可溶性微针可实现对亲水药物和疏水药物的分别包覆或同时包覆,解决了目前可溶性微针很难实现对疏水药物包覆的难题。
为实现上述目的,按照本发明的一个方面,提供了一种制备基于水溶性小分子的可快速溶解微针的方法,其特征在于,该方法具体是:先以水溶性小分子材料为溶质配制小分子水溶液,然后将所述小分子水溶液填入到微针模具中,干燥脱模从而得到基于小分子的可快速溶解的微针。
作为本发明的进一步优选,所述水溶性小分子材料其相对分子质量满足50~3000;所述小分子水溶液中,所述水溶性小分子材料的浓度为10w/v%-500w/v%。
作为本发明的进一步优选,所述水溶性小分子材料具体为环糊精及其衍生物、糖类及其水合物中的至少一种;
优选的,所述环糊精选自α-环糊精、β-环糊精、γ-环糊精、羟丙基-β-环糊精、2-羟丙基-β-环糊精、3-羟丙基-β-环糊精、2,3-二羟丙基-β-环糊精、2-羟基异丁基-β-环糊精、葡萄糖基-β-环糊精、麦芽糖基-β-环糊精、羟甲基-β-环糊精甲基-β-环糊精、二甲基-β-环糊精、三甲基-β-环糊精、随机甲基化-β-环糊精、羟乙基-β-环糊精、羟丁基-β-环糊精、磺丁基-β-环糊精、羧甲基-β-环糊精、羟丙基-γ-环糊精、甲基-γ-环糊精、二甲基-γ-环糊精、羟乙基-γ-环糊精、羟丁基-γ-环糊精、磺丁基-γ-环糊精、羧甲基-γ-环糊精、羟丙基-α-环糊精、甲基-α-环糊精、二甲基-α-环糊精、羟乙基-α-环糊精、羟丁基-α-环糊精、磺丁基-α-环糊精、羧甲基-α-环糊精、低聚乳酸基–β-环糊精、磷酸酯-β-环糊精、单(6-多烯多胺-6-去氧)–β-环糊精、磺酸酯–β-环糊精、单宁酸、多巴胺中的至少一种;
所述糖类选自蔗糖、海藻糖、棉子糖、葡萄糖、果糖、乳糖红糖、白糖、冰糖、甘露醇、木糖醇、阿拉伯糖、醛糖、酮糖、赤藓糖醇、阿糖醇、核糖、鼠李糖、麦芽糖中的至少一种。
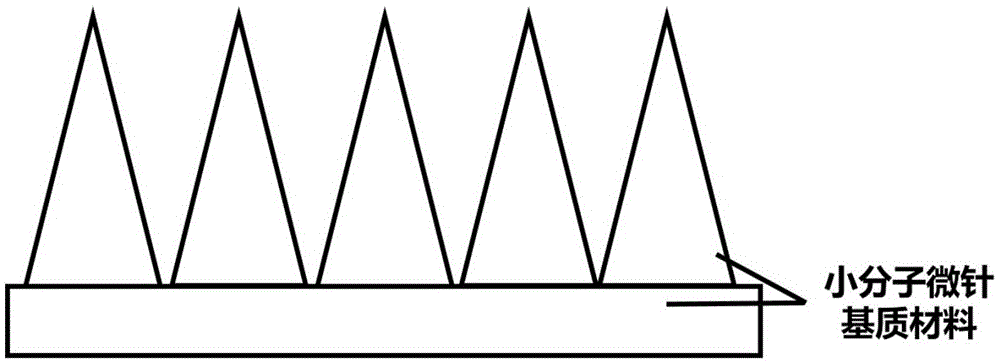
作为本发明的进一步优选,所述水溶性小分子材料具体为环糊精及其衍生物,相应的,得到的所述基于小分子的可快速溶解的微针具体为环糊精微针;所述环糊精微针呈从针体底面到针尖尖端的各个截面面积不断减小形成的立体形状,优选的,所述环糊精微针呈圆锥体形或棱锥体形;所述环糊精微针的长度为25-2500微米,优选的,长度为300-1200微米。
作为本发明的进一步优选,所述微针模具所采用的材料为聚二甲基硅氧烷、环氧树脂、聚四氟乙烯,聚偏氟乙烯、聚丙烯、聚醚砜、聚醚醚酮、云母、玻璃、硅、聚对苯二甲酸乙二醇酯、聚氯乙烯、铜、铝、金、银以及不锈钢中的一种或其中几种的复合物。
作为本发明的进一步优选,所述小分子水溶液中还分散有亲水药物和/或疏水药物,这些亲水药物、疏水药物包括蛋白质、疫苗、激素、小分子药物、大分子药物中的一种或多种;优选的,这些亲水药物、疏水药物包括胰岛素、表皮生长因子、维生素e、维生素a、环孢霉素、博来霉素、紫杉醇、阿霉素、盐酸阿霉素、艾拉、雷帕霉素、甲氨蝶呤、曲安奈德、金丝桃素、甲磺酸二氢麦角胺、利多卡因中的一种或多种;
当所述小分子水溶液中分散有亲水药物时,具体是先以水溶性小分子材料为溶质配制小分子水溶液,再向其中加入亲水药物;
当所述小分子水溶液中分散有疏水药物时,具体是先制备包合疏水药物的、且同时含有水溶性小分子材料成分的包合物粉末,再以该包合物粉末为溶质配制小分子水溶液。
作为本发明的进一步优选,将所述小分子水溶液填入到微针模具中,具体是采用模压、抽真空、离心、振荡中的一种手段或几种手段联用。
按照本发明的另一方面,本发明提供了上述方法制备得到的基于水溶性小分子的可快速溶解微针。
按照本发明的又一方面,本发明提供了上述方法制备得到的基于水溶性小分子的可快速溶解微针在制备经皮给药制剂中的应用。
作为本发明的进一步优选,所述经皮给药制剂具体是用于治疗脱发、银屑病、糖尿病、麻醉、止痛或浅表皮肤瘤的经皮给药制剂,或者是具有保湿美白因子、祛斑美容因子、抗皱因子、除皱因子、激素类药物、抗生素、小分子药物、蛋白类药物、疫苗类药物、植物提取因子类药物或中药复方类药物的经皮给药制剂。
通过本发明所构思的以上技术方案,与现有技术相比,由于完全基于水溶性小分子形成可快速溶解的微针(也包括微针阵列),完全排除了高分子材料的使用,一方面,制备过程简单快速、适于大规模生产,另一方面,这些微针溶解速度极快,仅需数分钟即可完全溶解。
本发明可以制备得到基于水溶性小分子的可快速溶解微针,所采用的小分子材料为水溶性分子,常温下在水中溶解性好;由于本发明是采用小分子材料作为小分子可溶性微针的主要成分,这些微针溶解速度极快,仅需数分钟(小于十分钟)即可完全溶解。另一方面,最终制得的微针中还可包覆亲水药物或疏水药物。当小分子水溶液中分散有亲水药物或疏水药物时,小分子微针可实现对亲水药物或疏水药物的分别包覆;当小分子水溶液中同时分散有亲水药物和疏水药物时,小分子微针可实现对亲水药物和疏水药物的同时包覆。本发明得到的微针可负载多种蛋白质、疫苗、激素、小分子药物、大分子药物等亲水性药物和疏水性药物。以水溶性小分子材料具体为环糊精及其衍生物为例(即,使用环糊精类小分子制备可溶性微针),可通过使疏水药物与环糊精进行复合,形成水溶性好的复合物,制备出现有可溶性微针很难实现的包载疏水药物的可溶性微针。同时,通过简单地调控疏水药物和环糊精的配比,例如将两者的摩尔比优选控制为5:1-1:10,即可调节可溶性微针中疏水药物的含量。
此外,本发明所用的小分子生物安全性好、廉价易得,适合于大规模生产。本发明通过对小分子材料及其种类进行优选,并控制其水溶液的浓度,能够制备出机械性能好的微针。利用本发明方法制得的小分子可溶性微针可用于经皮给药,相应的,可用于制备经皮给药制剂,如应用于制备治疗脱发、银屑病、糖尿病、麻醉、止痛或浅表皮肤瘤的经皮给药,或制备具有保湿美白因子、祛斑美容因子、抗皱因子用于经皮给药,优选地,应用于治疗脱发、银屑病、糖尿病、麻醉、止痛或浅表皮肤瘤的经皮给药;或制备具有保湿美白因子、祛斑美容因子、抗皱因子、除皱因子、激素类药物、抗生素、小分子药物、蛋白类药物、疫苗类药物、植物提取因子类药物或中药复方类药物的经皮给药制剂。这些经皮给药制剂的使用方式可以是光热与化疗联合治疗、光动力与化疗联合治疗、光热与光动力联合治疗等经皮给药治疗方式。
附图说明
图1为小分子可溶性微针示意图。
图2为羟丙基-β-环糊精小分子可溶性微针的光学显微镜图片。
图3为载有疏水模型染料的羟丙基-β-环糊精小分子可溶性微针的光学显微镜图片。
图4为载有亲水模型染料的羟丙基-β-环糊精小分子可溶性微针的光学显微镜图片。
图5为被羟丙基-β-环糊精小分子可溶性微针扎过的猪皮的光学显微镜照片。
图6为扎入猪皮后不同时间的羟丙基-β-环糊精小分子可溶性微针的长度变化,其中(a)为未经处理的微针侧面图,(b)为扎入猪皮后1分钟的微针侧面图。
具体实施方式
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合附图及实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。此外,下面所描述的本发明各个实施方式中所涉及到的技术特征只要彼此之间未构成冲突就可以相互组合。
实施例1
该实施例包括以下步骤:
(1)配制麦芽糖水溶液:将一定量麦芽糖固体溶于水中,搅拌数分钟,得到质量分数为100w/v%的澄清透明的麦芽糖水溶液。
(2)将麦芽糖水溶液填入到微针模具中:将步骤(1)中配好的麦芽糖水溶液加入到的微针模具(单个微针长度为300微米)表面,利用模压的方法使麦芽糖水溶液进入并填满模具基底。
(3)干燥脱模得到可快速溶解的麦芽糖微针:将步骤(2)中的得到的模具进行干燥处理、脱模,即可得到麦芽糖可溶性微针。
实施例2至实施例15
实施例2至实施例15所采用的参数、条件等如下表所示,除了表中给出的具体参数、条件设定外,其他未说明的参数、条件、处理手段等均与实施例1保持一致。
表1实施例2至实施例15所采用的参数、条件列表
实施例16
该实施例包括以下步骤:
(1)配制羟丙基-β-环糊精和亲水模型染料罗丹明b的混合水溶液:将一定量羟丙基-β-环糊精和罗丹明b粉末溶于水中,搅拌数分钟,得到羟丙基-β-环糊精质量分数为100w/v%、罗丹明质量分数为0.1wt%的澄清透明的混合水溶液。
(2)将混有罗丹明b的羟丙基-β-环糊精水溶液填入到微针模具中:将步骤(1)中配好的混有罗丹明b的羟丙基-β-环糊精混合水溶液加入到的微针模具(单个微针长度为450微米)表面,利用模压的方法使混合水溶液进入并填满模具基底。
(3)干燥脱模得到可快速溶解的羟丙基-β-环糊精微针:将步骤(2)中的得到的模具进行干燥处理、脱模,即可得到载有罗丹明b的羟丙基-β-环糊精可溶性微针。
实施例17
该实施例包括以下步骤:
(1)制备包合有疏水模型药物偶氮苯的羟丙基-β-环糊精包合物:取一定量羟丙基-β-环糊精粉末中,将其溶于水中,配成浓度为10w/v%的水溶液;将一定量偶氮苯用少量乙醇溶解,在一定的搅拌速度和温度下将偶氮苯的乙醇溶液加入到上述环糊精水溶液中,包合数小时。过滤除去不溶物,将滤液于旋转蒸发仪上旋蒸一定时间,除去少量的乙醇,即可得到超分子包合物水溶液;将超分子包合物水溶液进行冷冻干燥处理,即可得到包有偶氮苯的超分子包合物粉末。
(2)环糊精-偶氮苯包合物水溶液和环糊精基质溶液的配置:取适量上述步骤(1)中的超分子包合物粉末,加入一定体积的水,得到一定浓度的澄清透明的包合物水溶液;取适量羟丙基-β-环糊精,加入一定体积的水,搅拌数分钟,得到浓度为50w/v%的纯羟丙基-β-环糊精水溶液。
(3)包覆疏水药物的环糊精可溶性微针的制备:将步骤(2)中的超分子包合物水溶液加入到微针模板(单个微针长度为650微米)表面,采用抽真空处理的方式使超分子包合物水溶液填满模具;刮去模板表面多余的超分子包合物水溶液并回收;在模板表面继续加入纯的羟丙基-β-环糊精水溶液,采用抽真空处理的方式使其填满模具及其基底;干燥后脱模,即可得到包覆有偶氮苯的羟丙基-β-环糊精可溶性微针。
实施例18
该实施例包括以下步骤:
(1)制备包合有疏水药物雷帕霉素的羟乙基-β-环糊精包合物:取一定量羟乙基-β-环糊精粉末中,将其溶于水中,配成浓度为20w/v%的水溶液;将一定量雷帕霉素用少量乙醇溶解,在一定的搅拌速度和温度下将雷帕霉素的乙醇溶液加入到上述环糊精水溶液中,包合数小时。过滤除去不溶物,将滤液于旋转蒸发仪上旋蒸一定时间,除去少量的乙醇,即可得到超分子包合物水溶液;将超分子包合物水溶液进行冷冻干燥处理,即可得到包有雷帕霉素的超分子包合物粉末。
(2)环糊精-雷帕霉素包合物水溶液和环糊精基质溶液的配置:取适量上述步骤(1)中的超分子包合物粉末,加入一定体积的水,得到一定浓度的澄清透明的包合物水溶液;取适量羟乙基-β-环糊精,加入一定体积的水,搅拌数分钟,得到浓度为10w/v%的纯羟乙基-β-环糊精水溶液。
(3)包覆疏水药物的环糊精可溶性微针的制备:将步骤(2)中的超分子包合物水溶液加入到微针模板(单个微针长度为850微米)表面,采用抽真空处理的方式使超分子包合物水溶液填满模具;刮去模板表面多余的超分子包合物水溶液并回收;在模板表面继续加入纯的羟乙基-β-环糊精水溶液,采用抽真空处理的方式使其填满模具及其基底;干燥后脱模,即可得到包覆有雷帕霉素的羟乙基-β-环糊精可溶性微针。
效果验证
1、机械性能
取脱毛、清洁过的新鲜猪皮,将实施例16所述的羟丙基-β-环糊精可溶性微针(微针中包覆了红色的罗丹明b染料)尖端对准猪皮表层垂直刺入,用手指按压微针的基底部分,按压1分钟左右,除去猪皮表面的染料。将施加载有罗丹明b的羟丙基-β-环糊精可溶性微针微针后的猪皮置于光学显微镜下观察,如附图5所示,可看到施加微针的猪皮部位有清晰的孔洞,刺穿率达100%,表明该羟丙基-β-环糊精可溶性微针机械强度好,可有效刺穿猪皮表层。
2、微针溶解速度测试
取脱毛、清洁过的新鲜猪皮,将实施例9所述的羟丙基-β-环糊精可溶性微针尖端对准猪皮表层垂直刺入,用手指按压微针的基底部分,按压1分钟,然后将羟丙基-β-环糊精可溶性微针拔出。将上述扎入猪皮的羟丙基-β-环糊精可溶性微针置于光学显微镜下观察,如附图6所示,可看到羟丙基-β-环糊精可溶性微针在较短时间内即可完全溶解,在猪皮中溶解速度极快,因此在实际应用中微针所需施加时间短,且可快速释放其中包覆的药物。
3、微针中药物的稳定性
取新制的和在室温下(25℃)放置三个月的实施例18所述的包有雷帕霉素的羟乙基-β-环糊精可溶性微针,利用人脐静脉内皮细胞作为血管瘤的模型细胞,发现在室温下(25℃)放置三个月的包有雷帕霉素的羟乙基-β-环糊精可溶性微针和新制的微针具有基本相同的对人脐静脉内皮细胞的抑制作用,说明药物在微针中非常稳定,也说明本发明所述的小分子可溶性微针对于药物储藏具有杰出的性能。
除上述各个具体实施例外,根据实际需求,本发明所采用的水溶性小分子材料还可以是两种及以上水溶性小分子材料的混合物。
本领域的技术人员容易理解,以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!