一种壳聚糖包被替米考星微球的制备方法与流程
本发明涉及兽药与制剂领域,具体涉及一种壳聚糖包被替米考星微球的生产方法。
背景技术:
甲壳素在自然界中大量存在,其经乙酰化处理的产物—壳聚糖,分子结构中包含游离的氨基,能够与酸分子结合,从而成为天然多糖中仅有的碱性多糖。壳聚糖是一种重要的天然高分子多糖,具有良好的生物相容性和可降解性,以其为载体制成的载药纳米微球对特定器官组织具有靶向性,药物有缓释性。
壳聚糖由于具有很强的生理适应性、可完全分解性、可再生性等优异的特性,使其可应用于生物学界、医学界及化工等工业、农业及环保等不同领域。与传统的药剂相比较,以壳聚糖作为载体包覆6优点较为明显,可以降低服药的次数、延长药物的生理活性及减少药物本身的刺激性气味,并且可以降低药物的成本等,故具有比普通药物制剂较为明显的优越性能,近年来壳聚糖的研究与应用受到了越来越多科技人员的广泛关注。
动物规模养殖过程密度高等原因,养殖动物时常面临重大疾病尤其是传染性疾病的威胁。替米考星化学名称为4a-o-脱(2,6-二脱氧-3-c-甲基-a-l-核-吡喃已糖基)-20-脱氧-20(顺-3,5-二甲哌啶基)泰乐菌素,系20世纪80年代由英国elanco动物保健品公司开发成功的半合成大环内酯类畜禽专用抗生素,是顺反异构体的混合物。目前我国农业部已批准某些兽药厂生产替米考星原料、预混剂、溶液剂和注射液。替米考星为最新型大环内酯类抗生素,主要抗革兰氏阳性菌如金葡萄菌、肺炎球菌、链球菌等,对部分革兰氏阴性菌如流感嗜血杆菌、巴氏杆菌及家禽支原体的活性比泰乐菌素强。内附吸收快,组织穿透力强,分布容积广,半衰期可达1~2天,体内维持时间长。对猪、牛、绵羊等动物由敏感菌引起的感染性疾病,特别是畜禽呼吸道感染有显著疗效。
目前掩盖药物苦味的机制主要可概括为:加入矫味剂;避免味蕾与苦味药物直接接触;可逆和暂时地麻痹味蕾;通过与其他药物竞争苦味受体或阻断向大脑发送苦味信号。现有包被替米考星的方法有:以海藻酸钙为材质包被替米考星形成微囊,以纤维素包被替米考星,以淀粉、碳酸钙或磷酸氢钙中一种或者几种包被替米考星形成微囊后用树脂包被。
迄今未见壳聚糖作为包材,包被替米考星制成微球的报道。
技术实现要素:
针对现有技术的不足,本发明旨在提供一种壳聚糖包被替米考星的制备方法。
为达到上述目的,本发明采用以下技术方案。
一种壳聚糖包被替米考星微球的制备方法,包括以下步骤:
(1)壳聚糖的纯化:将冰醋酸、去离子水和壳聚糖混合,搅拌使壳聚糖完全溶解,再离心分离,收集上清液,调节上清液的ph值到7.8使壳聚糖析出;离心分离后收集壳聚糖沉淀,将沉淀洗涤、干燥、研磨,得到纯化后的壳聚糖粉末;
(2)壳聚糖的乙酸溶液的制备:将上述步骤(1)中纯化后的壳聚糖粉末溶解于1%的乙酸溶液中,调节ph至5.6,得到壳聚糖的乙酸溶液;
(3)壳聚糖包被替米考星微球的制备:将液体石蜡和曲拉通混合均匀,作为连续相;再将上述步骤(2)中壳聚糖的乙酸溶液与替米考星混合均匀,作为分散相;将分散相滴入处于搅拌状态下的连续相中,滴完后保持搅拌速度,反应一段时间;加入三聚磷酸钠,保持搅拌速度不变,反应一段时间;反应液离心分离,收集沉淀并洗涤,冷冻干燥,得到壳聚糖包被替米考星微球。
优选的,在步骤(1)中,用10%的氢氧化钠溶液调节上清液ph值到7.8。
优选的,在步骤(2)中,用1%的氢氧化钠溶液调节溶液的ph至5.6。
优选的,壳聚糖与替米考星的质量比为2:1;三聚磷酸钠与壳聚糖的质量比为10:3;液体石蜡与曲拉通的质量比为2:0.03。
原料替米考星粉平均粒径为100nm;壳聚糖的重均分子量为14kda,脱乙酰度为95%。
本发明的有益效果:本发明的方法以壳聚糖作为包材,反应温度在室温就可成功包被替米考星。该方法利用壳聚糖包被,掩盖替米考星的苦味;壳聚糖包被替米考星还具有缓释作用,使疗效延长、毒副作用降低。所使用的壳聚糖本身还具有改善控制胆固醇、抑制细菌活性、吸附和排泄重金属、预防和控制高血压、增强免疫效果等功效,较适用于缓控释辅料。
附图说明
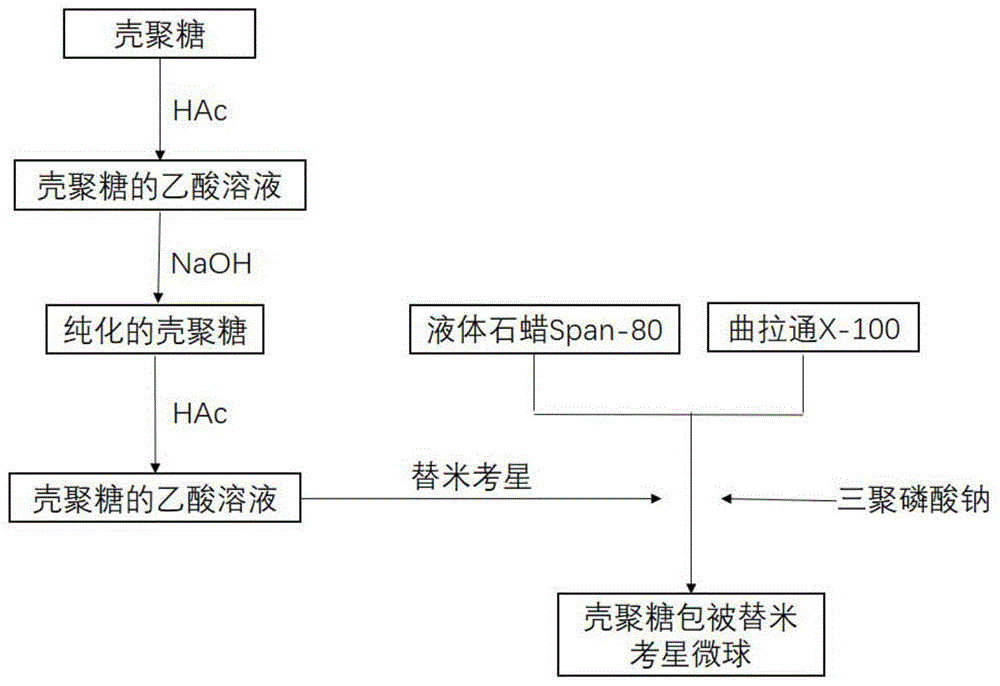
图1为壳聚糖包被替米考星微球的制备工艺流程图。
图2为壳聚糖包被替米考星微球在水溶液中替米考星的释放量曲线图。
具体实施方式
实施例1
(1)壳聚糖的纯化:向圆底烧瓶中加入2ml冰醋酸、100ml去离子水、7.6g壳聚糖,42℃水浴加热并磁力搅拌,设置磁力搅拌速度为4000r/min,1.5h后完全溶解;再离心分离,收集上清液后置于500ml圆底烧瓶中,滴加10%的氢氧化钠溶液调节上清液ph值到7.8使壳聚糖析出;静置3h,离心分离后收集壳聚糖沉淀,用去离子水将壳聚糖沉淀洗涤至ph为7.0,使用400目的纱布挤压过滤除去大部分水份后,40℃真空干燥8h,收集粉体再研磨得到纯化后的壳聚糖粉末;
(2)壳聚糖的乙酸溶液的制备:取0.3g上述步骤(1)中纯化后的壳聚糖加入到500ml的圆底烧瓶中,在圆底烧瓶中加入150ml1%的乙酸溶液,在35℃磁力搅拌20min后壳聚糖完全溶解,再滴加1%naoh溶液调节ph至5.6,得到壳聚糖的乙酸溶液;
(3)壳聚糖包被替米考星微球的制备:将上述步骤(2)中壳聚糖的乙酸溶液与0.15g的替米考星混合均匀;加90mg三聚磷酸钠,保持搅拌速度不变,室温反应120min;反应液离心分离20min,转速为4000r/min,收集沉淀,并去离子洗涤3次,冷冻干燥24h,得到壳聚糖包被替米考星微球(实施例1样品)。
实施例2
(1)壳聚糖的乙酸溶液的制备:取0.3g壳聚糖加入到500ml的圆底烧瓶中,在圆底烧瓶中加入150ml1%的乙酸溶液,在35℃磁力搅拌20min后壳聚糖完全溶解,再滴加1%naoh溶液调节ph至5.6,得到壳聚糖的乙酸溶液;
(2)壳聚糖包被替米考星微球的制备:将6g液体石蜡span-80加入圆底烧瓶,再加90mg的曲拉通x-100,室温搅拌120min,充分混匀,作为连续相;再将上述步骤(1)中壳聚糖的乙酸溶液与0.15g替米考星混合均匀,作为分散相;用恒压漏斗将分散相滴入200转/分钟的搅拌转速下的连续相中,滴完后保持室温和搅拌速度,反应5分钟;加入90mg的三聚磷酸钠,保持搅拌速度不变,室温反应120min;反应液离心分离20min,转速为4000r/min,收集沉淀,并去离子洗涤3次,冷冻干燥24h,得到壳聚糖包被替米考星微球(实施例2样品)。
实施例3
(1)壳聚糖的纯化:向圆底烧瓶中加入2ml冰醋酸、100ml去离子水、7.6g壳聚糖,42℃水浴加热并磁力搅拌,设置磁力搅拌速度为4000r/min,1.5h后完全溶解;再离心分离,收集上清液后置于500ml圆底烧瓶中,滴加10%的氢氧化钠溶液调节上清液ph值到7.8使壳聚糖析出;静置3h,离心分离后收集壳聚糖沉淀,用去离子水将壳聚糖沉淀洗涤至ph为7.0,使用400目的纱布挤压过滤除去大部分水份后,40℃真空干燥8h,收集粉体再研磨得到纯化后的壳聚糖粉末;
(2)壳聚糖的乙酸溶液的制备:取0.3g上述步骤(1)中纯化后的壳聚糖加入到500ml的圆底烧瓶中,在圆底烧瓶中加入150ml1%的乙酸溶液,在35℃磁力搅拌20min后壳聚糖完全溶解,再滴加1%naoh溶液调节ph至5.6,得到壳聚糖的溶液;
(3)壳聚糖包被替米考星微球的制备:将6g液体石蜡加入圆底烧瓶,再加90mg的曲拉通x-100,室温搅拌120min,充分混匀,作为连续相;再将上述步骤(2)中壳聚糖的乙酸溶液与0.15g替米考星混合均匀,作为分散相;用恒压漏斗将分散相滴入200转/分钟的搅拌转速下的连续相中,滴完后保持室温和搅拌速度,反应5分钟,收集反应液离心分离20min,转速为4000r/min,收集沉淀,并去离子洗涤3次,冷冻干燥24h,得到壳聚糖包被替米考星微球(实施例3样品)。
实施例4
(1)壳聚糖的纯化:向圆底烧瓶中加入2ml冰醋酸、100ml去离子水、7.6g壳聚糖,42℃水浴加热并磁力搅拌,设置磁力搅拌速度为4000r/min,1.5h后完全溶解;再离心分离,收集上清液后置于500ml圆底烧瓶中,滴加10%的氢氧化钠溶液调节上清液ph值到7.8使壳聚糖析出;静置3h,离心分离后收集壳聚糖沉淀,用去离子水将壳聚糖沉淀洗涤至ph为7.0,使用400目的纱布挤压过滤除去大部分水份后,40℃真空干燥8h,收集粉体再研磨得到纯化后的壳聚糖粉末;
(2)壳聚糖的乙酸溶液的制备:取0.3g上述步骤(1)中纯化后的壳聚糖加入到500ml的圆底烧瓶中,在圆底烧瓶中加入150ml1%的乙酸溶液,在35℃磁力搅拌20min后壳聚糖完全溶解,再滴加1%naoh溶液调节ph至5.6,得到壳聚糖的乙酸溶液;
(3)壳聚糖包被替米考星微球的制备:将6g液体石蜡加入圆底烧瓶,再加90mg曲拉通x-100,室温搅拌120min,充分混匀,作为连续相;再将上述步骤(2)中壳聚糖的乙酸溶液与0.15g替米考星混合均匀,作为分散相;用恒压漏斗将分散相滴入200转/分钟的搅拌转速下的连续相中,滴完后保持室温和搅拌速度,反应5分钟;加入90mg三聚磷酸钠,保持搅拌速度不变,室温反应120min;反应液离心分离20min,转速为4000r/min,收集沉淀,并去离子洗涤3次,冷冻干燥24h,得到壳聚糖包被替米考星微球(实施例4样品)。
实施例5
分别取0.1g实施例1、实施例2、实施例3、实施例4样品置于10ml的容量瓶中,再加入去离子水定容。在37℃恒温、震荡频率为60r/min条件下进行体外释放试验。分别在0h、0.5h、1h、1.5h、2h、2.5h、3h、3.5h、4h、4.5h、5h、5.5h定时取样测定溶液中替米考星的含量,计算累积释放百分率(%)。
图2为壳聚糖包被替米考星微球在水溶液中替米考星的释放量曲线。通过曲线可以看出,实施例1样品出现明显的突释现象。实施例4样品在长时间下相对稳定,相对实施例1样品、实施例2样品、实施例3样品具有更慢的药物释放速率,即实施例4样品具有良好的包被和缓释效果。
- 还没有人留言评论。精彩留言会获得点赞!