一种止血成骨一体化材料及其制备方法及其应用与流程
本发明涉及医用材料技术领域,具体涉及一种止血成骨一体化材料及其制备方法及其应用。
背景技术:
骨外科是以手术治疗为主的一门学科。出血是手术治疗过程中一项危险的并发症,术中失血过多一方面会造成患者生命体征不稳,甚至造成失血性休克或压迫性血肿,极不利于患者预后的恢复;另一方面,大量术中失血影响手术视野清晰度,不利于手术过程的开展。随着止血器械及新型止血材料的发展,术中止血控制的措施愈发成熟与完善。然而,骨外科手术由于骨髓腔渗血、邻近神经鞘膜出血、静脉丛出血等特殊情况,其无法依靠压迫、结扎或其他方法止血。除了术中失血造成病人与外科医生的问题,特殊类型出血还会进一步造成术后失血,以全膝关节置换术(tkr)为例,其术中、术后失血量约达人体总血量的45~60%。能够控制特殊类型出血的止血材料,能明显提升手术质量,缩短手术时间,提升患者预后,并进一步提升患者疗效满意度。
目前,针对骨外科手术的出血问题,在上世纪90年代,nelson等就提出了控制骨科手术出血的十项基本策略:术前估算输血量要求、重新考量输血标准、预演手术过程、低血压麻醉、缩短手术时间、延迟输血、调整病人体位减少静脉充血、使用选择性动脉栓塞、争取不流血的手术、使用新式入路避免出血。这十项原则一直沿用至今,其对于骨外科手术术中失血的控制及输血的应用具有重要的指导意义。但是,在临床工作中还是会遇到不能或不会接受输异体血液的患者,以及传统纱布压迫或血管钳结扎止血无效的特殊类型出血,因而一些新型术中止血器械与止血材料应运而生。
外科手术常用的止血器械有高频电刀(单极电凝、双极电凝)、超声刀、氩气刀、pk刀、vio电外科工作站、ligasure等。以骨外科手术最常使用的高频电刀和超声刀为例,高频电刀在止血后会产生严重热效应与大量烟雾,术后容易发生黏连,且不宜用于较精细的手术;超声刀操作迟缓,价格昂贵,切凝组织需具有一定张力。针对骨外科手术骨髓腔渗血、邻近神经鞘膜出血、静脉丛出血等特殊情况,目前还没有一款止血器械可以单独处理这类情况。而一些新型止血材料能够处理这类特殊情况,其与止血器械相辅相成,共同控制骨外科术中出血。
骨是一种有生命的高维管组织。当骨头被切开时,出血是很一个必须解决的临床症状。骨出血主要来源于小梁网的静脉通道。骨髓出血一直是止血器械无法解决的一个难题。骨蜡作为一种止血剂,在过去的一个世纪中被用于防止骨髓腔出血。如今,它主要由蜂蜡组成,并被石蜡和棕榈酸异丙酯软化。骨蜡的主要止血机理是通过创建一个物理屏障来阻止血液流动。然而,多篇文献报道了骨蜡的并发症,其包括:骨生长抑制、异物反应及异物肉芽肿生长等。此外,骨蜡也没有很好的成骨特性。
技术实现要素:
有鉴于此,本发明的目的在于提供一种止血成骨一体化材料及其制备方法,使得所述一体化材料能够同时具备更佳的止血和成骨功能;
本发明的另外一个目的在于提供上述一体化材料在骨外科手术、硬组织感染性炎症、硬组织肿瘤或囊肿等领域相关产品中的应用。
为了实现上述发明目的,本发明提供如下技术方案:
一种止血成骨一体化材料,包括生物陶瓷骨胶前体、淀粉凝胶前体,以及水相溶液;
其中,所述生物陶瓷骨胶前体包括生物陶瓷材料和淀粉;所述淀粉凝胶前体包括淀粉和金属盐,所述金属盐选自硝酸镁、硝酸锌、硝酸钙、硝酸钕、硝酸铝、氯化镁、氯化钙、氯化锌、氯化铯、氯化铝、氯化锶、硝酸锶中的一种或两种以上;所述水相溶液选自水、磷酸盐溶液、甘油溶液、抗生素溶液、蛋白水溶液中的一种或者几种混合液。
目前淀粉类的止血材料主要利用了淀粉的溶胀性质,企图使淀粉吸血,从而达到止血的目的,但是这种止血材料无法有效封堵有血压的出血状况;本发明将金属离子与淀粉混合组成淀粉凝胶前体,依靠水相溶液,能够形成半交联互穿网络加强了淀粉原有的抗冲击性质,使得新的互穿网络遇水后形成凝胶,对硬组织如骨的出血实现有效封堵;生物陶瓷骨胶配合水相溶液实现水化,可转化为更加稳定的晶形,为后期成骨做准备;两者相互配合,实现了成骨效果的改善;依靠水相溶液,淀粉凝胶前体和生物陶瓷骨胶形成凝胶状一体化材料,一方面可提升材料的封堵性能;另一方面提供材料的可塑性;再一方面使材料保水,防治快速固化,利于术中使用;
作为优选,所述一体化材料包括质量百分比为50-80%生物陶瓷骨胶前体和20-50%淀粉凝胶前体;在本发明具体实施方式中,所述一体化材料包括80%生物陶瓷骨胶前体和20%淀粉凝胶前体;或包括70%生物陶瓷骨胶前体和30%淀粉凝胶前体;或包括60%生物陶瓷骨胶前体和40%淀粉凝胶前体;或包括50%生物陶瓷骨胶前体和50%淀粉凝胶前体;或包括66.7%生物陶瓷骨胶前体和33.3%淀粉凝胶前体(也可理解为两者质量比为2∶1)。
在所述生物陶瓷骨胶前体中,包括质量百分比为30-100%的生物陶瓷陶瓷材料和0-70%的淀粉;更优选地,所述生物陶瓷骨胶前体包括30-80%的生物陶瓷陶瓷材料和20-70%的淀粉;在本发明具体实施方式中,所述生物陶瓷骨胶前体包括80%的生物陶瓷陶瓷材料和20%的淀粉;
作为优选,所述生物陶瓷陶瓷材料选自磷酸三钙、磷酸四钙、磷酸八钙、二水磷酸氢钙、无水磷酸氢钙、无定形磷酸钙、羟基磷灰石、焦磷酸钙、硅酸钙、硅酸三钙、硫酸钙、生物活性玻璃颗粒中的一种或两种以上,优选为其中的一种或两种;在本发明具体实施方式中,所述生物陶瓷材料为磷酸四钙和羟基磷灰石两种、磷酸三钙和生物活性玻璃颗粒两种或者硅酸三钙。
在所述淀粉凝胶前体中,包括质量百分比为0.00001-25%的金属盐和75-99.99999%的淀粉;进一步优选地,包括质量百分比为1-25%的金属盐和75-99%的淀粉;更优选地,包括质量百分比为1-10%的金属盐和90-99%的淀粉;在本发明具体实施方式中,所述淀粉凝胶前体包括10%的金属盐和90%的淀粉;或包括25%的金属盐和75%的淀粉;或包括12.5%的金属盐和87.5%的淀粉;
所述生物陶瓷骨胶前体和淀粉凝胶前体中的淀粉均可选自预糊化淀粉、马铃薯淀粉、玉米淀粉、蜡样淀粉、改性淀粉中的一种或两种以上。在本发明具体实施方式中,所述淀粉
作为优选,所述磷酸盐溶液选自磷酸氢二钠溶液、磷酸二氢钠溶液、磷酸二氢钾溶液、磷酸氢二钾溶液、磷酸钠溶液中的一种或两种以上。
所述水相溶液占生物陶瓷骨胶前体和淀粉凝胶前体总质量的0.05%~90%;作为优选,所述水相溶液占生物陶瓷骨胶前体和淀粉凝胶前体总质量的20-70%,更优选为30-50%,在具体实施时可选择35%。作为优选,所述水相溶液除水外,其他水相溶液的浓度为0.0001-49.9999%,更优选为10-40%,更优选为20-30%,在本发明具体实施方式中,所述水相溶液选自水或甘油溶液,所述甘油溶液的浓度为20%。
与其他对照的材料相比,本发明一体化材料能够有效封堵出血,其他对照材料无法封堵出血或需要施加外力才能够封堵出血;同时,本发明所述一体化材料具备较佳的成骨特性;基于这些试验效果,本发明提出了所述一体化材料在如下一个或多个方面的应用:
制备骨外科手术止血成骨材料、制备硬组织感染性炎症的成骨材料、制备硬组织感染性炎症的填充材料、制备硬组织肿瘤或囊肿的显影剂、制备治疗硬组织肿瘤或囊肿的药物载体。
基于上述应用,本发明提供了一种止血成骨产品,包括所述一体化材料以及占其总质量1-25%的抗菌物质、骨诱导因子、靶向药物或显影剂。根据所添加的物质,在实现本身所具备的止血成骨特性基础上,还可以应用于硬组织感染性炎症的填充、成骨、硬组织肿瘤或囊肿的治疗、显影等。
此外,本发明还提供了所述一体化材料的制备方法,包括:
步骤1、将生物陶瓷材料和淀粉混合,制备获得生物陶瓷骨胶前体;
将淀粉加入到金属盐溶液中,搅拌至淀粉糊化,干燥,获得淀粉凝胶前体;
步骤2、混合生物陶瓷骨胶前体和淀粉凝胶前体,并加入水相溶液,搅拌至胶状,获得所述一体化材料。
其中,所述获得淀粉凝胶前体的具体步骤如下:
将金属盐溶解于去离子水中,得到电解质溶液;将淀粉加入到电解质溶液中,在温度为33℃~120℃的条件下充分搅拌,至淀粉完全糊化,得到粘稠液体;将得到的粘稠液体在高温干燥,至完全干燥,而后用粉碎机打成粉末状固体,并过筛,获得所述淀粉凝胶前体。
由以上技术方案可知,本发明在生物陶瓷制备的过程中添加了淀粉凝胶前体,提供了一种生物陶瓷基止血成骨一体化材料,通过淀粉凝胶前体中形成的半交联互穿网络加强了淀粉原有的抗冲击性质,同时配合生物陶瓷骨胶,实现了成骨效果的改善;本发明一体化材料具有良好的可操作性和可塑性,生物陶瓷和淀粉的可降解特性和生物相容性使其可以避免产生异物反应及刺激肉芽肿生长。此外,本发明一体化材料内还可以根据需求添加其他功能性的药物或材料,以满足多种疾病治疗的需要。
附图说明
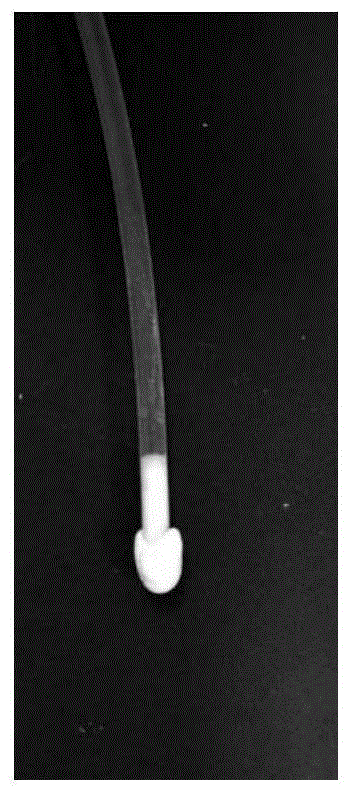
图1所示为本发明一体化材料的亚克力管出血封堵实验结果;
图2所示为本发明一体化材料的alp活力检测结果;
图3所示为本发明一体化材料的茜素红染色结果;
图4所示为本发明一体化材料的大鼠头骨止血封堵结果;
图5所示为本发明一体化材料的出血量实验结果;
图6所示为本发明一体化材料的microct影像学结果;
图7所示为本发明一体化材料组织学结果。
具体实施方式
本发明公开了一种止血成骨一体化材料及其制备方法及其应用,本领域技术人员可以借鉴本文内容,适当改进工艺参数实现。特别需要指出的是,所有类似的替换和改动对本领域技术人员来说是显而易见的,它们都被视为包括在本发明。本发明所述一体化材料及其制备方法和应用已经通过较佳实施例进行了描述,相关人员明显能在不脱离本发明内容、精神和范围内对本文所述一体化材料及其制备方法和应用进行改动或适当变更与组合,来实现和应用本发明技术。
在具体实施例中的对比试验中,除了各组应有的区别外,其他试验条件均保证一致,确保实验结果的可对比性。
以下就本发明所提供的一种止血成骨一体化材料及其制备方法及其应用做进一步说明。
实施例1:本发明所述一体化材料的制备及其体外止血试验
1、制备方法
a、淀粉凝胶前体的制备
按质量百分比25%,将硝酸钙溶解于去离子水中,得到电解质溶液;按质量百分比75%,将玉米淀粉加入到制备的电解质溶液中,在温度为80℃的条件下充分搅拌,至淀粉完全糊化,得到粘稠液体;
将得到的粘稠液体在置于高温干燥柜中过夜,至完全干燥,而后用粉碎机打成粉末状固体,并过60目筛。
b、生物陶瓷骨胶前体的制备
称量质量分数60%的磷酸四钙,20%的预糊化淀粉与20%的羟基磷灰石。
将三者均匀混合。
c、一体化材料的制备
将生物陶瓷骨胶前体,与淀粉凝胶前体按3:2的质量比例(60%和40%的比例)混合。室温下,向混合物中添加占总质量的35%的蒸馏水,搅拌均匀至形成胶状混合物,即得目标产物。
2、体外止血对比试验
a、对比组1
称量与1中生物陶瓷基止血成骨一体化材料等质量的磷酸四钙、羟基磷灰石(质量比3∶1);室温下,向其中添加占总质量的35%的蒸馏水,搅拌均匀至形成胶状混合物,即得目标产物。
b、对比组2
称取与1中生物陶瓷基止血成骨一体化材料等质量的磷酸四钙、羟基磷灰石与玉米淀粉。其中磷酸四钙质量分数60%,羟基磷灰石质量分数20%、玉米淀粉质量分数20%。室温下,添加占总质量的35%的蒸馏水,搅拌均匀至形成胶状混合物,即得目标产物。
c、亚克力管出血封堵实验
步骤(1):亚克力管出血模型的建立
取一根2米长,内径3mm的亚克力管;
将亚克力管一端朝下,此端作为封堵操作端,记此端水平高度为低位水平高度;
取足量水置于容器中,将亚克力管另一端置于大于低位水平高度1.8米的液面以下;
用50ml一次性针筒于封堵操作端抽吸,至出现虹吸现象,封堵操作端不断出水时,表明建模成功。
步骤(2):生物陶瓷基止血成骨一体化材料封堵
分别取0.3g生物陶瓷基止血成骨一体化材料与对照组1和对照组2材料,直接封堵于封堵操作端,观察封堵情况。
d、实验结果
本发明生物陶瓷基止血成骨一体化材料在无外界压力辅助的情况下实现对亚克力管的完全封堵(如图1),即对19600pa的水压进行封堵,大于人体最大收缩压18665pa(140mmhg),并能够持续24小时以上。
对照组1生物陶瓷材料被水流冲散,无法对亚克力管实现有效封堵。
对照组2生物陶瓷与淀粉材料虽然能够对亚克力管在有外界压力辅助的情况下能对亚克力管实现短暂封堵,但由于淀粉不具粘性,当撤除外界压力辅助时,材料无法抵御水压,从管口冲出,因而无法实现有效封堵。
实施例2:本发明所述一体化材料的制备及其体外成骨诱导试验
1、制备方法
a、淀粉凝胶前体的制备
按质量百分比10%,将氯化镁溶解于去离子水中,得到电解质溶液;按质量百分比90%,将蜡样淀粉加入到制备的电解质溶液中,在温度为80℃的条件下充分搅拌,至淀粉完全糊化,得到粘稠液体;
将得到的粘稠液体在置于高温干燥柜中过夜,至完全干燥,而后用粉碎机打成粉末状固体,并过60目筛。
b、生物陶瓷骨胶前体的制备
称量质量分数60%的磷酸三钙,20%的玉米淀粉与20%的生物活性玻璃。
将三者均匀混合。
c、一体化材料的制备
将生物陶瓷骨胶前体,与淀粉凝胶前体按2∶1的质量比例(66.7%和33.3%的比例)混合。室温下,向混合物中添加占总质量的35%的20%甘油溶液,搅拌均匀至形成胶状混合物,即得目标产物。
2、诱导成骨
步骤(1):材料浸提液的配制
a.将上述一体化材料与市售骨蜡(强生w810t,购于扬州市锐腾医疗器械有限公司)以0.1g/ml的浸提比例,于不含血清的高糖dmem中37℃,24小时。
b.将步骤a中浸提完成的液体过0.22μm滤芯,即得材料浸提液。
步骤(2):成骨诱导培养基的配置
在步骤(1)中的浸提液与高糖dmem中,加入10%胎牛血清,1%双抗,50μg/ml抗坏血酸钠和10mmβ甘油磷酸钠,制成成骨诱导培养基。
步骤(3):成骨诱导
选用对数增殖期的mc3t3-e1subclone14细胞系,在24孔板中以每孔2×105细胞的密度种板;待细胞融合率达90%以上时,更换成骨诱导培养基;每隔一日换液;成骨诱导培养14天。
3、alp活力
步骤(1):细胞裂解、蛋白提取
小心用pbs洗涤细胞三次;每孔加入ripa溶液500ml,冰上裂解细胞15min;4℃12000rpm离心30min,取上清液。
步骤(2):alp活力检测
蛋白质定量,按试剂盒说明书测定alp活力,计算alp活力。
4、茜素红染色
步骤(1):细胞固定
小心用pbs洗涤细胞三次;每孔加入多聚甲醛500ml,固定细胞15min。
步骤(2):茜素红染色
小心吸取上清,再用pbs洗涤细胞两次;加入1ml茜素红s染色液,室温下孵育20min;小心吸走茜素红s染色液,并用1ml蒸馏水小心洗涤;用显微镜观察钙结节情况。
5、试验结果
图2alp活力结果显示,实验组的alp活力值为44.29±1.73金氏单位/ml,远大于对照组与市售骨蜡,且具有统计学差异(p<0.05),提示本发明一体化材料具有良好的成骨特性。
图3茜素红染色结果显示,实验组钙结节数量明显多于对照组与市售骨蜡,提示本发明一体化材料具有良好的成骨特性。
实施例3:本发明所述一体化材料的制备及其小鼠止血成骨试验
1、制备方法
a、淀粉凝胶前体的制备
按质量百分比12.5%,将氯化钙溶解于去离子水中,得到电解质溶液;按质量百分比87.5%,将马铃薯淀粉加入到制备的电解质溶液中,在温度为80℃的条件下充分搅拌,至淀粉完全糊化,得到粘稠液体;
将得到的粘稠液体在置于高温干燥柜中过夜,至完全干燥,而后用粉碎机打成粉末状固体,并过60目筛。
b、生物陶瓷骨胶前体的制备
称量质量分数80%的硅酸三钙与20%的预糊化淀粉。
将两者均匀混合。
c、一体化材料的制备
将生物陶瓷骨胶前体,与淀粉凝胶前体按7∶3的质量比例(70%和30%的比例)混合。室温下,向混合物中添加占总质量的35%的蒸馏水,搅拌均匀至形成胶状混合物,即得目标产物。
2、对照材料
步骤(1):取与1中淀粉凝胶前体质量一致的马铃薯淀粉;
步骤(2):取与1中生物陶瓷骨胶前体质量一致的硅酸三钙;
步骤(3):将硅酸三钙,与马铃薯淀粉按7∶3的质量比例混合。室温下,向混合物中添加占总质量的35%的蒸馏水,搅拌均匀至形成胶状混合物,即得目标产物。
3、大鼠颅骨止血实验
步骤(1):对大鼠进行常规术前准备,准备称好质量的棉球。
步骤(2):大鼠颅骨缺损出血模型建立
取眼矢状位后方1cm,沿颅骨正中作一长3cm的切口,逐层分离周围组织,充分暴露颅骨顶骨;
用骨膜剥离器完全剥离暴露颅骨顶骨表面的骨膜;
用直径3mm的磨钻对一侧颅骨顶骨钻一直径3mm的骨缺损孔,至刚穿透第二层板障时停止,见骨缺损处大量出血,建模成功。
步骤(3):止血阶段
分别取0.05g本发明一体化材料和0.05g生物陶瓷与淀粉的对照材料直接填塞于骨缺损孔中,出血对照组不放任何材料。
观察止血情况5分钟,期间用称量好质量的棉球吸取骨出血,并称量吸血后的棉球质量。
步骤(4):骨缺损对照组建立
取原骨缺损对称点,即为骨缺损对照组处;
用同一直径3mm的磨钻对一侧颅骨顶骨钻一直径3mm的骨缺损孔,至刚穿透第二层板障时停止,见骨缺损处出血,对照组建立成功。
步骤(5):术后处理:常规逐层缝合,关闭切口。大鼠不禁食不禁水饲养。
步骤(6):组织学、影像学评价及出血量的评价(棉球质量差/大鼠质量)。
4、止血实验结果
本发明一体化材料具有良好的形状自适应性,其能够完全适应骨缺损孔洞形状,自适应填充,具有良好的封堵性质,其能够完全封堵骨出血伤口,不会被血流冲散,填充5分钟内未见活动性出血(如图4),同时具有良好的可操作性,其不粘手,易于操作。
对照材料具有一定的形状自适应性,其能够适应骨缺损孔洞形状,自适应填充;但遇血后即刻溃散,其不能够封堵骨出血伤口,溃散材料不易于操作,其出血量明显大于本发明一体化材料(图5);作为对照材料的生物陶瓷与淀粉材料无法在5分钟内对骨缺损实现封堵,所以未对其进行进一步影像学及组织学评价;此外,在加水混合后15分钟后开始固化,其形状自适应性大幅下降,其固化时间过快,不利于术中的随时使用。
5、影像学和组织学结果
microct影像学提示,相较于对照组,本发明一体化材料具有良好的骨长入特性,其成骨面积明显大于对照组(图6)。
组织学评价提示,本发明一体化材料具有良好的骨长入特性(图7)。
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!