一种小剂量白细胞介素2在制备治疗慢性痛风药物中的应用的制作方法
本发明涉及医药领域,具体涉及一种使用小剂量白细胞介素2治疗慢性难治性痛风的方法及其应用。
背景技术:
痛风是一种常见且复杂的关节炎类型,主要是由于血液中尿酸水平逐渐高于饱和浓度而导致尿酸盐晶体的沉积,这种沉积主要发生在外周关节及周围组织时就定义为痛风。痛风进程一般分为4个阶段:无症状高尿酸血症期、急性痛风性关节炎期、慢性痛风性关节炎期和肾脏病变期。急性痛风极度疼痛但具有自限性,发病数天到2周内可便自然缓解;痛风反复发作后则容易形成慢性痛风,慢性痛风会导致多关节肿痛,病情不能自行缓解,迁延不愈。此外痛风还经常和其它疾病伴随发生,包括代谢综合征,心血管疾病以及肾病。近年来痛风的流行率和发病率在发达国家逐步升高,在世界范围内都呈上升趋势,特别是国内,随着生活水平的提高以及饮食结构的改变,痛风的发病率逐年上升,约占人口的1-4%,平均每年发病率为2.68‰,男性为女性的2-6倍,严重影响人类生存质量。
调节性T细胞(Treg)是一组具有强大抗炎和免疫抑制作用的T细胞,主要通过分泌转化生长因子-β(TGF-β)等细胞因子维持机体的炎症稳态,是体内TGF-β的重要来源,而TGF-β具有阻止白细胞募集和炎性细胞因子释放的作用,是促进痛风缓解的主要细胞因子。本项目组前期的研究表明,相较正常对照,急性痛风病人的外周血Treg细胞数量显著增加,而慢性难治性痛风患者的Treg细胞数量显著减少,揭示Treg细胞数目与痛风进程密切相关。
IL-2在1976年作为T细胞的生长因子首次被发现,生物学功能广泛,能够对多种细胞类型如T细胞、B细胞、NK细胞、巨噬细胞和少突神经胶质细胞等产生作用,其中最显著的作用是影响T淋巴细胞的生长,IL-2的缺陷会导致自身免疫疾病的发生。静止的T细胞表面不表达IL-2R,对IL-2没有反应;受丝裂原或其它刺激活化后T细胞才能表达IL-2R,成为IL-2的靶细胞;而IL-2又可诱导靶细胞增加IL-2R的表达。在体内,IL-2对CD4+T细胞的作用是通过自分泌途径实现的,因为活化的CD4+T细胞能够产生大量的IL-2;而CD8+T细胞则通过旁分泌途径来维持细胞的生长。IL-2R在T细胞上的表达是一过性的,一般在活化后2~3天达到高峰,6~10天左右消失。随着IL-2R的消失,T细胞即失去对IL-2的反应能力。因此若要维持正常T细胞在体外长期生长,必须不断地用丝裂原或其它刺激物去刺激T细胞,以维持IL-2R的表达。值得关注的是Treg细胞持续性的表达高亲和力IL-2R,收到IL-2刺激之后Treg细胞增殖分化,鉴于Treg细胞数目对痛风进程具有重要影响,那么用小剂量的IL-2在临床上对慢性期痛风患者Treg细胞数目进行调节,将有望改变痛风进程,治疗痛风。
国内外对于痛风的药物治疗,主要从三个方面入手:抑制尿酸生成,促进尿酸排泄以及碱性药物中和,除此之外还有通过饮食的调整生活习惯的改变等,尚未报道使用IL-2进行治疗的工作,本研究将首次把IL-2用于慢性难治性痛风患者的治疗,具有开创性和前瞻性,为慢性难治性痛风的治疗开辟了新的方向。
技术实现要素:
本发明的目的在于提供一种小剂量白细胞介素2(IL-2)用于慢性痛风治疗药物中的新用途,该治疗药物以小剂量IL-2为主要活性成分,为临床治疗慢性难治性痛风增加一种有效的新药。同时为IL-2的临床应用增加一个新的用途和适应症。在慢性痛风患者中,该药物取得了较好的治疗效果。给予小剂量IL-2后,痛风患者的体内促炎因子明显减少,症状明显得到改善。可以治疗慢性难治性痛风。
本发明提供一种IL-2在制备慢性痛风治疗药物中的新应用,所述慢性痛风疾病为慢性难治性痛风。可以是由先天性嘌呤代谢紊乱、尿酸排泄障碍、继发于肾脏疾病或药物引起的高尿酸血症诱发的痛风。此类痛风的一个临床特点在于患者体内的Treg细胞数量显著减少。
本发明所使用的白细胞介素2是任何能够在体内发挥功能的白细胞介素2,优选人重组白细胞介素2冻干粉或液体注射剂,溶于无菌生理盐水,优选制成水溶液;本发明所述的药物包括白细胞介素2和药物上可使用的辅料和载体。辅料优选为十二烷基硫酸钠、甘露醇、磷酸二氢钠、磷酸氢二钠。
本发明提供的药物给药方式优选为皮下注射给药,白细胞介素2的低用药剂量优选为每次50万单位,每天一次,治疗时间优选为10~14天。
本发明的技术效果:
本发明首次提供了小剂量白细胞介素2在慢性难治性痛风药物中的应用。通过对慢性难治性痛风患者进行小剂量的IL-2药物治疗,结果显示病人体内的调节性T细胞数目显著升高,各种炎性因子显著减少,关节肿痛症状明显减轻。痛风发作率明显降低。
附图说明
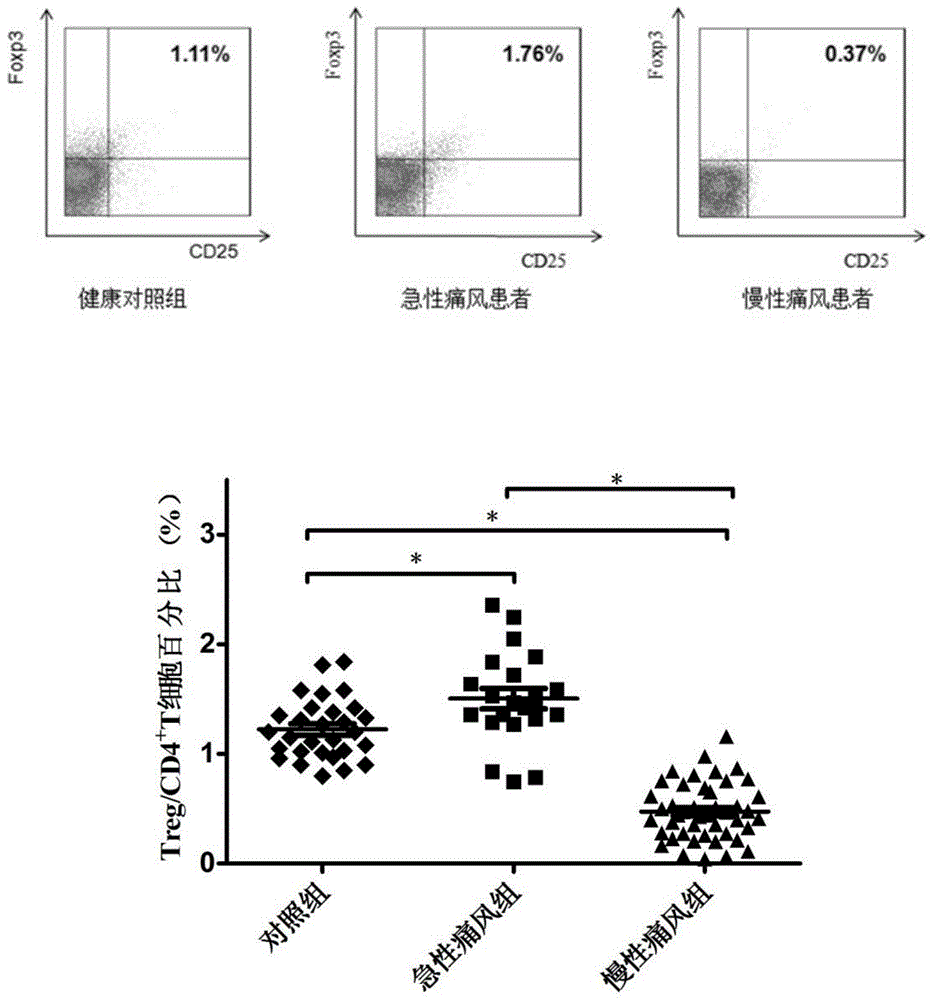
图1急慢性痛风患者外周血Treg细胞百分率比较;
图2治疗前后患者体内调节性T细胞数目变化;
图3治疗前后患者血清TGF-β和IL-1β比较;
具体实施方式:
以下通过具体的实施例来进一步说明本发明的内容,应理解本发明中所述的术语仅仅是为描述特别的实施方式,并非用于限制本发明。另外,对于本发明中的数值范围,应理解为还具体公开了该范围的上限值和下限值之间的每个中间值。在任何陈述值或陈述范围内的中间值以及任何其他陈述值或在所述的范围内的中间值之间的每个较小的范围也包括在本发明内。这些较小范围的上限值和下限值可独立地包括或排除在范围内。
为了更好的说明本发明,下面用具体临床实验实施例说明小剂量IL-2在慢性难治性痛风患者中具有良好的治疗效果。
1.受试者的选择:筛选12例慢性难治性痛风患者,以2015ACR/EULAR痛风诊断标准为依据,要求患者半年内痛风发作次数≥3次。
2.药物与试剂:本实施例中所使用的药物为IL-2注射剂。试剂主要包括细胞生物学实验试剂和试剂盒等,均可通过商业途径获得,具体包括:RNA提取试剂盒购自Roche生物科技有限公司;反转录试剂盒(First-Strand cDNA Synthesis Kit)购自Promega公司;SYBR Green Mix购自美国ABI公司;所用抗体都购于CST公司;所用ELSIA试剂盒都购于RD公司。本发明实施例中所提供的方法如果没有特殊说明均为常规方法。
3.治疗方法:入选患者住院完善相关检查后,小剂量的IL-2皮下注射,每天1次,每次50万单位,治疗10-14天。
4.症状观察和指标检查:
疗程结束后复查相关实验室指标,并随访3个月,评估痛风发病情况。
图1所示的Treg细胞在CD4+细胞中的百分比在急性痛风患者中高于健康人,在慢性痛风患者中明显低于健康人,此表达差异是本发明所基于的慢性痛风炎症相关机制,为IL-2在治疗慢性痛风患者中的应用提供了理论依据。IL-2在临床上对慢性期痛风患者Treg细胞数目进行调节。
图2和图3显示的结果表明,IL-2药物治疗后,慢性痛风患者体内的Treg和TGF-β明显升高,IL-1β明显被下调。Treg是一组具有强大抗炎和免疫抑制作用的T细胞,Treg数目增加表明体内炎症得到了抑制,TGF-β具有阻止白细胞募集和炎性细胞因子释放的作用,TGF-β升高表明机体炎症得到了缓解,IL-1β作为前炎性因子,其表达量和机体的炎症水平正相关,IL-1β明显被下调表明机体炎症水平降低。整体来说,IL-2治疗后机体痛风明显得到了缓解。
上述12例患者在接受治疗后,随后接受3个月随访,仅1例饮酒后发病1次,并且常规治疗3天后好转,其他均未发病,说明小剂量的白细胞介素2能够很好的治疗慢性难治性痛风患者。
以上显示和描述了本发明的基本原理、主要特征和本发明的优点。本行业的技术人员应该了解,本发明不受上述实施例的限制,上述实施例和说明书中描述的只是说明本发明的原理,在不脱离本发明精神和范围的前提下,本发明还会有各种变化和改进,本发明要求保护范围由所附的权利要求书、说明书及其等效物界定。
- 还没有人留言评论。精彩留言会获得点赞!