一种基于围术期危险预警的多模型互补增强机器学习方法与流程
本发明涉及智能医疗技术领域,具体为一种基于围术期危险预警的多模型互补增强机器学习方法。
背景技术:
当前特征提取和特征选择、人工神经网络、支持向量机、随机森林、xgboost等机器学习领域发展态势良好并应用于各服务业。目前主要基于患者的局部信息对围手术期单一种类的危险并发症进行预测,预测准确度不高,且以往模型在进行迁移时效果很不好,例如,一个预测术中低血压的模型,在预测术中高血压时往往不具备良好的表现。针对围手术期的预警,现有模型主要分为两类:第一种是利用病人手术前的基本信息、既往病史、检验检查报告、用药记录等数据进行评估预警。第二种是利用病人术中心电图信息来预测例如术中低血压等危险症状。以上方法都只运用了病人的片面数据,无法充分利用围手术期所能收集到的病人全量数据,因此对于病人术中术后并发症的预测准确度不高。例如,第一种方法在预测病人状态时,没有将病人术中生命监护仪中的诸如血压、心电等信息输入模型,因而只能给出一个基于术前静态数据的危险并发症评估。
同时,因为两种方法所用的变量种类完全不同,将两种方法进行组合也是困难的。本发明通过使用人工神经网络将不同算法的输出进行有机整合,将上述的两大类方法进行了有机的融合,形成一个全新的预测围手术期并发症的模型。通过整合不同模型的输出,本方法能充分利用患者全量数据,克服了原有方法只能利用部分患者数据做出某种特定并发症预测的不足,对患者可能出现的术中术后主要并发症进行一个静态加动态的综合评估预警,并且具有良好的准确性和稳定性。
技术实现要素:
本发明的目的在于提供一种基于围术期危险预警的多模型互补增强机器学习方法,该基于围术期危险预警的多模型互补增强机器学习方法具体步骤如下:
s1:对模型所采用的变量,尤其是术中生命监护仪相关信息进行处理;
s2:选取9个常用的分类算法,作为模型的子算法,以提高整个模型的稳定性和精确度;
s3:利用s2中所得数组中的每一层作为ann算法的输入信号,利用ann算法对各层信号进行分类,判别病人是否会出现相应的症状,建立预警模型。
优选的,s1中所述变量包括患者静态数据、患者术中生命监护仪的动态数据;患者静态数据包括患者基本信息、患者并存疾病、入院日药物、手术类型、术前实验结果、术中药物,患者术中生命监护仪的动态数据包括心电图、脑电波图。
优选的,患者静态数据,若为连续型变量则经单位化后直接输入模型,若为离散型变量则转化为“0”、“1”编码后输入模型;患者术中生命监护仪的动态数据,其波形予以拆分并得到收缩阶段、舒张阶段、收缩上升阶段、收缩衰减阶段以及总衰减阶段五个阶段,提取各个阶段的图形学特征作为相应的模型输入。
优选的,s2中所述9个子算法分别是:逻辑回归、xgboost、随机森林、svm、ann、knn、朴素贝叶斯、gbdt、lightgbm,并经过进一步的融合组成。
优选的,模型要同时预测多种术中及术后并发症,针对一个样本量为n的样本,若预测总共p种并发症,k个子算法的输出结果为一个n·k·p数组,所采用的各种分类算法均采用grid-search以及五折crossvalidation进行参数调教。
优选的,一个ann模型为一个将只含有“0”和“1”的向量,映射为“0”或“1”二分类的映射。
优选的,ann算法中神经网络的输入层神经元个数等于在s2中所采用的子算法个数k。
优选的,预警模型包括对术中低血压、急性肾损伤、静脉血栓、心血管并发症、神经系统并发症、术中心率失常进行监测预警。
与现有技术相比,本发明的有益效果是:本方法独创性的采用ann算法来融合其他多种算法,用于融合的ann模型的输入不再是传统的原始变量,而是经过一系列子算法对原始变量经过初步分类预测后的输出值,旨在取得一个全局稳健的预测评估模型,弥补了传统方法的不足。融合后的预测模型具有更加稳定的表现力,并且可以同时预测多种术中术后并发症。
附图说明
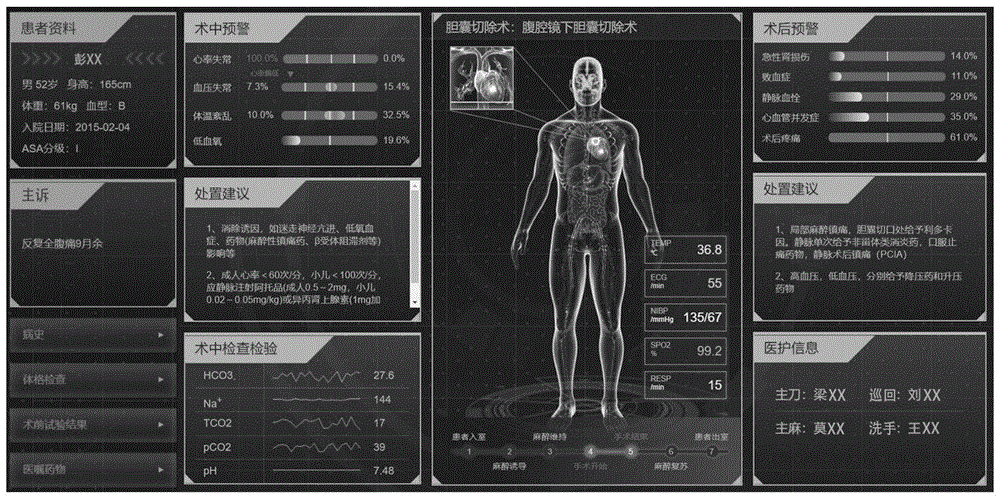
图1为本发明的部分界面示意图;
图2为心电图的阶段示意图;
图3为n个病人样本的神经网络示意图;
图4为本发明的流程示意图;
图5为本发明预警模型示意图。
具体实施方式
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合具体实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
实施例1
一种基于围术期危险预警的多模型互补增强机器学习平台,主要包括以下步骤:
s1:对模型所采用的变量,尤其是术中生命监护仪相关信息进行处理;
s2:选取9个常用的分类算法,作为我们模型的子算法,以提高整个模型的稳定性和精确度;
s3:利用s2中所得数组中的每一层作为ann算法的输入信号,利用ann算法对各层信号进行分类,判别病人是否会出现相应的症状,建立预警模型。
s1中所述变量包括患者静态数据、患者术中生命监护仪的动态数据;所述患者静态数据包括患者基本信息、患者并存疾病、入院日药物、手术类型、术前实验结果、术中药物,所述患者术中生命监护仪的动态数据包括心电图、脑电波图,具体以实际监测结果为根据。
所述的患者静态数据,若为连续型变量则经单位化后直接输入模型,若为离散型变量则转化为“0”、“1”编码后输入模型;所述的患者术中生命监护仪的动态数据,其波形予以拆分并得到收缩阶段、舒张阶段、收缩上升阶段、收缩衰减阶段以及总衰减阶段五个阶段,提取各个阶段的图形学特征作为相应的模型输入。
如心电图图2所示,我们基于一个完整的心动周期的波形予以拆分并得到收缩阶段、舒张阶段、收缩上升阶段、收缩衰减阶段以及总衰减阶段五个阶段。随后提取各个阶段的图形学特征作为相应的模型输入,具体流程如图2所示,图中数字1到5依次表示收缩阶段1、舒张阶段2、收缩上升阶段3、收缩衰减阶段4以及总衰减阶段5。
记病人的动态数据经过拆分以及特征提取后所得的数据为x2。那么病人的全量数据即为x=(x1,x2)。
s2中所述9个子算法分别是:逻辑回归、xgboost、随机森林、svm、ann、knn、朴素贝叶斯、gbdt、lightgbm,并经过进一步的融合组成。这些算法都是针对分类变量进行建模预测的成熟算法,在临床分类预测上已经被广泛采用。具体算法组成可以由实际数据进行适当修改和添加以达到最优预测性能。
假设我们采用了k个子算法,分别记为f1(x),···,fk(x),其中x为收集到的患者全量数据。每一个子算法实现了一个映射,即
其中j代表第j个要预测的并发症。由于我们的模型要同时预测多种术中及术后并发症,假设我们要预测总共p种并发症,那么基于所有并发症,k个子算法的输出结果为一个n·k·p数组,如图5所示,其中的每一层都是基于一个并发症的子算法输出。本步所采用的各种分类算法均采用grid-search以及五折crossvalidation进行参数调教。
记第二步中所得结果为fij(x),i=1,···,k;j=1,···,p,我们利用第二步中所得数组中的每一层作为ann算法的输入信号,每一层都对应一种术中或术后并发症,利用ann算法对各层信号进行分类,即判别病人是否会出现相应的症状。令一个ann模型为一个将只含有“0”和“1”的向量例如(10···1)映射为“0”或“1”二分类的映射,如下所示:
其中g表示一个ann映射。对于某一个并发症的全部n个病人样本,如图3所示,神经网络的输入层神经元个数等于我们在第二步中所采用的子算法个数k,对于矩阵中的每一行,假设我们已知真实输出值为tij,逐行输入g后,实际输出值为g(fij(x)),模型的参数调优基于预先设定损失函数为|tij-g(fij(x))|,i=1,···,k;j=1,···,p。
如图4所示,所述的预警模型包括对术中低血压、急性肾损伤、静脉血栓、心血管并发症、神经系统并发症、术中心率失常进行监测预警。
针对围术期相关预警的重要性,本方法独创性的采用ann算法来融合其他多种算法,用于融合的ann模型的输入不再是传统的原始变量,而是经过一系列子算法对原始变量经过初步分类预测后的输出值,旨在取得一个全局稳健的预测评估模型,弥补了传统方法的不足。融合后的预测模型具有更加稳定的表现力,并且可以同时预测多种术中术后并发症。
以上所述,仅为本发明较佳的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明揭露的技术范围内,根据本发明的技术方案及其发明构思加以等同替换或改变,都应涵盖在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!