一种复方氨基酸注射液及其制备方法与流程
本发明涉及医药制品技术领域,尤其涉及一种复方氨基酸注射液及其制备方法。
背景技术:
复方氨基酸注射液(18aa-v)一般是由色氨酸、亮氨酸、异亮氨酸、缬氨酸、甲硫氨酸、苯丙氨酸等18种氨基酸组成复方制剂,主要用于蛋白质摄入不足、吸收障碍等氨基酸不能满足机体代谢需要的患者,亦用于改善手术后病人的营养状况。
氨基酸在溶液中很不稳定,极易被氧化而产生一系列复杂的对人体有害的物质,其中较为明显会影响产品质量的问题是制剂中色氨酸成分在工艺过程中的降解。色氨酸的主要降解产物为5-羟色氨酸、2-羟色氨酸以及甲酰犬尿氨酸,使得药液颜色变深。基于上述复方氨基酸注射液的理化性质,大多数生产企业常采取两种措施控制产品质量:1.加入亚硫酸盐类抗氧剂或金属离子螯合剂来减少色氨酸降解;2.加入适量活性炭进行脱色,以达到注射剂的性状要求,这两种方法都为复方氨基酸注射液带来了一定的安全隐患。
技术实现要素:
有鉴于此,本发明提供了一种复方氨基酸注射液的制备方法,本发明提供的制备方法能够有效改善色氨酸降解的问题,提高药液稳定性,降低质量风险;本发明还提供了一种复方氨基酸注射液。
本发明提供一种复方氨基酸注射液的制备方法,包括以下步骤:
s1,生产前处理:分别用碱水、金属离子螯合剂溶液和注射用水对配制用容器和管路进行冲洗;
s2,取40%的注射用水置于配液罐中,投入处方量的氢氧化钠,边加边搅拌,搅拌至溶解;
s3,向配液罐内充入n2,保温50~75℃,然后按照顺序依次投入处方量的酪氨酸、异亮氨酸、亮氨酸、盐酸赖氨酸、甲硫氨酸、苏氨酸、缬氨酸、丙氨酸、盐酸精氨酸、门冬氨酸、谷氨酸、脯氨酸、丝氨酸、甘氨酸、苯丙氨酸、盐酸组氨酸、木糖醇、盐酸半胱氨酸,并逐一搅拌溶解;
s4,继续向配液罐内通入n2,保证配液罐内含氧量在3%以内,降温至40~55℃,加注射用水至近足量,再投入色氨酸,搅拌溶解后补水至全量,得到混合液;
s5,利用0.45μm、0.22μm微孔滤芯串联过滤混合液,然后利用0.22μm微孔滤芯过滤除菌;将过滤除菌后得到的混合液注入输液瓶中,轧盖封口、灭菌、灯检,即得到复方氨基酸注射液。
本发明还提供了一种利用上述制备方法制得的复方氨基酸注射液,每1000ml复方氨基酸注射液中,包含以下质量的原料:亮氨酸3.63-3.82g、异亮氨酸1.61-1.85g、缬氨酸1.23-1.47g、盐酸赖氨酸3.15-3.42g、苏氨酸1.86-2.05g、色氨酸0.32-0.45g、甲硫氨酸0.98-1.12g、盐酸半胱氨酸0.38-0.56g、苯丙氨酸2.72-2.97g、氢氧化钠1.05-1.44g、酪氨酸0.09-1.22g、盐酸精氨酸2.69-2.98g、盐酸组氨酸2.38-2.52g、丙氨酸1.79-1.91g、脯氨酸0.83-1.15g、丝氨酸0.56-0.89g、门冬氨酸1.08-1.33g、谷氨酸1.76-2.09g、甘氨酸3.10-3.43g、木糖醇45-55g;注射用水加至1000ml。
本发明提供的技术方案带来的有益效果是:
1.本发明提供的制备方法控制色氨酸投入前的温度以及配液罐内的含氧量,有效减少色氨酸的降解,使得复方氨基酸注射液的性质稳定,解决了复方氨基酸注射液(18aa-v)在制备过程中易发生变色的问题;
2.本发明通过调整各氨基酸的投入顺序,不需加入抗氧剂、金属离子螯合剂或使用活性炭脱色,简化了处方工艺,最终制备得到质量合格且稳定的制剂。
附图说明
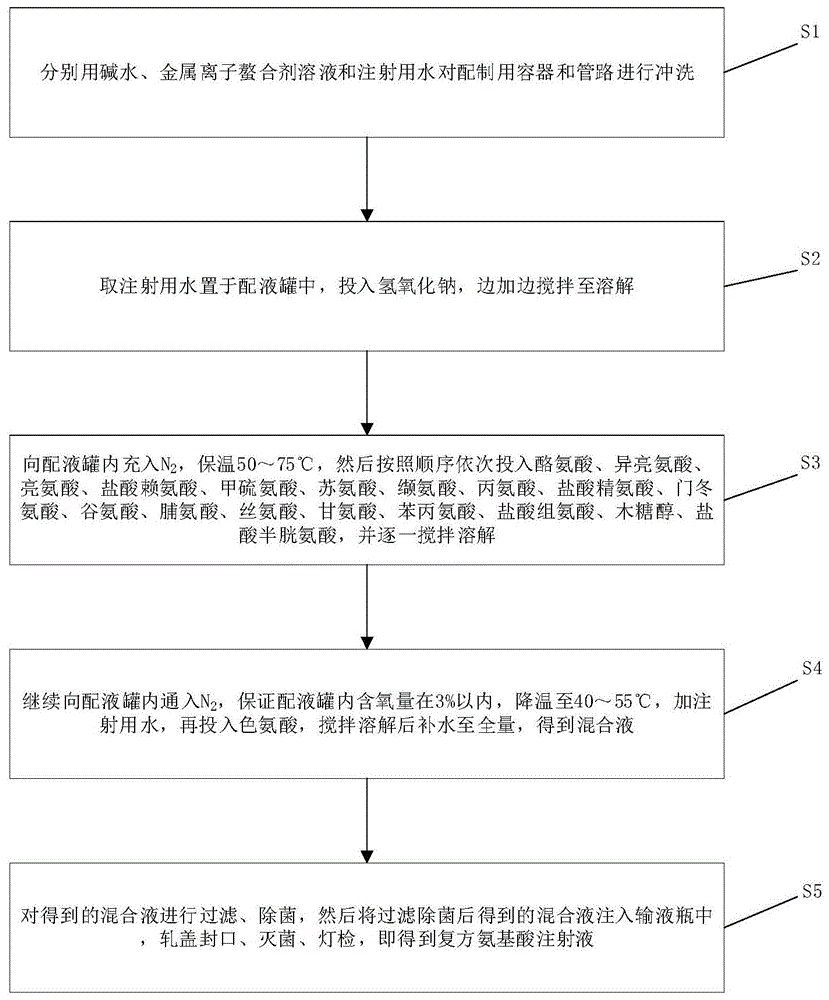
图1是本发明一种复方氨基酸注射液的制备方法的流程图。
具体实施方式
为使本发明的目的、技术方案和优点更加清楚,下面将结合附图对本发明实施方式作进一步地描述。
请参考图1,本发明的实施例提供了一种复方氨基酸注射液的制备方法,包括以下步骤:
步骤s1,生产前处理:分别用碱水、金属离子螯合剂溶液和注射用水对配制用容器和管路进行冲洗;
步骤s2,取40%的注射用水置于配液罐中,投入处方量的氢氧化钠,边加边搅拌,搅拌至溶解;
步骤s3,向配液罐内充入n2,保温50~75℃,然后按照顺序依次投入处方量的酪氨酸、异亮氨酸、亮氨酸、盐酸赖氨酸、甲硫氨酸、苏氨酸、缬氨酸、丙氨酸、盐酸精氨酸、门冬氨酸、谷氨酸、脯氨酸、丝氨酸、甘氨酸、苯丙氨酸、盐酸组氨酸、木糖醇、盐酸半胱氨酸,并逐一搅拌溶解;
步骤s4,继续向配液罐内通入n2,保证配液罐内含氧量在3%以内,降温至40~55℃,加注射用水至近足量,再投入色氨酸,搅拌溶解后补水至全量,得到混合液;
步骤s5,利用0.45μm、0.22μm微孔滤芯串联过滤混合液,然后利用0.22μm微孔滤芯过滤除菌;将过滤除菌后得到的混合液注入输液瓶中,轧盖封口、灭菌、灯检,即得到复方氨基酸注射液。
上述制备过程中,每1000ml复方氨基酸注射液中,包含以下质量的原料:亮氨酸3.63-3.82g、异亮氨酸1.61-1.85g、缬氨酸1.23-1.47g、盐酸赖氨酸3.15-3.42g、苏氨酸1.86-2.05g、色氨酸0.32-0.45g、甲硫氨酸0.98-1.12g、盐酸半胱氨酸0.38-0.56g、苯丙氨酸2.72-2.97g、氢氧化钠1.05-1.44g、酪氨酸0.09-1.22g、盐酸精氨酸2.69-2.98g、盐酸组氨酸2.38-2.52g、丙氨酸1.79-1.91g、脯氨酸0.83-1.15g、丝氨酸0.56-0.89g、门冬氨酸1.08-1.33g、谷氨酸1.76-2.09g、甘氨酸3.10-3.43g、木糖醇45-55g;注射用水加至1000ml。
下面结合实施例对本发明提供的复方氨基酸注射液及其制备方法进行详细说明。
实施例1:
分别用碱水、金属离子螯合剂溶液和注射用水对配制用容器和管路进行冲洗;取350ml注射用水置于配液罐中,投入1.1g氢氧化钠,边加边搅拌至溶解;向配液罐内充入n2,保温65℃,然后按照顺序依次投入1.03g酪氨酸、1.74g异亮氨酸、3.75g亮氨酸、3.33g盐酸赖氨酸、1.06g甲硫氨酸、1.95g苏氨酸、1.35g缬氨酸、1.82g丙氨酸、2.76g盐酸精氨酸、1.26g门冬氨酸、1.87g谷氨酸、0.98g脯氨酸、0.75g丝氨酸、3.22g甘氨酸、2.76g苯丙氨酸、2.43g盐酸组氨酸、52g木糖醇、0.46g盐酸半胱氨酸,并逐一搅拌溶解;继续向配液罐内通入n2,保证配液罐内含氧量在3%以内,降温至45℃,加420ml注射用水,再投入0.41g色氨酸,搅拌溶解后补水至1000ml,得到混合液;利用0.45μm、0.22μm微孔滤芯串联过滤混合液,然后利用0.22μm微孔滤芯过滤除菌;将过滤除菌后得到的混合液注入输液瓶中,轧盖封口、灭菌、灯检,即得到复方氨基酸注射液。
对比例1:
对比例1与实施例1的区别仅在于:配制过程中加入5g亚硫酸氢钠;其余则与实施例1基本相同。
对比例2:
对比例2与实施例1的区别仅在于:配制过程中加入3g亚硫酸氢钠;其余则与实施例1基本相同。
对比例3:
对比例3与实施例1的区别仅在于:配制过程中加入1g亚硫酸氢钠;其余则与实施例1基本相同。
对实施例1、对比例1-3制得的复方氨基酸注射液进行性状表征,结果见表1:
表1:实施例1、对比例1-3制得的复方氨基酸注射液的性状
表1可以看出,实施例1制得的复方氨基酸注射液与添加抗氧剂亚硫酸氢钠制得的复方氨基酸注射液相比,色氨酸的降解产物无明显差异,实施例1制备得到质量合格且稳定的制剂。
实施例2:
分别用碱水、金属离子螯合剂溶液和注射用水对配制用容器和管路进行冲洗;取400ml注射用水置于配液罐中,投入1.3g氢氧化钠,边加边搅拌至溶解;向配液罐内充入n2,保温70℃,然后按照顺序依次投入1.13g酪氨酸、1.64g异亮氨酸、3.68g亮氨酸、3.27g盐酸赖氨酸、1.03g甲硫氨酸、1.90g苏氨酸、1.25g缬氨酸、1.85g丙氨酸、2.72g盐酸精氨酸、1.12g门冬氨酸、1.81g谷氨酸、0.87g脯氨酸、0.67g丝氨酸、3.18g甘氨酸、2.83g苯丙氨酸、2.41g盐酸组氨酸、48g木糖醇、0.41g盐酸半胱氨酸,并逐一搅拌溶解;继续向配液罐内通入n2,保证配液罐内含氧量在3%以内,降温至50℃,加300ml注射用水,再投入0.35g色氨酸,搅拌溶解后补水至1000ml,得到混合液;利用0.45μm、0.22μm微孔滤芯串联过滤混合液,然后利用0.22μm微孔滤芯过滤除菌;将过滤除菌后得到的混合液注入输液瓶中,轧盖封口、灭菌、灯检,即得到复方氨基酸注射液。
实施例3:
分别用碱水、金属离子螯合剂溶液和注射用水对配制用容器和管路进行冲洗;取500ml注射用水置于配液罐中,投入1.42g氢氧化钠,边加边搅拌至溶解;向配液罐内充入n2,保温55℃,然后按照顺序依次投入1.21g酪氨酸、1.82g异亮氨酸、3.79g亮氨酸、3.40g盐酸赖氨酸、1.10g甲硫氨酸、2.01g苏氨酸、1.46g缬氨酸、1.89g丙氨酸、2.96g盐酸精氨酸、1.31g门冬氨酸、2.06g谷氨酸、1.13g脯氨酸、0.87g丝氨酸、3.42g甘氨酸、2.95g苯丙氨酸、2.50g盐酸组氨酸、54g木糖醇、0.54g盐酸半胱氨酸,并逐一搅拌溶解;继续向配液罐内通入n2,保证配液罐内含氧量在3%以内,降温至48℃,加200ml注射用水,再投入0.43g色氨酸,搅拌溶解后补水至1000ml,得到混合液;利用0.45μm、0.22μm微孔滤芯串联过滤混合液,然后利用0.22μm微孔滤芯过滤除菌;将过滤除菌后得到的混合液注入输液瓶中,轧盖封口、灭菌、灯检,即得到复方氨基酸注射液。
在不冲突的情况下,本文中上述实施例及实施例中的特征可以相互结合。
以上所述仅为本发明的较佳实施例,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!