一种具有缓释性的纳米颗粒包被的抗菌肽及其制备方法与流程
本发明涉及生物医药技术领域,具体地说,是一种具有缓释性的纳米颗粒包被的抗菌肽及其制备方法。
背景技术:
纳米材料由于其表面效应和小尺寸效应等优势广泛的应用于生物医学领域。在纳米材料中,纳米载药体系由于其诸多优点成为了材料与医学领域研究的热点。纳米载药体系指的是利用聚合物作为载体,将小分子的药物通过物理或化学方式以包封或者吸附的方式结合在其中,形成尺寸在纳米级别的药物。纳米载药的载体一般会选择生物相容性较高,或可进行修饰的聚合物。这一类载体可以人工合成的也可以是天然的。与传统的药物治疗手段不同,纳米载药主要具有一下的优势,第一是改善药物的溶解性并增强药物的稳定性,在药物到达治疗部位之前,尽量减少药物的损失;第二是提高药物的组织渗透性,膜透过能力和,增加给药途径;第三是增加药物的靶向性,提高药物的利用率,纳米载药体系在被修饰后,可以使纳米药物在到达机体的病变部位后才释放出有效的药物分子,发挥药效;第四是具有调节缓释控制释放的作用。
ll37是迄今为止在人体中发现的唯一一种阳离子抗菌肽。由于ll37对多种革兰阳性菌和革兰阴性菌具有杀伤作用,其中包括铜绿假单胞菌、淋病奈瑟菌、肺炎克雷伯菌、金黄色葡萄球菌等,因此ll37成为机体固有免疫的重要组成部分。ll37的抗菌活性前景广阔,同时具有多重生物活性,它被视为抗多重耐药细菌感染的新的希望。然而,目前由于体外制备抗菌肽费用高昂、存在抗原性、且直接回输极易被灭活等多种原因,使其应用得到了大大的限制,至今为止仍未用于临床。
牛血清白蛋白(bsa)具有低毒性,低免疫原性,稳定性强能共结合多种药物等优势。bsa作为药物缓释的载体具有广泛的应用前景。王树斌等人的研究表明表皮生长因子偶联牛血清白蛋白纳米粒荷载紫杉醇室温稳定性与血清稳定性均高于未被纳米粒包被的紫杉醇。肺部因其特殊的生理结构而适合作为局部或全身用药的给药部位。
利用常规戊二醛交联的方式可能使ll37分子之间交联,但是这种交联方式不利于维持ll37的生物活性。因此我们提出利用bsa分子之间的交联同时保持ll37结构完整,以时空扩增电荷密度的方案,此方案可以提高ll37的负载率并有助于稳定纳米结构,目前,关于该方面的研究还未见报道。
技术实现要素:
本发明的第一个目的是,针对现有技术中的不足,提供一种具有缓释性的纳米颗粒包被的抗菌肽。
本发明的第二个目的是,提供一种上述抗菌肽的制备方法。
为实现上述第一个目的,本发明采取的技术方案是:
一种具有缓释性的纳米颗粒包被的抗菌肽,包括纳米载药系统和负载在纳米载药系统上的抗菌肽,所述纳米载药系统为被还原的bsa分子,所述抗菌肽为经过巯基修饰的阳离子抗菌肽ll37,所述纳米载药系统被还原后暴露出巯基,再与抗菌肽通过二硫键连接,合成具有缓释性的纳米颗粒包被的抗菌肽。
优选地,所述被还原的bsa分子由下述方法制备得到:利用二硫苏糖醇处理bsa分子,bsa分子的二硫键被裂解并暴露出巯基,再利用十二烷基硫酸钠的作用使bsa分子暴露更多的巯基。
优选地,所述纳米颗粒包被的抗菌肽由下述方法制备得到:
1)将bsa,二硫苏糖醇和十二烷基硫酸钠溶于无菌的双蒸水中,使bsa的终浓度为40mg/ml,将该溶液在250r/min的磁力搅拌下进行70℃的水浴加热,得到还原的bsa溶液;
2)将的还原的bsa溶液用缓冲液稀释,将被稀释的bsa溶液加入到24孔板中,置于37℃的振荡器,以350r/min反应4.5h,合成bsa纳米颗粒;
3)将bsa和抗菌肽ll37加入到24孔板中,并置于37℃温度控制的振荡器中,转速为350r/min,4.5小时后合成ll37纳米颗粒;
4)使用超滤的方法去除纳米颗粒中的十二烷基硫酸钠,获得具有缓释性的纳米颗粒包被的抗菌肽。
更优选地,步骤1)中所述bsa,二硫苏糖醇和十二烷基硫酸钠的质量比为80:3:40。
更优选地,步骤2)中所述缓冲液为ph=4.8的2-(n-吗啉代)乙磺酸溶液,稀释后的还原的bsa溶液浓度为1mg/ml。
更优选地,步骤3)中所述bsa和抗菌肽ll37的质量比为9:1。
为实现上述第二个目的,本发明采取的技术方案是:
如上任一所述的纳米颗粒包被的抗菌肽的制备方法,包括下述步骤:
1)将bsa,二硫苏糖醇和十二烷基硫酸钠溶于无菌的双蒸水中,bsa的终浓度为40mg/ml,将该溶液在250r/min的磁力搅拌下进行70℃的水浴加热,得到还原的bsa溶液;
2)将的还原的bsa溶液用缓冲液稀释,将被稀释的bsa溶液加入到24孔板中,置于37℃的振荡器,以350r/min反应4.5h,合成bsa纳米颗粒;
3)将bsa和抗菌肽ll37加入到24孔板中,并置于37℃温度控制的振荡器中,转速为350r/min,4.5小时后合成ll37纳米颗粒;
4)使用超滤的方法去除纳米颗粒中的十二烷基硫酸钠,获得具有缓释性的纳米颗粒包被的抗菌肽。
优选地,步骤1)中所述bsa,二硫苏糖醇和十二烷基硫酸钠的质量比为80:3:40。
优选地,步骤2)中所述缓冲液为ph=4.8的2-(n-吗啉代)乙磺酸溶液,稀释后的还原的bsa溶液浓度为1mg/ml。
优选地,步骤3)中所述bsa和抗菌肽ll37的质量比为9:1。
本发明的优点在于:
1、利用常规戊二醛交联的方式可能使抗菌肽ll37之间交联,但是这种交联方式不利于维持抗菌肽ll37的生物活性。因此我们提出利用bsa分子之间的交联同时保持抗菌肽ll37结构完整,以时空扩增电荷密度的方案,bsa和抗菌肽ll37分子间形成二硫键网络,合成了结构稳定的ll37纳米颗粒,可以提高抗菌肽ll37的负载率并有助于稳定纳米结构。
2、本发明专利中使用的纳米载药体系是牛血清白蛋白bsa,bsa是天然存在的物质,与人工合成的高分子聚合物相比,bsa与小鼠或者人体的组织相容性更高,机体发生免疫排斥的几率低,反应轻。另外,bsa还具有低毒性,稳定性强能共结合多种药物等优势。
3、体外制备ll37的成本昂贵,且ll37在融入血浆之后易发生降解和失活,在体内发挥有效作用的量十分少,而在本发明中,利用二硫键之间的交联,使ll37成功包被在bsa这一载药体系中,这种化学交联方式使ll37在药物传输过程中不易被降解,并能够发挥靶向作用。
4、本发明中制备纳米颗粒的技术方法简单,耗时较短,且易操作,可应用于多种抗菌肽甚至不同抗生素的制备工艺中,为将来临床上各种药物的制备提供了一种新思路。
附图说明
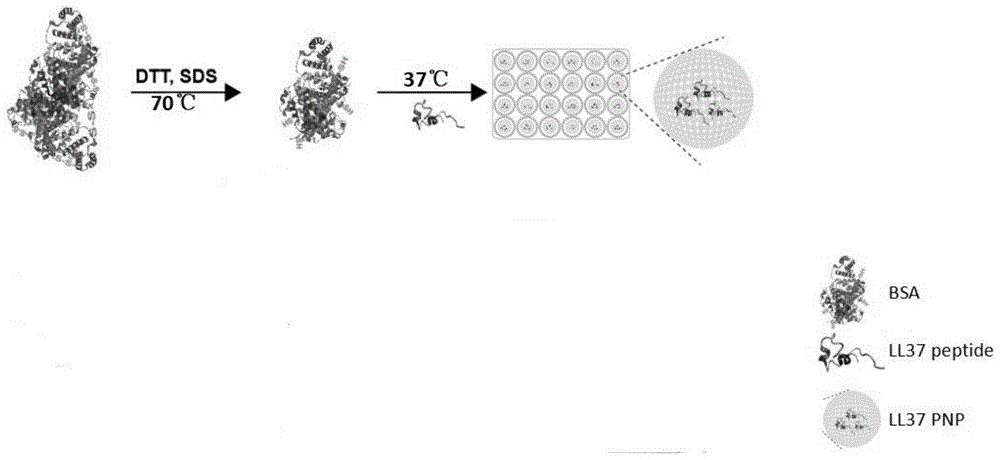
图1是本发明纳米颗粒包被的抗菌肽的制备的操作流程。
图2是带有fitc荧光的ll37(ll37-fitc40ug/ml,20ug/ml),带有fitc荧光的ll37纳米颗粒(ll37pnp-fitc40ug/ml,20ug/ml)与铜绿假单胞菌(pa)共培养后不同的时间段之后(0.5h,1.0h,2.0h,4.0h,8.0h,12.0h,24.0h,48.0h),通过流式细胞仪的检测,死亡的pa所占的比值。
图3是带有fitc荧光的ll37(ll37-fitc40ug/ml,20ug/ml),带有fitc荧光的ll37纳米颗粒(ll37pnp-fitc40ug/ml,20ug/ml)与铜绿假单胞菌(pa)共培养后不同的时间段之后(0.5h,1.0h,2.0h,4.0h,8.0h,12.0h,24.0h,48.0h),通过流式细胞仪的检测,所检测到的fitc的荧光强度。
具体实施方式
下面结合具体实施方式,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围;此外应理解,在阅读了本发明记载的内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本申请所附权利要求书所限定的范围。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市购获得的常规产品。
制备过程中需要的物质包括牛血清白蛋白(bsa),二硫苏糖醇(dtt),十二烷基硫酸钠(sds),经过巯基修饰的抗菌肽ll37(ll37peptide),2-(n-吗啉代)乙磺酸(mes)溶液,水浴加热锅,温控摇床,24孔板,所述经过巯基修饰的抗菌肽ll37购自吉尔生化有限公司。
实施1bsa纳米颗粒包被阳离子抗菌肽ll37的制备
所述制备方法具体如下:
1)将bsa40mg,dtt1.5mg和sds20mg溶于1ml无菌的双蒸水中,bsa的终浓度为40m/ml毫升,将该溶液置于250r/min的磁力搅拌之下进行70℃的水浴加热,得到还原的bsa溶液;
2)将40mg/ml的还原bsa溶液用mes缓冲液(ph=4.8)稀释至1mg/ml。将bsa溶液加入到24孔板中,将其置于37℃温度控制的振荡器中并以350r/min反应4.5个小时后以合成bsa纳米颗粒;
3)将bsa和合成ll37抗菌肽以9:1的质量比加入到24孔板中,并类似地置于37℃温度控制的振荡器中,转速为350r/min,4.5小时后合成ll37纳米颗粒;
4)最后使用超滤的方法去除纳米颗粒中的sds等物质,获得可用于后续实验的纳米颗粒。
实施例2
为了检测ll37纳米颗粒在药物传输过程中不易被降解,具有缓释作用,我们在试验中利用fitc标记ll37、带有fitc的ll37合成ll37纳米颗粒(ll37pnp)。带有fitc荧光的ll37(ll37-fitc40ug/ml,20ug/ml),带有fitc荧光的ll37纳米颗粒(ll37pnp-fitc40ug/ml,20ug/ml)与铜绿假单胞菌(pa)共培养后不同的时间段之后(0.5h,1.0h,2.0h,4.0h,8.0h,12.0h,24.0h,48.0h),通过流式细胞仪的检测,检测到fitc的荧光强度和死亡的细菌所占总体的比值。
流式的结果表明:pa的死亡率与加入的ll37,ll37pnp的浓度呈正相关。且随着时间的延长,pa的死亡率在ll37pnp组别中明显的上升(图2)。
另外,在共培养时间为2.0,4.0h的时候,ll37组中,带有fitc荧光的细菌量更多。但是时间延长到24.0,48.0h的时候,在ll37pnp组中,带有fitc荧光的细菌量明显多于ll37组(图3)。
实施例3bsa纳米颗粒包被阳离子抗菌肽ll37的制备
所述制备方法具体如下:
1)将bsa40mg,dtt1.5mg和sds20mg溶于1ml无菌的双蒸水中,bsa的终浓度为40m/ml毫升,将该溶液置于250r/min的磁力搅拌之下进行70℃的水浴加热,得到还原的bsa溶液;
2)将40mg/ml的还原bsa溶液用mes缓冲液(ph=4.8)稀释至1mg/ml。将bsa溶液加入到24孔板中,将其置于37℃温度控制的振荡器中并以350r/min反应4.5个小时后以合成bsa纳米颗粒;
3)将bsa和合成ll37抗菌肽以8:2的质量比加入到24孔板中,并类似地置于37℃温度控制的振荡器中,转速为350r/min,4.5小时后合成ll37纳米颗粒;
4)最后使用超滤的方法去除纳米颗粒中的sds等物质,获得可用于后续实验的纳米颗粒。
实施例4bsa纳米颗粒包被阳离子抗菌肽ll37的制备
所述制备方法具体如下:
1)将bsa40mg,dtt1.5mg和sds20mg溶于1ml无菌的双蒸水中,bsa的终浓度为40m/ml毫升,将该溶液置于250r/min的磁力搅拌之下进行70℃的水浴加热,得到还原的bsa溶液;
2)将40mg/ml的还原bsa溶液用mes缓冲液(ph=4.8)稀释至1mg/ml。将bsa溶液加入到24孔板中,将其置于37℃温度控制的振荡器中并以350r/min反应4.5个小时后以合成bsa纳米颗粒;
3)将bsa和合成ll37抗菌肽以7:3的质量比加入到24孔板中,并类似地置于37℃温度控制的振荡器中,转速为350r/min,4.5小时后合成ll37纳米颗粒;
4)最后使用超滤的方法去除纳米颗粒中的sds等物质,获得可用于后续实验的纳米颗粒。
实施例5plga纳米颗粒包被阳离子抗菌肽ll37的制备
将20mgplga聚合物溶于1ml二氯甲烷中,将20μlll37在20μl无菌水中加入到plga溶液中并在70w下超声处理(bransonsonifier,usa)15秒形成w/o初级乳液。将初级乳液用2ml溶解在无菌水中的1%(w/v)聚乙烯醇(pva,mw13000-23000,sigma-aldrich,de)进一步乳化,并再次在70w下超声处理15秒以产生w/o/w乳液。将该乳液一滴一滴地加入到50ml的0.3%(w/v)pva中,并在水浴上以600rpm和37℃搅拌1小时。然后通过离心在22000×g和4℃下在无菌水中洗涤纳米颗粒悬浮液两次40分钟。然后将所有颗粒冷冻干燥并冻干24小时,并在4℃下储存直至进一步使用。所有使用的材料都经过灭菌,程序在层流下进行。
实施例6实施例1、3~5颗粒性状的研究
采用nanozs激光粒度仪检测颗粒粒径,结果见表1;采用高效液相色谱法测定载药颗粒中ll37抗菌肽的吸光度,根据公式计算bsa纳米颗粒对ll37抗菌肽的载药率,具体结果见表1;利用fitc标记ll37、带有fitc的ll37合成ll37纳米颗粒与铜绿假单胞菌共培养24h,通过流式细胞仪的检测,检测到fitc的荧光强度,结果见表1。
表1纳米颗粒的粒径、载药率和缓释效果(n=5)
结果表明,实施例1制得的bsa纳米颗粒包被的阳离子抗菌肽ll37粒径大小均一,载药率高,缓释效果好,而实施例3、4在bsa和合成ll37抗菌肽混合过程中液体有明显白色浑浊析出,抗菌肽ll37利用率低,载药效果也低于实施例1,粒径之间差异较大,采用plga作为载体制备的纳米颗粒,载药率低,在缓释效果上,也逊色于bsa纳米颗粒包被的阳离子抗菌肽ll37。
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员,在不脱离本发明方法的前提下,还可以做出若干改进和补充,这些改进和补充也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!
- 一种纳米载药系统(DOX‑RGD‑BSA@AuNCs)药物传递和生物成像的制造方法与工艺
- 载多金属氧酸盐抗癌纳米制剂的制备的制造方法与工艺
- 一种新型包载雷公藤甲素和羟基喜树碱的多臂聚乙二醇纳米药物的制备方法与流程
- 肿瘤靶向光热响应可控释放药物纳米传输载体的制备方法与流程
- 一种液态金属药物体系及其制备和递送、释放方法与流程
- 一种基于直接竞争荧光免疫法定量检测叶酸功能化二氧化硅靶向纳米药物载体的方法与流程
- 一种靶向纳米药物载体及其制备方法和应用与流程
- 一种叶酸功能化二氧化硅靶向纳米药物载体的定量检测方法与流程
- 一种改性石墨烯与纳米纤维素复合温敏材料的制备方法与制造工艺
- 一种介孔碳纳米管复合纤维素温敏吸附材料的制备方法与制造工艺