一种肠癌腹膜转移预测模型及该模型的构建方法与流程
本发明涉及生物医学领域,更具体地,涉及一种肠癌腹膜转移预测模型及该模型的构建方法。
背景技术:
结直肠癌是全球第三大最常见的癌症,每年估计有10万新发病例,是癌症相关死亡事件的第三大原因(ca2019)。腹膜转移被认为是结直肠癌的终末期,结直肠癌患者中同时性腹膜转移的发生率约为5-10%,约有5%的患者在根治性切除术后被发现存在异时性的腹膜转移,大约25-44%的复发的患者存在腹膜转移。最近,细胞减灭术(cytoreductive,crs)联合腹腔热灌注化疗(hipec)治疗结直肠癌腹膜转移在全球的许多中心被广泛采用,这种治疗模式可使腹膜转移的患者中位生存期提高到32个月。早期诊断的同时性腹膜转移,即腹膜癌指数(pci)<20分时,可以获得完全性的crs+hipec治疗。然而在大多数腹膜转移患者都在较晚的阶段被诊断,往往不能实施完全的crs,其总生存期为10个月。术前诊断腹膜转移可以避免开腹探查以减少创伤,尽早行全身辅助化疗。新辅助化疗能够缩小并控制肿瘤,为完整性切除原发肿瘤,提高根治性切除率(ro切除)。
目前的影像学检查手段,包括增强ct(对<0.5cm的转移灶只有11%的敏感性)、mri、pet-ct等,对<0.5cm的腹膜转移灶检测不敏感。综合分析提取的腹膜转移癌的ct特征,对放射科医生做出诊断或发现高危患者的微小转移灶是非常有用的,这些特征包括t4分期,腹膜结节影、腹膜增厚、网膜增厚等。因此,整合这些腹膜转移的特异性特征,开发基于ct的诺模图(nomogram)对早期诊断至关重要。最近,一种基于ct表型、lauren分型、临近腹膜特征的nomogram图被开发出来,用于预测晚期胃癌隐匿性腹膜转移。该诺模图的诊断准确性>0.9,能够非常准确地预测隐匿性腹膜转移。该研究提示我们利用ct影像学特征联合临床病理参数,有望在术前准确的预测结直肠癌的腹膜转移。
然而目前针对结直肠癌腹膜转移的早期诊断的研究较少,尚缺乏有效的预测模型和预测方法。
技术实现要素:
本发明旨在克服上述现有技术的至少一种不足,提供一种肠癌腹膜转移预测模型,所述肠癌腹膜转移预测模型是基于ct特征的腹膜转移的诺模图,其预测准确性高,具有高灵敏度及特异度。
本发明的另一目的在于提供所述肠癌腹膜转移预测模型的构建方法。
本发明采取的技术方案是:
一种肠癌腹膜转移预测模型,所述预测模型为:
model=32.892+1.51*ct_stage+1.884*tumorlocation+20.447*distantmetastaticsites–19.898*thickenedgreateromentum–20.222*pelvicnodules;
其中,ct_stage为t分期;tumorlocation为肿瘤部位;distantmetastaticsites为远处转移部位;thickenedgreateromentum为大网膜增厚;pelvicnodules为盆腔种植结节。
本发明所述的肠癌腹膜转移预测模型是一种基于ct图像的诺模(nomogram)图,纳入了t分期,肿瘤部位,远处转移部位,大网膜增厚及盆腔种植结节,其能够用于早期术前诊断结直肠癌合并腹膜转移,能够准确的对每个肠癌患者进行个体化评分,术前预测腹膜转移的风险,其预测准确性高,具有高灵敏度及特异度。本发明的模型可以应用于结直肠癌合并早期腹膜转移的术前风险评估(非诊断性质的),随访监测每个患者根据模型术前预测腹膜转移的风险高低,再采取不同的预防和治疗措施,提高患者的生存率。
所述的肠癌腹膜转移预测模型的构建方法,包括如下步骤:
s1、建模变量选择:选择结直肠癌病例150~200例,随机分成训练集和验证集,分别包含腹膜转移组和无腹膜转移组,腹膜转移癌具体ct图像参数包括13项:肿瘤位置(左或右)、t分期、邻近器官侵犯(t4b)、n状态、腹膜斑块阴影、肿瘤增强程度、坏死、穿孔、pc转移部位、远处转移部位、腹水、大网膜增厚、盆腔种植结节;
s2、建模变量筛选:在训练组上,首先利用boruta算法在增强ct的腹膜转移特征中,筛选出与腹膜转移因变量相关的变量集,具体为:
(1)创建阴影特征(shadowfeature):对每个真实特征r,随机打乱顺序,得到阴影特征矩阵s,拼接到真实特征后面,构成新的特征矩阵n=[r,s];
(2)用新的特征矩阵n作为输入训练模型,能够输出特征的权重(featureimportance)模型,得到真实特征和阴影特征的权重;
(3)取阴影特征的特征权重的最大值w,真实特征中权重大于w的,记录一次命中;
(4)用(3)中记录的真实特征累计命中,标记特征重要或不重要,在boruta算法中增加fdr校正,用两步法参数切换两种检验方法;boruta算法中认为bonferroni校正太过保守,故默认增加了fdr校正;
(5)删除不重要的特征,重复1-4,直到所有特征都被标记;
s3、多变量回归模型的构建:对选出的变量集,应用前向逐步回归(forwardstep),根据aic准则(赤池信息准则)进一步筛选,最后得到肿瘤部位、t分期、远处转移部位、大网膜增厚以及盆腔种植结节这5个变量与腹膜转移密切相关;然后,对筛选出的5个变量,采用logistic回归模型建模即得肠癌腹膜转移预测模型。
优选地,在建模变量筛选前还包括对对连续变量的处理步骤:癌胚抗原水平(cea水平)以5ng/ml为分界点,小于5ng/ml为低水平,大于5ng/ml为高水平;年龄:以50、70为分界点,将其分为年轻(<50)、中年(50-69)、老年(>70)。
优选地,步骤s2中,权重模型为randomforest、lightgbm或xgboost。
与现有技术相比,本发明的有益效果为:本发明发现肿瘤部位、t分期、远处转移部位、网膜厚度、盆腔种植结节这5个因素与肠癌腹膜转移具有明显相关性,利用多变量回归构建了基于ct图像的诺模图(nomogram),纳入了t分期,肿瘤部位,远处转移部位,大网膜增厚及盆腔种植结节,能够准确的对每个肠癌患者进行个体化评分,术前预测腹膜转移的风险,其预测准确性高,具有高灵敏度及特异度。本发明的模型可以应用于结直肠癌合并早期腹膜转移的术前风险评估(非诊断性质的),随访监测每个患者根据模型术前预测腹膜转移的风险高低,再采取不同的预防和治疗措施,提高患者的生存率。
附图说明
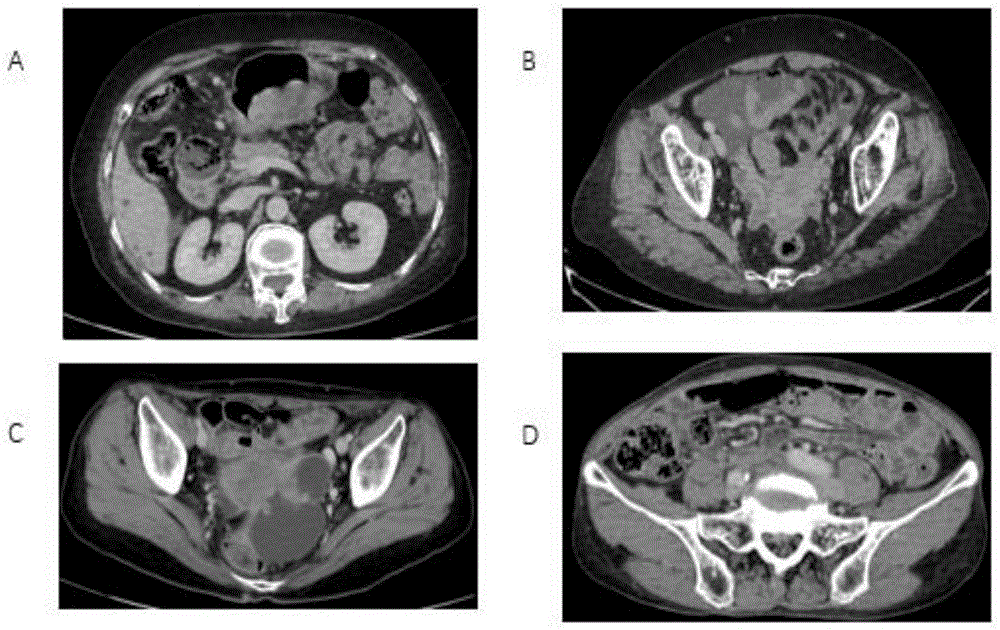
图1为增强ct中腹膜转移的典型特征图。
图2为roc曲线显示ct-based模型对腹膜转移的术前预测图。
图3为基于ct的nomogram图用于预测腹膜转移的风险预测图。
图4为在训练集(a,b)和测试集(c,d)中基于ct的nomogram图的决策曲线和校准曲线。
具体实施方式
本发明附图仅用于示例性说明,不能理解为对本发明的限制。为了更好说明以下实施例,附图某些部件会有省略、放大或缩小,并不代表实际产品的尺寸;对于本领域技术人员来说,附图中某些公知结构及其说明可能省略是可以理解的。
实施例1
一种肠癌腹膜转移预测模型,其构建方法如下:
1、建模变量选择:选择结直肠癌病例170例,随机分成训练集和验证集,分别包含腹膜转移组和无腹膜转移组,腹膜转移癌具体ct图像参数包括13项:肿瘤位置(左或右)、t分期、邻近器官侵犯(t4b)、n状态、腹膜斑块阴影、肿瘤增强程度、坏死、穿孔、pc转移部位、远处转移部位、腹水、大网膜增厚、盆腔种植结节,如图1所示,图1为增强ct中腹膜转移的典型特征,图1a:t4b,肿瘤侵犯局部临近腹膜;图1b:盆腔腹水;图1c:卵巢转移;图1d:腹膜转移肿瘤侵犯泌尿系统。
2、对连续变量的处理:癌胚抗原水平(cea水平)以5ng/ml为分界点,小于5ng/ml为低水平,大于5ng/ml为高水平;年龄:以50、70为分界点,将其分为年轻(<50)、中年(50-69)、老年(>70)。
3、建模变量筛选:在训练组上,首先利用boruta算法在增强ct的腹膜转移特征中,筛选出与腹膜转移因变量相关的变量集,具体为:
(1)创建阴影特征(shadowfeature):对每个真实特征r,随机打乱顺序,得到阴影特征矩阵s,拼接到真实特征后面,构成新的特征矩阵n=[r,s];
(2)用新的特征矩阵n作为输入训练模型,能够输出特征的权重(featureimportance)模型,如randomforest、lightgbm、xgboost,得到真实特征和阴影特征的特征重要性;
(3)取阴影特征的权重的最大值w,真实特征中权重大于w的,记录一次命中;
(4)用(3)中记录的真实特征累计命中,标记特征重要或不重要,在boruta算法中增加fdr校正,用两步法参数切换两种检验方法;boruta算法中认为bonferroni校正太过保守,故默认增加了fdr校正;
(5)删除不重要的特征,重复1-4,直到所有特征都被标记。结果原发肿瘤所在部位(左边或右边)、t分期、肿瘤强化程度、腹膜转移部位、远处转移部位、大网膜增厚,以及盆腔种植结节与肠癌腹膜转移相关。
4、多变量回归模型的构建:对选出的变量集,应用前向逐步回归(forwardstep),根据aic准则(赤池信息准则)进一步筛选,最后得到肿瘤部位、t分期、远处转移部位、大网膜增厚以及盆腔种植结节这5个变量与腹膜转移密切相关;然后,对筛选出的5个变量,采用logistic回归模型建模即得肠癌腹膜转移预测模型:
model=32.892+1.51*ct_stage+1.884*tumorlocation+20.447*distantmetastaticsites–19.898*thickenedgreateromentum–20.222*pelvicnodules。
本发明还对其进行了验证:多变量回归模型的验证:在训练集的曲线下面积(auc):0.929,(95%ci:0.879-0.979),敏感性:0.732,特异性:0.983,阳性预测值:82.26%,阴性预测值100%。
验证集:auc:0.855,(95%ci:0.764-0.946),敏感性:0.727,特异性:0.933.阳性预测值:82.35%,阴性预测值88.89%。
如图2所示为roc曲线显示ct-based模型对腹膜转移的术前预测图,其中左图为训练集,右图为验证集。通过对比训练集和验证集可知,所述的肠癌腹膜转移预测模型ct-based模型对腹膜转移的术前预测准确度高。
如图3所示为所述肠癌腹膜转移预测模型ct-basednomogram图术前预测腹膜转移的风险预测图。
肠癌腹膜转移预测模型ct-basednomogram评估如下:采用校正曲线(calibrationcurve)和决策曲线(decisioncurveanalysis)两种方法,分别在测试组和验证组上评价该ct-basednomogram的性能。以上建模及数据筛选与绘图,通过r软件(版本号3.3.1)实现,采用以下模块来进行:c060,glmnet,rms,pec,survminer,survmisc,compare,andprogramsofdecisioncurveanalysis。
训练集:校正曲线非常接近理想的45度对角线,表明该ct特征诺模图术前预测腹膜转移准确度很高(图4a),同时dcr曲线显示该诺模图能够明显给临床决策(诊断是否腹膜转移)带来明显益处(图4c)。
验证集:校正曲线同样显示诺模图准确度非常高(图4b),dca曲线显示诺模图预测腹膜转移带来的益处很大(图4d)。
通过上述实验可知,本发明所述肠癌腹膜转移预测模型ct-basednomogram对腹膜转移的早期术前诊断存在很高准确度和临床应用价值。
显然,本发明的上述实施例仅仅是为清楚地说明本发明技术方案所作的举例,而并非是对本发明的具体实施方式的限定。凡在本发明权利要求书的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明权利要求的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!