多重交联半月板修复用水凝胶及其制备方法与流程
本发明涉及一种多重交联半月板修复用水凝胶及其制备方法,属于医用材料技术领域。
背景技术:
据申请人了解,半月板损伤是最常见的膝关节损伤之一,因为膝关节处缺乏血供,大部分营养物质只能通过关节滑液的循环进行提供。一旦半月板发生损伤,很难进行自修复。半月板分为红区和白区,红区为周边血供区,该处的损伤较易愈合;一旦损伤发生在白区,即缺血供区,自愈合基本不会发生。
临床上常见的半月板修复技术有基于关节镜的内-外技术、外-内技术、全内技术、t-fix技术和半月板箭等。其中t-fix缝合技术由于操作相对简单,可针对各种类型的半月板损伤,在临床上很受欢迎。但上述方法仍存在愈后恢复时间长、效果不稳定等问题。在此基础上还开发出了愈合增强技术,如在缺损区域注入纤维蛋白凝块、为白区建立血供的环钻术、锉磨半月板等,但这些技术并未在临床上大量普及。
对于轻中度的半月板缺损可进行修补,但对于半月板的重度缺损只能进行半月板的完全摘除。半月板摘除后由于关节面直接接触,长此以往会造成关节软骨的磨损诱发退行性病变。目前重建完整半月板的方法有异种或同种异体半月板移植、天然或人工材料复合或不复合细胞构建的人工半月板,但由于伦理、疾病传播、无法模拟半月板天然结构等原因在临床上应用很少,大多停留在研究阶段。
专利号cn201210224724.5、授权公告号cn102716515b的中国发明专利,公开了一种修复半月板撕裂的生物材料及其制备方法,该材料由内层的脱细胞基质膜、中间层的多孔结构胶原基质膜、外层的软骨细胞形成的细胞层及细胞膜片构成。该修复材料具有一定的弹性、韧性和良好的生物活性,软骨细胞可以自行分泌细胞因子,并可通过关节腔滑液直接获得营养成分,加快半月板撕裂过程中与撕裂两端组织细胞间通讯连接的建立,促进材料中细胞与自体组织细胞迁入融合。然而,虽然该材料在兔模型上取得了不错的效果,但是其制备方法繁琐、耗时长,距临床应用还有很长一段路要走;且因材料中加入细胞,在临床应用和大规模生产上会面临挑战。
申请号cn201680050493.7、申请公布号cn108136069a的中国发明专利申请,公开了一种半月板修复粘合剂,包含:(a)具有至少一个游离异氰酸酯基的预聚物,预聚物能够结合至组织并且在暴露于水时在体内固化以形成压缩模量为1.9至14.4mpa且拉伸模量为5.0至30的聚合物;和(b)可在预聚物中混溶的油,油选自硅油、矿物油、植物油以及它们的组合。然而,其成分含有异氰酸酯,用于体内时可能会有一定的风险,且其并未提供模量数据,在半月板的稳定性未知。
申请号cn201710212986.2、申请公布号cn107648665a的中国发明专利申请,公开了一种植入体内用于修复半月板损伤的假体,该假体由天然聚合物、多糖、生长因子和粘附因子交联而成,是一种支架结构,支架内部具有干燥的小孔,孔径在50微米到500微米之间。但是,一方面其实际效果并未有数据证明;另一方面其材料中含有细胞因子,细胞因子在常温下的稳定性和临床应用上的安全性并未考虑到。
申请号cn201710725858.8、申请公布号cn107384306a的中国发明专利申请,公开了一种生物粘合剂,包括如下组分:组分a:功能化的星状高分子或/和功能化的梳状高分子,其中,功能化的星状高分子上带一种或多种活性基团,功能化的梳状高分子上带一种或多种活性基团;组分b:功能化的多糖,其中,功能化的多糖上带一种或多种活性基团;组分a的活性基团和组分b的活性基团可化学反应形成新的化学键。但是,一方面,该技术方案需要依赖星状高分子或梳状高分子作为起始原料,这就与本发明完全不同;另一方面,虽然该技术方案中的组分a和组分b可以分别带有不同活性基团且这些活性基团有着较大的选择范围,然而两组分应该分别带有哪些具体活性基团、应该分别带有多少比例/数量的具体活性基团,这些因素往往会导致最终所得材料的物理/化学特性有着根本差异,进而导致其用途迥异,但该技术方案中却并没有涉及此方面的内容。
申请人曾于2018年7月18日申请了中国发明专利申请(申请号cn201810806833.5、申请公布号cn109161037a),其中提供了一种水凝胶复合物,能配合临床关节镜,通过一次性微创注射,在任意缺损部位快速成胶进行填补,并且能够紧密粘附在缺损部位,达到促进软骨修复的效果。目前申请人在进一步的研发过程中获得了新的技术成果,并以此来申请专利。
技术实现要素:
本发明的主要目的是:克服现有技术存在的问题,提供一种多重交联半月板修复用水凝胶的成套原料试剂,采用该成套原料试剂可以制备多重交联半月板修复用水凝胶,用以修复缝合后的半月板;同时,还提供相应的多重交联半月板修复用水凝胶制剂,以及成套原料试剂、制剂的制备方法。
本发明解决其技术问题的技术方案如下:
一种多重交联半月板修复用水凝胶的成套原料试剂,由第一组分和第二组分构成,其特征是,所述第一组分为改性的胶原类物质,所述改性的胶原类物质具有含巯基和氨基的侧链,所述胶原类物质为胶原、去端肽胶原、明胶、胶原肽之一;所述第二组分为改性的多糖,所述改性的多糖具有含醛基和琥珀酰亚胺的侧链,所述多糖为透明质酸、葡聚糖、海藻酸钠、几丁质、淀粉之一。
采用该成套原料试剂可以制备出多重交联半月板修复用水凝胶,用以修复缝合后的半月板。
优选地,所述第一组分由以下方法制得:
m1.将所述胶原类物质溶于醋酸溶液以形成胶原-醋酸溶液,向胶原-醋酸溶液中加入活化剂进行活化反应;所述活化剂为edc与nhs的组合物,或dmtmm;
m2.活化反应后,向反应液中加入巯基化试剂和氨基化试剂进行接技改性反应;所述巯基化试剂为胱胺,所述氨基化试剂为己二酰二胺、碳酰胺、乙二胺、或丁二胺;
m3.接技改性反应后,向反应液中加入还原剂进行还原反应;所述还原剂为tcep或dtt;
m4.还原反应后,将反应液透析或超滤,并将所得产物冻干即得第一组分。
优选地,所述第二组分由以下方法制得:
p1.将所述多糖溶于纯化水以形成多糖溶液,向多糖溶液中加入高碘酸钠,避光反应;
p2.反应后,向反应液中加入阳离子交换树脂进行交换反应;
p3.交换反应后,除去阳离子交换树脂,向反应液中加入四丁基氢氧化铵进行反应;在反应后对反应液进行醇沉,并将沉淀进行干燥;
p4.将干燥后沉淀溶于dmso中形成dmso溶液,向dmso溶液中加入琥珀酰亚胺磷酸二苯酯进行反应;在反应后向反应液加正己烷并取沉淀,以丙酮洗涤沉淀后,将沉淀进行干燥,即得第二组分。
更优选地,m1中,所述胶原-醋酸溶液中胶原类物质的质量分数为1~100mg/ml,所述edc与nhs的组合物中edc与nhs的质量比为1:(1~2);活化反应的时间为至少30分钟;加入活化剂后,溶液中活化剂的质量分数为0.5~5%。
m2中,所述巯基化试剂与胶原类物质的质量比为0.2:1~10:1,所述氨基化试剂与胶原类物质的质量比为0.2:1~10:1;在接技改性反应过程中,采用盐酸和氢氧化钠溶液来调节反应液的ph值处于4~5的范围内;接技改性反应的时间为至少24小时;
m3中,所述还原剂与巯基化试剂的摩尔比为1:1,还原反应的时间为至少2小时;在还原反应过程中,采用盐酸和氢氧化钠溶液来调节反应液的ph值处于4~5的范围内;还原反应结束时采用氢氧化钠溶液调节ph值至8.0以上来终止反应;
m4中,所得第一组分于0℃~4℃保存;
m1至m3中,反应温度均为室温,室温指26℃±5℃。
更优选地,p1中,所述多糖溶液中多糖的质量分数为10~200mg/ml,所述高碘酸钠与多糖重复单元的摩尔比为0.25:1~1:1,反应时间为至少24小时;
p2中,所述阳离子交换树脂与反应液中多糖的质量比为10±5:1,反应时间为至少6小时;
p3中,采用绢丝过滤除去阳离子交换树脂;四丁基氢氧化铵与多糖重复单元的摩尔比为1:1~1:1.5,反应时间为至少6小时;醇沉时采用至少4倍反应液体积的乙醇,干燥时采用真空干燥箱且干燥时间至少48小时;
p4中,dmso溶液中干燥后沉淀的质量分数为10~50mg/ml,琥珀酰亚胺磷酸二苯酯与多糖重复单元的摩尔比为0.4:1~1:1,反应时间为至少2小时;正己烷的加入体积为反应液体积的至少3倍,洗涤所用丙酮的总体积为反应液体积的至少2倍,洗涤次数为至少3次;干燥时采用真空干燥箱且干燥时间至少48小时;所得第二组分于0℃~4℃保存;
所述多糖重复单元的摩尔量=多糖的质量÷多糖重复单元的分子量;p1至p4中,反应温度均为室温,室温指26℃±5℃。
采用以上优选方案的成套原料试剂,可以更好地制备出多重交联半月板修复用水凝胶。
本发明还提供:
一种多重交联半月板修复用水凝胶成套原料试剂的制备方法,所述成套原料试剂由第一组分和第二组分构成,其特征是,所述第一组分为改性的胶原类物质,所述改性的胶原类物质具有含巯基和氨基的侧链,所述胶原类物质为胶原、去端肽胶原、明胶、胶原肽之一;所述第二组分为改性的多糖,所述改性的多糖具有含醛基和琥珀酰亚胺的侧链,所述多糖为透明质酸、葡聚糖、海藻酸钠、几丁质、淀粉之一;
所述制备方法由第一组分的制备方法和第二组分的制备方法构成;
所述第一组分的制备方法包括以下步骤:
m1.将所述胶原类物质溶于醋酸溶液以形成胶原-醋酸溶液,向胶原-醋酸溶液中加入活化剂进行活化反应;所述活化剂为edc与nhs的组合物,或dmtmm;
m2.活化反应后,向反应液中加入巯基化试剂和氨基化试剂进行接技改性反应;所述巯基化试剂为胱胺,所述氨基化试剂为己二酰二胺、碳酰胺、乙二胺、或丁二胺;
m3.接技改性反应后,向反应液中加入还原剂进行还原反应;所述还原剂为tcep或dtt;
m4.还原反应后,将反应液透析或超滤,并将所得产物冻干即得第一组分;
所述第二组分的制备方法包括以下步骤:
p1.将所述多糖溶于纯化水以形成多糖溶液,向多糖溶液中加入高碘酸钠,避光反应;
p2.反应后,向反应液中加入阳离子交换树脂进行交换反应;
p3.交换反应后,除去阳离子交换树脂,向反应液中加入四丁基氢氧化铵进行反应;在反应后对反应液进行醇沉,并将沉淀进行干燥;
p4.将干燥后沉淀溶于dmso中形成dmso溶液,向dmso溶液中加入琥珀酰亚胺磷酸二苯酯进行反应;在反应后向反应液加正己烷并取沉淀,以丙酮洗涤沉淀后,将沉淀进行干燥,即得第二组分。
该制备方法能顺利制备出多重交联半月板修复用水凝胶成套原料试剂。
本发明还提供:
一种多重交联半月板修复用水凝胶,其特征是,由前文所述的多重交联半月板修复用水凝胶成套原料试剂经以下步骤配制获得:
t1.将第一组分溶于海藻糖-生理盐水中并以盐酸调节ph至弱酸性形成第一溶液,所述海藻糖-生理盐水为含有海藻糖的生理盐水;将第二组分溶于生理盐水中并以氢氧化钠溶液调节ph至弱碱性形成第二溶液;所述弱酸性指5.0<ph<7.0,所述弱碱性指7.0<ph<9.0;
t2.将第一溶液与第二溶液共混;在第一溶液与第二溶液的混合溶液中,所述第一组分的质量大于第二组分的质量;
t3.所述混合溶液随时间推移固化成胶,最终所得凝胶即为多重交联半月板修复用水凝胶成品。
t1中对于第一溶液采用含海藻糖的生理盐水进行配制,海藻糖可显著提高第一组分——改性胶原类物质的温度稳定性,从而延长其在室温下的保存时间;该胶可在t2后即通过针头注射到半月板缝合处或关节面软骨缺损处,然后混合溶液即在席夫碱反应下固化成胶,在此过程中,醛基与氨基之间发生席夫碱反应、巯基与琥珀酰亚胺之间发生加成反应、氨基与琥珀酰亚胺发生反应、巯基与巯基生成二硫键,如此即形成多重交联,同时上述交联键大部分为动态交联,可发生可逆反应,有利于自修复。固化成胶所需时间为30~600秒,之后所得凝胶的强度可达1~2mpa。
优选地,t1中,所述第一溶液中第一组分的浓度为5~40mg/ml;所述第二溶液中第二组分的浓度为5~40mg/ml;所述海藻糖-生理盐水中,氯化钠的浓度为9mg/ml、海藻糖的浓度为20~100mg/ml,所述生理盐水中氯化钠的浓度为9mg/ml,所述第一溶液的ph为5.5~6.0,所述第二溶液的ph为8.5~9.0;所述第一溶液中第一组分的浓度与第二溶液中第二组分的浓度相同;t2中,所述第一溶液与第二溶液的体积比为3:1。
(注:共混时可采用两注射器以连接头连通后往复互推以混合均匀,也可酌情采用其它混匀手段。)
采用以上优选方案,可使该多重交联半月板修复用水凝胶更易制得。
本发明还提供:
一种多重交联半月板修复用水凝胶的制备方法,其特征是,采用前文所述的多重交联半月板修复用水凝胶成套原料试剂,所述制备方法包括以下步骤:
t1.将第一组分溶于海藻糖-生理盐水中并以盐酸调节ph至弱酸性形成第一溶液,所述海藻糖-生理盐水为含有海藻糖的生理盐水;将第二组分溶于生理盐水中并以氢氧化钠溶液调节ph至弱碱性形成第二溶液;所述弱酸性指5.0<ph<7.0,所述弱碱性指7.0<ph<9.0;
t2.将第一溶液与第二溶液共混;在第一溶液与第二溶液的混合溶液中,所述第一组分的质量大于第二组分的质量;
t3.所述混合溶液随时间推移固化成胶,最终所得凝胶即为多重交联半月板修复用水凝胶成品。
该制备方法能顺利制备出多重交联半月板修复用水凝胶。
本发明还提供:
前文所述多重交联半月板修复用水凝胶的用途,其特征是,所述用途为用作药剂或用于制备药剂,所述药剂包括半月板修复剂、关节面软骨缺损修复剂。
本发明的多重交联半月板修复用水凝胶是多重交联高强度自修复保护凝胶,可施用于半月板缝合处从而形成保护屏障,一方面,可保护其在恢复期免受关节软骨的物理磨损,并能承受运动时上下关节面施加的循环应力而不破损;另一方面,动态交联赋予凝胶自修复功能,能自动修复凝胶本身微小的缺损,能促进缝合伤口的愈合、填补缝合处的微小空缺,从而促进半月板的修复,减短术后恢复时间并提升愈后效果;此外该凝胶也可作为关节面轻度缺损的填充,配合微骨折术修复软骨缺损。
附图说明
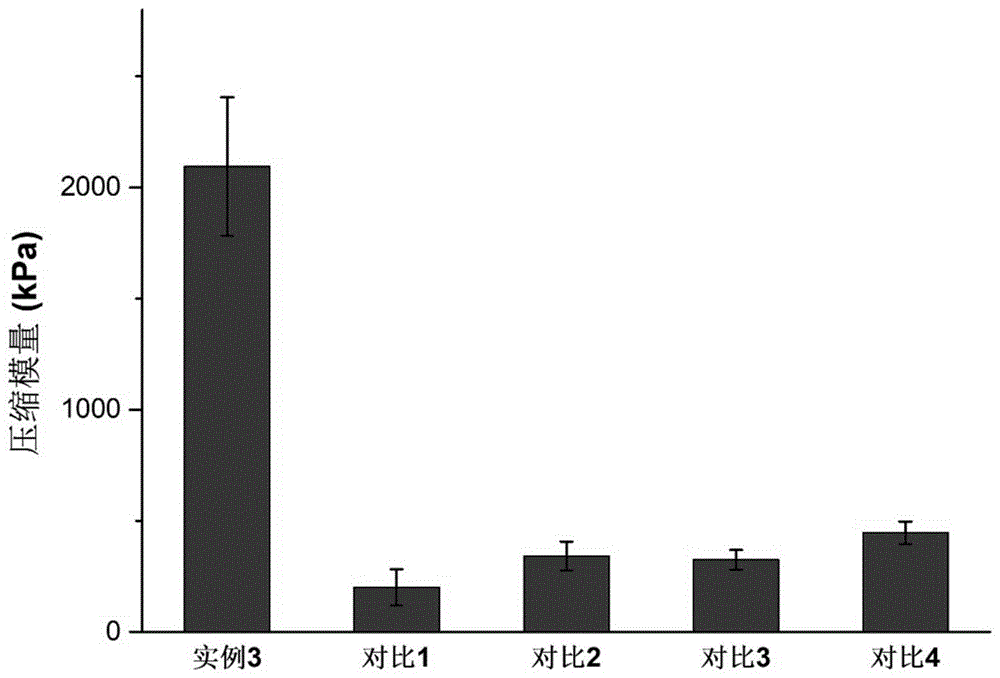
图1为本发明实施例3的结果示意图。
图2为本发明实施例4的结果示意图。
具体实施方式
下面结合实施例对本发明作进一步详细描述。但是本发明不限于所给出的例子。
实施例1、多重交联半月板修复用水凝胶成套原料试剂
本实施例的多重交联半月板修复用水凝胶成套原料试剂,由第一组分和第二组分构成,第一组分为改性的胶原类物质,改性的胶原类物质具有含巯基和氨基的侧链,胶原类物质为胶原、去端肽胶原、明胶、胶原肽之一;第二组分为改性的多糖,改性的多糖具有含醛基和琥珀酰亚胺的侧链,多糖为透明质酸、葡聚糖、海藻酸钠、几丁质、淀粉之一。(注:胶原有很多种类型,经实验验证胶原类型的不同并不影响本发明最终所得水凝胶的性能,因此各实施例中的胶原均采用i型胶原作为典型代表,但这并不能将本发明采用的胶原限制于i型胶原。)
本实施例的第一组分由以下方法制得:
m1.将胶原类物质溶于醋酸溶液(如0.2m醋酸)以形成胶原-醋酸溶液,胶原-醋酸溶液中胶原类物质的质量分数为1~100mg/ml,向胶原-醋酸溶液中加入活化剂进行活化反应(本实施例采用:反应过程中持续搅拌混合),溶液中活化剂的质量分数为0.5~5%(即每100ml溶液含活化剂0.5~5g);活化反应的时间为至少30分钟;活化剂为edc与nhs的组合物,或dmtmm;edc与nhs的组合物中edc与nhs的质量比为1:(1~2)。
m2.活化反应后,向反应液中加入巯基化试剂和氨基化试剂进行接技改性反应(本实施例采用:反应过程中持续搅拌),接技改性反应的时间为至少24小时,巯基化试剂与胶原类物质的质量比为0.2:1~10:1,氨基化试剂与胶原类物质的质量比为0.2:1~10:1;在接技改性反应过程中,采用盐酸和氢氧化钠溶液来调节反应液的ph值处于4~5的范围内;巯基化试剂为胱胺,氨基化试剂为己二酰二胺、碳酰胺、乙二胺、或丁二胺。
m3.接技改性反应后,向反应液中加入还原剂进行还原反应(本实施例采用:反应过程中持续搅拌),还原反应的时间为至少2小时,还原剂与巯基化试剂的摩尔比为1:1;在还原反应过程中,采用盐酸和氢氧化钠溶液来调节反应液的ph值处于4~5的范围内;还原反应结束时采用氢氧化钠溶液调节ph值至8.0以上来终止反应(本实施例采用:5m氢氧化钠溶液);还原剂为tcep或dtt。
m1至m3中,反应温度均为室温,室温指26℃±5℃。
m4.还原反应后,将反应液透析或超滤,并将所得产物冻干即得第一组分。所得第一组分于0℃~4℃保存。
关于m4中的透析或超滤,具体举例如下:
若采用透析,则选用截留分子量为10000的透析袋,透析外液为纯化水,外液体积为反应液体积的5倍,透析6次,每次4小时,然后收集。之后,冻干,4℃下保存。
若采用超滤,用0.1%naoh溶液洗超滤膜30分钟,随后用纯化水洗膜至滤出液ph7.0左右。将反应液进行超滤,控制进口端与出口端的压力平均值小于0.2mpa,洗滤液为纯化水,待滤出液体积达到反应液初始体积的10倍时,停止超滤,浓缩,收集。之后,冻干,4℃下保存。
本实施例含有多个实例,各实例中第一组分的具体制备参数如下表所示:
本实施例的第二组分由以下方法制得:
p1.将多糖溶于纯化水以形成多糖溶液,多糖溶液中多糖的质量分数为10~200mg/ml,向多糖溶液中加入高碘酸钠,高碘酸钠与多糖重复单元的摩尔比为0.25:1~1:1,避光搅拌反应,反应时间为至少24小时。
p2.反应后,向反应液中加入阳离子交换树脂、搅拌进行交换反应,阳离子交换树脂与反应液中多糖的质量比为10±5:1,反应时间为至少6小时。
p3.交换反应后,采用绢丝过滤除去阳离子交换树脂,向反应液中加入四丁基氢氧化铵、搅拌进行反应,四丁基氢氧化铵与多糖重复单元的摩尔比为1:1~1:1.5,反应时间为至少6小时;在反应后对反应液进行醇沉(采用至少4倍反应液体积的乙醇),并将沉淀进行干燥(采用真空干燥箱且干燥时间至少48小时)。
p4.将干燥后沉淀溶于dmso中形成dmso溶液,dmso溶液中干燥后沉淀的质量分数为10~50mg/ml,向dmso溶液中加入琥珀酰亚胺磷酸二苯酯进行反应,琥珀酰亚胺磷酸二苯酯与多糖重复单元的摩尔比为0.4:1~1:1,反应时间为至少2小时;在反应后向反应液加正己烷并取沉淀(正己烷的加入体积为反应液体积的至少3倍),以丙酮洗涤沉淀(洗涤所用丙酮的总体积为反应液体积的至少2倍,洗涤次数为至少3次),将沉淀进行干燥(采用真空干燥箱且干燥时间至少48小时),即得第二组分。所得第二组分于0℃~4℃保存。
p1至p4中,反应温度均为室温,室温指26℃±5℃。
各实例中第二组分的具体制备参数如以下各表所示:
注:关于多糖重复单元的摩尔量,以实例3为例,海藻酸钠重复单元的分子量为352.25g/mol,因此海藻酸钠重复单元的摩尔量为海藻酸钠的质量除以352.25g/mol,即约0.00284mol。
实施例2、多重交联半月板修复用水凝胶
本实施例的多重交联半月板修复用水凝胶,由实施例1的多重交联半月板修复用水凝胶成套原料试剂经以下步骤配制获得:
t1.将第一组分溶于海藻糖-生理盐水中并以盐酸调节ph至弱酸性,形成5~40mg/ml的第一溶液;海藻糖-生理盐水为含有海藻糖的生理盐水,其中氯化钠的浓度为9mg/ml、海藻糖的浓度为20~100mg/ml;弱酸性指5.0<ph<7.0,本实施例中第一溶液的ph为5.5~6.0。
将第二组分溶于生理盐水中并以氢氧化钠溶液调节ph至弱碱性,形成5~40mg/ml的第二溶液;生理盐水中氯化钠的浓度为9mg/ml;弱碱性指7.0<ph<9.0,本实施例中第二溶液的ph为8.5~9.0。
第一溶液中第一组分的浓度与第二溶液中第二组分的浓度相同。
注:在具体实施时,在t1步后先将各溶液过0.22μm滤头除菌,然后在无菌环境下分别灌装于2ml预灌封注射器中备用。
t2.将第一溶液与第二溶液按体积比3:1共混;在第一溶液与第二溶液的混合溶液中,第一组分的质量大于第二组分的质量。(注:共混时可采用两注射器以连接头连通后往复互推以混合均匀,也可酌情采用其它混匀手段。)注:在具体实施时,在t2步后即将混合溶液通过针头注射到半月板缝合处或关节面软骨缺损处。
t3.混合溶液随时间推移固化成胶,最终所得凝胶即为多重交联半月板修复用水凝胶成品。
本实施例包含若干实例,且各实例为实施例1各实例的延续。
本实施例的水凝胶中,醛基与氨基之间发生席夫碱反应、巯基与琥珀酰亚胺之间发生加成反应、氨基与琥珀酰亚胺发生反应、巯基与巯基生成二硫键,如此即形成多重交联,同时上述交联键大部分为动态交联,可发生可逆反应,有利于自修复。固化成胶所需时间为30~600秒,之后所得凝胶的强度可达1~2mpa。
实施例3、压缩模量测定实验
本实施例采用实施例2实例3水凝胶、对比水凝胶1、对比水凝胶2、对比水凝胶3、对比水凝胶4,分别测定它们的压缩模量。
对比水凝胶1至4共涉及4种组分,这4种组分分别由以下方法制得:
(1)1号组分:巯基化改性胶原,其制备过程如下:
将1gi型胶原溶于100ml0.2m醋酸中形成10mg/ml的溶液,依次加入1gedc和1gnhs,搅拌混合30分钟。再加入0.2g胱胺,室温下搅拌反应24小时,反应过程中用盐酸和氢氧化钠溶液调节体系ph维持在4~5之间。反应24小时后加入0.37gtcep,继续搅拌2小时。用5mnaoh调节ph8.0终止反应。上述产物采用超滤或透析的方式提纯,冻干。
将所得巯基化改性胶原溶于实施例2采用的海藻糖-生理盐水中并以盐酸调节ph至5.5,得到30mg/ml的溶液,过滤后灌装于2ml预灌封注射器中,作为1号组分a。
或者,将所得巯基化改性胶原溶于实施例2采用的生理盐水中并以氢氧化钠溶液调节ph至9.0,得到30mg/ml的溶液,过滤后灌装于2ml预灌封注射器中,作为1号组分b。
(2)2号组分:氨基化改性胶原,其制备过程如下:
将1gi型胶原溶于100ml0.2m醋酸中形成10mg/ml的溶液,依次加入1gedc和1gnhs,搅拌混合30分钟。再加入0.4g己二酰二胺,室温下搅拌反应24小时,反应过程中用盐酸和氢氧化钠溶液调节体系ph维持在4~5之间。用5mnaoh调节ph8.0终止反应。上述产物采用超滤或透析的方式提纯,冻干。
将所得氨基化改性胶原溶于实施例2采用的海藻糖-生理盐水中并以盐酸调节ph至5.5,得到30mg/ml的溶液,过滤后灌装于2ml预灌封注射器中,作为2号组分。
(3)3号组分:醛基化改性海藻酸钠,其制备过程如下:
称取1g海藻酸钠溶于100ml纯化水中,加入0.54g高碘酸钠,在避光条件下室温搅拌24小时。上述产物采用超滤或透析的方式提纯,冻干。
将所得醛基化改性海藻酸钠溶于实施例2采用的生理盐水中并以氢氧化钠溶液调节ph至9.0,得到30mg/ml的溶液,过滤后灌装于2ml预灌封注射器中,作为3号组分。
(4)4号组分:琥珀酰亚胺化改性海藻酸钠,其制备过程如下:
称取1g海藻酸钠溶于100ml纯化水中,再加入10g阳离子交换树脂,搅拌6小时。用绢丝滤去阳离子树脂后再加入1.57g四丁基氢氧化铵,搅拌12小时后用4倍于反应体积的乙醇沉淀,于真空干燥箱中干燥48小时。干燥后的产物以20mg/ml的浓度溶于20mldmso中,加入0.47g琥珀酰亚胺磷酸二苯酯,室温下反应2个小时后用3倍于反应液体积的正己烷沉淀出产物,然后用总计2倍体积于反应液体积的丙酮洗涤3遍,于真空干燥箱中干燥48小时。4℃下保存产物。
将所得琥珀酰亚胺化改性海藻酸钠溶于实施例2采用的生理盐水中并以氢氧化钠溶液调节ph至9.0,得到30mg/ml的溶液,过滤后灌装于2ml预灌封注射器中,作为4号组分。
实施例2实例3水凝胶由其第一溶液与第二溶液按体积比3:1共混而得。
对比水凝胶1由3体积的1号组分a和1体积的1号组分b共混而得(巯基与巯基生成二硫键)。
对比水凝胶2由3体积的1号组分a和1体积的4号组分共混而得(巯基与琥珀酰亚胺之间发生加成反应)。
对比水凝胶3由3体积的2号组分和1体积的3号组分共混而得(氨基与醛基之间发生席夫碱反应)。
对比水凝胶4由3体积的2号组分和1体积的4号组分共混而得(氨基与琥珀酰亚胺发生反应)。
共混时采用两注射器以连接头连通后往复互推以混合均匀。混合后,将以上各水凝胶的混合液中各取1ml注射到24孔板中,等待约3~5分钟使其原位成胶,然后在th-8206s伺服电脑卧式拉力试验机上测量各水凝胶的压缩模量,压缩速度10mm/min,压缩形变量2mm。
结果如附图1所示,其中,各样品的压缩模量为:实施例2实例3水凝胶,2094±311kpa;对比水凝胶1,200±82kpa;对比水凝胶2,341±65kpa;对比水凝胶3,326±44kpa;对比水凝胶4,446±51kpa。
由该结果可知,实施例2实例3水凝胶的压缩模量远远大于对比水凝胶1至4的压缩模量,这说明本发明采用的多重交联能够发挥出远超单一交联形式的性能。
需要说明的是,本发明实施例2的其余各实例所得水凝胶也按照上述方法检测其压缩模量,测定结果与实例3基本一致。由这些实验数据可知,实施例2各实例所得水凝胶具有优良的强度性能。
实施例4、海藻糖提高第一组分——改性胶原类物质的温度稳定性
以实施例2采用的海藻糖-生理盐水、生理盐水分别溶解实施例1实例6中的第一组分,得到第一溶液a和第一溶液b,浓度均为15mg/ml,其ph均用盐酸调至5.9。将第一溶液a和第一溶液b分别过0.22μm滤头除菌,然后在无菌环境下分别灌装于一系列的2ml预灌封注射器中,置于40℃储存。之后,分别在第0、5、10、20、30天取出,与实施例2实例6的第二溶液按体积比3:1共混成胶。
将所得凝胶分别按实施例3中所述的方法测量压缩模量。结果如附图2所示,从图中可以看出,添加海藻糖的第一组分所形成的凝胶的压缩模量要高于同期不添加海藻糖的第一组分所形成的凝胶(第0天除外),且随着储存时间的延长,差异越来越明显。这说明海藻糖的加入可以显著提高第一组分——改性胶原类物质在较高温度下的稳定性,减少其降解,即可以显著延长第一组分的保质期。
注:第30天时,不加海藻糖组混合后已无法成胶,故压缩模量为0。
除上述实施例外,本发明还可以有其他实施方式。凡采用等同替换或等效变换形成的技术方案,均落在本发明要求的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!