基于温敏聚合物/碳点的介孔硅复合纳米粒子的制备方法与流程
本发明属于化学合成技术领域,具体涉及一种基于温敏聚合物/碳点的介孔硅复合纳米粒子的制备方法。
背景技术:
纳米粒子,例如脂质体,聚合物胶束,树状聚合物,碳纳米管和介孔硅纳米粒子(msns),已被广泛用作药物载体,因为它们不仅可以提高药物的溶解度和稳定性,而且可以提高药物的生物利用度并减少其全身性副作用。其中,介孔硅纳米粒子(msns)是最常用的纳米载体之一。msns具有高度有序的孔结构,均匀且可调节的孔尺寸和狭窄的分布,较高的比表面积和较大的孔体积,为药物的储存和输送提供了巨大的空间。msns具有低毒性、突出的生物降解性和稳定性,使其适合注入人体。且msns低廉的价格也为广泛的市场应用提供了有力的保证。但是,当巨噬细胞进入血液后,裸露的msns很容易被巨噬细胞清除。对其进行修饰是解决上述问题的最常用方法,同时也可以使msns功能化,例如靶向和控释,使其成为更理想的药物输送载体。
响应性聚合物是在环境因素的刺激下可能会相应改变其物理或化学性质的聚合物,可用于修饰msns。经其修饰的msns会得到响应性或智能性等功能,它们对特定刺激(如ph、温度等)敏感。大多数肿瘤组织的细胞ph值(ph=6.0-7.0)略低于健康组织和血液的ph值(ph=7.4)。肿瘤部位的温度略高于正常组织。智能msns可能会对这些差异敏感并实现相应响应。因此,构建一种温度/ph双响应药物递送系统(dds),并使其具有精准的靶向性和控释能力是极具研究价值的。
技术实现要素:
为了实现msns功能化,使其成为更理想的药物输送载体,本发明的目的在于提供一种基于温敏聚合物/碳点的介孔硅复合纳米粒子的制备方法,本发明首先合成富含氨基的碳点(cds)、端氨基聚n-乙烯基己内酰胺(pnvcl-nh2)、醛基化介孔二氧化硅纳米粒子(msns-cho),然后通过端醛基和端氨基之间的席夫碱反应制备了以碳点(cds)和聚n-乙烯基己内酰胺(pnvcl)作为混合壳的介孔二氧化硅纳米粒子(cds/pnvcl@msns)。并以此作为药物输送载体对药物进行包裹,当载体进入肿瘤环境(ph=5.0)时,具有ph响应性的亚胺键断裂,介孔打开,将药物释放出来。利用cds荧光性质的变化实时监测负载在此载体上的药物分子的运输和释放,实现了药物运输载体的可控释放和实时监控。
为解决上述技术问题,本发明采用的技术方案为:基于温敏聚合物/碳点的介孔硅复合纳米粒子,所述介孔硅复合纳米粒子是,以基于碳点/端氨基聚n-乙烯基己内酰胺/(cds/pnvcl-nh2)和醛基化介孔二氧化硅纳米粒子(msns)为构筑单元,制备的以msns为载体,cds和pnvcl为混合壳的新型药物输送系统。
基于温敏聚合物/碳点的介孔硅复合纳米粒子的制备方法,包括如下步骤:
1)碳点(cds)的制备:以柠檬酸和尿素为碳源,微波反应得到cds;
2)端氨基聚n-乙烯基己内酰胺(pnvcl-nh2)的制备:以偶氮二异丁腈(aibn)为引发剂,2-氨基乙硫醇为链转移剂,1,4二氧六环为溶剂,引发n-乙烯基己内酰胺(nvcl)聚合,得到端氨基聚n-乙烯基己内酰胺(pnvcl-nh2);
3)醛基化介孔二氧化硅纳米粒子(msns-cho)的制备:
a)介孔二氧化硅纳米粒子(msns)的制备:以十六烷基三甲基溴化铵(ctab)、氢氧化钠溶液及正硅酸乙酯(teos)为原料,在硝酸铵和乙醇溶液的催化下,反应得到介孔二氧化硅纳米粒子(msns);
b)氨基化介孔二氧化硅纳米粒子(msns-nh2)的制备:以(3-氨基丙基)三乙氧基硅烷(aps)为引发剂,甲苯为溶剂,与介孔二氧化硅纳米粒子(msns)反应得到氨基化介孔二氧化硅纳米粒子(msns-nh2);
c)醛基化介孔二氧化硅纳米粒子(msns-cho)的制备:以超纯水为溶剂,msns-nh2与戊二醛反应得到醛基化介孔二氧化硅纳米粒子(msns-cho);
4)聚n-乙烯基己内酰胺嫁接介孔二氧化硅纳米粒子(pnvcl@msns)的制备:醛基化介孔二氧化硅纳米粒子(msns-cho)和端氨基聚n-乙烯基己内酰胺(pnvcl-nh2)发生席夫碱反应,得到聚n-乙烯基己内酰胺嫁接介孔二氧化硅(pnvcl@msns);
5)碳点(cds)和聚n-乙烯基己内酰胺(pnvcl)作为混合壳的介孔二氧化硅纳米粒子(cds/pnvcl@msns)的制备:聚n-乙烯基己内酰胺嫁接介孔二氧化硅纳米粒子(pnvcl@msns)和含有氨基的碳点(cds)发生席夫碱反应,得到具有碳点(cds)和聚n-乙烯基己内酰胺(pnvcl)作为混合壳的介孔二氧化硅纳米粒子(cds/pnvcl@msns);
优选地,上述的基于温敏聚合物/碳点的介孔硅复合纳米粒子的制备方法,步骤1)包括如下步骤:将柠檬酸和尿素溶解在超纯水中,在700w微波下反应3min后,用水冷却至室温,得到cds粗产物,然后将cds粗产物分散到超纯水中,通过将装有cds溶液和超纯水的透析袋搅拌过夜,透析去除多余的前体和小分子,冷冻干燥得到cds。
所述柠檬酸与尿素的质量比为3:1~5。
优选地,上述的基于温敏聚合物/碳点的介孔硅复合纳米粒子的制备方法,其特征在于:步骤2)包括如下步骤:将n-乙烯基己内酰胺(nvcl)、偶氮二异丁腈(aibn)、2-氨基乙硫醇和1,4二氧六环在室温下混合搅拌,待固体充分溶解后,68℃反应14h,反应结束后,通过旋转蒸发除去溶剂,并用乙醚洗涤、沉淀、过滤、干燥得到端氨基聚n-乙烯基己内酰胺(pnvcl-nh2)。
所述n-乙烯基己内酰胺(nvcl)、偶氮二异丁腈(aibn)和2-氨基乙硫醇的质量比=50~100:1~5:1。
优选地,上述的基于温敏聚合物/碳点的介孔硅复合纳米粒子的制备方法,步骤3)包括如下步骤:
a)介孔二氧化硅纳米粒子(msns)的制备:将十六烷基三甲基溴化铵(ctab)、氢氧化钠溶液和超纯水置于反应瓶中,将溶液保持在80℃,加入正硅酸乙酯(teos)后,剧烈搅拌2h,所得产物用超纯水洗涤后,加入硝酸铵、乙醇溶液70℃下搅拌过夜,反应结束后,离心、洗涤、干燥得到介孔二氧化硅纳米粒子(msns);
所述十六烷基三甲基溴化铵(ctab)、氢氧化钠和正硅酸乙酯(teos)的质量比=5:1~5:1~25。
b)将介孔二氧化硅纳米粒子(msns)和(3-氨基丙基)三乙氧基硅烷(aps)分散在无水甲苯中,70℃回流反应12h,反应结束后,离心、洗涤、干燥得到氨基化介孔二氧化硅(msns-nh2);
所述介孔二氧化硅纳米粒子(msns)和(3-氨基丙基)三乙氧基硅烷(aps)的质量比=2:1~5。
c)以超纯水为溶剂,msns-nh2与戊二醛反应,室温下搅拌4h,反应结束后,离心、洗涤、干燥得到醛基化介孔二氧化硅(msns-cho);
所述msns-nh2和戊二醛的质量比=1:1~10。
优选地,上述的基于温敏聚合物/碳点的介孔硅复合纳米粒子的制备方法,其特征在于:步骤4)包括如下步骤:取醛基化介孔二氧化硅纳米粒子(msns-cho)溶解于超纯水中,在室温下剧烈搅拌,将端氨基聚n-乙烯基己内酰胺(pnvcl-nh2)加入溶液中,磁力搅拌反应4h,反应结束后,离心、洗涤、干燥得到聚n-乙烯基己内酰胺嫁接介孔二氧化硅纳米粒子(pnvcl@msns)。
优选地,上述的基于温敏聚合物/碳点的介孔硅复合纳米粒子的制备方法,所述醛基化介孔二氧化硅纳米粒子(msns-cho)和端氨基聚n-乙烯基己内酰胺(pnvcl-nh2)的质量比=1:1~5。
优选地,上述的基于温敏聚合物/碳点的介孔硅复合纳米粒子的制备方法,步骤5)包括如下步骤:取聚n-乙烯基己内酰胺嫁接介孔二氧化硅纳米粒子(pnvcl@msns)溶解于超纯水中,在37℃搅拌下加入碳点(cds),磁力搅拌反应4h,反应结束后,离心、洗涤、冷冻干燥得到具有碳点(cds)和聚n-乙烯基己内酰胺(pnvcl)作为混合壳的介孔二氧化硅纳米粒子(cds/pnvcl@msns)。
优选地,上述的基于温敏聚合物/碳点的介孔硅复合纳米粒子的制备方法,所述聚n-乙烯基己内酰胺嫁接介孔二氧化硅纳米粒子(pnvcl@msns)和碳点(cds)的质量比=1:0.5~2。
上述的基于温敏聚合物/碳点的介孔硅复合纳米粒子作为纳米药物载体材料在药物控制释放中的应用。
本发明的有益效果:
1、本发明的目标产物基于温敏聚合物/碳点的介孔硅复合纳米粒子,作为dds构筑单元的cds、pnvcl和msns,是通过动态亚胺键将cds和pnvcl链段与msns连接制备的新型药物载药系统,亚胺键具有ph响应性,pnvcl具有温度响应性。在室温下,pnvcl链段可溶并拉伸,因此msns的介孔处于开放状态,抗癌药-阿霉素(dox)可以进入药物载体cds/pnvcl@msns的介孔中。当dox-cds/pnvcl@msns注入血液(ph=7.4)时,且肿瘤细胞温度略高于正常组织,pnvcl链经历疏水相变并在msns表面塌陷,可充当介孔内dox的“帽”。同时,亲水性cds可以提供亲水性,从而防止dox-cds/pnvcl@msns相互聚集。当体系的ph发生改变时,具有ph响应性的亚胺键断裂。当dox-cd/pnvcl@msns进入肿瘤环境(ph=5.0)时,具有ph响应性的亚胺键断裂,dox迅速释放。亚胺键的断裂也会导致cd的荧光猝灭和恢复,可用于实时监测药物的释放。因此,本发明的基于温敏聚合物/碳点的介孔硅复合纳米粒子可作为纳米药物载体材料在药物控制释放中应用。
2、本发明中,碳点(cds)具有良好的稳定性、低毒性、优异的生物相容性和易于功能化,在检测生物成像和生物传感器中具有广泛的应用。聚n-乙烯基己内酰胺(pnvcl)是一种良好的温度敏感性聚合物,具有无毒性、生物相容性好等优点,在生物医学领域有着广阔的应用前景。介孔硅纳米粒子(msns)具有低毒性、优异的生物降解性和稳定性使其适合注入人体,其高度有序的孔结构,均匀且可调节的孔尺寸和分布,较高的比表面积和较大的孔体积,也为药物的储存和输送提供了巨大的空间。所以msns被广泛的应用在药物载体领域。
附图说明
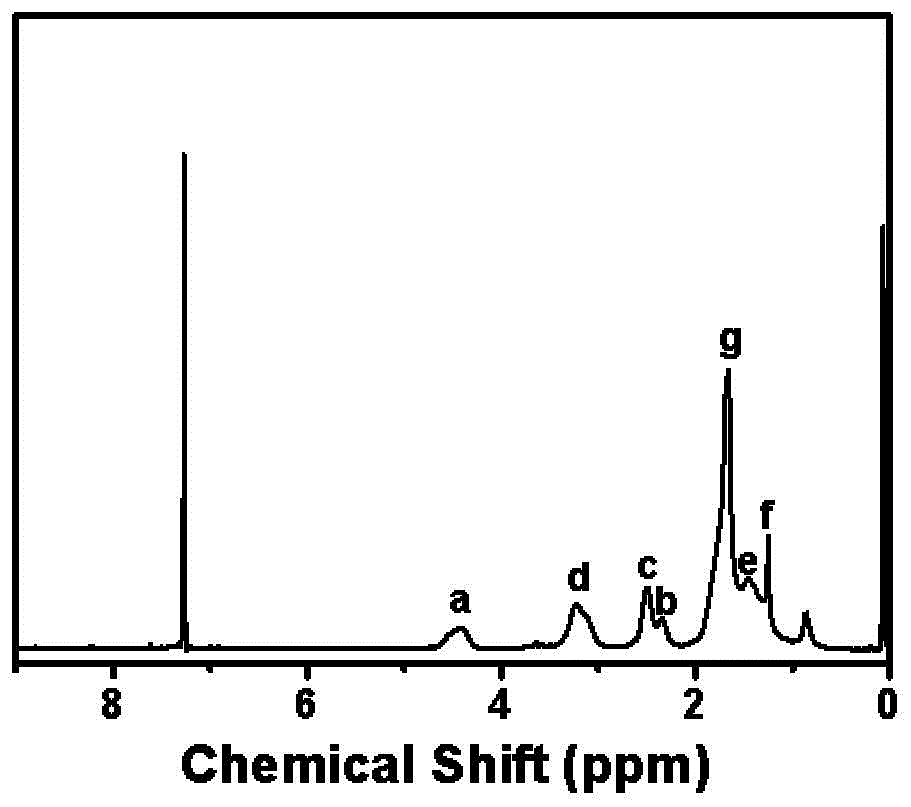
图1是pnvcl-nh2的1hnmr谱图。
图2是pnvcl-nh2的gpc流出曲线。
图3是msns的tem图。
图4是msns的吸附/解吸曲线。
图5是各构筑单元的ftir谱图。
图6是msns-cho的edx光谱图。
图7是各构筑单元的tga曲线。
图8是cds的tem图。
图9是cds的ftir谱图。
图10是cds/pnvcl@msns的tem图。
图11是cds/pnvcl@msns的edx图。
图12是dox-cds/pnvcl@msns释放dox的体外释放曲线(ph=7.4)。
图13是dox-cds/pnvcl@msns释放dox的体外释放曲线(t=37℃)。
图14是cds/pnvcl@msns的发射光谱。
图15是cds/pnvcl@msns在525nm处发射峰的强度。
图16是释放的dox百分比与cds的荧光强度之间的线性曲线。
具体实施方式
为了进一步理解本发明,下面结合实施例对本发明优选实施方案进行描述,但是应当理解,这些描述只是为进一步说明本发明的特征和优点,而不是对本发明权利要求的限制。
实施例1基于温敏聚合物/碳点的介孔硅复合纳米粒子(mcds:mpnvcl@msns=1:2)的制备
(一)端氨基聚n-乙烯基己内酰胺(pnvcl-nh2)的合成
称取5.0g(36mmol)nvcl和0.081g(0.495mmol)aibn置于250ml反应瓶中,用50ml1,4-二氧六环溶解,然后充氮气30min。将0.055g(0.72mmol)hsch2ch2nh2溶解在5ml1,4-二氧六环中,然后加入到上述反应液中,磁力搅拌下68℃反应14h。反应结束后,过滤,滤液旋转蒸发除去1,4-二氧六环,所得固体溶解在20ml二氯甲烷中,然后滴入200ml乙醚中沉淀,重复该操作三次。沉淀过滤、25℃真空干燥24h得到pnvcl-nh2,产率71%,备用。检测分析结果如图1~图2所示。
图1是pnvcl-nh2的1hnmr谱图。图中δ4.40(a)处的吸收峰为pnvcl链段中次甲基(-ch-ch2-)质子的化学位移,δ2.50(c)处的吸收峰为端基中氨基(-nh2)质子的化学位移,δ1.82(g)处的吸收峰为端基中亚甲基(-sch2-ch2-)质子的化学位移,δ2.25(b)处的吸收峰为pnvcl链段中亚甲基(-ch-ch2-)质子的化学位移,δ1.12~1.82(e+g+f)处的吸收峰为七元环中不与n和碳氧双键相邻的质子的化学位移。
图2是pnvcl-nh2的gpc流出曲线。从曲线上可以看出,只有单一峰,没有其它杂质峰。
综合图1和图2的结果,确认得到了端氨基聚n-乙烯基己内酰胺(pnvcl-nh2)。
合成路线如下所示:
(二)醛基化介孔二氧化硅纳米粒子(msns-cho)的制备
称取0.535gctab和1.75ml(2m)氢氧化钠溶液置于500ml反应瓶中,用240ml超纯水溶解,将溶液加热至80℃后加入2.5mlteos,透明溶液突然变成不透明,产生白色沉淀。剧烈搅拌2h后,白色产物用超纯水洗涤数次。加入40ml的nh4no3乙醇溶液(10mg/ml)在70℃下搅拌过夜,反应结束后,经过离心、乙醇洗涤、真空干燥得到所需msns,备用。
称取100mgmsns和150mgaps置于250ml反应瓶中,用50ml无水甲苯溶解。磁力搅拌下70℃反应12h,经过离心、乙醇洗涤、真空干燥得到msns-nh2。
将100mgmsns-nh2和1ml戊二醛置于反应瓶中,用4ml超纯水溶解。磁力搅拌下25℃反应4h,在室温下剧烈搅拌4小时后,经过离心、乙醇洗涤、真空干燥得到msns-cho。检测分析结果如图3~图6所示。
图3是msns的tem、sem和dls图。由图3分析表明,msns具有均匀的近球形结构和良好的分散性,平均直径约为140nm。
图4是msns的吸附/解吸曲线。从图4中可以看出,msns的孔径约为3.5nm,bet表面积大,约为720m2/g。此外,msns显示出典型的介孔材料的iv型等温线。
图5是msns-nh2的ftir谱图。msns-nh2的ftir光谱中的3440cm-1处的峰归属于氨基,表明msns的ftir光谱中没有该峰,表明该反应是成功的。
图6是msns-cho的edx光谱图。由图5和图6可以证实成功制备了msns-cho。
综合图3、图4、图5和图6的结果,确认得到了醛基化介孔二氧化硅纳米粒子(msns-cho)。
(三)聚n-乙烯基己内酰胺嫁接介孔二氧化硅(pnvcl@msns)的制备
称取50mgmsns-cho置于反应瓶中,用20ml超纯水溶解,在磁力搅拌下加入150mgpnvcl-nh2,室温下反应4h,经液氮冷冻、抽真空、通氮气,循环操作三次后,在氮气保护下,110℃下反应24h。反应结束后经过离心、超纯水洗涤、真空干燥得到pnvcl@msns。检测分析结果如图5、图7所示。
图5是pnvcl@msns的ftir谱图。图5中显示典型的二氧化硅骨架振动掩盖了c=n的特征振动。1455cm-1处特征峰的强度减弱,表明发生了醛与氨基的反应,并可能进一步接枝。
图7是pnvcl@msns的tga曲线。pnvcl@msns的重量损失(27.5%)比msns(12.4%)更大,进一步表明嫁接是成功的。
综合图5和图7的结果,确认得到了聚n-乙烯基己内酰胺嫁接介孔二氧化硅(pnvcl@msns)。
(四)碳点(cds)的制备
分别取0.3g柠檬酸和0.5g尿素置于反应瓶中,用10ml超纯水溶解。溶液在700w微波下反应3min,然后用水冷却至室温,得到产物。然后将cds粗产物溶解到10ml超纯水中。通过将装有cds溶液和超纯水的透析袋搅拌过夜,使用透析去除多余的前体和小分子。最后,冷冻干燥得到cds。检测分析结果如图8~图9所示。
图8是cds的tem和dls图。从图中可以看出,碳点的平均直径约为4nm。
图9是cds的ftir谱图。从图中可以看出,碳点表面富含氨基,这可以通过特殊的n-h(3192cm-1,3417cm-1)和c-n(1188cm-1)振动以及c-n-c(1410cm-1)来证明。
综合图8和图9的结果,确认得到了富含氨基的cds。
(五)碳点(cds)和聚n-乙烯基己内酰胺(pnvcl)作为混合壳的介孔二氧化硅纳米粒子的制备
取50mgpnvcl@msns置于反应瓶中,用20ml超纯水溶解。然后在37℃剧烈搅拌下将100mgcds添加到溶液中反应4h。经过离心、超纯水洗涤、冷冻干燥得到cds/pnvcl@msns。检测分析结果如图10、图11所示。
图10是cds/pnvcl@msns的tem图。从图中可以看出,与裸露的msns相比,它具有相似的球形形态和略大的直径分布。由于介孔被直径较小的球形颗粒覆盖,因此很难观察到它们的表面。
图11是cds/pnvcl@msns的edx图。从图中可以看出,cds/pnvcl@msns中的n,o,s含量高于msns-cho,但si的比例降低,表明cds和pnvcl与msns的有效结合。
图7是cds/pnvcl@msns的tga图。从图7中可以看出,cds/pnvcl@msns的重量损失(34.6%)比pnvcl@msns(27.5%)更大,进一步表明产物制备是成功的。
综合图7、图10和图11的结果,确认得到了cds/pnvcl@msns。
实施例2基于温敏聚合物/碳点的介孔硅复合纳米粒子(mcds:mpnvcl@msns=1:1)的制备
步骤(一)~步骤(四)同实施例1。
步骤(五)如下:
取100mgpnvcl@msns置于反应瓶中,用20ml超纯水溶解。然后在37℃剧烈搅拌下将100mgcds添加到溶液中反应4h。经过离心、超纯水洗涤、冷冻干燥得到cds/pnvcl@msns。
实施例3基于温敏聚合物/碳点的介孔硅复合纳米粒子(mcds:mpnvcl@msns=2:1)的制备步骤(一)~步骤(四)同实施例1。
步骤(五)如下:
取100mgpnvcl@msns置于反应瓶中,用20ml超纯水溶解。然后在37℃剧烈搅拌下将50mgcds添加到溶液中反应4h。经过离心、超纯水洗涤、冷冻干燥得到cds/pnvcl@msns。
实施例4性能测试
1、药物装载/释放测试
分别取50mgcds/pnvcl@msns和15mgdox置于反应瓶中,用pbs溶液(ph=7.4)溶解,磁力搅拌下25℃反应72h。然后将溶液在37℃下再培养24h,以密封介孔内的dox。在37℃下离心、超纯水洗涤、冷冻干燥,得到载药颗粒dox-cds/pnvcl@msns。将载药颗粒分散在dmf中,利用紫外可见分光光度计在波长为485nm处测定dox的吸光度,进而绘制释放曲线。利用下式计算载药量和载药率:
式中w1为复合纳米粒子中包载dox的质量(mg),w2为加入的dox的质量(mg),w3为复合纳米粒子的质量(mg)。
在不同的ph值(ph=5.0、6.5和7.4)和温度(25℃,37℃)下进行药物释放实验。将包含4mgdox-cds/pnvcl@msns的4ml溶液放入透析袋(mwco:3kda)中,然后将其浸入装有20mlpbs的试管中,培养32h以上。以预定的时间间隔取出4ml溶液,并补充4ml新鲜pbs。通过紫外可见分光光度计在485nm处测定收集溶液的吸光度值。累积药物释放百分比(er)公式计算如下:
式中er为dox的释放率,ve为补充的pbs溶液体积,v0为缓冲溶液总体积,ci为第i次更换溶液的dox浓度(μg/ml),cn为最后一次更换溶液dox的浓度(μg/ml),mdox为复合纳米粒子中dox的总量。
cds/pnvcl@msns载药能力检测分析结果如图12、图13所示。
图12是不同温度下dox-cds/pnvcl@msns释放dox的体外释放曲线(ph=7.4)。从图中可以看出,在中性条件下25℃时的药物释放速率明显快于37℃时的药物释放速率。pnvcl在25℃下可溶并拉伸,此时介孔保持开放,外部的dox容易进入,并导致内部的dox快速释放;pnvcl在37℃时经历了疏水相变并塌陷在msns的表面,从而阻塞了介孔并阻碍了dox的释放。因此,药物在室温下容易包封,并且可以避免药物在血液和正常组织中的泄漏。
图13是不同ph下dox-cds/pnvcl@msns释放dox的体外释放曲线(t=37℃)。从图中可以看出,药物释放速率随ph值的降低而增大。首先dox是阳离子性药物,易于在酸性环境中溶解;其次,连接msns和cds/pnvcl的亚胺键在酸性条件下破裂,cds和pnvcl脱落,导致介孔打开和药物释放。
2、荧光性检测
cds/pnvcl@msns分散在37℃的乙酸缓冲液(ph=5.0)中。在预定的时间点,将样品离心,并收集上清液以通过荧光分光光度法记录cds的荧光。检测分析结果如图14~图16所示。
图14是cds/pnvcl@msns分散液在乙酸缓冲液(ph=5.0)中不同时间的发射光谱,图15是cds/pnvcl@msns分散液在乙酸缓冲液(ph=5.0)中不同时间的525nm发射峰的强度。从图14、图15中可以看出,cds具有出色的荧光特性。当将cds嫁接到msns上时,cds发生荧光猝灭,而当亚胺键断裂cds和pnvcl从介孔硅表面脱落是,cd的荧光恢复,药物释放出来。因此,cds/pnvcl@msns在酸性环境中表现出极弱的荧光,并且其荧光强度随时间逐渐增加。这种趋势与在乙酸缓冲液中释放药物的趋势相同。
图16是释放的dox百分比与cds的荧光强度之间的线性拟合图(ph=5.0)。图中释放的dox百分比(y)与cd的荧光强度(x)之间的线性拟合结果表明,其线性方程具有良好的相关性:y=96.09x-26.80(r2=0.9939)。通过以实时定量方式观察cds的荧光强度,可以准确监测从dox-cds/pnvcl@msns中释放的dox。
综合所述,从图1是pnvcl-nh2的1hnmr谱图,图2是pnvcl-nh2的gpc流出曲线,图3是msns的tem图,图4是msns的吸附/解吸曲线,图5是各构筑单元的ftir谱图,图6是msns-cho的edx光谱图,图7是各构筑单元的tga曲线,图8是cds的tem图,图9是cds的ftir谱图,图10是cds/pnvcl@msns的tem图,图11是cds/pnvcl@msns的edx图,图12是dox-cds/pnvcl@msns释放dox的体外释放曲线(ph=7.4),图13是dox-cds/pnvcl@msns释放dox的体外释放曲线(t=37℃),图14是cds/pnvcl@msns的发射光谱,图15是cds/pnvcl@msns在525nm处发射峰的强度,图16是释放的dox百分比与cds的荧光强度之间的线性曲线可知,本发明从实施例1~实施例3制备了基于温敏聚合物/碳点的介孔硅复合纳米粒子,其ph敏感性是因为亚胺键是酸敏感键,在ph=5左右的酸性环境中,亚胺键断裂,介孔封堵结构被破坏,使得内部的客体分子被释放出来。其温度敏感性是因为pnvcl的lcst接近人体的生理温度,在其附近发生相分离,塌缩在疏水的内核表面,从而能够达到缓慢释放内部包裹的客体分子的效果。
可以理解的是,以上关于本发明的具体描述,仅用于说明本发明而并非受限于本发明实施例中所描述的技术方案,本领域的普通技术人员应当理解,仍然可以对本发明进行修改或等同替换,以达到相同的技术效果,只要满足使用需要,都在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!
- 介孔碳‑氧化硅负载纳米MoO3与纳米金属颗粒的复合材料的制备方法与制造工艺
- 一种Ag担载介孔Pb3Nb2O8光催化剂及其制备方法和应用与制造工艺
- 一种球形含铝介孔复合材料和负载型催化剂及其制备方法和应用以及环己酮丙三醇缩酮的方法与制造工艺
- 一种球形含铝介孔复合材料和负载型催化剂及其制备方法和应用以及乙酸乙酯的制备方法与制造工艺
- 采用尿醛树脂作有机骨架制备氨基功能化介孔二氧化硅的方法与制造工艺
- 一种基于介孔硅的抗菌包装膜的制备方法及应用与制造工艺
- 一种球形含铝介孔复合材料和负载型催化剂及其制备方法和应用以及乙烯聚合的方法与制造工艺
- 一种具有规整形貌的介孔硅球的制备方法
- 一种快速高效功能化改性介孔材料的方法
- 有序介孔碳/Ni纳米粒子块状电极的制备及电催化应用