一种中药来源的功能性食品桃花精、制备工艺及其质量控制与成分分析方法与流程
本发明属于功能性食品领域,具体涉及一种中药来源的功能性食品桃花精、制备工艺及其质量控制与成分分析方法。
背景技术:
糖尿病(dm)一直是医学领域面临的挑战之一,是威胁人类健康的流行病。大约90%的患者患有2型糖尿病,其特征是高血糖、碳水化合物、脂肪和蛋白质代谢紊乱和胰岛素抵抗。这些代谢紊乱会加速心肌病的发展。大量研究表明,糖尿病及其病理生理后果直接导致心肌功能的改变和异常,常被称为糖尿病性心肌病(dcm)。dcm的高发病率和高死亡率已经成为临床管理的一大挑战,引起了医学专家的广泛关注。临床需要新的药物或治疗手段。天然中草药在预防和治疗dcm方面具有巨大的潜力,且副作用小,因此,越来越受到人们的关注。
本发明提供的复方中药桃花精,主要由桃仁、藏红花、黄精、桑叶四味中药组成,它们都是药食同源的物质,既是中药也是食品。方中桃仁含有多种营养成分及生物活性物质,主要化学成分有复杂的脂肪酸类、苷类、甾醇及其糖苷、黄酮及其糖苷、蛋白质、氨基酸等成分,苷类主要含有苦杏仁苷;藏红花的化学成分比较复杂,其中富含黄色素与红色素,其中主要含有羟基红花黄色素a、6-羟基山萘酚-3,6-双氧-葡萄糖苷、6-羟基山萘酚-3-氧-β-芸香糖-6-氧-β-葡萄糖苷等多种化学活性成分;黄精含5-羟甲基糠醛、薯蓣皂苷等成分,在抗菌、解压抗疲劳、抗衰老和治疗心血管疾病等方面均有较好作用。本发明提供复方中药桃花精及其颗粒的制备工艺及药效学研究,同时采用hplc法对复方中药桃花精中5-羟甲基糠醛、苦杏仁苷、羟基红花黄色素a、6-羟基山萘酚-3,6-双氧-葡萄糖苷、6-羟基山萘酚-3-氧-β-芸香糖-6-氧-β-葡萄糖苷、薯蓣皂苷等成分进行定量。
技术实现要素:
本发明提供一种复方中药桃花精,其特征在于所述中药配方包含如下重量份配比的原料:桃仁1.0-5.0份、藏红花0.1-1.0份、黄精0.5-4.0份、桑叶1.0-6.0份。
本发明的另一实施方案提供一种复方中药桃花精提取物,其特征在于所述复方中药桃花精提取物的制备方法包括如下步骤:
(1)按重量份计,取桃仁1.0-5.0份、黄精0.5-4.0份,加水加热提取1-3次,过滤收集提取液,并将其浓缩至相对密度1.10-1.15后,喷雾或冷冻干燥,得干粉a;
(2)按重量份计,取藏红花0.1-1.0份、桑叶1.0-6.0份粉碎后,加入发酵剂拌均匀后,喷洒适量水,控制温度在30-60℃,发酵48-72小时后,加入体积分数30%-85%乙醇溶液,加热提取1-3次,过滤收集提取液,喷雾或冷冻干燥,得干粉b。
(3)将步骤(1)得到的干粉a与步骤(2)得到的干粉b混匀即得所述复方中药桃花精提取物。
步骤(1)中所述加热优选加热至70℃至回流温度,水的用量优选桃仁与黄精质量之和的8-12倍,每次提取时间优选0.5-2.0h;
步骤(2)中所述发酵剂选自六神曲或酵母粉,优选六神曲,其用量优选为藏红花与桑叶质量之和的2%-15%,更优选为5%-8%,水的用量以能充分浸润物料(藏红花、桑叶等)为宜,本领域的技术人员可以根据物料(藏红花、桑叶等)的性质进行合理选择;乙醇溶液的用量优选为藏红花与桑叶质量之和的3-8倍,所述加热优选加热至60℃至回流温度,每次提取时间优选0.5-2.0h。
本发明的另一实施方案提供上述复方中药桃花精提取物的hplc指纹图谱,其特征在于当hplc色谱条件如下时,所述复方中药桃花精提取物的hplc指纹图谱基本与图1或图2一致;
hplc色谱条件如下:
色谱柱为intersilc18,规格:250mm×4.6mm,5μm;
流动相:乙腈为a相,0.085wt%的磷酸水溶液为b相;
梯度洗脱:0~60min,b相体积百分比为95%→85%;60~70min,b相体积百分比为85%→82%,70~115min,b相体积百分比为82%→100%,115~120min,b相体积百分比为100%;流速:1.0ml·min-1;柱温:30℃;检测波长:254nm;进样量10μl。
本发明的另一实施方案提供上述复方中药桃花精提取物的hplc指纹图谱,其特征在于所述复方中药桃花精提取物的hplc指纹图谱基本与图1一致,具有42个特征指纹色谱峰,其中峰8为5-羟甲基糠醛,峰20为苦杏仁苷,峰23为羟基红花黄色素a,峰27为6-羟基山萘酚-3,6-双氧-葡萄糖苷,峰28为6-羟基山萘酚-3-氧-β-芸香糖-6-氧-β-葡萄糖苷,峰42为薯蓣皂苷。
本发明的另一实施方案提供上述复方中药桃花精提取物的hplc指纹图谱在复方中药桃花精质量控制、成分分析中的应用。
本发明的另一实施方案提供一种组合物,其特征在于所述组合物以上述复方中药桃花精提取物作为有效成分。该组合物还可包括食品或药学上可接受的辅料。该组合物的剂型优选固体制剂、液体制剂、半固体制剂。进一步优选片剂、胶囊、粉剂、口服液或颗粒剂。所述组合物用于食品或药品领域。
本发明的另一实施方案提供一种桃花精颗粒,其特征在于所述桃花精颗粒的制备方法包括如下步骤:
取上述复方中药桃花精提取物,加入食品或药品可接受的辅料充分混匀、制粒,过10目筛后,于40-60℃下干燥,整粒,分装即得所述桃花精颗粒。所述食品或药品可接受的辅料优选果糖、益生元、果粉等,包括但不限于赤藓糖醇、低聚异麦芽糖和阿斯巴甜等辅料。
本发明的另一实施方案提供上述复方中药桃花精、复方中药桃花精提取物、桃花精颗粒在制备预防和/或治疗糖尿病并发症的功能性食品或药品中的应用。
本发明的另一实施方案提供上述复方中药桃花精、复方中药桃花精提取物、桃花精颗粒在制备预防和/或治疗糖尿病心肌病的功能性食品或药品中的应用。
本发明的另一实施方案提供上述复方中药桃花精、复方中药桃花精提取物、桃花精颗粒在制备减少ros的产生、抑制nlrp3激活的功能性食品或药品中的应用。
本发明所述的水优选蒸馏水、纯净水、重蒸水或去离子水。本发明所述功能性食品的种类包括但不限于饮料、糖果、口服液、片剂、胶囊。
附图说明
图1是复方中药桃花精提取物的hplc指纹图谱。
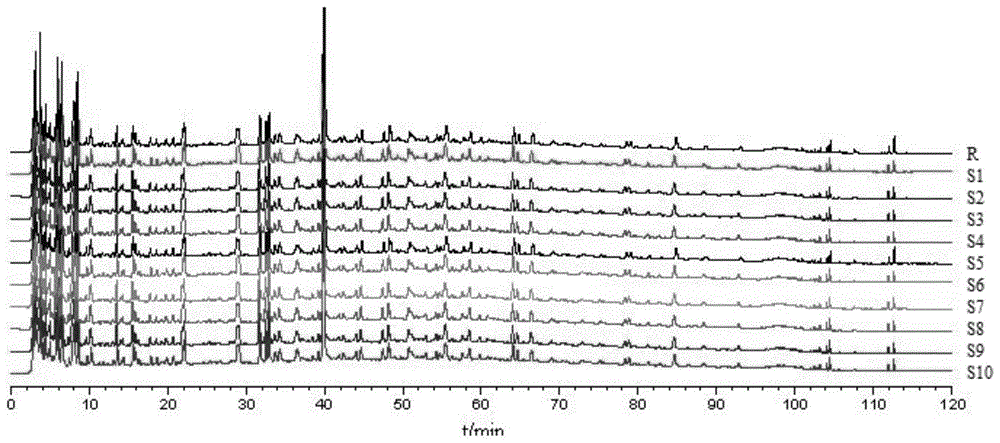
图2是10批复方中药桃花精提取物的hplc比较图谱。
图3是混合对照品的hplc图谱,(峰1为5-羟甲基糠醛;峰2为苦杏仁苷;峰3为羟基红花黄色素a;峰4为6-羟基山萘酚-3,6-双氧-葡萄糖苷;峰5为6-羟基山萘酚-3-氧-β-芸香糖-6-氧-β-葡萄糖苷;峰6为薯蓣皂苷)
图4是thj对dcm小鼠心肌肥厚及功能障碍的影响图;a.典型m型超声心动图;b.左室射血分数(lvef);c.左室缩短分数(lvfs);d.左室收缩期末容积(lvesv);e.左室舒张末期容积(lvedv);值表示为平均值sd(n=6-8),与对照组比较,*p<0.05,**p<0.01。
图5是thj对dcm小鼠心肌纤维化及病理结构紊乱的影响图,a.马松组织间质和血管周围三色染色的代表性图像,b.心脏组织纵向和横向he染色的代表性图像,c.左心室心脏组织的典型电子显微图像。
图6是thj对dcm小鼠氧化应激的影响图,a.具有代表性的dhe染色图像及dhe强度,b.心肌组织中mda水平,c.心肌组织sod活性,d.gsh-px在心肌组织中的活性,值以sd均值表示,**p<0.01vsdcm组。
图7是thj对炎症因子及nlrp3相关mrna水平的影响图,a.il-6水平,b.tnf-α水平,c.il-1β水平,相对mrna表达水平的半胱天冬酶1(d),nlrp3(e),txnip(f),asc(g),il-1β(h)的心肌组织,n=6-8。**p<0.01vsdcm组。
图8是thj对nlrp3相关蛋白表达水平的影响图,左侧图是nlrp3、txnip、半胱天冬酶1p20、il-1βp17、asc和β-actin表达,右侧直方图是其表达水平的定量值,经统计学处理显示,##p<0.01vscon组;**p<0.01vsdcm组。
图9是thj对sirt1通路的影响图,a.nad+/nadh比率,b.westernbloting检测sirt1、ac-sod2、ac-foxo3a蛋白表达水平,c.小鼠用sirt1沉默质粒处理12周,dcmh和thj干预后sirt1蛋白表达水平,d.转染sisirt1后的dhe强度水平,e.转染sisirt1后mda水平,f.转染sisirt1后的sod水平,数值显示为三个不同实验的平均相对标准偏差,##p<0.01vscon组;**p<0.01vsdcm组,&&p<0.01vsscrb组。
图10是抑制sirt1可抵消thj的抗炎活性图,a.小鼠用sirt1沉默质粒处理12周,诱导dcm再使用thj干预,检测nlrp3、半胱天冬酶1p20和il-1βp17的蛋白表达水平,b.dcm小鼠的tnf-α水平,c.dcm小鼠的il-6水平,数值以“平均数±相对标准偏差”显示,##p<0.01vscon组;**p<0.01vsdcm组;&&p<0.01vsscrb组。
具体实施方式
为了便于对本发明的进一步理解,下面提供的实施例对其做了更详细的说明。但是这些实施例仅供更好地理解发明而并非用来限定本发明的范围或实施原则,本发明的实施方式不限于以下内容。
实施例1
配方:桃仁1.0份、黄精0.5份、藏红花0.1份、桑叶1.0份
(1)按配方量,取桃仁100g、黄精50g,加去离子水(1.2l)加热至回流温度提取2次(每次提取0.5h),过滤收集提取液,并将其浓缩至相对密度1.10-1.15后,喷雾干燥,得干粉a;
(2)按配方量,取藏红花10g、桑叶100g粉碎后,加入2.2g六神曲拌均匀后,喷洒适量水(充分浸润),控制温度在40-45℃,发酵60小时后,加入体积分数30%乙醇溶液(880g),加热至回流温度提取2次(每次提取0.5h),过滤收集提取液,喷雾干燥,得干粉b;
(3)将步骤(1)得到的干粉a与步骤(2)得到的干粉b混匀即得所述复方中药桃花精提取物(简称thj)。
实施例2
配方:桃仁5.0份、藏红花1.0份、黄精4.0份、桑叶6.0份
(1)按配方量,取桃仁500g、黄精400g,加去离子水(10.8l)加热至70℃提取3次(每次提取2.0h),过滤收集提取液,并将其浓缩至相对密度1.10-1.15后,喷雾干燥,得干粉a;
(2)按配方量,取藏红花100g、桑叶600g粉碎后,加入105g六神曲拌均匀后,喷洒适量水(充分浸润),控制温度在55-60℃,发酵48小时后,加入体积分数85%乙醇溶液(2100g),加热至70℃提取3次(每次提取2.0h),过滤收集提取液,喷雾干燥,得干粉b;
(3)将步骤(1)得到的干粉a与步骤(2)得到的干粉b混匀即得所述复方中药桃花精提取物。
实施例3
取适量实施例1制备的thj,加入食品药品可接受的辅料(如果糖、赤藓糖醇、低聚异麦芽糖和阿斯巴甜中的一种或几种)充分混匀、制粒,过10目筛后,于60℃以下干燥,整粒,分装即得所述桃花精颗粒。
实施例4
1仪器与试药
岛津高效液相色谱仪(prominenuflc,lc/labsoluion色谱工作站),日本岛津公司;德国sartorius电子天平,型号cpa225d,德国塞多利斯公司;超声波发生器,型号kq-5200de数控,昆山超声仪器有限公司。乙腈、甲醇,色谱级,美国honeywell公司;超纯水,由美国millipore纯水仪制,美国millipore公司;5-羟甲基糠醛(批号111626-201610,含量为99.2%)、苦杏仁苷(批号110820-201607,含量为90.7%)、羟基红花黄色素a(批号111637-201609,含量为91.9%)、薯蓣皂苷(批号111707-201703,含量为96.1%)等对照品,均购自中国药品生物制品检定研究院;6-羟基山萘酚-3,6-双氧-葡萄糖苷(批号201610,含量为98.0%)、6-羟基山萘酚-3-氧-β-芸香糖-6-氧-β-葡萄糖苷(批号201611,含量为98.0%)等对照品,购自上海盛中医药化工有限公司;thj批号20170516(s1),20170517(s2),20170518(s3),20170519(s4),20170520(s5),20170521(s6),20170522(s7),20170523(s8),20170524(s9),20170525(s10),由第四军医大学药物研究所研制。
2指纹图谱测定方法与结果
2.1色谱条件色谱柱为intersilc18(250mm×4.6mm,5μm);流动相:乙腈(a)-0.085%磷酸水溶液溶液(b),梯度洗脱,0~60min,b95%→85%;60~70min,b85%→82%,70~115min,b82%→100%,115~120min,b100%。记录时间为120min。流速:1.0ml·min-1;柱温:30℃;检测波长:254nm;进样量10μl。
2.2参比物及供试品溶液的制备
2.2.1参比物溶液的制备称取羟基红花黄色素a对照品10.88mg,置于10ml量瓶中加甲醇至刻度,摇匀,即得浓度为1.0mg·ml-1的参比物溶液。
2.2.2供试品溶液的制备取本品3g,研细,混匀,称取1g,精密称定,置于10ml量瓶中,加水适量,超声处理(功率250kw,频率40khz)30min,放凉,加水至刻度,摇匀,静置,取上清液滤过,取续滤液,即得。
2.3方法学考察
2.3.1精密度试验取供试品溶液(批号20170516),连续进样6次,分别对共有峰的相对保留时间和相对峰面积进行分析考察。结果各共有峰的相对保留时间与相对峰面积rsd值分别小于2.0%和3.0%,表明该方法精密度良好。
2.3.2稳定性试验取供试品溶液(批号20170516),分别于各时间点即0,2,4,8,12,24h进样,考察共有峰的相对保留时间和相对峰面积。结果各共有峰相对保留时间与相对峰面积rsd值分别小于2.0%、3.0%,表明供试品溶液在24h内具有良好的稳定性。
2.3.3重复性试验取6份供试品(批号20170516),按供试品溶液的制备与色谱条件进行分析,分别对共有峰的相对保留时间和相对峰面积进行分析考察。结果各共有峰相对保留时间与相对峰面积rsd值分别小于2.0%和3.0%,表明该方法重复性良好。
2.3.4指纹图谱建立及相似度分析取10批thj样品,分别按供试品溶液的制备与色谱条件进行分析,进样量20μl,记录指纹图谱(图1),峰23为羟基红花黄色素a即参比物,建立指纹图谱。10批样品共有色谱峰的相对保留时间与相对峰面积的rsd值均分别小于2.0%、3.0%,与指纹图谱研究技术的要求相符(图1、2)。运用中药色谱指纹图谱相似度评价系统(2004a)对10批thj的指纹图谱进行相似度分析,结果,对选定42个共有色谱峰进行谱峰匹配,得出了样品指纹图谱的共有模式;整体相似度为0.966~0.985;表明这10批thj的化学成分一致性较好。
3含量测定方法与结果
3.1色谱条件余同2.1项。
3.2对照品溶液的配制分别精密称取5-羟甲基糠醛10.08mg、羟基红花黄色素a16.32mg、6-羟基山萘酚-3,6-双氧-葡萄糖苷5.10mg、6-羟基山萘酚-3-氧-β-芸香糖-6-氧-β-葡萄糖苷4.59mg、薯蓣皂苷10.41mg置5ml量瓶中,加甲醇至刻度,摇匀,得混合对照品溶液为a溶液;另取苦杏仁苷16.54mg置2ml量瓶中,加a溶液至刻度,摇匀,即得混合对照品溶液为b溶液,5-羟甲基糠醛、苦杏仁苷、羟基红花黄色素a、6-羟基山萘酚-3,6-双氧-葡萄糖苷、6-羟基山萘酚-3-氧-β-芸香糖-6-氧-β-葡萄糖苷、薯蓣皂苷对照品浓度分别为2.000、7.501、3.000、1.000、0.900、2.001mg·ml-1作为储备液。
3.3供试品溶液的制备同2.2.2项(图1)。
3.4线性关系分别精密量取储备液0.01,0.05,0.10,0.25,0.50和1.00ml置于各个1ml量瓶中并加甲醇稀释至刻度,用0.22μm微孔滤膜滤过,进样。以各对照品的质量浓度(x,μg·ml-1)为横坐标,峰面积值(y)为纵坐标,通过计算,得线性方程,结果见表1和图3,表明各对照品在相应浓度范围内线性关系良好。
表1对照品的线性方程及其浓度范围
3.5精密度试验精密吸取供试品溶液(批号20170516),重复进样5次,测得5-羟甲基糠醛、苦杏仁苷、羟基红花黄色素a、6-羟基山萘酚-3,6-双氧-葡萄糖苷、6-羟基山萘酚-3-氧-β-芸香糖-6-氧-β-葡萄糖苷、薯蓣皂苷的相对标准差(rsd)分别为1.00%,0.91%,0.97%,0.94%,0.95%,0.87%%,表明该方法精密度良好。
3.6重复性试验精密称取6份样品(批号20170516),分别按2.2.2项下方法制备供试品溶液,按3.3项下色谱条件进样测定。结果,5-羟甲基糠醛、苦杏仁苷、羟基红花黄色素a、6-羟基山萘酚-3,6-双氧-葡萄糖苷、6-羟基山萘酚-3-氧-β-芸香糖-6-氧-β-葡萄糖苷、薯蓣皂苷平均含量分别为0.23401、28.88276、10.50596、0.56850、0.59498、3.33605mg·g-1,rsd值分别为1.02%,1.22%,1.06%,1.16%,1.15%,0.98%,表明该方法具有良好重复性。
3.7稳定性试验精密吸取供试品溶液(批号20170906),分别在第0,2,4,8,12和24h进样。结果,5-羟甲基糠醛、苦杏仁苷、羟基红花黄色素a、6-羟基山萘酚-3,6-双氧-葡萄糖苷、6-羟基山萘酚-3-氧-β-芸香糖-6-氧-β-葡萄糖苷、薯蓣皂苷的峰面积的rsd值分别为0.82%,0.92%,0.88%,0.87%,0.96%,表明该溶液在24h内稳定性。
3.8加样回收率试验精密量取桃花精颗粒(批号20170516,其中5-羟甲基糠醛、苦杏仁苷、羟基红花黄色素a、6-羟基山萘酚-3,6-双氧-葡萄糖苷、6-羟基山萘酚-3-氧-β-芸香糖-6-氧-β-葡萄糖苷、薯蓣皂苷分别为0.23401、28.88276、10.50596、0.56850、0.59498、3.33605mg·g-1)1.0g,按表2分别添加对照品(苦杏仁苷、羟基红花黄色素a)和混合对照品溶液(精密称取5-羟甲基糠醛、6-羟基山萘酚-3,6-双氧-葡萄糖苷、6-羟基山萘酚-3-氧-β-芸香糖-6-氧-β-葡萄糖苷、薯蓣皂苷适量,制成每1ml甲醇中含量分别为0.2300,0.5700,0.6000,3.3000mg)0.8.00ml或1.00ml或1.20ml,再加水至刻度,按照3.3项下方法制备供试品溶液,共制备6份样品,按照3.1项下色谱条件进样测定。结果见表2,表明该方法回收率良好。
表2加样回收率测定结果
3.9含量测定精密量取10批样品,分别按照3.3项下方法制备供试品,按照3.1项下色谱条件测定。各批样品中5-羟甲基糠醛、苦杏仁苷、羟基红花黄色素a、6-羟基山萘酚-3,6-双氧-葡萄糖苷、6-羟基山萘酚-3-氧-β-芸香糖-6-氧-β-葡萄糖苷、薯蓣皂苷的平均含量(mg·g-1)、rsd见表3。
表3thj中7个成分含量测定结果(n=3)
4讨论
采用pda检测器全波长对thj样品进行测定,依据三维色谱图及对应波长下峰的信息量,结果254nm时信息量较多,同时5-羟甲基糠醛(最大吸收279nm)、苦杏仁苷(最大吸收210nm)、羟基红花黄色素a(最大吸收403nm)、6-羟基山萘酚-3,6-双氧-葡萄糖苷(最大吸收337nm)、6-羟基山萘酚-3-氧-β-芸香糖-6-氧-β-葡萄糖苷(最大吸收337nm)、薯蓣皂苷(最大吸收205nm)等6个化合物与相邻各峰有良好的分离度,故将其作为hplc指纹图谱的定性波长与6个化合物的定量波长。
由于中药复方中成分复杂,等度洗脱难以充分洗脱,所以采用梯度洗脱的方法。对不同流动相系统乙腈-磷酸水溶液、甲醇-水、乙腈-醋酸水溶液、乙腈-水进行比较,结果,乙腈-0.085%磷酸水溶液流动相理想。
本制剂主要成分为水溶性成分,所以使用水作为溶剂,采用不同时间(10、15、20、30、40、50、60min)泡、超声处理方法或加热回流,结果,加水超声30min较理想。对不同柱温与流速进行比较,柱温超过或低于30℃,但大部分色谱峰分离度小或不能分开;流速高于或低于1.0ml·min-1,大部分色谱峰分离度差;色谱记录时间,在120min之后,无色谱峰出现。因此,选择便于控制的柱温30℃,流速1.0ml·min-1和记录时间为120min。
总之,通过上述研究,表明笔者建立的thj的hplc指纹图谱方法与含量测定方法,具有良好的分析评价能力,具有准确简便、稳定可靠等优势。因此,该方法可作为本制剂质量的有效评价方法。
实施例5
1.材料与方法
1.1动物
雄性c57bl/6小鼠,体重20-25g,8周龄,由空军军医大学实验动物中心提供。
1.2试药
thj,西安荷默奇医药科技有限公司按本发明实施例方法生产;链脲佐菌素(stz)购自sigma公司。
1.3饲料:普通饲料、高脂高糖饲料,购自空军军医大学。
1.4仪器:血糖仪(强生稳豪倍易型血糖仪)、血糖试纸(强生稳豪型血糖试纸)。
2.方法
2.1糖尿病小鼠模型的制备与分组
将雄性c57bl/6小鼠,体重20-25g,8周龄,适应性饲养2周后,给予高脂高糖饲料4周,连续三天腹腔注射链脲佐菌素(stz,60mg/kg,溶解于柠檬酸缓冲液,ph=4.5),空白组注射相同剂量的柠檬酸缓冲液。于注射后7天、14天用血糖仪测量空腹血糖(fbg),fbg>11.1mm为造模成功。将糖尿病小鼠随机分为模型组(dm;n=15),thj低剂量(thj-l125mg/kg/d;n=15),thj中剂量(thj-m,250mg/kg/d;n=15),thj高剂量(thj-h,500mg/kg/d;n=15)及空白对照组(,等容量生理盐水,n=15)。
在保持22℃室温下,将动物置于12/12h光/暗循环下。所有动物都可以自由饮水,糖尿病小鼠用高脂高糖饲料喂养,而正常组组小鼠用正常饮食喂养。各组分别灌胃给药12周,空白组和模型组分别灌胃等体积蒸馏水。
2.2体重、血糖
每7d称量体重,每14d测量空腹血糖。
2.3超声心动图
小鼠心脏功能通过经胸超声心动图进行评估,超声系统采用visualsonicsvevo770(加拿大安大略省多伦多市)。通过调节氧气中1.0%异氟醚的吸入量,将动物麻醉,使心率保持在每分钟400-500次,并在整个麻醉过程中放置在一个温垫上。采用30mhz线性传感器测量左室舒张末期直径(lvedd)、左室收缩末期直径(lvesd)、左室舒张末期内径(lvidd)和收缩末期内径(lvids)、舒张末期室间隔厚度(ivsd)和收缩末期厚度(ivss)和舒张末期左室后壁厚度(lvpwd)和乳头肌层面的收缩(lvpws)。采用计算机算法计算左室射血分数(lvef)、左室缩短分数(lvfs)、左室收缩末期容积(lvesv)和左室舒张末期容积(lvedv)。用计算机算法计算左心室射血分数(lvef)、左心室分数缩短(lvfs)、左室收缩末期容积(lvesv)和左室舒张末期容积(lvedv)。所有的测量都是基于6个连续的心脏周期。
2.4组织病理切片
将小鼠心脏固定于4%多聚甲醛溶液中保存,然后用蜡块包埋,5μm切片,苏木精-伊红(he)染色观察心肌组织形态,masson三色观察细胞外胶原沉积。
2.5生化检测
超声细胞粉碎机(宁波新芝生物jy92-iin);台式高速冷冻离心机(healforceneofuge15r);纯水仪(青岛富勒姆科技fbz2001-up-p);涡旋混合器(servicebiomx-f);酶标检测仪(biotekepoch);全自动生化分析仪(深圳雷杜生命科技chemray240)。
2.6统计学处理
使用spss22.0分析数据。结果表示为平均值±标准差。t检验用于评估多重因素之间的差异,在p<0.05时考虑统计学意义。
3结果
3.1thj降低糖尿病(dm)小鼠全身代谢异常如表4所示,模型组小
表4thj预防了dm小鼠的全身代谢异常(n=8)
*p<0.05,**p<0.01vs.dm组
鼠经高脂饲料(hfd)和链脲佐菌素(stz)干预后,葡萄糖和脂质(tg、tc)均显著增加(p<0.05),血液中胰岛素水平显著降低(p<0.05),胰岛素敏感性也受损,表现出明显系统性dm代谢异常。thj治疗后,血糖和血脂水平下降,胰岛素敏感性呈剂量依赖性提高。以60mg/kg剂量为最佳。提示thj能改善hfd和stz对dm小鼠的全身代谢异常。
3.2thj改善dm诱导的心肌功能障碍小动物超声心动图记录了hfd和stz干预后小鼠左室缩短分数(lvfs)和左室射血分数(lvef)。如图4a-c所示,与对照组相比,糖尿病心肌病(dcm)组lvef和lvfs明显降低,而thj处理显著提高了lvef和lvfs;此外,thj处理降低了dcm小鼠左室舒张末期体积(lvedv,图4d)和左室收缩末期体积(lvesv,图4e),hfd+stz处理使其增加。提示thj治疗能明显改善dcm小鼠心肌功能障碍。
3.3thj改善dm性dcm小鼠心肌纤维化及病理结构紊乱心肌功能障碍部分是由心肌纤维化引起的,后者可引起心脏的病理结构紊乱和重构。马松染色(deh)如图5a所示,与对照组相比,dcm小鼠心脏组织间质及血管周围胶原明显增多。与dcm组相比,间质区和血管周围纤维化和胶原含量均下降。he染色结果显示,dcm小鼠心脏纵、横切面病变严重,心肌细胞及肥厚心肌明显紊乱。thj组的病理结构改变明显减轻(图5b)。用透射电镜观察显微组织的变化:对照组小鼠可见典型的对称肌纤维,纤维旁有组织良好的肌节和线粒体(图5c),而dcm心脏组织左室超微结构损伤严重,包括肌纤维破裂和不规则。thj治疗组上述变化明显改善,高剂量组心脏超微结构与正常组相似。
3.3thj改善dm性dcm小鼠心脏组织ros水平dhe染色检测ros水平,图6a和b可见,dcm组的dhe荧光强度明显高于con组。thj治疗12周后,心脏内ros的生成明显减少。同时,dcm组mda水平明显升高,thj组mda水平明显降低。dcm组sod、gsh-px酶活性明显降低(图6c、d),thj对sod、gsh-px酶活性的影响呈剂量依赖性。结果表明,thj具有明显抑制dcm小鼠的氧化应激作用。
3.4thj抑制dcm小鼠炎症反应和nlrp3炎症小体的活化图7结果显示,tnf-ail-6、il-1β在dcm组显著增加。thj-l、thj-m、thj-h治疗后,剂量依赖性的显著降低tnf-a、il-6、il-1β水平。dcm组动物左心室组织中的mrna水平、nlrp3、caspase-1、xnip、asc和il-1β水平明显高于con组(图7d-h);nlrp3的蛋白质、pro-caspase-1、caspase-1、txnip、asc和il-1β含量也高于con组(图8)。thj治疗后nlrp3mrna蛋白水平、pro-caspase-1、激活caspase-1、txnip、asc、激活il-1β都显著降低。
3.5thj通过激活sirt1抑制氧化应激我们检测了sirt1信号通路。dcm组的nad+/nadh比值低于con组(图9a);thj处理后显著升高nad+/nadh比值并呈剂量依赖性。检测sirt1及其两个主要下游蛋白foxo3a和sod2;westernbloting结果如图9b所示;与con组相比,dcm组sirt1表达水平明显降低,ac-sod2、ac-foxo3a表达水平均升高。有趣的是,与dcm组相比,thj处理显著逆转了这些变化。为了评估sirt1在thj治疗过程中的作用,通过转染使sirt1沉默。结果如图9c所示,12周的沉默处理降低了sirt1的蛋白表达水平;与scrb组相比,sisirt1组的ros和mda水平较高,sod水平较低,说明thj对氧化应激的抑制作用被sisirt1所抵消。
3.6抑制sirt1可抵消thj的抗炎活性如图10a所示,与scrb组相比,sisirt1解除了thj对nlrp3炎性小体激活的抑制作用;同时,证实sisirt1干预解除了dcm小鼠抑制tnf-α和il-6的效应(图10b和c)。
讨论
在本研究中,我们发现hfd和stz治疗可使血糖、tg和tc水平升高,并诱导胰岛素抵抗。thj治疗12周后,血糖、血脂水平均呈剂量依赖性下降,胰岛素抵抗明显改善,提示thj改善了dm小鼠的全身代谢紊乱。此外,dm小鼠表现出收缩和舒张功能障碍、纤维化、病理损伤和心肌超微结构紊乱等dcm特征。thj治疗改善了心功能障碍,减少了肌纤维、线粒体的病理改变,提示thj保护了dcm小鼠心肌结构的改变。
糖尿病的主要特征是慢性高血糖和高脂血症,这导致了心功能障碍的发生。葡萄糖和脂质代谢的增加增加了线粒体中活性氧的产生,破坏了诱导氧化应激的抗氧化系统。ros引起蛋白质、dna或rna损伤,诱导心肌细胞凋亡,导致心肌收缩力下降,最终导致心肌细胞纤维化。与既往研究一致,dhe染色检测到dcm心脏组织中ros水平升高,抗氧化蛋白(gsh-px、sod)下降,mda水平升高。但thj处理后,小鼠体内ros和mda水平降低,抗氧化蛋白水平呈剂量依赖性升高,提示thj对dcm小鼠心脏的氧化应激具有保护作用。
在糖尿病状态下,慢性高血糖可诱导促炎细胞因子的分泌,引起持续性炎症反应,加重或加重心肌损伤。在这项研究中,促炎细胞因子tnf-a,il-6,在dcm小鼠il-1β水平增加。许多作品表明nlrp3inflammasome调节il-1β激活在糖尿病及其并发症(尺码)。高水平的葡萄糖激活nlrp3炎性小体,同时伴有txnip激活,txnip是清除活性氧的蛋白硫氧还蛋白的抑制剂。nlrp3炎性小体包含nlrp3、caspase募集域(asc)和caspase-1。一旦激活一些刺激,nlrp3结合适配器asc,催化pro-caspase-1格式化一个活跃的caspase-1p10/20四聚物过程pro-il-1β进入成熟形成il-1β。研究的影响在nlrp3thjinflammasome,nlrp3,txnip,caspase-1il-1β被pcr和西方大量发现。信使rna和蛋白质水平的nlrp3、txnipcaspase-1p10及il-1βp17被发现在dcm组增加,表明nlrp3inflammasome在dcm激活。thj治疗组,信使rna和蛋白质水平的nlrp3,txnipcaspase-1p10,il-1βp17显著下降,显示剂量依赖的方式。提示thj可抑制dm诱导的nlrp3炎症小体活化。
抗氧化蛋白和nlrp3受sirt1调控,为进一步了解thj、sirt1的抗氧化、抗炎机制。sirt1是一种依赖烟酰胺腺嘌呤二核苷酸(nad+-)的组蛋白去乙酰化酶,在调节应激反应如氧化应激、炎症、凋亡等方面发挥重要作用。sirt1诱导foxo3a去乙酰化,从而增加foxo3a调节抗氧化蛋白(sod和cat)和dna修复的能力。sirt1可直接诱导sod2去乙酰化,提高sod2的抗氧化能力。因此,本研究通过检测sirt1蛋白的表达水平及其下游(ac-foxo3a和ac-sod2)来评价thj对sirt1通路的调节作用。有趣的是,thj处理增加了sirt1、ac-foxo3a和ac-sod2的蛋白表达水平,增加了dcm小鼠的nad+/nadh,而nad+/nadh下降。既往研究表明,sirt1对血管内皮细胞中nlrp3的激活具有负调控作用。鉴于sirt1在dcm中的关键作用,我们在体内使用sisirt1来探讨thj的保护作用是否依赖于sirt1。结果显示,sirt1表达水平被sisirt1阻断,同时伴有nlrp3炎症激活和氧化应激的增强。这些结果表明,thj抑制氧化应激和nlrp3炎症反应的机制是sirt1依赖性的。
结论:thj可以保护心肌组织免受dm的伤害。thj的有益作用可能依赖于减少ros的产生和抑制nlrp3的激活,后者抑制促炎细胞因子的过度释放,进一步的研究表明这些保护作用与sirt1通路相关。本研究丰富了thj在dcm中的抗氧化应激、抗炎作用及机制,进一步促进了thj的临床应用。
- 还没有人留言评论。精彩留言会获得点赞!