一种替比培南酯细粒剂组合物及其制备方法与流程
1.本发明属于药物技术领域,具体涉及一种替比培南酯制剂及其制备方法。
背景技术:
2.替比培南酯为白色结晶性粉末、无臭。本品在甲醇及乙腈中易溶,在乙醇中溶解,在乙醚中微溶,在水中极微溶解。有旋光性,比旋度为+10.3
°
~+10.7
°
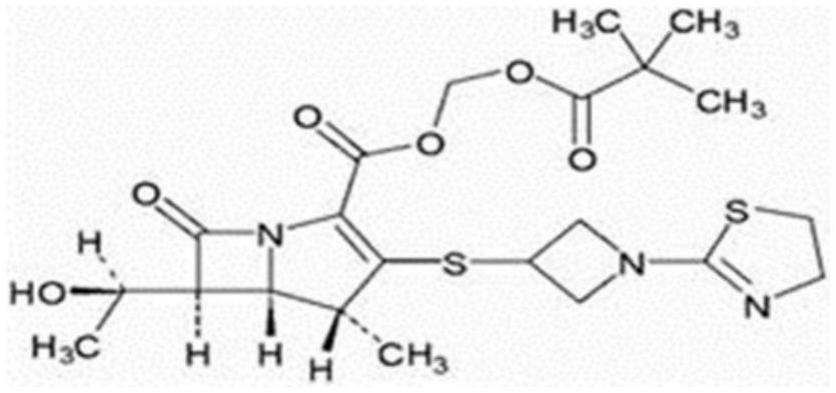
。替比培南酯,其化学名称为:(+)-(4r,5s,6s)-6-[(1r)-1-羟乙基]-4-甲基-7-氧代-3-{[1-(2-噻唑啉-2-基)-3-氮杂环丁烷基]硫}-1-氮杂双环[3.2.0]庚-2-烯-2-羧酸叔戊酰氧甲酯,分子式:c
22
h
31
n3o6s2,分子量为497.63,其化学结构式如下:
[0003][0004]
替比培南酯最初由惠氏制药的leaderle在日本进行研发,替比培南酯细粒剂由日本明治公司研制,于2009年4月获得日本厚生省批准,并于2009年8月在日本首次上市,商品名(
オラペネ
)。
[0005]
替比培南酯是替比培南的前体药物,口服后被酯酶水解释放出母体药物替比培南,与细菌青霉素结合蛋白(pbp)结合,抑制细菌细胞壁的合成,是目前唯一一个可以口服的碳青霉烯类抗生素。用于儿科病人耳鼻喉和上呼吸道感染的治疗。它是第一个用于肺炎链球菌抗药株感染的治疗,包括持续性中耳炎和细菌性肺炎的培南类药物。小儿肺炎是威胁我国儿童健康的严重疾病,无论是发病率还是病死率均居首位。替比培南酯作为儿科专用的抗肺炎、中耳炎、副鼻腔炎药物,具有较好的市场前景。
[0006]
扬州市星斗药业有限公司已申请专利“一种含有替比培南的颗粒及其制备方法”(申请号:201210374642.9),公开了一种含替比培南的颗粒及其制备方法,该颗粒以羟丙基纤维素为粘合剂,以填充剂和替比培南药物制粒,所用的填充剂的量为40%~80%(w/w),替比培南的量为5%~20%(w/w)将得到的颗粒过筛,用乙基纤维素、胃溶型丙烯酸树脂和羟丙甲纤维素为包衣材料分别包衣,乙基纤维素、胃溶型丙烯酸树脂和羟丙甲纤维素用量为4%~30%(w/v),过筛后得到含替比培南颗粒。
[0007]
南京卡文迪许生物工程技术有限公司和珠海亿邦制药股份有限公司已申请专利“替比培南酯口服固体制剂及其制备方法”(申请号:201310044254.9),公开了一种替比培南酯口服固体制剂及其制备方法,本发明的口服固体制剂,是由颗粒、隔离包衣层、掩味包衣层和着色娇味包衣层组成,所述的颗粒是由替比培南酯、微晶纤维素以及粘合剂制成。
[0008]
北京济美堂医药研究有限公司已申请专利“一种替比培南酯颗粒剂及其制备方法”(申请号:201310233950.4),该专利涉及一种替比培南酯颗粒剂及其制备方法。其颗粒剂是将替比培南酯、微晶纤维素、乳糖、羧甲基淀粉钠,混合均匀后用加水制软材,置挤出滚
圆机中制备丸芯,并用流化床干燥,包衣。其中包衣层含有树脂层和粉衣层。
[0009]
海口市制药厂有限公司已申请专利“替比培南酯颗粒剂组合物、其制备方法及应用”(申请号:201510727927.x),公开一种替比培南酯颗粒剂组合物及其制备方法,所述的组合物由替比培南酯原料药和填充剂、黏合剂、包衣液组成,所述的制备工艺采用流化床工艺制粒后,包隔离层、掩味层及矫味层。
[0010]
郑州明泽医药科技有限公司已申请专利“一种替比培南酯制剂及其制备方法”(申请号: 201610339658.4),公开了一种替比培南酯制剂及其制备方法。所述替比培南酯制剂由颗粒、第一包衣层和第二包衣层制成;所述颗粒由替比培南酯、d-甘露醇、微晶纤维素、蔗糖和羟丙基纤维素组成;所述第一包衣层由乙基纤维素混悬液、滑石粉、羟丙基纤维素和纯化水组成;所述第二包衣层由丙烯酸乙酯-甲基丙烯酸甲酯共聚物水分散体、滑石粉、羟丙基甲基纤维素、阿司帕坦和纯化水组成。本发明制成的颗粒进行了两层包衣;其中乙基纤维素无毒、无药理活性,是理想的不溶性材料;而丙烯酸乙酯-甲基丙烯酸甲酯共聚物水分散体用作颗粒剂等的胃溶型薄膜包衣材料,形成的膜能耐唾液,故在服用时,可掩盖药物的不舒适味。其不溶于水和消化液中,但能膨胀并具有渗透性。
[0011]
河南全宇制药股份有限公司已申请专利“一种替比培南酯颗粒剂及其制备方法”(申请号:201610534878.2),该专利提供了一种替比培南酯颗粒剂及其制备方法,涉及药物及其制备技术领域。一种替比培南酯颗粒剂,包括以下重量份的原料:替比培南酯600~700份,稀释剂3500~4500份,羟丙基纤维素40~50份,包衣剂ⅰ455~470份,包衣剂ⅱ380~400份,所述包衣剂ⅰ由乙基纤维素混悬液和滑石粉以重量比10~20:1组成,所述包衣剂ⅱ由胃溶型丙烯酸树脂、滑石粉、羟丙基甲基纤维素和阿司帕坦以重量比25~40:1~3:1:1.5~2.5组成。
[0012]
北京达因高科儿童药物研究院有限公司已申请专利“一种含替比培南酯组合物的口服制剂及其制备方法”(申请号:201711253432.3),该专利涉及一种含替比培南酯组合物的口服制剂及其制备方法。该药物制剂先将活性成分替比培南酯制成固体分散体,然后将固体分散体粉碎过筛处理后,与适宜的稀释剂、粘合剂、甜味剂、润滑剂、色素及香精按常规制粒工艺制备替比培南酯口服制剂。
[0013]
山东省药学科学院已申请专利“一种替比培南酯细粒剂的制备方法”(申请号: 201811425167.7),该专利涉及一种替比培南酯细粒剂的制备方法,所述替比培南酯细粒剂,包含四部分组成:核心颗粒、隔离衣、掩味衣和着色矫味层;其中核心颗粒采用高剪切混合制粒机制备,隔离衣和掩味衣采用流化床切喷工艺制备,着色矫味层将掩味衣颗粒添加矫味剂、着色剂、香精后采用高剪切混合制粒机制备。
[0014]
本品为小儿用碳青霉烯类抗生素药,且替比培南酯的苦味极大,因此稳定性和口感问题成为制约本制剂成为小儿用药的主要因素之一。
技术实现要素:
[0015]
针对现有技术的不足,一种替比培南酯细粒剂组合物及其制备方法,提高本品的稳定性,保证其体外溶出曲线与原研一致,使其质量与疗效与原研一致,并改善口感,使小儿易于接受。
[0016]
本发明制备工艺首先采用干法制粒技术将原料药制成核心颗粒,然后采用流化床
旋流侧喷工艺包掩味包衣层、着色矫味包衣层。其中核心颗粒采用干法制粒工艺使用干法制粒机,所得颗粒粒度范围窄,颗粒较均匀,硬度适于颗粒包衣,且制备过程无水与其他溶剂参与,保证了产品稳定性;旋流侧喷工艺用于掩味包衣层及着色矫味包衣层的包衣,物料旋转翻腾有规律,包埋式侧喷减少包衣液的损耗,对粉末包衣的包衣效率、均匀度优于底喷包衣。综上所述,所采用的制备工艺适于本发明的开发,可以连续有效的生产产品,简化了生产工艺,缩短了生产时间。
[0017]
本发明提供了一种替比培南酯细粒制剂组合物,是由核心颗粒、掩味包衣层和着色矫味包衣层组成,所述核心颗粒是由替比培南酯、填充剂以及粘合剂制成;所述掩味包衣层是由掩味包衣材料、增塑剂和抗粘剂制成;所述着色矫味包衣层由着色矫味包衣材料、着色剂、矫味剂和香精制成。
[0018]
所述填充剂选自甘露醇、乳糖、蔗糖、微晶纤维素、淀粉的一种或两者以上混合物。优选蔗糖、微晶纤维素;蔗糖的用量占所述颗粒剂组合物总重量的5%~65%,微晶纤维素用量占所述颗粒剂组合物总重量的5%~65%。
[0019]
所述粘合剂选自羟丙甲基纤维素、羟丙基纤维素、聚维酮的一种或两种以上的混合物。优选羟丙基纤维素;羟丙基纤维素的用量占所述颗粒剂组合物总重量的1%~10%。
[0020]
所述掩味包衣材料选自乙基纤维素、羟丙甲基纤维素、羟丙基纤维素、醋酸纤维素、丙烯酸树脂的一种或两种以上的混合物。优选乙基纤维素、尤特奇ne30d、羟丙甲基纤维素;乙基纤维素的用量占所述颗粒剂组合物总重量的2%~10%,尤特奇ne30d的用量占所述颗粒剂组合物总重量的2%~10%,羟丙甲基纤维素的用量占所述颗粒剂组合物总重量的 1%~5%
[0021]
所述增塑剂选自聚乙二醇、硅油、柠檬酸三乙酯、三醋酸甘油酯的一种或两种以上的混合物。优选柠檬酸三乙酯,柠檬酸三乙酯的用量占所述颗粒剂组合物总重量的0.5%~5%。
[0022]
所述抗粘剂选自滑石粉、硬脂酸钙、硬脂酸镁。优选滑石粉,滑石粉的用量占所述颗粒剂组合物总重量的0.5%~5%。
[0023]
所述着色矫味包衣材料选自羟丙甲基纤维素、羟丙基纤维素的一种或两种以上的混合物。优选羟丙甲基纤维素,羟丙甲基纤维素的用量占所述颗粒剂组合物总重量的1%~10%。
[0024]
所述着色剂选自胭脂红、日落黄、柠檬黄、苋菜红、红氧化铁、黄氧化铁的一种或两种以上的混合物。优选胭脂红、日落黄,胭脂红的用量占所述颗粒剂组合物总重量的 0.001%~5%,日落黄的用量占所述颗粒剂组合物总重量的0.001%~5%。
[0025]
所述矫味剂剂选自阿司帕坦、三氯蔗糖、蔗糖的一种或两种以上的混合物。优选阿司帕坦、蔗糖,阿司帕坦的用量占所述颗粒剂组合物总重量的0.5%~5%,蔗糖的用量占所述颗粒剂组合物总重量的0.5%~10%。
[0026]
所述香精剂选自桃味香精、橙味香精、樱桃香精、杏香精、香兰素、乙基香兰素的一种或两种以上的混合物。优选香兰素、乙基香兰素,香兰素的用量占所述颗粒剂组合物总重量的0.1%~5%,乙基香兰素的用量占所述颗粒剂组合物总重量的0.1%~5%。
[0027]
另一方面,本发明提供了上述替比培南酯细粒剂组合物的制备方法,包括如下步骤: 1)粉碎过筛:替比培南酯粉碎后过100目筛处理,填充剂粉碎后过80目筛,香精过80 目
筛;
[0028]
2)预混合:取替比培南酯、填充剂、粘合剂置于混合机中进行预混合10分钟;
[0029]
3)制粒:采用干法制粒工艺,取混合物料置于干法制粒机中,制粒;
[0030]
4)筛分颗粒:收集40目~120目筛之间的颗粒;
[0031]
5)掩味层包衣液配制:取抗粘剂加入纯化水中,配成混悬液,均质机匀化,过80目筛,再加入增塑剂、掩味层包衣材料搅拌,备用;
[0032]
6)掩味层包衣:采用流化床旋流侧喷工艺,取颗粒置于流化床中,喷入包衣液,控制包衣增重在5%~15%,干燥;
[0033]
7)着色矫味层包衣液配制:取着色矫味层包衣材料、矫味剂、色素及香精,加30%乙醇水溶液溶解,均质机匀化后过80目筛;
[0034]
8)着色矫味层包衣:采用流化床旋流侧喷工艺,取掩味层包衣后颗粒置于流化床中,喷入包衣液,控制包衣增重在4%~10%,干燥至颗粒水分小于1%;检测中间体,进行颗粒分装及外包,即得。
[0035]
与现有技术相比,本发明涉及的替比培南酯细粒剂及其制备工艺具有如下优点:(1) 药物在水、0.1mol/l盐酸、ph4.0磷酸盐缓冲液及ph6.8磷酸盐缓冲液四种溶出介质中的行为与原研相似;(2)制备工艺简单,适合工业化大生产。
附图说明
[0036]
图1.实施例1~实施例3样品与原研在水中溶出曲线图。
[0037]
图2.实施例1~实施例3样品与原研在0.1mol/l盐酸中溶出曲线图。
[0038]
图3.实施例1~实施例3样品与市售品在ph4.0缓冲液中溶出曲线图。
[0039]
图4.实施例1~实施例3样品与市售品在ph6.8缓冲液中溶出曲线。
具体实施方式
[0040]
下面结合实施例对本发明进一步描述,但本发明并不为实施例所限制。
[0041]
本实施例涉及一种替比培南酯细粒剂的制备方法实施例1:
[0042]
处方组分组成见表1:
[0043]
表1实施例1的处方组成
[0044][0045][0046]
制备方法:
[0047]
1)粉碎过筛:替比培南酯粉碎后过100目筛处理,蔗糖粉碎后过80目筛,香;兰素、乙基香兰素过80目筛;
[0048]
2)预混合:取替比培南酯、微晶纤维素、蔗糖、羟丙基纤维素置于混合机中进行预混合 10分钟;
[0049]
3)制粒:采用干法制粒工艺,取混合物料置于干法制粒机中,制粒;
[0050]
4)筛分颗粒:收集40目~120目筛之间的颗粒;
[0051]
5)掩味层包衣液配制:取滑石粉加入纯化水中,配成混悬液,均质机匀化,过80目筛,再加入柠檬酸三乙酯、乙基纤维素混悬液、羟丙甲基纤维素、尤特奇ne30d搅拌,备用;
[0052]
6)掩味层包衣:采用流化床旋流侧喷工艺,取颗粒置于流化床中,喷入包衣液,控制包衣增重在15%~30%,干燥;
[0053]
7)着色矫味层包衣液配制:取羟丙甲基纤维素、胭脂红、日落黄、阿司帕坦、蔗糖、香兰素、乙基香兰素,加30%乙醇水溶液溶解,均质机匀化后过80目筛;
[0054]
8)着色矫味层包衣:采用流化床旋流侧喷工艺,取掩味层包衣后颗粒置于流化床中,喷入包衣液,控制包衣增重在4%~10%,干燥至颗粒水分小于1%;检测中间体,进行颗粒分装及外包,即得。
[0055]
实施例2:
[0056]
本实施例涉及一种替比培南酯细粒剂的制备方法:
[0057]
处方组分组成见表2:
[0058]
表2实施例2的处方组成
[0059][0060][0061]
制备方法:参照实施例1的方法制备。
[0062]
实施例3:
[0063]
本实施例涉及一种替比培南酯细粒剂的制备方法:
[0064]
处方组分组成件表3:
[0065]
表3实施例3的处方组成
[0066][0067][0068]
制备方法:参照实施例1的方法制备。
[0069]
实施例1~3与原研药溶出行为的测定及比较
[0070]
对本发明所述替比培南酯细粒剂与原研药的溶出曲线对比试验如下:由实施例1-~3制得的替比培南酯细粒剂(采用12个计量单位即12袋进行测定)、参照中国药典2015年版四部0931溶出度测定法第二法的试验装置,分别以水、0.1mol/l盐酸、ph4.0磷酸盐缓冲液及ph6.8磷酸盐缓冲液为溶出介质,转速为每分钟50转,计算药物的累积溶出量,并绘制溶出曲线,结果见表4~7,溶出曲线图见图1~4。
[0071]
表4替比培南酯细粒剂自制品与原研在水中的溶出曲线对比
[0072]
取样时间点(min)实施例1实施例2实施例3原研57.810.28.510.01020.222.719.823.81524.725.821.533.02029.333.728.634.23034.637.433.136.04540.144.838.642.66045.147.543.847.59050.055.548.952.2
12055.257.554.259.8
[0073]
表5替比培南酯细粒剂自制品与原研在0.1mol/l盐酸中的溶出曲线对比
[0074]
取样时间点(min)实施例1实施例2实施例3原研529.430.426.925.01020.021.018.116.61515.615.814.311.1
[0075]
表6替比培南酯细粒剂自制品与原研在ph4.0磷酸盐缓冲液的溶出曲线对比
[0076][0077][0078]
表7替比培南酯细粒剂自制品与原研在ph6.8磷酸盐缓冲液的溶出曲线对比
[0079]
取样时间点(min)实施例1实施例2实施例3原研516.817.220.619.61029.530.132.831.61543.036.639.139.62046.746.248.845.83056.651.853.252.54568.967.970.066.46071.371.472.571.09077.479.281.578.212081.785.585.582.7
[0080]
结论:本发明提供的替比培南酯细粒剂的制备方法使其在水、0.1mol/l盐酸、ph4.0 磷酸盐缓冲液及ph6.8磷酸盐缓冲液四种溶出介质中的溶出行为与原研药的溶出行为一致。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1