生物传感器探针用保护膜材料的制作方法
本公开涉及用于保护构成生物传感器的探针的膜材料。更具体而言,提供能够防止构成插入到体内的生物传感器探针的酶、介体的流出的保护膜用聚合物材料。
背景技术:
生物传感器是指利用或模仿生物体具有的分子识别能力来测量物质的系统,例如为如下的测定装置,即,将酶-底物、抗原-抗体、激素-受体等组合中的一者作为检测体(测定对象物质),另一者作为接受体,将通过检测体与其接受体之间的分子识别反应而产生的化学变化用转换器转换成电信号,根据得到的电信号的强度来测定检测体的量。
作为生物传感器中使用的生物分子,除上述以外,还包括基因、糖链、脂质、肽、细胞、组织等。其中,使用了酶的生物传感器的开发进展最快,其代表例为使用了葡萄糖氧化酶(glucoseoxidase;gox)的葡萄糖传感器。
自我血糖测定所使用电化学式葡萄糖传感器大体上为如下的构成,即,在其表面形成了电极的绝缘基板上隔着间隔件而配置有罩子。上述电极上配置有包含检测体响应性酶、氧化还原介体(电子传导体)等的试剂,该部分成为分析部。用于导入血液的流路的一端与该分析部连通,上述流路的另一端朝着外部开口,此处成为供血口。使用了这样的传感器的血糖值的测定例如像下述那样进行。即,首先,将上述传感器安装于专用的测定装置(测量仪)。然后,用刺血针刺伤指尖等而使其出血,使上述传感器的供血口与其接触。血液由于毛细现象而被吸入传感器的流路中,通过其而导入到分析部,在此与上述试剂接触。然后,检测体响应性酶e(例如gox、gdh)通过与血液中的葡萄糖发生特异性的反应而将葡萄糖氧化。氧化还原介体m接受通过氧化而产生的电子。将接受了电子而被还原的氧化还原介体m用电极以电化学的方式氧化。根据通过还原体氧化还原介体m的氧化而得到的电流值、电荷量的大小,可简便地检测出血液中的葡萄糖浓度,即血糖值。
这样的电化学式血糖传感器在糖尿病治疗的血糖值管理中发挥重要的作用,糖尿病患者能够基于血糖值进行合适的胰岛素给药、饮食控制。然而,必须一天若干次地测定血糖值,每次的血液采集会加深患者的痛苦,难以维持生活的质量(qualityoflife;qol)。
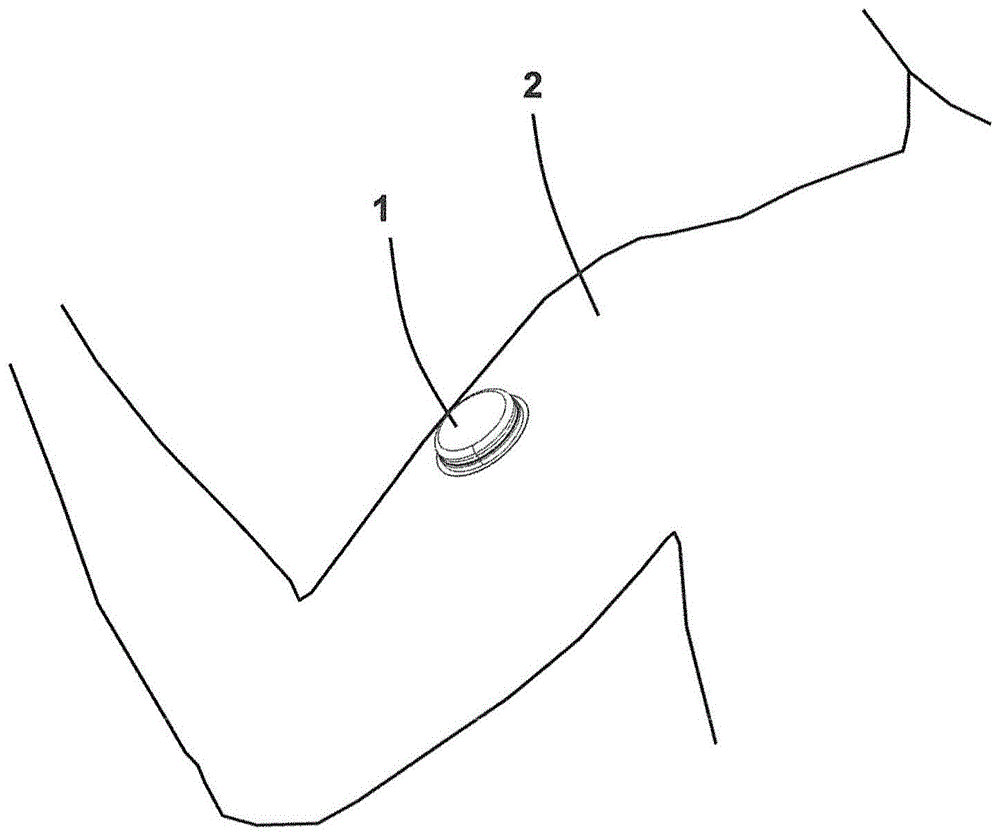
已开发有埋入型安培式葡萄糖传感器。将这样的埋入型安培式葡萄糖传感器1的主体10贴附于生物体2,将探针部分11插入到生物体内,从而持续地进行血糖值的测定(图1和2)。由此,无需每次进行血液采集而能够长时间地测定血糖值。
日本厚生劳动省进行了“平成9年远程诊疗通知(平成9年12月24日日本健政发第1075号厚生省健康政策局长通知)”,示出了远程诊疗的基本的想法、根据与日本医师法第20条等的关系所应注意的事项。其后,鉴于信息通信设备的开发、普及的状况,在2015年8月10日关于使用了信息通信设备的诊疗(所谓的“远程诊疗”)向日本各都道府县知事进行了事务联络。根据2015年通知,远程诊疗事实上被解禁,在2016年,使用信息通信设备3(智能手机)和专属应用软件来与生物传感器1进行无线数据通信的远程诊疗工具开始面世(图3)。此外,在2017年7月14日,关于远程诊疗的操作,再次以众所周知的清晰的主旨进行了通知(日本医政发0714第4号)。根据2015年通知,就远程诊疗而言,只要能够确认当事人为医生和患者本人,则即使对于组合了视频电话、电子邮件、社交网络服务等信息通信设备的远程诊疗,在可得到能代替直接的当面诊疗的程度的关于患者身心状况的有用信息的情况下,也不直接与日本医师法第20条等抵触。由于该2017年通知,利用了信息通信设备的远程诊疗将会进一步发展。因此,可期待埋入型传感器的需要日益高涨。
专利文献1公开了使用无线发送器、安装于患者并插入到皮肤中的电化学传感器控制装置,记载了使用无线发送器将收集的有关检测体量的数据传送至显示装置的技术。另外,专利文献1还公开了安装在这样的电化学传感器中的包含乙烯基吡啶等杂环式氮基的膜。这些膜限制电化学传感器中的检测体向工作电极的扩散。在不具有膜的葡萄糖传感器中,葡萄糖向检测层的流量与葡萄糖浓度一同线性增加,在到达检测层的全部葡萄糖被消耗的过程中,测定的输出信号与葡萄糖的流量成线性比例,葡萄糖的消耗在检测层中受到限制的情况下,测定信号发生饱和而与葡萄糖的流量或浓度不成线性比例。因此,专利文献1中采用了在检测层上形成包含聚乙烯基吡啶等杂环式氮基的扩散限制膜,使葡萄糖向检测层的流量减少,由此防止传感器的饱和的技术。
专利文献2公开了包含具有至少一个亲水性嵌段和至少一个疏水性嵌段的单一嵌段共聚物的扩散阻隔件,该扩散阻隔件与专利文献1同样是控制分析物从电极系统的外侧向酶分子的扩散的部件。另外,这样的酶分子被固定至电极而形成酶层。就这样的酶层的制造而言,例如像专利文献3公开的那样,能够通过吸附、捕捉而将酶固定至工作电极,并用戊二醛等进行交联从而更加牢固地进行固定。
现有技术文献
专利文献
专利文献1:日本特表第2010-517054号说明书
专利文献2:日本特表第2015-515305号说明书
专利文献3:国际公开第2007/147475号
技术实现要素:
发明要解决的课题
埋入型传感器的探针长时间插入在体内,因此作为构成要素的检测体响应性酶、氧化还原介体流出的机会增大。如果检测体响应性酶、氧化还原介体流出到传感器外部,则不仅传感器灵敏度劣化,还会对生物体造成伤害。另外,如果检测体响应性酶、氧化还原介体流出到外部,则传感器的耐久性也降低。因此,防止检测体响应性酶、氧化还原介体的流出的对策是非常重要的。
如果想要将构成埋入型生物传感器的探针的检测体响应性酶和氧化还原介体二者固定化来防止流出,则能够使用的酶和介体聚合物的组合、传感器的结构会受限。因此,期望开发在包含酶和/或氧化还原介体的检测层上形成而能够防止酶和氧化还原介体向外部流出的膜。另外,这样的膜不能阻碍葡萄糖等检测体侵入到内部。因此,本公开的课题在于提供一种保护膜,其为了适用于埋入型生物传感器的探针,不阻碍检测体向内部的侵入,且防止酶和氧化还原介体向外部的流出。
用于解决课题的手段
本公开提供一种膜结构体作为在生物传感器的探针中有用的膜结构体,其具备至少包含检测体响应性酶和氧化还原介体的检测层、以及在上述检测层上形成的保护膜,上述保护膜单独包含式(1)所示的聚(苯乙烯-无规-4-乙烯基吡啶-无规-甲基丙烯酸丙二醇酯),或者包含共聚物混合物,上述共聚物混合物包含:式(1)所示的聚(苯乙烯-无规-4-乙烯基吡啶-无规-甲基丙烯酸丙二醇酯);以及式(2)所示的聚(4-乙烯基吡啶)-嵌段-聚(甲基丙烯酸c1-15烷基酯)或式(3)所示的聚(4-乙烯基吡啶-无规-甲基丙烯酸2-羟基乙酯)。需要说明的是,式中,单体间的斜线不是表示3种单体单元为式中的记载顺序,而是表示除了单体单元间的反应性所引起的不均匀以外无规律地键合。
[化学式1]
[式中,m表示1~20的整数,x、y和z分别表示3种单体单元即苯乙烯、4-乙烯基吡啶、甲基丙烯酸丙二醇酯的摩尔百分率且x+y+z=100,w表示数均分子量。]
[化学式2]
[式中,r表示碳数1~15的烷基,p和q分别表示2种单体单元即4-乙烯基吡啶、甲基丙烯酸c1-15烷基酯的重复单元,w表示数均分子量。]
[化学式3]
[式中,s和t分别表示2种单体单元即4-乙烯基吡啶、甲基丙烯酸2-羟基乙酯的摩尔百分率且s+t=100,w表示数均分子量。]
上述式(1)所示的聚合物是以苯乙烯、4-乙烯基吡啶、甲基丙烯酸丙二醇酯作为单体单元的无规共聚物,苯乙烯的摩尔百分率x为5~30,优选为10~30,进一步优选为15~25,4-乙烯基吡啶的摩尔百分率y为45~65,优选为50~60,甲基丙烯酸丙二醇酯的摩尔百分率z为15~30,优选为20~25,只要x、y和z的合计定为100,则x、y和z可以不是整数。另外,上述聚合物的数均分子量为40~80×103,优选为45~65×103。
上述式(2)所示的聚合物是由聚(4-乙烯基吡啶)和聚(甲基丙烯酸c1-15烷基酯)形成的嵌段共聚物,构成聚(4-乙烯基吡啶)的4-乙烯基吡啶的重复单元p和构成聚(甲基丙烯酸c1-15烷基酯)的甲基丙烯酸烷基酯的重复单元q各自以构成上述聚合物的各嵌段的数均分子量为50~200×103、优选为60~100×103的方式选定即可。
上述式(2)所示的聚合物中,聚(甲基丙烯酸c1-15烷基酯)的c1-15烷基表示碳数1~15的烷基,例如可举出甲基、乙基、丙基、丁基、戊基、己基、庚基、辛基、壬基、癸基、十一烷基、十二烷基、十三烷基、十四烷基、十五烷基、以及它们的异构体,优选为c3-6烷基。
上述式(3)所示的聚合物对于提高生物相容性是有利的,是以4-乙烯基吡啶、甲基丙烯酸2-羟基乙酯作为单体单元的无规共聚物,4-乙烯基吡啶的摩尔百分率s为40~80,优选为60~70,甲基丙烯酸2-羟基乙酯的摩尔百分率t为20~60,优选为30~40,只要s和t的合计定为100,则s和t可以不是整数。另外,上述聚合物的数均分子量为20~500×103,优选为60~300×103。
上述聚合物可以利用聚乙二醇二缩水甘油醚(pegdge)等交联剂进行过交联。
上述保护膜可以进一步含有例如聚(丙烯酸2-甲氧基乙酯)作为添加剂。由此,保护膜的生物相容性提高。
发明效果
如果在构成埋入型生物传感器的探针的包含酶、介体的检测层上使用本公开的共聚物或共聚物混合物形成保护膜,则能够不阻碍葡萄糖等检测体侵入到内部且防止检测层所包含的酶、介体流出到外部。
附图说明
图1为示出埋入型生物传感器安装于生物体(人体)的状态的示意图。
图2为示出安装于生物体(人体)的状态的埋入型生物传感器的截面图。
图3为将测定数据与智能手机进行无线通信的埋入型生物传感器的示意图。
图4为本公开的一个具体例的埋入型生物传感器的探针的制造工序。
图5为本公开的一个具体例的埋入型生物传感器的探针的制造工序。
图6为本公开的一个具体例的埋入型生物传感器的探针的制造工序。
图7为本公开的一个具体例的埋入型生物传感器的探针表面侧的平面图。
图8为图7的a-a’切割线处的截面图。
图9为图8的b-b’切割线处的截面图。
图10为图8的c-c’切割线处的截面图。
图11为示出将本公开的共聚物用于保护膜的探针的葡萄糖响应特性的曲线图。
图12为示出将本公开的共聚物用于保护膜的探针的耐久性的曲线图。
图13为示出将本公开的共聚物混合物用于保护膜的探针的葡萄糖响应特性的曲线图。
图14为示出将本公开的共聚物混合物用于保护膜的探针的耐久性的曲线图。
图15为示出将本公开的共聚物混合物用于保护膜的探针的葡萄糖响应特性的曲线图。
图16为示出将本公开的共聚物混合物用于保护膜的探针的耐久性的曲线图。
图17为示出将比较例的聚合物用于保护膜的探针的葡萄糖响应特性的曲线图。
图18为示出将比较例的聚合物用于保护膜的探针的耐久性的曲线图。
图19为示出将参考例的聚合物用于保护膜的探针的葡萄糖响应特性的曲线图。
图20为示出将参考例的聚合物用于保护膜的探针的耐久性的曲线图。
具体实施方式
1.埋入型生物传感器的探针的制造方法
对于应用本公开的膜结构体的某具体例的埋入型生物传感器1的探针11的制造方法进行说明。以下所示的结构和制造方法为本公开的一个具体例,只要能够作为探针使用,则不限于下述的构成。
(1)绝缘性基板的准备
埋入型生物传感器1包含主体10和探针11,探针11大体为钥匙形状,上述钥匙形状包含插入到生物体内的感应部分、和用于与生物传感器主体10的内部电路进行电连接的端子部分。感应部分以能够插入到体内的方式形成得较细,端子部分以插入到生物传感器主体10从而形成电连接的方式具有一定的大小。因此,首先准备钥匙形状的绝缘性基板111(图4a)。上段示出从表面侧观察的平面图,下段示出从背面侧观察的平面图(以下相同)。该绝缘性基板111只要是能够作为插入到生物体内的探针而使用的材料和厚度,则没有特别限定,例如可以使用约200μm厚的聚对苯二甲酸乙二醇酯(pet)。
(2)导电性薄膜的形成
在绝缘性基板111的两面通过溅射法、蒸镀法、离子镀等沉积碳或者选自金、银、铂或钯等金属中的导电性金属材料,由此形成导电性薄膜112(图4b)。导电性薄膜的优选的厚度为10nm~数百nm。
(3)电极引线的形成
对于在绝缘性基板111的表面侧形成的导电性薄膜112,通过激光绘图形成达到绝缘性基板111的表面的深度的槽113,从而将工作电极引线112a与参比电极引线112b分离并电绝缘(图5c)。
(4)绝缘性抗蚀膜的形成
在绝缘性基板111的表面侧除了作为用于与工作电极114和参比电极115以及主体10电连接的工作电极用端子114a和参比电极用端子115a而使用的区域以外的部分,通过溅射法、丝网印刷法等形成具有开口的绝缘性抗蚀膜116a,并在绝缘性基板111的背面侧除了作为用于与对电极117和主体10电连接的对电极用端子117a而使用的区域以外的部分,通过溅射法、丝网印刷法等形成具有开口的绝缘性抗蚀膜116b(图5d)。绝缘性抗蚀膜的优选的厚度为5~40μm。
(5)参比电极的形成
在形成于绝缘性基板111的表面侧的抗蚀膜116a的参比电极用的开口通过丝网印刷法、喷墨法使ag/agcl沉积,从而形成参比电极115(图5e)。参比电极的优选的厚度为5~40μm。
(6)检测层的形成
在工作电极114上将碳粒子等导电性粒子的悬浮液、检测体响应性酶的水溶液和氧化还原介体的水溶液进行涂布干燥,从而形成包含导电性粒子、检测体响应性酶和氧化还原介体的检测层118(图6f)。本公开中,“检测体响应性酶”是指能够特异性地催化检测体的氧化或还原的生物化学物质。只要能够用于生物传感器的检出目的,则可以为任意生物化学物质。例如,以葡萄糖作为检测体的情况下,适宜的检测体响应性酶为葡萄糖氧化酶(glucoseoxidase;gox)、葡萄糖脱氢酶(glucosedehydrogenase;gdh)等。“氧化还原介体”是指中介电子传导的氧化还原物质,在生物传感器中承担由检测体(分析物)的氧化还原反应而产生的电子的传导。例如,包括吩嗪衍生物等,但不限于此,只要能够用于生物传感器的检出目的,则可以为任意氧化还原物质。检测层的优选的厚度为5~80μm。
(7)保护膜的形成
将感应部分浸渍在包含保护膜用聚合物的溶液中,在感应部分的两面、侧面和顶端形成保护膜119(图6g)。保护膜119不覆盖工作电极用端子114a、参比电极用端子115a和对电极用端子117a,至少覆盖工作电极114、参比电极115、对电极117和检测层118,形成为插入到生物体内的长度以上。保护膜的优选的厚度为5~200μm。
2.埋入型生物传感器的探针的内部结构
进一步说明应用本公开的膜结构体的埋入型生物传感器的探针的内部结构。
将图7的a-a’切割线处的截面图示于图8。在绝缘性基板111的两侧形成有导电性薄膜112。就表面侧的导电性薄膜112而言,通过槽113分离为工作电极引线112a和参比电极引线112b的2个引线并且电绝缘。工作电极引线112a的一部分作为工作电极114发挥功能,在工作电极114上形成有检测层118。另外,在绝缘性抗蚀膜116a的开口部分形成参比电极115,并与参比电极引线112b电连接。背面侧的导电性薄膜112成为对电极引线112c,其一部分作为对电极117发挥功能。
将图8的b-b’切割线处的截面图示于图9。在绝缘性基板111的表面侧形成有工作电极114,其上形成有检测层118,在背面侧形成有对电极117。此外,可知感应部分的周围全部被本公开的保护膜119覆盖。
将图8的c-c’切割面处的截面图示于图10。在绝缘性基板111的表面侧形成有被槽113电分离的工作电极引线112a和参比电极引线112b,其上形成有绝缘性抗蚀膜116a。在绝缘性抗蚀膜116a的开口部形成有参比电极115。在基板111的背面侧形成有对电极引线112c,其上形成有绝缘性抗蚀膜116b。此外,可知感应部分的周围全部被本公开的保护膜119覆盖。
实施例
[实施例1]
<探针的制作>
(1)绝缘性基板的准备
如图5a所示,裁切聚对苯二甲酸乙二醇酯(pet)(toray株式会社制lumirrorre20#188;189μm厚)从而准备钥匙形状的绝缘性基板。
(2)导电性薄膜的形成
如图5b所示,在上述绝缘性基板的两面通过溅射法沉积金,由此形成导电性薄膜(厚度30nm)。
(3)电极引线的形成
如图5c所示,对于在绝缘性基板的表面侧形成的导电性薄膜,通过激光绘图形成达到绝缘性基板的表面的深度的槽,从而将工作电极引线与参比电极引线分离而电分离。
(4)绝缘性抗蚀膜的形成
如图5d所示,在绝缘性基板的表面侧除了作为用于与工作电极和参比电极以及埋入型生物传感器的主体电连接的工作电极用端子和参比电极用端子而使用的区域以外的部分,通过丝网印刷法形成具有开口的绝缘性抗蚀膜,并在绝缘性基板的背面侧除了作为用于与对电极和主体电连接的对电极用端子而使用的区域以外的部分,通过丝网印刷法形成具有开口的绝缘性抗蚀膜(厚度10~15μm)。
(5)参比电极的形成
如图5e所示,在形成于绝缘性基板的表面侧的抗蚀膜的参比电极用的开口通过丝网印刷法使ag/agcl沉积,从而形成参比电极(厚度10~15μm)。
(6)检测层的形成
如图6f所示,以从在绝缘性基板的表面侧形成的绝缘性抗蚀膜的开口部露出的导电性薄膜作为工作电极,适量涂布作为导电性粒子的碳粒子的悬浊液、作为对于葡萄糖的检测体响应性酶的葡萄糖氧化酶(glucoseoxidase;gox)的水溶液和作为氧化还原介体的吩嗪衍生物的水溶液并干燥,从而形成检测层(厚度15μm)。
(7)保护膜的形成
如图6g所示,将感应部分浸渍在包含交联剂和保护膜用聚合物的乙醇溶液中,在感应部分的两面、侧面和顶端形成保护膜(厚度5~40μm)。
更具体而言,在将600mg式(4)所示的聚(苯乙烯-无规-4-乙烯基吡啶-无规-甲基丙烯酸丙二醇酯)(mw/mn=1.8,m=2)[共聚物(4)]、47mg作为交联剂的聚乙二醇二缩水甘油醚(pegdge)(mn=1000)溶于1ml溶剂(乙醇95%、4-(2-羟基乙基)-1-哌嗪乙磺酸(hepes)缓冲液(10mm,ph8)5%)而得到的溶液中,将上述制造的探针以10分钟间隔浸渍6次。其后,在室温下干燥48小时,由此形成交联的保护膜,得到探针a。将上述保护膜的形成条件汇总于表1。
[化学式4]
<探针特性的测定>
[葡萄糖响应特性]
将探针a安装于埋入型安培式葡萄糖传感器,并在37℃的磷酸缓冲生理盐水(pbs,ph7)中设置探针。在该pbs溶液中以500秒为间隔逐次添加葡萄糖50、100、200、300、400、500mg/dl,持续测定电流响应值(na)。
在葡萄糖浓度0~500mg/dl的范围中显示出高的线性,葡萄糖响应性良好。将结果示于图11,汇总于表2。
[耐久性]
将探针a在37℃的磷酸缓冲生理盐水(pbs,ph7)中保存。在保存前(第0日)和保存后第7日,将探针a安装于埋入型安培式葡萄糖传感器,在37℃的磷酸缓冲生理盐水(pbs,ph7)中设置探针。在该pbs溶液中以500秒为间隔逐次添加葡萄糖50、100、200、300、400、500mg/dl,持续测定电流响应值(na)。以第0日的在葡萄糖浓度500mg/dl下的电流响应值作为100%,算出各浓度下的响应率(%)。
保存后第7日的响应特性在葡萄糖浓度0~500mg/dl的范围中显示出高的线性,与第0日相比几乎没有变化,耐久性良好。将结果示于图12,汇总于表2。
[实施例2]
<探针的制作>
在保护膜的形成中,变更保护膜用聚合物,除此以外,与实施例1同样地进行,制作探针。
更具体而言,在将600mg式(5)所示的聚(苯乙烯-无规-4-乙烯基吡啶-无规-甲基丙烯酸丙二醇酯)(mw/mn=1.6;m=约16)[共聚物(5)]、47mg作为交联剂的聚乙二醇二缩水甘油醚(pegdge)(mn=1000)溶于1ml溶剂而得到的溶液中,将实施例1中制造的探针以10分钟间隔浸渍6次。在室温下干燥48小时,由此形成保护膜,得到探针b。将上述保护膜的形成条件汇总于表1。
[化学式5]
<探针特性的测定>
[葡萄糖响应特性]
对于探针b的葡萄糖响应特性,与实施例1同样地进行测定。
在葡萄糖浓度0~500mg/dl的范围中显示出高的线性,葡萄糖响应性良好。将结果示于图11,汇总于表2。
[耐久性]
对于探针b的耐久性,与实施例1同样地进行测定。
保存后第7日的响应特性在葡萄糖浓度0~500mg/dl的范围中显示出高的线性,与第0日相比几乎没有变化,耐久性良好。将结果示于图12,汇总于表2。
[实施例3]
在保护膜的形成中,变更保护膜用聚合物,除此以外,与实施例1同样地进行,制作探针。
更具体而言,在将300mg式(4)所示的聚(苯乙烯-无规-4-乙烯基吡啶-无规-甲基丙烯酸丙二醇酯)(mw/mn=1.8,m=2)[共聚物(4)]、300mg式(5)所示的聚(苯乙烯-无规-4-乙烯基吡啶-无规-甲基丙烯酸丙二醇酯)(mw/mn=1.6;m=约16)[共聚物(5)]、47mg作为交联剂的聚乙二醇二缩水甘油醚(pegdge)(mn=1000)溶于1ml溶剂而得到的溶液中,将实施例1中制造的探针以10分钟间隔浸渍6次。在室温下干燥48小时,由此形成保护膜,得到探针c。将上述保护膜的形成条件汇总于表1。
<探针特性的测定>
[葡萄糖响应特性]
对于探针c的葡萄糖响应特性,与实施例1同样地进行测定。
在葡萄糖浓度0~500mg/dl的范围中显示出高的线性,葡萄糖响应性良好。将结果示于图11,汇总于表2。
[耐久性]
对于探针c的耐久性,与实施例1同样地进行测定。
保存后第7日的响应特性在葡萄糖浓度0~500mg/dl的范围中显示出高的线性,与第0日相比几乎没有变化,耐久性良好。将结果示于图12,汇总于表2。
[实施例4]
<探针的制作>
在保护膜的形成中,变更保护膜用聚合物,除此以外,与实施例1同样地进行,制作探针。
更具体而言,在将300mg式(4)所示的聚(苯乙烯-无规-4-乙烯基吡啶-无规-甲基丙烯酸丙二醇酯)(mw/mn=1.8,m=2)[无规共聚物(4)]和300mg式(6)所示的聚(4-乙烯基吡啶)-嵌段-聚(甲基丙烯酸2,2-二甲基乙酯)(mw/mn=1.15;w’=77.0-g-80.0×103)[嵌段共聚物(6)]、47mg作为交联剂的聚乙二醇二缩水甘油醚(pegdge)(mn=1000)溶于1ml溶剂(乙醇95%、4-(2-羟基乙基)-1-哌嗪乙磺酸(hepes)缓冲液(10mm,ph8)5%)而得到的溶液中,将上述制造的探针以10分钟间隔浸渍8次。其后,在室温下干燥48小时,由此形成交联的保护膜,得到探针d。将上述保护膜的形成条件汇总于表3。
[化学式6]
<探针特性的测定>
[葡萄糖响应特性]
对于探针d的葡萄糖响应特性,与实施例1同样地进行测定。
在葡萄糖浓度0~500mg/dl的范围中显示出高的线性,葡萄糖响应性良好。将结果示于图13,汇总于表4。
[耐久性]
对于探针d的耐久性,与实施例1同样地进行测定。
保存后第7日的响应特性在葡萄糖浓度0~500mg/dl的范围中显示出高的线性,与第0日相比几乎没有变化,耐久性良好。将结果示于图14,汇总于表4。
[实施例5]
<探针的制作>
在保护膜的形成中,变更保护膜用聚合物,除此以外,与实施例4同样地进行,制作探针。
更具体而言,在实施例4中,代替式(6)所示的聚(4-乙烯基吡啶)-嵌段-聚(甲基丙烯酸2,2-二甲基乙酯)[嵌段共聚物(6)],使用式(7)所示的聚(4-乙烯基吡啶)-嵌段-聚(甲基丙烯酸正丁酯)(mw/mn=1.3;w”=6.0-g-4.5×103)[嵌段共聚物(7)],除此以外,与实施例4同样地形成保护膜,得到探针e。将上述保护膜的形成条件汇总于表3。
[化学式7]
<探针特性的测定>
[葡萄糖响应特性]
对于探针e的葡萄糖响应特性,与实施例1同样地进行测定。
在葡萄糖浓度0~500mg/dl的范围中显示出高的线性,葡萄糖响应性良好。将结果示于图13,汇总于表4。
[耐久性]
对于探针e的耐久性,与实施例1同样地进行测定。
保存后第7日的响应特性在葡萄糖浓度0~500mg/dl的范围中显示出高的线性,与第0日相比几乎没有变化,耐久性良好。将结果示于图14,汇总于表4。
[实施例6]
在保护膜的形成中,变更保护膜用聚合物,除此以外,与实施例4同样地进行,制作探针。
更具体而言,在实施例4中,代替式(6)所示的聚(4-乙烯基吡啶)-嵌段-聚(甲基丙烯酸2,2-二甲基乙酯)[嵌段共聚物(6)],使用式(8)所示的聚(4-乙烯基吡啶-无规-甲基丙烯酸2-羟基乙酯)(mw/mn=1.2)[无规共聚物(8)],除此以外,与实施例4同样地形成保护膜,得到探针f。将上述保护膜的形成条件汇总于表3。
[化学式8]
<探针特性的测定>
[葡萄糖响应特性]
对于探针f的葡萄糖响应特性,与实施例1同样地进行测定。
在葡萄糖浓度0~500mg/dl的范围中显示出高的线性,葡萄糖响应性良好。将结果示于图13,汇总于表4。
[耐久性]
对于探针f的耐久性,与实施例1同样地进行测定。
保存后第7日的响应特性在葡萄糖浓度0~500mg/dl的范围中显示出高的线性,与第0日相比几乎没有变化,耐久性良好。将结果示于图14,汇总于表4。
[实施例7]
在保护膜的形成中,变更保护膜用聚合物,除此以外,与实施例4同样地进行,制作探针。
更具体而言,在实施例4中,代替式(6)所示的聚(4-乙烯基吡啶)-嵌段-聚(甲基丙烯酸2,2-二甲基乙酯)[嵌段共聚物(6)],使用式(9)所示的聚(4-乙烯基吡啶-无规-甲基丙烯酸2-羟基乙酯)(mw/mn=1.6)[无规共聚物(9)],除此以外,与实施例4同样地形成保护膜,得到探针g。将上述保护膜的形成条件汇总于表3。
[化学式9]
<探针特性的测定>
[葡萄糖响应特性]
对于探针g的葡萄糖响应特性,与实施例1同样地进行测定。
在葡萄糖浓度0~500mg/dl的范围中显示出高的线性,葡萄糖响应性良好。将结果示于图13,汇总于表4。
[耐久性]
对于探针g的耐久性,与实施例1同样地进行测定。
保存后第7日的响应特性在葡萄糖浓度0~500mg/dl的范围中显示出高的线性,与第0日相比几乎没有变化,耐久性良好。将结果示于图14,汇总于表4。
[实施例8]
在保护膜的形成中,变更保护膜用聚合物,除此以外,与实施例1同样地进行,制作探针。
更具体而言,在将300mg式(5)所示的聚(苯乙烯-无规-4-乙烯基吡啶-无规-甲基丙烯酸丙二醇酯)(mw/mn=1.6,m=约16)[无规共聚物(5)]和300mg式(6)所示的聚(4-乙烯基吡啶)-嵌段-聚(甲基丙烯酸2,2-二甲基乙酯)(mw/mn=1.15;w’=77.0-g-80.0×103)[嵌段共聚物(6)]、47mg作为交联剂的聚乙二醇二缩水甘油醚(pegdge)(mn=1000)溶于1ml溶剂(乙醇95%、4-(2-羟基乙基)-1-哌嗪乙磺酸(hepes)缓冲液(10mm,ph8)5%)而得到的溶液中,将上述制造的探针以10分钟间隔浸渍8次。其后,在室温下干燥48小时,由此形成交联的保护膜,得到探针h。将上述保护膜的形成条件汇总于表5。
<探针特性的测定>
[葡萄糖响应特性]
对于探针h的葡萄糖响应特性,与实施例1同样地进行测定。
在葡萄糖浓度0~500mg/dl的范围中显示出高的线性,葡萄糖响应性良好。将结果示于图15,汇总于表6。
[耐久性]
对于探针h的耐久性,与实施例1同样地进行测定。
保存后第7日的响应特性在葡萄糖浓度0~500mg/dl的范围中显示出高的线性,与第0日相比几乎没有变化,耐久性良好。将结果示于图16,汇总于表6。
[实施例9]
在保护膜的形成中,变更保护膜用聚合物,除此以外,与实施例8同样地进行,制作探针。
更具体而言,在实施例8中,代替式(6)所示的聚(4-乙烯基吡啶)-嵌段-聚(甲基丙烯酸2,2-二甲基乙酯)[嵌段共聚物(6)],使用式(7)所示的聚(4-乙烯基吡啶)-嵌段-聚(甲基丙烯酸正丁酯)(mw/mn=1.3;w”=6.0-g-4.5×103)[嵌段共聚物(7)],除此以外,与实施例8同样地形成保护膜,得到探针i。将上述保护膜的形成条件汇总于表5。
<探针特性的测定>
[葡萄糖响应特性]
对于探针i的葡萄糖响应特性,与实施例1同样地进行测定。
在葡萄糖浓度0~500mg/dl的范围中显示出高的线性,葡萄糖响应性良好。将结果示于图15,汇总于表6。
[耐久性]
对于探针i的耐久性,与实施例1同样地进行测定。
保存后第7日的响应特性在葡萄糖浓度0~500mg/dl的范围中维持线性,耐久性良好。将结果示于图16,汇总于表6。
[实施例10]
在保护膜的形成中,变更保护膜用聚合物,除此以外,与实施例8同样地进行,制作探针。
更具体而言,实施例8中,代替式(6)所示的聚(4-乙烯基吡啶)-嵌段-聚(甲基丙烯酸2,2-二甲基乙酯)[嵌段共聚物(6)],使用式(9)所示的聚(4-乙烯基吡啶-无规-甲基丙烯酸2-羟基乙酯)[无规共聚物(9)],除此以外,与实施例8同样地形成保护膜,得到探针j。将上述保护膜的形成条件汇总于表5。
<探针特性的测定>
[葡萄糖响应特性]
对于探针j的葡萄糖响应特性,与实施例1同样地进行测定。
在葡萄糖浓度0~500mg/dl的范围中显示出高的线性,葡萄糖响应性良好。将结果示于图15,汇总于表6。
[耐久性]
对于探针k的耐久性,与实施例1同样地进行测定。
保存后第7日的响应特性在葡萄糖浓度0~500mg/dl的范围中维持线性,耐久性良好。将结果示于图16,汇总于表6。
[比较例1]
在保护膜的形成中,变更保护膜用聚合物,增加在交联剂溶液中的浸渍次数,除此以外,与实施例1同样地进行,制作探针。
更具体而言,在将300mg式(4)所示的聚(苯乙烯-无规-4-乙烯基吡啶-无规-甲基丙烯酸丙二醇酯)(mw/mn=1.8,m=2)[无规共聚物(4)]和300mg聚(4-乙烯基吡啶)(mw=160,000)[p4vp]、47mg作为交联剂的聚乙二醇二缩水甘油醚(pegdge)(mn=1000)溶于1ml溶剂(乙醇95%、4-(2-羟基乙基)-1-哌嗪乙磺酸(hepes)缓冲液(10mm,ph8)5%)而得到的溶液中,将上述制造的探针以10分钟间隔浸渍9次。其后,在室温下干燥48小时,由此形成交联的保护膜,得到探针k。将上述保护膜的形成条件汇总于表7。
<探针特性的测定>
[葡萄糖响应特性]
对于探针k的葡萄糖响应特性,与实施例1同样地进行测定。
在葡萄糖浓度0~500mg/dl的范围中显示出高的线性,葡萄糖响应性良好。将结果示于图17,汇总于表8。
[耐久性]
对于探针k的耐久性,与实施例1同样地进行测定。
保存后第7日的响应特性在葡萄糖浓度超过100mg/dl时降低至48%,耐久性不良。将结果示于图18,汇总于表8。
[比较例2]
在保护膜的形成中,变更保护膜用聚合物,增加在交联剂溶液中的浸渍次数,除此以外,与实施例1同样地进行,制作探针。
更具体而言,在将300mg式(5)所示的聚(苯乙烯-无规-4-乙烯基吡啶-无规-甲基丙烯酸丙二醇酯)(mw/mn=1.6,m=约16)[无规共聚物(5)]和300mg聚(4-乙烯基吡啶)(mw=160,000)[p4vp]、47mg作为交联剂的聚乙二醇二缩水甘油醚(pegdge)(mn=1000)溶于1ml溶剂(乙醇95%、4-(2-羟基乙基)-1-哌嗪乙磺酸(hepes)缓冲液(10mm,ph8)5%)而得到的溶液中,将上述制造的探针以10分钟间隔浸渍9次。其后,在室温下干燥48小时,由此形成交联的保护膜,得到探针l。将上述保护膜的形成条件汇总于表7。
<探针特性的测定>
[葡萄糖响应特性]
对于探针l的葡萄糖响应特性,与实施例1同样地进行测定。
在葡萄糖浓度0~500mg/dl的范围中显示出高的线性,葡萄糖响应性良好。将结果示于图17,汇总于表8。
[耐久性]
对于探针l的耐久性,与实施例1同样地进行测定。
保存后第7日的响应特性在葡萄糖浓度超过100mg/dl时降低至36%,耐久性不良。将结果示于图18,汇总于表8。
[比较例3]
在保护膜的形成中,变更保护膜用聚合物,增加交联剂的量,增加在交联剂溶液中的浸渍次数,除此以外,与实施例1同样地进行,制作探针。
更具体而言,在将800mg聚(4-乙烯基吡啶)(mw=160,000)[p4vp]、62mg作为交联剂的聚乙二醇二缩水甘油醚(pegdge)(mn=1000)溶于1ml溶剂(乙醇95%、4-(2-羟基乙基)-1-哌嗪乙磺酸(hepes)缓冲液(10mm,ph8)5%)而得到的溶液中,将上述制造的探针以10分钟间隔浸渍9次。其后,在室温下干燥48小时,由此形成交联的保护膜,得到探针m。将上述保护膜的形成条件汇总于表7。
<探针特性的测定>
[葡萄糖响应特性]
对于探针m的葡萄糖响应特性,与实施例1同样地进行测定。
在葡萄糖浓度0~500mg/dl的范围中显示出高的线性,葡萄糖响应性良好。将结果示于图17,汇总于表8。
[耐久性]
对于探针m的耐久性,与实施例1同样地进行测定。
保存后第7日的响应特性在葡萄糖浓度超过100mg/dl时降低至22%,耐久性不良。将结果示于图18,汇总于表8。
[参考例1]
在保护膜的形成中,变更保护膜用聚合物,增加交联剂的量,增加在交联剂溶液中的浸渍次数,除此以外,与实施例1同样地进行,制作探针。
更具体而言,将800mg式(7)所示的聚(4-乙烯基吡啶)-嵌段-聚(甲基丙烯酸正丁酯)(mw/mn=1.3;w”=6.0-g-4.5×103)[嵌段共聚物(7)]、62mg作为交联剂的聚乙二醇二缩水甘油醚(pegdge)(mn=1000)溶于1ml溶剂(乙醇95%、4-(2-羟基乙基)-1-哌嗪乙磺酸(hepes)缓冲液(10mm,ph8)5%)而得到的溶液中,将上述制造的探针以10分钟间隔浸渍12次。其后,在室温下干燥48小时,由此形成交联的保护膜,得到探针n。将上述保护膜的形成条件汇总于表9。
<探针特性的测定>
[葡萄糖响应特性]
对于探针n的葡萄糖响应特性,与实施例1同样地进行测定。
在葡萄糖浓度0~500mg/dl的范围中显示出高的线性,葡萄糖响应性良好。将结果示于图19,汇总于表10。
[耐久性]
对于探针n的耐久性,与实施例1同样地进行测定。
保存后第7日的响应特性在葡萄糖浓度超过200mg/dl时降低至46%,耐久性不良。将结果示于图20,汇总于表10。
[参考例2]
在保护膜的形成中,变更保护膜用聚合物,增加交联剂的量,除此以外,与实施例1同样地进行,制作探针。
更具体而言,在将800mg式(8)所示的聚(4-乙烯基吡啶-无规-甲基丙烯酸2-羟基乙酯)[无规共聚物(8)]、62mg作为交联剂的聚乙二醇二缩水甘油醚(pegdge)(mn=1000)溶于1ml溶剂(乙醇95%、4-(2-羟基乙基)-1-哌嗪乙磺酸(hepes)缓冲液(10mm,ph8)5%)而得到的溶液中,将上述制造的探针以10分钟间隔浸渍8次。其后,在室温下干燥48小时,由此形成交联的保护膜,得到探针o。将上述保护膜的形成条件汇总于表9。
<探针特性的测定>
[葡萄糖响应特性]
对于探针o的葡萄糖响应特性,与实施例1同样地进行测定。
在葡萄糖浓度0~500mg/dl的范围中显示出高的线性,葡萄糖响应性良好。将结果示于图19,汇总于表10。
[耐久性]
对于探针o的耐久性,与实施例1同样地进行测定。
保存后第7日的响应特性在葡萄糖浓度超过200mg/dl时降低至25%,耐久性不良。将结果示于图20,汇总于表10。
[参考例3]
在保护膜的形成中,变更保护膜用聚合物,增加交联剂的量,除此以外,与实施例1同样地进行,制作探针。
更具体而言,在将800mg式(9)所示的聚(4-乙烯基吡啶-无规-甲基丙烯酸2-羟基乙酯)[无规共聚物(9)]、62mg作为交联剂的聚乙二醇二缩水甘油醚(pegdge)(mn=1000)溶于1ml溶剂(乙醇95%、4-(2-羟基乙基)-1-哌嗪乙磺酸(hepes)缓冲液(10mm,ph8)5%)而得到的溶液中,将上述制造的探针以10分钟间隔浸渍8次。其后,在室温下干燥48小时,由此形成交联的保护膜,得到探针p。将上述保护膜的形成条件汇总于表9。
<探针特性的测定>
[葡萄糖响应特性]
对于探针p的葡萄糖响应特性,与实施例1同样地进行测定。
在葡萄糖浓度0~500mg/dl的范围中显示出高的线性,葡萄糖响应性良好。将结果示于图19,汇总于表10。
[耐久性]
对于探针p的耐久性,与实施例1同样地进行测定。
保存后第7日的响应特性在葡萄糖浓度超过200mg/dl时降低至32%,耐久性不良。将结果示于图20,汇总于表10。
[参考例4]
在保护膜的形成中,变更保护膜用聚合物,增加交联剂的量,除此以外,与实施例1同样地进行,制作探针。
更具体而言,在将400mg式(8)所示的聚(4-乙烯基吡啶-无规-甲基丙烯酸2-羟基乙酯)[无规共聚物(8)]和400mg式(9)所示的聚(4-乙烯基吡啶-无规-甲基丙烯酸2-羟基乙酯)[无规共聚物(9)]、62mg作为交联剂的聚乙二醇二缩水甘油醚(pegdge)(mn=1000)溶于1ml溶剂(乙醇95%、4-(2-羟基乙基)-1-哌嗪乙磺酸(hepes)缓冲液(10mm,ph8)5%)而得到的溶液中,将上述制造的探针以10分钟间隔浸渍8次。其后,在室温下干燥48小时,由此形成交联的保护膜,得到探针q。将上述保护膜的形成条件汇总于表9。
<探针特性的测定>
[葡萄糖响应特性]
对于探针q的葡萄糖响应特性,与实施例1同样地进行测定。
在葡萄糖浓度0~500mg/dl的范围中显示出高的线性,葡萄糖响应性良好。将结果示于图19,汇总于表10。
[耐久性]
对于探针q的耐久性,与实施例1同样地进行测定。
保存后第7日的响应特性在葡萄糖浓度超过200mg/dl时降低至30%,耐久性不良。将结果示于图20,汇总于表10。
[表1]
[表2]
[表3]
[表4]
[表5]
[表6]
[表7]
[表8]
[表9]
[表10]
可确认,如果将使用了本公开的聚合物混合物的保护膜用于探针的感应部分,则葡萄糖响应性良好,且与以往的聚合物相比,耐久性提高。
产业上的可利用性
本公开的具备至少包含检测体响应性酶和氧化还原介体的检测层、以及在上述检测层上形成的保护膜的膜结构体在埋入型生物传感器的探针中是有用的。
附图标记说明
1:埋入型生物传感器;
10:主体;
11:探针;
111:绝缘性基板;
112:导电性薄膜;
112a:工作电极引线;
112b:参比电极引线;
112c:对电极引线;
113:槽;
114:工作电极;
115:参比电极;
116:绝缘性抗蚀膜;
117:对电极;
118:检测层;
119:保护膜;
2:生物体;
3:信息通信设备。
- 还没有人留言评论。精彩留言会获得点赞!