用于治疗敏感性皮肤的提取物和含有该提取物的皮肤病学组合物的制作方法
[0001]
本发明涉及新的细菌提取物,其可用于保护和/或治疗敏感性皮肤和/或反应性不耐受性皮肤,特别是通过在皮肤神经源性炎症上的靶向作用。本发明还涉及含有这种细菌提取物作为活性成分的化妆品或皮肤病学组合物。
背景技术:
[0002]
表皮是一种多层次上皮,可作为免于其环境和伤害的保护屏障。在其多种生理功能中,表皮具有构成免于微生物入侵机体的生物、物理和化学屏障的功能。表皮的这种物理屏障特性特别是与其结构有关。例如,表皮通常分为基底层,其由构成表皮生发层的角质形成细胞组成,所谓的棘突层由几层多面体细胞组成,最后是一组上层称为角质层(或角化层),由分化末期的角质形成细胞(称为角质细胞)组成。表皮的化学屏障特性尤其取决于许多抗微生物肽在表皮表面的释放。在表皮细胞结构组织的功能障碍、或表皮化学屏障功能的缺陷可导致皮肤的炎症状态。
[0003]
炎症是机体对以下几种类型侵袭的正常免疫防御反应:传染性、热性、机械性、化学性、病变性或过敏性。其特征在于四点:发红、发热、肿胀和疼痛。急性皮肤炎症是对有害物质的立即反应,持续时间短(几天或几周),通常是突然发作并且特征在于剧烈肿胀。急性炎症可自发痊愈或经治疗痊愈。当炎症无法自愈,持续或恶化达数月甚至数年时,发生慢性病。炎症反应是一个动态过程,涉及几个连续的步骤:血管(血管舒张)、白细胞外渗和免疫细胞趋化作用以及最后进行清理。白细胞外渗是指循环的免疫细胞、淋巴细胞、嗜中性粒细胞和单核细胞活跃地穿过血管壁以及在病变部位的积累。中性粒细胞具有通过趋化作用吸引其他炎性细胞的功能,并具有通过分泌抗微生物的物质和蛋白酶来清理受伤部位的功能。单核细胞通过趋化性迁移并分化为巨噬细胞,从而清理受损区域。它们分泌生长因子、炎性细胞因子(例如,il-1,特别是il-1β、tnfα)、蛋白酶、前列腺素和ifn,从而允许炎症的维持和/或放大。在血管阶段之后是清理过程,与白细胞渗出同步。这是去除坏死组织和病原体的过程。
[0004]
皮肤神经源性炎症定义为神经末梢的原发性炎症过程的诱导和/或放大,因此其是通过激活分泌神经肽(如p物质)的表皮内神经纤维诱导的皮肤炎症。皮肤神经源性炎症具体涉及敏感性皮肤,反应性不耐受性皮肤和瘙痒性炎症性皮肤病。瘙痒(le prurit)定义为导致需要抓挠的不适感。最近,出现了瘙痒受体(de pruriceptor)的概念,其是感知瘙痒的特异性受体,但是它们与伤害受体(nociceptifs)家族的区别仍在争论中。这些瘙痒受体使用表皮内的ao-纤维,尤其是c-纤维。他们分泌神经肽:p物质、降钙素基因相关肽(cgrp)和血管活性肠肽(vip)。最近,已经清楚地确定蛋白酶(胰蛋白酶、组织蛋白酶g、凝血酶等)在诱发瘙痒中的作用。实际上,蛋白酶激活的受体2(par-2)已被定义为瘙痒激活的第二个主要途径(misery等,nat.rev.neurol 10,408-416,2014)。
[0005]
皮内神经纤维与皮肤细胞以及内分泌、淋巴和免疫系统的细胞直接或间接相互作
用。这些交流导致了神经-免疫-皮肤-内分泌系统的定义。为了发挥作用,该系统需要使用由不同性质的分子、神经递质、细胞因子和生长因子组成的通用语言。这些分子是由皮肤细胞、驻留和募集的免疫细胞、以及表皮内神经末梢合成和释放的。表皮和真皮细胞还可以产生神经递质、酶、神经营养蛋白、细胞因子、趋化因子和生长因子。这些介质调节皮肤神经支配和炎症反应。在炎症的情况下,通过感觉神经末梢和皮肤细胞分泌的这些介质的作用,可以激活在皮肤中转运或组成性存在的免疫细胞。该过程导致细胞因子和神经递质的第二波释放,其产生炎症的放大循环。
[0006]
最近出现了一个新的概念,表明角质形成细胞也是皮肤神经源性炎症的主要参与者。
[0007]
由神经肽产生的皮肤神经源性炎症与敏感性皮肤以及不耐受性皮肤的反应性有关。敏感性皮肤的概念反映了每个人皮肤的敏感性水平。尽管可能在任何年龄都有敏感性皮肤,但这在婴儿和老年人中极为常见。婴儿的皮肤大约是成人皮肤厚度的五分之一,因此对化学、物理和微生物损害以及紫外线极为敏感。成年皮肤的屏障功能会随着年龄,因新陈代谢的减慢而逐渐减弱。随着皮肤老化,其逐渐变得缺乏脂质,这使其更容易被诸如肥皂之类的碱性物质刺激。
[0008]
当皮肤具有非常低的敏感性阈值时,即,它对最小的外部刺激反应过度,这被称为不耐受性皮肤、或反应性不耐受性皮肤。不耐受性皮肤更容易受到外界伤害,其特征在于每天不舒服和高度应激性。一些或多或少带有标记的特征,使人们可以识别它。例如,脸部不耐受性皮肤是红色和有刺痛的。它会紧绷、发热或发痒。它也会引起灼烧感。不耐受性皮肤通常是变应性的,因此对美容护理产品的成分特别敏感。
[0009]
敏感性皮肤实际上是容易出现刺痛、过热、发麻和瘙痒、有时伴随发红的皮肤。这些不适感在响应刺激时而加剧,而这些刺激对正常皮肤并不会引起击惹。皮肤的这种超敏反应是由于其耐受性阈值降低所致。皮肤越敏感,其耐受阈值越低,当耐受阈值处于最低值时,这称为不耐受性皮肤。这种超敏反应可以通过多种因素来解释:
[0010]-与化学刺激物,如某些肥皂、家用洗涤剂或污染接触时会发生的炎症反应;触发这些物质的阈值,从而引起敏感或不耐受性皮肤。
[0011]-改变表皮屏障功能。然后,这种现象会促进皮肤脱水,尤其是潜在刺激物的渗透。
[0012]-心理因素,例如压力;
[0013]-激素因素;
[0014]-物理因素,例如阳光、温度变化(热/冷)、风、空调、暖气、硬水。
[0015]
皮肤覆盖有一层保护膜,称为表面亲脂膜。该膜是最外层的屏障,也是最脆弱、最易受干扰和最能代表皮肤健康的屏障;它主要由以下组成:皮脂腺分泌的脂肪物质、和角质细胞角质化阶段细胞降解产生的脂质、以及亲水性化合物,如汗水、甘油、尿素、天然保湿因子、盐、皮肤菌群的代谢产物等。该表面膜高度暴露,并且对环境压力、卫生习惯和皮肤状况敏感。保持甚至改善这种屏障功能,尤其是对于最敏感的皮肤非常重要。并且,虽然众所周知,皮肤屏障变弱的不耐受性皮肤的人群需要使用生理类似的脂质剂进行护理,尤其是润肤剂和生理保湿剂,但同样重要的是避免使皮肤接触任何可能降解表面亲脂膜的物质,例如表面活性成分或防腐剂。
[0016]
敏感或不耐受性皮肤是一种非过敏性机制,涉及炎症反应而未识别出特异性过敏
原。
[0017]
皮肤高反应性的病理生理机制尚未明确阐明,但有一种趋势鉴别出两种可能起作用的因素。一方面,通过水分流失和角质细胞间脂质的改变,皮肤屏障改变。皮肤对外部(甚至是极小的)刺激物和刺激和击惹变得更加敏感,导致炎性细胞因子和来自花生四烯酸级联反应的化合物释放。另一方面,神经系统疾病可能与皮肤的敏感性和反应性有关。到达表皮细胞的神经纤维,在外部刺激的作用下产生引起神经源性炎症即皮肤神经源性炎症的神经递质(例如物质p)。
[0018]
因此,需要一种组合物,其能够治疗、预防和保护敏感性皮肤、不耐受性皮肤,其炎性成分是神经源性炎症。
[0019]
本发明的目的是满足这些需求,换句话说,提出一种组合物,其通过减少或抑制皮肤神经源性炎症来保护和/或改善敏感性皮肤或不耐受性皮肤的状况。
[0020]
申请人首次证明了从地下水中分离出的细菌菌株(或细菌)lmb64衍生的细菌提取物在组织再生和皮肤损伤愈合中的有益特性。申请人在专利申请wo2012/085182中描述了这种细菌。更具体地,描述并例举说明称为s0、e0和es0的提取物,所述提取物分别由以下组成:从生物质分离的培养上清液、裂解细胞的生物质、以及将培养物在碱性ph下孵育数小时后的上清液。测试级分e0和es0,结果表明这些提取物e0和es0具有以下能力:诱导细胞因子和朗格汉斯细胞(对于e0)成熟、以及激活tlr2/tlr4/tlr5受体、拮抗par和诱导抗微生物肽(对于es0)。这些结果使得可以考虑将此类提取物用于治疗炎性疾病,例如瘙痒、牛皮癣、湿疹或特应性皮炎。
技术实现要素:
[0021]
发明人出人意料地表明特定新型细菌提取物在预防和/或治疗皮肤神经源性炎症中的效果。
[0022]
实际上,发明人已经证明该细菌提取物对由物质p诱导角质形成细胞释放的il-1β和tnf-α具有抑制作用。
具体实施方式
[0023]
根据第一个实施方案,本发明的目的是根据本发明的细菌提取物及其在预防和/或治疗皮肤神经源性炎症中的用途。
[0024]
特别地,预防和/或治疗皮肤神经源性炎症,包括保护和/或治疗敏感性皮肤或不耐受性皮肤,或由其组成。
[0025]
特别地,预防和/或治疗皮肤神经源性炎症包括保护和/或治疗敏感性皮肤,或由其组成。
[0026]
特别地,预防和/或治疗皮肤神经性源性炎症包括保护和/或治疗不耐受性皮肤,或由其组成。
[0027]
细菌lmb64已被表征和定义为属于β-变形杆菌纲,奈瑟氏菌(neisseriaceae)亚科,并且可能属于尚未定义的新属。分析编码16s核糖体arn(arnr)的基因序列,有可能将该细菌定位在靠近色杆菌属(chromobacterium)、paludimonas、lutelia和glubenkania属的地方,与其共享95%的序列相似性。这种非致病性细菌是革兰氏阴性细菌,已经从地下水中
分离。更具体地,细菌lmb64是棒状的,长度约为2.3μm
±
0.3μm、宽度约为1.0μm
±
0.1μm。该细菌的具体特征是极鞭毛的存在。
[0028]
编码16s arnr的基因几乎已完全测序(1487bp,对应于序列seq id no.1)。细菌lmb64具有10948bp的环状质粒。该质粒已完全测序,序列显示在seq id no:2中。
[0029]
根据另一个实施方案,从其获得根据本发明的细菌提取物的细菌包含至少一个质粒,其包含序列seq id no:2,或与序列seq id no:2具有至少80%同一性,有利地与序列seq id no:2具有至少85%、至少90%、至少95%、或至少97%,以及更优选至少98%同一性的任何序列。
[0030]
同样,从其获得根据本发明的细菌提取物的细菌是非致病性革兰氏阴性菌,其属于β变形杆菌纲、奈瑟氏菌亚科,所述细菌包含16s arnr,其包含序列seq id no:1,或与序列seq id no:1具有至少80%、或至少90%、或至少95%、或至少97%同一性的任何序列,以及所述细菌包含至少一个质粒,其含有seq id no:2、或与序列seq id no:2具有至少80%同一性,有利地与序列seq id no:2具有至少85%、至少90%、至少95%、或至少97%,以及更优选至少98%同一性的任何序列。
[0031]
举例来说,这种细菌以菌株lmb64表示,该菌株以申请人的名义于2010年4月8日保藏在巴黎巴斯德研究所国家微生物保藏中心(cncm),保藏号i-4290。
[0032]
有了这种基因型信息,再加上有关无硫介质中生长的特征、该细菌的非丝状性质,本领域技术人员将不难发现/鉴定另一种能够获得本发明的细菌提取物的细菌。可以在完全能克服的选择过程之后进行这样另一种细菌的鉴定,可以在基因型上稍有不同,但就细菌提取物而言符合本发明的表型标准,而且这是基于本申请中包含的以及在申请wo2012/085182中包含的信息,结合本领域技术人员的常识。
[0033]
在本发明的上下文中,两个核酸序列之间的“百分比同一性”是指在最好比对(最佳比对,该百分比纯粹是统计学上的,并且这两个序列之间的差异随机分布并在整个长度上)后获得的两个待比较序列之间的相同核苷酸的百分比。两个核酸序列之间的序列比较通常在以最佳比对进行之后通过比较这些序列来进行,其中所述比较可以按区段或按“比较窗”进行。除手动外,还可以借助smith和waterman的局部同源性算法(1981)[ad.app.math.2:482]、借助needleman和wunsch的局部同源性算法(1970)[j.mol.biol.48:443]、借助pearson和lipman的相似性检索方法(1988)[proc.natl.acad.sci.usa 85:2444]、或借助使用这些算法的计算机软件(威斯康星州遗传学软件包,遗传学计算机组,575science dr.,madison,wi中的gap、bestfit、fasta和tfasta,或blast n或blast p比较软件)可以实现比较这些序列的最佳比对。
[0034]
通过比较以最佳方式比对的这两个序列来确定两个核酸序列之间的百分比同一性,其中相对于用于两个序列之间最佳比对的参考序列,待比较的核酸序列可以包括添加或缺失。为计算百分比同一性,通过确定两个序列之间核苷酸相同的位置数,用该相同位置的数除以比较窗口中的位置总数,并将所得结果乘以100,以得到这两个序列之间的百分比同一性。
[0035]
例如,可以使用blast程序,特别是“blast 2序列”(tatusova等人,“blast 2序列-一种比较蛋白质和核苷酸序列的新工具”,fems microbiol lett.174:247-250),在网站http://www.ncbi.nlm.nih.gov/gorf/bl2.html上是可获得的,使用默认参数(特别是对于
参数“开放空位罚分”:5和“延伸空位罚分”:2;其中选定矩阵为例如程序建议的矩阵“blosum 62”)。通过程序直接计算待比较的两个序列之间的百分比同一性。也可以使用其他程序,如“align”或“megalign”软件(dnastar)。
[0036]
根据本发明的细菌,特别是细菌lmb64,其包含至少一个质粒,所述质粒包含序列seq id no.2,或与所述序列seq id no.2具有至少80%、优选85%、90%、95%和98%同一性的任何序列。所述细菌,特别是细菌lmb64的其他特征将在下面的实施例中详述。
[0037]
通常,术语“根据本发明的细菌提取物”用于描述包含存在于细菌的胞质中的可溶性化合物的集合,从发酵介质中分离细菌细胞之后获得,其裂解、特别是冻融,重悬在水性溶剂中并回收包含以下成分的液体级分:胞质成分、可溶性细胞内细胞化合物、可溶性膜化合物/分子、可溶性跨膜化合物/分子、可溶性周质化合物/分子和可溶性鞭毛化合物/分子,特别是蛋白质。
[0038]
表达“可溶性膜化合物/分子、可溶性跨膜化合物/分子、可溶性周质化合物/分子和可溶性鞭毛化合物/分子”是指细胞质或细胞周质间隙、膜或跨膜空间、或在鞭毛上所含的蛋白质和其他可溶性化合物,并通过本发明细菌的裂解而释放。这些蛋白质和化合物是通过根据本发明的方法获得的,换句话说,从发酵介质中分离出该细胞质之后,在裂解的细菌的细胞质上进行液/固分离(例如通过冷冻-解冻)之后,回收液相。这些可溶的胞质、膜、周质和/或鞭毛细胞内蛋白或化合物包括,例如,核糖体、与细胞代谢相关的酶、脂多糖、糖、脂蛋白、膜和周质,它们通过裂解而释放并溶于水或水性溶剂中。
[0039]
细菌通过二元裂变繁殖,这意味着每个细菌生长,然后分裂为被细胞壁形成的分隔隔膜分隔开两个子细胞。在分裂过程中,adn复制自身和其它成分。各种合成和降解的酶系统参与细胞分裂。
[0040]
细菌生长是细菌所有成分的有序增长。它导致细菌数量增加。在生长过程中,培养介质中的营养物质耗尽,并且富含细菌分泌和排泄在培养介质中的生物分子,并溶解在该介质以及代谢副产物中。
[0041]
表述“培养介质”是指至少包含细菌生长和增殖所必需的营养物的任何介质。细菌可以在液体、固体或半液体介质中生长。优选地,培养介质是允许生物质生长和回收并允许产生根据本发明的细菌提取物的液体介质。
[0042]
适当的培养介质应包含促进细菌生长和繁殖的营养物质。通常,合适的生长介质可以包括水、碳源、氮源和盐。
[0043]
可以提及“发酵介质”或细菌培养物,其对应于在其生长和发育结束时含有细菌的培养介质。
[0044]
在实践中,根据本发明的细菌提取物,特别是细菌lmb64的提取物,可以从根据本发明的细菌在允许所述细菌生长、发育和繁殖的培养介质中的培养物中获得,从液相中分离出细胞,例如离心后、以沉淀或生物质的形式分离出细胞之后回收细胞。对该生物质进行处理,例如通过冻融,以渗透和降解细胞膜和壁。根据本发明的提取物可以通过以下获得:将处理过的生物质,特别是融化的生物质与碱性缓冲液混合,然后进行混合物的固/液分离,例如通过离心。由此获得代表根据本发明的提取物的水相。
[0045]
可以通过任何液/固分离方式从发酵介质中回收生物质。因此,更具体地,可以使用本领域技术人员已知的技术,从含有培养介质残留溶质和细菌排泄并溶解在发酵介质中
的生物分子的液体级分中,分离主要含有全细胞、含表面蛋白的细胞碎片、和/或位于细菌周质间隙的蛋白质的细胞生物质。
[0046]
作为说明,可以通过选自以下的技术进行液/固分离:离心、沉降、过滤、超滤、倾析(la d
é
cantation)。
[0047]
优选地,通过离心包含细菌培养物的发酵介质进行液/固分离,一方面,以便分离固相,即包含细胞和细胞碎片的生物质沉淀物,另一方面,以便分离液相,即上清,其包含发酵过程中排出的可溶性分子和未被细菌消耗的培养介质的残留化合物。
[0048]
固相,即获得的生物质,特别是离心沉淀物,经历导致细胞膜破裂的步骤,例如冷冻、然后解冻。
[0049]
可在任何负温度下进行冷冻使水固化,形成细胞内和膜间晶体,从而使膜至少部分破裂。
[0050]
特别地,可以在-10℃、或-20℃、或-30℃、-40℃、-50℃、-60℃或约-80℃的温度进行冷冻。优选地,在约-20℃进行冷冻。
[0051]
冻结时间和速度本身并不重要。冻结时间可取决于温度,例如,一到几小时的时间段是合适的。即使没有必要,冷冻的固相也可以存储几天、几周或几个月。
[0052]
冷冻或解冻的速率也不是关键的,并且将寻求条件以允许改变细菌壁和膜。
[0053]
术语“解冻”是指回到允许冰晶融化的正温度。
[0054]
壁和膜的透化和破裂的步骤也可以通过化学、超声或机械手段,例如去污剂、离液剂、玻璃珠来进行。
[0055]
该步骤允许释放可溶性细胞质细胞内化合物,因此存在于裂解或受损细胞的固相中。
[0056]
然后,将水性溶剂形式的液相加入该固相中,以重悬裂解或受损的细胞,并提取可溶于所述溶剂的细胞质可溶性化合物。
[0057]
水性溶剂优选是缓冲液,特别是碱性缓冲液。优选地,该碱性缓冲液是tris缓冲液或精氨酸缓冲液或tris-精氨酸缓冲液。优选地,其是精氨酸缓冲液。精氨酸浓度可以包含在0.1至1m之间,特别是在0.3至0.5m之间。tris浓度可以包含在1至100mm之间,特别是20mm。碱性缓冲液的ph可以在8至12之间,优选在9至11之间。
[0058]
该重悬浮步骤允许提取包含在裂解或受损细胞的生物质中的细胞质可溶性化合物。
[0059]
最后,进行液/固分离以回收包含可溶性细胞质细胞内化合物的液态水相,特别是缓冲的液态水相。
[0060]
由此获得的该液相代表根据本发明的提取物。
[0061]
用于重悬浮步骤的固相/水性液相的比例可以包含在1至10%w/v之间。
[0062]
使用碱性缓冲液可以使外膜更具渗透性,并促进分子从周质间隙扩散到液体介质中。使用碱性缓冲液使其可能稳定化合物,特别是可溶性蛋白质,并防止它们在较长的存储时间内聚集,以及防止它们因蛋白酶作用而降解。
[0063]
可进行一个或多个过滤步骤以澄清提取物并得到根据本发明的纯化提取物。
[0064]
可通过任何允许澄清液相、或澄清缓冲液相的合适方法进行过滤。通过过滤进行的这种澄清,使得能够去除在第二液/固分离步骤中没有去除的悬浮颗粒,并且目的在于产
生根据本发明的纯化的、澄清的细菌提取物。
[0065]
可以通过过滤、超滤或渗滤的任何方式进行过滤。
[0066]
有利地,过滤通过在截留值为0.4μm、优选0.2μm的过滤器或滤芯式过滤器上过滤来进行。在这种情况下,细菌提取物的特征在于,细菌提取物中存在的化合物的尺寸小于或等于0.2μm。
[0067]
优选地,可以使用不带静电电荷的过滤器或预过滤器,以避免吸收任何负责全部或部分提取物活性的生物分子。
[0068]
在实施例中将更详细地描述不同的步骤。必须理解,对于本说明书有关领域的技术人员来说显而易见的对过程、介质或步骤顺序的任何修改,都必须被认为落入本发明的范围内。
[0069]
根据一个实施方案,根据本发明的方法包括制备根据本发明的细菌提取物的方法,所述方法包括以下步骤:
[0070]
a)在合适的介质中培养根据本发明的细菌,特别是lmb64,以获得细菌培养物;
[0071]
b)所述培养物的液/固分离和去除液相;
[0072]
c)将固相的细胞裂解、
[0073]
d)将裂解的固相重悬于水性液相中,优选缓冲的水性液相,
[0074]
e)液/固分离并回收液相,
[0075]
f)可选地,过滤液相。
[0076]
在一个优选的实施方案中,固相细胞裂解的步骤c)通过冷冻接着解冻来进行。
[0077]
根据一个具体的实施方案,该细菌是非致病性革兰氏阴性细菌,属于β变形杆菌纲的奈瑟氏菌亚科,其包含16s arnr,所述16s arnr含有序列seq id no:1、或与序列seq id no:1具有至少80%同一性的任何序列,更具体地,其是细菌lmb64。
[0078]
优选地,该细菌包含至少一种质粒,其包含序列seq id no:2、或与序列seq id no:2具有至少80%同一性的任何序列。
[0079]
根据一个实施方案,本发明涉及通过如上所述的根据本发明的方法获得的、或可获得的细菌提取物。
[0080]
在一个实施方案中,本发明涉及根据本发明的细菌提取物,特别是通过根据本发明的方法获得或可获得的提取物,其用于预防、治疗、预防和治疗皮肤神经源性炎症。
[0081]
有利地,皮肤神经源性炎症包括敏感性皮肤和/或不耐受性皮肤。
[0082]
根据另一个实施方案,本发明涉及化妆品或皮肤病学组合物,其包含至少一种根据本发明的细菌提取物,以及至少一种化妆品或皮肤病学可接受的赋形剂,用于预防、治疗、预防和治疗皮肤神经源性炎症。
[0083]
根据另一个实施方案,本发明涉及化妆品或皮肤病学组合物用于保护和/或治疗敏感或不耐受性皮肤的用途,所述化妆品或皮肤病学组合物包含至少一种根据本发明的细菌提取物,以及至少一种化妆品或皮肤病学可接受的赋形剂。特别地,这是敏感或不耐受性皮肤,其起源是皮肤神经源性炎症。
[0084]
本发明还涉及一种化妆品或皮肤病学组合物在制备用于预防、治疗、预防和治疗皮肤神经源性炎症的医药产品中的用途,所述化妆品或皮肤病学组合物包含至少一种根据本发明的细菌提取物、和至少一种化妆品或皮肤病学可接受的赋形剂。
[0085]
本发明还涉及一种用于预防和/或治疗皮肤神经源性炎症的方法,所述方法包括向有需要的个体施用有效量的化妆品或皮肤病学组合物,所述化妆品或皮肤病学组合物包含至少一种根据本发明的细菌提取物,以及至少一种化妆品或皮肤病学的可接受的赋形剂。
[0086]
有利地,皮肤神经源性炎症包括敏感性皮肤和/或不耐受性皮肤。
[0087]
在本发明中,“化妆品或皮肤病学可接受的”是指用于制备化妆品或皮肤病学的组合物,所述组合物通常是安全的、无毒的并且在生物学上或其他方面都不是不期望的,并且对于化妆品或皮肤病学的用途,特别是通过局部施用是可接受的。
[0088]
根据一个具体的实施方案,根据本发明的组合物为适合局部施用的形式。
[0089]
根据本发明的化妆品或皮肤病学组合物可以是通常用于局部施用的形式,即洗剂、泡沫、凝胶、分散体、乳剂、喷剂、精华、膜(masques)或乳膏、凝胶剂、尤其是胶束(micellar)凝胶剂、以及特别是允许皮肤渗透以改善有效成分的性质和可及性的赋形剂。有利地,其将是乳霜、浓乳霜、洗剂、眼睛护理产品、uv护理产品。
[0090]
除了根据本发明的细菌提取物的化合物之外,这些组合物通常还包含生理学可接受的介质,其通常基于水或溶剂(例如醇、醚或二醇)。它们还可包含表面活性成分、络合剂、防腐剂、稳定剂、乳化剂、增稠剂、胶凝剂、湿润剂、润滑剂、微量元素、精油、香料、染料、消光剂、化学或矿物过滤器、保湿剂、热水等。
[0091]
有利地,根据本发明的组合物将包含基于组合物总重量的0.05至10wt%、优选0.1至5wt%、更优选0.5至3wt%的本发明细菌提取物。
[0092]
根据本发明的组合物提供整天保持舒适的保护。其特别适用于应用到敏感性皮肤、反应性皮肤、特别是是婴儿皮肤。
[0093]
优选地,根据本发明的组合物用于预防、保护和/或治疗敏感性皮肤。
[0094]
通常,敏感性皮肤由皮肤的特定反应性所定义。这种皮肤反应性通常通过不适迹象的表现形式来表达,这种不适感是由于受试者接触可能具有多种起源的触发元素而引起的。这可能涉及将化妆品应用于敏感性皮肤的表面、食物摄入、暴露于突然的温度变化、空气污染和/或紫外线或红外线。还有与年龄和皮肤类型相关的因素。因此,敏感性皮肤在干性或油性皮肤中比在普通皮肤中更为常见。在本发明的意义上,敏感性皮肤涵盖易过敏的和不耐受性皮肤。
[0095]
这样的组合物可以根据技术人员众所周知的方法来制造。
[0096]
通过阅读以下实施例将更好地理解本发明,这些实施例说明本发明而非限制其范围。
[0097]
实施例1:培养细菌lmb64
[0098]
举例来说,优选的培养介质包含氯化铵、硫酸镁和酵母提取物。还应注意,如在申请wo2012/085182和其他中所示,可以使用其他类似的介质,并且因此必须将其视为本说明书的整体部分。本领域技术人员的任何调整也必须被认为是本发明的一部分。
[0099]
下面描述示例性的培养过程。在此应记住,该实施例仅用于说明目的,绝不应视为限制性的。
[0100]
菌株lmb64在三个步骤中生长,即第一接种、分批模式的预培养(或预发酵)、和最后的分批补料模式的培养(添加葡萄糖)。
[0101]
接种:用一管wcb lmb64接种含有1000ml无菌介质的锥形瓶。然后将锥形瓶放置在恒温振荡箱中并摇动。当肉汤的细胞密度足够时,停止培养。然后将细胞冷却,直至转移到预发酵罐中。
[0102]
预培养:然后将约16l的介质装满预发酵罐,然后进行完全灭菌。
[0103]
在对罐进行灭菌后,将两个卫星瓶连接到预发酵罐,然后加料块:
[0104]-含有无菌50%葡萄糖溶液的瓶。立即将该溶液(葡萄糖分批预培养)转移到培养介质中,以使初始葡萄糖浓度达到20g/l。
[0105]-将上述接种步骤中含有接种物的锥形瓶接种在预发酵罐中。
[0106]
启动预培养,然后自动调节。举例来说,可以提及以下参数:温度、搅拌速度、压力、空气流速或po2。
[0107]
通过测量620nm处的光密度来监测细胞生长。达到足够的密度时,可通过冷却停止预培养。
[0108]
培养:然后在发酵罐中装入127l调节至ph 7.0的介质,然后完全灭菌。使用三个卫星瓶:
[0109]-含有无菌葡萄糖溶液的瓶。将该溶液立即转移到培养介质中,以达到20g/l的初始葡萄糖浓度。
[0110]-消泡剂的瓶。在培养期间中自动添加该消泡剂,以控制罐中的泡沫水平。
[0111]-分批补料葡萄糖的瓶。在培养期间添加该溶液以促进细胞生长。
[0112]
启动培养,然后自动调节。举例来说,还可以提及以下参数:温度、ph、搅拌、压力、空气流速、po2。
[0113]
在最初存在于介质中的葡萄糖耗尽(po2升高)后,触发添加分批补料的葡萄糖溶液,从而实现高密度细胞生长。葡萄糖完全消耗后,停止发酵。在此阶段,发酵必须自动冷却。在整个培养过程中,通过测量620nm处的光密度来监测细胞生长。使用重量法测定培养结束时获得的干燥生物质的量(g/l)。
[0114]
实施例2:提取根据本发明的级分
[0115]
通过优选实施方案的示例方式给出以下实施例,但是绝不能将其视为限制性的。
[0116]
将培养步骤的产物离心之后通常获得根据本发明的细菌提取物,将培养步骤的产物离心以除去上清和保留生物质、即细胞、表面蛋白、位于细菌周质间隙中的蛋白和细菌的细胞间蛋白(由于冷冻步骤存在)。对于离心步骤之后,从发酵罐到离心机的转移线是无菌的。然后必须通过在离心机上连续离心分离发酵物。离心以150l/h(
±
30l/h)进行,转鼓转速为10900
±
1000rpm。将细胞收集在装有一次性袋中。在超高温巴氏杀菌过程中去除上清液。该离心步骤之后是将沉淀在-20℃冷冻至少一小时的步骤。
[0117]
在发酵罐中将一百一十升tris精氨酸提取缓冲液灭菌。将在室温下预先解冻的细胞经蠕动泵转移到发酵罐中。所需的接触时间为1到7小时。加到一次性袋中后,tris和精氨酸的目标浓度为约0.3m l
–
精氨酸和20mm tris。
[0118]
然后,必须通过在离心机中连续离心来分离发酵物。以100l/h(
±
30l/h)进行离心,转鼓转速为10900
±
1000rpm。根据流出物的浊度自动开始部分沉降,浊度的设定点为20%。在一半的体积待分离时手动触发一系列的总倾析操作。将上清收集在一次性使用的袋中。在超高温巴氏杀菌过程中去除细胞。
[0119]
按顺序进行两个过滤步骤,以澄清上清液并产生根据本发明的无菌细菌提取物。过滤由过滤/分配系统控制。一次性深过滤器滤芯放置在其过滤器壳体内。多头过滤器装备有其压力计以确保过滤状态安全。预过滤模块用大约92l
±
5l的纯净水冲洗,待过滤产品袋连接并摇动。最后,将0.2μm 30
″
pes滤芯式过滤器连接到其余的过滤系统。用蠕动泵以初始流量240l/h
±
10l进行过滤。当过滤器上游的压力达到1.2bar时,降低过滤流速。将全部过滤产物无菌收集在装有400l一次性袋的容器中。将过滤产品袋在天平盘上称重,并在+5℃下储存直至分配。使用后,断开灭菌过滤器的连接,并通过完整性测试进行检查。
[0120]
实施例3:根据本发明的细菌提取物对皮肤神经源性炎症的作用
[0121]
这项研究的目的是评估根据本发明的细菌提取物在皮肤炎症中的调节特性。为此,提出了一种体外实验方法,该方法基于测量通过物质p激活的人表皮角质形成细胞产生和释放的肿瘤坏死因子-α(tnf-α)和白介素-1β(il-1β),建议作为皮肤神经源性炎症的体外模型。
[0122]
操作规程
[0123]
该研究是在正常人的表皮角质形成细胞上进行的,这些细胞来自新生的包皮。使用常规实验室程序在无血清介质中培养这些细胞。在介质中不存在(对照条件)或存在要测试的化合物(根据本发明的细菌提取物和参考产物)、以及任选地暴露至物质p的情况下,在介质中培养的这些角质形成细胞上进行皮肤神经源性炎症的标记物的测定。物质p诱导的应激之前3小时和之后的24小时中,对角质形成细胞进行处理。通过添加物质p(0.5μm)诱发炎症应激后24小时,对促炎细胞因子(tnf-α和il-1β)的水平进行定量。同时,将化合物cp96345(选择性的nk-1r抑制剂)作为参考产物以1μm进行测试。每个实验条件都是在两个不同的角质形成细胞供体上进行的。
[0124]
在孵育介质中测量tnf-α和il-1β产物,并通过酶联免疫吸附测定(elisa)进行定量。由于数据未通过正态性检验,因此使用非参数检验确定抑制百分比,以进行统计分析(
*
p<0.05;
**
p<0.01或
***
p<0.001),然后进行dunn多重比较检验作为事后检验。
[0125]
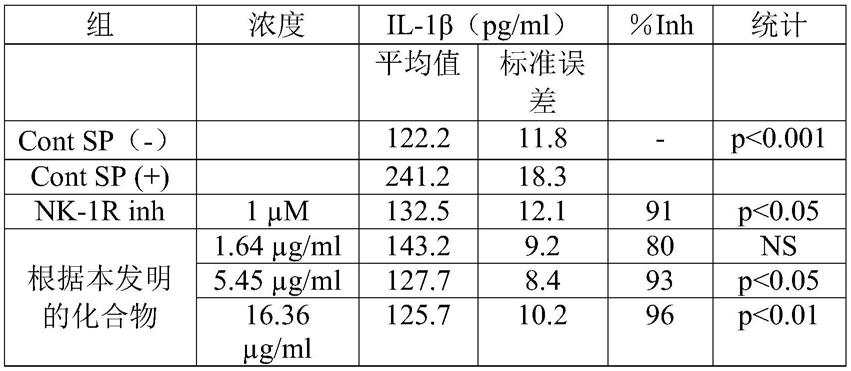
il-1β释放的结果(pg/mg总蛋白)总结于下表1中:
[0126][0127]
conc:浓度,inh:抑制,stats:相对于cont(+)的统计;e.s.:平均值的标准误差;cont:对照(无测试产物);sp(-):无物质p;sp(+):有物质p存在。
[0128]
角质形成细胞暴露于物质p会诱导实质上和统计学上显著释放il-1β。用1μm的cp96345处理可大大降低(91%,p<0.05)il-1β产生。该结果非常令人信服:使用该nk-1r抑
制剂可验证该测试。用根据本发明的化合物处理角质形成细胞,允许浓度依赖性地抑制由物质p诱导的il-1β释放。虽然第一个测试浓度(1.64μg/ml蛋白质)未达到显著水平,但仍可将该il-1β释放降低80%。在5.45μg/ml和16.36μg/ml(μl/ml蛋白质)的浓度下,这种抑制在统计学上是显著的(93%和96%抑制,分别为p<0.05和p<0.01)。
[0129]
下表2总结tnf-α释放的结果(pg/mg总蛋白):
[0130][0131]
conc:浓度,inh:抑制,stats:相对于cont(+)的统计;e.s.:平均值的标准误差;cont:对照(无测试产物);sp(-):无物质p;sp(+):有物质p存在。
[0132]
角质形成细胞暴露于物质p会诱导实质上和统计学上显著地释放tnf-α。以1μm的cp96345处理显著降低(90%,p<0.05)tnf-α的产生。这个结果也非常令人信服:使用这种nk-1r抑制剂可以验证该测试。用根据本发明的细菌提取物处理角质形成细胞允许浓度依赖性地抑制由物质p诱导的tnf-α释放。根据本发明的最低测试浓度的细菌提取物抑制tnf-α的释放达60%。尽管这种抑制作用没有达到显著性阈值,但是所证实的浓度-反应作用清楚地表明,根据本发明的细菌提取物在该测试中非常活跃。在16.36μg/ml蛋白质的浓度下,这种抑制在统计学上是显著的(77%抑制,p<0.01)。
[0133]
因此,发明人证明了根据本发明的细菌提取物能够显著抑制经由物质p产生的细胞因子产生;因此,根据本发明的这种细菌提取物可有效治疗皮肤神经源性炎症。
[0134]
实施例4:在正常人表皮角质形成细胞的模型中,根据本发明的细菌提取物对先天免疫基因表达谱的影响
[0135]
皮肤的屏障功能还包括防御微生物。上皮在先天宿主防御中起积极作用。皮肤抗微生物系统尤其基于某些表面脂质和某些组成型蛋白的存在。这些蛋白质具有抗微生物活性。而且,表皮表面的酸化在没有皮肤抗微生物防御的情况下起重要作用。因此,皮肤不仅充当物理屏障,而且充当化学屏障。基于可诱导的抗微生物肽的分泌,先天免疫还具有适应性成分。抗微生物肽通过影响上皮细胞和炎性细胞,影响细胞增殖和细胞因子产生,作为炎症介质而起重要作用。它们的作用方式包括破坏感染性微生物的质膜或进入微生物,以干扰细胞内代谢。皮肤中研究最多的抗微生物肽是β-防御素和抗菌素(cath
é
licidines)。人β-防御素是在人上皮细胞中发现的主要抗微生物肽分类,在皮肤中已鉴定出其中的四种,hbd 1-4。尽管它们属于同一家族,但它们受到不同途径的调节。人β-防御素2(hbd2)是一种4kda肝素结合肽,是主要的皮肤抗微生物肽之一。可通过分泌反映炎性状态的细胞因子(il-1α和il-1β和tnf-α)、或通过与细菌或真菌接触而诱导表达hbd2肽。
[0136]
这项研究的目的是,通过对与先天免疫有关的两个基因的rt-pcr技术,评估本发明的细菌提取物对正常人表皮角质形成细胞的基因表达的影响。
[0137]
对来自三个供体的正常人表皮角质形成细胞进行该研究。这些细胞在第三次传代时使用。使用常规实验室程序,在补充了表皮生长因子(egf)、垂体提取物(pe)和庆大霉素的标准介质中培养这些细胞。
[0138]
在三种浓度下测试根据本发明的细菌提取物:0.4、2和10μg/ml(μg/ml蛋白质)。
[0139]
同时,将氯化钙作为参考产物以1.5mm进行测试。
[0140]
将角质形成细胞接种在24孔板中(每孔50,000个细胞),并在培养介质中培养24小时。然后用测试介质取代该介质,所述测试介质含有或不含(对照条件,dmso)根据本发明的细菌提取物、或氯化钙(参考产物);在这些条件下将细胞孵育48小时。在该孵育期结束时,将细胞在缓冲溶液中洗涤,并立即在-80℃的温度下冷冻。
[0141]
对于在每种条件下从细胞提取的总arn通过rt-qpcr方法分析标记物的表达。根据供应商的说明,使用tripure 试剂在每个样本中提取总arn。通过毛细管电泳评估arn的数量和质量。通过在寡(dt)和transcriptor逆转录酶的存在下对总arn进行逆转录来合成adnc。然后在聚合酶链反应(pcr)步骤之前调节adnc的量。
[0142]
根据供应商的数据,使用系统(roche)进行pcr。
[0143]
数据由microsoft excel软件进行分析。
[0144]
在pcr循环中连续测量荧光掺入扩增adn中的情况。这产生了荧光强度和每个标记物相对表达值的pcr循环数之间的图形表示。
[0145]
本研究中使用的pcr技术包括两个参考基因(rpl13a和tbp);因为这些基因的表达是组成型的,因此在理论上是稳定的,所以这些基因用于数据归一化。因此,在所有条件下,将靶基因的表达水平与这两个参考标记物的平均表达水平进行比较。
[0146]
参数rq(相对定量)定义为相对表达/100。所有结果均以倍增因数表示,如果rq>1则代表基因过表达的倍数,或者如果rq<1则代表基因低表达的倍数。
[0147]
下表3对治疗条件与对照条件的影响进行了分类。
[0148]
效果分类倍增因数(fc)强刺激fc>3刺激3>fc>2轻度刺激,待确认2>fc>1.5-1.5>fc>-1.5轻度抑制,待确认-1.5>fc>-2抑制-2>fc>-3强抑制-3>fc无表达循环数>33
[0149]
通过未配对学生氏检验的组间比较进行统计分析。
[0150]
结果
[0151]
用1.5mm氯化钙作为阳性对照处理正常人的表皮角质形成细胞可诱导先天免疫中靶向基因的强表达:该结果证实了实验条件(表4)。
[0152][0153]
pam:抗微生物肽
[0154]
表5总结了在三种测试浓度下本发明细菌提取物的作用。
[0155][0156]
pam:抗微生物肽
[0157]
发明人证明,所有测试浓度的根据本发明的细菌提取物均以浓度依赖性方式诱导hbd2和s100a7基因的表达。
[0158]
根据本发明的细菌提取物具有增加诱导抗微生物肽的能力。通过刺激先天免疫,抗微生物肽可诱导皮肤防御并帮助保护皮肤屏障。
[0159]
所有这些结果,即减少皮肤神经源性炎症并结合保护皮肤屏障的辅助手段,表明根据本发明的细菌提取物确实作用于敏感和/或不耐受性皮肤。
[0160]
(电子形式的原件)
[0161]
(该表不是国际申请的一部分,也不算作其表)
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1