新的医疗装置、递送运载体及其制造的制作方法
本公开涉及透皮递送贴剂、片剂、胶囊和丸剂,以及口腔贴剂和皮肤贴剂,其各自可以包含提供药剂诸如药物或营养品的制剂。药物可以是一种或多种大麻素。
背景技术:
皮肤贴剂可以采用整体式贴剂或储库型贴剂的形式(参见,weimann的美国专利特许证号9,562,340&10,272,125)。整体式贴剂可以采用夹层的形式,其中暴露于大气的面是背衬,其中相反的面是剥离衬垫,并且其中夹层的填充是包括粘合剂和药剂诸如药物或营养品的基质。在将贴剂施加到皮肤之前,将剥离衬垫去除并丢弃。
关于储库型贴剂,储库可以包含为药物或营养品的药剂。储库还包含液体载体和胶凝剂。可以通过一起采用“馄饨(ravioli)”构造的背衬和可渗透膜来限定储库。可渗透膜任选地涂覆有介导粘合剂与皮肤结合的粘合剂。粘合剂的一侧上是可渗透膜,而另一侧上是剥离衬垫。在将贴剂施加到皮肤之前,将剥离衬垫去除并丢弃。
使用皮肤贴剂递送辣椒素以减轻疼痛。贴剂递送辣椒素。辣椒素作用于周围伤害性感受器。贴剂可以施加约一小时,其中结果是减轻疼痛数周(参见,peppinetal(2011)j.painres.4:385-392)。皮肤贴剂还用于递送罗替高汀(rotigotine)以治疗帕金森病,并且其中该贴剂在24小时内提供连续药物递送,导致与连续静脉输注的血浆药代动力学相似的血浆药代动力学。罗替高汀对多巴胺受体起作用(参见,elshoffetal(2015)drugs.75:487-501)。给出另一个实例,皮肤贴剂可以为绝经后的妇女提供雌激素用于治疗,并为避孕提供乙炔基雌二醇和诺孕曲明。避孕贴剂使用7天,而其提供与每日口服避孕药的全身浓度相似的全身浓度(参见,jungetal(2013)drugs.13:223-233)。
本公开提供了舌下片剂、胶囊、丸剂和条状物,以及口腔贴剂和皮肤贴剂。这些物体在本文中作为包含一种或多种药物的新颖的且促进的片剂、胶囊、条状物和贴剂提供。还提供了不包含一种或多种药物的这些相同的新颖的且促进的物体,例如如可能发现用作安慰剂。
本公开解决了对于提供药剂诸如大麻素、褪黑激素、辣椒素、利多卡因、水杨酸、西地那非或维生素诸如维生素b1、维生素d3、维生素b12或维生素c的舌下片剂、胶囊和丸剂、皮肤贴剂、舌下贴剂和口腔贴剂的未满足需求。
技术实现要素:
简言之,本公开提供了能够用于口腔贴剂、舌下贴剂、丸剂、片剂或皮肤贴剂的组合物,其中所述组合物包括以下中的一种或多种:无官能度丙烯酸粘合剂和仅具有oh官能度的粘合剂,进一步包括选自氮酮、油酸和二甲基亚砜(dmso)的促进剂中的多种中的一种;具有增粘剂的聚异丁烯(pib粘合剂),所述增粘剂使用以1-50%,任选地与环脂族烃树脂混合的丙烯酸压敏粘合剂改善对皮肤的粘合;具有促进剂:3%的氮酮或油酸的pib粘合剂,使来自pib的透皮递送增加了一倍;具有包含至少一种萜烯的浓度为80-95%的cbd的大麻油;用大麻二酚(cbd)和四氢大麻酚(thc)饱和的半固体水凝胶;包括油的半固体水凝胶,所述油基本上由与乙醇/水(80/20,vol/vol)、任选地与选自氮酮、油酸和苧烯中的一种或多种促进剂组合的cbd和thc(80-95%,wt/vol)组成;用cbd和thc油(80-95%,wt/vol)饱和的半固体水凝胶,其中所述油与etoh/水(80/20,vol/vol)、任选地与选自氮酮、油酸和苧烯中的一种或多种促进剂混合;或或thc(80-95%)与1-20%etoh或与1-10%etoh/水(80/20,vol/vol)混合的thc油,其中包括多于10%的乙醇能够降低如可由储库型贴剂(reservoirpatch)确定的thc递送的通量。还提供了包括以上组合物中的一种的口腔贴剂、舌下丸剂、舌下片剂或舌下贴剂。
还包括的是一种用于制造以上贴剂的方法,所述方法包括使thc、薄膜、粘合剂和背衬组合以生成未切割贴剂的步骤,进一步包括未切割贴剂以产生能够施加到人皮肤或施加到人颊囊的切割贴剂。
具体实施方式
除非上下文另外明确指出,否则如本文包括所附权利要求中所使用的单词的单数形式,诸如“一个/种(a)”、“一个/种(an)”和“该/所述(the)”包括它们相应的复数引用。本文引用的所有参考文献通过援引并入,程度如同每一个单独的专利和已公布的专利申请以及图片、附图、序列表、光盘等均明确且单独地指出为通过援引并入一样。
大麻素
本公开提供了皮肤贴剂、制剂、不包含制剂的皮肤贴剂以及包括制剂的皮肤贴剂。优选的制剂包括一种或多种大麻素。来自大麻(cannabissativa)的主要大麻素是大麻二酚(cbd)、大麻色原烯(cannabichromene)(cbc)、大麻萜酚(cannabigerol)(cbg)、δ-9-四氢大麻酚(δ-9-thc)和大麻酚(cannabinol)(cbn)(appendinoetal(2008)j.nat.prod.71:1427-1430)。临床试验已经证实,源自大麻(cannabis)的制剂,可以改善多发性硬化的神经性疼痛,改善癌症患者的食欲和睡眠品质,减轻纤维肌痛患者的疼痛,并用作止吐药,用于化疗诱导的恶心和呕吐(参见,healthcanada(feb.2013)informationforhealthcareprofessionals.cannabis(marihuana,marijuana)andthecannabinoids(152pages))。本公开还提供了四氢次大麻酚(tetrahydrocannabinovarin)(thcv),其是thc的丙基类似物,以及次大麻二酚(cannabidivarin)(cbdv),其是cbd的丙基类似物。
提供了包括给定比率的thc和cbd两者的制剂和组合物,诸如比率为约95/5、约90/10、约80/20、约70/30、约60/40、约50/50、约40/60、约30/70、约20/80、约10/90和约5/95(按重量计)。给药包含thc和cbd两者的制剂比仅包含thc或仅包含安慰剂的制剂可具有更大的减轻疼痛的影响(参见,johnsonetal(2010)j.painsymptommanagement.39:167-179;notcuttetal(2004)anaesthesia.5944-452)。
以下大麻素中的多种中的一种可以包括在本公开的组合物中。大麻素和相关化合物进一步包括,例如,大麻色原烯;二羟基大麻酚(cannabitriol);大麻环酚(cannabicyclolol);大麻艾尔松(cannabielsoin);脱氢大麻二酚(cannabinodiol);δ-8-四氢大麻酚;大麻苯并二氢吡喃-4-酮(cannabichromanone);大麻香豆酮(cannabicoumaronone);大麻二吡喃环烷(cannabicitran);10-氧代-δ-6a10a-四氢大麻酚;大麻环醚萜酚;δ-7-异四氢大麻酚;cblva;cbv;cbeva-b;cbcva;δ-9-thcva;cbdva;cbgva;divarinolicacid;槲皮素;山柰酚(kaemferol);二氢山柰酚;二氢槲皮素;大麻黄酮素b(cannflavinb);异牧荆素(isovitexin);芹菜素(apigenin);柚皮素(naringenin);圣草酚(eriodictyol);木犀草素;荭草素(orientin);金雀花黄苷(cytisoside);牡荆素(vitexin);大麻烯(canniprene);3,4'-二羟基-5-甲氧基联苄;二氢藜芦醇;3,4'-二羟基-5,3'-二甲氧基-5'-异戊二烯基;cannabistilbene1;cannabistilbene11a;cannabistilbene11b;cannithrene1;cannithrene2;大麻螺酮(cannabispirone);异大麻螺酮;大麻螺烯酮-a(cannabispirenon-a);大麻螺烯酮-b;大麻螺二烯酮(cannabispiradienone);α-大麻螺烷酚(alpha-cannabispiranol);β-大麻螺烷酚;乙酰基-大麻螺醇(acetyl-cannabispirol);7-羟基-5-甲氧基茚满-1-螺-环己烷;5-羟基-7-甲氧基茚满-1-螺环己烷;豆蔻酸、棕榈酸、油酸、硬脂酸、亚油酸、亚麻酸、花生酸、二十碳烯酸、山萮酸、木蜡酸、5,7-二羟基茚满-1-环己烷;大麻螺二烯酮;3,4'-二羟基-5-甲氧基联苄;大麻烯(canniprene);大麻螺酮;cannithrenei;cannithrene2;α-大麻螺烷酚;乙酰基-大麻螺醇;催吐叶醇(vomifoliol);二氢催吐叶醇;β-紫罗兰酮;二氢猕猴桃内酯(dihydroactinidiolide);问荆碱(palustrine);沼泽定(palustridine);加-大麻碱(plus-cannabisativine);脱水大麻碱(anhydrocannabisativine);dihydroperiphylline;大麻酰胺-a(cannabisin-a);大麻酰胺-b;大麻酰胺-c;大麻酰胺-d;克罗酰胺(grossamide);大麻酰胺-e;大麻酰胺-f;大麻酰胺-g等(参见,例如flores-sanchezandverpoorte(2008)secondarymetabolismincannabis.phytochem.rev.7:615-639)。
在排他性实施方式中,本公开可以排除包括cbd、cbc)、cbg、δ-9-thc、cbn或以上清单的任何化学品的任何制剂、组合物、装置或方法。可以排除的是采用液体大麻素制剂形式的任何制剂、组合物、装置或方法,其中至少20%、至少40%、至少60%、至少80%、至少90%或至少95%的总大麻素是四氢大麻酚酸(tetrahydrocannabinolicacid)(thca)。同样,可以排除的是采用油制剂形式的任何制剂、组合物、装置或方法,其中油制剂包含一种或多种大麻素,其中至少20%、至少40%、至少60%、至少80%、至少90%、至少95%的总大麻素是四氢大麻酚酸(thca)。
测量大麻素
大麻素可以通过多种技术进行分离、纯化、分析和量化。可用的设备和方法包括,例如,气相色谱法、hplc(高压液相色谱法、高效液相色谱法)、质谱法、飞行时间质谱法、气相色谱-质谱法(gc-ms)和液相色谱-质谱法(lc-ms)。用于分离和分析的设备可从waterscorp.,米尔福德(milford),马萨诸塞州(ma);agilent,福斯特城(fostercity),加利福尼亚州(ca);appliedbiosystems,福斯特城,加利福尼亚州;以及bio-radcorp.,赫拉克勒斯(hercules),加利福尼亚州获得。公开了用于大麻素的hplc分级和鉴定的方法、设备和制造商(参见,例如peschelw(2016)qualitycontroloftraditionalcannabistinctures.sci.pharm.84:567-584;scheidweilerkbetal(2012)simultaneousquantificationoffreeandglucuronidatedcannabinoidsinhumanurinebyliquidchromatographytandemmassspectrometry.clin.chim.acta.413:1839-1847)。
本公开提供了在线监测纯化,即thc的量化以及杂质的量化。在线监测可以通过uplc方法或通过其他方法。超高效液相色谱法(uplc)与hplc类似,除了uplc在柱床中使用较小的颗粒以及使用较大的压力之外。颗粒的直径可以小于2微米,并且压力可以接近15,000psi。uplc还使用更高的流速,并且可以提供出色的分辨率和在小于30秒的范围内的运行时间(wrenandtchelitcheff(2006)j.chromatographya.1119:140-146;swartz,m.e.(may2005)separationscienceredefined)。已经描述了将uplc应用于大麻素(参见,jameyetal(2008)j.analyticaltoxicology.32:349-354;badawietal(2009)clinicalchemistry.55:2004-2018)。用于大麻素分析的合适的uplc柱包括,例如
可以使用标记的大麻素、标记的萜烯和其中大麻素或萜烯影响标记的配体的结合特性的标记的配体,来评估与大麻素受体、萜烯和萜烯受体结合结合的大麻素的生化特性。有用的标记物包括放射性标记物、表位标签、荧光染料、电子致密试剂、底物或酶,例如在酶联免疫分析法或fluorettes中所使用的(参见,例如rozinovandnolan(1998)chem.biol.5:713-728)。
大麻素编号系统
本公开使用如由pertweergetal(2010)internationalunionofbasicandclinicalpharmacology.lxxix.cannabinoidreceptorsandtheirligands:beyondcb1andcb1.pharmacol.rev.62:588-631所阐述的命名法。关于同一化合物的不同编号系统,aviv(us2004/0110827)声明:“应当指出的是,由于历史原因,这些大麻素类似物仍遵循先前的命名法命名,其中萜烯环是用于编号系统的基础。然后,thc型大麻素的手性中心在碳原子3和4处。现在,公认的命名法是基于酚环作为用于编号的起点。因此,先前被描述为δ-1-thc的thc后来被重命名为δ-9-thc,类似地,δ-6-thc被重命名为δ-8-thc,并且手性中心在碳原子6a和10a处。”aviv也有关于对映体的这种评论:“δ-9-thc由mechoulamr.等人在1967年建立,并被发现具有(-)-(3r,4r)立体化学。后来发现,大麻素的精神活性存在于天然(3r,4r)oh系列中,而相反的对映体合成系列(3s,4s)不含这些不期望的效果。”
根据agurell(1988)pharmacologicalrevs.38:21-43,萜烯编号系统使用δ-1-thc,而二苯并吡喃系统使用δ-9-thc是指相同的化学品。这两种编号系统都可以用于thc、cbd和cbn。
根据chulgin,最广泛使用的编号系统识别大麻素的两个不同部分的萜烯性质和芳香性质两者。在此,从带有该支链甲基基团的环碳对萜烯进行编号并且将其编号为7,以及然后对异丙基基团的其余三个碳顺序编号。这种编号系统的优点在于,无论中心环是闭合的还是打开的,这种编号系统均是可适用的。其他编号系统是联苯编号系统、化学文摘系统(chemicalabstractssystem)(取代的二苯并吡喃编号)和托德(todd)编号系统(吡喃编号)(参见,chulginat(1969)recentdevelopmentsincannabischemistry.j.psychedelicdrugs.pp.397-415。
大麻油、其他油和提取物
大麻油或大麻籽油是通过压榨大麻籽获得的。它是包含约80%的必需脂肪酸的食用油,但它不是cbd大麻油。
大麻二酚(cbd)大麻油可以使用工业大麻植物的茎的超临界二氧化碳(co2)提取来制造。cbd大麻油通常包含20-40%cbd。为了生产99.8%纯的结晶cbd,使用分馏进一步加工cbd油。
大麻(marijuana)提取油是大麻植物诸如大麻(sativa)或印度大麻(indica)的提取物。提取物是不同%的cbd、thc和其他大麻素的固体或半固体。大麻thc提取物(油)可以具有最高达80%的高%的thc以及约10-20%的一些cbd。
大麻cbd提取物可以具有最高达90%的高%的cbd以及最高达10%的低%的thc。大麻提取物中大麻素的百分数取决于用于提取的大麻植物中那些物质的含量。通过使用丁烷、乙醇或关键的co2提取进行提取。
在此列出了大麻油供应商(参见,例如,medicalmarijuana,inc.,波威市(poway),加利福尼亚州;nutiva,里士满(richmond),加利福尼亚州;entouragenutritionaldistributors,科泉市(coloradosprings),加利福尼亚州)。例如,已经描述了在波兰(poland)的大麻地(参见,例如,l.grabowskaetal(2009)breedingandcultivationofindustrialhempinpoland.herbapolonica.55:328-334;l.grabowskaetal(2008)maintenancebreedingofpolishhempcultivarbeniko.j.naturalfibers.5:208-217)。在波兰种植并且适应波兰气候和土壤条件的大麻种类(品种)包括bialobrzeskie、beniko、silesia、tygra和wielkopolskie。
由于可以在不从萜烯中反萃取cbd大麻油的情况下生产cbd大麻油,因此本公开的透皮制剂提供了天然萜烯是否促进cbd透皮皮肤穿透的信息,以及关于天然萜烯一旦穿过皮肤吸收后如何提供医学特性的信息。
基质实施方式
可用于制粒剂和喷雾剂的赋形剂是具有给定比率或比率范围的聚乙烯吡咯烷酮/乙酸乙烯酯(pvp/va)的聚乙烯吡咯烷酮共聚物。本公开提供了比率为10/90、20/80、30/70、40/60、50/50、60/40、70/30、80/20、90/10的pvp/va(或任何两种聚合物的组合)以及比率为约10/90、约20/80、约30/70、约40/60、约50/50、约60/40、约70/30、约80/20、约90/10的任何两种聚合物的组合。同样,本公开可以排除具有的比率为10/90、20/80、30/70、40/60、50/50、60/40、70/30、80/20、90/10或约10/90、约20/80、约30/70、约40/60、约50/50、约60/40、约70/30、约80/20、约90/10等的pvp/va组合物(或其可以排除任何两种聚合物的组合)。pvp/va共聚物具有在水性液相形成期间在活性成分周围均匀分布的能力(参见,sekura的us2016/0058866)。聚合物和共聚物可从sigma-aldrich,圣路易斯(st.louis),密苏里州(mo),nipponshokubaico.,ltd.,大阪(osaka),日本,basfcorp.,弗洛勒姆帕克(florhampark),新泽西州(nj)和ashland,沙夫豪森(schaffhausen),瑞士(switzerland)获得。
在制造实施方式的方法中,整体式贴剂可以如下制成。火麻油(cannabisoil)或一种或多种纯大麻素可以仅与渗透促进剂组合,或仅与载体组合,或与渗透促进剂和载体两者组合。载体可以包括例如,油酸和十二烷基甲基亚砜中的一种或多种。然后将一种或多种纯萜烯或精油,或精油和一种或多种纯萜烯的组合与以上组合混合。然后,将聚合物诸如硅酮聚合物混合。最后,将混合物铺展为一片或多片,在室温下固化数小时或更长。干燥之后,施加泡沫背衬层,且然后将产品切割成适合于施加到人皮肤的形状(例如,正方形、矩形、椭圆形、圆边正方形或圆边矩形、圆形)。
可以适当地保持在牙龈(牙床)上的层压体采用半渗透外层、具有药物的储库、背衬层的形式,其中背衬层面向牙龈。唾液可以进入穿过半渗透外层,穿过储库,以及然后使药品与牙龈接触以在血流中吸收。药物可以是冷冻干燥的或可以作为水凝胶基质存在于储库中。本公开提供了一种或多种聚合物,诸如乙基纤维素、丁基纤维素、羟丁基纤维素或聚乙烯醇的背衬层。无定形或半结晶赋形剂基质可以由甲基纤维素、乙基纤维素、羟丙基甲基纤维素、乙酸邻苯二甲酸纤维素或乙酸丁酸纤维素制成。在排他性实施方式中,本公开可以排除这些聚合物中的一种或多种。
在储库-分布实施方式中,药物或营养品可以均匀地分布在整个储库中,或者可以以较高的浓度分布在储库的中心,或者可以以较高的浓度分布在贴剂就位并粘附至皮肤上时靠近皮肤的储库区域处。
增粘剂
本公开提供了包括以下中的一种或多种的组合物、贴剂和方法:escorez1000系列-脂族树脂;escorez2000系列-芳族改性的脂族树脂;escorez5300系列-水白色氢化环脂族树脂;escorez5400系列-浅色氢化环脂族树脂;escorez5600系列-浅色氢化芳族改性的环脂族树脂;
水凝胶
水凝胶是水溶性聚合物的3维交联网络。水凝胶的多孔结构可以通过改变交联密度来改变。交联度可以改变负载药物的速率,并且它可以改变药物释放的速率。本公开可以涵盖由以下聚合物之一组成的,或者替代地,包括以下聚合物(例如,作为嵌段聚合物)中的一种或多种的水凝胶。聚合物包括聚(环氧乙烷)(peo)、聚(环氧丙烷)(ppo)、聚(丙交酯-co-乙醇酸)(plga)、聚(n-异丙基丙烯酰胺)(pnipam)、聚(富马酸亚丙酯)(ppf)、聚(己内酯)(pcl)、聚(氨酯)(pu)和聚(有机膦氮烯)(pop)。嵌段聚合物的实例是peo-ppo-peo。在排他性实施方式中,本公开可以排除包括peo、ppo、plga、pnipam、ppf、pcl、pu或pop的水凝胶。本公开还涵盖了包含环糊精的水凝胶,其中环糊精与水凝胶交联(参见,hoareetal(2008)hydrogelsindrugdelivery:progressandchallenges.polymer.49:1993-2007)。本公开的水凝胶可以是乙烯乙酸乙烯酯、海藻酸、树胶、聚乙烯醇水凝胶;硅酮水凝胶;聚乙烯醇/右旋糖酐水凝胶;海藻酸盐水凝胶;海藻酸盐-吡咯水凝胶;明胶/壳聚糖水凝胶;聚丙烯酸水凝胶;光交联聚丙烯酸水凝胶;酰胺化果胶水凝胶;果胶水凝胶;明胶水凝胶;聚乙二醇(peg)水凝胶;羧甲基纤维素/明胶水凝胶;壳聚糖水凝胶及其混合物或其共聚物等。具有交联的水凝胶是可获得的(leeetal(2003)eur.j.pharm.biopharm.56:407-412)。
在干燥的水凝胶上印刷活性成分和赋形剂
干燥的水凝胶可以采用“干凝胶”或薄膜的形式。可以通过将水凝胶冷冻干燥来制成干凝胶。薄膜可以通过蒸发干燥或从有机溶液中浇铸制成。可以使用点样装置将微滴施加在干燥的水凝胶或薄膜的预定位置(参见,例如,schermer的us6,642,054)。在干燥的水凝胶或薄膜采用层形式的情况下,微滴可以仅施加到一侧或施加到两侧。在待施加多于一种类型的药物的情况下并且在至少两种药物彼此不相容的情况下,或者在待施加药物和赋形剂的情况下,并且在这些是彼此不相容的情况下,则这些可以施加在干燥的水凝胶或薄膜上的不同位置处。微滴的液滴大小可以是例如0.05纳升(nl)-10,000nl、0.5nl-200nl、10nl-100nl等。药物、活性成分和/或赋形剂未掺入干燥的水凝胶中,而是印刷在其一个或多个表面上。在干燥的水凝胶上印刷避免了由于药物、活性成分和/或赋形剂与水凝胶本身不相容而引起的问题。参见,stabenau的us2008/0095848,其通过援引以其全文并入。
环糊精
环糊精是具有亲油中心腔和亲水性外表面的(α-1,4)-连接的α-d-吡喃葡萄糖单元的环状寡糖。作为其分子结构和形状的结果,它们可以通过将药物或其他分子捕获在其内腔中而充当分子容器。在药物环糊精复合物形成期间不会形成或破坏共价键,并且在水性溶液中,复合物容易离解并且游离的药物分子与结合在环糊精腔内的分子保持平衡(参见,tiwarietal(2010)cyclodextrinsindeliverysystems:applications.j.pharm.bioalliedsci.2:72-79)。为羟丙基(hp)、甲基(m)和磺丁基醚(sbe)取代基的环糊精的衍生物可用作药物赋形剂。
用于例如大麻素/环糊精复合物中的环糊精包括β-环糊精,诸如羟丙基-β-环糊精、磺丁基醚-β-环糊精、麦芽氧基(maltoxyl)-β-环糊精和甲基化的环糊精。涵盖的是α-环糊精(6个吡喃葡萄糖单元)、β-环糊精(7个吡喃葡萄糖单元)和γ-环糊精(8个吡喃葡萄糖单元)。甲基化的环糊精可以提高大麻素的水性溶解度、溶出度速率和生物利用度。
本公开提供了包括其中糊精未与药剂复合的糊精的皮肤贴剂(或口腔贴剂),以及包括其中糊精实际上与药剂复合的糊精的皮肤贴剂(或口腔贴剂)。
在排他性实施方式中,本公开可以排除包括环糊精或包括α-环糊精或包括β-环糊精或包括γ-环糊精的制剂。还可以排除的是包括环糊精的装置,诸如包括糊精的粘合性皮肤贴剂或包括糊精的口腔贴剂。
基质、载体、粘结剂、片剂、丸剂、制造方法
基质、载体或粘结剂可以包括例如水凝胶、聚氧乙烯、聚乙烯吡咯烷酮、羟丙基纤维素、乙基纤维素、甲基纤维素、烷基纤维素、veegums粘土、海藻酸盐、pvp、海藻酸、羧甲基纤维素钙、微晶纤维素、泼拉克林钾(polacrillinpotassium)、海藻酸钠、玉米淀粉、马铃薯淀粉、预糊化淀粉、玉米淀粉、改性淀粉、卡洛巴蜡(carnubawax)、蒙脱土粘土(montmorriloniteclays)诸如膨润土、树胶、紫胶、琼脂、槐豆胶、刺梧桐胶、果胶(pecitin)、黄芪胶等。在排他性实施方式中,可以排除的是以上聚合物、粘土、蜡、水凝胶、淀粉和树胶中的一种或多种。多元醇可以用作例如载体。
多元醇包括丙二醇和甘油,并且优选的(聚)烷氧基衍生物包括聚烷氧基醇,尤其是2-(2-乙氧基乙氧基)乙醇
在us4,829,056中公开了适用于口含片剂的树胶,其通过援引以其全文并入。提供了锭剂和舌下丸剂,并且这些可以包括磷酸钠、磷酸钾、瓜尔胶、阿拉伯胶、槐豆胶、黄胞胶、角叉菜胶、槐树豆胶、加特胶、果胶、黄芪胶、金合欢胶、甘露醇、山梨糖醇、乳糖、改性乳糖、麦芽糖醇、甘露醇、硬脂酸镁、羟丙基甲基纤维素薄膜、非结晶糖或非结晶糖醇中的一种或多种。
可以通过使用微粒、颗粒剂、双层、增塑剂等的熔融制粒、熔融挤出来制造基质(参见,wright的us2016/0151502)。可以用设置在基材上的硅酮粘合剂、共聚物、嵌段聚合物、增粘树脂、热熔涂覆工艺来制造贴剂(参见,fung的us2014/0349108)。可以用背衬、剥离衬垫、压敏粘合剂、硅酮凝胶粘合剂制造贴剂(参见,kumar的us2014/0287642)。可以用赋形剂、崩解剂、溶胀剂、薄膜、粘结剂等制造皮肤贴剂、口腔贴剂、片剂(salama的us2014/0079740)。这些专利文件中的每一个均通过援引以其全文并入本文。详述了热熔挤出、颗粒剂、片剂、穿粘膜贴剂、透皮贴剂和制造方法(crowleyetal(2007)drugdevelopmentindustrialpharmacy.33:909-926;repkaetal(2007)drugdevelopmentindustrialpharmacy.33:1043-1057)。
关于舌下片剂、舌下丸剂和舌下条状物,用于压制颗粒剂、用于施加涂层和润滑剂的设备是可获得的(参见,herry的us2010/0233257)。关于舌下片剂和口含片剂,公开了涉及例如交联的羧甲基纤维素、乳糖、微晶纤维素、结合液体的配方,以及设备诸如干燥机、混合机-颗粒机、压缩机(参见,例如,us9,308,212)。公开了透皮吸收促进剂、填充剂、粘结剂、载体、用于模制和固化舌下片剂的设备(gould的us9,220,747)。这些专利文件中的每一个均通过援引以其全文并入本文。
小孔和孔
本公开可以涵盖薄膜、片、层、膜等,包括具有多个小孔或孔的那些。在一些方面,小孔或孔具有的平均直径为20nm、40nm、50nm、100nm、200nm、300nm、400nm、500nm、600nm、800nm、0.001mm、0.002、0.005mm、0.010mm、0.015mm、0.020mm、0.025mm、0.030mm、0.040mm、0.050mm、0.075mm、0.10mm、0.20mm、0.30mm、0.40mm、0.50mm等。同样,孔可以具有其中可以由这些值中的任何两个括起来的范围的直径范围。在其他方面,小孔或孔具有的直径在20-40nm、40-60nm、60-80nm、50-100nm、100-200nm、200-400nm、400-600nm、600-800nm、800-1,000nm、0.001-0.002mm、0.001-0.005mm、0.005-0.010mm、0.010-0.020mm、0.020-0.040mm、0.025-0.050mm、0.050-0.075mm、0.075-0.10mm、0.10-0.20mm、0.20mm-0.40mm、0.25-0.50mm、0.50-0.75mm、0.50-1.00mm、0.1-0.2mm等的范围内。在排他性实施方式中,本公开可以排除具有拥有任何以上平均值的小孔或孔或由任何以上范围可描述的薄膜、片、层等。
在不暗示任何限制的情况下,多孔膜可以采用亲水性多孔膜和疏水性多孔膜的形式。可以通过醇或表面活性剂使疏水性膜,诸如疏水性聚乙烯(pe)膜更亲水(参见,calis的wo2010/072233)。本公开的膜中的孔可以具有的平均直径为约5微米、约10、约15、约20、约25、约30、约40、约50、约60、约70、约80、约90、约100、约110、约120、约130、约140、约150、约160、约170、约180、约190或约200微米等。同样,膜中的孔可以具有的平均直径是在5-20微米、20-40微米、40-60微米、60-80微米、80-100微米、100-120微米、120-140微米、140-160微米、160-180微米、180-200微米等范围内的某个值。在排他性实施方式中,本公开可以排除以以上“约”值之一表征或以以上范围之一表征的任何膜。
对于任何给定薄膜、片或层等,多个小孔的面积或多个孔的面积可以占据表面积的约1%、约2%、约4%、约6%、约8%、约10%、约15%、约20%、约25%、约30%、约35%、约40%、约45%、约50%、约55%、约60%、约65%、约70%、约75%、约80%、约85%、约90%等。在排他性实施方式中,本公开可以排除其中面积不占据给定百分数值中的一个或多个,或者其中面积不占据在以上给定百分数值中的任何两个之间的范围的任何薄膜、片或层。上述参数也可以应用于具有穿孔的薄膜、片或层,其中用于穿孔的面积的值是与薄膜、片或层的表面齐平地测量的。
增溶剂和表面活性剂
增溶剂诸如洗涤剂、表面活性剂、有机溶剂和离散剂可用于本公开。这些可以是聚乙二醇(peg)、丙二醇、次乙酸二丁酯、甘油、邻苯二甲酸二乙酯(邻苯二甲酸酯)、三乙酰甘油、柠檬酸酯-柠檬酸三乙酯、柠檬酸乙酰基三乙酯、柠檬酸三丁酯、柠檬酸乙酰基三丁酯、苯甲酸苄酯、山梨糖醇、木糖醇、己二酸双(2-乙基己基)酯、矿物油、多元醇诸如甘油和山梨糖醇、甘油酯诸如甘油、三乙酸酯;脂肪酸甘油三脂、聚氧乙烯山梨聚糖、脂肪酸酯诸如tweens、聚氧乙烯单烷基醚诸如brij系列和myrj系列、蔗糖单酯、羊毛脂酯、羊毛脂醚中的一种或多种。这些可从sigma-aldrich,圣路易斯,密苏里州获得。在排他性实施方式中,可以排除的是包括这些增溶剂或表面活性剂中的一种或多种的任何组合物、制剂、皮肤贴剂和方法。
本公开可以涵盖包括以下一种或多种表面活性剂的组合物、制剂、装置和方法:诸如山梨聚糖三油酸酯、山梨聚糖单油酸酯、山梨聚糖单月桂酸酯、聚氧乙烯(20)山梨聚糖单月桂酸酯、聚氧乙烯(20)山梨聚糖单油酸酯、油基聚氧乙烯(2)醚、硬脂酰基聚氧乙烯(2)醚、月桂基聚氧乙烯(4)醚、氧乙烯和氧丙烯的嵌段共聚物、二乙二醇二油酸酯、油酸四氢糠基酯、油酸乙酯、肉豆蔻酸异丙酯、棕榈酸异丙酯、单油酸甘油酯、单硬脂酸甘油酯、单蓖蓖麻酸甘油酯、鲸蜡醇、硬脂醇、氯化鲸蜡基吡啶鎓、橄榄油、单月桂酸甘油酯、玉米油、棉籽油和葵花籽油。在排他性实施方式中,本公开可以排除以上化学品中的一种或多种,并且还可以排除包括任何以上化学品的组合物、制剂、装置和方法。
缓冲液和ph值
本公开可以包括包含具有如在室温下测量的pka的缓冲液的制剂,缓冲液诸如硼酸(pka9.2)、ches(pka9.5)、n-二(羟乙基)甘氨酸(pka8.3)、hepes(pka7.5)、mes(pka6.1)、mops(pka7.2)、pipes(pka6.8)、tris(pka8.1)、咪唑(pka6.9)、甘氨酸(pka2.3)、乙酸盐(pka4.7)、柠檬酸盐(pka6.4)、磷酸盐(pka7.21、2.16、12.32)、苹果酸盐(pka5.13)、二甲砷酸盐(cacodylate)(pka6.27)等。同样,本公开可以排除包括以上缓冲液中的一种或多种的制剂,并且可以排除包括这些制剂之一的装置。不考虑任何缓冲液,本公开提供了具有的如在室温下可测量的ph值为以下的制剂或提供制剂的组分:约3.0、3.1、3.2、3.3、3.4、3.5、3.6、3.7、3.8、3.9、4.0、4.1、4.2、4.3、4.4、4.5、4.6、4.7、4.8、4.9、5.0、5.1、5.2、5.3、5.4、5.5、5.6、5.7、5.8、5.9、6.0、6.1、6.2、6.3、6.4、6.5、6.6、6.7、6.8、6.9、7.0、7.1、7.2、7.3、7.4、7.5、7.6、7.7、7.8、7.9、8.0、8.1、8.2、8.3、8.4、8.5、8.6、8.7、8.8、8.9、9.0等。在排他性实施方式中,本公开可以排除具有的如在室温下可测量的ph值为以下的制剂或可以排除制剂的组分:约3.0、3.1、3.2、3.3、3.4、3.5、3.6、3.7、3.8、3.9、4.0、4.1、4.2、4.3、4.4、4.5、4.6、4.7、4.8、4.9、5.0、5.1、5.2、5.3、5.4、5.5、5.6、5.7、5.8、5.9、6.0、6.1、6.2、6.3、6.4、6.5、6.6、6.7、6.8、6.9、7.0、7.1、7.2、7.3、7.4、7.5、7.6、7.7、7.8、7.9、8.0、8.1、8.2、8.3、8.4、8.5、8.6、8.7、8.8、8.9、9.0等。可以测量作为纯组分的组分的ph,即在与其他组分组合以生成制剂之前测量。
口腔贴剂、舌下贴剂及相关丸剂、片剂和条状物
本公开涵盖用于口中的基于贴剂的递送系统。在口中,用于药物递送的区域包括舌下粘膜(舌下方的区)和颊粘膜(面颊内膜)。通过将药物与表面活性剂组合进行配制或作为与亲水性环糊精的复合物进行配制或通过使用纳米悬浮液(粒径在纳摩尔范围内,诸如50nm至150nm),可以促进低水溶解度药物的颊给药(参见,raoetal(2011)int.j.nanomedicine.6:1245-1251)。可以通过碾磨、均质化或超声处理来制造纳米颗粒。
颊囊是在面颊与牙床之间的空间。将颊剂型插入到颊囊中(参见zerbe的us8,735,374,将其以其全文并入本文)。口腔贴剂可以包括当暴露于水时,导致乳化剂的水合诱导形成的乳化剂。当水与乳化剂接触时,乳液可自发地,即,在没有大量能量供应或没有剪切力的情况下形成。当抵靠牙床放置时,被吸进口腔贴剂的唾液可以是水的来源。自-乳化剂增强了制剂粘附到粘膜表面的趋势,从而促进了药物诸如大麻素的吸收(参见,dam的us7,709,536和bender的us8,642,080,其各自通过援引以其全文并入本文)。
这描述了制造的溶剂浇铸和直接碾磨方法。在不暗示任何限制的情况下,口腔贴剂可以由两个层压体组成,其中将粘合剂聚合物的水性溶液浇铸在不可渗透的背衬片上。一种类型的粘合剂薄膜可以包括羟丙基纤维素和有机酸的醇溶液。即使在存在流体下,该粘合剂薄膜也适当地停留至少12小时。可以通过溶剂浇铸或通过直接碾磨来制造粘合剂贴剂。在溶剂浇铸中,将全部赋形剂和药物分散在有机溶剂中,并涂覆在剥离衬垫片上。在溶剂蒸发后,将保护性材料的薄层层压在涂覆的剥离衬垫片上以形成层压体。然后将层压体切割成贴剂(koyiandkhan(2015)buccalpatches:areview.int.j.pharmaceuticalsciencesres.4:83-89)。
在直接碾磨中,在不使用溶剂的情况下产生贴剂。通常在不存任何液体的情况下,通过直接碾磨或通过捏合来将药物和赋形剂混合。碾磨后,将材料在剥离衬垫上轧制。然后施加背衬层。直接碾磨避免了残留溶剂的问题(koyiandkhan(2015)buccalpatches:areview.int.j.pharmaceuticalsciencesres.4:83-89)。
涉及溶剂浇铸方法和热熔挤出方法。在不暗示任何限制的情况下,可以通过溶剂浇铸方法和通过热熔挤出方法制造颊薄膜。溶剂浇铸涉及溶解水溶性聚合物以形成粘性溶液。将赋形剂溶解在溶剂中,以给出澄清的粘性溶液。然后,将两种溶液混合(水溶性聚合物溶液;赋形剂溶液),并然后浇铸成薄膜,并然后使其干燥。这涉及热熔挤出。药物或药物的组合处于干燥状态,并将其填充入料斗中,混合,加热,并然后以熔融状态挤出。形成的熔融的块用于浇铸薄膜(madhavietal(2013)buccalfilmdrugdeliverysystem--aninnovativeandemergingtechnology.j.mol.pharm.org.processingres.vol.1,issue3(6pages))。
在不暗示任何限制的情况下,可以通过将聚合物溶解在溶剂中以产生粘性溶液来制造粘膜粘合剂贴剂。聚合物可以是羟丙基甲基纤维素(hpmc)e5lv和
用于评估药物释放的弗朗兹(franz)扩散池
弗朗兹扩散池用于测量整体式贴剂(monolithicpatch)和储库型贴剂的药物释放动力学。描述了弗朗兹扩散池(参见,cavallarietal(2013)eur.j.pharm.biopharm.83:405-414;franz(1968)onthediffusionoftritiatedwaterthroughskin.j.invest.dermatol.50:260;balazs,sipos,danciu(2015)biomedicalopticsexpress.7:67-78;simonetal(2016)int.j.pharmaceutics.512:234-241;jungetal(2016)int.j.cosmet.sci.38:646-650;technicalbrief2009,vol.10,developmentandvalidationinvitroreleasetestingmethodsforsemisolidformulations,particlesciences,bethlehem,pa)。弗朗兹扩散池和用于透皮扩散测试的设备是可获得的(teledynehansonresearch,chatsworth,la)。
如下文所描述的,本发明的发明人使用弗朗兹池来评估释放动力学。为了测试其中使用半固体粘合剂基质的透皮整体式贴剂的释放动力学,弗朗兹池自顶到底具有以下组件:(1)用于密封供体室的顶部的塞子;(2)供体室;(3)位于供体室的最底部的贴剂,其中贴剂的粘合剂侧附连在人尸体皮肤上;(4)定位于贴剂正下方的人尸体皮肤;(5)定位于皮肤正下方的接收室。接收室填充有乙醇/水溶液;(6)定位于接收室的底部的磁力搅拌器。
为了测试透皮储库型贴剂的释放动力学,弗朗兹池自顶到底具有以下组件:(1)用于密封供体室的顶部的塞子;(2)供体室;(3)供体室中的乳膏或凝胶;(4)微孔膜(来自lydallperformancematerials,inc.,罗切斯特(rochester),新罕布什尔州(nh)的
用于测试本公开的贴剂的弗朗兹池的接收溶液
这涉及用于测试本公开的整体式贴剂和皮肤贴剂的接收溶液。接收溶液可以是用于可溶于水的药物的盐水溶液,或者用于不很好地可溶于盐水的药物的醇-水溶液。
根据bartosovaandbajgar(2012)currentmedicinalchemistry.19:4671-4677,皮肤吸收(dermalabsorption)涉及以下这些步骤:(1)穿透.物质进入皮肤的具体层,诸如是“角质层”的该层;(2)渗透.这是穿过一层到另一层的穿透,其中这些层在结构和功能上都彼此不同;(3)吸收.物质被摄入到淋巴或血流。角质层是亲油的,而相反,表皮和真皮是亲水性的。因此,亲油分子可以以更大的速率穿过角质层,而相反,亲水性分子可以以更大的速率穿过表皮和真皮。转移速率可以由弗里克定律(frick'slaw)表示:jss=(kp)(co)。jss是每单位面积的稳态通量。kp是给定溶质在给定媒介物中的渗透系数(厘米/小时)。co是供体室中的溶质的浓度。kp预测同一媒介物在给定浓度下的化学品的穿透率。kp独立于浓度和时间。
根据上述bartosova和bajgar,用于体外皮肤吸收测试的指导可从oecd(2004)oecdguidelineforthetestingofchemicals.skinabsorption:invitromethod.pages1-8)获得。扩散池常用于测量体外皮肤吸收,并且这些可以是静态类型或流通类型。弗朗兹扩散池具有以下结构,自顶到底按次序为:供体室(包含测试物质,诸如药物);膜(其中安置皮肤的支撑膜);带有允许进入受体室的采样端口的受体室;受体室的下半部周围是用于维持温度的水夹套;在受体腔室内部的底部处,并与受体室中的流体接触的是磁力搅拌器。任选地,研究员可以包括具有标准品,诸如苯甲酸、咖啡因和睾酮的皮肤吸收测试。
同样,根据上述bartosova和bajgar,使用的剂量浓度最高达10mg/cm2或最高达10微升/cm2。在向皮肤施加剂量之前,用受体流体将皮肤样品平衡10-30分钟。通过确定经皮水分丢失或经皮电阻的方法检查皮肤的屏障完整性。可以确定的动力学参数包括通量(j)、渗透系数(kp)和扩散系数(d)。当测试期到达其预定的终点时,例如,在三小时后或24小时后,一些测试物质可能仍定位于皮肤内部,即皮肤细胞的膜和胞质溶胶中。皮肤内部的测试物质可以任选地包括在吸收的总物质的值中。
人皮肤的来源
对于cbd和thc,发明人使用了接收溶液乙醇/水混合物(按重量计30/70)。尸体皮肤,发明人从组织库诸如在亚利桑那州的凤凰城(phoenixaz)的科学关怀(sciencecare)接受皮肤。在科学关怀中将供体人皮肤取皮成由角质层和部分表皮层组成的约250微米的厚度,并将其在干冰上运送给发明人。
在接收供体人皮肤之后,发明人通过将皮肤解冻至室温,在蒸馏水中洗涤并切割成圆片以适配弗朗兹池开口的直径,来准备用于在弗朗兹池中进行测试的皮肤。在将贴剂放在人皮肤上之前,发明人用纸巾干燥皮肤。将附连有贴剂的皮肤放在上供体室与下接收室之间,并将其紧紧夹住。在那之后,将接收溶液填充到接收室中,确保没有气泡被捕获在皮肤之下。测试通常持续24hr,并在不同时间段后从接收室抽取出150ml的等分试样,并将其在hplc上进行分析。接收溶液中药物浓度对比时间的显示由示出了药物从贴剂穿过皮肤进入接收溶液的透皮通道的动力学的图呈现。
测量薄膜和贴剂的厚度
可以使用穿刺测试和质构分析仪,诸如
可以用螺纹量规测量贴剂厚度,其中厚度可以在贴剂上的不同位置点处测量。为了测量表面ph,可以使贴剂在琼脂板(2%w/v)表面上溶胀2小时,以及然后用ph纸测量ph。通过将贴剂放在琼脂板上后在六小时内每小时称重,可以测量溶胀(参见,vermaetal(2014)effectofnovelmucoadhesivebuccalpatchesofcarvediolonisopenaline-inducedtachycardia.j.adv.pharm.technol.res.5:96-103)。停留时间测量以下时间:贴剂粘附到粘膜上,其中贴剂粘贴在基材上,其中基材重复上下运动直到贴剂分开(参见,ismailetal(2003)designandcharacteristicsofmucoadhesivebuccalpatchescontainingcetylpyridiniumchloride.actapharm.53:199-212。
用于储库型贴剂装置的凹坑型储库(dimple-stylereservoir)对比球囊型储库(balloon-stylereservoir)
在球囊实施方式中,本公开可以包括符合像密封袋(或像连续袋)或像密封球囊的储库。在这种实施方式中,储库由与背衬分离并且与可渗透层分离的材料制成。在这种实施方式中,储库可以通过粘合剂或热密封附连或不附连至背衬或可渗透层。
在凹坑实施方式中,储库在远侧具有带有凹坑(或外翻)的背衬,其中凹坑适于容纳药物,以及其中储库在近侧具有可渗透层。换句话说,防止药物从外翻中溢出的是这种可渗透层。
背衬和可渗透层彼此附连,以防止药物泄漏。可以经由粘合剂或热密封进行附连。本公开可以排除其中这种附连是通过粘合剂的装置,以及可以排除其中这种附连是通过热密封的装置。
本公开可以排除具有球囊储库的装置。在其他实施方式中,本公开可以排除具有凹坑储库的装置。
在凹坑实施发方式中,可渗透层可以包括多个狭缝、多个微小孔,或者由多孔层制成。本公开可以排除具有凹坑储库的装置。
凹坑储库型装置可以包括(或排除)存在于药物与可渗透层之间的层。同样,凹坑储库型装置可以包括(或排除)存在于面向皮肤的可渗透层的一侧上的层,其中该层与可渗透层大量接触。在皮肤的可渗透层的一侧的这种层可以在粘合剂层和可剥性背衬层的远侧。
可渗透层可以包括可渗透聚丙烯薄膜(us2006/0024520;us20016/115585)、可渗透聚乙烯薄膜(us4,793,003;wo2006/070672);可渗透聚氨酯薄膜(us9,566,423)。
随着时间的进程改变递送速率的储库的形状
本公开的储库可以预定形状制造,使得当患者佩戴贴剂装置时的时间范围期间,活性剂在数小时的进程中释放到皮肤或粘膜表面的速率不同。例如,储库可以是锥形的,其中宽的表面(锥体的底部)位于贴剂装置的远侧部分,以及其中锥体的点位于贴剂装置的近侧部分。近侧意指贴剂装置最靠近皮肤的一侧,远侧意指贴剂装置最远离皮肤的一侧。使用锥体储库时,药物从贴剂转移到皮肤或粘膜表面的速率随着时间的推移逐渐降低。储库可以是半球形的,类似于胶滴,其中胶滴的底部最靠近贴剂装置的近侧,而胶滴的圆形表面最靠近贴剂装置的远侧。半球形储库给予药物释放的初始快速速率,随后药物释放速率快速降低。储库还可以具有垂直于贴剂的面向皮肤的部分,即垂直于皮肤贴剂的可剥性释放的边缘(在贴剂具有可剥性释放的情况下)。参见herrman的us6,207,181,其通过援引以其全文并入本文。本公开可以排除具有锥形储库、半球形储库的装置和/或半球形储库。
本公开的储库型装置可以具有仅一个锥形储库、仅两个锥形储库、仅三个锥形储库、至少一个锥形储库、至少两个锥形储库、至少三个锥形储库。储库型装置可以具有仅一个、仅两个、仅三个、至少一个、至少两个、至少三个半球形储库。储库型装置可以具有仅一个、仅两个、仅三个、至少一个、至少两个、至少三个垂直侧面的储库。此外,储库型装置可以具有一个或多个仅锥形储库、一个或多个仅半球形储库、一个或多个仅平行侧面的储库、仅一个或多个锥形储库和一个或多个半球形储库的组合、仅一个或多个锥形储库和一个或多个平行侧储库的组合、仅一个或多个半球形和一个或多个平行侧储库的组合,或锥形、平行侧和半球形储库的全部三种的组合。本公开还提供了模糊形状的储库,诸如单独地或与锥形、半球形和/或平行形状的储库组合的类似于褶皱的、部分填充的球囊的储库。本公开还提供了单独地或与锥形、半球形和/或平行形状的储库组合的具有热狗形状的储库。
损害对贴剂装置的干预的脆性中空突出物
在实施方式中,本公开提供或可以排除损害使用者进行物理提取活性成分的尝试和/或损害使用者通过溶剂进行提取活性成分的尝试的贴剂装置。使用者可能想要从皮肤贴剂中回收活性成分,以进行口服自给药或用于注射。脆性中空突出物优选地作为从粘合剂贴剂的主体起的突出物,例如,作为从粘合剂贴剂的远侧背衬起的突出物(远侧意指离皮肤最远的一侧)出现。可以类似于“纤毛”的脆性中空突出物被制造成使得它们比粘合剂贴剂的主体更脆性,或者比任何粘合剂贴剂的“壁”更脆性。当使用者尝试物理地回收活性成分时,脆性突出物会破坏,释放出活性成分的拮抗剂。同样,当使用者尝试使用溶剂以提取活性成分时,脆性突出物溶解(在某种程度上)释放活性成分的拮抗剂。脆性中空突出物是刚性的,并且具有的壁比贴剂装置本体的壁更薄,其中目的是确保物理干预优选地使脆性中空突出物破裂(释放拮抗剂)并促进释放的拮抗剂与活性成分的紧密靠近和混合。参见,royds的us7,740,879和royds的us2012/0238970,其通过援引并入本文。在排他性实施方式中,本公开可以排除包括脆性中空突出物的任何贴剂装置,和/或可以排除可由溶剂等溶解的突出物。
快速溶解的薄膜
可以快速溶解的薄膜提供药物或其他活性物质,例如,用于口腔贴剂或舌下装置充当水的来源,以及其中将水吸进贴剂或装置中并溶解薄膜,导致药物从薄膜中释放以及药物向使用者的粘膜表面迁移。
薄膜已经被用作丸剂和片剂的替代方案。薄膜可以包含活性成分,其中活性成分均匀地分布在整个薄膜中(yang的us2005/0184427,其通过援引以其全文并入本文)。可以使用各种技术,诸如在干燥薄膜之前使用增加粘度的化学品作为薄膜的液体组合物的一部分来增强均匀性。增强均匀性的另一种技术是以避免在薄膜(其中底表面存在于表面或基材上)的顶表面上形成皮的方式干燥薄膜。与使用热空气的强制空气干燥机一样,热干燥的问题在于表面生长皮。皮阻断水蒸发,导致内部水蒸气积累,其中蒸气撕开薄膜,引起波纹并引起药物分布不均匀。通过将液体薄膜组合物倒在表面或基材上,并且仅加热底部(而不是顶部),可以增强均匀性(参见,magoon的us4,631,837)。替代地或除了底部加热之外,可以通过将成膜聚合物与活性成分和水以及还有多元醇组合来产生薄膜基质。多元醇增加粘度。多元醇具有通式hoch2(choh)nch2oh,并且包括山梨糖醇、赤藓糖醇、甘油、甘露醇和阿拉伯糖醇(lin(1961)j.biol.chem.236:31-36,gerlsma(1968)j.biol.chem.243:957-961)。成膜聚合物包括短梗霉聚糖、羟丙基甲基纤维素、羟乙基纤维素、聚乙烯吡咯烷酮、羧甲基纤维素和聚乙烯醇。在排他性实施方式中,本公开可以排除包括多元醇、成膜聚合物或薄膜中的一种或多种的任何装置。
乳液和自乳化剂
本公开提供了乳液、乳化剂、自乳化剂、乳膏和洗剂。以下提供了自乳化剂的实例。已经对自乳化药物递送系统(sedds)和纳米自乳化药物递送系统(snedds)进行了综述(参见,cherniakovetal(2015)expertopin.drugdeliv.12:1121-1133)。自乳化剂包括单硬脂酸甘油酯、单油酸甘油酯和cremophor
增溶剂sl-11是一种提供适于包含疏水性药物的纳米乳液的自乳化剂(nofamericacorp.,尔湾市(irvine),加利福尼亚州)。可以通过以下这些步骤制造粒度小于50纳米的乳液:(1)将药物溶解在合适的溶剂,诸如乙醇中;(2)将(1)中制备的药物溶液添加到增溶剂sl-11中,充分混合以使内容物完全溶解;(3)制造具有溶剂的药物/sl-11溶液;(4)在50度下蒸发溶剂约1小时以去除溶剂,或在氮气流下去除溶剂;(5)制造sl-11和药物的浓缩溶液;(6)可以通过使用(5)中的浓缩溶液来制备软胶囊(nofamericacorp.,尔湾市,加利福尼亚州)。
以下提供了其他-非限制性实例。根据shahetal(1994)int.j.pharmaceutics.106:15-23,可以使用具有不同脂肪酸和聚乙二醇(peg)链长的经聚乙二醇处理的甘油酯(polyglycolyzedglyceride)(pgg)制造自乳化剂,其中这些在水中产生油自乳化。所得乳液的品质取决于所选择的油和乳化剂对,以及取决于作为乳化剂的pgg的浓度。一种合适的油是具有中链甘油三酯的油(辛酸和癸酸;neobee
自乳化剂的又其他-非限制性实例由chambinetal(2004)int.j.pharmaceutics.278:79-89提供。这描述了使用来自月桂酰基聚乙二醇甘油酯家族的赋形剂
devani(2004)j.pharmacypharmacology.56:307-316,提供了使用药物达那唑和甲芬那酸的以下实例。在自乳化药物递送系统(sedds)中,药物分散在与水接触就会乳化的油-表面活性剂混合物中。自乳化系统可以基于labrafilz家族的经聚乙二醇处理的油(polyglycolysedoil),使用tween80和tween20作为表面活性剂。亲水性更高的油-表面活性剂混合物示出更易于乳化以及较小的粒度。观察到在混合物的亲水亲油平衡(hlb)与达那唑和甲芬那酸两者的溶解度之间的线性关系,其中亲水性更高的混合物示出越大的药物溶解度值。
这提供了其他-非限制性实例。zupancicetal(2016)eur.j.pharm.biopharm.109:113-121描述了由长链脂质(lc-sedds)、中链脂质(mc-sedds)、短链脂质(sc-sedds)和无脂质(nl-sedds)构成的sedds的乳化特性。药物依诺肝素经由疏水性离子对掺入所选的sedds中。所选的lc-sedds、mc-sedds和nl-sedds的平均液滴大小范围在30与40nm之间。包含30%captex8000、30%capmulmcm、30%cremophorel和10%丙二醇的mc-seeds和包含31.5%labrafil1944、22.5%capmulpg-8、9%丙二醇、27%cremophorel和10%dmso的nl-sedds展示出的粘液扩散是lc-sedds的2倍。mc-sedds和nl-sedds两者均示出持续的体外依诺肝素释放。口服给药的mc-sedds和nl-sedds产生的绝对依诺肝素生物利用度分别为2.02%和2.25%。
进一步关于乳液,可以通过亲水亲油平衡(hlb)来表征乳化剂。hlb系统编号为1到20。hlb值为3至6是亲油的,并且这些形成油包水乳液(参见,vadlamudi,hyndavi,andtejeswari(2014)currentdrugdiscoverytechnologies.11:169-180)。hlb值为8至18是亲水性的,并且这些形成水包油乳液(参见,grimberg,nagel,andaitken(1995)environ.sci.technol.29:1480-1487)。
渗透促进剂
本公开提供了例如与皮肤贴剂或口腔贴剂一起使用的渗透促进剂。合适的渗透促进剂包括23-月桂基醚、抑蛋白酶多肽、氮酮、苯扎氯铵、氯化鲸蜡基吡啶鎓、鲸蜡基三甲基溴化铵、环糊精、葡聚糖硫酸酯、月桂酸、月桂酸/丙二醇、溶血磷脂酰胆碱、薄荷醇、甲氧基水杨酸酯、油酸甲酯、油酸、磷脂酰胆碱、聚氧乙烯、聚山梨酸酯80、edta钠、甘氨胆酸钠、甘氨脱氧胆酸钠、月桂基硫酸钠、水杨酸钠、牛磺胆酸钠、牛磺脱氧胆酸钠、亚砜和烷基甙(alkylglycosides)(参见,shojaeietal(june2001)systemicdrugdeliveryviathebuccalmucosalroute.pharmaceuticaltechnology.pages70-81)。本公开的其他促进剂是1-辛醇、2-乙基己醇、1-壬醇、1-癸醇等。
本公开的渗透促进剂可以是具有脂质相和水相的两相组合物。可以通过混合棕榈酸异丙酯和卵磷脂来制备脂质相。水相可以是水和表面活性剂的混合物。表面活性剂可以是
plogel是“pluronic卵磷脂有机凝胶”(pharmedicaenterprise,雪兰莪州(selangor),马来西亚(malaysia))。plogel采用水性相(240ml泊洛沙姆407、山梨酸钾、水)和有机相(60ml卵磷脂、棕榈酸异丙酯、山梨酸)的形式。本公开可以排除包括plogel、泊洛沙姆407、山梨酸钾、棕榈酸异丙酯、山梨酸、卵磷脂等中的一种或多种的任何制剂、组合物,装置,方法等。
在排他性实施方式中,本公开可以排除涵盖以上聚合物、聚合物化合物和交联的聚合物组合物之一的任何制剂、组合物、装置、方法等。
在其他排他性实施方式中,本公开可以排除包括亚砜诸如dmso、氮酮和氮酮类似物诸如月桂氮
生物粘合剂材料
当溶胀时,本公开的生物粘合剂聚合物产生其中药物可以穿过其扩散的柔性网络。生物粘合剂材料充当用于保留药剂的基质,直到将贴剂施加到消费者的皮肤或粘膜表面上为止。生物粘合剂材料包括羟丙基纤维素、carbopol、聚(乙烯吡咯烷酮)、羧甲基纤维素钠、羟乙基纤维素、聚卡波非、果胶、壳聚糖、黄胞胶、槐豆胶、羟丙基甲基纤维素、聚(乙烯醇)、聚(异戊二烯)、聚(异丁烯)(参见,shojaeietal(june2001)systemicdrugdeliveryviathebuccalmucosalroute.pharmaceuticaltechnology.pages70-81)。
具有多个粘合剂层的皮肤贴剂
本公开提供了包括多个粘合剂层的皮肤贴剂、层压片以及相关方法。在一种实施方式中,整体式贴剂从最远侧到最近侧具有以下这些层:(1)背衬;(2)粘合剂;(3)包含活性剂的载体层;(4)接触粘合剂以及(5)保护性衬垫。在排他性实施方式中,本公开可以排除这种实施方式。
在特征在于具有“速率控制层”的其他实施方式中,整体式贴剂从远侧到近侧具有以下这些层:(1)背衬;(2)粘合剂;(3)包含活性剂的载体层;(4)粘合剂层;(5)速率控制聚合物层;(6)粘合剂层;以及(7)保护性衬垫。在排他性实施方式中,本公开可以排除这种实施方式。
以下涉及其中存在“载体层”并且其中载体层在远侧表面和侧向表面上被粘合剂层围绕并与之接触,以及其中载体层在近侧表面上被“活性成分可渗透的皮肤接触粘合剂层”围绕并与之接触的实施方式。更通常而言,本公开涵盖采用其中第一层具有远侧表面、近侧表面和侧向表面的皮肤贴剂或其他医疗装置的形式的“帽形件(hat)实施方式”。在这种“帽形件实施方式”中,远侧表面、近侧表面和侧向表面都被“帽形件层”围绕并与之接触。帽形件层可以是粘合剂层,或它可以是不可渗透的背衬层。术语“帽形件实施方式”和“帽形件层”是指以下事实:“帽形件层”以与男人的帽子覆盖他的头的顶部以及他的耳朵、前额和他的头的后部相同的方式覆盖第一层。本公开提供了从远侧到近侧具有以下这些层的装置:(1)背衬;(2)粘合剂;(3)载体层;(4)活性成分可渗透的皮肤接触粘合剂;以及(5)保护性衬垫。在这种实施方式中,“帽形件”可以覆盖载体层的侧向侧,以及也覆盖“活性成分可渗透的皮肤接触粘合剂层”的侧向侧。在排他性实施方式中,本公开可以排除上述“帽形件”实施方式。
在其他“帽形件”实施方式中,本公开从远侧到近侧提供:(1)背衬;(2)粘合剂层;(3)载体层;(4)活性成分可渗透层;(5)速率控制聚合物层;以及(6)活性成分可渗透的皮肤接触层。“帽形件”采用背衬加粘合剂层的形式,并且它们覆盖了所有这四个层:载体层、活性成分可渗透层、速率控制聚合物层和活性成分可渗透的皮肤接触层的侧向侧。在排他性实施方式中,本公开可以排除上述“帽形件”实施方式。
在其他排他性实施方式中,本公开可以排除以下装置,其中:(1)载体层与背衬层直接且大量接触;(2)载体层与粘合剂层直接且大量接触;(3)粘合剂层与速率控制聚合物层直接且大量接触;(4)粘合剂层与保护性衬垫直接且大量接触;(5)其中装置包括“帽形件”层配置;(6)载体层与活性成分可渗透层直接且大量接触,(7)活性成分可渗透的皮肤接触层与保护性层直接且大量接触;(8)活性成分可渗透的皮肤接触层与剥离衬垫或保护性衬垫直接且大量接触;(9)其中装置的至少部分具有“帽形件”配置,并且其中仅一层被帽形件覆盖(在近侧面和侧向面上围绕);(10)其中装置的至少部分具有“帽形件”配置,并且其中仅两层被帽形件覆盖(在近侧面和侧向面上围绕);(11)其中装置的至少部分具有“帽形件”配置,并且其中仅三层被帽形件覆盖(在近侧面和侧向面上围绕);(12)其中装置的至少部分具有“帽形件”配置,并且其中仅四层被帽形件覆盖(在近侧面和侧向面上围绕)。本公开的排他性实施方式涵盖以上排他项的任何组合。以上可以适用于其中“储库”任选地代替“载体层”的储库型贴剂。同样,以上可以适用于整体式贴剂。
电实施方式
本公开涵盖用于离子电渗入疗法的电穿孔(electroporative)或电穿孔递送活性物质诸如药物的具有电路的皮肤贴剂装置。以下布置使用电力将药物自“保持器”离开并进入皮肤。该布置从最远侧层到最近侧层包括以下。当将贴剂粘附地放在皮肤上时,远侧意指贴剂距皮肤最远的部分,以及近侧意指贴剂距皮肤最近的部分。布置可以是:(1)具有位于堆层的顶部上的远侧端(或层)以及存在于大部分层的下方但位于“保持器”的顶部上的近侧端的导电粘合剂电极;(2)可以包括二氧化锰的正极层;(3)电解质层;(4)可以包括锌粉的负极层;以及(5)医用电极”。医用电极直接接触皮肤,并且电流自医用电极离开流动通过保持器(将药物驱动自保持器离开并进入皮肤),且然后流过皮肤,并且到导电电极的近侧端。在贴剂中,导电粘合剂电极的任何部分都不会接触医用电极。绝缘体可以用于(在贴剂的结构中)将导电粘合剂电极与医用电极分开。保持器可以是与贴剂分开的结构,或可以将保持器制造成与贴剂连接。参见,nitzan的us7,643,874和nitzan的us2010/0030129,其通过援引以其全文并入本文。
在排他性实施方式中,本公开可以排除包括一个或多个电极的任何装置。而且,公开可以排除其中与粘合剂贴剂分开制造的储库(或基质、层、多孔本体等)以及其中使用者例如医师或患者将储库与贴剂组装以产生稳定相关的贴剂和储库的任何装置。
营养品和药物
本公开提供了制剂、乳液等,以及口腔贴剂和皮肤贴剂,其中制剂、乳液、口腔贴剂和皮肤贴剂包含任选地与一种或多种大麻素组合的维生素b1、维生素d3、维生素b12或维生素c中的一种或多种。同样,制剂、乳液、口腔贴剂和皮肤贴剂可以包含西地那非。
制造方法和设备
将两个条状物在边缘处密封在一起,并协调横向密封以产生囊并填充囊
提供了以下方法:将两个条状物进料到带有辊的机器中以使条状物以相同速度移动,且使两个条状物向下移动,其中使第一条状物的第一面与第二条状物的第一面接触。使第一面接触第二条状物的第一面,以准备加热两个条状物的边缘,从而将两个条状物密封在一起,并准备以横向加热,以一定的距离和时间间隔加热,从而在两个条状物的夹层中产生多个口袋。当两个条状物向下移动时,定位第一条状物和第二条状物以形成向下移动的较厚的夹层。类似于轮子或辊的加热器,将在2-条状物夹层的边缘上向下夹紧,导致2-条状物夹层形成长的封闭管。当2-条状物夹层向下移动时,同时发生的是同时加热/密封横向夹具对。横向夹具在长的2-条状物夹层中产生单独的囊。当加热棒向下夹紧时,产生的是先前填充的囊的顶部密封,以及尚未填充的囊的底部密封。当产生囊时,每个囊的填充与通过加热轮子在边缘处的加热/密封同时发生,以及与通过横向棒的加热同时发生,其中当产生囊时,填充是通过向下到达到长的夹层中以填充每个囊的长管。参见,tucker的us6,871,477,其通过援引以其全文并入。第一条状物可以包括粘合剂层和可渗透膜,第二条状物可以是不可渗透的背衬,并且凝胶可以包括以凝胶形式的大麻素。
从轧辊中展开三个不同的层,从两个层中剥离剥离衬垫,将三个层对齐在一起以形成复合物,并将复合物轧制到轧辊上
本公开提供了可以展开多个轧辊,任选地具有从轧辊中的一个或多个上剥离剥离层,并且将剥离的剥离层卷取在空的转鼓或轧辊上的机械。例如,三个不同的轧辊可以包括三个不同的层压体,第一层压体包括:(1)保护性背衬;(2)合并的运输增强区和包容区(zoneofcontainment);以及(3)剥离层。第二层压体可以包括:(1)粘合剂层;(2)运输控制区;以及(3)剥离衬垫。而第三层压体可以包括:(1)支撑薄膜;(2)粘合剂;以及(3)在上述方法期间没有去除的可去除衬垫。机械可以分别在第一、第二和第三层压体的三个旋转机构上包括三个轧辊。机械可以包括用于卷取剥离衬垫的卷取轧辊。机械可以包括位于第一层压体和第二层压体的移动夹层的相对侧上的用于将两个层压体组合在一起的一对辊。同样,机械可以包括位于新产生的3-部分夹层的相对侧上的一对辊,其中3-部分夹层采用第一和第二层压体以及进入的第三层压体的组合(彼此接触)的形式。进入的第三层压体同时从其轧辊上展开,并然后与第一和第二层压体的复合物组合。然后,通过位于移动的最终产品的相对侧上的辊对来移动最终产品,以及还通过单独的辊,例如称为上辊、下轧辊和惰辊的辊来移动最终产品。以上公开的机械还可以包括用于将层压体密封在一起的装置,用于增强层压体密封在一起的电晕放电,用于在层压体从其轧辊展开时在层压体中的一个或多个上沉积药物或粘合剂或其他组合物的装置,以及用于将三个层压体的夹层分离成贴剂的切割装置。参见us5,370,924,其通过援引以其全文并入本文。
可以组装层状装置,以及然后将其通过真空成型或在不存在真空的情况下通过热密封来密封。在排他性实施方式中,本公开可以排除使用以下中的一种或多种制成的机械、方法和贴剂:真空成型、热密封、电晕放电、一个或多个展幅轧辊(crimproll)或配合压区(cooperatingnip)。
提供具有被通道分开的棒状区域的压板,并使用压板冲压层压体,以及在避免在包含药物和基质的区域上提供压力的同时,在需要崩塌的区域上提供压力
本公开提供了机械,诸如具有由通道分开的棒状区域的压板,并且其中棒状区域任选地被加热。压板可以用于选择性地压缩层压体的部分,其中层压体(“工件”)包括作为蜂窝区域的上层和作为皮肤粘合剂的下层。压板选择性地压缩远侧侧(右边缘和左边缘),导致层压体的远侧侧崩塌。任选地,仅预定要崩塌的层压体的部分提供有粘合剂。蜂窝区域可以是网状的,或者它可以是非网状的。蜂窝区域可以由发泡的热塑性树脂制成。蜂窝大小可以为约0.05、约0.1、约0.2、约0.4、约0.6、约0.80、约1.0、约1.2、约1.4、约1.6、约1.8、约2.0、约2.5、约3.0或约4.0毫米。崩塌的区域使得药物不能容易地通过崩塌的区域。在实施方式中,未崩塌的中心区(在压板制造过程期间存在于通道下方的区)可以包含与位于近侧的介质层接触的位于远侧的药物释放基质层(其包含药物),穿过介质层药物可以扩散。穿过其药物可以扩散的介质层可以是例如凝胶、乳膏或软膏。“远侧”意指将贴剂附连在皮肤上时远离皮肤,而“近侧”意指当贴剂附连在皮肤上时最靠近皮肤的贴剂的一侧上。贴剂的压缩侧向部分可以称为“带部”。参见,bello的us5,505,958,其通过援引以其全文并入本文。
在排他性实施方式中,本公开可以排除具有非压缩的蜂窝区域的贴剂装置、具有压缩的蜂窝区域的贴剂装置、具有位于远侧的药物基质以及药物以其方式穿过其可以扩散到皮肤的位于近侧的凝胶、乳膏、软膏或其他介质的层状结构。同样,本公开可以排除任何组合物、层压体、层状结构和经由加热层状结构或经由加热层压体制成的贴剂。
将药物放置在两个网状物之间,将两个网状物密封在一起,将密封的网状物压接以形成口袋,并切割密封的网状物
本公开提供了用于使用每个网状物都在辊上的两个不同的网状物作为起始材料的机械和方法,其中每个网状物包括薄膜、粘合剂层、不可渗透层、多孔层等中的一个或多个。最终产品采用密封在一起的两个网状物的形式,并且其中活性成分诸如包括大麻素和萜烯之一或二者的组合物包含在其中。在方法中,第一供应轧辊提供一个网状物,以及第二供应轧辊提供第二网状物。当网状物沿传送带移动时,各个“站点”处的机械会更改网状物之一或更改两个网状物。任选的一个站点是电晕放电站点。在通过两个展幅轧辊的操作将两个网状物结合在一起之前,电晕放电更改了一个或两个网状物的表面化学。电晕放电更改了表面化学以改善第一网状物和/或第二网状物的粘合特性。当要粘接非相似的材料(第一网状物的一种材料以及第二网状物的另一种材料)时,电晕放电是优选的。非相似的材料可以是例如聚酯聚合物和乙烯丙烯酸聚合物。
另一个站点是沉积站点,当网状物向展幅轧辊移动时,其将活性物质沉积在网状物之一上。沉积站点可以包括包含药物的储库以及从储库导向其中要沉积药物的网状物表面上的位置的管。沉积站点优选地在电晕站点之后出现。而且,沉积站点和电晕站点优选地作用在同一网状物上,尽管任选地,沉积站点可以在第一网状物上运行,而电晕站点可以在第二网状物上运行。这两个网状物在采用第一展幅轧辊和第二展幅轧辊的形式的站点中牢固地紧固在一起。这些轧辊类似于齿轮,在于第一展幅轧辊具有突出物,并且第二展幅轧辊具有凹陷,这些凹陷以“舌和槽”的方式混杂地作用,以将两个网状物压缩在一起,以及同时将连接的网状物冲压成口袋状形状。将啮合在一起的第一展幅轧辊和第二展幅轧辊的区域称为“配合压区”。
最终,在网状物通过电晕站点、药物沉积站点和展幅轧辊之后,通过旋转模切割机切割连接的网状物,以产生适合销售的柔性包装物或柔性贴剂。电机可以驱动辊。同样,电机可以驱动展幅轧辊。参见,williams的us4,782,647,其通过援引并入本文。
将切割的贴剂与未切割的贴剂带分开,并将切割的贴剂转移到载体上
这仅描述了用于制造粘合剂贴剂,例如,整体式装置和储库型装置的程序中的一个步骤。该程序涉及切割机、类似楔形物的传送装置和辊。辊以传送带的方式用于移动第一网状物和第二网状物。第一网状物采用以下形式:在顶部上的辅助层薄膜,以及然后在其正下方是位于载体薄膜的顶部上的包含药物的粘合剂层。然后稍后将具有这三个层的第一网状物增补有处理层,其中结果是由四个层组成(顶部上的处理层、然后辅助层薄膜、然后包含药物的粘合剂层以及底部上的载体薄膜)的网状物。较早发生的切割过程已经将辅助层薄膜和包含药物的粘合剂层切割成块。将第一网状物在一个方向,例如,向左移动,并然后在类似楔形物的传送装置的帮助下,将正方形物与载体薄膜分离(然后将载体薄膜向右移动)并也与辅助层薄膜和处理层(其向上移动)的组合分离,其中正方形物最终存在于载体薄膜上。此时,块彼此分离,并然后将用切割过程产生的任何废料丢弃。这是指其中切隔产生离散的块并在块之间产生废料的情况。支撑薄膜支撑块并向左移动。参见,asmussen的us6,059,913,其以其全文并入本文。
切割层压体以产生完全切出的区域,以及在其中的部分切割(刻划)的区域
本公开的机械、方法和工件包括层压体的片,其中将片的形状(矩形、椭圆形、圆形)完全切穿层压体,并且其中切出的层压体的边缘称为“周缘”(外切)。在切出的层压体为圆形的情况下,周缘与周向区域相同。除了在周缘处进行切割之外,在切割操作期间在周缘内的区域中同时对片进行切割(内切)。内切具有比外切小的直径。同样,内切具有比外切小的深度。在3-层层压体(剥离层;压敏粘合剂;背衬)的情况下,外切切开穿过全部三个层,而内层切开仅部分穿过顶层(剥离层)。这种部分切割更适当地称为“刻划”而不是“切割”。这种2-距离切割方法的目的是刻划剥离层,以促进使用者容易去除衬垫,以及同时避免在贴剂储存期间粘合剂从贴剂泄漏。用于2-距离切割方法的机械可以采用覆盖有切割压模(类似于饼干成型切割刀)的辊的形式。每个饼干成型切割刀一直通过层压体进行冲压。在每个饼干成型切割刀内均存在其大小使得其仅部分切穿层压体的顶层(从而仅刻划顶层)的第二(较小直径)饼干成型切割刀。在替代的机械中,第一辊承载一系列仅较大直径(和更长的切割距离)的饼干成型切割刀,而第二辊则承载一系列较小直径(和刻划距离)的饼干成型切割刀。在操作中,两个辊同时操作,并且第一辊上的饼干成型切割刀与第二辊上的饼干成型切割刀精确地对齐,并且在操作中,对于每个贴剂,切割(切穿所有层)与刻划同时发生。参见,sablotsky的us5,656,285,其通过援引以其全文并入。除了一个切割辊(或两个切割辊)之外,机械还可以具有用于驱动层压体的片的压力辊和支撑辊。在排他性实施方式中,本公开可以排除具有刻划区域,诸如刻划的剥离层的粘合剂皮肤贴剂。
穿孔的贴剂与废料网状物的有效分离
在粘合剂贴剂的制造期间,从由各种层组成的片上冲压出或切割出贴剂。这些层可以包括背衬、包含药物的基质、皮肤粘合剂和剥离层。在切割期间,当将废料网状物从片上拉出时,尚未与废料网状物分离的穿孔的贴剂中的一些可能会依附在废料网状物上。当将废料网状物拉出时维持这种依附时,结果是将与废料网状物一起的依附的穿孔的贴剂的不期望的丢弃。这种类型的不期望的依附可以通过以下增加:粘合剂从穿孔的贴剂的边缘流出,接着粘合剂流动以接触废料网状物。可以通过接触穿孔的贴剂且在将废料网状物向上拉以最终丢弃时将穿孔的贴剂推到水平移动的传送带上的一个或多个探头实现穿孔的贴剂的有效分离。探头可以采用旋转辊的形式,其中辊上覆盖有具有相同形状和完全相同尺寸的块(或与穿孔的贴剂相比,以面积计,尺寸为小约5%、小约10%、小约15%、小约20等)。如从“上方”观察,这些块可以具有的形状是正方形、矩形、椭圆形、圆形等,并且具有与穿孔的贴剂相对应的形状。从而,当辊旋转时,每个块都在相应的穿孔的贴剂上向下按压(当穿孔的贴剂继续在传送带上移动时),同时通过辊的旋转将废料网状物同时分开并向上拉。使用覆盖有块状探头的辊的替代方案是覆盖有柔性鬃的辊。当辊旋转时,鬃在穿孔的贴剂弹性地向下按压,鬃保持弯曲,使穿孔的贴剂与废料网状物分离。同时,按压在废料网状物上的鬃首先会弯曲很大,但是当废料网状物被向上拉时,鬃会弹出到它们的全(未弯曲的)长。参见,grader的us2017/0136648,其通过援引以其全文并入本文。在排他性实施方式中,本公开可以排除包括用于防止穿孔的贴剂粘附到废料网状物上的具有块的辊或具有鬃的辊的制造机械和方法。
制造散剂和凝胶
本公开提供了制造散剂的方法,包括将大麻素诸如thc与乙醇、peg、肉豆蔻酸异丙酯、carbopol、三乙醇、渗透促进剂、丙酮和水中的一种或多种组合并混合,并然后使用热量进行干燥,然后碾磨以形成散剂,并然后任选地添加低级醇,诸如乙醇、丙醇或丁醇,以形成凝胶。
防止形成药物晶体
如果不期望的晶体在任何溶液,诸如用于粘合剂的溶液、用于粘合剂/药物混合物的溶液或用于放置在储库中的药物基质的溶液中形成,则可获得加热步骤来防止这样的晶体。用于浇铸薄膜的程序可以包括使用浇铸溶液、干燥箱、层压机和退火炉。“退火”是指加热接着冷却至室温。可以使得退火的是液体分散体或由液体分散体形成的制品。模切已经发生后可能会出现不期望的晶体。即使用干燥剂去除水后,也可出现不期望的晶体。避免形成药物晶体的方法可以包括浇铸储库溶液以形成药物储库薄膜。药物储库薄膜可以在镀铝的聚对苯二甲酸乙二醇酯
排他性实施方式
本公开可以排除包括以下中的一种或多种的组合物、制剂、皮肤贴剂、使用方法、制造方法:辣椒素、2-花生四烯酸甘油(2-arachidonylglycerol)、姜黄素、单油酸甘油酯、单硬脂酸甘油酯、卵磷脂、金合欢胶、木糖醇、羧甲基纤维素、自乳化剂、甘油单硬脂酸酯、甘油单油酸酯、cremophor
可以排除的是具有1-5%促进剂的药物组合物。可以排除的是具有0.5-5%中和剂或具有任何量的中和剂的药物组合物。可以排除的是具有按重量计大于0%-5%或其任何量的肉豆蔻酸异丙酯的组合物。可以排除的是具有按重量计0%-10%的carbopol或具有任何量的carbopol的药物组合物。可以排除的是具有约10%乙醇、约15%、约20%、约24%、约30%、约35%、约40%、约45%、约50%、约55%、约60%、约65%、约70%、约75%、约80%、约85%、约90%乙醇的药物组合物。
为了递送大麻素,例如,溶剂/共溶剂的系统可以是乙醇(溶剂)/丙二醇(共溶剂)。溶剂可以是无水醇、乙醇、丙醇或异丙醇。共溶剂可以是丙二醇或peg。溶剂/共溶剂的比率(按重量计)可以为约5/95、约10/90、约15/85、约20/80、约25/75、约30/70、约35/65、约40/60、约45/55、约50/50、约55/45、约60/40、约65/35、约70/30、约75/25、约80/20、约85/15、约90/10、约95/5等。在排他性实施方式中,本公开可以排除其中比率为5/95、约10/90、约15/85、约20/80、约25/75、约30/70、约35/65、约40/60、约45/55、约50/50、约55/45、约60/40、约65/35、约70/30、约75/25、约80/20、约85/15、约90/10、约95/5等的溶剂/共溶剂组合物。
排除结构
本公开可以排除具有多于一个储库的粘合剂贴剂装置、口腔贴剂装置、舌下药物递送装置。本公开的贴剂装置可以具有仅一个储库、仅两个储库、仅三个储库、仅四个储库。本公开可以排除微针,并且可以排除具有微针的贴剂装置。本公开可以排除包括双层压体层、包括三层压体层,包括四层压体层的任何粘合剂贴剂装置、口腔贴剂装置、舌下药物递送装置。同样,本公开可以排除双层压体层,排除三层压体层以及排除四层压体层。
另外排他性实施方式
可以排除的是具有的乙醇含量为按重量计约5%、约10%、约15%、约20%、约25%、约30%、约35%、约40%、约45%、约50%、约55%、约60%、约65%、约70%、约75%、约80%、约85%、约90%、约95%的制剂。同样,可以排除的是具有的按重量计的乙醇含量涵盖约5%、约10%、约15%、约20%、约25%、约30%、约35%、约40%、约45%、约50%、约55%、约60%、约65%、约70%、约75%、约80%、约85%、约90%、约95%、约100%的制剂。此外,可以排除的是具有的按重量计的乙醇含量涵盖(等于以下的范围或包括以下的范围)为5-10%、10-15%、15-20%、20-25%、25-30%、30-35%、35-40%、40-45%、45-50%、50-55%、55-60%、60-65%、65-70%、70-75%、75-80%、80-85%、85-90%、90-95%或95-100%的范围的制剂。也可以排除的是涵盖以上制剂的一种或多种的装置。
本公开可以提供包括乙醇和丙二醇(或单硬脂酸甘油酯或单油酸甘油酯或甘油单酯或甘油二酯或甘油三酯或peg或磷脂或表面活性剂),以及其中比率(重量/重量基准)为约5/95、10/90、15/85、20/80、25/75、30/70、35/65、40/60、45/55、50/50、55/45、60/40、65/35、70/30、75/25、80/20、85/15、90/10或95/5的制剂。在排他性实施方式中,还可以排除的是包括乙醇和丙二醇(或单硬脂酸甘油酯或单油酸甘油酯或甘油单酯或甘油二酯或甘油三酯或peg或磷脂或表面活性剂),以及其中比率(重量/重量基准)为约5/95、10/90、15/85、20/80、25/75、30/70、35/65、40/60、45/55、50/50、55/45、60/40、65/35、70/30、75/25、80/20、85/15、90/10或95/5的制剂。
可以排除具有基于重量具体浓度的丙二醇或任何其他化合物的制剂。可以排除的是可以排除包含约约0.1%、约0.2%、约0.4%、约0.6%、约0.8%、约1.0%、约2%、约4%、约6%、约8%、约10%、约15%、约20%、约25%、约30%、约35%、约40%、约45%、约50%等的丙二醇、聚乙二醇(peg)、聚亚烷基二醇、乙醇、乳液(例如,水中的油滴、油中的水滴、脂质体悬浮液)、胶体、溶剂、透皮吸收促进剂、稳定剂、增溶剂(例如,表面活性剂、洗涤剂)、胶凝剂(以干燥状态或以水合状态)、水凝胶(以干燥状态或以水合状态)、粘合剂或任何其他化合物的制剂。
同样,可以排除的是涵盖(等于以下的范围或包括以下的范围)0-0.1%、0-5%、0-10%、0-20%、0-30%、0-40%、0-50%、5-10%、5-15%、5-20%、5-40%、5-50%、10-20%、10-30%、10-40%、10-50%、10-60%、10-70%、20-30%、20-40%、20-50%、20-60%、20-70%、20-80%、30-40%、30-50%、30-60%、30-70%、30-80%、40-50%、40-60%、40-70%、40-80%、40-90%、50-60%、50-70%、50-80%、50-90%、60-70%、60-80%、60-90%、60-100%、70-80%、70-85%、70-90%、70-95%、70-100%、80-85%、80-90%、80-95%、80-100%、85-90%、85-95%、85-100%等范围的丙二醇、聚乙二醇(peg)、乙醇、乳液(例如,水中的油滴、油中的水滴、脂质体悬浮液)、胶体、溶剂、透皮吸收促进剂、稳定剂、增溶剂(例如,表面活性剂、洗涤剂)、胶凝剂(以干燥状态或以水合状态)、水凝胶(以干燥状态或以水合状态)、粘合剂或任何其他化合物的制剂。在其他方面,本公开可以包括(涵盖、包含)包括处于所列举“约”值中任何一个以及处于所列举的范围内的任何一个的一种或多种以上化学品的制剂、组合物、装置或方法。
在不暗示任何限制的情况下,本公开可以排除包括以下化合物中的一种或多种的组合物,并且还可以排除包括以下化合物中的一种或多种的装置。可以排除的是以下化合物,该化合物是丁丙诺啡(buprenorphine)、可乐定(clonidine)、雌二醇、芬太尼(fentanyl)、格拉司琼(granisetron)、哌甲酯(methylphenidate)、硝酸甘油、奥昔布宁(oxybutynin)、东莨菪碱(scopolamine)、司来吉兰(selegiline)、睾酮(testosterone)、疫苗、流行性感冒病毒疫苗、哺乳动物激素、哺乳动物激素的合成类似物、化学修饰的哺乳动物激素、利多卡因、雌激素、水杨酸、避孕药、利斯的明(rivastigmine)、罗替高汀(rotogotine)、妥洛特罗(tulobuterol)、肾上腺素激动药、胆碱酯酶抑制药、多巴胺受体激动剂、奥昔布宁、安非他酮(bupropion)、伐尼克兰(varenicline)、尼古丁、抗抑郁药、戒烟药物、胆碱酯酶抑制药、哌甲酯、丁丙诺啡、阿片样物质镇痛药(opioidanalgesicagent)、舒马普坦(sumatriptan)、抗病毒药、抗逆转录酶病毒药、哺乳动物类固醇、哺乳动物类固醇的化学类似物、用于注意缺陷多动障碍的药等。
在实施方式中,本公开可以排除以下储库型装置:其中背衬不直接接触储库;或其中储库不直接接触亲水性多孔膜;或其中亲水性多孔膜不直接接触剥离衬垫;或其中储库不包含以下全部:(1)液体载体、(2)胶凝剂和(3)cbd。同样,可以排除的是不包括以上全部的储库型装置。
在实施方式中,可以排除的是粘合剂聚合物,或包括粘合剂聚合物的装置,其中该粘合剂聚合物与胺反应。还可以排除的是粘合剂聚合物或包括粘合剂聚合物的装置,其中该粘合剂聚合物具有任何游离的羟基基团。
可以排除的是粘合剂聚合物或包括粘合剂聚合物的装置,其中该粘合剂聚合物具有超过1个游离的羟基基团/100个粘合剂聚合物的原子。
可以排除的是粘合剂聚合物或包括粘合剂聚合物的装置,其中该粘合剂聚合物具有超过5个游离的羟基基团/100个粘合剂聚合物的原子。
同样,可以排除的是粘合剂聚合物或包括粘合剂聚合物的装置,其中该粘合剂聚合物具有超过10个游离的羟基基团/100个粘合剂聚合物的原子
此外,可以排除的是粘合剂聚合物或包括粘合剂聚合物的装置,其中该粘合剂聚合物具有超过20个游离的羟基基团/100个粘合剂聚合物的原子等。
在实施方式中,可以排除的是以下整体式装置:其中背衬不与皮肤粘合剂的基质直接接触;其中皮肤粘合剂的基质不与可剥离衬垫直接接触;其中基质不包括cbd;或以上全部。
还可以排除的是制剂或包括制剂的装置,其中该制剂具有超过1%的胶凝剂、超过2%、超过3%、超过4%、超过5%、超过6%、超过7%、超过8%、超过9%、超过10%、超过12%、超过14%或超过16%的胶凝剂。同样,可以排除的是制剂或包括制剂的装置,其中该制剂具有低于1%的胶凝剂、低于2%、低于3%、低于4%、低于5%、低于6%、低于7%、低于8%、低于9%、低于10%、低于12%、低于14%或低于16%的胶凝剂。
还可以排除的是制剂或包括制剂的装置,其中该制剂具有超过1%的透皮吸收促进剂、超过2%、超过3%、超过4%、超过5%、超过6%、超过7%、超过8%、超过9%、超过10%、超过12%、超过14%或超过16%的透皮吸收促进剂。同样,可以排除的是制剂或包括制剂的装置,其中该制剂具有低于1%的透皮吸收促进剂,低于2%、低于3%、低于4%、低于5%、低于6%、低于7%、低于8%、低于9%、低于10%、低于12%、低于14%或低于16%的透皮吸收促进剂。
在其他实施方式中,可以排除的是制剂、组合物、包括制剂的装置、包括组合物的装置,其中所述制剂或组合物具有的按重量计的cbd(或thc、或cbd和thc的结合重量)含量低于1%、低于2%、低于3%、低于4%、低于5%、低于6%、低于8%、低于10%、低于12%、低于14%、低于16%、低于18%、低于20%、低于25%、低于30%、低于35%、低于40%、低于45%、低于50%、低于55%、低于60%、低于65%、低于70%、低于75%等。同样,可以排除的是制剂、组合物、包括制剂的装置、包括组合物的装置,其中所述制剂或组合物具有的按重量计的cbd(或thc,或cbd和thc的结合重量)含量大于5%、大于6%、大于7%、大于8%、大于10%、大于12%、大于14%、大于16%、大于18%、大于20%、大于25%、大于30%、大于35%、大于40%、大于45%、大于50%、大于55%、大于60%、大于65%、大于70%等。在实施方式中,可以排除的是制剂、组合物、包括制剂的装置或包括组合物的装置,其中按重量计的百分数由上述“低于”或“大于”参数中的一个或多个限定。“组合物”可以指例如皮肤粘合剂的基质,或指亲水性多孔膜中的流体等。替代地,本公开可以包括如由“低于”参数或“大于”参数所阐述的以上组合物中的一种或多种。
而且,在实施方式中,可以排除的是以下任何装置:不包括闭塞系统聚合物薄膜、不包括聚乙烯闭塞聚合物薄膜、不包括pet闭塞聚合物薄膜、不包括由聚乙烯和pet两者制成的闭塞聚合物薄膜。同样,可以排除的是具有覆盖贴剂的装置以及不包括覆盖贴剂的装置。
在实施方式中,极性有机液体可以包括或可以排除以下中的一种或多种:甲醇,乙醇,丙醇,异丙醇,丁醇,戊醇,乙酸,丙酸,丁酸,戊酸,己酸,辛酸,癸酸,月桂酸,肉豆蔻酸,棕榈酸,硬脂酸,棕榈油酸,油酸,亚油酸,亚麻酸,具有5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24或更多个碳的直链烷烃,具有5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24或更多个碳的主链的支链烷烃,具有5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24或更多个碳的直链链烯烃(烯烃),具有5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24或更多个碳的主链的支链链烯烃(烯烃)等。替代地,本公开可以包括以上极性有机液体中的一种或多种。
本公开可以排除包括精油、植物油、蔬菜油或鱼油的组合物、装置、方法。同样,本公开可以排除包括一种或多种萜烯的组合物、装置、方法。可以排除的是包括薄荷油、橙油、柠檬油、火麻油、大麻油等中的一种或多种的组合物、装置、方法。同样,可以排除的是包括以下中的一种或多种的任何组合物、装置或方法:α-红没药醇、龙脑、α-石竹烯、β-石竹烯、榄香烯(α、β、γ或δ)、苧烯、莰烯、樟脑、δ-3-蒈烯、石竹烯氧化物、α-柏木烯(alpha-cedreen)、柠檬醛(citral)、桉树脑、β-桉叶油醇(beta-eudesmol)、桉叶油-7(11)-烯-4-醇(eudesm-7(11)-en-4-ol)、法呢烯(farnesene)、葑醇(fenchol)、α-愈创烯(alpha-guaiene)、香叶醇、愈创醇(guaiol)、大牻牛儿烯b(germacreneb)、愈创木-1(10)-11-二烯(guaia-1(10)-11-diene)、葎草烯(humulene)、α-葎草烯、异龙脑、芳樟醇、薄荷醇、香叶烯、α-香叶烯、β-香叶烯、橙花醇(nerol)、顺式-罗勒烯、反式-罗勒烯、α-水芹烯、α-蒎烯、β-蒎烯、长叶薄荷酮(pulegone)、桧烯、α-萜品烯、α-萜品醇、萜品油烯、萜品醇、百里酚(thymol)、反式-2-蒎烷醇(trans-2-pinanol)、芹烷-3,7(11)-二烯(selina-3,7(11)-diene)或朱栾倍半萜(valencene)。
同样,可以排除的是包括以下中的一种或多种的制剂、组合物、装置、锭剂或舌下丸剂:磷酸钠、磷酸钾、瓜尔胶、阿拉伯胶、槐豆胶、黄胞胶、角叉菜胶、槐树豆胶、加特胶、果胶、黄芪胶、金合欢胶、甘露醇、山梨糖醇、乳糖、改性乳糖、麦芽糖醇、甘露醇、硬脂酸镁、羟丙基甲基纤维素薄膜、非结晶糖或非结晶糖醇。
可以排除的是包括薄荷醇和肉豆蔻酸异丙酯的任何制剂、组合物、装置、方法等,该薄荷醇和肉豆蔻酸异丙酯处于以下比率(重量/重量)之一:200/10、180/10、160/10、140/10、120/10、100/10、90/10、80/10、70/10、60/10、50/10、40/10、30/10、20/10、15/10、10/10等,或以下比率之一:10/10、10/15、10/20、10/30、10/40、10/50、10/60、10/70、10/80、10/90、10/100、10/120、10/140、10/160、10/180、10/200等。同样,可以排除的是由以上两个比率值中的任何范围限定的组合物。同样,可以排除的是包括薄荷醇和肉豆蔻酸异丙酯的任何制剂、组合物、装置、方法等,该薄荷醇和肉豆蔻酸异丙酯处于以下比率(重量/重量)之一:约200/10、约180/10、约160/10、约140/10、约120/10、约100/10、约90/10、约80/10、约70/10、约60/10、约50/10、约40/10、30/10、20/10、15/10、10/10等,或以下比率之一:约10/10、约10/15、约10/20、约10/30、约10/40、约10/50、约10/60、约10/70、约10/80、约10/90、约10/100、约10/120、约10/140、约10/160、约10/180、约10/200等。同样,可以排除的是由以上两个比率值中的任何范围限定的组合物。
在装置实施方式中,本公开的装置基本上不含不是cbn的全部大麻素。在组合物实施方式中,本公开的组合物基本上不含不是cbn的全部大麻素。
在装置实施方式中,本公开的装置基本上不含四氢大麻酚(thc)、四氢大麻酚酸(thc-a)、大麻酚(cbn)和大麻色原烯(cbc)中的一种或多种。同样,本公开的装置基本上不含四氢大麻酚(thc)、四氢大麻酚酸(thc-a)、大麻酚(cbn)和大麻色原烯(cbc)中的每一种。在组合物实施方式中,本公开的组合物基本上不含四氢大麻酚(thc)、四氢大麻酚酸(thc-a)、大麻酚(cbn)和大麻色原烯(cbc)中的一种或多种。同样,本公开的组合物基本上不含四氢大麻酚(thc)、四氢大麻酚酸(thc-a)、大麻酚(cbn)和大麻色原烯(cbc)中的每一种。
在一方面,术语“基本上不含”可以意指thc、thc-a、cbn和cbc中的一种或多种的摩尔量的存在量是低于20%、低于15%、低于10%、低于5%、低于4%、低于2%、低于1%、低于0.5%、低于0.1%、低于0.05%或低于0.01%的cbd。在其他方面,术语“基本上不含”可以意指thc、thc-a、cbn和cbc中的每一种的摩尔量的存在量是低于20%、低于15%、低于10%、低于5%、低于4%、低于2%、低于1%、低于0.5%、低于0.1%、低于0.05%或低于0.01%的cbd。
以下测量方法考虑了组合物的物理性质以及包括组合物的容器或基质的物理性质。在测量“基本不含”的组合物时,可以测量的是由该组合物包括的全部化合物,其中该组合物采用油剂、糊剂、浆料、粘合剂、散剂、溶液等的形式,或采用容纳、包含、吸收、吸附等油剂、糊剂、浆料、粘合剂、散剂、溶液等的基质、储库、以及浸渍织物、烧瓶、导管的形式。
在不暗示任何限制的情况下,本公开可以排除包括以下化合物中的一种或多种的组合物,并且还可以排除包括以下化合物中的一种或多种的装置。可以排除的是以下化合物,该化合物是丁丙诺啡、可乐定、雌二醇、芬太尼、格拉司琼、哌甲酯、硝酸甘油、奥昔布宁、东莨菪碱、司来吉兰、睾酮、疫苗、流行性感冒病毒疫苗、哺乳动物激素、哺乳动物激素的合成类似物、化学修饰的哺乳动物激素、利多卡因、雌激素、水杨酸、避孕药、利斯的明、罗替高汀、妥洛特罗、肾上腺素激动药、胆碱酯酶抑制药、多巴胺受体激动剂、奥昔布宁、安非他酮、伐尼克兰、尼古丁、抗抑郁药、戒烟药物、胆碱酯酶抑制药、哌甲酯、丁丙诺啡、阿片样物质镇痛药、舒马普坦、抗病毒药、抗逆转录酶病毒药、哺乳动物类固醇、哺乳动物类固醇的化学类似物、用于注意缺陷多动障碍的药等。
在实施方式中,本公开可以排除以下储库型装置:其中背衬不直接接触储库;或其中储库不直接接触亲水性多孔膜;或其中亲水性多孔膜不直接接触剥离衬垫;或其中储库不包含以下全部:(1)液体载体、(2)胶凝剂和(3)cbd。同样,可以排除的是不包括以上全部的储库型装置。
在实施方式中,可以排除的是粘合剂聚合物,或包括粘合剂聚合物的装置,其中该粘合剂聚合物与胺反应。还可以排除的是粘合剂聚合物或包括粘合剂聚合物的装置,其中该粘合剂聚合物具有任何游离的羟基基团,其中粘合剂聚合物具有超过1个游离的羟基基团/100个粘合剂聚合物的原子,其中粘合剂聚合物具有超过5个游离的羟基基团/100个粘合剂聚合物的原子,其中粘合剂聚合物具有超过10个游离的羟基基团/100个粘合剂聚合物的原子,其中粘合剂聚合物具有超过20个游离的羟基基团/100个粘合剂聚合物的原子等。对于该排他性实施方式,技术人员应理解,任何聚合物均由大量原子,例如约五千个原子组成。
在实施方式中,可以排除的是以下整体式装置:其中背衬不与皮肤粘合剂的基质直接接触;其中皮肤粘合剂的基质不与可剥离衬垫直接接触;其中基质不包括cbd;或以上全部。
还可以排除的是制剂或包括制剂的装置,其中该制剂具有超过1%的胶凝剂、超过2%、超过3%、超过4%、超过5%、超过6%、超过7%、超过8%、超过9%、超过10%、超过12%、超过14%或超过16%的胶凝剂。同样,可以排除的是制剂或包括制剂的装置,其中该制剂具有低于1%的胶凝剂、低于2%、低于3%、低于4%、低于5%、低于6%、低于7%、低于8%、低于9%、低于10%、低于12%、低于14%或低于16%的胶凝剂。
还可以排除的是制剂或包括制剂的装置,其中该制剂具有超过1%的透皮吸收促进剂、超过2%、超过3%、超过4%、超过5%、超过6%、超过7%、超过8%、超过9%、超过10%、超过12%、超过14%或超过16%的透皮吸收促进剂。同样,可以排除的是制剂或包括制剂的装置,其中该制剂具有低于1%的透皮吸收促进剂,低于2%、低于3%、低于4%、低于5%、低于6%、低于7%、低于8%、低于9%、低于10%、低于12%、低于14%或低于16%的透皮吸收促进剂。
在其他实施方式中,可以排除的是制剂、组合物、包括制剂的装置、包括组合物的装置,其中所述制剂或组合物具有的按重量计的cbd(或thc、或cbd和thc的结合重量)含量低于1%、低于2%、低于3%、低于4%、低于5%、低于6%、低于8%、低于10%、低于12%、低于14%、低于16%、低于18%、低于20%、低于25%、低于30%、低于35%、低于40%、低于45%、低于50%、低于55%、低于60%、低于65%、低于70%、低于75%等。同样,可以排除的是制剂、组合物、包括制剂的装置、包括组合物的装置,其中所述制剂或组合物具有的按重量计的cbd(或thc,或cbd和thc的结合重量)含量大于5%、大于6%、大于7%、大于8%、大于10%、大于12%、大于14%、大于16%、大于18%、大于20%、大于25%、大于30%、大于35%、大于40%、大于45%、大于50%、大于55%、大于60%、大于65%、大于70%等。在实施方式中,可以排除的是制剂、组合物、包括制剂的装置或包括组合物的装置,其中按重量计的百分数由上述“低于”或“大于”参数中的一个或多个限定。“组合物”可以指例如皮肤粘合剂的基质,或指亲水性多孔膜中的流体等。替代地,本公开可以包括如由“低于”参数或“大于”参数所阐述的以上组合物中的一种或多种。
而且,在实施方式中,可以排除的是以下任何装置:不包括闭塞系统聚合物薄膜、不包括聚乙烯闭塞聚合物薄膜、不包括pet闭塞聚合物薄膜、不包括由聚乙烯和pet两者制成的闭塞聚合物薄膜。同样,可以排除的是具有覆盖贴剂的装置以及不包括覆盖贴剂的装置。
在实施方式中,极性有机液体可以包括或可以排除以下中的一种或多种:甲醇,乙醇,丙醇,异丙醇,丁醇,戊醇,乙酸,丙酸,丁酸,戊酸,己酸,辛酸,癸酸,月桂酸,肉豆蔻酸,棕榈酸,硬脂酸,棕榈油酸,油酸,亚油酸,亚麻酸,具有5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24或更多个碳的直链烷烃,具有5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24或更多个碳的主链的支链烷烃,具有5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24或更多个碳的直链链烯烃(烯烃),具有5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24或更多个碳的主链的支链链烯烃(烯烃)等。替代地,本公开可以包括以上极性有机液体中的一种或多种。
吸入实施方式
用于吸入的气溶胶和干粉制剂是可获得的。参见,mitchell,nagel,wiersema,anddoyle(2003)aapspharmscitech.4(4)article54(9pages);asaietal(2016)pharm.res.33:487-497;kopschetal(2017)int.j.pharm.529:589-596;fishlerandsznitman(2017)inhalation.11:21-25。气化器可从例如storzandbickel(图特林根(tuttlingen),德国)、arizertech(滑铁卢(waterloo),加拿大)、organicex(拉斯维加斯(lasvegas),内华达州(nv))以及elementaltechnologies(西雅图(seattle),华盛顿州(wa))获得。
实施例
整体式贴剂实施方式,如在weimann的us2017/0071870中描述的
以下文字来自weimann的us2017/0071870(序列号15/265,823),其通过援引以其全文并入本文。
透皮整体式cbd贴剂制剂:粘合剂聚合物:60-95,cbd:5-20,透皮吸收促进剂:0-20,粘合剂聚合物:来自hankel的丙烯酸酯、来自dowcorning的硅酮。来自basf的pib,cbd:纯结晶粉末,透皮吸收促进剂:油酸、棕榈酸异丙酯(ipp)、二甲基亚砜(dmso)、1,2-丙二醇(1,2-pg)、肉豆蔻酸异丙酯(ipm)。在这种实施例中,干燥的粘合剂基质的厚度为30-50微米。贴剂的区可以是正方形或椭圆形的。贴剂的最佳大小是20cm2乘以40cm2。
在整体式设计中,层压在背衬材料上的剥离衬垫涂覆有cbd和pib或胺相容性硅酮皮肤粘合剂的混合物。整体式cbd贴剂如何工作:步骤1.将cbd溶解在乙醇或1,2pg中并混合到粘合剂溶液中,以及如果需要,添加透皮吸收促进剂。步骤2.借助于“辊式刮刀”涂覆方法将粘合剂混合物分配在剥离衬垫上,并在烘箱中干燥1min至3min的干燥时间或直到全部残留溶剂均低于1ppm。步骤3.借助于夹压将干燥的粘合剂薄膜层压到背衬薄膜上,并切开边缘以进一步模切贴剂。步骤4.将层压体放在模切机上,并切割适当大小的贴剂,并随后将其包装在囊和盒子中。
cbd如何从贴剂制剂穿过皮肤递送到身体
通过将cbd溶解在不同的粘合剂中来制备整体式贴剂的制剂,并使用弗朗兹扩散池方法穿过人尸体皮肤进行cbd透皮通量。我们从包括pib粘合剂和10%cbd的制剂中发现了cbd的最高透皮通量。这示出,测量为20cm2的贴剂可以递送每天约5mg的cbd的全身剂量。
示例性整体式贴剂发明制剂:制剂1.10%cbd在etoh中。制剂2.10%cbd在etoh/h2o(9/1)中。制剂3.透皮吸收促进剂:1,2pg、ipp、油酸、dmso。
在第一整体式装置中,将皮肤粘合剂与cbd混合以限定粘合剂和cbd的整体式混合物。皮肤粘合剂涂覆在优选地是闭塞的背衬上。皮肤粘合剂优选地是胺相容性硅酮粘合剂。
在第二整体式装置中,将皮肤粘合剂与cbd(其可以作为基本上纯的cbd或包括cbd和其他大麻素的大麻植物的油提取物存在)混合以限定粘合剂和cbd的基本上整体式混合物。皮肤粘合剂优选地为具有的粘均分子量范围是约30,000道尔顿至约70,000道尔顿、优选地约35,000道尔顿至约65,000道尔顿以及更优选地约40,000道尔顿至约60,000道尔顿的聚异丁烯粘合剂。
整体式贴剂的制造方法
将cbd溶解在乙醇或1,2-丙二醇(1,2pg)中并混合到粘合剂溶液中,以及如果需要,添加透皮吸收促进剂。借助于“辊式刮刀”涂覆方法将粘合剂混合物分配在剥离衬垫上,并在烘箱中干燥1min至3min的干燥时间或直到全部残留溶剂均低于1ppm。借助于夹压将干燥的粘合剂薄膜层压到背衬薄膜上,并切开边缘以进一步模切贴剂。将层压体放在模切机上,并切割适当大小的贴剂,并随后将其包装在囊和盒子中。
参考weimann的usp10,272,125的图2,描绘了用于递送cbd的整体式透皮药物递送装置40的实施例。整体式透皮装置40包括先前关于储库透皮装置20的背衬22描述的类型的背衬42。将与治疗有效量的cbd混合的皮肤粘合剂的基质44涂覆在背衬42的一侧上。基质44优选地被配制成将装置20粘附到使用者的皮肤上不小于约24小时的周期,同时避免对使用者的皮肤的可感知的皮肤刺激。在与粘附至背衬42的表面相反的基质44的表面上,剥离衬垫48可剥离地粘附至基质44上。剥离衬垫48的第一侧49背离基质44,并且剥离衬垫48的第二侧51的一部分粘附至基质44上。为了使用整体式透皮装置40,将剥离衬垫48剥离并且将粘合剂基质44的暴露表面施加到皮肤上。
包括基质44的皮肤粘合剂优选地包括丙烯酸酯压敏粘合剂、聚异丁烯压敏粘合剂以及胺相容性硅酮压敏粘合剂中的至少一种。合适的丙烯酸酯粘合剂包括durotak87-2516。合适的聚异丁烯粘合剂包括具有的粘均分子量范围是约30,000道尔顿至约70,000道尔顿、优选地约35,000道尔顿至约65,000道尔顿以及更优选地约40,000道尔顿至约60,000道尔顿的那些。
基质44优选地包括具有如以上描述的粘均分子量的聚异丁烯粘合剂和粘合/粘度调节剂。粘合/粘度调节剂优选地是矿物油或硅酮流体,其存在量范围是基质44的按重量计约百分之一(1)至约百分之十(10)、更优选地基质44的按重量计约百分之二(2)至约百分之六(6)以及还更优选地基质44的按重量计约百分之三(3)至约百分之四(4)。适合用作粘合/粘度调节剂的矿物油具有的分子量的范围为100至约1000道尔顿、更优选地约200至约600道尔顿、甚至更优选地约350道尔顿至约450道尔顿以及还更优选地约400道尔顿。适合用作粘合/粘度调节剂的硅酮流体优选地包括具有的在20℃下的运动粘度范围为约100cst至约1000cst的-oh封端的聚二甲基硅氧烷。可用作粘合/粘度调节剂的可商购的硅酮流体包括dowcominq7-9120流体,其可获得的运动粘度(在20℃下)为20、100、350、1000和12,500cst。在硅酮粘合/粘度调节剂的优选实例中,使用q7-9120100cst或1000cst(或其混合物)。
优选的聚异丁烯粘合剂不供应有矿物油。在某些优选的实例中,基质44的聚异丁烯组分是vistanexlm聚异丁烯粘合剂。在其他优选的实例中,基质44的聚异丁烯组分是由basf供应的oppanolb13聚异丁烯粘合剂。
在其他实例中,基质44的粘合剂组分可以包括丙烯酸粘合剂和聚异丁烯粘合剂的共混物,以及优选地,丙烯酸粘合剂和具有以上所述的粘均分子量(约30,000道尔顿至约70,000道尔顿、优选地约35,000道尔顿至约65,000道尔顿以及更优选地约40,000道尔顿至约60,000道尔顿)的聚异丁烯粘合剂的共混物。当丙烯酸粘合剂与这样的聚异丁烯粘合剂组合时,基质44中粘合剂总量的按重量计的丙烯酸粘合剂的量优选地为约百分之一至约百分之50。在一种实例中,基质44的粘合剂组分包括基质44中粘合剂总量的按重量计的百分之80的oppanolb13以及基质44中粘合剂总量的按重量计的百分之二十的durotak87-2516。
整体式装置还可以包括一种或多种透皮吸收促进剂,包括油酸、棕榈酸异丙酯(ipp)、dmso、1,2丙二醇和肉豆蔻酸异丙酯(ipm)。透皮吸收促进剂的量范围为优选地基质的按重量计零至约百分之十(10)。在排他性实施方式中,本公开可以排除具有多于一种类型的透皮吸收促进剂的任何贴剂或任何制剂。
装置的皮肤接触面积为优选地至少约10cm2、更优选地至少约15cm2以及还更优选地至少约18cm2。同时,装置的皮肤接触面积优选地不超过约30cm2、优选地不超过约25cm2以及还更优选地不超过约22cm2。在给定通量速率下,可以选择皮肤接触面积以达到期望的每日cbd剂量(或在具有治疗利益的任何时间段内的剂量)。以上文字来自weimann的usp10,272,125。
辊式刮刀涂覆
在不暗示对本发明的任何限制的情况下,刮刀涂覆是通过施加过量的涂覆液体在连续的网状物上形成薄的液体涂层的方法,涂覆液体随后通过与刚性支撑的网状物紧密接近保持的刚性刮刀计量。涂层的厚度主要取决于刮刀与网状物之间的间距或间隙,以及取决于间隙的几何形状(坡口面角度、长度)。辊涂是通过使用两个或更多个旋转轧辊在连续网状物上形成薄的液体薄膜,使得流体在一对旋转轧辊之间的小间隙中的流动是控制涂覆的薄膜的厚度和均匀性的主要因素的方法。涂层的厚度主要取决于相邻轧辊之间的间隙及其相对速度。辊涂机的两种基本类型的区别在于间隙中轧辊表面移动的相对方向:在向前辊涂中,轧辊表面在相同方向上移动,而在反向辊涂中,轧辊表面在相反方向上移动。就流场而言,刮刀涂覆是向前辊涂的子集,其中一个表面是固定的。参见,coyle,d.j(1997)knifeandrollcoatinginliquidfilmcoating(ed.s.f.kistlerandp.m.schweizer).chapman&hall,london;w.rehnby,m.gustafsson,m.skrifvars(june2008)conferencepaper,coatingoftextilefabricswithconductivepolymersforsmarttextileapplications,pages100-103。
储库型贴剂实施方式的实施例.
储库型贴剂制造方法
本发明人已经使用了以下用于储库型贴剂的制造方法,其中方法使用指示的阶段:
阶段1.凝胶分配器.在膜上分配活性凝胶溶液。在这一点上,制造阶段可以由活性凝胶的孤立的团迹来表示。
阶段2.热密封压机.凝胶覆盖有可热密封的薄膜,并在凝胶周围进行热密封。在这一点上,制造阶段可以由被薄膜层围绕的中心中的团迹表示。
阶段3.轻触切割(kisscut)压机.沿热密封环的周缘进行轻触切割。在这一点上,制造阶段可以由被薄膜层围绕的中心处的团迹表示,并且其中该层的内部侧是完整的并且其中外部层是穿孔的。根据一种来源,“轻触切割是……用于提供转换的胶带解决方案的方法。在轻触切割过程期间,每个件的周长都被锋利的金属模具或精密的激光束冲压出……切割不会穿透件的背衬材料(衬垫)。即使模具或激光一直贯穿材料的可用部分进行了干净的切割,它也仅仅“轻触”了衬垫片。这允许将单一或多种粘合剂材料保留在衬垫片或轧辊上,直到最终使用者准备去除它们为止。”(
阶段4.轻触切割压机.储库被覆盖薄膜覆盖,并沿覆盖周缘进行轻触切割。在制造这一点上,在阶段3中获得的制造的制品被另一层围绕,其中这种层是覆盖薄膜。
阶段5.切穿压机.穿过过度延伸的剥离衬垫切割贴剂,以更容易剥。在这一点上,制造的制品类似于在阶段4中获得的制品,除了该制造的制品被切碎成段,其中每个段都适合于附连在人患者或人消费者的皮肤上。
如在weimann的us2017/0071870中所述的储库型贴剂
以下文字和结构编号来自weimann的usp10,272,125,其通过援引以其全文并入本文。参考usp10,272,125的图1,描绘了用于cbd的透皮递送的储库型透皮递送装置20。储库型透皮递送装置20包括背衬22和亲水性多孔膜24。背衬22和亲水性多孔膜24彼此附连,以限定用作储库26的封闭容积。包括cbd、液体载体和胶凝剂的制剂27设置在储库26中。亲水性多孔膜24的第一侧34与制剂27接触。亲水性多孔膜24的第二侧36背离背衬22,并且涂覆有皮肤粘合剂30。皮肤粘合剂30优选地被配制成将装置20粘附到使用者的皮肤上不小于约24小时的周期,同时避免对使用者的皮肤的可感知的皮肤刺激。优选的皮肤粘合剂30包括胺相容性硅酮压敏粘合剂。在某些实例中,提供了胺相容性硅酮皮肤粘合剂30,其包括硅醇封端的聚二甲基硅氧烷和硅酸酯树脂的三甲基甲硅烷氧基封端的反应产物。皮肤粘合剂优选地作为有机溶剂溶液提供,该有机溶剂溶液包括在有机溶剂如庚烷或乙酸乙酯中的按重量计约百分之50至约百分之70的固体粘合剂并且具有在20℃下约400mpa-s至约1300mpa-s、优选地约450mpa-s至约1250mpa-s以及更优选地约500mpa-s至约1200mpa-s的粘度。
剥离衬垫28的第一表面29可剥离地粘附到皮肤粘合剂30上,并且剥离衬垫28的第二表面31背离皮肤粘合剂30。合适的剥离衬垫包括涂覆有可剥离地可粘附到硅酮、聚异丁烯和硅酮粘合剂的剥离涂层的闭塞聚合物薄膜,诸如聚酯、聚丙烯。剥离衬垫28的第一表面29上的合适的剥离涂层包括含氟聚合物和硅酮聚合物。适合用作剥离衬垫28的可商购的涂覆的剥离衬垫包括由3m,明尼阿波利斯(minneapolis),明尼苏达州(minn.)供应的scotchpak1022、9741、9744、9748和9755,以及由foxriverco.供应的fra314和315。为了使用储库型透皮装置20,将剥离衬垫28从皮肤粘合剂30上剥离,从而暴露皮肤粘合剂30,并且施加装置20,使得皮肤粘合剂30接触使用者的皮肤。
这样的胺相容性硅酮粘合剂的合适的实例包括由dowcorning供应的bio-psa7-4301和7-4302皮肤粘合剂。bio-psa7-4301是可获得的在庚烷中的高接触粘性的胺相容性硅酮粘合剂,其中固体含量为百分之60和百分之70,并且在20℃下的相应的粘度为450mpa-s和1600mpa-s。bio-psa7-4302是在乙酸乙酯中的高接触粘性的胺相容性硅酮粘合剂,其中固体含量为按重量计百分之60且在20℃下的粘度为1200mpa-s。将皮肤粘合剂30在膜24上涂覆至每单位面积的厚度,优选地为约10至约20g/m2、更优选地约12-18g/m2以及还更优选地约14-16g/m2。
亲水性多孔膜24具有的平均流量孔径(meanflowporesize)优选地为不超过约1微米、优选地不超过约0.8微米、还更优选地不超过约0.4微米以及甚至更优选地不超过约0.2微米。同时,多孔膜24具有的平均流量孔径优选地不小于约0.02微米、更优选地不小于约0.04微米、还更优选地不小于约0.06微米以及甚至更优选地不小于约0.08微米。平均流量孔径可以根据公布的pct申请wo2010072233的第17页第22行至第18页第4行中阐述的方法确定。
在相同或其他实例中,亲水性多孔膜24具有的孔隙率优选地为至少约百分之60、更优选地至少约百分之65以及还更优选地至少约百分之70。同时,亲水性多孔膜24具有的孔隙率优选地不超过约百分之90、更优选地不超过约百分之85以及还更优选地不超过约百分之80。孔隙率值可以如wo2010072233的第7页第24至27行中描述的进行计算。
在相同或其他实例中,亲水性多孔膜24具有的厚度优选地不超过约50微米、优选地不超过约40微米以及甚至更优选地不超过约35微米。同时,亲水性多孔膜24具有的厚度优选地不小于约10微米、更优选地不小于约20微米以及还更优选地不小于约25微米。可以如wo2010072233的第18页第19-21行中描述的确定膜厚度。
在相同或其他实例中,亲水性多孔膜24具有的如通过gurley测试方法(根据iso5636-5)确定的透气度优选地为优选地至少约10sec/50ml、更优选地至少约20sec/50ml以及还更优选地至少约25sec/50ml。同时,亲水性多孔膜24具有的透气度优选地不超过约50sec/50ml、更优选地不超过约40sec/50ml以及还更优选地不超过约35sec/50ml。
在相同或其他实例中,亲水性多孔膜24具有的如由astmd882-12确定的机器方向上的拉伸强度优选地为优选地至少约10mpa、更优选地至少约15mpa以及还更优选地至少约20mpa。在相同或其他实例中,亲水性多孔膜24具有的如由astmd882-12确定的机器方向上的伸长率百分数优选地为优选地至少约百分之10、更优选地至少约百分之15以及还更优选地至少约百分之20。
亲水性多孔膜24优选地包括至少一种聚合物材料。在一种实例中,亲水性多孔膜24包括聚烯烃聚合物和包括亲水性聚合物和任选地表面活性剂的亲水性组分。如本文所用的,术语“亲水性”在用于描述多孔膜时是指在20℃下提供至少0.5升/(m2hbar)的脱盐水穿过膜的水通量的膜。
基于膜24的总干重,聚烯烃聚合物的含量为优选地按重量计小于或等于百分之98,并且基于膜的总干重,一种或多种亲水性组分的含量为优选地至少2重量百分比。在某些优选的实例中,通过以下形成膜:将聚烯烃聚合物与一种或多种亲水性组分和任选的添加剂与溶剂组合以形成呈凝胶、溶液或均匀混合物的形式的共混物,紧接着将共混物挤出。合适的聚烯烃(诸如聚乙烯)、亲水性组分和添加剂描述于wo2010072233。
在其他优选的实施方式中,装置包括透皮贴剂制剂,该制剂包括由一侧的微孔亲水性或疏水性膜以及另一侧的闭塞薄膜构造的呈“馄饨”形状的储库。
在实施方式中,装置包括包含范围为1%至50%cbd的高浓度的cbd的透皮储库型贴剂制剂,如用羟烷基纤维素胶凝化的触变醇或醇/水溶液。此外,装置包括透皮储库型贴剂制剂,该制剂包括包含用羟烷基纤维素胶凝化的触变醇或醇/水溶液并且包含范围为1%至50%的高浓度的cbd以及浓度范围为0%至10%的皮肤透皮吸收促进剂的储库。
还涵盖的是包括以下的透皮贴剂制剂:由一侧的微孔亲水性或疏水性膜以及另一侧的闭塞薄膜构造的呈“馄饨”形状的储库,其中微孔膜涂覆有硅酮粘合剂的薄层。在递送实施方式中,20cm2的储库型贴剂能够全身性递送的cbd为约0.5mg/天、约1.0mg/天、约1.5mg/天、约2.0mg/天、约5.0mg/天、约10mg/天、约15mg/天、约20mg/天、约25mg/天、约30mg/天、约35mg/天、约40mg/天等。
在其他递送实施方式中,20cm2的储库型贴剂能够全身性递送的cbd为至少0.5mg/天、至少1.0mg/天、至少1.5mg/天、至少2.0mg/天、至少5.0mg/天、至少10mg/天、至少15mg/天、至少20mg/天、约25mg/天、约30mg/天、至少35mg/天、至少40mg/天等。
丸剂制剂的实施例(西地那非、大麻二酚)
开发舌下丸剂制剂并测试其活性成分大麻二酚和西地那非。丸剂的制剂为:崩解剂(9克);微晶纤维素(24克);糖精钠(0.75克);甘露醇(100克);硬脂酸镁(1.5克)。活性成分:15克(cbd,西地那非)。总计(150.5克)。
开发丸剂制剂以满足可接受的性能标准,诸如:硬度、脆碎度和崩解;硬度(大于4kg/cm2);脆碎度(小于2%);崩解(小于100sec)。舌下丸剂是使用手动丸剂压机制成的。
实验室结果如下。柠檬酸西地那非舌下丸剂的性能:直径(0.6cm);厚度(0.435cm);平均重量(124.5mg);硬度(10.3千克/cm2);脆碎度(0.6%),崩解(90sec)。大麻二酚舌下丸剂的性能:直径(0.6cm);厚度(0.435cm);平均重量(134.1mg);硬度(8千克/cm2);脆碎度(0.2%),崩解(75sec)。大麻二酚以具有的纯度为99.8%(0.00%thc)的结晶形式从大麻提取物中获得。
根据发明人对舌下丸剂制剂的经验,我们正在配制一种浓度的丸剂活性成分。主要想法是找到将提供快速崩解以及可接受硬度的赋形剂的最佳集合。目标如下:包含10mg的活性成分的130mg丸剂;或包含20mg的活性成分的240mg的丸剂制剂。保持活性成分恒定,发明人可以测试随硬脂酸镁的浓度而变的崩解时间。关于大麻二酚(cbd),大麻二酚(cbd)的该量将为10mg,并且丸剂的总质量将始终为130mg。发明人拥有只能制造这种大小的丸剂的机器。关于西地那非,西地那非也相同:10mg西地那非和130mg总质量的丸剂,具有不同量的硬脂酸镁。变量将是硬脂酸镁和将抵消硬脂酸镁重量变化的其他成分。
供应商:崩解剂(来自spipharma,威明顿市(wilmington),特拉华州(de)的pharmaburst500);微晶纤维素(来自fmcbiopolymer的avicel102);糖精钠(spectrumchemicalmfg.corp.);甘露醇(来自rpiresearchproductsinternational);硬脂酸镁(spectrumchemicalmfg.corp.)。西地那非和大麻素可从例如sigma-aldrich,圣路易斯,密苏里州获得。对于丸剂和片剂的测试,脆碎度、硬度、溶出度和崩解可以通过来自copleyscientific,ltd.,诺丁汉(nottingham),英国的设备进行评估。设备包括脆碎度测试仪系列fr(fr1000、fr2000、friabimatsa400),崩解测试仪(dtg1000、dtg2000、dtg4000)和溶出度装置(篮子、桨叶、盘上桨叶(paddleoverdisk)、圆柱体和竖直扩散池(弗朗兹池))。脆碎度是片剂在压缩下碎裂、破碎或破裂的趋势。pharmaburst500包含甘露醇、山梨糖醇、交聚维酮(crospovidone)、二氧化硅、天冬苯丙二肽酯和硬脂酸镁(参见,h.kathpaliaandk.jogi.co-processedexcipients.areview.worldj.pharma.res.3:3863-3885)。
这提供了关于cbd舌下丸剂和西地那非舌下丸剂的实验室数据。在测试这些类型的丸剂中的每一种时,一个变量是崩解剂的量,并且另一个变量是微晶纤维素的量。恒定参数是糖精钠、甘露醇、硬脂酸镁和活性成分。实验涉及一组包括cbd的制剂批次,以及另一组包括西地那非的制剂批次。对于这两种类型的批次中的每个,数量如下:崩解剂(0、3、6、9、12、15和18克崩解剂);微晶纤维素(33、30、27、24、21、18和15克微晶纤维素)、糖精钠(0.75克)、甘露醇(100克)、硬脂酸镁(1.5克)、活性成分(cdb或西地那非)(15克)。批次的总重量为150.5克。
参照weimann的us2017/0071870中的数据的粘合剂、增粘剂和促进剂的实施例
与具有促进剂氮酮和油酸以及dmso的pib相比,添加无官能度丙烯酸粘合剂durotak87-900a和仅具有oh官能度的粘合剂durotak87-2510。氮酮是“1-十二烷基氮杂环庚烷-2-酮”。
具有增粘剂的pib粘合剂,这些增粘剂使用以1-50%混合的丙烯酸压敏粘合剂改善对皮肤的粘合。还使用环脂族烃树脂,诸如来自exxonmobil的escorez
具有促进剂:3%的氮酮或油酸的pib粘合剂,使来自pib的透皮递送增加了一倍。本公开提供了示出透皮通量的图。
参照weimann的us2017/0071870中的数据的大麻油、水凝胶、cbd和thc的实施例
使用具有包含不同萜烯的高浓度为80-95%的cbd的大麻油改善cbd的透皮递送。本公开提供了来自具有结晶cbd的基质对比具有80%cbd的大麻油的基质的透皮通量的图。
从用高浓度cbd和thc80-95%的cbd和thc油饱和的半固体水凝胶中递送cbd和thc。在具有比率为80/20的etoh/水,还具有促进剂氮酮、油酸和苧烯的混合物中,使油饱和。本公开提供了透皮通量的图。
示出在储库型贴剂中高浓度thc(80-95%)与1-20%etoh或与etoh/水80/20(1-10%)混合的thc油递送高透皮剂量的thc。添加多于10%的乙醇降低通量。本公开提供了透皮通量的图。
来自weimann的us2017/0071870的实施例
具有薄荷醇、樟脑和水杨酸的cbd贴剂。
实施例
具有0.01%辣椒的cbd贴剂。
实施例
具有营养活性成分的cbd。
实施例
贴剂中的比率为1/1的cbd/thc产生2/1的透皮剂量比率。本公开提供了透皮通量的图。
药物和营养品实例
本公开了提供了褪黑激素贴剂、利多卡因贴剂、薄荷醇、樟脑、水杨酸贴剂、具有二氢杨梅素的悬垂贴剂、维生素b1贴剂、维生素d3贴剂、维生素b12贴剂、维生素c贴剂、西地那非舌下丸剂、西地那非速溶条状物、西地那非口腔贴剂、大麻酚舌下丸剂、大麻酚速溶条状物、大麻酚口腔贴剂等。
本公开的皮肤贴剂通量数据
图13示出了与混合有thc油的整体式贴剂相比,来自不同水凝胶基质的thc的24小时体外通量的比较。图13示出了与混合有相同的thc油的整体式贴剂相比,来自不同比率的etoh/水混合物的thc的24小时体外透皮通量。图13的结果指明,来自储库型贴剂的thc通量取决于乙醇/水的比率。当乙醇与水的比率为60/40(用thc饱和的)时,观察到最大的thc通量,并且thc通量是整体式贴剂的thc通量约2.5倍。对于图13,左边的数据条来自具有pib的整体式贴剂。包含与thc油混合的60%etoh和40%水的液体水凝胶递送的thc通量是具有相同浓度的thc的整体式贴剂的3倍。
右边的三个数据条来自储库型贴剂。这些储库型贴剂不包含任何粘合剂。然而,当施加到皮肤上时,这些储库型贴剂通过覆盖贴剂保持在皮肤上的适当位置。
在实施方式中,储库型贴剂使用的etoh/水的比率为约5/95(vol/vol)、约10/90(vol/vol)、约15/85(vol/vol)、约20/80(vol/vol)、约25/75(vol/vol)、约30/70(vol/vol)、约35/65(vol/vol)、约40/60(vol/vol)、约45/55(vol/vol)、约50/50(vol/vol)、约55/45(vol/vol)、约60/40(vol/vol)、约65/35(vol/vol)、约70/30(vol/vol)、约75/25(vol/vol)、约80/20(vol/vol)、约85/15(vol/vol)、约90/10(vol/vol)、约95/5(vol/vol)等。在排他性实施方式中,本公开可以排除包含以这些比率中的任一比率的etoh/水的任何储库型贴剂,并且可以排除具有以这些比率中的任一比率的etoh/水的任何储库型制剂。在实施方式中,这些具体比率可以用于限定任何其他溶剂的比率,诸如二甲基亚砜/水的比率。
同样,在实施方式中,储库型贴剂使用以下etoh/水比率:其中乙醇百分数(vol/vol)为0.1-5%etoh之间,其中其余为水,5-10%etoh之间,其中其余为水,10-15%etoh之间,其中其余为水,15-20%etoh之间,其中其余为水,20-25%etoh之间,其中其余为水,25-30%etoh之间,其中其余为水,30-35%etoh之间,其中其余为水,35-40%etoh之间,其中其余为水,40-45%etoh之间,其中其余为水,45-50%etoh之间,其中其余为水,50-55%etoh之间,其中其余为水,55-60%etoh之间,其中其余为水,60-65%etoh之间,其中其余为水,65-70%etoh之间,其中其余为水,70-75%etoh之间,其中其余为水,75-80%etoh之间,其中其余为水,80-85%etoh之间,其中其余为水,85-90%etoh之间,其中其余为水,90-95%etoh之间,其中其余为水,95-99.5%etoh之间,其中其余为水等。在排他性实施方式中,本公开可以排除包含以这些比率范围中的任一范围(或以这些比率的任何组合或总和)的etoh/水的任何储库,并且可以排除具有以这些比率范围中的任一范围的etoh/水的任何储库型制剂。在实施方式中,这些具体比率范围可以用于限定任何其他溶剂的比率范围,诸如二甲基亚砜/水的比率。
本公开的皮肤贴剂数据
图11示出了来自不同比率的etoh/水饱和溶液的cbd穿过人尸体表皮的透皮通量。图11示出了如用于储库型贴剂构造的来自不同比率的不同乙醇/水溶液的cbd的体外透皮通量的结果。来自比率为80/20的乙醇水以及饱和浓度cbd的溶液的cbd通量显著地且出乎意料地是来自整体式贴剂的cbd通量的约10倍。因此,本公开公开了由用大麻素诸如cbd和thc以及其他大麻素饱和的乙醇/水混合物制备的储库型贴剂制剂比整体式贴剂递送更大的透皮通量。
本公开的皮肤贴剂数据
图8和图9示出了来自整体式贴剂的cbd的透皮通量。那些结果的重要性如下。图8示出了来自用包含30%的cbd的丙烯酸粘合剂以及包含12%cbd的pib粘合剂配制的整体式贴剂的cbd通量的比较。它示出了,甚至在丙烯酸粘合剂中用3倍浓度的cbd,cbd通量也比来自较低浓度(12%)的cbd的pib粘合剂的cbd通量低得多。因此,pib制剂优于丙烯酸制剂。
图9示出了具有30%cbd以及3%添加最佳的促进剂的丙烯酸整体式贴剂的cbd通量。即使添加促进剂,cbd通量也比来自pib粘合剂的低得多。因此,pib制剂优于具有促进剂的丙烯酸制剂。
未示出,但由本发明人测试的是具有硅酮粘合剂biopsa7-4302的制剂示出没有cbd通量。因此,pib制剂优于硅酮粘合剂整体式制剂。
本公开的皮肤贴剂数据
图10示出了在存在不同的透皮通量促进剂下,来自pib粘合剂的cbd的24小时体外通量的比较。图10是指整体式贴剂。用cbd饱和的pib粘合剂中浓度为3%的油酸对cbd透皮通量具有最佳的增强效果,仅使通量增加约50%。图10示出了增强因子(24小时通量增加)是1.5-倍。
使用弗朗兹扩散池方法穿过人尸体表皮体外测量大麻素的透皮通量。从接收溶液中取出300微升的样品,并通过hplc分析穿过表皮的大麻素物质的量。
获得了溶解在纯液体促进剂中的cbd的cbd通量的结果。这样的制剂在递送更大透皮剂量的大麻素的储库型贴剂的应用中是新颖的,前提是它们不引起皮肤刺激。图10示出了来自pib整体式贴剂的cbd通量的结果,所有均具有12%cbd(pib粘合剂中cbd的饱和浓度)和3%的促进剂。
在实施方式中,这公开了适合于图10的整体式贴剂、适合于不同于由图10所表示的整体式贴剂的整体式贴剂以及任选地适合于储库型贴剂的油酸、dmso和苧烯的比率。合适的比率(vol/vol/vol)包括油酸/dmso/苧烯的比率为约5/5/90;约5/10/85;约5/15/80;约5/20/75;约5/25/70;约5/30/65;约5/35/60;约5/40/55;约5/45/50;约5/50/45;约5/55/40;约5/60/35;约5/65/30;约5/70/25;约5/75/20;约5/80/15/约5/85/10;以及约5/90/5等。
同样,合适的比率(vol/vol/vol)包括油酸/dmso/苧烯的比率为约10/5/85;约10/10/80;约10/15/75;约10/20/70;约10/25/65;约10/30/60;约10/35/55/约10/40/50;约10/45/45/约10/50/40;约10/55/35;约10/60/30;约10/65/25;约10/70/20;约10/75/15/约10/80/10;约10/85/5等。
此外,合适的比率(vol/vol)包括油酸/dmso/苧烯的比率为约20/5/75;约20/10/70;约20/15/65;约20/20/60;约20/25/55;约20/30/50;约20/35/45;约20/40/40;约20/45/35;约20/50/30;约20/55/25;约20/60/20;约20/65/15;约20/70/10;约20/75/5等。
另外,合适的比率(vol/vol/vol)包括油酸/dmso/苧烯的比率为约40/5/55/约40/10/50;约40/15/45;约40/20/40;约40/25/35;约40/30/30;约40/35/25;约40/40/20;约40/45/15;约40/50/10;约40/55/5等。
另外的合适的比率(vol/vol/vol)包括油酸/dmso/苧烯的比率为约50/5/45;约50/10/40;约50/15/35;约50/20/30;约50/25/25;约50/30/20;约50/35/15;约50/40/10;约50/45/5等。
合适的比率(vol/vol/vol)也包括油酸/dmso/苧烯的比率为约60/5/35;约60/10/30;约60/15/25;约60/20/20;约60/25/15;约60/30/10;约60/35/5等。
同样,合适的比率(vol/vol/vol)包括油酸/dmso/苧烯的比率为约70/5/25;约70/10/20;约70/15/15;约70/20/10;约70/25/5等。
合适的比率(vol/vol/vol)进一步包括油酸/dmso/苧烯的比率为约80/5/15;约80/10/10;约80/15/5。其他合适的比率(vol/vol/vol)是油酸/dmso/苧烯的比率为约90/5/5。
关于以上比率清单中的术语“约”,术语约意指任何给定比率涵盖从下一个较低比率到下一个较高比率的范围(但不包括包围该范围的值)。在排他性实施方式中,本公开可以排除任何组合物,并且可以排除包含任何组合物的任何装置,其中该组合物满足如以上所阐述的值或范围。必要时,对于排他性实施方式,以上比率可以用于指vol/vol/vol或wt/wt/wt。
本公开的皮肤贴剂数据
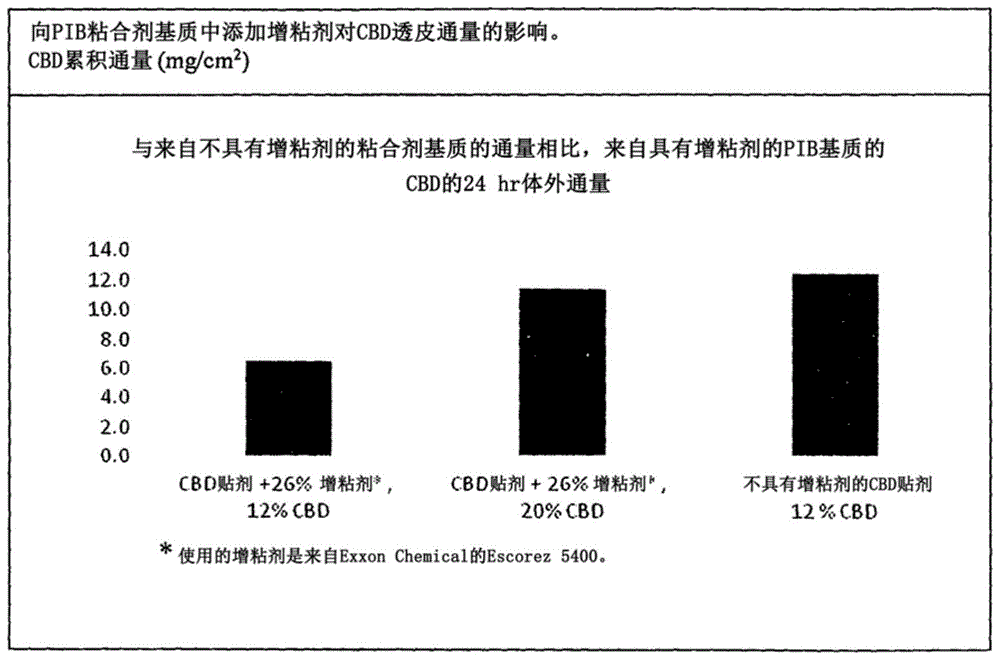
图3示出了与来自不具有增粘剂的粘合剂基质的通量相比,来自具有增粘剂的pib基质的cbd的24小时体外通量。这涉及图3。增粘剂是当添加到粘合剂中时,它们增加该粘合剂的接触粘性和粘合强度的化合物。当我们的pib粘合剂与不同的药物或营养品提取物混合时,会损失一些粘合强度,这可引起对皮肤的粘性差,以及因此引起活性成分从pib粘合剂到达皮肤的通量不足。因此,需要向粘合剂中添加物质以增加其在粘合剂与皮肤之间的粘合力。发明人正在使用从所有可获得的丙烯酸型和硅酮型医用粘合剂中都能提供大麻素到皮肤的最佳分配的pib粘合剂。然而,对皮肤的粘合不是最好的。将期望添加增粘剂物质。环脂族烃树脂可以用于使各种粘合剂聚合物增粘。但是,它们尚未用于pib粘合剂中。我们发现,由exxonmobilchemical制造的环脂族树脂之一
这涉及图3。体外结果表明,的确,在20%的cbd浓度下达到了饱和,并且cbd的通量实际上与来自包含饱和浓度为12%的cbd的饱和的未增粘的pib粘合剂基质的cbd通量相同。pib粘合剂的化学组成是溶解在庚烷中产生约3,000厘泊的溶液的分子量在12,000-50,000道尔顿之间的pib聚合物。将增粘树脂
这涉及确定pib粘合剂中的cbd的百分饱和度,以及确定包含增粘剂的pig粘合剂中的cbd的百分饱和度。关于图3,百分饱和度是使用以下两者确定的:(1)测试粘合剂基质中增加的cbd浓度,直到出现浊度为止;和(2)对具有增加浓度的贴剂制剂运行通量实验,找到透皮通量达到稳定期的起始浓度。
关于粘合剂的剥离强度,发明人使用判断和估计来制备具有26%的增粘树脂的贴剂。escorez5400已经用于许多粘合剂中,但未用在pib中。发明人首次使用它,并且发明人的结果表明它作为增粘剂起作用。发明人通过从发明人自己的手臂皮肤上剥离具有增粘剂和不具有增粘剂的制剂来估计它们两者的剥离强度。为了获得在具有26%的增粘树脂escorez5400的pib粘合剂中的cbd的饱和浓度,发明人需要添加更多的cbd以达到浊度。pib粘合剂中的饱和浓度为约18%cbd。然而,cbd的透皮通量没有增加。它与来自没有增粘剂的用cbd饱和的pib的通量相同。
使用增粘剂的益处将是,其用于可包含额外的活性成分连同可能会不利地影响贴剂对皮肤的粘合的大麻素,如添加液体萜烯的制剂。
发明人发现,escorez5400增粘剂增加了cbd在pib粘合剂中的溶解度,其中这使更大浓度的cbd用于制造皮肤贴剂。从而预期这将导致更大的cbd通量到达患者,其中皮肤贴剂与患者的皮肤接触。
在实施方式中,本公开提供了具有约26%增粘树脂,即约26%增粘剂、约12%、约14%、约16%、约18%、约20%、约22%、约24%、约26%、约28%、约30%、约32%或约34%增粘剂等的贴剂。同样,本发明提供了具有12%、14%、16%、18%、20%、22%、24%、26%、28%、30%、32%或34%增粘剂等的贴剂。在范围实施方式中,本公开提供了具有在以下范围内的增粘剂的贴剂:10-12%增粘剂、12-14%、14-16%、16-18%、18-20%、20-22%、22-24%、24-26%、26-28%、28-30%、30-32%或32-34%增粘剂等,或由这些连续范围中的任何两个的总和或这些连续范围中的任何三个的总和或这些连续范围中的任何四个的总和组成的范围等。在排他性实施方式中,本公开可以排除具有以上增粘剂值、具有“约”增粘剂值中的任一个或具有以上增粘剂范围中的任一个的贴剂。
本公开的皮肤贴剂数据
来自饱和的丙烯酸酯粘合剂以及来自饱和的pib粘合剂基质(整体式贴剂)的cbd的24小时体外通量的比较
来自丙烯酸酯粘合剂基质的cbd透皮通量与来自pib粘合剂基质的通量的比较。图8示出了来自整体式贴剂的cbd的透皮通量。图1比较了来自用包含30%的cbd的丙烯酸粘合剂以及包含12%cbd的pib粘合剂配制的整体式贴剂的cbd通量。它示出了,甚至在丙烯酸粘合剂中用3倍浓度的cbd,cbd通量也比来自较低浓度(12%)的cbd的pib粘合剂的cbd通量低得多。因此,pib制剂优于丙烯酸制剂。durotak87-900a是一种由常见的丙烯酸基单体,诸如丙烯酸2-乙基己酯、丙烯酸丁酯和丙烯酸异辛酯构成的非官能丙烯酸共聚物。durotak87-2510和durotak87-2287是由丙烯酸基单体构成的-oh(羟基)官能丙烯酸共聚物。丙烯酸羟乙酯单体durotak87-2516是双重官能度:由至少一种丙烯酸基单体和其他两种单体,诸如丙烯酸和丙烯酸羟乙酯构成的-oh(羟基)和-cooh(羧基)。测试由henkelcorporation(斯坦福德(stamford),康涅狄格州(ct);布里奇沃特(bridgewater),新泽西州(nj))供应的四种丙烯酸酯粘合剂的cbd透皮通量:durotak87-900a(无官能团)、durotak87-2516(具有-oh和-cooh官能团两者)、durotak87-2510和durotak87-2287(均具有-oh官能团)。pib粘合剂也由henkelcorp.供应。
高浓度的cbd并不是用于优化来自丙烯酸酯粘合剂的cbd的透皮通量的决定因素。来自硅酮粘合剂biopsa-7-4302的测试的cbd的体外通量是不可检测的。我们的pib基质制剂为cbd从基质扩散到皮肤提供了最佳的热力学。
实施例.本公开的丙烯酸粘合剂的化学性质和增粘剂的化学性质
duro-tak87-4287是以丙烯酸2-乙基己酯作为主要重复单体单元的共聚物。duro-tak87-4287是一种具有乙酸乙烯酯的共聚物,并且包含oh官能团,因为丙烯酸2-羟乙酯也是聚合物组合物的一部分(wolff(2014)pharm.res.31:2186-2202)。
实施例.本公开的皮肤贴剂数据
与pib粘合剂相比,来自用30%的cbd饱和的丙烯酸酯粘合剂durotak87-2287的cbd的体外通量。
图9示出了向丙烯酸酯粘合剂中添加促进剂对cbd通量的影响。在durotak87-2287粘合剂基质中使用三种促进剂:浓度为3%的azon、cbd以及油酸,测试了向丙烯酸粘合剂中添加促进剂的效果。cbd的浓度为30%。添加促进剂诸如azon、油酸以及dmso并不显著改善来自丙烯酸粘合剂基质的cbd通量,并且即使没有促进剂,仍然远低于来自pib粘合剂基质的cbd通量。
图9示出,pib粘合剂基质是用于从整体式贴剂高透皮递送大麻素的整体式粘合剂基质的优选的或最佳选择。
化学促进剂主要用于增加活性成分的皮肤穿透通道。当被混合到包含活性成分的基质中并被放置在皮肤上时,活性成分和促进剂分子两者都将分配到皮肤中。制剂的意图是使活性成分和促进剂两者具有最高可能的分配。然而,必须知道紧密接触的两个相之间的分配和扩散是由正在接触的相中的渗出液的溶解度的热力学支配。
在透皮递送系统的情况下,我们将紧密接触的两个相可视化。“供体”相可以是包含活性成分和促进剂的整体式粘合剂、乳膏、凝胶或液体,以及“接收”相则是皮肤。重要的是,活性成分物质和促进剂在两个相中的溶解度参数是活性成分和促进剂是否会扩散到皮肤中的决定因素。
例如,由于皮肤的角质层(人皮肤的最外层)是亲油的(非极性),因此它为溶解活性成分和促进剂的亲油物质提供了有利的环境。因此,为了引起物质从“供体”基质中的高分配,必须提供不利的环境用于溶解那些亲油物质。这意指粘合剂基质、乳膏、凝胶或液体必须比角质层更少地亲油的或对活性成分物质和促进剂更少地可溶。
基于溶剂的粘合剂基于非极性或稍微极性聚合物,诸如丙烯酸类。因此,亲油物质将溶解在粘合剂中,并且不良地分配到皮肤中。由于大多数促进剂也是亲油的,因此它们也将不良地从亲油的基质分配到皮肤中。因此,大多数促进剂在整体式贴剂中不是非常富有成效的。促进剂不会分配到皮肤中,而且高速率在为活性成分提供穿过皮肤的通道上有效。图9公开了来自在存在一些化学促进剂下的丙烯酸粘合剂的cbd的体外通量。
促进剂的优点在于,当与药物在透皮系统中混合时,期望从粘合剂基质分配到皮肤中。缺点可能在于,它们可能引起皮肤刺激。表1示出了6小时后,来自透皮吸收促进剂中的10%的cbd穿过人尸体皮肤的cbd累积通量(微克/cm2)。数据示出,用于cbd的透皮递送的最好的透皮吸收促进剂是油酸。
发明人发现用于cbd的透皮递送的最好的透皮吸收促进剂是油酸。etoh仅用作水凝胶的促进剂。在粘合剂中不使用是因为它在制造透皮贴剂期间在粘合剂基质在烘箱中干燥期间蒸发。1,2丙二醇在粘合剂中用作温和的促进剂以及难溶于纯粘合剂基质药物,例如雌二醇的增溶剂(ludwigweimann’sformulationofthepmspatchusingestradiolinanacrylicadhesivematrix)油酸具有高沸点,并且可以用于整体式贴剂制剂中。基于具有3%油酸的pib粘合剂的cbd贴剂仅示出cbd透皮通量的50%增加。(参见上图)ef=1.5。增强因子ef=(具有促进剂的透皮通量/不具有促进剂的透皮通量)。显著增强在ef=3-10的范围内。图9示出了具有30%cbd以及3%添加最佳的促进剂的丙烯酸整体式贴剂的cbd通量。即使添加促进剂,cbd通量也比来自pib粘合剂的低得多。因此,pib制剂优于具有促进剂的丙烯酸制剂。未示出,但由发明人进行了测试,结果是具有硅酮粘合剂biopsa7-4302的制剂示出没有cbd通量。因此,pib制剂优于硅酮粘合剂整体式制剂。
比较本公开的体外透皮通量与由其他皮肤贴剂提供的体外透皮通量的实施例。
表2提供了比较了来自本公开(lifetechglobal)的透皮贴剂的透皮通量与来自marysmedicinals以及来自papa&berkley的透皮贴剂的透皮通量的数据。如所示,来自本公开(lifetechglobal)的透皮通量的值优于使用比较皮肤贴剂的用弗朗兹池测试获得的透皮通量的值。
本发明不受本公开的组合物、试剂、方法、诊断、实验室数据等的限制。而且,本发明不受本文公开的任何优选的实施方式的限制。
- 还没有人留言评论。精彩留言会获得点赞!