治疗类固醇激素相关疾病或障碍的组合物和方法与流程
治疗类固醇激素相关疾病或障碍的组合物和方法
[0001]
相关申请的交叉引用
[0002]
本申请根据35 u.s.c.
§
119(e)要求于2018年6月1日提交的美国临时申请号62/679,386的优先权,其以其全部内容通过引用并入本文。
背景技术:
[0003]
孕酮、雌激素、雄激素和糖皮质激素受体属于一类广泛的类固醇激素受体。类固醇激素受体是配体依赖性的细胞内转录因子,其已显示影响多种癌症的发生和生长,所述癌症包括但不限于前列腺癌、乳腺癌、卵巢癌、肺癌、白血病和淋巴瘤。激素疗法已显示出通过调节类固醇激素受体活性来治疗这类癌症的希望。这些结果表明,调节类固醇激素受体活性可能是治疗多种癌症和其他激素受体相关疾病和障碍的潜在靶标。
[0004]
在本领域中仍存在对用于类固醇激素受体相关疾病和/或障碍的治疗的新型组合物和方法的未满足的需求。本发明满足这种未满足的需求。
技术实现要素:
[0005]
本发明提供了治疗受试者中至少一种疾病或障碍的方法。在某些实施方式中,方法包括向受试者施用治疗上有效量的茜草(rubia cordifolia)的草药提取物或其级分。在某些实施方式中,方法包括向受试者施用存在于茜草的草药提取物或其级分中的任何活性化学种类。
[0006]
在某些实施方式中,至少一种疾病或障碍与至少一种类固醇激素受体的活性或选自brd4、brd2、细胞周期蛋白d1、p53、gata3、聚[adp-核糖]聚合酶-1(parp-1)和cd47的至少一种蛋白质的表达相关。
[0007]
在某些实施方式中,存在于草药提取物中的活性化学种类选自如下化合物和其盐、溶剂化物、异构体、互变异构体或前药:1,3,6-三羟基-2-甲基-9,10-蒽二酮3-o-[α-l-鼠李吡喃糖基-(1
→
2)-6-o-乙酰基-β-d-吡喃葡萄糖苷](rga)、3,6-三羟基-2-甲基-9,10-蒽二酮3-o-[α-l-鼠李吡喃糖基-(1
→
2)-β-d-吡喃葡萄糖苷](rg)
[0008][0009]
在某些实施方式中,草药提取物或其级分包括rga或其盐、溶剂化物、异构体、互变异构体或前药。
[0010]
在某些实施方式中,草药提取物或其级分进一步包括rg或其盐、溶剂化物、异构体、互变异构体或前药。
[0011]
在某些实施方式中,至少一种类固醇激素受体是选自孕酮受体、雌激素受体、雄激素受体和糖皮质激素受体的至少一种。
[0012]
在某些实施方式中,与至少一种类固醇激素受体的活性相关的至少一种疾病或障碍是选自前列腺癌、乳腺癌、卵巢癌、肺癌、子宫癌、胰腺癌、结肠癌,肝细胞癌、恶性胶质瘤、多发性骨髓瘤、nut癌、白血病和淋巴瘤的癌症。
[0013]
在某些实施方式中,癌症是治疗耐药性癌症,选自去势耐药性前列腺癌、恩杂鲁胺耐药性前列腺癌、糖皮质激素受体介导的耐药性前列腺癌、brca1(双链断裂修复)缺陷性癌症、双阴性乳腺癌和三阴性乳腺癌。
[0014]
在某些实施方式中,与至少一种类固醇激素受体的活性相关的至少一种疾病或障碍选自前列腺增生、库兴综合征、雄激素性脱发、痤疮、皮脂溢、多毛症(过多的体毛)、化脓性汗腺炎、性功能障碍、性早熟(男性和女性)、多囊卵巢综合症、乳房痛(乳房疼痛/压痛)、乳腺纤维瘤、乳房组织增生(乳房增大)、巨乳房(乳房肥大)、男子女性型乳房、黄褐斑、月经过多、子宫内膜组织异位、子宫内膜增生、子宫内膜异位、子宫纤维瘤和创伤后应激障碍(ptsd)。
[0015]
在某些实施方式中,与至少一种蛋白质的表达相关的至少一种疾病或障碍选自亨廷顿舞蹈病、精神分裂症、牛皮癣、套细胞淋巴瘤、乳腺癌、膀胱癌、垂体腺瘤、甲状旁腺腺瘤、胰腺癌、头颈部鳞状细胞癌和非小细胞肺癌。
[0016]
在某些实施方式中,方法下调选自brd4、brd2、细胞周期蛋白d1、p53、gata3、聚[adp-核糖]聚合酶-1(parp-1)和cd47的至少一种蛋白质的表达。
[0017]
在某些实施方式中,施用抑制受试者中组蛋白h3的高度乙酰化。
[0018]
在某些实施方式中,施用促进受试者中癌性肿瘤细胞的吞噬作用。
[0019]
在某些实施方式中,施用抑制受试者中吲哚胺-吡咯2,3-双加氧酶(ido)活性。
[0020]
在某些实施方式中,进一步向受试者施用至少一种免疫检查点抑制剂。在某些实施方式中,至少一种免疫检查点抑制剂选自抗pd1、抗pd-l1和抗ctla4。在某些实施方式中,至少一种免疫检查点抑制剂选自伊匹单抗、阿维鲁单抗、派姆单抗、纳武单抗、德瓦鲁单抗和阿特朱单抗。
[0021]
在某些实施方式中,受试者是哺乳动物。
[0022]
在某些实施方式中,受试者是人。
附图说明
[0023]
为了说明本发明,在附图中描绘了本发明的某些实施方式。然而,本发明不限于附图中描绘的实施方式的精确安排和手段。
[0024]
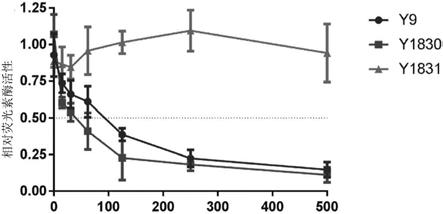
图1是显示茜草的某些草药水提取物制品(y9、y1830、y1831)对22rv1前列腺癌细胞中双氢睾酮(dht)诱导的雄激素受体介导的转录活性的影响。在测量荧光素酶活性之前,用某些批次的茜草水提取物处理转染前列腺特异性抗原(psa)荧光素酶报道基因的22rv1细胞24小时。
[0025]
图2a-2b是一组曲线图,其显示了通过固相二氧化硅萃取(dsc18)柱后,茜草提取物的某些乙醇提取的级分(图2a:y1830;图2b:y9)的抗雄激素受体(ar)活性。使用22rv1 psa-荧光素酶报道基因试验评估抗ar活性。
[0026]
图2c是lc-ms光谱(-ve扫描模式),显示了来自50%乙醇级分的2个峰,分别指定为具有mw 578.4的1,3,6-三羟基-2-甲基-9,10-蒽二酮3-o-[α-l-鼠李吡喃糖基-(1
→
2)-β-d-吡喃葡萄糖苷](rg)和具有mw 620.4的1,3,6-三羟基-2-甲基-9,10-蒽二酮3-o-[α-l-鼠李吡喃糖基-(1
→
2)-6-o-乙酰基-β-d-吡喃葡萄糖苷](rga)。在75%的乙醇级分中观察到rga和rg的分离的蒽醌部分,并被指定为具有mw 270.2的1,3,6-三羟基-2-甲基-9,10-蒽二酮(tmt)。
[0027]
图2d是经过或不经过naoh处理的rga的lc-ms光谱(-ve扫描模式)。lc-ms光谱显示,rga在用碱处理后水解成rg,除去了乙酰基部分。
[0028]
图3是lc-ms光谱(+ve扫描模式),其显示包括rga的级分可以包含m/z=757.4(m+h),m/z=332,m/z=495的额外的分子。
[0029]
图4a-4b是曲线图,其显示在双氢睾酮(dht)存在下,相同剂量的y9、y1830、rg(或包含rg的级分)、rga(或包含rga的级分)和tmt(或包含tmt的级分)对22rv1 ar-荧光素酶报道细胞中ar介导的转录反应的影响。
[0030]
图4c-4d是曲线图,其显示y1830、rg(或包含rg的级分)和rga(或包含rga的级分)对psa(图4c)和klk2(图4d)的mrna的影响。将22rv1细胞用y1830、rga或rg处理过夜,并提取mrna进行qrt-pcr,以确定psa和klk2相对于β-肌动蛋白标准化的mrna表达水平。
[0031]
图5a-5g是图像或曲线图,其显示y1830、rga(或包含rga的级分)和rg(或包含rg的级分)对22rv1和pc3 psa-荧光素酶报道细胞中地塞米松(dex)诱导的糖皮质激素受体(gr)介导的转录反应的影响。图5a是针对lncap、22rv1和pc3细胞中ar和gr蛋白表达的蛋白质印迹分析。图5b-5c是曲线图,其显示在22rv1或pc3 ar-荧光素酶报道细胞中响应于某些剂量的dex的荧光素酶活性。图5d-5e是曲线图,其显示y1830、rg(或包含rg的级分)和rga(或包含rga的级分)对22rv1和pc3 psa-荧光素酶报道细胞中dex诱导的糖皮质激素受体介导的转录反应的影响。图5f-5g是曲线图,其显示使用qrt-pcr在存在或不存在dex的情况下y1830对sgk1(gr的靶基因)mrna表达的影响。
[0032]
图6a-6d是图像和曲线图,其显示y1830、rga(或包含rga的级分)和rg(或包含rg的级分)对标准lncap细胞或gr过表达的lncap细胞的ar或gr驱动的荧光素酶活性的影响。图6a是对于lncap和gr过表达的lncap细胞中ar和gr蛋白表达的蛋白质印迹分析。图6b是曲线图,其显示lncap和gr过表达的lncap细胞对dht和dex的反应。图6c是一组曲线图,其显示y1830、rga(或包含rga的级分)、rg(或包含rg的级分)和恩杂鲁胺(enza)对lncap细胞中ar驱动的荧光素酶活性的影响。图6d是一组曲线图,其显示y1830、rga(包含rga的级分)、rg(或包含rg的级分)和enza对gr过表达的lncap细胞中ar(用dht刺激)或gr(用dex刺激)驱动的荧光素酶活性的影响。lncap细胞和gr过表达的lncap细胞二者均携带具有ar反应元件的荧光素酶报道基因。
[0033]
图7a-7e是曲线图,其显示在存在或不存在dht或dex的情况下持续4天的某些前列腺细胞系的生长。
[0034]
图8a-8b是蛋白质印迹分析,其显示在存在或不存在dht和mg132的情况下,y1830、rga(或包含rga的级分)和rg(或包含rg的级分)对在22rv1细胞中gr、ar、截短的ar(ar-v)、β-连环蛋白(b-cat)和细胞周期蛋白d1(cycd1)的蛋白表达的影响。在存在或不存在dht和mg132的情况下,用y1830、rga(或包含rga的级分)和rg(或包含rg的级分)处理22rv1细胞24
小时。蛋白质印迹分析用于使用蛋白质特异性抗体确定蛋白表达。
[0035]
图9a-9b是蛋白质印迹分析,其显示在存在或不存在dht和mg132的情况下,y1830、rga(或包含rga的级分)和rg或包含rg的级分对mcf7细胞中era、erb、gr、pr-b、pra、ar、ar-v、b-cat和cycd1的蛋白表达的影响。在存在或不存在e2和mg132的情况下,用y1830、rga(或包含rga的级分)和rg(或包含rg的级分)处理mcf7细胞24小时。蛋白质印迹分析用于使用蛋白质特异性抗体确定蛋白表达。
[0036]
图10是蛋白质印迹分析,其显示在存在或不存在e2的情况下,y1830、rga(或包含rga的级分)和rg(或包含rg的级分)对mcf7细胞中p53、h2ax、h2ax-丝氨酸139、parp1和gata3蛋白质的蛋白表达的影响。在存在或不存在e2的情况下,用y1830、rga(或包含rga的级分)和rg(或包含rg的级分)处理mcf7细胞24小时。蛋白质印迹分析用于使用蛋白质特异性抗体确定蛋白表达。
[0037]
图11a-11b是蛋白质印迹分析,其显示在存在或不存在e2的情况下在mcf7细胞中(图11a),和在存在或不存在dht的情况下在22r1细胞中(图11b),y1830、rga(或包含rga的级分)和rg(或包含rg的级分)对brd4、brd2的蛋白表达和赖氨酸9、14和27处组蛋白乙酰化的影响。在存在或不存在e2或dht的情况下,用y1830、rga(或包含rga的级分)和rg(或包含rg的级分)处理细胞24小时。蛋白质印迹分析用于使用蛋白质特异性抗体确定蛋白表达。β-肌动蛋白或组蛋白3用于标准化蛋白质负载。
[0038]
图12a-12c是曲线图,其显示在存在(图12c)或不存在(图12b)e2的情况下,y1830、rga(或包含rga的级分)和rg(或包含rg的级分)对mcf7、t4d、mdamb453和mdamba231细胞的细胞生长的影响,持续4天。
[0039]
图13是曲线图,其显示在体外测定中茜草的某些制品对吲哚胺-吡咯2,3-双加氧酶(ido)活性的影响。将500μg/ml的y1830、y9或n9加入到裂解的hek293细胞中,该细胞已在1mm l-色氨酸存在90分钟的情况下用小鼠ido表达质粒转染了48小时。使用基于比色的试验测量培养基中犬尿氨酸的浓度。
[0040]
图14是一组曲线图,其比较了固相萃取c18柱的y1830的某些乙醇洗脱对ar活性和ido活性的抑制轮廓。e10%、e30%、e50%和e75%(其中e=乙醇)提取物的lc-ms化学剖面显示在下部图上。
[0041]
图15a-15b是曲线图,其显示y1830、rga(或包含rga的级分)和rg(或包含rg的级分)对治疗期间裸鼠的22rv1肿瘤生长和体重的影响。
具体实施方式
[0042]
本发明在一个方面涉及出乎意料的发现:茜草植物(也称为普通茜草(common madder)、印度茜草(indian madder)、manjistha、majith、tamaralli或manditti)的草药提取物是许多常见疾病和障碍的病理学涉及的某些受体、蛋白质和酶的有效抑制剂。
[0043]
一方面,本发明提供了使用茜草的草药提取物或其级分或在草药提取物或其级分中存在的任何活性化学种类来治疗多种疾病和障碍的方法。在某些实施方式中,该方法可用于治疗与类固醇激素受体相关的至少一种疾病或障碍,例如但不限于孕酮受体、雌激素受体、雄激素受体和糖皮质激素受体。在其他实施方式中,方法可用于治疗与选自brd4、brd2、细胞周期蛋白d1、p53、gata3和cd47的至少一种蛋白质的表达相关的至少一种疾病或
障碍。在仍其他实施方式中,草药提取物和从其中分离的活性化学种类可用于治疗选自前列腺癌、乳腺癌、卵巢癌、肺癌、子宫癌、胰腺癌、结肠癌、肝细胞癌、恶性胶质瘤、多发性骨髓瘤、nut癌、白血病和淋巴瘤的至少一种癌症。
[0044]
在仍其他实施方式中,草药提取物和从其中分离的活性化学种类可用于治疗与组蛋白h3的高度乙酰化相关的疾病,例如但不限于亨廷顿舞蹈病和精神分裂症。
[0045]
方法
[0046]
一方面,本发明提供了治疗受试者中至少一种疾病或障碍的方法。在某些实施方式中,该方法包括向受试者施用治疗有效量的茜草的草药提取物或其级分,或该草药提取物或其级分中存在的任何活性化学种类。
[0047]
在某些实施方式中,草药提取物中存在的活性化学种类是1,3,6-三羟基-2-甲基-9,10-蒽二酮3-o-[α-l-鼠李吡喃糖基-(1
→
2)-6-o-乙酰基-β-d-吡喃葡萄糖苷](rga),或其盐、溶剂化物、异构体、互变异构体或前药。
[0048][0049]
在某些实施方式中,在草药提取物中存在的活性化学种类是1,3,6-三羟基-2-甲基-9,10-蒽二酮3-o-[α-l-鼠李吡喃糖基-(1
→
2)-β-d-吡喃葡萄糖苷](rg),或其盐、溶剂化物、异构体、互变异构体或前药。
[0050][0051]
在某些实施方式中,该方法治疗与至少一种类固醇激素受体的活性相关的至少一种疾病或障碍。在其他实施方式中,至少一种类固醇激素受体选自孕酮受体、雌激素受体、雄激素受体和糖皮质激素受体。在仍其他实施方式中,该方法下调选自雄激素受体、雌激素受体α和孕酮受体的至少一种类固醇激素受体的表达。在仍其他实施方式中,该方法抑制糖皮质激素受体的活性。
[0052]
在某些实施方式中,至少一种疾病或障碍是癌症。在其他实施方式中,癌症是选自前列腺癌、乳腺癌、卵巢癌、肺癌、子宫癌、胰腺癌、结肠癌、肝细胞癌、恶性胶质瘤、多发性骨髓瘤、nut癌、白血病和淋巴瘤的至少一种。
[0053]
在仍其他实施方式中,癌症是癌症的治疗耐药性形式。在仍其他实施方式中,癌症是选自去势耐药性前列腺癌、恩杂鲁胺耐药性前列腺癌、brca1(双链断裂修复)缺乏性癌症和糖皮质激素受体介导的耐药性前列腺癌的至少一种。在仍其他实施方式中,癌症是双阴性乳腺癌或三阴性乳腺癌。在仍其他实施方式中,三阴性乳腺癌是mba-mb-231或mba-mb-453乳腺癌。
[0054]
在某些实施方式中,至少一种疾病或障碍是前列腺增生。
[0055]
在某些实施方式中,至少一种疾病或障碍是选自如下的激素功能疾病或障碍:库兴综合征、雄激素性脱发、痤疮、皮脂溢、多毛症(过多的体毛)、化脓性汗腺炎、性功能障碍、性早熟(男性和女性)、多囊卵巢综合症、乳房痛(乳房疼痛/压痛)、乳腺纤维瘤、乳房组织增生(乳房增大)、巨乳房(乳房肥大)、男子女性型乳房、黄褐斑、月经过多、子宫内膜组织异位、子宫内膜增生、子宫内膜异位和子宫纤维瘤。
[0056]
在某些实施方式中,方法治疗与至少一种类固醇激素受体的活性相关的至少一种精神障碍。在其他实施方式中,至少一种精神障碍是创伤后应激障碍(ptsd)。
[0057]
在某些实施方式中,方法治疗与至少一种选自以下的蛋白质表达相关的至少一种疾病或障碍:brd4、brd2、细胞周期蛋白d1、p53、gata3、聚[adp-核糖]聚合酶-1(parp-1)和cd47。在其他实施方式中,与至少一种蛋白质的表达相关的至少一种疾病或障碍选自与本文其他地方描述的至少一种癌症和至少一种炎症疾病或障碍。
[0058]
在某些实施方式中,方法下调了受试者中的brd4表达,从而抑制组蛋白h3的高度乙酰化。在其他实施方式中,方法减少组蛋白3赖氨酸27的乙酰化(h3ac-lys27)但没有减少h3 ac-lys9或h3 ac-lys14的乙酰化。在仍其他实施方式中,方法治疗与组蛋白h3的高度乙酰化相关的至少一种疾病或障碍,所述至少一种疾病或障碍选自但不限于本文其他地方描述的至少一种癌症、炎症性疾病和障碍、自身免疫性疾病和障碍、亨廷顿舞蹈病和精神分裂症。
[0059]
在某些实施方式中,方法下调了受试者中的cd47表达。不受限于任何具体理论,肿瘤细胞上cd47表达的下调可以防止巨噬细胞对肿瘤细胞的吞噬作用的抑制。在其他实施方式中,方法促进受试者中癌肿瘤细胞的吞噬作用。
[0060]
在某些实施方式中,方法下调了受试者中的细胞周期蛋白d1表达。在其他实施方式中,方法治疗选自牛皮癣、套细胞淋巴瘤、乳腺癌、膀胱癌、垂体腺瘤、甲状旁腺腺瘤、胰腺癌、头颈部鳞状细胞癌和非小细胞肺癌的至少一种疾病或障碍。
[0061]
在某些实施方式中,方法抑制受试者中的吲哚胺-吡咯2,3-双加氧酶(ido)的活性。
[0062]
在某些实施方式中,方法可用作基于免疫疗法的治疗方案的一部分。在其他实施方式中,方法进一步包括向受试者施用至少一种免疫检查点抑制剂。在仍其他实施方式中,免疫检查点抑制剂选自抗pd1、抗pd-l1和抗ctla4。在其他实施方式中,免疫检查点抑制剂选自伊匹单抗、阿维鲁单抗、派姆单抗、纳武单抗、德瓦鲁单抗和阿特朱单抗。
[0063]
在某些实施方式中,方法进一步包括向受试者施用至少一种另外的抗癌剂。在其他实施方式中,至少一种另外的抗癌剂是化疗剂。
[0064]
在另一方面,本发明提供了调节受试者中一种或多种类固醇激素受体的方法,用于除了治疗疾病或障碍的目的。在某些实施方式中,本发明提供了终止受试者中妊娠的方
法。在其他实施方式中,本发明提供了在受试者中避孕的手段。在仍其他实施方式中,方法包括向受试者施用治疗有效量的茜草的草药提取物或其级分,或草药提取物或其级分中存在的任何活性化学种类。
[0065]
在某些实施方式中,受试者是哺乳动物。在其他实施方式中,受试者是人。
[0066]
在某些实施方式中,将草药提取物口服施用至受试者。在其他实施方式中,以选自如下的至少一种形式施用草药提取物:丸剂、片剂、胶囊、汤剂、茶剂、浓缩液、糖衣丸、液体、滴剂和软胶囊。
[0067]
在某些实施方式中,本发明的草药提取物可以是水提取物。可以通过包括以下步骤中的至少一个的方法来制备水提取物:干燥本发明的草药,将干燥的草药研磨成草药粉,将草药粉加入一定量的水中以形成混合物,将混合物加热至高温下持续一段时间,使混合物冷却至室温,移出和除去任何不溶的固体。
[0068]
在某些实施方式中,将草药粉以每1毫升水100毫克草药的比例添加到水中。在某些实施方式中,将混合物加热至约80℃的温度持续约1小时。在某些实施方式中,通过将混合物离心以形成小球然后倾析并收集水提取物,留下固体小球来除去未溶解的固体。
[0069]
本发明的活性化合物可以具有一个或多个立体中心,并且每个立体中心可以以(r)或(s)构型独立地存在。在一个实施方式中,本文所述的化合物以旋光或外消旋形式存在。本文所述的化合物包括具有本文所述的治疗上有用的性质的外消旋、旋光、区域异构和立体异构形式或其组合。旋光形式的制备可以以任何合适的方式进行,包括但不限于,通过用重结晶技术的外消旋形式的解析、由旋光起始原料合成、手性合成或使用手性固定相的色谱分离。在一个实施方式中,一种或多种异构体的混合物用作本文所述的治疗性化合物。在另一个实施方式中,本文所述的化合物包含一个或多个手性中心。这些化合物可以通过任何手段制备,包括立体选择合成、对映选择合成和/或分离对映异构体和/或非对映异构体的混合物。化合物及其异构体的解析通过任何手段实现,其包括但不限于化学方法、酶促方法、分级结晶、蒸馏和色谱法。
[0070]
在一个实施方式中,本发明的活性化合物作为互变异构体存在。所有互变异构体都包括在本文叙述的化合物的范围内。
[0071]
在一个实施方式中,本文所述的化合物被制备为前药。“前药”是体内转化成母体药物的试剂。在一个实施方式中,在体内施用后,将前药化学转化为化合物的生物学、药学或治疗活性形式。在另一个实施方式中,前药通过一个或多个步骤或方法被酶促地代谢为化合物的生物学、药学或治疗活性形式。
[0072]
施用/剂量/制剂
[0073]
施用方案可以影响由什么构成有效量。治疗性制剂可以在本发明中考虑的疾病或障碍的发作之前或之后被施用至受试者。进一步,几个分开的剂量以及交错的剂量可以被每日或顺序地施用,或剂量可以被连续地输注,或可以是弹丸注射(bolus injection)。进一步,根据治疗或预防情况的紧急状态指示,治疗性制剂的剂量可以成比例地增加或减少。
[0074]
施用本发明的组合物至患者,优选地哺乳动物,更优选地人,可以使用已知的程序以对治疗在本发明中考虑的疾病或障碍有效的剂量和持续时间段实施。实现治疗效果必需的治疗性化合物的有效量可以根据如下因素变化,比如患者中的疾病或障碍的状态;患者的年龄、性别和重量;和治疗性化合物治疗在本发明中考虑的疾病或障碍的能力。可以调节
剂量方案以提供最佳的治疗反应。例如,几个分开的剂量可以被每日施用,或根据治疗情况的紧急状态指示的,剂量可以成比例地减少。本发明的治疗性化合物的有效剂量范围的非限制性实例是大约1和1,000mg/kg体重/每天。可以施用可用于实践本发明的药物组合物以递送从1ng/kg/天至100mg/kg/天的剂量。本领域普通技术人员将能够研究相关因素并且做出关于治疗性化合物的有效量的决定而不需要过度实验。
[0075]
本发明的药物组合物中的活性成分的实际剂量水平可以变化,以便于获得的活性成分量对具体的患者、组合物和施用模式实现期望的治疗反应是有效的,而对患者是无毒的。
[0076]
具体地,所选择的剂量水平取决于多种因素,包括所用具体化合物的活性,施用时间,化合物的排泄速率,治疗的持续时间,与所述化合物组合使用的其他药物、化合物或材料,所治疗患者的年龄、性别、体重、状况、一般健康状况和既往病史,以及医学领域众所周知的类似因素。
[0077]
具有本领域普通技术的医师(例如医师或兽医)可以容易地确定和开处方有效量的需要的药物组合物。例如,医师或兽医可以以比为了实现期望的治疗效果所需要的低的水平开始在药物组合物中采用的本发明化合物的剂量,并且逐渐地增加剂量直到取得期望的效果。
[0078]
在具体实施方式中,以剂量单位形式配制化合物是特别有利的,以易于施用和剂量均匀。如本文所使用,剂量单位形式是指适合作为待治疗患者的单一剂量(unitary dosage)的物理上离散的单位;每个单位都包含预定量的治疗化合物,该化合物经计算可与所需的药物媒介物结合以产生所需的治疗效果。本发明的剂量单位形式由(a)治疗化合物的独特特征和待实现的具体治疗效果,以及(b)在配药/配制这种用于治疗本发明中考虑的疾病或障碍的治疗性化合物的领域中固有的局限性决定并直接取决于它们。
[0079]
在某些实施方式中,使用一种或多种药学上可接受的赋形剂或载体配制本发明的组合物。在其他实施方式中,本发明的药物组合物包括治疗有效量的本发明的化合物和药学上可接受的载体。在仍其他实施方式中,本发明的化合物是组合物中唯一的生物活性剂(即能够治疗癌症)。在仍其他实施方式中,本发明的化合物是组合物中治疗有效量的唯一生物活性剂(即,能够治疗癌症)。
[0080]
载体可以是溶剂或分散介质,其包含,例如,水、乙醇、多元醇(例如,甘油、丙二醇和液体聚乙二醇等)、其合适的混合物和植物油。可以维持适当的流动性,例如,通过使用包衣比如卵磷脂、在分散的情况下通过维持需要的颗粒大小和通过使用表面活性剂。可以通过多种抗细菌剂和抗真菌剂实现防止微生物活动,例如对羟基苯甲酸酯类、氯丁醇、苯酚、抗坏血酸、硫柳汞等。在许多情况下,在组合物中包括等渗剂将是优选的,例如,糖、氯化钠或多元醇比如甘露醇和山梨醇。可以通过在组合物中包括延迟吸收的试剂例如单硬脂酸铝或明胶来实现可注射组合物的延长吸收。
[0081]
在某些实施方式中,本发明的组合物以范围为每天1-5次或更多的剂量施用于患者。在其他实施方式中,本发明的组合物以包括但不限于每天、每两天、每三天一次至每周一次和每两周一次的剂量范围施用至患者。对本领域技术人员而言显而易见的是,本发明的多种组合物的施用频率将因个体而异,这取决于许多因素,其包括但不限于年龄、待治疗的疾病或障碍、性别、整体健康状况和其他因素。因此,本发明不应被解释为限于任何具体
的剂量方案,并且将通过考虑与患者有关的所有其他因素的主治医生来确定待施用于任何患者的精确剂量和组合物。
[0082]
用于施用的本发明的化合物和/或组合物可以在如下范围内:约1mg至约10,000mg、约20mg至约9,500mg、约40mg至约9,000mg、约75mg至约8,500mg、约150mg至约7,500mg、约200mg至约7,000mg、约400mg至约6,000mg、约500mg至约5,000mg、约750mg至约4,000mg、约1,000mg至约3,000mg、约1,000mg至约2,500mg、约20mg至约2,000mg和这些之间的任何和所有整体或部分增量。
[0083]
在某些实施方式中,本发明涉及包装的药物组合物,其包括容纳治疗有效量的本发明化合物单独或与第二药物组合的容器;以及使用该化合物治疗、预防或减轻本发明考虑的疾病或障碍的一种或多种症状的说明书。
[0084]
制剂可以以与常规的赋形剂——即药学上可接受的有机或无机载体物质,其适于口服、肠胃外、鼻、静脉内、皮下、肠内或本领域已知的任何其他合适的施用模式——的混合物被应用。药物制品可以被灭菌,并且如果期望,可以与辅助剂,如润滑剂、防腐剂、稳定剂、润湿剂、乳化剂、用于影响渗透压缓冲剂的盐、着色剂、调味剂和/或芳香族物质等混合。在期望时,它们也可以与其他活性剂组合。
[0085]
本发明的任何组合物的施用途径包括口鼻、直肠、阴道内、肠胃外、口腔、舌下或局部。可将本发明中使用的化合物配制为通过任何合适的途径施用,例如通过:口服或肠胃外,例如,经皮、经粘膜(如舌下、舌、(经)口腔、(经)尿道、阴道(如,经-和环阴道地)、鼻(内)和(经)直肠)、膀胱内、肺内、十二指肠内、胃内、鞘内、皮下、肌肉内、皮内、腹膜内、动脉内、静脉内、支气管内、吸入和局部施用。
[0086]
合适的组合物和剂型包括例如片剂、胶囊剂、囊片、丸剂、软胶囊(gel caps)、含片、分散剂、悬浮剂、溶液、糖浆、颗粒剂、珠、经皮贴剂、凝胶、粉剂、粒剂、乳浆剂(magmas)、锭剂、乳膏剂、糊剂、膏药、洗剂、盘剂、栓剂、经鼻或口服施用的液体喷雾剂、用于吸入的干粉或气雾制剂、用于膀胱内施用的组合物和制剂等。应当理解,可用于本发明的制剂和组合物不限于本文所述的具体制剂和组合物。
[0087]
口服施用
[0088]
对于口服应用,具体合适的是汤剂、茶剂(teas)、浓缩液、片剂、糖衣丸、液体、滴剂、栓剂或胶囊、囊片和软胶囊。预期用于口服用途的组合物可以根据本领域已知的任何方法来制备,并且这种组合物可以包含选自适合用于制造片剂的惰性、无毒的药物赋形剂的一种或多种药剂。这样的赋形剂包括例如惰性稀释剂,例如乳糖;制粒剂和崩解剂,例如玉米淀粉;结合剂,例如淀粉;和润滑剂,例如硬脂酸镁。片剂可以是未包衣的,或其也可以使用已知的技术进行包衣,以提高审美(elegance)或延迟活性成分的释放。用于口服用途的制剂也可以硬的明胶胶囊形式存在,其中活性成分与惰性稀释剂混合。
[0089]
对于口服施用,本发明的化合物可以是片剂或胶囊的形式,其通过常规的手段使用药学上可接受的赋形剂比如结合剂(例如,聚乙烯吡咯烷酮、羟丙基纤维素或羟丙基甲基纤维素);填料(例如,玉米淀粉、乳糖、微晶纤维素或磷酸钙);润滑剂(例如,硬酯酸镁、滑石或二氧化硅);崩解剂(例如,淀粉乙醇酸钠);或湿润剂(例如,月桂基硫酸钠)制备。用于口服施用的液体制品可以是溶液、糖浆或悬浮液的形式。液体制品可以通过常规的手段使用如下药学上可接受的添加剂制备,比如悬浮剂(例如,山梨醇糖浆、甲基纤维素或氢化食用
脂肪);乳化剂(例如,卵磷脂或金合欢胶);非水性媒介物(例如,杏仁油、油酯或乙醇);和防腐剂(例如,对羟基苯甲酸甲酯或丙酯、或山梨酸)。在药学领域熟知用于改变活性成分的起始粉末或其它微粒状材料的粒化技术。粉末通常与粘合剂材料混合为较大的永久性自由流动的团块或颗粒,其被称为“成粒”。例如,使用溶剂的“湿”成粒工艺的特征一般在于粉末与粘合剂材料组合,并且使用水或有机溶剂在导致形成湿颗粒状物质的条件下将其弄湿,然后溶剂必须从其蒸发。
[0090]
熔融成粒通常在于使用在室温下为固体或半固体的材料(即具有相对低的软化点或熔点范围)以促进粉末状或其它材料的成粒,其必须是在缺乏添加的水或其它液体溶剂的情况下。当加热至熔点范围中的温度时,低熔点固体液化以充当粘合剂或成粒介质。液化的固体自身在与其接触的粉末状材料的表面之上扩散,并且当冷却时,形成固体颗粒状物质,其中初始材料结合在一起。然后,所得的熔融成粒可以提供至压片机或被封装,用于制备口服剂型。通过形成固体分散物或固溶体,熔融成粒改善了活性成分(即药物)的溶解速率和生物利用度。
[0091]
美国专利号5,169,645公开了具有改进的流动性质的直接可压缩的含蜡颗粒剂。当蜡在熔融物中与某些流动改进添加剂混合,接着混合物冷却和成粒时,获得颗粒剂。在某些实施方式中,仅蜡自身熔化在蜡(一种或多种)和添加剂(一种或多种)的熔融组合中熔化,并且在其它情况下,蜡(一种或多种)和添加剂(一种或多种)二者都熔化。
[0092]
本发明还包括多层片剂,其包括提供延迟释放本发明的一种或多种化合物的层,和提供立即释放用于治疗本发明考虑的疾病或障碍的药物的进一步的层。使用蜡/ph敏感性聚合物混合物,可以获得其中包裹(entrap)活性成分的胃不溶性组合物,以确保其延迟释放。
[0093]
肠胃外施用
[0094]
如本文所用,药物组合物的“肠胃外施用”包括特征在于物理破坏受试者组织和通过组织中的裂口(breach)来施用药物组合物的任何施用途径。因此,肠胃外施用包括但不限于通过注射组合物、通过手术切口施加组合物、通过穿透组织的非手术伤口施加组合物等施用药物组合物。具体地,考虑肠胃外施用包括但不限于皮下、静脉内、腹膜内、肌内、胸骨内注射和肾透析输注技术。
[0095]
适用于肠胃外施用的药物组合物的制剂包括与药学上可接受的载体例如无菌水或无菌等渗盐水组合的活性成分。这样的制剂可以以适合于弹丸施用或连续施用的形式制备、包装或出售。可注射制剂可以以单位剂型例如在含有防腐剂的安瓿或多剂量容器中制备、包装或出售。用于肠胃外施用的制剂包括但不限于悬浮液、溶液、在油性或水性媒介物中的乳剂、糊剂和可植入的缓释或可生物降解的制剂。这样的制剂可以进一步包含一种或多种另外的成分,其包括但不限于悬浮剂、稳定剂或分散剂。在用于肠胃外施用的制剂的一个实施方式中,以干燥(即粉末或颗粒)形式提供活性成分,以便用合适的媒介物(例如无菌无热原的水)进行重构,然后肠胃外施用该重构的组合物。;
[0096]
药物组合物可以以无菌可注射的水性或油性悬浮液或溶液的形式制备、包装或出售。该悬浮液或溶液可以根据已知技术进行配制,并且除了活性成分之外,还可以包含另外的成分,例如本文所述的分散剂、湿润剂或悬浮剂。例如,可以使用无毒的肠胃外可接受的稀释剂或溶剂(诸如水或1,3丁二醇)制备此类无菌可注射的制剂。其他可接受的稀释剂和
溶剂包括但不限于林格溶液、等渗氯化钠溶液和固定油,例如合成甘油单酯或甘油二酯。有用的其他可肠胃外施用的制剂包括包含以微晶形式、在脂质体制品中或作为可生物降解的聚合物系统的组分的活性成分的那些制剂。用于缓释或植入的组合物可以包含药学上可接受的聚合或疏水材料,例如乳液、离子交换树脂、微溶聚合物或微溶盐。
[0097]
控释的制剂和药物递送系统
[0098]
在某些实施方式中,本发明的制剂可以但不限于是短期、快速失效(rapid-offset)、以及受控的,例如,缓释、延迟释放和脉冲释放制剂。
[0099]
术语缓释以其常规的意思使用,指的是如此药物制剂,其在延长的时段内提供逐步的药物释放,并且其可以在延长的时段内导致基本上恒定的药物血液水平——但是非必须的。时段可以长达一个月或更长,并且应当是比以弹丸形式施用的相同量的药剂更长的释放。
[0100]
对于缓释,化合物可以使用为化合物提供缓释性质的合适的聚合物或疏水材料配制。因此,本发明的方法内可用的化合物可以以微粒的形式施用,例如,通过注射,或通过以晶片或圆片的形式植入施用。
[0101]
在本发明的一个实施方式中,使用缓释制剂,本发明的化合物单独地或与另一种药剂结合施用至患者。
[0102]
术语延迟释放在本文以其常规的意思使用,指的是如此药物制剂,其在药物施用后的一些延迟之后提供药物的初始释放,并且其可以包括从约10分钟上至约12小时的延迟——但是非必须的。
[0103]
术语脉冲释放在本文以其常规的意思使用,指的是如此药物制剂,其以在药物施用后产生药物的脉冲血浆分布的方式提供药物的释放。
[0104]
术语立即释放以其常规的意思使用,指的是如此药物制剂,其在药物施用后立即提供药物的释放。
[0105]
如本文所用,短期指的是在药物施用后上至并包括约8小时、约7小时、约6小时、约5小时、约4小时、约3小时、约2小时、约1小时、约40分钟、约20分钟、约10分钟或约1分钟和在药物施用后其任何或所有整体或部分增量的任何时段。
[0106]
如本文所用,快速失效指的是在药物施用后上至并包括约8小时、约7小时、约6小时、约5小时、约4小时、约3小时、约2小时、约1小时、约40分钟、约20分钟、约10分钟或约1分钟和其任何和所有整体或部分增量的任何时段。
[0107]
给药
[0108]
本发明化合物的治疗有效量或剂量取决于患者的年龄和体重、患者当前的医疗状况以及本发明中考虑的疾病或障碍的进展。技术人员能够根据这些和其他因素确定合适的剂量。
[0109]
本发明的化合物的合适的剂量可以在每天约0.01mg至约5,000mg的范围中,诸如每天约0.1mg至约1,000mg,例如每天约1mg至约500mg,诸如每天约5mg至约250mg。该剂量可以以单剂量或以多剂量施用,例如每天1至5次或更多次。当使用多剂量时,每剂的量可以是相同的或不同的。例如,每天1mg的剂量可以以两个0.5mg的剂量施用,在剂量之间具有约12小时的间隔。
[0110]
应当理解,在非限制性实例中,可以每天、每隔一天、每2天、每3天、每4天或每5天
施用每天给药的化合物的量。例如,利用每隔一天施用,则可以在周一开始每天5mg的剂量,在周三施用第一个随后每天5mg的剂量,在周五施用第二个随后每天5mg的剂量等等。
[0111]
在其中患者的状况确实有所改善的情况下,根据医生的判断,任选地连续给予本发明的抑制剂的施用;可选地,暂时降低或暂时中止正施用的药物的剂量,持续一定长度的时间(即,“休药期”)。休药期的长度任选地在2天和1年之间变化,仅作为实例包括,2天、3天、4天、5天、6天、7天、10天、12天、15天、20天、28天、35天、50天、70天、100天、120天、150天、180天、200天、250天、280天、300天、320天、350天或365天。在休药期期间的剂量减少包括10%-100%,仅作为实例包括,10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%或100%。
[0112]
一旦患者状况的改善发生,如果必要,可施用维持剂量。随后,根据疾病或障碍,施用的剂量或频率或二者降低到保持改善的疾病的水平。在某些实施方式中,患者在症状和/或感染的任何复发时需要长期间歇治疗。
[0113]
用于本发明的方法的化合物可以以单位剂型配制。术语“单位剂型”是指适合作为经受治疗的患者的单一剂量的物理离散单位,其中每个单位包含经计算以产生期望的治疗效果的预定量的活性物质,其任选地与合适的药物载体结合。单位剂型可以是单次日剂量或多次日剂量(例如,每天约1至5次或更多次)中的一个。当使用多次日剂量时,每剂的单位剂型可以是相同的或不同的。
[0114]
任选地,在实验动物中确定这种治疗方案的毒性和治疗疗效,其包括但不限于ld50(使50%的群体致死的剂量)和ed50(对50%的群体治疗有效的剂量)的确定。毒性和治疗效果之间的剂量比是治疗指数,其表示为ld50和ed50之间的比。从动物研究获得的数据任选地用于配置用于人的剂量范围。这种化合物的剂量优选地在循环浓度的范围内,该循环浓度包括具有最小毒性的ed50。任选地,剂量在该范围内变化,这取决于采用的剂型和使用的施用途径。
[0115]
除非另有说明,否则本发明的实践采用分子生物学(包括重组技术)、微生物学、细胞生物学、生物化学和免疫学的常规技术,其在技术人员的能力范围内。这些技术在文献中被充分地解释,诸如“molecular cloning:a laboratory manual”,第二版(sambrook,1989);“oligonucleotide synthesis”(gait,1984);“animal cell culture”(freshney,1987);“methods in enzymology”“handbook of experimental immunology”(weir,1996);“gene transfer vectors for mammalian cells”(miller and calos,1987);“current protocols in molecular biology”(ausubel,1987);“pcr:the polymerase chain reaction”,(mullis,1994);“current protocols in immunology”(coligan,1991)。这些技术适用于本发明的多核苷酸和多肽的产生,并且因此可以在进行和实践本发明时考虑。在下面的部分中将讨论用于具体实施方式的具体有用的技术。
[0116]
仅使用常规实验,本领域技术人员将认识到或能够确定本文所述的具体程序、实施方式、权利要求和实施例的许多等同方案。这样的等同方案被认为在本发明的范围内,并由所附的权利要求书涵盖。例如,应该理解,用本领域公认的替代方案并且仅使用常规实验对反应条件(包括但不限于反应时间、反应大小/量和实验试剂)的改进在本申请的范围内。
[0117]
定义
[0118]
如本文所用,以下每个术语在本部分中具有与其相关的含义。
[0119]
除非另有定义,否则本文所用的所有技术和科学术语通常具有与本发明所属领域的普通技术人员通常所理解的相同的含义。通常,本文所用的命名法以及动物药理学、药物学、分离科学和有机化学中的实验室程序是本领域众所周知的和常用的。应当理解,只要本教导仍然可操作,步骤的顺序或用于执行某些动作的顺序就无关紧要。此外,可以同时进行或不同时进行两个或更多个步骤或动作。
[0120]
如本文所用,冠词“一个”和“一种”是指该冠词的语法对象中的一个或多于一个(即,至少一个)。举例来说,“一个元件”是指一个元件或多于一个元件。
[0121]
如本文所用,术语“约”将被本领域普通技术人员理解,并且将在使用它的上下文中在一定程度上有所变化。如本文中所用,当指代诸如量、持续时间等的可测量值时,术语“约”旨在涵盖偏离规定值的
±
20%或
±
10%,更优选
±
5%,甚至更优选
±
1%和仍更优选
±
0.1%的变化,因为这样的变化适合执行所公开的方法。
[0122]
如本文所用,术语“癌症”被限定为特征在于异常细胞快速且不受控制生长的疾病。癌细胞可以局部扩散,也可以通过血液和淋巴系统扩散到身体的其他部分。多种癌症的实例包括但不限于骨癌、乳腺癌、前列腺癌、卵巢癌、宫颈癌、皮肤癌、胰腺癌、结肠直肠癌、肾癌、肝癌、脑癌、淋巴瘤、白血病、肺癌等。
[0123]
在一个方面,与受试者有关的术语“共同施用的(co-administered)”和“共同施用(co-administration)”是指向受试者施用本发明的化合物和/或组合物,连同也可以治疗或预防本文所考虑的疾病或障碍的化合物和/或组合物。在某些实施方式中,作为单一治疗方法的一部分,共同施用的化合物和/或组合物被分开施用或以任何种类的组合施用。可以以任何种类的组合将共同施用的化合物和/或组合物配制成在多种固体、凝胶和液体制剂下的固体和液体的混合物,以及作为溶液。
[0124]
如本文所用,术语“组合物”或“药物组合物”是指在本发明中有用的至少一种化合物与药学上可接受的载体的混合物。药物组合物有利于将化合物施用至患者或受试者。本领域存在多种施用化合物的技术,包括但不限于静脉内、口服、气溶胶、肠胃外、眼、鼻、肺和局部施用。
[0125]
如本文所用,“疾病”是其中动物不能维持内稳态的动物的健康状态,并且其中如果疾病没有得到改善,则动物的健康继续恶化。
[0126]
如本文所用,“障碍”在动物中是如下健康状态:其中动物能够维持内稳态,但是其中动物的健康状态比它在不存在障碍的情况下将具有的健康状态较不利。不加以治疗,障碍不必然引起动物的健康状态的进一步降低。
[0127]
如本文所用,术语“提取物”是指衍生自天然来源例如草药或其他植物材料的化合物或药物的浓缩制品或溶液。提取物可以通过许多方法制备,其包括将草药浸泡在溶液中或干燥并研磨草药成粉末并将粉末溶解在溶液中。在将一定量的期望化合物溶解在溶液中之后,可以通过除去一部分溶剂来进一步浓缩提取物。提取物也可以被过滤或离心以从溶液中移出任何固体材料。
[0128]
如本文所用,短语“抑制”是指以可测量的量减少分子、反应、相互作用、基因、mrna和/或蛋白质的表达、稳定性、功能或活性或对其完全防止。抑制剂是例如结合以部分或完全阻断刺激,减少、防止、延迟激活、失活、脱敏或下调蛋白质、基因和mrna的稳定性、表达、功能和活性的化合物,例如拮抗剂。
[0129]
术语“患者”、“受试者”或“个体”在本文可交换地使用,并且指的是服从本文描述的方法的任何动物或其细胞,无论在体外或在原位。在非限制性实施方式中,患者、受试者或个体是人。在其他实施方式中,患者是非人哺乳动物,包括,例如,家畜和宠物,诸如绵羊、牛、猪、犬科、猫科和鼠科哺乳动物。在仍其他实施方式中,患者是鸟类动物或鸟。优选地,患者、个体或受试者是人。
[0130]
如本文所用,术语“药学上可接受的”是指不消除化合物的生物活性或性质并且相对无毒的材料,比如载体或稀释剂,即,可以将材料施用至个体,而不会引起不期望的生物效应或以有害的方式与其中所包含的组合物的任何组分相互作用。
[0131]
如本文所用,术语“药学上可接受的载体”是指参与在患者体内或向患者运载或运输本发明中有用的化合物,使得其可以执行其预期的功能的药学上可接受的材料、组合物或载体,比如液体或固体填料、稳定剂、分散剂、悬浮剂、稀释剂、赋形剂、增稠剂、溶剂或封装材料。通常,将这种构建体从身体的一个器官或部分运载或运输到身体的另一器官或部分。从与制剂的其他成分(包括本发明中有用的化合物)相容的意义上讲,每种载体必须是“可接受的”,并且对患者无害。可以用作药学上可接受的载体的材料的一些实例包括:糖,比如乳糖、葡萄糖和蔗糖;淀粉,比如玉米淀粉和马铃薯淀粉;纤维素和其衍生物,比如羧甲基纤维素钠、乙基纤维素和乙酸纤维素;粉状黄蓍胶(powdered tragacanth);麦芽;明胶;滑石;赋形剂,比如可可脂和栓剂蜡;油,比如花生油、棉籽油、红花油、芝麻油、橄榄油、玉米油和大豆油;乙二醇,比如丙二醇;多元醇,比如甘油、山梨糖醇、甘露糖醇和聚乙二醇;酯,比如油酸乙酯和月桂酸乙酯;琼脂;缓冲剂,比如氢氧化镁和氢氧化铝;表面活性剂;藻酸;无热原水;等渗盐水;林格溶液;乙醇;磷酸盐缓冲溶液;和药物制剂中使用的其他无毒相容性物质。
[0132]
如本文所用,语言“药学上可接受的盐”指的是由药学上可接受的无毒的酸(其包括无机酸、有机酸、其溶剂化物、水合物、或笼形物)制备的施用的化合物的盐。
[0133]
如本文使用的,“预防”、“防止”或“阻止”意思是避免或延迟与受试者中的疾病或病症相关联的症状的发作,所述受试者在施用药剂或化合物开始时还没有发展出这样的症状。
[0134]“治疗性”处理是出于减少或消除那些征兆的目的给展示病理学征兆的受试者施用的处理(治疗)。
[0135]
如本文所用,术语“治疗有效量”是指足以或有效地预防或治疗(延迟或预防发作、预防进展、抑制、减少或逆转)本文所述或考虑的疾病或病症(包括缓解此类疾病或病症的症状)的量。
[0136]
如本文所用,术语“治疗”或“处理”被限定为施加或施用治疗性药剂(即,本发明的化合物(单独或与另一种药剂组合))至患者,或施加或施用治疗性药剂至来自患者的分离的组织或细胞系(例如,用于诊断或离体应用),所述患者具有本文考虑的病症、本文考虑的病症的症状或发展出本文考虑的病症的可能性,目的是治疗、治愈、减轻、缓解、改变、补救、改善、改进或影响本文考虑的病症、本文考虑的病症的症状或发展出本文考虑的病症的可能性。基于从药物基因组学(pharmacogenomics)领域获得的知识,这样的治疗可以被特异性地定制或修改。
[0137]
范围:遍及本公开内容,本发明的多个方面可以以范围格式呈现。应当理解范围格
式的描述仅仅为了便利和简洁,并且不应当解释为对本发明的范围的僵化的限制。因此,范围的描述应当被认为已经具体地公开了该范围内的所有可能的子范围以及个体数值。例如,范围诸如1至6的描述应当被认为已经具体地公开了子范围诸如1至3、1至4、1至5、2至4、2至6、3至6等,以及该范围内的单个和部分数字,例如,1、2、2.7、3、4、5、5.3和6。不管范围的宽度如何,这都适用。
[0138]
在此使用以下缩写:
[0139]
ar
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
雄激素受体
[0140]
ar-v
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
截短的雄激素受体
[0141]
bet
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
布罗莫结构域(溴结构域)和额外终端
[0142]
brd
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
含布罗莫结构域的蛋白质
[0143]
cycd1
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ
细胞周期蛋白d1
[0144]
dex
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
地塞米松
[0145]
dht
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
双氢睾酮
[0146]
e2
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
17β-雌二醇
[0147]
gr
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
糖皮质激素受体
[0148]
hplc
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
高效液相色谱
[0149]
ido
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
吲哚胺-吡咯2,3-双加氧酶
[0150]
lc-ms
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ
液相色谱-质谱联用
[0151]
lncap-gr
ꢀꢀꢀꢀꢀꢀ
糖皮质激素受体过表达的lncap细胞
[0152]
mw
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
分子量
[0153]
nmr
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
核磁共振
[0154]
parp-1
ꢀꢀꢀꢀꢀꢀꢀꢀ
聚[adp-核糖]聚合酶-1
[0155]
psa
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
前列腺特异性抗原
[0156]
qpcr
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
定量聚合酶链反应
[0157]
rg
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
1,3,6-三羟基-2-甲基-9,10-蒽二酮3-o-[α-l-鼠李吡喃糖基
[0158]
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ-
(1
→
2)-β-d-吡喃葡萄糖苷]
[0159]
rga
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
1,3,6-三羟基-2-甲基-9,10-蒽二酮3-o-[α-l-鼠李吡喃糖基
[0160]
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ-
(1
→
2)-6-o-乙酰基-β-d-吡喃葡萄糖苷]
[0161]
sirpa
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ
信号调节蛋白-α
[0162]
ssdna
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ
单链dna
[0163]
tmt
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
1,3,6-三羟基-2-甲基-9,10-蒽二酮
[0164]
以下实施例进一步说明了本发明的方面。但是,它们决不是对本文所述的本发明的教导或公开内容的限制。
[0165]
实施例
[0166]
参考以下实验实施例进一步详细描述本发明。提供这些实施例仅出于说明的目的,并且除非另有说明,否则它们不旨在是限制性的。因此,本发明决不应解释为限于以下实施例,而应解释为涵盖由于本文提供的教导而变得显而易见的任何和所有变型。
[0167]
无需进一步描述,相信本领域的普通技术人员可以使用前面的描述和下面的说明性实施例来制备和利用本发明的化合物并实践所要求保护的方法。因此,以下工作实施例
具体指出了本发明的优选实施方式,并且不应解释为以任何方式限制本公开内容的其余部分。
[0168]
材料和方法
[0169]
茜草提取物制备方法
[0170]
干茜草(rubia cordofolia)提取物粉末购自商业来源:y1830(标记为rubiae radix et rhizoma),来自purapharm china;y9(标记为茜草),来自e-fong usa;和y1831(标记为茜草),来自e-fong china。将100mg干粉通过涡旋溶解在2ml离心管中的1ml hplc级水中持续2分钟。然后将草药水混合物在80℃水浴中加热30分钟。将草药水混合物在室温下在台式离心机中以12,000rpm离心5分钟。将上清液转移至新的2ml管中,并用作100mg/ml的草药水提取物。
[0171]
psa-荧光素酶试验方法
[0172]
psa荧光素酶报道细胞
[0173]
22rv1或lncap前列腺癌细胞用于筛选研究。用psa启动子-pgl4.2荧光素酶报道基因稳定转染了22rv1或lncap细胞系。使用dht(25nm)刺激雄激素受体活性持续24h。
[0174]
荧光素酶试验
[0175]
在37℃-co2培养箱中,以30、100、300和1000μg/ml的草药提取物处理报道细胞24小时。使用dht(25nm)刺激雄激素受体活性。使用地塞米松(50nm)刺激糖皮质激素受体活性。使用荧光素酶裂解缓冲液裂解细胞,然后加入含荧光素的荧光素酶缓冲液以产生发光。使用发光酶标仪(luminescence microplate reader)记录发光。
[0176]
前列腺癌细胞培养方法
[0177]
22rv1或lncap前列腺癌细胞在补充有5%fbs、50μg/ml卡那霉素的rpmi 1640培养基中,在37℃、5%co2培养箱中,在康宁t75细胞培养瓶中生长。
[0178]
乳腺癌细胞培养方法
[0179]
mcf7、t47d、mda-mb-453、mda-mb-231乳腺癌细胞在补充有5%fbs、50μg/ml卡那霉素的rpmi 1640培养基中,在37℃、5%co2培养箱中,在康宁t75细胞培养瓶中生长。
[0180]
蛋白表达/蛋白质印迹试验方法
[0181]
使用2
×
sds样品缓冲液(62.5mm tris-hcl、2%sds、10%甘油、50mm dtt和0.05%溴酚蓝)进行总细胞裂解。将样品超声处理10s以剪切dna。使用含有0.4%np40的tris缓冲盐水分离细胞核。然后将细胞提取物通过10%sds-聚丙烯酰胺凝胶电泳,并用miniprotein ii转移装置(bio-rad)转移至0.2μm硝酸纤维素膜(bio-rad laboratories,hercules,ca)。封闭膜,并在含有5%脱脂奶的tbs-t缓冲液(1
×
tbs缓冲液,0.2%tween 20)中进行探测。使用单克隆兔抗ar(1:5000)检测雄激素受体(abcam#133273)、糖皮质激素受体(d8h2)兔单克隆抗体#3660、erα抗体(f-10):sc-8002、brd4(e2a7x)兔单克隆抗体#13440、brd2(d89b4)兔单克隆抗体#5848、parp(46d11)兔单克隆抗体#9532、乙酰基组蛋白h3(lys27)(d5e4)兔单克隆抗体#8173并且用1:2500稀释的单克隆肌动蛋白抗体(sigma,st.louis,mo)检测β-肌动蛋白作为内部对照,以确认相等的蛋白质负载。然后将膜与辣根过氧化物酶缀合的抗小鼠igg和抗兔igg(1:5,000;sigma)一起温育。使用增强的化学发光试剂(perkin-elmer life science products,波士顿,马萨诸塞州)来可视化免疫反应条带,并使用nih的imagej软件对蛋白质条带的密度进行扫描分析。
[0182]
细胞生长试验方法
[0183]
将1ml培养基(无酚红rpmi1640、5%炭透析fbs、50μg/ml卡那霉素(kanamyacin))中的20,000个细胞接种到24孔板的每个孔中,并在5%co2的37℃培养箱中温育过夜。向每个孔中添加不同浓度的草药提取物,以使最终浓度为50μg/ml至500μg/ml。对于前列腺癌细胞,使用dht(25nm)刺激雄激素受体活性。对于糖皮质激素受体过表达的lncap细胞,使用地塞米松(50nm)刺激糖皮质激素受体活性。对于所有乳腺癌细胞,使用e2(10nm)刺激er活性。不含任何类固醇激素的对照培养基用作对照设置。温育4天后,将细胞固定,并用50%乙醇中的0.5%亚甲基蓝染色2小时,然后用自来水洗涤以除去未结合的染料。将板风干,然后通过在室温下摇动3小时将细胞溶解在1%的十二烷基肌氨酸钠(月桂酰肌氨酸钠)中。基于通过分光光度计(molecular devices)在595nm下测量的细胞吸收的亚甲基蓝的量来定量细胞的生长。所有实验均在一式三份的孔中进行,并重复至少三次。
[0184]
nrf2的实时定量pcr(rt-qpcr)和下游基因
[0185]
使用roche high pure rna分离试剂盒从草药处理的细胞中提取rna。然后使用用于rt-qpcr的bio-rad iscript advanced cdna合成试剂盒从rna样品中生成cdna。在cfx pcr机器(bio-rad)中,使用人nrf2、ho1、nqo1和β-肌动蛋白引物(表1)和itaq
tm
universalgreen supermix进行qpcr。使用纯化的pcr产物生成的标准曲线,基于相对于内部对照β-肌动蛋白的阈值循环的变化,计算相对mrna表达。
[0186]
表1
[0187][0188]
ido活性试验方法
[0189]2×
106个hek293细胞用小鼠ido(2μg/10cm平板)转染48小时。对于一块板,使用1ml pbs将细胞收集到2ml管中。将细胞以3,500rpm离心1分钟。然后将细胞在冰冷的pb缓冲液(1ml ph 6.5)中进行超声处理。通过在4℃下以12,000rpm离心5分钟来澄清细胞裂解。将25μl细胞裂解溶液与期望浓度的草药提取物(25μl)混合。反应缓冲液包含50μl pb缓冲液(100mm,ph 6.5)、10μl亚甲基蓝(2.5%)、100μl过氧化氢酶(20mg/ml)、250μl l-色氨酸(500mm),以及每10ml总溶液中加入70mg维生素c。然后将反应缓冲液添加到细胞裂解溶液中。使该溶液在37℃下反应1.5小时。加入30%(25μl)的三氯乙酸,并在50℃下温育1小时。加入0.8%的埃利希(ehrlich)试剂[4-(二甲基氨基)苯甲醛,在乙酸中80mg/10ml,100μl,得自sigma aldrich]。使用紫外可见光谱仪测量540nm处的吸光度,以确定犬尿氨酸浓度。
已发现540nm处的吸光度与样品中犬尿氨酸的含量具有正相关。
[0190]
抑制裸鼠中22rv1前列腺癌生长
[0191]
将100μl基质胶(matrigel)中的22rv1前列腺癌细胞的5
×
106个细胞皮下注射到10周龄的雄性ncr裸鼠中。当22rv1肿瘤达到5mm
×
5mm时,给小鼠口服y1830(水提取物,500mg/kg,po,b.i.d,n5)和rga(或包含rga的级分)(y1830的当量剂量:2.2mg/kg,po,b.i.d.)持续11天。通过使用公式长度
×
宽度2/2估算肿瘤体积。
[0192]
实施例1:草药提取物筛选和潜在活性化合物鉴定
[0193]
茜草是一种在中国和印度的传统药物中使用的草药,在当地被称为茜草(manjistha)。传统医学声称该草药可用于“清洁和冷却血液”,从血液中去除多余的热量和天然毒素,支持肝肾功能,促进月经健康,减少体内多余的水分,减少发烧和关节炎,以及支持血液和尿液的健康流动。
[0194]
茜草的水提取物是从y1830(标记为rubiae radix et rhizoma,得自茜草植物的干燥的根和根茎,来自purapharm china)和y9(茜草,来自e-fong usa)制备的。制备的提取物对双氢睾酮(dht)诱导的雄激素受体(ar)介导的转录活性具有抑制作用,如通过在22rv1前列腺癌细胞中使用荧光素酶报道基因试验所确定的。从y1831(茜草,来自e-fong china)制备的第三种水提取物在抑制ar活性方面未显示任何可观察到的活性(图1)。
[0195]
将y9和y1830(100mg/ml)水提取物通过固相柱(discovery dsc18 1g),并用多种浓度的乙醇/水溶液洗脱。使用前列腺特异性抗原(psa)-荧光素酶报道基因试验(图2a-2b),来自两种水提取物中的50%和75%乙醇洗脱显示出在22rv1细胞中的抗ar活性。基于乙醇洗脱的lc-ms谱中观察到的两个峰的质量以及itokawa等人phytochemistry,1989,28,3465-8,将50%乙醇洗脱液中的两个主要峰指定为mw 578.4的1,3,6-三羟基-2-甲基-9,10-蒽二酮3-o-[α-l-鼠李吡喃糖基-(1
→
2)-β-d-吡喃葡萄糖苷](rg)和mw 620.4的1,3,6-三羟基-2-甲基-9,10-蒽二酮3-o-[α-l-鼠李吡喃糖基-((1
→
2)-6-o-乙酰基-β-d-吡喃葡萄糖苷](rga)。在75%的洗脱液中还发现了rga和rg的分离的蒽醌部分,并指定为mw 270.2的1,3,6-三羟基-2-甲基-9,10-蒽二酮(tmt)(图2c)。
[0196][0197]
实施例2:rga、rg和tmt的分离和阳性鉴定
[0198]
然后从茜草提取物中进行rg和rga的大规模纯化。将2.5g的y1830溶于80℃的10ml hplc级水中持续30分钟。然后将y1830的溶液以10000rpm离心10分钟,并使上清液通过固相柱(discovery dsc18 10g)。用50ml 10%etoh和50ml 30%etoh顺序洗涤该柱,最后用30ml 50%etoh洗脱含有rg、rga和tmt的级分。将50%etoh级分真空干燥,然后重新溶解在3ml 50%etoh中,然后通过第二个固相柱(discovery dsc18 10g)。然后用30ml 0.1%甲酸、30ml 10:90[(甲醇:乙腈88:12):(0.1%甲酸)]、30ml 30:70[(甲醇:乙腈88:12):(0.1%甲酸)]和30ml 45:55[(甲醇:乙腈88:12):(0.1%甲酸)]洗涤第二个柱。通过用30ml 60:40[(甲醇:乙腈88:12):(0.1%甲酸)]洗脱来收集含rg的级分。另外的25ml 60:40[(甲醇:乙腈88:12):(0.1%甲酸)]被洗脱并丢弃,因为其含有rg和rga二者的混合物。然后通过用3 0ml 75:25[(甲醇:乙腈88:12):(0.1%甲酸)]洗脱来收集含有rga的级分。然后将该级分真空干燥。
[0199]
为了产生足够的tmt进行测试,通过添加0.5m hcl并在65℃下搅拌过夜,将rg水解。将反应混合物用naoh中和并真空干燥。将干燥的样品溶于3ml100%etoh中,并通过固相柱(discovery dsc18 10g)。用30ml 30:70[(甲醇:乙腈88:12):(0.1%甲酸)]、30ml 45:55[(甲醇:乙腈88:12):(0.1%甲酸)]和30ml75:25[(甲醇:乙腈88:12):(0.1%甲酸)]洗涤柱以除去任何残留的rg。用30ml100%(甲醇:乙腈88∶12)洗脱包含tmt的级分,并真空干燥。lc-ms(-ve扫描模式)用于确认纯化的rg、rga和tmt的纯度。
[0200]
由于乙酰基可以可选地连接至rga的β-d-吡喃葡萄糖苷部分的3或4位碳,因此两
个异构体具有与rga相同的分子量——在rga中乙酰基与β-d-吡喃葡萄糖苷的6位碳附接。进行了nmr研究以确认合适的rga结构。为了确认rga的最终化学结构,将nmr-c600用于1h扫描和将nmr-c400用于
13
c扫描。
[0201]1h-nmr(dmso-d6)δ:1.06(3h,d,j=6hz,rha-me),1.90(3h,s,ac-me),2.13(3h,s,c-2-me),5.25(1h,rha-1h),5.25(1h,d,j=7.8hz,rha-1h),7.21(1h,q,j=1.2,8.4hz,h-7),7.21(1h,s,h-4),7.45(1h,d,j=2.4hz,h-5),8.08(1h,d,j=8.4hz,h-8),13.20(1h,s,c-6-oh)13c-nmr(dmso)δ:186.86(c-9),182.12(c-10),170.78(ac-co),163.98(c-1),161.77(c-6),60.49(c-3),35.81(c-4a),132.35(c-10a),130.19(c-8),125.03(c-8a),121.95(c-7),121.00(c-2),113.04(c-5),111.08(c-9a),105.75(c-4),100.65(c-1”),97.74(c-1’),77.48(c-3’),76.74(c-2’),74.48(c-5’),72.42(c-4”),70.92(c-3”),70.75(c-2”),70.49(c-4’),69.00(c-5”),63.79(c-6’),20.86(ac-me),18.57(c-6”),9.20(c-2-me)。nmr谱确认rga的最终化学结构为1,3,6-三羟基-2-甲基-9,10-蒽二酮3-o-[α-l-鼠李吡喃糖基-(1
→
2)-6-o-乙酰基-β-d-吡喃葡萄糖苷]。
[0202]
另外,发现以50%甲醇溶液中的0.2n naoh处理rga(1,3,6-三羟基-2-甲基-9,10-蒽二酮3-o-[α-l-鼠李吡喃糖基-(1
→
2)-6-o-乙酰基-β-d-吡喃葡糖苷])10分钟可除去rga的乙酰基,得到rg(图2d)。
[0203]
通过比较(使用lc-ms)纯化的rg、rga和tmt的峰面积与y9、y1830和y1831的水提取物的峰面积来进行y9、y1830和y1831的提取物中rg、rga和tmt含量的定量(表2)。草药的每个提取物中的rga量与草药水提取物的抗ar活性有一些相关性。发现y1830提取物比y9和y1831提取物含有更多的rga,并且y1830提取物表现出最大的抗ar活性(图1)。
[0204]
表2.y9、y1830和y1831中rg、rga和tmt的定量。
[0205][0206]
当在lc-ms检测中使用正扫描模式时,除了rga之外,还可以检测到再多一些的化合物,其中m/z=757.4(m+h)、m/z=332、m/z=495(图3),其在含rga的级分中也可能是潜在的活性化合物。
[0207]
实施例3:分离的化合物的抗ar活性
[0208]
在dht的存在下(图4a-4b),测试了当量剂量的y9、y1830、rg(或包含rg的级分)、rga(或包含rga的级分)和tmt(或包含tmt的级分)对在22rv1细胞中ar介导的转录反应的抑制作用。结果指示,rga(或包含rga的级分)显示出与y1830水提取物非常相似的抗ar活性,而rg(或包含rg的级分)和tmt(包括tmt的级分)显示出对ar非常弱的活性。qpcr结果表明,y1830和rga(或包含rga的级分)在抑制内源ar靶基因psa和klk2的mrna表达中具有相似的活性(图4c-4d)。rg(或包含rg的级分)未显示出这种活性水平。这些结果证实rga(或包含rga的级分)在茜草的ar抑制活性中起关键作用。
[0209]
实施例4:使用提取物和分离的化合物治疗前列腺癌
[0210]
基于先前的结果,假设茜草和rga在治疗前列腺增生和前列腺癌方面具有潜在的
应用。因为测试的22rv1细胞是显示对恩杂鲁胺耐药性的去势耐药性前列腺癌细胞,所以茜草和rga可用于治疗显示恩杂鲁胺耐药性的去势耐药性前列腺癌细胞。
[0211]
约30%的恩杂鲁胺耐药性患者显示糖皮质激素受体(gr)过表达。gr可替代ar功能并驱动恩杂鲁胺耐药性前列腺癌中肿瘤生长。发现y1830水提取物和rga(或包含rga的级分)对在22rv1和pc3 psa-荧光素酶报道细胞中地塞米松(dex)诱导的转录反应具有抑制作用(图5a-5e)。y1830水提取物和rga(或包含rga的级分)也抑制了在22rv1或pc3细胞中dex诱导的sgk1 mrna的表达。结果显示,y1830和rga(或包含rga的级分)可能是gr过表达介导的恩杂鲁胺耐药性前列腺癌的潜在治疗方法。
[0212]
当糖皮质激素受体(gr)在lncap细胞中过表达时(图6a),lncap-gr细胞变得对dex刺激有反应,如荧光素酶活性所反映的(图6b)。当将恩杂鲁胺处理与y1830或rga(或包含rga的级分)处理进行比较时,恩杂鲁胺只可抑制dht诱导的转录反应,而不能抑制dex诱导的转录反应(图6c)。y1830水提取物和rga(或包含rga的级分)可有效抑制dht或dex诱导的转录反应(图6d)。
[0213]
进一步测试了在存在或不存在dht或dex的情况下,恩杂鲁胺、y1830、rga(或包含rga的级分)和rg(或包含rg的级分)抑制不同前列腺细胞系生长的能力。发现22rv1细胞的生长轻微依赖于dht,而不依赖于dex(图7a-7b)。如所预期的,发现22rv1对恩杂鲁胺处理具有耐药性。在存在或不存在dht和dex的情况下,y1830和rga(或包含rga的级分)对22rv1细胞显示出相似的生长抑制作用(表3)。结果指示,在存在dht或dex的情况下,22rv1细胞的生长更易受y1830和rga(或包含rga的级分)影响。在没有dht的情况下,发现lncap细胞不易受恩杂鲁胺、y1830或rga(或包含rga的级分)处理影响。然而,发现dht刺激lncap细胞生长(图7c)。在存在dht的情况下,lncap细胞对恩杂鲁胺、y1830和rga(或包含rga的级分)的处理更为敏感(表3)。发现dex刺激gr过表达lncap(lncap-gr)细胞生长,并使lncap细胞对恩杂鲁胺具有耐药性。在存在dht或dex的情况下,y1830和rga(或包含rga的级分)有效抑制lncap-gr细胞生长。在存在dex的情况下,y1830和rga也抑制pc3细胞生长,但效果较差。在所有条件下,多至500μg/ml的rg(或包含rg的级分)对细胞生长均未显示任何抑制作用。总之,y1830和rga(或包含rga的级分)显示出相似的细胞生长抑制作用,但效力受细胞类型以及是否存在dht或dex影响。这些结果表明y1830和rga(或包含rga的级分)可用于治疗雄激素依赖性和雄激素非依赖性前列腺癌。另外,如在22rv1细胞试验中所示例的,y1830和rga(或包含rga的级分)可用于治疗恩杂鲁胺耐药性癌症。如在lncap-gr dex条件下所示例的,y1830和rga(或包含rga的级分)也可用于抑制gr介导的恩杂鲁胺耐药性。
[0214]
表3.用于抑制不同前列腺细胞系生长的多种化合物的ic
50
。
[0215][0216]
rga和rg的ic
50
标准化为y1830的当量浓度。发现1mg/ml的y1830含有4.4μg/ml的rga。
[0217]
dht:将25nm加入22rv1细胞中。将2nm加入到lncap细胞或lncap-gr(gr过表达)细胞中。
[0218]
dex(地塞米松):将50nm加入到记录的细胞。
[0219]
温育4天后确定细胞生长。将ic 50确定为抑制50%细胞生长所需的浓度。
[0220]
实施例5:y1830和rga/包括rga的级分对激素受体蛋白表达的影响
[0221]
在存在或不存在dht的情况下,发现在22rv1细胞中y1830和rga(或包含rga的级分)下调ar和ar-v(截短的ar)而不下调gr(图8a)。y1830和rga对ar蛋白质的下调可以通过添加mg132(蛋白酶体抑制剂)来抵消(图8b)。不旨在限于任何具体理论,该结果表明y1830和rga(或包含rga的级分)对ar蛋白质的下调可能涉及蛋白酶体途径(一条或多条)的激活。还发现y1830和rga(或包含rga的级分)抑制gr活性而不下调gr蛋白质表达。
[0222]
在存在或不存在dht的情况下,y1830和rga(或包含rga的级分)对细胞周期蛋白d1(cycd1)的蛋白表达具有强抑制作用,并且对β-连环蛋白(catenin)(b-cat)的蛋白表达具有中等抑制作用(图8a)。但是,y1830和rga对cycd1和b-cat蛋白质的下调不受添加mg132的影响。该结果表明,蛋白酶体途径(一条或多条)的激活不是y1830和rga(或包含rga的级分)下调cycd1和b-cat的作用机制。rg(或包含rg的级分)对gr、ar、ar-v、b-cat或cycd1的蛋白表达没有影响(图8a-8b)。
[0223]
在存在或不存在17β-雌二醇(e2)的情况下,发现y1830和rga(或包含rga的级分)下调mcf7乳腺癌细胞中的雌激素受体era、ar、孕酮受体pr(a和b)并轻微下调雌激素受体erb(图9a)。通过添加mg132抵消era和ar蛋白质的下调。然而,mg132不影响pr的下调(图9b)。这些结果表明蛋白酶体途径(一条或多条)参与ar和era下调,但不参与erb和pr。同样,y1830和rga(或包含rga的级分)没有抑制mcf7细胞的gr蛋白表达,类似于在22rv1细胞中观
察到的结果。
[0224]
在存在或不存在e2的情况下,y1830和rga(或包含rga的级分)对细胞周期蛋白d1(cycd1)的蛋白表达具有强抑制作用,并且对β-连环蛋白(b-cat)的表达具有中等抑制作用(图9a)。然而,mg132不影响y1830和rga(或包含rga的级分)对cycd1或b-cat蛋白质的下调。该结果表明蛋白酶体途径(一条或多条)的激活不是mcf7细胞中y1830和rga对cycd1和b-cat下调的作用机制。rg(或包含rg的级分)对所有检查的蛋白质的蛋白表达没有任何影响。
[0225]
在mcf7细胞中,在存在或不存在e2的情况下,y1830和rga(或包含rga的级分)触发组蛋白2ax丝氨酸139磷酸化作用,这是dna双链断裂的标志。还发现y1830和rga(或包含rga的级分)下调聚[adp-核糖]聚合酶-1(parp-1)蛋白质,该蛋白质在修复单链dna(ssdna)断裂中具有重要作用。另外,y1830和rga下调野生型mcf7细胞中的肿瘤蛋白质p53(图10)。这些结果表明y1830和rga(或包含rga的级分)可能阻碍dna修复过程。已知gata3与era以正反馈回路运行,因此,预期观察到y1830和rga(或包含rga的级分)同时下调era蛋白质和gata3蛋白质。cd47(在肿瘤细胞上)的下调通过阻止信号调节蛋白质-α(sirpa)对巨噬细胞的抑制而促进了巨噬细胞对肿瘤细胞的吞噬作用。因此,可能的是y1830和rga(或包含rga的级分)对cd47的下调在免疫疗法应用中可能有用(图10)。
[0226]
布罗莫结构域蛋白(brd2、brd3、brd4)的bet(布罗莫结构域和额外终端结构域(extra-terminal domain))亚家族对于erα和ar依赖性增强子激活和基因转录都很重要。bet抑制剂已显示抑制乳腺癌细胞生长,包括三阴性乳腺癌(tnbc)。y1830和rga(或包含rga的级分)降低了mcf7(有或没有e2)或22rv1(有或没有dht)中的brd2和brd4蛋白表达(图11a-11b)。y1830和rga(或包含rga的级分)选择性降低mcf7和22rv1细胞中的h3k27乙酰化(图11a-11b)。y1830和rga(或包含rga的级分)对h3k9乙酰化或h3k14乙酰化没有大的影响(图11a-11b)。这些结果表明y1830和rga(或包含rga的级分)可以减少brd蛋白质与erα和ar靶基因的启动子/增强子区域的结合,并因此影响它们的转录。这些结果还表明,y1830和rga(或包含rga的级分)不是组蛋白乙酰基转移酶(hat)的泛抑制剂(pan-inhibitor)。仅发现y1830和rga(或包含rga的级分)抑制依赖于h3k27ac的基因子集的转录。
[0227]
在存在或不存在e2的情况下,持续4天测量了y1830、rga(或包含rga的级分)和rg(或包含rg的级分)对mcf7、t4d、mdamb453和mdamba231乳腺癌细胞生长的影响。结果指示,t4d细胞生长几乎完全依赖于e2(图12a)。尽管mcf7细胞的细胞生长并非绝对依赖于e2,但是添加e2(10nm)确实使mcf7细胞的生长加快了一倍(图12a)。mdamb453和mdamba231细胞生长不依赖于e2(图12a)。在存在或不存在e2的情况下,y1830和rga(或包含rga的级分)对mcf7细胞的生长表现出相似的抑制作用,而rg对mcf7细胞的生长抑制作用非常弱(图12b-12c)。当t4d细胞处于e2刺激下时,y1830和rga(或包含rga的级分)显示出对t4d细胞生长的强抑制作用(图12c)。y1830和rga(或包含rga的级分)也抑制了双阴性(er-ve、pr-ve)mdamb-453细胞和三阴性(er-ve、pr-ve、her2-ve)mdamb-231细胞的生长(图12b-12c)。
[0228]
实施例6:y1830和rga对吲哚胺-吡咯2,3-双加氧酶(ido)的抑制
[0229]
吲哚胺-吡咯2,3-双加氧酶(ido)是负责代谢l-色氨酸,将其转化为犬尿氨酸的酶。ido可能在对抗pd1和抗ctla4疗法的抗性中发挥关键作用。ido抑制剂增强动物中不同类型肿瘤中抗pd1、抗pd-l1、抗ctla4疗法的作用。对茜草(y1830、y9、n9)的不同制品在500μg/ml下的ido抑制活性进行了测试。提取物在体外试验中显示出对ido活性的约50%的抑制
作用(图13)。比较了y1830的不同乙醇洗脱对ar活性和ido活性的抑制轮廓(图14)。对于ido,y1830的30%etoh和50%etoh洗脱显示出实质的抑制作用。对于ar,30%etoh洗脱无活性,而50%etoh和75%etoh洗脱显示了抑制作用。30%etoh具有针对ido的选择性活性,这表明在30%etoh的级分中存在,而在50%etoh和75%etoh洗脱中不存在的至少一种化合物负责该活性。发现对于30%etoh级分,在26分钟时mw为366.04的质量峰是独特的(图14)。
[0230]
实施例7:y1830和rga(或包含rga的级分)抑制裸鼠中22rv1肿瘤生长。
[0231]
将22rv1细胞(恩杂鲁胺耐药性前列腺癌细胞)皮下植入雄性裸鼠中。当肿瘤达到5mm
×
5mm时,将y1830水提取物(500mg/kg,bid,po)和rga(或包含rga的级分)以y1830的当量剂量用于治疗动物,持续11天。如图15a中所示,从第2天到第11天,y1830显示出对22rv1肿瘤生长的显著抑制(p<0.05)。从第2天到第6天,rga(或包含rga的级分)显示出对22rv1肿瘤生长的显著抑制(p<0.05)(图15a)。两种处理均未引起动物体重减轻,这意味着对动物没有显著的总体毒性(图15b)。总之,y1830比包括rga的级分具有更强的抗22rv1肿瘤生长的抗肿瘤活性。因此,可以进一步得出结论,除rga中含有y1830总提取物的级分中的分子以外的化合物也可能具有抗肿瘤活性或防止肿瘤发展为耐药性。
[0232]
其他实施方式
[0233]
本文对变量的任何定义中的要素列表的列举包括将该变量定义为所列要素的任何单个要素或组合(或子组合)。本文中的实施方式的叙述包括该实施方式作为任何单个实施方式或与任何其他实施方式或其部分组合。
[0234]
本文引用的每个专利、专利申请和出版物的公开内容通过引用以其全部内容并入本文。尽管已经参考具体的实施方式公开了本发明,但是显然,本领域的普通技术人员可以设计出本发明的其他实施方式和变型而不脱离本发明的真实精神和范围。所附权利要求书旨在被解释为包括所有这样的实施方式和等同变型。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1