视网膜和/或光感受相关症状的改善或预防用药物、以及改善或预防视网膜和/或光感受相关症状的物质的筛选方法
1.本发明涉及视网膜和/或光感受相关症状的改善或预防用药物、以及改善或预防视网膜和/或光感受相关症状的物质的筛选方法。
背景技术:
2.视网膜是感受来自外界的光信息的中枢神经组织,可以说人从外界获取的信息中有八成以上是通过视觉获得的。作为迄今为止仍没有治疗方法的代表性的视觉障碍的原发病,可列举出视网膜变性疾病。视网膜变性的特征在于视细胞脱落导致的不可逆的视觉功能丧失,作为其原发病的视网膜色素变性在我国位于后天失明原因的第三位、黄斑变性(萎缩性)位于第四位,均占据前位,出于大量的患者数及视觉障碍的严重性,希望开发出预防方法或治疗方法。在全世界中视网膜色素变性或老年性黄斑变性也在失明原因中占据前位。这样的视网膜变性疾病的病理进程机制包括遗传、衰老、环境等多种因素,但具有视觉细胞死亡这一共通表现。认为长期暴露在光下,会引发代谢废物或细胞应激的积蓄,从而引起视细胞或视网膜色素上皮的衰老或细胞死亡等,导致包括老年性黄斑变性症或视网膜色素变性的视网膜变性疾病的发病或恶化。该现象作为光损伤而为人所知,尤其最近因电脑显示器等发出的蓝光导致的光损伤受到关注。从保护视网膜、抑制变性进程的角度出发,减弱因长期暴露在光下导致的光损伤是非常重要的。
3.本申请的发明人鉴定出主要在视网膜上表达的泛素化酶,并从该酶敲除小鼠的分析中新发现了该酶调控视网膜视细胞的明暗适应(光应答敏感度)(专利文献1)。视细胞中的明暗适应的分子机制基本尚未解明,但如果可通过视网膜泛素化酶的功能分析,解明视细胞中的蛋白质泛素化介导的明暗适应调节的新的分子机制,则可期待基于全新的分子机理来开发视网膜色素变性和老年性黄斑变性进程的抑制药等。现有技术文献专利文献
4.专利文献1:国际公开第wo2018/169090号
技术实现要素:
本发明要解决的技术问题
5.本发明的技术问题在于提供一种视网膜和/或光感受相关症状的改善或预防用药物。此外,本发明的技术问题在于提供一种改善或预防视网膜和/或光感受相关症状的物质的筛选方法。进一步,本发明的技术问题在于提供一种光暴露诱导视网膜变性抑制剂及视网膜保护剂。解决技术问题的技术手段
6.为了解决上述技术问题,本发明包括以下各发明。
1.一种视网膜和/或光感受相关症状的改善或预防用药物,其含有保持或促进
unc119的磷酸化状态的物质作为有效成分。
2.根据所述[1]所述的药物,其中,保持或促进unc119的磷酸化状态的物质为钙调神经磷酸酶抑制剂或酪蛋白激酶2激活剂。
3.根据所述[2]所述的药物,其中,钙调神经磷酸酶抑制剂为环孢菌素或他克莫司。
4.根据所述[3]所述的药物,其中,视网膜和/或光感受相关症状为选自由老年性黄斑变性、视网膜色素变性、莱伯先天性黑内障、斯特格氏病(stargardt disease)、视锥视杆细胞营养不良、糖尿病性视网膜病变、黄斑水肿、视网膜缺血、视网膜动脉阻塞、视网膜静脉阻塞、光敏性癫痫发作、光敏性癫痫、精神障碍、日光性视网膜病变、视疲劳、视网膜功能退化、睡眠障碍、偏头痛及光损伤组成的组中的至少一种疾病。
5.根据所述[4]所述的药物,其中,视网膜和/或光感受相关症状为选自由老年性黄斑变性、视网膜色素变性、莱伯先天性黑内障、斯特格氏病、视锥视杆细胞营养不良、糖尿病性视网膜病变、黄斑水肿、视网膜缺血、视网膜动脉阻塞、视网膜静脉阻塞、日光性视网膜病变、视疲劳、视网膜功能退化及光损伤组成的组中的至少一种疾病。
6.一种改善或预防视网膜和/或光感受相关症状的物质的筛选方法,其包括选择抑制钙调神经磷酸酶的物质的工序。
[0007]
根据所述[6]所述的筛选方法,其包括:使钙调神经磷酸酶、钙调蛋白、unc119、受试物质接触的工序;确认unc119的磷酸化状态的工序;及选择使unc119的磷酸化状态与未接触受试物质时的unc119的磷酸化状态相比得以增强的受试物质的工序。
[0008]
根据所述[7]所述的筛选方法,其中,使钙调神经磷酸酶、钙调蛋白、unc119、受试物质接触的工序为使受试物质与表达钙调神经磷酸酶、钙调蛋白和unc119的细胞接触。
[0009]
根据所述[6]所述的筛选方法,其包括:使钙调神经磷酸酶、钙调蛋白、unc119、受试物质接触的工序;确认钙调神经磷酸酶与unc119相互作用的工序;及选择使钙调神经磷酸酶与unc119的相互作用与未接触受试物质时的两者的相互作用相比得以减弱的受试物质的工序。
[0010]
一种改善或预防视网膜和/或光感受相关症状的物质的筛选方法,其包括选择激活酪蛋白激酶2的物质的工序。
[0011]
根据所述[10]所述的筛选方法,其包括:在atp存在下使酪蛋白激酶2、unc119、受试物质接触的工序;确认unc119的磷酸化状态的工序;及选择使unc119的磷酸化状态与未接触受试物质时的unc119的磷酸化状态相比得以增强的受试物质的工序。
[0012]
根据所述[11]所述的筛选方法,其中,在atp存在下使酪蛋白激酶2、unc119、受试物质接触的工序为在atp存在下使受试物质与表达酪蛋白激酶2和unc119的细胞接触的工序。
[0013]
一种视网膜变性抑制剂,其含有保持或促进unc119的磷酸化状态的物质作为有效成分。
[0014]
根据所述[13]所述的视网膜变性抑制剂,其中,视网膜变性伴有选自光暴露导致的视锥细胞的结构破坏、视杆细胞的结构破坏、及视细胞层厚度减少中的至少一种。
[0015]
一种视网膜保护剂,其含有保持或促进unc119的磷酸化状态的物质作为有效成分。发明效果
[0007]
根据本发明能够提供一种视网膜和/或光感受相关症状的改善或预防用药物。由于可将已在临床使用的钙调神经磷酸酶抑制剂用作有效成分,因此可提供安全性高的药。此外,通过本发明的筛选方法,能够获得有助于改善或预防视网膜和/或光感受相关症状的物质,进而能够提供一种新型的视网膜和/或光感受相关症状的改善或预防用药物。并且,本发明能够提供一种光暴露诱导视网膜变性抑制剂及视网膜保护剂。
附图说明
[0008]
图1为示出通过免疫荧光染色观察给药他克莫司且诱导光损伤的小鼠的视网膜中的视杆细胞的外节的结果的图。图2为示出通过免疫荧光染色观察给药他克莫司且诱导光损伤的小鼠的视网膜中的视锥细胞的结果的图。图3为示出测定给药他克莫司且诱导光损伤的小鼠的视网膜的视细胞层的厚度的结果的图。图4为示出通过免疫荧光染色观察给药环孢菌素且诱导光损伤的小鼠的视网膜中的视杆细胞的外节的结果的图。图5为出通过免疫荧光染色观察给药环孢菌素且诱导光损伤的小鼠的视网膜中的视锥细胞的结果的图。图6为示出测定给药环孢菌素且诱导光损伤的小鼠的视网膜的视细胞层的厚度的结果的图。图7为示出通过体外激酶测定确认酪蛋白激酶2引起的unc119磷酸化的结果的图。
具体实施方式
[0009]
本申请的发明人鉴定出主要在视网膜中表达的泛素化酶klhl18,并从klhl18敲除小鼠的分析中发现了klhl18调控视网膜视细胞的明暗适应(光应答敏感度)(专利文献1)。并且,本申请的发明人发现klhl18的靶蛋白为unc119,并发现了可通过靶蛋白的磷酸化及去磷酸化调控靶蛋白的分解。进一步,鉴定出催化unc119的磷酸化的酶为酪蛋白激酶2(casein kinase 2,以下也记为“ck2”),催化去磷酸化的酶为钙调神经磷酸酶(calcineurin)。
[0010]
[药物]本发明提供含有保持或促进unc119的磷酸化状态的物质作为有效成分的视网膜和/或光感受相关症状的改善或预防用药物。另外,在本发明中,“症状”也包括疾病等。此外,在本发明中,“改善”也包括治疗等,其改善的程度没有特别限定,也包括症状的缓解或治愈等。“预防”的程度没有特别限定,也用于指阻止发病、抑制进程等。
[0011]
保持或促进unc119的磷酸化状态的物质,可以为抑制磷酸化unc119的去磷酸化的物质,也可以为促进unc119的磷酸化的物质。由于催化unc119的去磷酸化的酶为钙调神经磷酸酶,因此抑制磷酸化unc119的去磷酸化的物质可以为钙调神经磷酸酶抑制剂。作为钙调神经磷酸酶抑制剂,可适当地使用公知的钙调神经磷酸酶抑制剂。公知的钙调神经磷酸酶抑制剂可以为环孢菌素或他克莫司。此外,由于催化unc119的磷酸化的酶为ck2,因此促进unc119的磷酸化的物质可以为ck2激活剂。
[0012]
环孢菌素(ciclosporin)作为免疫抑制剂的有效成分而广为人知,在日本也被批准为医疗用药品,并列于nhi药价目录(nhi price listing)中。环孢菌素也被称为环孢素(cyclosporin)、环孢菌素a、环孢素a、csa等。环孢菌素是日本药典收录药品。日本药典中记载如下。
[0013]
通用名称:环孢菌素(ciclosporin),别名:环孢素a化学名称:环[
‑
[(2s,3r,4r,6e)
‑3‑
羟基
‑4‑
甲基
‑2‑
甲氨基
‑6‑
辛烯酰]
‑
l
‑2‑
氨基丁酰
‑
n
‑
甲基甘氨酰
‑
n
‑
甲基
‑
l
‑
亮氨酰
‑
l
‑
缬氨酰
‑
n
‑
甲基
‑
l
‑
亮氨酰
‑
l
‑
丙氨酰
‑
d
‑
丙氨酰
‑
n
‑
甲基
‑
l
‑
亮氨酰
‑
n
‑
甲基
‑
l
‑
亮氨酰
‑
n
‑
甲基
‑
l
‑
缬氨酰]分子式:c
62
h
111
n
11
o
12
分子量:1202.61结构式:
[0014]
[化学式1]
[0015]
他克莫司(tacrolimus)作为免疫抑制剂的有效成分而广为人知,在日本也被批准为医疗用药品,并列于nhi药价目录中。他克莫司也被称为fk506。日本药典中收录为他克莫司水合物,本发明中使用的他克莫司也可以为他克莫司水合物。日本药典中记载如下。
[0016]
通用名称:他克莫司水合物(tacrolimus hydrate)化学名称:(3s,4r,5s,8r,9e,12s,14s,15r,16s,18r,19r,26as)
‑
5,19
‑
二羟基
‑3‑
{(1e)
‑2‑
[(1r,3r,4r)
‑4‑
羟基
‑3‑
甲氧基环己基]
‑1‑
甲基乙烯基}
‑
14,16
‑
二甲氧基
‑
4,10,12,18
‑
四甲基
‑8‑
(2
‑
丙烯
‑1‑
基)
‑
15,19
‑
环氧
‑
5,6,8,11,12,13,14,15,16,17,18,19,24,25,26,26十六氢
‑
3h
‑
吡啶并[2,1
‑
c][1,4]氧杂氮杂环二十三烷
‑
1,7,20,21(4h,23h)
‑
四酮一水合物分子式:c
44
h
69
no
12
·
h2o分子量:822.03
[0017]
[化学式2]
[0018]
视网膜和/或光感受相关症状,可以为在视网膜中表现的症状,也可以为在除视网膜以外的器官或组织中表现的症状。在视网膜中表现的症状,可以为起因于视网膜并在视网膜中表现的症状,也可以为起因于除视网膜以外的器官或组织并在视网膜中表现的症状。在除视网膜以外的器官或组织中表现的症状,仅限于起因于视网膜的症状。起因于视网膜的症状,例如可以为日常生活中接收的光刺激或光胁迫(light stress)导致的症状,也可以为暴露于强光导致的症状。
[0019]
作为视网膜和/或光感受相关症状,可列举出老年性黄斑变性、视网膜色素变性、莱伯先天性黑内障、斯特格氏病(青少年性黄斑变性)、视锥视杆细胞营养不良、糖尿病性视网膜病变、黄斑水肿、视网膜缺血、视网膜动脉阻塞、视网膜静脉阻塞、光敏性癫痫发作、光敏性癫痫、精神障碍、日光性视网膜病变、视疲劳、视网膜功能退化(例如,衰老导致的退化等)、睡眠障碍、偏头痛及光损伤(例如,由在户外明亮处的活动、运动、登山、电脑显示器等发出的蓝光等导致的光损伤)、伴有超敏反应、视觉失认症的精神障碍(例如,抑郁症、抑郁状态、双相障碍(躁郁症)、自闭症、精神发育障碍、精神分裂症等)等。作为在视网膜中表现的症状,可列举出老年性黄斑变性、视网膜色素变性、莱伯先天性黑内障、斯特格氏病、视锥视杆细胞营养不良、糖尿病性视网膜病变、黄斑水肿、视网膜缺血、视网膜动脉阻塞、视网膜静脉阻塞、日光性视网膜病变、视疲劳、视网膜功能退化及光损伤等。
[0020]
本发明的视网膜和/或光感受相关症状的改善或预防用药物,也可以称为视网膜保护用药物、视网膜变性抑制用药物、视网膜老化抑制用药物、超敏反应的改善或抑制用药物、光诱导性疾病的改善或抑制用药物、光诱导性病变的改善或预防用药物。
[0021]
本发明的药物,可以在上述有效成分中适当地掺合药学上允许的载体、以及添加剂而制成制剂。具体而言,可以制成片剂、包衣片剂、丸剂、散剂、颗粒剂、胶囊剂、液体制剂、混悬剂、乳剂等口服制剂;注射剂、输液、栓剂、软膏、贴剂等非口服制剂。载体或添加剂的掺合比例可以根据医药领域通常采用的范围而适当设定。可掺合的载体或添加剂没有特别限制,例如可列举出水、生理盐水、其他水性溶剂、水性或油性基质等各种载体;赋形剂、粘合剂、ph调节剂、崩解剂、吸收促进剂、润滑剂、着色剂、矫味剂、香料等各种添加剂。
[0022]
作为赋形剂,例如可列举出乳糖、白糖、d
‑
甘露醇、淀粉、结晶纤维素、轻质无水硅酸;作为粘合剂,例如可列举出结晶纤维素、白糖、d
‑
甘露醇、糊精、羟丙基纤维素、羟丙基甲基纤维素、聚乙烯吡咯烷酮等高分子化合物等;作为润滑剂,例如可列举出硬脂酸镁、硬脂酸钙、滑石粉、胶体二氧化硅等;作为崩解剂,例如可列举出淀粉、羧甲基纤维素、羧甲基纤
维素钙、交联羧甲基纤维素钠、羧甲基淀粉钠等;作为湿润剂,可列举出甘油、丁二醇、丙二醇、山梨糖醇、三乙酸甘油酯等;但并不限定于此。也可以根据需要用包衣剂(白糖、明胶、羟丙基纤维素、羟丙基甲基纤维素苯二甲酸酯等)进行包衣,此外也可以以两层以上进行包衣。
[0023]
注射剂的情况下,将有效成分溶解或分散在生理盐水等水性基质或允许注射用的油性基质中,制成静脉给药用、肌肉给药用或皮下给药用的注射剂即可。可以根据需要添加缓冲剂、ph调节剂、等渗剂、助溶剂、悬浮剂、稳定剂等添加剂。
[0024]
注射剂的情况下,作为水性基质,例如可列举出生理盐水、注射用水、林格氏液等输液。作为油性基质,例如可列举出丙二醇、聚乙二醇、芝麻油、大豆油、玉米油、花生油、棉籽油、橄榄油、丙二醇脂肪酸酯等。作为缓冲剂,例如可列举出磷酸盐、乙酸盐、碳酸盐、柠檬酸盐、硼酸盐、谷氨酸盐、ε
‑
氨基己酸盐、tris缓冲液等缓冲液等。作为ph调节剂,例如可列举出盐酸、磷酸、硫酸、碳酸等无机酸;乙酸、酒石酸、乳酸、柠檬酸、琥珀酸等有机酸;氢氧化钠等无机碱;柠檬酸钠、酒石酸钠等有机碱。作为等渗剂,例如可列举出氯化钠等无机盐类;d
‑
甘露醇、山梨糖醇、木糖醇等糖醇;果糖、葡萄糖、半乳糖、核糖、木糖、甘露糖、麦芽三糖、麦芽四糖等糖类;甘氨酸、精氨酸等氨基酸。作为助溶剂,例如可列举出聚乙二醇、丙二醇、d
‑
甘露醇、苯甲酸苄酯、乙醇、三氨基甲烷、胆固醇、三乙醇胺、碳酸钠、柠檬酸钠、卵磷脂、或聚山梨醇酯80等非离子表面活性剂。作为悬浮剂,例如可列举出硬脂基三乙醇胺、十二烷基硫酸钠、十二烷基氨基丙酸、卵磷脂、单硬脂酸甘油酯等表面活性剂、或聚乙烯醇、聚乙烯吡咯烷酮、羧甲基纤维素钠、甲基纤维素、羟甲基纤维素等。作为稳定剂,例如可列举出白蛋白、球蛋白、明胶、山梨糖醇、乙二醇、丙二醇、抗坏血酸等。
[0025]
作为本发明的药物的有效成分的环孢菌素及他克莫司已在临床上使用多年,因此本发明的药物可以对人或其他哺乳动物(例如,大鼠、小鼠、兔、羊、猪、牛、猫、狗、猴子等)安全地给药。
[0026]
将环孢菌素或他克莫司用作有效成分时,本发明的药物的每日给药量,可以根据临床使用的环孢菌素或他克莫司的每日给药量而适当设定。
[0027]
[视网膜变性抑制剂、视网膜保护剂]本发明提供含有保持或促进unc119的磷酸化状态的物质作为有效成分的视网膜变性抑制剂。此外,本发明提供含有保持或促进unc119的磷酸化状态的物质作为有效成分的视网膜保护剂。本申请的发明人对给药了他克莫司或环孢菌素的小鼠进行光损伤诱导,制作视网膜冰冻切片并用激光扫描共聚焦显微镜观察视网膜视细胞层,结果确认到视锥细胞及视杆细胞的结构得以保持,并未被破坏,视细胞层的厚度也得以保持,并未减少(参考实施例1)。因此,本发明的视网膜变性抑制剂及视网膜保护剂对治疗或预防光损伤是有效的。
[0028]
本发明的视网膜变性抑制剂及视网膜保护剂能够以上述药物的实施方案中说明的物质作为有效成分。此外,本发明的视网膜变性抑制剂及视网膜保护剂能够以上述药物的实施方案中说明的方式而制备成各种剂型,并能够对人或其他哺乳动物(例如,大鼠、小鼠、兔、羊、猪、牛、猫、狗、猴子等)安全地给药。
[0029]
[筛选方法]本发明提供一种改善或预防视网膜和/或光感受相关症状的物质的筛选方法。本
发明的筛选方法可以是选择抑制钙调神经磷酸酶的物质的方法,也可以是选择激活ck2的物质的方法。对于抑制钙调神经磷酸酶的物质,可以为对抑制钙调神经磷酸酶的底物的去磷酸化的物质进行选择的方法,对于激活ck2的物质,可以为对促进ck2的底物的磷酸化的物质进行选择的方法。
[0030]
在本发明的筛选方法中,视网膜和/或光感受相关症状,可以为在视网膜中表现的症状,也可以为在除视网膜以外的器官或组织中表现的症状。在视网膜中表现的症状,可以为起因于视网膜并在视网膜中表现的症状,也可以为起因于除视网膜以外的器官或组织并在视网膜中表现的症状。在除视网膜以外的器官或组织中表现的症状,仅限于起因于视网膜的症状。作为视网膜和/或光感受相关症状的具体实例,可以列举出上述例示出的各种症状。
[0031]
供于本发明的筛选方法的受试物质没有特别限定,可以为核酸、肽、蛋白质、非肽性化合物、合成化合物、发酵产物、细胞提取液、细胞培养上清液、植物提取液、哺乳动物的组织提取液、血浆等。受试物质可以是新型的物质,也可以是公知的物质。这些受试物质也可以形成盐。作为受试物质的盐,优选生理学上允许的酸或碱的盐。
[0032]
本发明的筛选方法可以包括选择抑制钙调神经磷酸酶的物质的工序。当抑制钙调神经磷酸酶的物质为抑制钙调神经磷酸酶的底物的去磷酸化的物质时,本发明的筛选方法,例如可以为包括下述工序的方法:使钙调神经磷酸酶、钙调蛋白(calmodulin)、底物、受试物质接触的工序;确认底物的磷酸化状态的工序;及选择使底物的磷酸化状态与未接触受试物质时的底物的磷酸化状态相比得以增强的受试物质的工序。此外,例如也可以为包括下述工序的方法:使钙调神经磷酸酶、钙调蛋白、底物、受试物质接触的工序;确认钙调神经磷酸酶与底物的相互作用的工序;及选择使钙调神经磷酸酶与底物的相互作用与未接触受试物质时的两者的相互作用相比得以减弱的受试物质的工序。
[0033]
钙调神经磷酸酶的底物为选自公知的钙调神经磷酸酶的底物即可。作为钙调神经磷酸酶的底物,例如可列举出nfatc1(活化t细胞核因子1,nuclear factor of activated t cells 1)、dnm1(发动蛋白1,dynamin 1)等,但并不限定于此。优选作为主要在视网膜中表达的泛素化酶klhl18的靶蛋白的unc119。以下,对本发明的筛选方法中钙调神经磷酸酶的底物为unc119的情况进行详细说明,但对于使用除unc119以外的底物的情况,也能够以相同的方式实施。
[0034]
本发明的筛选方法可以为包括下述工序的方法:使钙调神经磷酸酶、钙调蛋白、unc119、受试物质接触的工序;确认unc119的磷酸化状态的工序;选择使unc119的磷酸化状态与未接触受试物质时的unc119的磷酸化状态相比得以增强的受试物质的工序。使钙调磷酸酶、钙调蛋白、unc119、受试物质接触的工序可以为,制备含有钙调神经磷酸酶、钙调蛋白、unc119的溶液,并向该溶液中添加受试物质的方法;也可以为培养表达钙调神经磷酸酶、钙调蛋白、unc119的细胞,并向该细胞培养液中添加受试物质的方法。
[0035]
本发明的筛选方法中使用的钙调神经磷酸酶可以为来自任何生物的钙调神经磷酸酶,也可以为哺乳动物的钙调神经磷酸酶。作为哺乳动物,可列举出人、黑猩猩、猴子、狗、牛、小鼠、大鼠、豚鼠等,优选为人的钙调神经磷酸酶。钙调神经磷酸酶,可以使用作为试剂而市售的重组钙调神经磷酸酶、或市售的试剂盒(例如,enzo life sciences,inc.制造的“钙调神经磷酸酶活性检测试剂盒”)中所含有的重组钙调神经磷酸酶,也可以利用公知的
基因重组技术制备重组钙调神经磷酸酶而进行使用。
[0036]
钙调神经磷酸酶(也称为蛋白磷酸酶2b(pp2b)、蛋白磷酸酶3(ppp3))为由作为催化亚基的钙调神经磷酸酶a和作为调节亚基的钙调神经磷酸酶b构成的异源二聚体,通过与钙调蛋白结合而激活。因此,能够将编码钙调神经磷酸酶a的基因和编码钙调神经磷酸酶b的基因适当导入宿主细胞,从而制作钙调神经磷酸酶表达细胞。对所制得的钙调神经磷酸酶表达细胞进行培养,进而能够使用公知的方法(例如,亲和柱)从其培养上清液或细胞提取物中获得重组钙调神经磷酸酶。
[0037]
将人的钙调神经磷酸酶a及钙调神经磷酸酶b的氨基酸序列以及对其进行编码的基因的碱基序列的登录号(accession number)示于表1中。通过将选自表1中记载的ppp3ca、ppp3cb、ppp3cc中的任意一个和选自ppp3r1、ppp3r2中的任意一个导入宿主细胞,可制作钙调神经磷酸酶表达细胞。除人以外的生物的钙调神经磷酸酶a及钙调神经磷酸酶b的碱基序列信息以及氨基酸序列信息可以从公知的数据库(ddbj/genbank/embl等)中获得。
[0038]
[表1]
[0039]
本发明的筛选方法中使用的钙调蛋白可以为来自任何生物的钙调蛋白,也可以为哺乳动物的钙调蛋白。作为哺乳动物,可列举出人、黑猩猩、猴子、狗、牛、小鼠、大鼠、豚鼠等,优选为人的钙调蛋白。钙调蛋白可以使用作为试剂而市售的重组钙调蛋白、或市售的试剂盒(例如,enzo life sciences,inc.制造的“钙调神经磷酸酶活性检测试剂盒”)中所含有的钙调蛋白,也可以利用公知的基因重组技术制备钙调蛋白而进行使用。
[0040]
人的钙调蛋白具有钙调蛋白1、钙调蛋白2及钙调蛋白3这三个种类,通过将编码其中任一种蛋白的基因导入宿主细胞,能够制备钙调蛋白表达细胞。对钙调蛋白表达细胞进行培养,能够使用公知的方法(例如,亲和柱)从其培养上清液或细胞提取物中获得重组钙调蛋白。将人的钙调蛋白1、钙调蛋白2及钙调蛋白3的氨基酸序列以及对其进行编码的基因的碱基序列的登录号示于表2中。除人以外的生物的钙调蛋白的碱基序列信息以及氨基酸序列信息可以从公知的数据库(ddbj/genbank/embl等)中获得。
[0041]
[表2] 基因名称碱基序列氨基酸序列钙调蛋白1calm1nm_006888np_008819钙调蛋白2calm2nm_001743np_001734钙调蛋白3calm3nm_005184np_005175
[0042]
本发明的筛选方法中使用的unc119可以为来自任何生物的unc119,也可以为来自哺乳动物的unc119。作为哺乳动物,可以列举出人、黑猩猩、猴子、狗、牛、小鼠、大鼠、豚鼠等,优选为人的unc119。对于unc119,利用公知的基因重组技术制备重组unc119而进行使用
即可。unc119表达细胞例如可以通过将编码unc119的基因导入宿主细胞而制备,并可通过对所制得的unc119表达细胞进行培养,利用公知的方法(例如,亲和柱)从其培养上清液或细胞提取物中获得重组unc119。
[0043]
人unc119的氨基酸序列及对其进行编码的基因的碱基序列的登录号分别为nm_005148及np_005139。除人以外的生物的unc119的碱基序列信息以及氨基酸序列信息可以从公知的数据库(ddbj/genbank/em bl等)中获得。
[0044]
本发明的筛选方法中使用的表达钙调神经磷酸酶、钙调蛋白、unc119的细胞,可以为表达内源性钙调神经磷酸酶、钙调蛋白、unc119的细胞;也可以为表达源自所导入的基因的重组钙调神经磷酸酶、重组钙调蛋白、重组unc119的细胞;还可以为表达组合了内源性蛋白质和重组蛋白质的钙调神经磷酸酶、钙调蛋白、unc119的细胞。优选为表达重组钙调神经磷酸酶、重组钙调蛋白、重组unc119的细胞。该细胞可通过将编码钙调神经磷酸酶a的基因、编码钙调神经磷酸酶b的基因、编码钙调蛋白的基因、编码unc119的基因共转染至宿主细胞中而制备。各基因的碱基序列信息如上所述。宿主细胞只要为能够表达所导入的各基因产物的细胞,则没有特别限定。例如,可列举出hek293t细胞、neuro2a细胞、nih3t3细胞等。这些细胞也可适宜地用作上述的重组钙调神经磷酸酶表达细胞、重组钙调蛋白表达细胞、重组unc119表达细胞中使用的宿主细胞。
[0045]
在使钙调神经磷酸酶、钙调蛋白、unc119、受试物质接触的工序中,通过制备含有钙调神经磷酸酶、钙调蛋白、unc119的溶液并向该溶液中添加受试物质的方法进行时,向溶液中添加的钙调神经磷酸酶、钙调蛋白及unc119的量没有特别限定,以摩尔比计可以为约1:1:1。只要能够在后续工序中确认unc119的磷酸化状态,则受试物质的添加量没有特别限定。可以设定浓度范围以多种浓度添加受试物质。
[0046]
所使用的溶液没有特别限定,可以适当地使用可用于蛋白质的磷酸化反应的公知的缓冲液。例如,可以列举出含有1mm cacl2、100mm nacl、1mg/ml bsa、0.025%np
‑
40、1mm dtt的50mm tris
‑
hcl(ph7.5)缓冲液。溶液的温度及接触时间,只要为钙调神经磷酸酶和钙调蛋白形成复合体并能够催化unc119的去磷酸化的条件即可。例如,溶液温度可以为37℃、接触时间可以为30分钟。
[0047]
在使钙调神经磷酸酶、钙调蛋白、unc119、受试物质接触的工序中,通过对表达钙调神经磷酸酶、钙调蛋白、unc119的细胞进行培养并向其培养液中添加受试物质的方法进行时,受试物质的添加量只要为不会显著抑制细胞的增殖及重组蛋白质的表达的量即可。可以设定浓度范围以多种浓度添加受试物质。受试物质的添加时间没有特别限定,可以为约0.5小时~约48小时。
[0048]
当使用表达钙调神经磷酸酶、钙调蛋白、unc119的细胞时,制备用于测定unc119的磷酸化量的细胞裂解液,供于后续工序。细胞裂解液的制备方法没有特别限定,从公知的方法中适当选择即可。具体而言,可以用以下的方法制备。去除培养液,用tbs(tris缓冲盐溶液:20mm tris
‑
hcl ph7.4,150mm nacl)将细胞洗涤两次,使用裂解缓冲液(20mm tris
‑
hcl ph7.4,150mm nacl,1%np
‑
40,磷酸酶抑制剂混合物(roche公司)),进行吹打使其溶解,在冰上静置10分钟。离心分离(14,000rpm,半径5.4cm,10分钟,4℃)后,回收上清液,加入等量的2
×
样本缓冲液(0.1m tris
‑
hcl ph6.8,1%sds,5%β巯基乙醇,10%甘油,0.02%bpb),在室温下静置30分钟。
[0049]
在确认unc119的磷酸化状态的工序中,利用公知的方法测定unc119的磷酸化量即可。例如,可以为可分离磷酸化/非磷酸化形态的电泳法、向溶液中添加磷酸被标记的atp的方法、使用可识别磷酸化的抗体的方法等。具体而言,可以使用phos
‑
tag sds
‑
page(产品名称,fujifilm wako pure chemical corporation)、
32
p标记atp(perkinelmer co.,ltd.,其他)、抗磷酸化丝氨酸抗体(abcam公司,产品编号:ab9332)等。
[0050]
选择使unc119的磷酸化状态与未接触受试物质时的unc119的磷酸化状态相比得以增强的受试物质的工序中,对未接触受试物质的样本(对照组)的unc119的磷酸化量与接触了受试物质的样本(受试物质组)的unc119的磷酸化量进行比较,选择磷酸化量增加的受试物质即可。受试物质使unc119的磷酸化量增加的程度没有特别限定,例如可以选择与未接触受试物质的样本相比,增加120%以上、130%以上、140%以上、150%以上、170%以上、180%以上、190%以上、200%以上的受试物质。
[0051]
本发明的筛选方法可以为包括下述工序的方法:使钙调神经磷酸酶、钙调蛋白、unc119、受试物质接触的工序;确认钙调神经磷酸酶与unc119的相互作用的工序;及选择使钙调神经磷酸酶与unc119的相互作用与未接触受试物质时的两者的相互作用相比得以减弱的受试物质的工序。
[0052]
在本实施方式中,对于使钙调神经磷酸酶、钙调蛋白、unc119、受试物质接触的工序,可以通过制备含有钙调神经磷酸酶、钙调蛋白、unc119的溶液并向该溶液中添加受试物质的方法进行,也可以通过将unc119固相化并向其中添加钙调神经磷酸酶、钙调蛋白、受试物质的方法进行。钙调神经磷酸酶、钙调蛋白及unc119的用量、测试物质的添加量、溶液、溶液温度、接触时间如上所述。
[0053]
在确认钙调神经磷酸酶与unc119的相互作用的工序中,利用公知的方法测定钙调神经磷酸酶与unc119的相互作用即可。具体而言,例如可以为fret(荧光共振能量转移:fluorescence resonance energy transfer)、alphascreen(扩增荧光近距离均相实验:amplified luminescence proximity homogeneous assay)、免疫沉淀法、酶联免疫吸附测定法(elisa法)等。
[0054]
选择使钙调神经磷酸酶与unc119的相互作用与未接触受试物质时的两者的相互作用相比得以减弱的受试物质的工序中,对未接触受试物质的样本(对照组)的unc119的磷酸化量与接触了受试物质的样本(受试物质组)的钙调神经磷酸酶与unc119的相互作用量进行比较,选择相互作用量减少的受试物质即可。对减弱钙调神经磷酸酶与unc119的相互作用量的程度没有特别限定,例如可以选择与未接触受试物质的样本相比,减少90%以下、80%以下、70%以下、60%以下、50%以下、40%以下、30%以下的受试物质。
[0055]
本发明的筛选方法可以包括选择激活ck2的物质的工序。当激活ck2的物质为促进ck2的底物的磷酸化的物质时,本发明的筛选方法例如可以为包括下述工序的方法:在atp存在下使ck2、底物、受试物质接触的工序;确认底物的磷酸化状态的工序;及选择使底物的磷酸化状态与未接触受试物质时的底物的磷酸化状态相比得以增强的受试物质的工序。
[0056]
ck2的底物从公知的ck2的底物中选择即可。作为ck2的底物,例如可列举出brd4(溴结构域蛋白4,bromodomain containing 4)、kbt bd8(kelch repeat and btb domain containing 8)等,但并不限定于此。优选作为主要在视网膜中表达的泛素化酶klhl18的靶蛋白的unc119。以下,对本发明的筛选方法中ck2的底物为unc119的情况进行详细说明,但
对于使用除unc119以外的底物的情况,也能够以相同的方式实施。
[0057]
本发明的筛选方法可以为包括下述工序的方法:在atp存在下使ck2、unc119、受试物质接触的工序;确认unc119的磷酸化状态的工序;及选择使unc119的磷酸化状态与未接触受试物质时的unc119的磷酸化状态相比得以增强的受试物质的工序。在atp存在下使ck2、unc119、受试物质接触的工序可以为制备含有ck2、unc119、atp的溶液并向该溶液中添加受试物质的方法;也可以为用含有atp的培养液对表达ck2、unc119的细胞进行培养并向该培养液添加受试物质的方法。
[0058]
对于本发明的筛选方法中使用的unc119,与上述相同,可以适宜地使用利用公知的基因重组技术制备的重组unc119。
[0059]
本发明的筛选方法中使用的ck2可以为来自任何生物的ck2,也可以为哺乳动物的ck2。作为哺乳动物,例如可列举出人、黑猩猩、猴子、狗、牛、小鼠、大鼠、豚鼠等,优选为人的ck2。对于ck2,可以使用作为试剂而市售的重组ck2,也可以利用公知的基因重组技术制备重组ck2而进行使用。
[0060]
ck2可以通过由作为催化亚基的阿尔法(α或α’)和作为调节亚基的贝塔(β)形成异源四聚体来表达活性。异源四聚体可以是ααββ、αα’ββ、α’α’ββ中的任意一种。因此,能够通过向宿主细胞中导入编码α的基因和编码β的基因这两种基因;或者导入编码α’的基因和编码β的基因这两种基因、或者导入编码α的基因、编码α’的基因及编码β的基因这三种基因,从而制备ck2表达细胞。可通过对制得的ck2表达细胞进行培养,利用公知的方法(例如,亲和柱)从其培养上清液或细胞提取物中获得重组ck2。
[0061]
将人的ck2阿尔法亚基(α)、阿尔法亚基(α’)及贝塔亚基(β)的氨基酸序列及对其进行编码的基因的碱基序列的登录号示于表3中。除人以外的生物的ck2的碱基序列信息及氨基酸序列信息可以从公知的数据库(ddbj/genbank/embl等)中获得。
[0062]
[表3]亚基基因名称碱基序列氨基酸序列阿尔法(α)csnk2a1nm_001895np_001886阿尔法(α’)csnk2a2nm_001896np_001887贝塔(β)csnk2bnm_001320np_001311
[0063]
本发明的筛选方法中使用的表达ck2、unc119的细胞可以为表达内源性ck2、unc119的细胞;也可以为表达源自所导入的基因的重组ck2、重组unc119的细胞;还可以为表达组合了内源性蛋白质和重组蛋白质的ck2、unc119的细胞。优选为表达重组ck2、重组unc119的细胞。该细胞可通过将编码ck2的基因、编码unc119的基因共转染至宿主细胞中而制备。具体而言,可通过共转染编码ck2阿尔法亚基(α)的基因、编码ck2贝塔亚基(β)的基因、编码unc119的基因,或者共转染编码ck2阿尔法亚基(α’)的基因、编码ck2贝塔亚基(β)的基因、编码unc119的基因,或者共转染编码ck2阿尔法亚基(α)的基因、编码ck2阿尔法亚基(α’)的基因、编码ck2贝塔亚基(β)的基因、编码unc119的基因而制备。可用作宿主细胞的细胞如上所述。
[0064]
在atp存在下使ck2、unc119、受试物质接触的工序中,通过制备含有ck2、unc119、atp的溶液并向该溶液中添加受试物质的方法进行时,向溶液中添加的ck2及unc119的量没有特别限定,以摩尔比计可以为约1∶1。atp的添加量没有特别限定,可以为10μm~1000μm。
只要能够在后续工序中确认unc119的磷酸化状态,则受试物质的添加量没有特别限定。可以设定浓度范围以多种浓度添加受试物质。
[0065]
所使用的溶液没有特别限定,可适当使用可用于蛋白质的磷酸化反应的公知的缓冲液。例如,可列举出添加了40μm的atp的“1
×
蛋白激酶用nebuffer”(neb公司)。溶液的温度及接触时间只要为ck2能够催化unc119的磷酸化的条件即可。例如,溶液温度可以为30℃、接触时间可以为30分钟。
[0066]
在atp存在下使ck2、unc119、受试物质接触的工序中,在通过用含有atp的培养液对表达ck2、unc119的细胞进行培养并向该培养液中添加受试物质的方法进行时,atp的添加量没有特别限定,可以为10μm~1000μm。受试物质的添加量只要为不会显著抑制细胞的增殖及重组蛋白质的表达的量即可。可以设定浓度范围以多种浓度添加受试物质。受试物质的添加时间没有特别限定,可以为约0.5小时~约48小时。
[0067]
使用表达ck2和unc119的细胞时,制备用于测定unc119的磷酸化量的细胞裂解液,供于后续工序。细胞裂解液的制备方法没有特别限定,从公知的方法中适当选择即可。具体而言,可以利用上述例示出的方法制备细胞裂解液。
[0068]
在确认unc119的磷酸化状态的工序中,利用公知的方法测定unc119的磷酸化量即可。例如,可以为可分离磷酸化/非磷酸化形态的电泳法、向溶液中添加磷酸被标记的atp的方法、使用可识别磷酸化的抗体的方法等。具体而言,可以使用phos
‑
tag sds
‑
page(产品名称,fujifilm wako pure chemical corporation)、
32
p标记atp(perkinelmer co.,ltd.,其他)、抗磷酸化丝氨酸抗体(abcam公司,产品编号:ab9332)等。
[0069]
选择使unc119的磷酸化状态与未接触受试物质时的unc119的磷酸化状态相比得以增强的受试物质的工序中,对未接触受试物质的样本(对照组)的unc119的磷酸化量与接触了受试物质的样本(受试物质组)的unc119的磷酸化量进行比较,选择磷酸化量增加的受试物质即可。受试物质使unc119的磷酸化量增加的程度没有特别限定,例如可以选择与未接触受试物质的样本相比,增加120%以上、130%以上、140%以上、150%以上、170%以上、180%以上、190%以上、200%以上的受试物质。
[0070]
本发明包含以下各发明。(a)一种视网膜和/或光感受相关症状的改善或预防方法,其包含以保持或促进unc119的磷酸化状态的物质的有效量对哺乳动物给药。(b)一种保持或促进unc119的磷酸化状态的物质,其用于改善或预防视网膜和/或光感受相关症状。(c)一种保持或促进unc119的磷酸化状态的物质在制备视网膜和/或光感受相关症状的改善或预防用药物中的应用。本发明(a)、(b)或(c)中,保持或促进unc119的磷酸化状态的物质可以为钙调神经磷酸酶抑制剂或酪蛋白激酶2激活剂,钙调神经磷酸酶抑制剂可以为环孢菌素或他克莫司。在本发明(a)、(b)或(c)中,视网膜和/或光感受相关症状为选自由老年性黄斑变性、视网膜色素变性、莱伯先天性黑内障、斯特格氏病、视锥视杆细胞营养不良、糖尿病性视网膜病变、黄斑水肿、视网膜缺血、视网膜动脉阻塞、视网膜静脉阻塞、光敏性癫痫发作、光敏性癫痫、精神障碍、日光性视网膜病变、视疲劳、视网膜功能退化、睡眠障碍、偏头痛及光损伤组成的组中的至少一种疾病。
实施例
[0071]
以下,通过实施例对本发明进行详细说明,但本发明并不限定于此。
[0072]
[实施例1:针对给药钙调神经活性抑制物质的小鼠的光损伤试验](1)光损伤试验方法将4周龄的balb/c小鼠(japan slc,inc.)在黑暗下饲养12小时,使其暗适应。自暗适应开始8小时后,在黑暗下于背部皮下注射他克莫司(fk506,abcam公司)(给药量10mg/kg)或环孢菌素(cyclosporine a,abcam公司)(给药量100mg/kg)。对对照组小鼠给药dmso。在暗适应结束前30分钟,在黑暗下用散瞳剂盐酸环喷托酯(santen pharmaceutical co.,ltd.)滴眼。接着,将小鼠放入周围的四个面和底面装有镜子的箱子中,由蓝色led灯照射蓝光。蓝色led灯的波长为约450nm,到达小鼠的光约为7000勒克斯。照射3小时蓝光后在普通的明亮环境(荧光灯照亮约30勒克斯的环境)中饲养9小时。以此为一个循环,重复6天。即,六天中每天进行给药和蓝光照射(3小时),诱导光损伤。
[0073]
(2)组织学分析(a)免疫荧光染色在最后一次照射蓝光的次日,对小鼠实施安乐死,摘取眼球。使用4%多聚甲醛/pbs(磷酸盐缓冲液)在室温下固定5分钟。用pbs洗涤固定后的眼球,使用oct冰冻切片包埋剂(sakura finetek japan co.,ltd.公司制造)包埋眼球。通过低温恒温器制备厚度为20μm的视网膜冰冻切片,并将其贴附在载玻片上,于室温下将冰冻切片干燥。将切片用pbs洗涤两次后,用封闭缓冲液(5%正常驴血清/0.1%tritonx
‑
100/pbs)在室温下封闭1小时。然后,于4℃与第一抗体反应整夜。将切片用pbs洗涤3次后,在室温下与第二抗体反应2小时。作为第一抗体,使用抗视紫红质抗体(视紫红质、兔多克隆、santa cruz biotechnology,inc.制造,1:500稀释)、抗s
‑
视蛋白抗体(s
‑
视蛋白(蓝锥视蛋白)、羊多克隆、santa cruz biotechnology,inc.制造,1:500稀释)及抗m
‑
视蛋白抗体(m
‑
视蛋白(绿锥视蛋白)、兔多克隆、millipore公司制造,1:500稀释),作为第二抗体,使用alexa flour 488标记抗体(thermo fisher scientific inc.制造,1:500稀释)及cy3标记抗体(jackson immunoresearch laboratories制造,1:500稀释)。二次抗体的反应结束后,用pbs洗涤三次,使用封固剂进行封固。此外,对所有样本均使用dapi进行细胞核染色。使用激光扫描共聚焦显微镜(lsm700,carl zeiss公司制造)获得所有的荧光图像。
[0074]
(b)视细胞层厚度的测量将以与上述相同的方式制得的小鼠视网膜切片用pbs洗涤两次,然后使用dapi进行细胞核染色,并测量与视神经不同距离的视细胞层的厚度。具体而言,用激光扫描共聚焦显微镜(lms700,carl zeiss公司制造)获得图像,使用图像分析软件metamorph(molecular devices公司)测量视细胞层的厚度。
[0075]
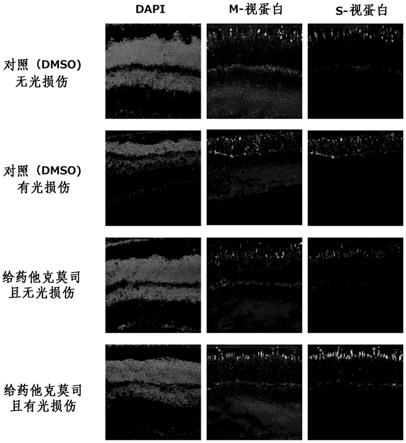
(3)给药他克莫斯的结果(a)免疫荧光染色将对给药他克莫司的小鼠的视网膜视细胞层进行观察的结果示于图1及图2中。图1为使用抗视紫红质抗体对视杆细胞外节进行染色的结果,图2为使用抗s
‑
视蛋白抗体及抗m
‑
视蛋白抗体对视锥细胞进行染色的结果。从图1中清晰地观察到,诱导光损伤的对照小鼠(给药dmso)的视杆细胞外节受到了损害,但给药他克莫司且诱导光损伤的小鼠以与未诱导
光损伤的对照小鼠以及给药他克莫司且未诱导光损伤的小鼠同等程度地保持了视杆细胞外节的结构。此外,从图2可以清晰地观察到,诱导光损伤的对照小鼠(给药dmso)的视锥细胞受到了损害,但给药他克莫司且诱导光损伤的小鼠以与未诱导光损伤的对照小鼠以及给药他克莫司且未诱导光损伤的小鼠同等程度地保持了视锥细胞的结构。
[0076]
(b)视细胞层厚度的测量将测定的给药他克莫司的小鼠的视网膜视细胞层厚度的结果示于图3中。从图3可以清晰地观察到,诱导光损伤的对照小鼠(给药dmso)的视细胞层的厚度明显变薄,但给药他克莫司且诱导光损伤的小鼠以与未诱导光损伤的对照小鼠以及给药他克莫司且未诱导光损伤的小鼠同等程度地保持了视细胞层的厚度。由这些结果可知,通过给药他克莫司,抑制了因光暴露导致的视细胞的变性,保持了视细胞的结构。
[0077]
(4)给药环孢菌素的结果(a)免疫荧光染色将对给药环孢菌素的小鼠的视网膜视细胞层进行观察的结果示于图4及图5中。图4为使用抗视紫红质抗体对视杆细胞外节进行染色的结果,图5为使用抗s
‑
视蛋白抗体及抗m
‑
视蛋白抗体对视锥细胞进行染色的结果。从图4中清晰地观察到,诱导光损伤的对照小鼠(给药dmso)的视杆细胞外节受到了损害,但给药环孢菌素且诱导光损伤的小鼠以与未诱导光损伤的对照小鼠以及给药环孢菌素且未诱导光损伤的小鼠同等程度地保持了视杆细胞外节的结构。此外,从图5可以清晰地观察到,诱导光损伤的对照小鼠(给药dmso)的视锥细胞受到了损害,但给药环孢菌素且诱导光损伤的小鼠以与未诱导光损伤的对照小鼠以及给药环孢菌素且未诱导光损伤的小鼠同等程度地保持了视锥细胞的结构。
[0078]
(b)视细胞层厚度的测量将测定的给药环孢菌素的小鼠的视网膜视细胞层厚度的结果示于图6中。从图6可以清晰地观察到,诱导光损伤的对照小鼠(给药dmso)的视细胞层的厚度明显变薄,但给药环孢菌素且诱导光损伤的小鼠以与未诱导光损伤的对照小鼠以及给药环孢菌素且未诱导光损伤的小鼠同等程度地保持了视细胞层的厚度。由这些结果可知,通过给药环孢菌素,抑制了光暴露导致的视细胞的变性,并保持了视细胞的结构。
[0079]
[实施例2:ck2引起的unc119的磷酸化](1)unc119表达质粒的制备为了制备表达在n端加了6
×
his(6
×
组氨酸)标签的unc119的质粒,通过pcr以从plasml d购入的人unc119克隆(hscd00330844)为模板对人unc119全长cdna片段进行扩增,并整合于pet
‑
28b载体(novagen)。
[0080]
(2)带6
×
his标签的unc119的表达和提纯用大肠杆菌(bl21(de3))表达带6
×
his标签的unc119蛋白质,并提纯。用lb培养基使导入了pet
‑
28b
‑
unc119的大肠杆菌增殖至od600nm为0.6,用1mm的iptg进行处理后在25℃下培养3小时30分钟,通过离心回收菌体。使用超声处理缓冲液(20mm tris
‑
hcl ph7.4,1mm edta,150mm nacl,1%tritonx
‑
100,1mm dtt,50mm咪唑,1mm pmsf,2μg/ml亮抑蛋白酶肽,5μg/ml抑蛋白酶多肽,3μg/ml胃蛋白酶抑制剂)溶解进行了集菌的大肠杆菌,然后进行
离心。于4℃将上清液与ni
‑
nta琼脂糖(qiagen)混合2小时。用洗涤缓冲液(20mm tris
‑
hcl ph7.4,1%np
‑
40,150mm nacl,5mm edta)洗涤珠子,用洗脱缓冲液(200mm咪唑,150mm nacl,20mm tris
‑
hcl,ph7.4,0.1%tritonx
‑
100,1mm dtt)洗脱。
[0081]
(3)体外激酶测定在30℃下使20μg已提纯的带6
×
his标签的unc119蛋白质在含有50单位的ck2(neb)和40μm的atp的1
×
蛋白激酶用nebuffer(neb公司)中反应30分钟。加入等量的2
×
样本缓冲液(0.1m tris
‑
hcl ph6.8,1%sds,5%β巯基乙醇,10%甘油,0.02%bpb),在室温下静置30分钟,终止反应。
[0082]
(4)phos
‑
tag sds
‑
page通过使用了phos
‑
tag丙烯酰胺(wako)的sds
‑
page,按照产品说明书对体外激酶测定后的样本进行检测(参考文献1:mol.cell.proteomics.5(4):749
‑
757(2006);参考文献2:proteomics 11(2):319
‑
323(2011))。
[0083]
(5)结果将sds
‑
page的结果示于图7中。通过phos
‑
tag sds
‑
page,在未与ck2反应的样本中观察到一条带6
×
his标签的unc119蛋白质的条带(黑色箭头),另一方面,在与ck2进行了反应的样本中,除了黑色箭头的条带以外还观察到上方的条带(白色箭头),确认到ck2引起的unc119的磷酸化。
[0084]
另外,本发明并不限定于上述各个实施方案及实施例,可对权利要求所示的范围进行各种变更,将分别由不同的实施方案公开的技术手段进行适当组合而得到的实施方案也包括在本发明的技术范围内。此外,本说明书中记载的学术文献以及专利文献均作为参考而援用在本说明书中。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1