用于递送分子负荷物的外泌体脉管的制作方法
背景技术:
本公开涉及可促进分子负荷物(cargo)的递送的一种或多种外泌体(exosome),并且更具体地,涉及具有官能化表面以将一种或多种分子负荷物运输至期望的生物细胞和/或组织的一种或多种外泌体。
影响用于将分子负荷物递送到特定细胞或组织的纳米技术的三个约束包括:生物相容性、分子负荷物装载效率和/或递送系统对感兴趣的细胞或组织的特异性。例如,为了生物相容性,递送系统必须对受体生物体无毒和/或在生理条件下维持其完整性(例如,在ph7下稳定和/或避免免疫检测)。另外,分子负荷物递送系统应当能够递送各种各样的感兴趣的分子(例如,用于遗传操作的dna、用于基因沉默的rna、治疗剂和/或分子抑制剂)。
常规的分子负荷物递送系统由基础递送容器和用于将分子负荷物装载到该容器的方案组成。此外,常规的分子负荷物递送技术然后可以分为两类:纳米颗粒技术和脂质囊泡技术。然而,纳米颗粒和脂质体囊泡技术二者可能经历关于上述的约束和/或考虑的多个缺点。
可以在常规分子负荷物递送系统中使用的示例纳米颗粒包括:金、银和/或钛。实际上,已经建立了用于将多种官能团并因此将多种生物活性分子共价连接至纳米颗粒金属的方案。然而,虽然许多纳米颗粒是生物相容性的,但是它们随着时间的推移倾向于在体内积聚并且可能产生毒性。
脂质体是可以制备成具有各种尺寸(例如直径在几十纳米(nm)至约10-20微米(μm)范围内)的合成脂质囊泡。此外,脂质体的形状、尺寸、形态和功能可以通过改变脂质的化学/物理结构和组成来工程化。脂质体已经用于化学化合物递送和其他治疗目的。然而,生物相容性仍然是个问题,因为脂质体不模拟精确的细胞(例如,包括脂质和蛋白质)特性。因此,纳米颗粒(例如由金制成的那些)的广泛效用由于其固有的非生物降解性而是有问题的;并且基于脂质体的技术缺乏与靶细胞和/或组织的质膜相互作用所需的某些脂质和/或蛋白质。
另外的常规分子负荷物递送技术包括使用外泌体作为递送血管。然而,用于装载外泌体的现代方案是低效的、时间依赖性的和/或对其有害;因此,基本上抑制常规的基于外泌体的分子负荷物递送技术的功能。例如,通过电穿孔将核酸序列包封在外泌体中是低效的(例如,仅小部分的对象外泌体适当地装载有分子负荷物和/或该过程可以损害外泌体)。在另一个实例中,点击化学用于官能化外泌体的表面,使得分子负荷物可以外部地附接。虽然该过程不遭受电穿孔的低效,但是它需要在苛刻条件下持续搅拌24小时,这可以不利地改变外泌体形态和/或生物化学。因此,常规技术不足以有效地使用外泌体来运输负荷物。
技术实现要素:
下文呈现发明内容以提供对本发明的一个或多个实施例的基本理解。此发明内容并非意图识别关键或重要元素,或描绘特定实施例的任何范围或权利要求书的任何范围。其唯一目的是以简化形式呈现概念作为稍后呈现的更详细描述的序言。在本文中所描述的一个或多个实施例中,描述可以促进分子负荷物的运输和/或递送的分子和/或方法。
根据一个实施例,提供了一种分子。所述分子可以包含化学改性的分子负荷物,所述负荷物键合(bond)到外泌体的表面生物分子上。所述表面生物分子可以位于所述外泌体的双层膜上,与所述外泌体的细胞质相对。这种分子的优点可以是使用一种或多种外泌体来递送一种或多种治疗化合物。
在一些实例中,表面生物分子可以是选自由蛋白质、抗体、抗原、磷脂、糖脂、核酸、多糖、糖和双层膜的离域主链分子组成的组的化合物。这种分子的优点可以是外泌体的天然存在的表面结构可以用于促进与分子负荷物的一种或多种生物缀合。
根据一个实施例,提供了一种方法。所述方法可以包括通过将化学改性的分子负荷物键合至位于外泌体的双层膜上并且与外泌体的细胞质相对的表面生物分子来使外泌体官能化。这种方法的优点可以是形成一个或多个外泌体脉管(vessel)以促进一种或多种分子负荷物的运输和/或递送。此外,含有疏水基团或碳链的表面生物分子也可以嵌入在双层膜支架内。
在一些实例中,所述方法还可包括通过将第二化学改性的分子负荷物键合至位于双层膜上并与细胞质相对的第二表面生物分子来官能化外泌体。这样的方法的优点可以是一个或多个合成的外泌体脉管可同时装载各种类型的分子负荷物以增强一种或多种运输和/或递送功能。
根据一个实施例,提供了一种方法。所述方法可以包括基于位于外泌体的双层膜上并且与外泌体的细胞质相对的表面生物分子的组成,通过分子探针从多种外泌体中分离外泌体。这样的方法的优点在于,特定类型的外泌体可以用于产生一个或多个外泌体脉管以运输和/或递送分子负荷物。
在一些实例中,所述方法还可以包括通过外泌体将分子负荷物递送至生物细胞。外泌体可以对生物细胞具有化学亲和力。这种方法的优点可以是外泌体将分子负荷物靶向特异性运输和/或递送至目标生物细胞。
附图说明
图1示出了根据本文描述的一个或多个实施例的示例非限制性外泌体脉管的图,所述外泌体脉管可以具有用一种或多种分子负荷物官能化的表面。
图2示出了根据本文描述的一个或多个实施例的可促进外泌体脉管形成的示例性非限制性官能化过程的图,该外泌体脉管可运输和/或递送一种或多种分子负荷物。
图3示出了根据本文描述的一个或多个实施例的可以促进将一种或多种分子负荷物附着至外泌体表面的示例非限制性配体改性的图。
图4示出了根据本文描述的一个或多个实施例的可促进形成外泌体脉管的示例非限制性官能化过程的图,该外泌体脉管可运输和/或递送一种或多种分子负荷物。
图5示出了根据本文描述的一个或多个实施例的可促进形成外泌体脉管的示例非限制性官能化过程的图,该外泌体脉管可运输和/或递送一种或多种分子负荷物。
图6示出了根据本文描述的一个或多个实施例的示例非限制性递送过程的图,该递送过程可以包括将一种或多种分子负荷物运输至靶生物细胞和/或组织的质膜的一个或多个外泌体脉管。
图7示出了根据本文描述的一个或多个实施例的可促进分离一种或多种目标外泌体的示例非限制性芯片上探针的图。
图8示出了根据本文描述的一个或多个实施例的可以捕获一种或多种目标外泌体以实现一种或多种分子负荷物的特定递送功能的示例非限制性分离过程的图。
图9示出了根据本文描述的一个或多个实施例的可以促进使一种或多种外泌体官能化以促进一种或多种分子负荷物的运输和/或递送的示例非限制性方法的流程图。
图10示出了根据本文所描述的一个或多个实施例的可以促进使一种或多种外泌体官能化以促进一种或多种分子负荷物的运输和/或递送的示例性非限制性方法的流程图。
图11示出了根据本文描述的一个或多个实施例的可以包括分离一种或多种目标外泌体以促进一种或多种分子负荷物的特异性递送功能的示例非限制性方法的流程图。
图12示出了根据本文描述的一个或多个实施例的可以包括分离一种或多种目标外泌体以促进一种或多种分子负荷物的特定递送功能的示例非限制性方法的流程图。
具体实施方式
以下详细描述仅仅是说明性的,并不意图限制实施例和/或实施例的应用或使用。此外,不意图受前述背景技术或发明内容部分或详细描述部分中呈现的任何明确或暗示的信息的限制。
现在参考附图描述一个或多个实施例,其中相同的附图标记始终用于指代相同的元件。在以下描述中,为了解释的目的,阐述了许多具体细节以便提供对一个或多个实施例的更透彻的理解。然而,显然,在各种情况下,可以在没有这些具体细节的情况下实践一个或多个实施例。
考虑到常规分子负荷物递送系统的上述问题,本公开可实施以产生一种或多种分子形式的这些问题中的一个或多个的解决方案和/或可利用外泌体作为容器来运输和/或递送分子负荷物的方法。例如,本文所述的外泌体脉管可满足上述有效生物分子递送系统的三个限制。生物相容性限制可通过从体液和/或细胞培养基中的细胞分离天然分泌的外泌体来满足,其还可在生理条件下维持外泌体的基本稳定性。装载效率限制可通过在容易存在于具有化学改性分子负荷物的外泌体表面上的表面生物分子(例如,磷脂、蛋白质和/或碳水化合物)之间形成共价键来满足(例如,大多数反应步骤可在键合在外泌体表面上的生物分子上进行以避免对外泌体的苛刻反应条件)。此外,一个或多个外泌体脉管可通过将特异性抗体共价附接至外泌体表面来实现对靶生物细胞和/或组织的特异性。作为蛋白质本身,抗体可经官能化以与除蛋白质以外的生物分子反应。
本文描述的各种实施例可以涉及官能化的外泌体脉管和/或促进分子负荷物的运输和/或递送的方法。例如,本文描述的一个或多个实施例可以包括将一种或多种分子负荷物(例如,核酸和/或蛋白质)与位于一种或多种外泌体的表面上的一种或多种生物分子缀合;从而将所述一种或多种分子负荷物装载到外泌体脉管以运输和/或递送到一种或多种期望的生物细胞和/或组织。在一个或多个实施例中,缀合可以通过一种或多种分子负荷物与一种或多种表面生物分子之间的一个或多个共价键来建立。此外,通过将一种或多种抗体和/或抗原与外泌体的一种或多种表面生物分子缀合,对象外泌体可以是对特定的、靶生物细胞和/或组织具有化学亲和力的容器。
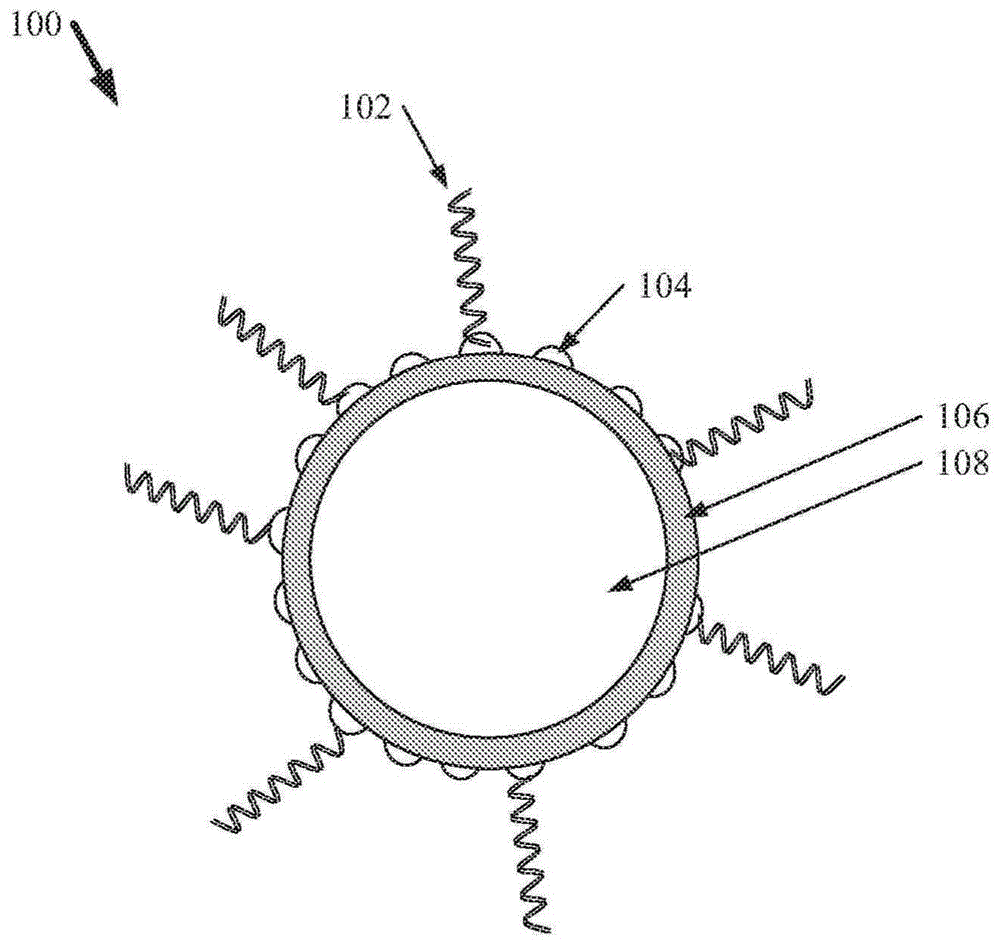
图1示出了用一种或多种分子负荷物102官能化的示例非限制性外泌体脉管100的图。例如,图1描绘了示例性外泌体脉管100,其包含与外泌体脉管100的一种或多种表面生物分子104缀合的一种或多种核酸分子负荷物102(例如,其中图1中所示的波浪线可以代表一种或多种核酸)。
如本文所用,术语"外泌体"可以指内吞起源的小囊泡(例如,具有30至200nm的直径),其可以通过多囊泡体和/或质膜与细胞外环境的融合来分泌。外泌体可以包含多种生物分子,包括但不限于:跨膜蛋白、胞质蛋白、酶、表面蛋白、核酸、脂质、其组合和/或类似物。如图1所示,外泌体可以包含双层膜106,其限定外泌体内部的细胞质108的。本领域普通技术人员将容易地认识到,双层膜106可以包含磷脂双层和/或细胞质108可以容纳对象外泌体的各种特征(例如,酶、蛋白、核酸、其组合和/或类似物)。外泌体可以通过一种或多种不同的体液(如:唾液、尿液、血液、血清、血浆、汗液、泪液、其组合、和/或类似物)被输送遍及整个生物体。在各种实施例中,本文所述的一个或多个外泌体脉管100可以是具有与双层膜106的表面缀合(例如,通过一种或多种天然存在的表面结构)的一种或多种分子负荷物102的外泌体。
一个或多个外泌体脉管100可包含一个或多个表面生物分子104。一个或多个表面生物分子104可位于双层膜106的表面上和/或至少部分位于双层膜106内。例如,一个或多个表面生物分子104可位于双层膜106上与细胞质108相对(例如,位于一个或多个外泌体脉管100的内部之外)。示例性表面生物分子104可包括但不限于:蛋白质、抗体、抗原、磷脂、糖脂、核酸、多糖、糖、碳水化合物、酶、外泌体双层膜106支架、其组合等。
此外,所述一种或多种表面生物分子104可以包含一种或多种靶官能团,其可以促进与所述一种或多种分子负荷物102缀合。可以包含在所述一种或多种表面生物分子104内的示例性靶官能团可以包括但不限于:伯胺(例如,赖氨酸基团、精氨酸基团、其组合和/或类似基团)、半胱氨酸基团、磷酸酯基团、羟基基团、羧基基团、其组合和/或类似基团。在一种或多种实施例中,所述一种或多种靶官能团可以与所述一种或多种分子负荷物102建立共价键,以促进所述一种或多种分子负荷物102与外泌体脉管100的表面缀合(conjugation)。外泌体脉管100可以包含在双层膜106上和/或双层膜106内的多种不同类型的表面生物分子104。此外,图1中描绘的表面生物分子104的数目是示例性的,并且本领域普通技术人员将认识到,所述一种或多种外泌体脉管100可以包含比图1中示出的十七种更少或额外的表面生物分子104。
一种或多种分子负荷物102可以通过与一种或多种表面生物分子104的化学相互作用而径向地布置在外泌体脉管100的表面上和/或可以包括一种或多种核酸(例如,如图1所示)和/或一种或多种蛋白质(例如,抗体和/或抗原)。例如,分子负荷物102中的一种或多种可以是由一种或多种核酸定义的一种或多种治疗性化学化合物。一种或多种外泌体脉管100可以将一种或多种治疗性化学化合物运输和/或递送至一种或多种靶生物细胞和/或组织。另外,分子负荷物102中的一种或多种可以是抗体和/或抗原中的一种或多种,其可以用对特定生物细胞和/或组织的化学亲和力官能化一种或多种外泌体脉管100。在一种或多种实施例中,一种或多种外泌体脉管100可以包括各种类型的分子负荷物102的混合物。
图2示出了根据本文描述的一个或多个实施例的示例非限制性第一缀合方案200的图,其可促进一种或多种分子负荷物102与一种或多种表面生物分子的缀合。为了简洁起见,省略了对在本文中描述的其他实施例中采用的类似元件的重复描述。如图2所示,示例性第一缀合方案200可包括使初始外泌体202与一种或多种分子负荷物102缀合以形成一个或多个外泌体脉管100。在一个或多个实施例中,可将一种或多种分子负荷物102和/或一种或多种初始外泌体202在碱性溶液(例如,具有大于或等于7且小于或等于10的ph)中混合在一起以促进第一缀合方案200。
一种或多种初始外泌体202可以包含一种或多种表面生物分子104,其可以被靶向以与一种或多种分子负荷物102缀合。此外,一种或多种分子负荷物102(例如,包含如图2所示的核酸,和/或一种或多种蛋白质,例如抗体和/或抗原)可以包含一种或多种反应性官能团204。一种或多种反应性官能团204可以与一种或多种表面生物分子104的一种或多种官能团化学相互作用,以在一种或多种分子负荷物102和一种或多种表面生物分子104之间建立共价键。
可包含一个或多个反应性官能团204的示例性化合物可包括但不限于:胺反应性化合物、磷酸盐反应性化合物、羟基反应性化合物、羧基反应性化合物、抗体、抗原、其组合等。胺反应性化合物可包括能够与胺反应以形成共价键的任何反应性基团。示例性胺反应性化合物可包括但不限于:n-羟基琥珀酰亚胺("nhs")酯、磺基-n-羟基琥珀酰亚胺酯、亚氨酯、氟苯基酯、环氧化物、异硫氰酸酯、异氰酸酯、磺酰氯、醛、碳二亚胺、酰基叠氮化物、酸酐、氟苯、碳酸酯、其组合等。例如,一个或多个官能团可与氨基酸的一个或多个侧链偶联,所述氨基酸如精氨酸和/或赖氨酸的伯胺。磷酸盐反应性化合物可包括能够与磷酸盐基团反应以形成共价键的任何反应性基团。例如,磷酸盐反应性化合物可包括但不限于:碳二亚胺、烷基、芳基、酰基、其组合等。羟基反应性化合物可包括能够与羟基反应以形成共价键的任何反应性基团。示例性羟基反应性化合物可包括但不限于:烷基、芳基、酰基、其组合等。羧基反应性化合物可包括能够与羧基反应以形成共价键的任何反应性基团。
在各种实施例中,一个或多个外泌体脉管100可以运输核酸(例如,合成核酸)以实现多种治疗功能。例如,包含在一个或多个分子负荷物102内的一个或多个核酸可以是免疫刺激寡核苷酸,其可以激活与一个或多个外泌体脉管100相互作用的生物细胞和/或组织固有的一个或多个免疫信号传导网络。例如,一个或多个分子负荷物102可以包含合成核酸,其可以:引发抗原呈递和/或共刺激,激活先天免疫细胞(例如,巨噬细胞和/或树突细胞,诱导促炎细胞因子的产生,其组合,和/或类似物。在另一个实例中,由一个或多个外泌体脉管100运输和/或递送的一个或多个分子负荷物102可以包含合成核酸,其可以在对象生物细胞和/或组织内执行一种或多种治疗技术,包括但不限于:反义技术、核糖核酸("rna")干扰技术、剪接转换技术、基于信使rna的治疗、其组合和/或类似物。
在一个或多个实施例中,一种或多种抗体和/或抗原可用作一种或多种反应性官能团204。例如,一种或多种分子负荷物102可包含与一种或多种抗体键合的一种或多种核酸,其中所述一种或多种抗体可与位于初始外泌体202上的一种或多种表面抗原(例如,用作如本文所述的一种或多种表面生物分子104)建立一种或多种抗体-抗原相互作用,以促进所述一种或多种分子负荷物102的缀合。在另一个实例中,一种或多种分子负荷物102可包含与一种或多种抗原键合的一种或多种核酸,其中所述一种或多种抗原可与位于初始外泌体202上的一种或多种表面抗体(例如,用作如本文所述的一种或多种表面生物分子104)建立一种或多种抗原-抗体相互作用,以促进所述一种或多种分子负荷物102的缀合。
图3示出了根据本文所述的一个或多个实施例的示例非限制性生物缀合方案300的示意图,该方案300可将一种或多种分子负荷物102缀合至一种或多种表面生物分子104(例如,如关于第一缀合方案200所述)。为简洁起见,省略了本文所述的其它实施例中采用的类似元件的重复描述。
可利用多种生物缀合反应来促进一种或多种分子负荷物102与一种或多种表面生物分子104的缀合;例如:烷化、酰化、二硫键合、抗体-抗原相互作用、胺键合、磷酸酯键合、核酸退火、其组合等。在各种实施例中,一种或多种分子负荷物102的一种或多种反应性官能团204可与一种或多种表面生物分子104的一种或多种靶官能团反应以建立生物缀合反应。
例如,生物缀合方案300描述了示例性生物缀合反应,其中反应性官能团204可以是胺反应性化合物,一种或多种表面生物分子104的靶官能团可以是伯氨基。图3描述了根据本文描述的各种实施例的示例性分子负荷物102结构。例如,图3中显示的示例性分子负荷物102可以包含一种或多种键合到nhs反应性官能团204的核酸(例如,由一条或多条波浪线表示)。如图3中所示,反应性官能团204(例如,nhs酯)可以键合到一种或多种核酸的五撇("5’")端。另外,图3描述了根据本文描述的各种实施例的示例性表面生物分子104结构。图3中示出的示例性表面生物分子104可以是包含附着到胺(例如,赖氨酸,如图3中所描述)的多肽链302的蛋白质。如图3中所示,一种或多种靶官能团可以位于一种或多种表面生物分子104的远端。
在示例性的生物缀合方案300中,可将一种或多种含有分子负荷物102的核酸引入初始外泌体202的一个或多个表面生物分子104中,所述引入在ph大于或等于7且小于或等于9的环境中进行。一种或多种反应性官能团204的化学亲和力可促进一种或多种反应性官能团204与一种或多种靶官能团之间形成共价键。例如,一种或多种分子负荷物102可共价键合至包含在一种或多种蛋白质表面生物分子104的赖氨酸结构内的伯氨基。如图3所示,所得的生物缀合可使得分子负荷物102的一种或多种核酸键合至一种或多种表面生物分子104(例如,初始外泌体202的表面上的一种或多种蛋白质);从而形成可运输和/或递送一种或多种键合的核酸的外泌体脉管100。
虽然图3描述了一种或多种分子负荷物102和/或一种或多种表面生物分子104的示例性结构,但本文所述的生物缀合的构造不限于此。例如,一种或多种反应性官能团204和/或一种或多种靶官能团可包括本文所述的各种化学类别和/或实施例支持的任何化学结构。另外,虽然图3描述了一种或多种核酸与一种或多种蛋白质的生物缀合,但本文所述的生物缀合的构造不限于此。例如,如本文所述,一种或多种分子负荷物102可包括一种或多种蛋白质(例如抗体和/或抗原),和/或一种或多种表面生物分子可以是抗体、抗原、磷脂、糖脂、核酸、多糖、糖、碳水化合物、外泌体双层膜106支架、其组合等。
图4示出了根据本文描述的一个或多个实施例的示例非限制性第二缀合方案400的示意图,其可促进一种或多种分子负荷物102与一种或多种表面生物分子104的缀合。为了简洁起见,省略了对在本文中描述的其他实施例中采用的类似元件的重复描述。如图4所示,示例性第二缀合方案400可包括使初始外泌体202与一种或多种分子负荷物102缀合以形成一个或多个外泌体脉管100。在一个或多个实施例中,可将一种或多种分子负荷物102和/或一种或多种初始外泌体202在碱性溶液(例如,具有大于或等于7且小于或等于9的ph)中混合在一起以促进第二缀合方案400。
第二缀合方案400可以例示:一种或多种分子负荷物102可以包含键合至一种或多种反应性官能团204的一种或多种抗体(例如,在图4中描绘为"y"形结构)。如本文关于图2和/或3所述,一种或多种反应性官能团204可以促进一种或多种分子负荷物102的一种或多种抗体键合至初始外泌体202的一种或多种表面生物分子104。通过将一种或多种抗体键合至外泌体脉管100的表面,可以使外泌体脉管100官能化以靶向特定生物细胞和/或组织。例如,携带含有抗体的分子负荷物102的一种或多种外泌体脉管100(例如,如图4所示)可以化学吸引至包含可以键合至抗体的抗原类型的一种或多种生物细胞和/或组织。换句话说,抗体分子负荷物102(例如,如图4所示)可以使一种或多种外泌体脉管100与一种或多种靶生物细胞和/或组织之间的抗体-抗原相互作用成为可能;从而增加对一种或多种外泌体脉管100的运输和/或递送功能的特异性。另外,在一种或多种实施例中,一种或多种分子负荷物102可以包含一种或多种抗原(未示出)以使一种或多种外泌体脉管100与包含特定抗体的一种或多种靶生物细胞和/或组织之间的抗体-抗原相互作用成为可能。
图5示出了根据本文所述的一个或多个实施例的示例非限制性第三缀合方案500的示图,其可促进一种或多种分子负荷物102与一种或多种表面生物分子104的缀合。为了简洁起见,省略了对在本文中描述的其他实施例中采用的类似元件的重复描述。如图5所示,示例性第三缀合方案500可包括使初始外泌体202与多个分子负荷物102缀合以形成一个或多个外泌体脉管100。在一个或多个实施例中,可将一种或多种分子负荷物102和/或一种或多种初始外泌体202在碱性溶液(例如,具有大于或等于7且小于或等于9的ph)中混合在一起以促进第二缀合方案400。
第三缀合方案500示例了一个或多个外泌体脉管100可以包括多种不同类型的分子负荷物102。例如,图5描绘了示例性外泌体脉管100,其包括包含一种或多种核酸的第一类型的分子负荷物102和包含一种或多种抗体的第二类型的分子负荷物102(例如,一个或多个波浪线可以表示核酸和/或一个或多个"y"形结构可以表示抗体)。如第三缀合方案500中所示,各种类型的分子负荷物102可以同时缀合至一种或多种初始的外泌体202。例如,包含核酸的分子负荷物102和包含抗体的分子负荷物102可以同时缀合至一种或多种初始的外泌体202。或者,一种或多种第一类型的分子负荷物102(例如,包含一种或多种核酸)可以与一种或多种初始的外泌体202缀合,由此所得到的外泌体脉管100可以进一步与一种或多种第二类型的分子负荷物102(例如,包含一种或多种抗体)缀合。
多种不同类型的分子负荷物102的缀合可增强一个或多个外泌体脉管100的功能性。例如,如本文所述,缀合一个或多个核酸分子负荷物102可使得一个或多个外泌体脉管100能够运输和/或递送治疗性化合物。此外,将蛋白质(例如,抗体和/或抗原)分子负荷物102缀合到对象外泌体脉管100可以整合对治疗性化合物的运输和/或递送的特异性。因此,与核酸分子负荷物102和蛋白质(例如,抗体和/或抗原)分子负荷物102缀合的一个或多个外泌体脉管100可有利地运输和/或递送治疗性化合物以靶向生物细胞和/或组织。
图6示出了根据本文描述的一个或多个实施例的可通过一个或多个外泌体脉管100促进的示例非限制递送过程600的图。为了简洁起见,省略了本文描述的其他实施例中采用的类似元件的重复描述。如图6中所示,一个或多个外泌体脉管100可将一种或多种分子负荷物102运输至一种或多种生物细胞和/或组织的质膜602。
例如,一个或多个外泌体脉管100可以将一个或多个分子负荷物102运输穿过质膜602。在一个或多个实施例中,一个或多个外泌体脉管100可以经由一个或多个表面生物分子104和/或位于质膜602上和/或质膜602内的一个或多个细胞受体之间的一种或多种相互作用粘附到质膜602。此外,在各种实施例中,由于一个或多个表面生物分子104和位于质膜602上的一个或多个靶抗原604之间的抗体-抗原相互作用,一个或多个外泌体脉管100可以被吸引到和/或以其他方式粘附到质膜602。例如,一个或多个外泌体脉管100可以包括一个或多个分子负荷物102,其包含对质膜602(例如,对位于质膜602的表面上的靶抗原604和/或靶抗体)具有化学亲和力的蛋白质(例如,抗体和/或抗原)。一旦粘附到质膜602,一个或多个外泌体脉管100可以:经由细胞内信号通路诱导可溶性信号转导;与质膜602融合,从而将一个或多个分子负荷物102转移穿过质膜602;和/或经由吞噬作用、微细胞溶质、受体介导的内吞作用和/或筏介导的内吞作用被内吞。例如,在一个或多个实施例中,一个或多个外泌体脉管100可以通过受体介导的内吞作用被内化到一个或多个生物细胞和/或组织中,其中位于外泌体脉管100的表面(例如,位于双层膜106上)上的一个或多个配体(例如,表面生物分子104和/或分子负荷物102)可以接合位于质膜602上的一个或多个细胞受体(例如,清道夫受体)。此外,一个或多个外泌体脉管100可以通过一个或多个内吞作用机制被内化。
图7示出了根据本文所述的一个或多个实施例的示例非限制性芯片上探针700的图,该探针可以用于从多个外泌体样品中分离一种或多种初始外泌体202。为了简洁起见,省略了对在本文中描述的其他实施例中采用的类似元件的重复描述。如图7所示,一种或多种芯片上探针700可以包含附着于基质704的一种或多种分子探针702(例如,在图7中由虚线描绘)。一种或多种分子探针702可以是单链核酸复合物(例如,在图7中由波浪线表示),其可以与键合在一种或多种初始外泌体202的双层膜106表面上的一种或多种单链核酸互补。
如图7所示,一个或多个分子探针702可以固定到一个或多个基质704。可以包括一个或多个基质704的示例材料可以包括但不限于:硅、聚二甲基硅氧烷("pdms")、聚(甲基丙烯酸甲酯)("pmma")、其组合等。在一个或多个实施例中,一个或多个分子探针702可以通过物理吸附、硫醇、胺、核酸-生物素、其组合等固定到一个或多个基质704。
图8示出根据本文描述的一个或多个实施例的示例非限制性外泌体分离过程800的图,可以执行该外泌体分离过程800来将一个或多个初始外泌体202与多个外泌体样品分离。为了简洁起见,省略了对在本文中描述的其他实施例中采用的类似元件的重复描述。如图8所示,外泌体分离方法800可以利用一种或多种芯片上探针700来收集一种或多种感兴趣的初始外泌体202。
可以将包含多个外泌体的样品引入(例如,通过光刻技术、浸没在所需溶液中、或微流体系统)一个或多个芯片上探针700。当一个或多个外泌体通过一个或多个芯片上探针700时,外泌体表面上的一种或多种化学化合物可以被吸引到固定于一个或多个基质704的一个或多个分子探针702和/或以其他方式与其相互作用。不具有对一个或多个分子探针702具有化学亲和力的一种或多种表面化合物的外泌体可以在没有相互作用的情况下通过一个或多个芯片上探针700。相反,包含对分子探针702具有化学亲和力的一种或多种表面化合物的外泌体可以与一个或多个分子探针702化学相互作用(例如,退火)和/或由此被其捕获。因此,外泌体分离方法800可以基于对包含一个或多个分子探针702(例如,一个或多个第二部分708)的化学化合物的选择来分离具有特定表面组成的外泌体。
例如,可以用一种或多种包含与一种或多种分子探针702互补的单链核酸的蛋白质(例如,抗体和/或抗原)对一种或多种初始外泌体202的表面进行工程改造。例如,可以合成包含与第二部分键合的第一部分的核酸-抗体复合物802。核酸-抗体复合物802的第一部分可以是与单链核酸分子探针702互补的单链核酸。核酸-抗体复合物802的第二部分可以是具有与感兴趣的初始外泌体202的一种或多种表面生物分子104键合的亲和力的一种或多种抗体。例如,一种或多种抗体可以具有与一种或多种抗原表面生物分子104键合的亲和力(例如具有引发抗体-抗原与位于感兴趣的初始外泌体202上的一种或多种表面生物分子104相互作用的亲和力)。因此,一种或多种核酸-抗体复合物802可以用与一种或多种分子探针702互补的单链核酸官能化靶初始外泌体202的表面。如图8所示,一种或多种核酸-抗体复合物802可以进一步与一种或多种分子探针702退火,从而芯片上探针700可以捕获一种或多种感兴趣的初始外泌体202(例如,包括特异性表面生物分子104的一种或多种初始外泌体202,如可以帮助通过一个或多个外泌体血管100的运输特异性的特异性抗原)。
虽然图8描绘了包括具有相同或基本上相同的化学结构的多个分子探针702的片上探针700;但是分子探针702的结构并不限于此。例如,在一个或多个实施例中,包括在片上探针700内的一个或多个分子探针702可以具有与包括在片上探针700内的一个或多个其他分子探针702不同的结构。例如,第一分子探针702可以包括第一单链核酸序列,而第二分子探针702可以包括不同的单链核酸序列。包括具有两个或更多个不同结构的多个分子探针702的片上探针700可以通过外泌体分离过程800来分离两种或更多种不同类型的靶外泌体。
在一个或多个实施例中,通过外泌体分离过程800分离的外泌体可以充当用于本文所述的一种或多种生物缀合反应的初始外泌体202,以形成一个或多个外泌体脉管100。例如,外泌体分离过程800可以用于使一种或多种分子负荷物102与具有特定表面结构(例如,表面生物分子104的特定组合物)的初始外泌体202缀合,以增强和/或实现递送过程600的一种或多种特征。例如,其中对于递送过程600靶向一种或多种特定生物细胞和/或组织可能是有利的,外泌体分离过程800可以分离具有一种或多种表面生物分子104的初始外泌体202,所述表面生物分子104对感兴趣的生物细胞和/或组织的一种或多种生物分子具有化学亲和力;从而促进一种或多种分子负荷物102向特定生物细胞和/或组织的运输和/或递送。在另一种情况下,通过外泌体分离过程800靶向的一种或多种表面生物分子104可以增强和/或实现一种或多种靶生物细胞和/或组织对一种或多种分子负荷物102的摄取(例如,增强和/或实现一种或多种内吞过程,例如吞噬作用、微细胞溶质、受体介导的内吞作用和/或筏介导的内吞作用)。
图9示出了根据本文描述的一个或多个实施例的可以使用一个或多个外泌体脉管100促进运输和/或递送一个或多个分子负荷物102的示例非限制性方法900的流程图。为了简洁起见,省略了对在本文中描述的其他实施例中采用的类似元件的重复描述。
在902,方法900可以包括通过将一种或多种化学改性的分子负荷物102键合到一种或多种表面生物分子104来官能化一种或多种外泌体(例如,一种或多种初始外泌体202),所述表面生物分子104位于一种或多种外泌体的双层膜106上并且与一种或多种外泌体的细胞质108相对。例如,官能化可以根据本文所述的第一缀合方案200、第二缀合方案400和/或第三缀合方案500来进行。例如,一种或多种分子负荷物102可以包含一种或多种核酸和/或蛋白质(例如,抗体和/或抗原)和/或一种或多种反应性官能团204(例如,胺反应性化合物、磷酸盐反应性化合物、羟基反应性化合物、抗体和/或抗原)。此外,一种或多种表面生物分子104可以包含一种或多种官能团,其可以促进与一种或多种反应性官能团204的化学相互作用(例如,共价键合和/或抗体-抗原相互作用)。示例性表面生物分子104可以包括:蛋白质(例如,抗体和/或抗原)、磷脂、糖脂、核酸、多糖、糖、双层膜106的离域主链分子、酶、其组合等。作为官能化的结果,一种或多种分子负荷物102可以径向布置键合到一种或多种初始外泌体202的表面,以形成一种或多种外泌体脉管100。
在904处,方法900可以包括通过外泌体将一种或多种化学改性的分子负荷物102递送到一种或多种生物细胞和/或组织。例如,904处的递送可以根据本文描述的递送过程600进行。在一个或多个实施例中,键合到一种或多种外泌体(例如,键合到一种或多种初始外泌体202)的一种或多种化学改性的分子负荷物102可以使得一个或多个外泌体脉管100能够靶向一种或多种特定生物细胞和/或组织,以递送一种或多种分子负荷物102。例如,分子负荷物102中的一种或多种可以包括可以被特异性吸引到一种或多种感兴趣的生物细胞和/或组织的一种或多种抗原的一种或多种抗体。此外,一个或多个外泌体脉管100可以通过引发以下来递送一种或多种分子负荷物102:经由细胞内信号通路诱导可溶性信号转导;与一种或多种生物细胞和/或组织的质膜602融合,从而将一种或多种分子负荷物102跨质膜602转移;和/或经由吞噬作用、微细胞溶质、受体介导的内吞作用和/或筏介导的内吞作用的内吞作用。例如,在一个或多个实施例中,一个或多个外泌体脉管100可以通过受体介导的内吞作用内化到一种或多种生物细胞和/或组织中,其中位于外泌体脉管100的表面(例如,位于双层膜106上)上的一种或多种配体(例如,表面生物分子104和/或分子负荷物102)可以接合位于质膜602上的一种或多种细胞受体(例如,清道夫受体)。一种或多种分子负荷物102的递送可以促进一种或多种治疗性疗法,诸如:反义技术、核糖核酸("rna")干扰技术、剪接转换技术、基于信使rna的治疗剂、基于微rna的治疗剂、其组合等。
图10示出根据本文描述的一个或多个实施例的可以使用一个或多个外泌体血管100促进运输和/或递送一个或多个分子负荷物102的示例非限制性方法1000的流程图。为了简洁起见,省略了在本文描述的其它实施例中采用的类似元件的重复描述。
在1002,方法1000可以包括通过使一种或多种化学改性的分子负荷物102与位于一种或多种外泌体的双层膜106上并与一种或多种外泌体的细胞质108相对的一种或多种表面生物分子104键合,来官能化一种或多种外泌体(例如,一种或多种初始外泌体202)。例如,可以根据本文描述的第一缀合方案200、第二缀合方案400和/或第三缀合方案500来进行官能化。例如,一种或多种化学改性的分子负荷物102可以包含一种或多种核酸和/或蛋白质(例如,抗体和/或抗原)和/或一种或多种反应性官能团204(例如,胺反应性化合物、磷酸盐反应性化合物、羟基反应性化合物、抗体和/或抗原)。此外,一种或多种表面生物分子104可以包含一种或多种能够促进与一种或多种反应性官能团204的化学相互作用(例如,共价键合和/或抗体-抗原相互作用)的官能团。示例性表面生物分子104可以包括但不限于:蛋白质(例如,抗体和/或抗原)、磷脂、糖脂、核酸、多糖、糖、双层膜106的离域主链分子、酶、其组合等。作为官能化的结果,一种或多种分子负荷物102可以径向布置与一种或多种初始外泌体202的表面键合,以形成一种或多种外泌体脉管100。
在1004,方法1000可以包括通过将一种或多种第二化学改性的分子负荷物102与位于双层膜106上并与细胞质108相对的一种或多种第二表面生物分子104键合而将一种或多种外泌体官能化。例如,在1004的官能化可以根据本文所述的第三缀合方案500进行。例如,一种或多种第二化学改性的分子负荷物102可以包括一种或多种核酸和/或蛋白质(例如,抗体和/或抗原)和/或一种或多种反应性官能团204(例如,胺反应性化合物、磷酸盐反应性化合物、羟基反应性化合物、抗体和/或抗原)。一种或多种第二化学改性的分子负荷物102的一种或多种反应性官能团204可以促进与一种或多种第二表面生物分子104的一个或多个键合(例如,生物缀合反应、共价键合和/或抗体-抗原相互作用)。在一个或多个实施例中,一种或多种化学改性的分子负荷物102和一种或多种第二化学改性的分子负荷物102可以具有不同的化学组成,以便将不同的功能性赋予一种或多种外泌体脉管100。例如,一种或多种化学改性的分子负荷物102和一种或多种第二化学改性的分子负荷物102可以经由一种或多种生物缀合反应同时和/或顺序地与一种或多种初始外泌体202键合(例如,一种或多种化学改性的分子负荷物102的生物缀合可以在基本上不抑制一种或多种第二化学改性的分子负荷物102的生物缀合的情况下进行)。通过用多种不同的化学改性的分子负荷物102将一种或多种外泌体(例如,一种或多种初始外泌体202)官能化,一种或多种所得的外泌体脉管100可以表现出多种功能性(例如,治疗功能性和靶特异性递送)。
在1006处,方法1000可以包括通过外泌体将一种或多种化学改性的分子负荷物102递送到一种或多种生物细胞和/或组织。例如,在1006处的递送可以根据本文描述的递送过程600进行。在一个或多个实施例中,键合到一种或多种外泌体(例如,键合到一种或多种初始外泌体202)的一种或多种化学改性的分子负荷物102可以使得一种或多种外泌体脉管100能够靶向一种或多种特定生物细胞和/或组织,以递送一种或多种分子负荷物102。例如,分子负荷物102中的一种或多种可以包括可以被特异性地吸引到一种或多种感兴趣的生物细胞和/或组织的一种或多种抗原的一种或多种抗体。此外,一种或多种外泌体脉管100可以通过引发以下来递送一种或多种分子负荷物102:经由细胞内信号通路诱导可溶性信号转导;与一种或多种生物细胞和/或组织的质膜602融合,从而将一种或多种分子负荷物102转移穿过质膜602;和/或经由吞噬作用、微细胞溶质、受体介导的内吞作用和/或筏介导的内吞作用的内吞作用。例如,在一个或多个实施例中,一种或多种外泌体脉管100可以通过受体介导的内吞作用被内化到一种或多种生物细胞和/或组织中,其中位于外泌体脉管100的表面(例如,位于双层膜106上)上的一种或多种配体(例如,表面生物分子104和/或分子负荷物102)可以接合位于质膜602上的一种或多种细胞受体(例如,清道夫受体)。一种或多种分子负荷物102的递送可以促进一种或多种治疗性疗法,诸如:反义技术、核糖核酸("rna")干扰技术、剪接转换技术、基于信使rna的治疗剂、基于微rna的治疗剂、其组合等。
图11示出了根据本文描述的一个或多个实施例的示例、非限制性方法1100的流程图,该方法可以促进使用一个或多个外泌体脉管100运输和/或递送一个或多个分子货物102。为了简洁起见,省略了在本文所述的其他实施例中采用的类似元件的重复描述。
在1102,方法1100可以包括:基于位于一种或多种外泌体的双层膜106上并且与所述一种或多种外泌体的细胞质108相对的一种或多种表面生物分子104的组成,通过一种或多种分子探针702从多种外泌体中分离一种或多种外泌体。例如,在1102的分离可以根据本文描述的外泌体分离方法800进行。在一种或多种实施例中,一种或多种分子探针702可以包含在一种或多种芯片上探针700内,其中所述一种或多种分子探针702可以固定到一种或多种基质704。此外,一种或多种分子探针702可以包含与一种或多种基质704键合的第一部分706(例如,包含一种或多种核酸)和/或一种或多种分子探针702的第二部分708(例如,包含一种或多种抗体和/或抗原)。第二部分708可以与外泌体表面上的一种或多种表面生物分子104发生化学相互作用(例如,通过一种或多种生物缀合和/或抗体-抗原相互作用)。包含第二部分708的化学化合物可以具有与特定化学化合物键合和/或以其他方式相互作用的化学亲和力;由此,通过一种或多种分子探针702分离的外泌体可以是包含一种或多种特定化学化合物的外泌体(例如,根据本文描述的生物缀合反应和/或抗体-抗原相互作用)。例如,第二部分708可以包含一种或多种抗体和/或包含被一种或多种抗体靶向的一种或多种抗原的一种或多种外泌体,其可以被一种或多种分子探针702捕获,从而进行分离。在各种实施例中,芯片上探针700可以包含多种分子探针702,其包含不同的化学化合物,以分离具有不同表面组成的多种外泌体。
在1104处,方法1100可以包括用一种或多种分子负荷物102将表面官能化。例如,可以根据本文描述的第一缀合方案200、第二缀合方案400和/或第三缀合方案500进行官能化。例如,一种或多种分子负荷物102可以包含一种或多种核酸和/或蛋白质(例如,抗体和/或抗原)和/或一种或多种反应性官能团204(例如,胺反应性化合物、磷酸盐反应性化合物、羟基反应性化合物、抗体和/或抗原)。作为官能化的结果,可以将一个或多个分子团102以径向安排键合到一个或多个初始外排体202的表面上,以形成一种或多种外泌体脉管100。
图12示出了根据本文描述的一个或多个实施例的可以使用一个或多个外泌体脉管100来促进运输和/或递送一个或多个分子负荷物102的示例非限制性方法1200的流程图。为了简洁起见,省略了在本文描述的其他实施例中采用的类似元件的重复描述。
在1202,方法1200可以包括:基于位于一种或多种外泌体的双层膜106上并且与一种或多种外泌体的细胞质108相对的一种或多种表面生物分子104的组合物,通过一种或多种分子探针702从多种外泌体中分离一种或多种外泌体。例如,在1102的分离可以根据本文所述的外泌体分离过程800进行。在一种或多种实施例中,一种或多种分子探针702可以包含在一种或多种芯片上探针700内,其中一种或多种分子探针702可以固定到一种或多种基质704上。此外,一种或多种分子探针702可以包括与一种或多种基质704键合的第一部分706(例如,包括一种或多种核酸)和/或一种或多种分子探针702的第二部分708(例如,包括一种或多种抗体和/或抗原)。第二部分708可以与外泌体表面上的一种或多种表面生物分子104发生化学相互作用(例如,通过一种或多种生物缀合和/或抗体-抗原相互作用)。包括第二部分708的化合物可以具有与特定化合物键合和/或以其他方式相互作用的化学亲和力;由此,通过一种或多种分子探针702分离的外泌体可以是包括一种或多种特定化合物的外泌体(例如,根据本文所述的生物缀合反应和/或抗体-抗原相互作用)。例如,第二部分708可以包括一种或多种抗体和/或包括被一种或多种抗体靶向的一种或多种抗原的一种或多种外泌体,其可以被一种或多种分子探针702捕获,从而进行分离。在各种实施例中,芯片上探针700可以包括多种分子探针702,其包括不同的化合物,以分离具有不同表面组成的多种外泌体。
在1204,方法1200可包括将一种或多种分子负荷物102键合到位于双层膜106上并与细胞质108相对的一种或多种第二表面生物分子104。例如,在1204的键合可根据本文描述的第一缀合方案200、生物缀合方案300、第二缀合方案400和/或第三缀合方案500进行。例如,一种或多种分子负荷物102可包含一种或多种核酸和/或蛋白质(例如,抗体和/或抗原)和/或一种或多种反应性官能团204(例如,胺反应性化合物、磷酸盐反应性化合物、羟基反应性化合物、抗体和/或抗原)。此外,一种或多种第二表面生物分子104可包含一种或多种能促进与一种或多种反应性官能团204的化学相互作用(例如,共价键合和/或抗体-抗原相互作用)的官能团。示例性第二表面生物分子104可包括但不限于:蛋白质(例如,抗体和/或抗原)、磷脂、糖脂、核酸、多糖、糖、双层膜106的离域主链分子、酶、其组合等。由于键合,一个或多个分子负荷物102可以以径向排列键合到一个或多个分离的外泌体的表面,以形成一种或多种外泌体脉管100。
在1206,方法1200可以包括通过一种或多种外泌体(例如,一个或多个外泌体脉管100)将一种或多种分子负荷物102递送至一种或多种生物细胞和/或组织,其中所述一种或多种外泌体可以对一种或多种生物细胞和/或组织具有化学亲和力。例如,在1206的递送可以根据本文描述的递送过程600进行。在一个或多个实施例中,键合到一种或多种分离的外泌体(例如,键合到一种或多种初始外泌体202)的一种或多种分子负荷物102可以使一种或多种外泌体脉管100能够靶向一种或多种特定生物细胞和/或组织,以递送一种或多种分子负荷物102。例如,在1202,基于一种或多种外泌体对一种或多种生物细胞和/或组织的化学亲和力,可以分离一种或多种外泌体(例如,可以促进与一种或多种分子探针702的一种或多种化学相互作用的相同表面生物分子104也可以促进与一种或多种生物细胞和/或组织的一种或多种化学相互作用)。此外,一种或多种外泌体脉管100可以通过以下方式递送一种或多种分子负荷物102:经由细胞内信号通路诱导可溶性信号转导;与一种或多种生物细胞和/或组织的质膜602融合,从而将一种或多种分子负荷物102转移穿过质膜602;和/或经由吞噬作用、微细胞溶质、受体介导的内吞作用和/或筏介导的内吞作用的内吞作用。例如,在一个或多个实施例中,一种或多种外泌体脉管100可以通过受体介导的内吞作用被内化到一种或多种生物细胞和/或组织中,其中位于外泌体脉管100表面(例如,位于双层膜106上)的一种或多种配体(例如,表面生物分子104和/或分子负荷物102)可以接合位于一种或多种生物细胞和/或组织的质膜602上的一种或多种细胞受体(例如,清道夫受体)。一种或多种分子负荷物102的递送可以促进一种或多种治疗性疗法,诸如:反义技术、核糖核酸("rna")干扰技术、剪接转换技术、基于信使rna的治疗剂、基于微rna的治疗剂、其组合等。
此外,术语"或"意在表示包含性的"或"而不是排他性的"或"。也就是说,除非另外指定或从上下文清楚可见,否则"x采用a或b"意在表示自然包含性排列中的任一者。也就是说,如果x采用a;x采用b;或x采用a和b两者,那么"x采用a或b"在前述实例中的任一者下得到满足。此外,如在本说明书和附图中所使用的冠词"一"通常应被解释为表示"一个或多个",除非另外指定或从上下文清楚可见是针对单数形式。如本文中所使用,术语"实例"和/或"示例性"用于表示充当示例、实例或说明。为避免疑义,本文中所揭示的标的物不受此些实例限制。此外,本文中被描述为"示例"和/或"示例性"的任何方面或设计未必应被解释为比其它方面或设计优选或有利,也不意味着排除所属领域的技术人员已知的等效示例性结构和技术。
当然,出于描述本发明的目的而描述组件、产品和/或方法的每一可想到的组合是不可能的,但所属领域的技术人员可认识到,本发明的许多进一步组合和排列是可能的。此外,就在具体实施例、权利要求书、附录和图中使用术语"包含"、"具有"、"拥有"等来说,这些术语旨在以类似于术语"包括"的方式为包含性的,如"包括"在用作权利要求书中的过渡词时被解释。已出于说明的目的而呈现各种实施例的描述,但不旨在为详尽的或限于所揭示的实施例。在不脱离所描述的实施例的范围的情况下,许多修改和变化对于所属领域的技术人员将是显而易见的。选择本文所使用的术语以最佳地解释实施例的原理、对市场上发现的技术的实际应用或技术改进,或使所属领域的技术人员能够理解本文所揭示的实施例。
- 还没有人留言评论。精彩留言会获得点赞!