Scg3作为治疗靶标在制备治疗血管增生型或渗出型疾病的药物中的应用的制作方法
本申请是分案申请,其原申请的申请日为2016年5月6日、申请号为201610297883.6、发明名称为“定量配体组学技术在系统鉴别配体及配体疗法中的应用”。
本发明涉及用定量配体组学技术来系统地鉴别疾病相关的细胞配体、年龄相关的细胞配体以及受体特异性配体,并用它们作为靶标来开发各种配体疗法。分泌粒蛋白iii(secretograniniii,scg3)可作为靶标来开发配体疗法的各种药物,以治疗各种血管增生型疾病,包括糖尿病视网膜病变、糖尿病黄斑水肿、血管增生型糖尿病视网膜病变、血管增生型老年性黄斑病变和各种肿瘤。
背景技术:
细胞配体如胰岛素、血管内皮生长因子(vascularendothelialgrowthfactor,vegf)等是非常有价值的治疗靶标。有益的配体如胰岛素,可直接用于疾病治疗。而vegf在血管增生型疾病中是有害的配体,可通过阻断vegf来治疗疾病。与细胞内蛋白相比,细胞配体作为治疗靶标的优点是,它能在细胞外直接调控相对应的细胞表面受体,从而影响许多不同细胞的功能。然而,开发配体疗法的瓶颈是现有技术不能有效鉴别未知配体。而更为困难的是,如何预测哪些配体会在病理过程中起关键作用并有治疗价值。因此,有治疗价值的配体通常都是因个而异地被鉴别出来。在本发明之前,配体组学技术还从未被报道过,也不可能系统地鉴别所有能与细胞表面结合的配体、疾病特异性配体、年龄相关性配体或受体特异性配体,并系统地分析它们的治疗价值。
常规的噬菌体展示技术被广泛地应用于从抗体文库及多肽文库中鉴别有特异性结合功能的抗体和多肽。然而,这些鉴别出来的抗体和多肽并不是内源性配体,也不能提供病理机制及配体疗法的靶标。噬菌体展示技术只能从常规的cdna细胞蛋白文库中鉴别出高比例的错位读码框的非内源性与非正常多肽,其原因主要是细胞蛋白的读码框在噬菌体展示技术cdna文库读码框的不可预测性。因此,常规的噬菌体展示技术并不能用于鉴别真正的细胞配体。基于同样原因,尽管常规噬菌体展示技术可以与下一代基因测序方法(nextgenerationdnasequencing,ngs)相结合,但这一结合并不能鉴别真正的内源性配体,主要是因为蛋白读码框的不可预测性。
为解决这一难题,新开发的开放性读码框噬菌体展示技术(openreadingframephagedisplay,opd)能有效地鉴别具有特殊结合力和功能性的细胞蛋白,包括细胞配体及吞噬配体(caberoyetal.,j.mol.recognit.,23:74-83(2010);caberoyetal.,exp.cellres.,316:245-257(2010))。虽然已有研究人员将开放性读码框噬菌体展示技术与下一代基因测序相结合来鉴别细胞内蛋白与蛋白的相互作用(diniroetal.,nucleicacidsres.,38:e110(2010))。但是opd-ngs技术还没有被用来系统鉴别所有细胞配体、疾病特异性配体,受体特异性配体及年龄相关性配体。
目前的opd技术鉴别疾病特异性配体有如下困难:1)传统的筛选方法只能低效率鉴别被噬菌体展示技术提纯的细胞配体;2)并不能系统地测定所有鉴别出的配体的结合力和功能活性;3)并不能系统地鉴别哪些是疾病特异或年龄相关的配体。因此,目前所有已知的疾病相关的配体都是因个而异地被鉴别出来,快速可靠地挑选有治疗价值的配体来发展新的配体疗法十分困难。
scg3属于多功能分泌粒蛋白家族,在神经内分泌细胞及内分泌细胞中表达(taupenotetal.,n.engl.j.med.,348:1134-1149(2003))。该蛋白家族成员分泌粒蛋白ii(secretograninii,scg2)是一个分泌神经素(secretoneurin)的前体激素,而分泌神经素具有血管增生因子的活力(kirchmairetal.,circulation,109:777-783(2004))。然而,目前对scg3功能的了解是非常有限的。文献显示,scg3能从功能改变的胰腺β细胞中分泌出来。因此,该蛋白很有可能在一型糖尿病中被调高。此前的蛋白组学研究也显示,scg3也可以从激活的血小板中释放出来,并在动脉粥样硬化斑块中表达增高。而动脉粥样硬化是糖尿病血管病变的病症之一。scg3在多个肿瘤细胞中的表达也增高(wangetal.,cancerlett,352:169-178(2014))。scg3纯合子基因敲除小鼠没有任何表型异常(kinsleyetal.,emboj.,9:395-399(1990)),然而vegf杂合基因敲除小鼠在胚胎期死亡(ferraraetal.,nature,380:439-442(1996))。说明与vegf相比,scg3对正常血管及其它正常细胞功能的调控是非常低的。然而,scg3此前从未被报道过是一个血管内皮因子或其它细胞的配体。
技术实现要素:
鉴于以上问题,本发明的目的是提供提供新的方法来系统地鉴别所有细胞表面的配体、疾病相关配体,年龄相关配体及受体特异性配体。本发明的核心技术是将噬菌体展示技术,尤其是opd与ngs相结合来鉴别所有配体并定量测定它们的结合力及功能活性。定量比较整组配体组学数据将系统地鉴别疾病特异性配体、年龄相关性配体及受体特异性配体。
疾病特异性配体可能与发病机理有关,因此是开发新型配体疗法的理想靶标。过量表达有益的配体或特异阻断有害的配体能达到疾病治疗的目的。
具体实施方式之一,细胞结合力筛选采用配体组学技术系统地鉴别所有能结合到细胞表面的配体并测定它们的结合力。定量比较病理细胞和正常细胞的整组配体组学数据,能系统地鉴别疾病特异性配体。同样的,比较衰老的细胞和年轻的细胞也能系统地鉴别与年龄相关的配体。
另一个实施方式是噬菌体展示技术与细胞吞噬筛选相结合,去鉴别所有细胞的吞噬配体。筛选出的配体可被ngs系统地鉴别并测定它们的吞噬能力。定量分析病理与正常细胞的整组配体组学数据,能系统地鉴别疾病相关的细胞吞噬配体。同样的,比较衰老和年轻细胞的配体组学数据,能系统地鉴别年龄相关的细胞吞噬配体。
本发明中的细胞结合力和细胞吞噬筛选,可用于体内或体外实验。其中一个应用是体内噬菌体筛选技术系统地鉴别所有疾病相关的血管内皮因子或配体。血管内皮因子的筛选是基于它们在体内对不同器官血管内皮的结合力。定量配体组学技术能系统地鉴别所有血管内皮结合因子并测定它们的结合力。定量分析病理与正常器官的定量配体组学数据能系统地鉴别疾病相关的血管内皮因子或配体。同样地分析衰老的和正常的器官也能够鉴别出所有与年龄相关的血管内皮因子。
另一个实施方式是利用受体表达与受体不表达细胞,如受体基因敲除或受体基因沉默细胞进行噬菌体结合力筛选。所有细胞表面结合配体进一步被ngs鉴别,并测定它们的结合力。定量分析受体表达与不表达细胞的整组配体组学数据能系统地鉴别所有受体特异的配体。
相似的应用是细胞吞噬功能筛选与受体表达和不表达吞噬细胞相结合,筛选所有细胞吞噬受体。然后这些受体进一步被ngs鉴别并测定它们的吞噬能力。定量分析受体表达与不表达的吞噬细胞的所有配体组学数据,能系统鉴别受体特异的细胞吞噬配体。
附图说明
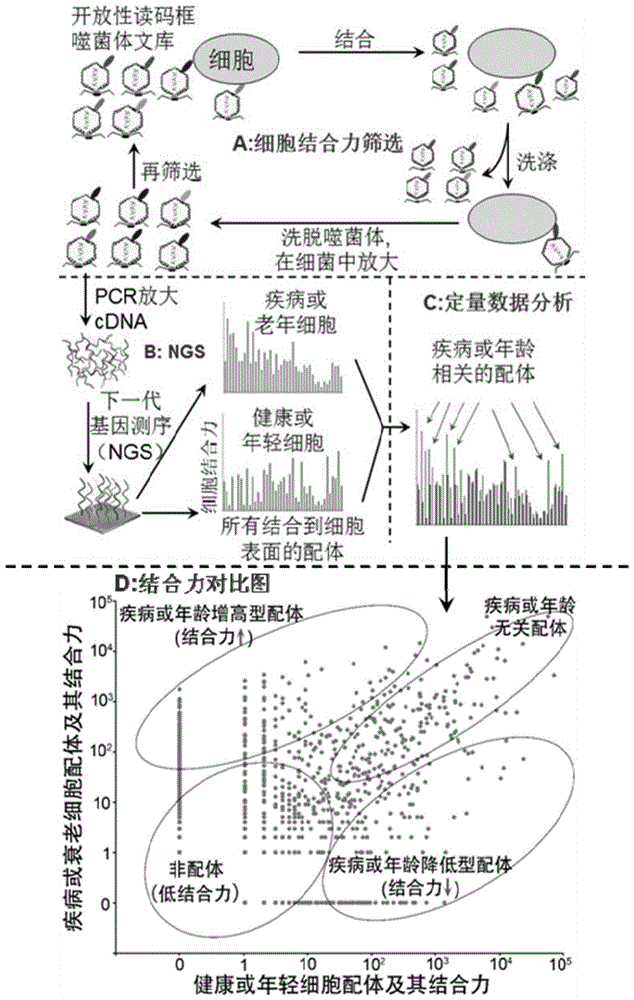
图1是配体组学技术系统鉴别疾病特异或年龄相关的细胞配体的示意图;其中,(a)表示噬菌体展示技术通过多轮细胞结合力筛选来挑选能结合到细胞表面的配体;(b)表示ngs鉴别所有筛选出的细胞配体:插入到噬菌体中的文库cdna通过聚合酶链反应(pcr)放大或限制性内切酶切割,并进一步被ngs鉴别;ngs鉴别出的cdna拷贝数直接与配体的亲合力相关;因此,配体组学技术能系统鉴别所有细胞表面结合的配体并测定它们的结合力;(c)表示定量分析疾病细胞与正常细胞的整组配体组学数据能系统鉴别疾病相关的配体;同样的,定量分析衰老与年轻细胞的整组配体组学数据,能系统地鉴别年龄相关的配体;(d)表示疾病与正常细胞的配体结合力对比或分析图,能进一步将所有鉴别的配体分成四类;在疾病细胞中结合力调高的配体称之为疾病增高型配体,在疾病细胞中结合力降低的配体称之为疾病降低型配体,亲和力在正常细胞与疾病细胞中没有变化的配体称之为疾病无关配体,亲和力很低的配体称之为假配体或非配体;同样的,结合力对比分析图也能将衰老细胞与年轻细胞的配体分成四类,包括年龄增高型配体、年龄降低型配体、年龄无关配体及非配体;本配体结合力分析图是一个示意图;
图2是配体组学技术用细胞吞噬功能来鉴别疾病特异或年龄相关的细胞吞噬配体的示意图;其中(a)表示多轮噬菌体细胞吞噬功能的筛选能筛出所有能被细胞吞噬的配体;(b)表示ngs系统地鉴别所有被筛选出来的吞噬配体;ngs鉴别出的文库cdna的拷贝数相当于配体的吞噬能力,因此,配体组学技术能系统地鉴别所有细胞表面的吞噬配体并测定它们的吞噬能力;(c)表示定量比较疾病吞噬细胞与正常吞噬细胞的整个配体组学数据,能系统地鉴别疾病相关的吞噬配体;同样的定量分析衰老与年轻吞噬细胞的整个配体组学数据能系统地鉴别出年龄相关的吞噬配体;(d)表示配体吞噬力活性分析图能将所有鉴别的配体分为四类:包括疾病增高型吞噬配体、疾病降低型吞噬配体、疾病无关吞噬配体及非配体,将相似的功能活力分析图应用于衰老与正常的细胞也能鉴别出年龄增高型吞噬配体、年龄降低型吞噬配体、年龄无关吞噬配体及非配体;本配体吞噬活力分析图是一个示意图;
图3是显示如何用配体组学技术在体内系统鉴别疾病特异或年龄相关的血管内皮因子或配体的示意图;其中,(a)表示多轮噬菌体体内结合力筛选能在不同的器官中筛出血管内皮因子或配体;(b)表示ngs能系统鉴别所有被筛出的配体,它们的cdna的拷贝数相当于配体细胞结合能力,因此,配体组学技术能系统地鉴别所有血管内皮因子并测定它们的结合力;(c)表示定量比较疾病与正常器官的整个配体组学数据,能系统鉴别出疾病相关的血管内皮因子;同样地,定量比较衰老的与年轻的器官的配体组学数据,也能系统地鉴别出年龄相关的血管内皮因子;(d)表示配体结合力分析图能进一步对比疾病与正常器官,并将所有鉴别的血管内皮因子分成四类:疾病增高型血管内皮配体、疾病降低型配体、疾病无关配体及非配体;同样的结合力分析图也能用于分析衰老与年轻的器官,并进一步将所有鉴别出的血管内皮因子分成年龄增高型血管内皮配体、年龄降低型配体、年龄无关配体及非配体;本配体结合力分析图是一个示意图;
图4是显示如何用配体组学技术在受体表达与受体不表达细胞上鉴别受体特异性配体;(a)表示多轮结合力筛选筛出细胞表面结合配体;(b)表示ngs系统地鉴别所有被筛出的配体并定量测定它们的结合活力;(c)表示定量比较受体表达与受体不表达细胞的整组配体组学数据能系统鉴别出所有受体特异性配体;(d)表示配体结合力分析图能进一步分析受体表达与不表达细胞,并进一步鉴别在受体表达细胞中结合力升高的受体特异性配体;本图是配体结合力分析示意图;
图5是显示如何用配体组学技术在受体表达与非表达的吞噬细胞上系统地鉴别受体特异性吞噬配体;其中,(a)表示多轮基于细胞吞噬功能的噬菌体筛选能筛出所有细胞表面的吞噬配体;(b)表示ngs能系统地鉴别所有被筛出的吞噬配体并测定它们的吞噬活力;(c)表示定量地比较受体表达与受体不表达的吞噬细胞的配体组学数据,能系统地鉴别受体特异的吞噬配体;(d)表示配体吞噬活力分析图能进一步对比受体表达与受体不表达吞噬细胞,并在受体表达细胞中鉴别出吞噬功能增强的受体特异性配体;本配体活力分析图是一个示意图;
图6是基于实验数据的真实的配体结合力分析图,以显示配体组学技术能在糖尿病小鼠中鉴别出疾病特异的血管内皮因子;如图3所示,配体组学技术在该实验中被应用到得了四个月糖尿病的小鼠与正常小鼠;图6的配体结合力分析图分析了所有被鉴别的血管内皮因子及它们对视网膜血管内皮的结合力,并鉴别了糖尿病特异的视网膜血管内皮因子;通过这一技术scg3和肝癌衍生的生长因子相关蛋白3(hepatoma-derivedgrowthfactorrelatedprotein3,hdgfrp3orhrp-3)被分别鉴定为糖尿病增高型配体和糖尿病降低型配体;结合力分析图的皮尔逊相关系数(pearsoncorrelationcoefficient)r=0.489;
图7是用各种不同的体外功能分析鉴定scg3是一个血管增生因子;其中,(a)表示用humanumbilicalveinendothelialcells(huvecs)细胞做分析的细胞增生实验,铺细胞在48孔板并与vegf165(50ng/ml),scg3(1μg/ml)或磷酸缓冲盐溶液(pbs)培育48小时,并计数每孔的细胞数(n=4);(b-d)小管形成试验(tubeformationassay)。huvec细胞与vegf(50ng/ml),scg3(300ng/ml)或pbs培育3小时;(b)表示小管形成实验的影像图;(c)表示定量分析图7b中小管形成的长度;(d)表示定量分析图7中小管分叉点数;(e)表示上皮细胞渗透实验示意图;(f)表示定量分析在24小时之内渗过的荧光素(fitc)标记的右旋糖酐(dextran,3kda);scg3,200ng/ml;vegf,100ng/ml;n=3;(g)表示westernblot分析scg3诱导的erk1/2蛋白激酶的激活,表皮细胞生长因子(egf)是阳性对照;scg3,1μg/ml;egf,100ng/ml,所有的数据平均值±s.e.m.,t检验。
图8是显示scg3是糖尿病增高型血管增生因子,而hrp-3是糖尿病降低型血管增生因子;角膜血管增生实验是在得了四个月糖尿病的小鼠和正常小鼠上进行;小片滤纸预先浸在scg3(250ng/μl),hrp-3(1μg/μl),vegf(100ng/μl)或pbs溶液,然后将预浸过的滤纸移植到角膜内,诱导血管增生,一共六天时间;(a)表示典型的角膜血管增生图片;(b)表示dii荧光染料标记的角膜血管;(c-e)表示在角膜内移植了血管增生因子六天后,定量分析角膜血管增生;(c)表示角膜血管枝数;(d)表示角膜血管的分叉节点数;(e)表示总体血管增生指数;*显示血管增生因子所浸透的滤纸移植的位置;每组角膜样品数显示在图标的下方,平均值±s.e.m;单因素方差分析((one-wayanovatest);
图9是显示抗scg3抗体治疗能缓解糖尿病小鼠眼视网膜血管渗透;其中,(a)表示亲和力纯化过的抗scg3抗体可以抑制scg3诱导的人视网膜微血管上皮细胞(humanretinalmicrovascularendothelialcells,hrmvecs)增生;该细胞培养于96孔板内,并加入scg3(1μg/ml),anti-scg3ab(2μg/ml),scg3加抗体或pbs对号(n=8);(b)表示抗scg3抗体治疗能缓解糖尿病小鼠视网膜血管渗出;亲和力纯化过的抗scg3抗体或对照抗体(0.36μg/1μl/眼)(n=5)打入小鼠一只眼睛的玻璃体内,另一只眼睛注入pbs生理盐水对照;在治疗四小时后,静脉注射伊文思蓝(evensblue),分析视网膜血管渗透量。数据在对照pbs标准化后,表达成减少渗透的百分比,n=5;平均值±s.e.m.,单因素方差分析;
图10是显示抗scg3抗体治疗能改良脉络膜新生血管形成(choroidalneovascularization,cnv);用激光诱导脉络膜血管增生(4点/眼),7天后在一只小鼠的眼睛注射亲和力纯化过的抗scg3抗体(0.36μg/1μl/眼),另一只眼注射pbs对照;14天后,用荧光素血管照影分析脉络膜血管相关的视网膜渗出;
图11是配体组学技术的实际实验数据鉴别scg3是一个肿瘤增高型配体血管内皮因子或配体;配体组学技术的分析如图3所示;在正常与视网膜母细胞瘤(retinoblastoma,rb)小鼠上进行定量配体组学分析,鉴别所有的血管内皮因子;用结合力分析图来定量比较rb与正常视网膜相关的血管内皮配体组学数据,并分析出肿瘤相关的配体;皮尔逊相关系数r=0.860。
具体实施方式
下面结合附图对本发明的具体实施方式做进一步详细的说明,但不应以此限制本发明的保护范围。
本发明用不同噬菌体筛选技术、细胞类型,结合opd和ngs,达到用定量配体组学技术来系统鉴别不同性质配体的目的。包括所有能结合到细胞表面的配体,疾病相关的配体、年龄相关的配体和受体特异性配体,来发展新型的配体疗法用于治疗各种疾病。
本发明的一个实施方案(图1)是通过多轮细胞结合力的噬菌体筛选来鉴别细胞配体。在这一方法中将所要选择的细胞和噬菌体文库一起培育。结合到细胞表面上的噬菌体可以被洗脱下来,通过细胞裂解、改变ph值,或者蛋白酶的切割释放出来。释放出的噬菌体可以在细菌里放大,用作新一轮的筛选给料。经过几轮筛选,噬菌体中插入的cdna文库,可以用pcr放大或限制性内切酶切出,并被ngs鉴别。ngs分析筛选出的噬菌体样品,可鉴别几百亿个插入的文库cdna。因此,所有被筛选出的配体都能被ngs鉴别。同时,cdna的拷贝数也相当于相关配体的相对细胞结合力。因此,配体组学技术能系统地鉴别所有细胞表面的配体,并同时测定它们的相对细胞结合力。定量分析病理细胞和正常细胞的所有配体组学数据组,能系统鉴别出疾病特相关的细胞配体。结合力分析图能进一步比较疾病细胞和正常细胞,从而把所有鉴别出的配体分为四类。病理细胞表面结合力增强的配体称之为疾病增高型配体,病理细胞表面结合力降低的配体称之为疾病降低型,对正常细胞和病理细胞结合力没有变化的称之为疾病无关配体。结合能力非常低的配体称为非配体。同样地,定量比较衰老细胞和年轻细胞的所有配体组学数据,能系统地鉴别出年龄相关的细胞配体。结合力分析图能进一步比较老年细胞和年轻细胞,并将所有鉴别出的配体分类成年龄增高型配体、年龄降低型配体、年龄无关配体和非配体。
本发明的另一个实施方案是通过多轮的细胞吞噬功能筛选来筛出表达吞噬配体的噬菌体(图2)。所有被筛选出的配体的cdna也同样可以被ngs鉴别。在这一实施方案中,ngs所鉴别出文库cdna的拷贝数相当于所鉴别配体的吞噬活力。因此,配体组学技术能系统鉴别所有细胞表面的吞噬配体,并同时测定它们的吞噬功能活力。系统地比较疾病吞噬细胞和正常吞噬细胞的所有配体组学数据,将系统地鉴别疾病相关的吞噬配体。吞噬功能活力分析图能进一步对比疾病细胞和正常细胞的吞噬配体,并进一步将它们分类成在疾病细胞中吞噬功能升高的疾病增高型吞噬配体,在疾病细胞中吞噬功能降低的疾病降低型吞噬配体,在疾病细胞和正常细胞中功能没有变化的疾病无关吞噬配体,吞噬功能很低的配体称之为非配体。同样的实施方案定量比较老年吞噬细胞和年轻吞噬细胞的所有配体组学数据,进一步鉴别与年龄相关的吞噬配体。定量吞噬功能活力分析图能比较年老细胞和年轻吞噬细胞,并将所有鉴别的配体分类成年龄增高型吞噬配体、年龄降低型吞噬配体、年龄无关吞噬配体及非配体。
配体组学技术能广泛地应用到体内和体外的不同细胞。如图3所示,多轮体内亲和力筛选能筛出血管内皮结合配体,所筛出的配体能进一步被ngs鉴别。定量分析疾病器官和正常器官的所有配体组学数据,能系统地鉴别出疾病相关的血管内皮因子或配体。配体结合力分析图能进一步比较疾病与正常的细胞或器官,并进一步把所有鉴别出的血管内皮因子或配体分类成疾病增高型配体、疾病降低型配体、疾病无关配体和非配体。同样的应用也能通过配体组学技术分析比较老年器官和年轻器官的配体组学数据,并进一步鉴别出所有与年龄相关的血管内皮因子。配体结合力分析图能进一步比较老年器官和年轻器官,从而将所有鉴别出的血管内皮因子分成年龄增高型配体、年龄降低型配体、年龄无关配体及非配体。本发明将通过两个实例展示配体组学技术如何能系统地鉴别糖尿病特异的或肿瘤特异的血管内皮因子,进一步阐述它们的毒理机制,并通过研发配体疗法,达到治疗疾病的目的。
本发明的另一个应用是通过配体组学技术来分析受体特异性配体(图4)。通过选用表达或不表达特定受体的细胞,多轮细胞结合力筛选能筛出细胞表面所有配体。所有被筛出的配体可被ngs鉴别并同时测定它们的细胞结合力。定量分析受体表达与受体不表达细胞的所有配体组学数据,能系统地鉴别出受体特异性配体。
本发明的另一个类似实施方案是将配体组学技术用来鉴别受体特异性吞噬配体(图5)。通过选用表达或不表达特定受体的吞噬细胞,多轮细胞吞噬功能筛选能选出所有细胞表面的吞噬配体。所有被筛选出的吞噬配体可用ngs鉴别并测定它们的吞噬功能活力。定量分析所有受体表达与受体不表达细胞的配体组学数据能系统地鉴别出受体特异性吞噬配体。
疾病增高型配体对疾病细胞的结合力是增加的,这是因为它们相对应的受体在疾病细胞表面的表达也增加了。因此,它们调控疾病细胞的能力也增强了。反之,疾病降低型配体的受体在疾病细胞表面表达降低,对疾病细胞的调控能力也因此减弱,利用它们进行疾病治疗也要难得多。因此,疾病增高型配体比疾病降低型配体或疾病不变型配体更具有作为治疗靶标的价值。有益的配体可直接用于疾病治疗。而抑制有害的配体也可治疗疾病。
同样的年龄增高型配体能更多地结合到老年细胞表面是因为它们的受体在老年细胞表面表达增高。因此,年龄增高型配体比年龄降低型配体或年龄不变型配体具有更多的治疗价值。如果年龄增高型配体是一个有益的配体,则可直接被用来做药物治疗。如果年龄增高型配体是一个有害益的配体,阻断它们的功能则可被用来治疗老年性疾病。
定量配体组学技术可用来分析所有正常和疾病的细胞。举例来说,配体组学分析可用来研究肿瘤细胞和正常细胞的不同,从而鉴别出肿瘤特异的细胞配体。肿瘤增高型配体更多地结合到肿瘤细胞表面是因为它们的受体在肿瘤细胞表面表达增加。因此它们对肿瘤生长的调控,如细胞凋亡、细胞增殖、细胞存活、细胞分化、细胞黏着都可被进一步研究。如果细胞肿瘤增高型配体具有保护作用,比如造成肿瘤细胞凋亡,那么这些配体可直接用来进行肿瘤治疗。如果肿瘤增高型是有害的配体,比如能增加肿瘤细胞繁殖速度,抑制这些有害的配体也能用来治疗肿瘤。同时,配体组学技术能分析干细胞和分化细胞的不同,来进一步鉴别干细胞特异的配体。
任何分离出来的细胞,比方说各种各样细胞系、原代细胞都可用来在体外进行定量配体组学分析。生物体内的细胞,比如血管内皮细胞,也可以在活体动物上,如活体小鼠上,进行配体组学分析,如本发明中的两个实施例。定量配体组学技术也能被用于分离出的组织或器官,再通过细胞结合或吞噬来筛选特定的细胞配体。
开放性读码框噬菌体展示技术的cdna文库应该是作为定量配体组学技术应用的最佳选择。而传统的噬菌体展示技术的cdna文库,不但含有正确读码框,还含有高比例的非正确读码框克隆。虽然它们也能用来做配体组学分析,但高比例的非正确读码框的噬菌体克隆能干扰内源性配体的鉴别。因此,普通的噬菌体展示技术用一般的cdna文库去鉴别内源性细胞配体的效率是非常低的。
噬菌体展示技术可以用各种不同的噬菌体,如线状噬菌体(filementousphage,包括m13,fl和fd噬菌)、t7噬菌体,lamda噬菌体和t4噬菌体。开放性读码框cdna文库可直接构建到这些不同噬菌体的载体中,并结合ngs来直接进行定量配体组学分析,从而系统地鉴别细胞表面所有的配体,疾病相关配体、年龄相关配体和受体特异性配体。
应当理解,上述详细说明和下述实施例只是为了描述与示范,而不应理解为是对本发明范围的限制。对于本领域技术人员而言显而易见的是,在不背离本发明精神和范围的情况下,可以对所公开的实施方案作出许多变化和修改。此外,此处引用的所有专利、专利申请和出版物均以参考的方式再次引入。
实施例1:系统鉴别糖尿病视网膜病变特异性血管内皮配体或因子
全球糖尿病患者有三亿七千八百万,其中有九千三百万人患糖尿病视网膜病变(diabeticretinopathy,rd)。糖尿病视网膜病变是一个主要的致盲原因,其中包括糖尿病黄斑水肿(diabeticmacularedema,dme)和增生型糖尿病视网膜病变(proliferativediabeticretinopathy,pdr)。全球有二千一百万糖尿病黄斑水肿患者与一千七百万增生型糖尿病视网膜病变患者。
糖尿病视网膜病变的临床特征是血管通透性增加、内皮细胞死亡、无细胞毛细血管增加、白细胞淤滞、晚期的血管增生、视网膜出血及视力减退。兰尼单抗(lucentis,ranibizumab)在2012年被美国fda批准做为第一个抗血管增生型治疗dme的药物。临床试验证明lucentis治疗dme的疗效介于21%到37%之间。lucentis的上市引发了一场用抗血管内皮增生因子vegf来治疗糖尿病黄斑水肿的研发热潮。随后开发的药物阿柏西普(eylea,aflibercept)和康柏西普(conbercept)是vegf诱饵受体(decoyreceptor)。其它抗vegf的治疗药物还包括avastin(bevacizumab)和macugen(pegaptanib)。这些研究证明抗血管生成疗法是一个有效的治疗糖尿病黄斑水肿的方法。但抗vegf的疗效是有限的。下一个研究的热点是如何发现新的有效的血管形成因子并作为治疗靶标,研发出新的抗血管渗出或增生疗法来治疗糖尿病黄斑水肿及增生型糖尿病视网膜病变。
如图3显示,本发明的一个实施例是用配体组学技术来鉴别糖尿病视网膜病变特异的血管增生因子,并开发出抗血管生成疗法来治疗糖尿病黄斑水肿及增生型糖尿病视网膜病变。
体内细胞结合力筛选:
用链脲霉素(streptozotocin,stz)诱导小鼠糖尿病,将stz(50μg/g体重,连续五天)腹腔注射到小鼠(c57bl/6,6周大),来杀死胰岛细胞,诱导小鼠糖尿病。如小鼠的血糖高于350mg/dl,则认为小鼠得了糖尿病,一般小鼠在注射stz之后2-4个星期,将会得糖尿病。在得了糖尿病4个月后,小鼠将被用来做配体组学分析。
两个用小鼠胚胎和小鼠眼睛构建的噬菌体开放读码框cdna文库(opdlibraries)在以前的文献中被描述(leblancetal.,plosone,10:e0127904(2015))。这两个文库在细菌中放大并用cscl纯化,用pbs经过透析后测定噬菌体滴度(空斑形成单位,pfu)。相同滴度的这两个文库进行合并之后,直接静脉注射到4个月的糖尿病小鼠和对照小鼠中(~1x1012pfu/小鼠),进行体内噬菌体结合力筛选。经过20分钟血循环之后,未结合到血管内皮细胞的噬菌体,通过心脏灌流而洗出体外。结合到视网膜血管内皮细胞的噬菌体将和视网膜一同被分离出来。分离出的视网膜在含有1%tritonx-100的pbs溶液中匀浆以释放结合到血管内皮的噬菌体。释放出的噬菌体经过噬菌斑测定(plaqueassay)之后,在细菌中放大,并用做下一轮筛选的给料。经过3轮体内结合力筛选,所有被筛出的噬菌体克隆的外源性插入cdna,被pcr放大,并被ngs鉴定。为测定体内结合力筛选及定量的可靠性,构建了两个分别展示人vegf(vegf-phage)和绿色萤光蛋白(greenfluorescentprotein,gfp-phage)的单克隆噬菌体。这两个克隆被以同样的比例1:1,000稀释到噬菌体文库中。然后将这一混合的文库用来做噬菌体体内筛选。经过3轮体内筛选之后,拥有非小鼠密码子的vegf-phage和gfp-phage能被ngs从小鼠噬菌体文库中鉴别出来并定量测定它们的结合力。
配体组学数据分析:
实验结果显示一共有489,126和473,965个有效的文库cdna被ngs从糖尿病和正常的视网膜中鉴别出来,并匹配到1,548和844个在ncbiccds文库中的蛋白(表1)。
ngs鉴别出的cdna拷贝数相当于对应配体的血管内皮结合力。经过3轮体内筛选,gfp-phage相对减少及vegf-phage相对增多(表1)。这一结果证明了配体组学技术能定量地测定它们的血管内皮结合力。这一结果也证实了gfp-phage可以用来做为背景对照或非配体的对照(图6)。
表1定量配体组学技术鉴别糖尿病眼病(dr)特异的血管内皮因子
注:*p<0.001,dr与对照对比,卡方检验。结合力比例=(dr+1)/(对照+1)。
配体血管内皮结合力在糖尿病视网膜病变中总体变化在经过配体结合力对比图得到进一步分析(图6)。结果显示,整个配体组学的血管内皮结合力在4个月的糖尿病小鼠中显著地改变,皮尔逊相关系数等于0.489。大量的疾病增高型和疾病降低型血管内皮因子被鉴别出来,显示它们相对应的受体在血管内皮细胞表面表达相对应地升高或降低。卡方检验统计学处理(chi-squaretest,χ2test)定量比较糖尿病与正常视网膜血管内皮的整组配体组学数据总共鉴别了277个疾病增高型和89个疾病降低型血管内皮配体。
并非所有鉴别出的血管内皮配体都是血管增生因子。有些配体可能调控细胞凋亡或炎症反应。举例来说,鉴别出的两个糖尿病相关的血管内皮配体是淀粉样前体蛋白(amyloidprecursorprotein,app)和c1qb。从app中释放出的贝塔淀粉样蛋白(β-amyloid)是一个已知的血管内皮配体,直接作用于rage受体(receptorforadvancedglycationendproducs,晚期糖基化终产物受体)。而rage受体的表达在糖尿病血管内皮上是增高的。c1qb是补体1q的β亚单位,c1q至少有两个血管内皮受体,cc1qr和gc1qr/p33。这两个受体的激活都能产生炎症性细胞活素(proinflammatorycytokines)。前期结果研究显示c1q在动脉粥样硬化位点上的表达是增高的。而动脉粥样硬化是糖尿病血管症状的病症之一。因此,c1qb和app的鉴别进一步证实了定量配体组学技术能系统地鉴别糖尿病相关的血管内皮因子。
scg3被鉴别为一个新型的血管增生因子:
scg3被定量配体组学技术鉴别为糖尿病增高型配体。scg3对正常血管的结合力非常低,不能被配体组学技术所检测。但scg3对糖尿病视网膜血管的结合力增高至少1,731倍(图6,表1),显示scg3是一个高度疾病特异的血管内皮配体。人的scg3genbankaccession号是nm_013243与mn_001165257;小鼠的scg3genbankaccession号是nm_009130与nm_00164790。
作为具体实施例,本发明进一步用几种不同的体外实验证实scg3是一个血管增生因子。这些体外实验包括血管内皮细胞增殖实验、小管形成实验、内皮细胞渗透实验(图7a-7f)。在内皮细胞增生实验中,人脐带血管内皮细胞(huvecs)在48孔板中与vegf165(50ng/ml),scg3(1μg/ml)或pbs培育48小时。计算每孔细胞的数量。结果显示scg3能增加内皮细胞增生(图7a)。同样的实验结果在人视网膜微血管内皮细胞(hrmvecs)也得到了证实(图9a)。在小管形成实验中,将基质胶(matrigel)铺于96孔板内,然后将huvec细胞铺在基质胶上,并与vegf(50ng/ml),scg3(300ng/ml)或pbs培育3小时。照相分析细胞形状并定量小管形成长度和小管分叉节点数。结果显示scg3能增加小管形成(图7b-c)。在内皮细胞渗透试验中,将huvec细胞铺于半透膜上培育至细胞全部融合。然后将scg3(200ng/ml),vegf(100ng/ml)或pbs对照加入到细胞上的培养液中。同时将荧光素标记的右旋糖酐(3kda)加入到半透膜下的细胞培养液。培育24小时后,吸取上层培养液,并定量渗透过单层细胞的荧光素。结果显示scg3能增加内皮细胞渗透。同时信号传递研究显示scg3能在huvec细胞中激活erk1/2蛋白激酶。这些实验结果显示scg3是一个血管增生因子。
scg3是一个糖尿病视网膜病变(dr)增高型血管内皮生长因子:
scg3在本实施实例中被定量配体组学技术鉴别为疾病增高型血管内皮因子或配体(图6)。同时hrp-3被鉴别为疾病降低型血管内皮因子。体内角膜血管增生实验进一步比较了它们在糖尿病和正常小鼠中不同的血管增生活力。将小片滤纸(0.125mm2/片)预先在hrp-3,vegf和pbs的溶液中,在4℃浸泡2小时。浸泡过的滤纸直接移植到c57bl/6小鼠(8-10周大)角膜夹层内(1个滤纸/角膜;2个滤纸/小鼠)。6天后,用裂隙灯显微镜照相分析每只角膜血管增生情况。测定每只角膜的血管数量及血管的分枝节点数目。同时测定角膜血管增生的综合指数来确定每只角膜的血管数量、血管密度和血管长度。小鼠吸入co2死亡后,用dii荧光染料通过心脏灌流标志所有的血管(图8)。
对比糖尿病小鼠与正常小鼠结果显示,scg3在糖尿病小鼠中促进血管增生能力显著增高(图8)。显示scg3是一个真正的疾病增高型血管内皮生长因子。相对应的是,hrp-3的结果显示它的血管增生活力刚好相反,只能刺激正常小鼠的血管增生,而没有任何刺激糖尿病小鼠血管增生的活力。然而vegf的血管增生活力在糖尿病小鼠与正常小鼠中几乎一样,没有变化。这些实验结果显示,在糖尿病小鼠和正常小鼠中scg3、hrp-3和vegf有三种非常不同类型的刺激血管增生的活力。这些结果进一步说明定量配体组学技术的可靠性以及可做为一个新工具来系统地鉴别疾病特异的细胞配体。这些实验数据也进一步提示scg3和vegf能通过不同的受体来调控血管增生。因此,可以通过抑制这两种不同的血管增生因子来达到交替治疗或结合治疗的目的,以进一步增加治疗糖尿病眼病、糖尿病黄斑水肿和增生型糖尿病视网膜病变的临床疗效。
糖尿病视网膜病变配体疗法的基础设计:
vegf的抑制剂如兰尼单抗(lucentis)和阿柏西普(eylea)已被美国食品药品管理局批准用于糖尿病黄斑水肿的临床治疗。因此,本实施例也研究了scg3作为疾病增高型血管内皮生长因子对糖尿病视网膜病变的治疗价值。亲和力纯化过的抗scg3抗体能直接抑制scg3诱导的hrmvec的细胞增殖(图9a)。伊文思蓝实验验证了抗scg3抗体能抑制糖尿病小鼠视网膜血管渗出。简而言之,抗scg3抗体和对照抗体(0.36μg/1μl/眼)直接打到糖尿病小鼠眼睛的玻璃体内,pbs对照打到对侧眼睛。一个半小时之后,伊文思蓝静脉注射,并在小鼠体内循环2.5小时。通过心脏灌流洗出血管内所有伊文思蓝。分离小鼠视网膜并提取伊文思蓝,超速离心后直接测定伊文思蓝的浓度。所得结果与对测眼睛的pbs进行比较。与对照抗体相比,抗scg3抗体能在糖尿病小鼠中减缓视网膜血管的渗透(图9b)。这一结果显示scg3是一个非常有价值的配体靶标,能用来开发新的抗血管渗透或生成疗法来治疗糖尿病视网膜病变、糖尿病黄斑水肿和增生型糖尿病视网膜病变。
新生血管型老年性黄斑病变及抗scg3治疗:
老年性黄斑病变(age-relatedmaculardegeneration,amd)是一个主要的致盲病。到2020年,全球将有一亿九千六百万老年性黄斑病变患者。到2040年,将达二亿八千八百万。血管增生型老年性黄斑病变(neovascularamd)在临床的特征是脉络膜新生血管增生(choroidneovascularization,cnv)。这一疾病影响大约10%-15%的amd患者,但是却能在amd病人中造成90%有严重视力衰退的疾病案例。血管生长因子在血管增生型老年性黄斑病变的病理机制中有着重要的作用。
多个抗vegf药物如lucentis和eylea已经被批准用于血管增生型老年性黄斑病变和糖尿病黄斑水肿的临床治疗。由于上面的实验结果显示,抗scg3抗体能抑制糖尿病小鼠的视网膜血管渗出。因此,抗scg3抗体也有可能被用来在小鼠上治疗脉络膜新生血管增生(cnv)。
在c57bl/6小鼠(7-8周大)上,用激光诱导脉络膜新生血管增生,做为血管增生型老年性黄斑病变的动物模型。所用激光是二极管激光(75-μm每斑,0.1秒时间长,110mw)。每个视网膜上打4个激光斑。激光打击后视网膜有小泡凸起。7天之后,亲和力纯化的抗scg3抗体(0.36μg/1μl/眼)或pbs直接注射到小鼠眼睛的玻璃体内,对照眼注射pbs溶液。14天后,用荧光素血管照影方法直接测定由脉络膜血管增生引发的视网膜血管渗出。荧光素直接注入小鼠的腹腔内。注入荧光素十分钟后进行荧光素血管照影检测。结果显示,抗scg3抗体能够缓解脉络膜血管增生(图10)。该实验显示,scg3是一个有价值的配体靶标,能用于抗血管增生疗法来治疗血管增生型老年性黄斑病变。
实施例2系统鉴别肿瘤特异的血管内皮和因子
本发明的另一个实施方案和应用示例是,将配体组学技术应用于肿瘤小鼠,并系统地鉴别出肿瘤特异性血管内皮细胞。并在体内直接鉴别肿瘤相关的血管内皮因子。
许多血管增生因子已被证明在肿瘤的生长中能促进血管增生,对肿瘤的生长起着决定性作用。好多血管增生因子和血管抑制因子已被鉴别出来,有几个已经被美国食品药品管理局批准,用于肿瘤的抑制血管增生疗法。然而,由于各种技术困难,所有已知的血管内皮因子都是通过各种各样的方法因个而异地鉴别出来。因此,不知道还有多少肿瘤相关的血管内皮配体或因子需要被鉴别并用于肿瘤治疗。同时这一困难也限制了我们进一步开发新型肿瘤配体疗法的能力。本实施例将用配体组学技术系统地鉴别肿瘤特异性血管内皮因子来进行新型配体疗法的基础设计。
配体组学的体内结合力筛选:
本实施例采用视网膜母细胞瘤(retinoblastoma,rb)作为一个肿瘤病例,rb是最常见的小儿眼内肿瘤。转基因小鼠表达sv40t抗原,会自发地形成rb。这些视网膜母细胞瘤小鼠被用来做肿瘤模型,来展示定量配体组学技术能系统地鉴别肿瘤特异性血管内皮因子,并用于肿瘤治疗。
rb的转基因小鼠可用基因型鉴定来确定。rb可在8周大的转基因小鼠上通过眼底检查的方式来证实。体内噬菌体结合力筛选试验可在16周大的rb小鼠和正常小鼠上来进行血管内皮因子的筛选,如示例1(图3)。总共进行了3轮的体内结合力筛选,所有被筛出的肿瘤血管和正常血管内皮细胞结合配体,通过ngs来测定。所鉴别的文库cdna的拷贝数相当于对应配体的血管内皮相对结合力。
定量配体组学技术分析:
配体组学分析的结果显示共有703,279和725,793个cdna序列被ngs在rb和对照视网膜上检测出来。这些基因序列配比到ncbiccds文库中的1,857和1,137个蛋白(表2)。定量分析rb和对照视网膜上所有被鉴别出的配体及它们的结合力,系统地分析出了所有视网膜母细胞瘤特异的血管内皮配体。配体血管内皮结合力在糖尿病视网膜病变中总体变化在经过配体结合力对比图得到进一步分析(图11)。这些结果显示,整个配体组学的血管内皮结合力在4个月的糖尿病小鼠中显著地改变,皮尔逊相关系数r=0.860。其中包括222个结合活力在rb血管内皮升高的rb增高型配体及77个在rb血管内皮结合力降低的rb降低型配体(p<0.001,χ2test)(表2)。
表2定量配体组学技术鉴别视网膜母细胞瘤(rb)特异的血管内皮因子
注:*p<0.001,rb与对照对比,卡方检验。结合力比例=(rb+1)/(对照+1)。
在表1和表2中的定量配体组学分析,揭示了视网膜母细胞瘤和糖尿病视网膜病变之间相似与不同的变化。举例来说,在这两种疾病中scg3的结合力在疾病内皮细胞上都增加了。与视网膜母细胞瘤血管增生相比,糖尿病视网膜病变血管内皮会产生凋亡跟无内皮细胞微细血管(acellularcapillaries)。因此,血管增生对糖尿病眼病来说是一个晚期的作用。因此,hrp-3在糖尿病视网膜病变血管内皮结合力的降低有可能会造成血管内皮凋亡。因此,延缓scg3诱导的血管增生。反之,scg3和hrp-3两个配体结合力在视网膜母细胞瘤rb血管内皮上的结合力都增加,说明它们都有可能参与刺激肿瘤血管增生。这意味着,抑制这两个血管增生因子都有可能治疗rb肿瘤。但在糖尿病视网膜病变中抑制这两个受体却对血管内皮细胞凋亡和增生有不同的影响。这些数据显示,定量配体组学技术能系统地分析疾病相关的血管内皮因子,来进一步了解它们对疾病发病机制的调控,并系统地鉴别治疗靶标。这一方法也能用来系统地分析不同肿瘤之间配体组学结合力的变化,并系统地发现肿瘤特异血管内皮因子。同样地,这一方法能够用来系统地鉴别同一个肿瘤在不同阶段的配体组学结合力的变化,来达到系统地鉴别阶段特异的肿瘤血管内皮因子。特殊阶段的血管内皮因子能用来开发出阶段特异的抑制血管增生肿瘤疗法。
抗血管生成的肿瘤疗法的基础设计:
抗血管生成是一个非常重要的肿瘤治疗方法。scg3对正常血管的结合力非常低,不能被配体组学技术所检测。但scg3对rb血管内皮的结合力增高至少198倍(表2)。scg3有可能是非常特异的肿瘤血管生长因子,来诱导视网膜母细胞瘤的血管增生。同样的作用也有可能发生在其它肿瘤上。因此,不同的抗体包括人性化的单克隆抗体、单链抗体(scfv)来抑制scg3有可能达到抗血管增生的肿瘤治疗的目的。同样的,各种各样的小分子化合物、多肽、核苷酸适体也能用来抑制scg3对血管内皮的结合与功能调控,达到治疗视网膜母细胞瘤和其它各种肿瘤的目的。scg3具有的特点是在正常血管中它的刺激血管增生的活力几乎是零(图8,表1,表2)。但它的受体表达在肿瘤血管内皮上是大幅增加的(表2)。以前的研究提示scg3本身的表达在肿瘤细胞中也是被调高的。因此,scg3是一个非常有价值的抑制血管增生的配体可用来治疗各种肿瘤。这个一疗法对正常血管内皮的副作用可能很低,能选择性地抑制肿瘤生长。
同样的,各种抗体、小分子化合物、多肽、核苷酸适体能特异性抑制scg3血管内皮结合力和功能调控的,都有可能用来抑制血管增生,达到治疗糖尿病黄斑水肿、增生型糖尿病视网膜病变、血管增生型老年性黄斑病变和各种肿瘤。这一疗法对正常血管内皮的副作用可能很低。其它类似的方法,如小干扰核糖核酸(sirna)、小发夹rna(shrna)和微rna(mirna)也能用来特异性地基因沉默scg3的表达来抑制血管增生,达到治疗糖尿病黄斑水肿、增生型糖尿病视网膜病变、血管增生型老年性黄斑病变和各种肿瘤。同样的,scg3也能被用来做为血管生长因子来诱导血管增生,治疗缺血性疾病如糖尿病脚病、缺血性中风、冠状动脉疾病或慢性组织损伤。
- 还没有人留言评论。精彩留言会获得点赞!