缓释抗逆性益生菌晶球及其制备方法与流程
本发明属于益生菌技术领域,具体涉及缓释抗逆性益生菌晶球及其制备方法。
背景技术:
益生菌是一类定植于人体肠道、生殖系统内的对宿主有益的活性微生物。益生菌通过调节宿主黏膜与系统免疫功能或通过调节肠道内菌群平衡,起到促进营养吸收、防治肠道相关疾病、增强机体免疫力和延缓衰老等生理作用,进而产生健康功效并改善宿主的健康状况。
目前在传统生产益生菌,尤其是干燥过程以及储存过程中,由于益生菌本身的特性,容易造成有效益生菌活菌的大量损失,进而需要提高生产成本,同时也会造成生产资料浪费的问题;而且在服用益生菌后,益生菌进入肠道要经历胃酸的低ph环境,还要经历小肠的弱碱环境以及胆盐等消化液,能够保持活性到达小肠末端及大肠定殖的活性益生菌极少。
因此,能够提高益生菌在生产、真空冷冻干燥、后期储存过程中及不良环境中存活率方法或技术是非常重要的,以此来增加最终到达小肠末端及大肠定殖的活性益生菌的数量,保证益生菌进入肠道后益生功能的发挥,同时还不会给宿主带来任何的健康隐患。
技术实现要素:
为了解决和克服现有技术中存在的问题,本发明提供了缓释抗逆性益生菌晶球及其制备方法,通过该方法制备的缓释抗逆性益生菌晶球耐酸、耐胆盐、耐氧,能够在小肠末端及大肠缓慢释放益生菌,增加益生菌的存活率及在常温环境下的储存稳定性。
为实现上述发明目的,本发明采用以下技术方案予以实现:
本发明提供了缓释抗逆性益生菌晶球的制备方法,其包括如下步骤:
(1)益生菌的发酵和收集:益生菌经培养发酵后离心,得到益生菌菌泥;
(2)抗逆性包埋一层:将步骤(1)的益生菌菌泥与抗逆性一层包埋剂均匀混合,搅拌静置后,得到益生菌包埋一层菌泥;
(3)抗逆性包埋二层:将步骤(2)的益生菌包埋一层菌泥与抗逆性二层包埋剂均匀混合,搅拌静置后,得到益生菌包埋二层菌泥;
(4)益生菌芯材的制备:将步骤(3)的益生菌包埋二层菌泥与脱脂乳粉溶液搅拌混合后,搅拌静置后,得到益生菌芯材;
(5)晶球制备和清洗:将步骤(4)的益生菌芯材加入到酸性溶液中混合后,使用生理盐水进行多次清洗,得到抗逆性益生菌晶球;
(6)抗逆性包埋三层:将步骤(5)的抗逆性益生菌晶球放入海藻酸钠溶液中搅拌均匀后收集,再放入氯化钙溶液中继续搅拌,得到缓释抗逆性益生菌晶球;
(7)硬化:将步骤(6)的缓释抗逆性益生菌晶球放入硬化剂中静置,收集得到硬化缓释抗逆性益生菌晶球;
(8)干燥:将步骤(7)的硬化缓释抗逆性益生菌晶球进行冷冻干燥,收集得到缓释抗逆性益生菌晶球成品。
进一步的,所述步骤(1)中益生菌菌泥固形物含量保持在50%~90%。
进一步的,所述步骤(2)的抗逆性一层包埋剂包括、磷酸氢二钾、磷酸二氢钾、氯化钠、l-半胱氨酸盐酸盐和纯水,所述微孔淀粉添加量为抗逆性一层包埋剂质量的20%~30%,所述益生菌菌泥与抗逆性一层包埋剂的质量比为1∶1~1∶5。
进一步的,所述微孔淀粉的平均孔径与益生菌菌体大小相仿。
进一步的,所述步骤(3)中抗逆性二层包埋剂包括β-环糊精、磷酸氢二钾、磷酸二氢钾、氯化钠、l-半胱氨酸盐酸盐和纯水,所述β-环糊精的添加量为抗逆性二层包埋剂质量的30%~35%,所述益生菌包埋一层菌泥与抗逆性二层包埋剂的质量比为1∶1~1∶5。
进一步的,所述β-环糊精的平均孔径大于微孔淀粉。
进一步的,所述步骤(4)中脱脂乳粉溶液包括脱脂乳粉、l-半胱氨酸盐酸盐、甘油和纯水,所述脱脂乳粉的添加量为脱脂乳粉溶液质量的8%~20%,所述益生菌包埋二层菌泥与脱脂乳粉的质量比为1∶1~1∶5。
进一步的,所述步骤(5)中酸性溶液包括盐酸、硫酸、草酸、磷酸和硝酸,其ph=3~5。
进一步的,所述步骤(6)海藻酸钠溶液包括海藻酸钠、氯化钠和纯水,其添加量为海藻酸钠溶液质量的0.1%~0.5%。
进一步的,所述步骤(6)中氯化钙溶液包括氯化钙、氯化钠和纯水,其添加量为氯化钙溶液质量的5%~15%。
进一步的,所述步骤(7)中硬化剂溶液包括壳聚糖、葡聚糖和纯水,其中壳聚糖的添加量为硬化剂溶液质量的3%~8%,所述壳聚糖与葡聚糖的质量比为1∶1~1∶3;所述缓释抗逆性益生菌晶球和硬化剂的质量比为1∶1~1∶5。
进一步的,所述步骤(8)中干燥参数设置如下:
a、产品预冻:导热油温度-43~-50℃,品温≤-40℃;
b、冷阱预冷:导热油温度-43~-50℃,品温≤-40℃,真空度0.01-0.03mbar;
c、一次升华:导热油温度6-10℃,冷阱温度≤-50℃,真空度0.18-0.22mbar;
d、解析干燥:导热油温度27-30℃,冷阱温度≤-50℃,真空度0.18-0.22mbar。
本发明还提供了由所述缓释抗逆性益生菌晶球的制备方法制得的缓释抗逆性益生菌晶球。
进一步的,所述缓释抗逆性益生菌晶球在25℃储存12月后的剩余活菌量为原活菌量的50%~74%。
本发明与现有技术相比,具有以下优点和有益效果:
1、本发明的缓释抗逆性益生菌晶球是通过对益生菌进行3层抗逆性包埋、硬化和干燥制得的,其中包埋剂中的微孔淀粉的平均孔径与益生菌菌体大小相仿,而β-环糊精的平均孔径大于微孔淀粉,这样不仅能够很好的将益生菌菌体逐层嵌入包埋剂内,还可以使益生菌的最外层形成一层肠溶性海藻酸钙薄膜,防止肠道内较低的ph值对益生菌晶球的破坏,并使益生菌进入肠道后可以缓慢释放,保持益生菌的活性。
2、通过本发明制备方法制备的缓释抗逆性益生菌晶球具有耐酸、耐胆盐、耐氧的优点,能够在小肠末端及大肠缓慢释放益生菌,增加益生菌的存活率及在常温环境下的储存稳定性,同时还有效地降低了益生菌在干燥时的损失率,提高菌粉的活菌数量,增加进入肠道活性益生菌的数量,且该缓释抗逆性益生菌晶球无毒无害,在益生菌利用上具有广阔的应用前景。
附图说明
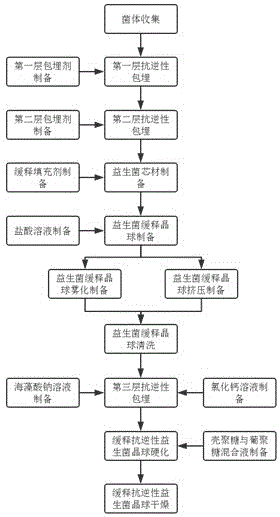
图1为本发明所述的缓释抗逆性益生菌晶球的制备工艺流程图。
具体实施方式
以下结合具体实施例对本发明的技术方案做进一步详细的说明。
实施例1
本发明所述的缓释抗逆性益生菌晶球的制备工艺流程图如图1所示,具体的制备步骤如下:
1、益生菌的发酵和收集:益生菌经培养发酵后离心,收集得到益生菌菌泥;
2、抗逆性包埋一层:将益生菌菌泥与抗逆性一层包埋剂按照1∶1~1∶5的质量比进行均匀混合,50~200rpm搅拌20~30min,4℃静置1~3h得到益生菌包埋一层菌泥。
其中,抗逆性一层包埋剂包括微孔淀粉、磷酸氢二钾、磷酸二氢钾、氯化钠、l-半胱氨酸盐酸盐和纯水,而微孔淀粉的添加量为抗逆性一层包埋剂质量的20%~30%。并且,本发明选择的微孔淀粉的平均孔径与益生菌菌体大小相仿,可以便于益生菌菌体嵌入微孔淀粉孔径内,以此来提高益生菌耐酸、耐胆盐、耐氧的抗逆性。
3、抗逆性包埋二层:将益生菌包埋一层菌泥与抗逆性二层包埋剂按照1∶1~1∶5的质量比进行混合,50~200rpm低速搅拌20min后,4℃静置1~3h,得到益生菌包埋二层菌泥。
其中,抗逆性二层包埋剂包括β-环糊精、磷酸氢二钾、磷酸二氢钾、氯化钠、l-半胱氨酸盐酸盐和纯水,而β-环糊精的添加量为抗逆性二层包埋剂质量的30%~35%。并且,本发明选择的β-环糊精的平均孔径大于微孔淀粉,便于将已经过第一层包埋后的益生菌菌体进行第二层包埋,从而进一步提高益生菌菌体耐酸、耐胆盐、耐氧的抗逆性。
4、益生菌芯材制备:益生菌包埋二层菌泥与脱脂乳粉溶液按照1∶1~1∶5的质量比混合,1000~2500rpm高速搅拌10~30min后,-4℃静置4~16h,得到益生菌芯材。
其中,脱脂乳粉溶液包括脱脂乳粉、l-半胱氨酸盐酸盐、甘油和纯水,而脱脂乳粉的添加量为脱脂乳粉溶液质量的8~20%。
5、益生菌晶球制备和清洗:将益生菌芯材通过挤压或雾化喷洒的方式加入到ph=3~5的酸性溶液中,50~200rpm搅拌20~50min后使用4℃生理盐水进行多次清洗,得到抗逆性益生菌晶球。
其中,酸性溶液包括盐酸、硫酸、草酸、磷酸和硝酸。
6、抗逆性包埋三层:将抗逆性益生菌晶球放入海藻酸钠溶液中,20~200rpm搅拌20min后,收集晶球再放入氯化钙溶液中20~200rpm搅拌20min后,收集得到缓释抗逆性益生菌晶球。
其中,海藻酸钠溶液包括海藻酸钠、氯化钠和纯水,ph7.0,而海藻酸钠添加量为海藻酸钠溶液质量的0.1%~0.5%;氯化钙溶液包括氯化钙、氯化钠和纯水,ph7.0,而氯化钙的添加量为氯化钙溶液质量的5%~15%。
第三次的包埋可以使益生菌晶球在裸露的脱脂乳晶球外表,形成一层肠溶性海藻酸钙薄膜,防止胃酸较低的ph值对脱脂乳晶球的破坏,并使益生菌进入肠道后可以缓慢释放,保持益生菌的活性。
7、缓释抗逆性益生菌晶球的硬化:将收集的缓释抗逆性益生菌晶球按照1∶1~1∶5的质量比放入硬化剂溶液中,静置20~50min,收集得到硬化的缓释抗逆性益生菌晶球。
其中,硬化剂溶液包括壳聚糖、葡聚糖和纯水,ph7.0,壳聚糖与葡聚糖的质量比为1∶1~1∶3,壳聚糖的添加量为硬化剂溶液质量的3%~8%。
8、缓释抗逆性益生菌晶球的干燥:将硬化的缓释抗逆性益生菌晶球放入真空冷冻干燥机,进行干燥,最终得到缓释抗逆性益生菌晶球成品。
真空冷冻干燥的过程对于缓释抗逆性益生菌晶球非常重要,要制得合格且高质量的成品,需要严格控制整个真空冷冻干燥过程,因为在真空冷冻干燥过程中低温以及渗透压均可能对菌体造成伤害,而真空冷冻干燥分为4个阶段,产品预冻、冷阱预冷、一次升华和解析干燥,其参数设置如下:
(1)产品预冻:导热油温度-43~-50℃,自然压力下,当品温降至-40℃,则终止预冷,保持品温≤-40℃1-2h;
(2)冷阱预冷:导热油温度-43~-50℃,自然压力下,当冷阱温度降至-50℃以下,则终止预冷,保持品温≤-40℃、真空度0.01-0.03mbar1-2h;
(3)一次升华:导热油温度6-10℃、冷阱温度≤-50℃、真空度0.18-0.22mbar升温18-28h,再保温2-3h;
(4)解析干燥:导热油温度27-30℃、冷阱温度≤-50℃、真空度0.18-0.22mbar升温1-4h,再在真空度0.005-0.015mbar下保温4h以上直到真空度升至0.025mbar,停止干燥。
本实施例中,所有的溶液均需经过高压蒸汽灭菌后使用。
实施例2
本实施例中制备了缓释抗逆性青春双歧杆菌晶球,其具体的制备步骤如下:
1、青春双歧杆菌的发酵和收集:采用灭菌的m1培养基,于37℃低转速恒温恒碱培养青春双歧杆菌16h,通过碟片式离心机离心后,收集青春双歧杆菌菌泥,而菌泥固形物含量在50%~90%。
其中,m1培养基的配方为葡萄糖30g,蔗糖5g,牛肉蛋白胨10g,牛肉浸粉6.5g,酵母浸粉5g,柠檬酸氢二胺2g,柠檬酸三铵2g,无水乙酸钠2g,磷酸氢二钾2g,磷酸二氢钾3g,硫酸镁0.25g,硫酸锰0.25g,吐温801g,纯水1000g,灭菌前调节培养基ph为6.8。
2、抗逆性包埋一层:将步骤1的青春双歧杆菌菌泥与1抗逆性一层包埋剂1按照1∶1~1∶5的质量比进行均匀混合,50~200rpm搅拌20min后,4℃静置1~3h,得到青春双歧杆菌包埋一层菌泥;其中抗逆性一层包埋剂的配方为微孔淀粉20g,磷酸氢二钾0.5g,磷酸二氢钾0.5g,氯化钠9g,l-半胱氨酸盐酸盐1g,纯水69g:
3、抗逆性包埋二层:将步骤2的青春双歧杆菌包埋一层菌泥与抗逆性二层包埋剂按照1∶1~1∶5的质量比进行混合,50~200rpm搅拌20min后,4℃静置1~3h,得到青春双歧杆菌包埋二层菌泥;其中,抗逆性二层包埋剂配方为β-环糊精30g,磷酸氢二钾0.5g,磷酸二氢钾0.5g,氯化钠9g,l-半胱氨酸盐酸盐1g,纯水59g。
4、青春双歧杆菌芯材制备:将步骤3的青春双歧杆菌包埋二层菌泥与脱脂乳粉溶液按照1∶1~1∶5的质量比混合,1000~2500rpm高速搅拌10~30min后-4℃静置4~16h,得到青春双歧杆菌芯材;其中,脱脂乳粉溶液的配方为脱脂乳粉12g,l-半胱氨酸盐酸盐2g,甘油1g,纯水100g,调节ph6.8。
5、青春双歧杆菌晶球制备和清洗:将步骤4的青春双歧杆菌芯材通过挤压或雾化喷洒的方式加入到ph为3~5的盐酸溶液中,50~200rpm搅拌20~50min后,使用4℃的生理盐水反复清洗2~5次后,收集得到抗逆性青春双歧杆菌晶球。
6、抗逆性包埋三层:将步骤5收集的抗逆性青春双歧杆菌晶球放入海藻酸钠溶液中,20~200rpm搅拌20min后,收集晶球再放入氯化钙溶液中20~200rpm搅拌20min后,收集缓释抗逆性青春双歧杆菌晶球;其中,海藻酸钠溶液的配方为海藻酸钠5g,氯化钠0.5g,纯水1000g,调节ph7.0;氯化钙溶液的配方为氯化钙12g,氯化钠0.5g,纯水1000g,调节ph7.0。
7、缓释抗逆性青春双歧杆菌晶球的硬化:将步骤6收集的缓释抗逆性青春双歧杆菌晶球按照1∶1~1∶5的质量比放入硬化剂溶液中,静置20~50min,后收集硬化的缓释抗逆性青春双歧杆菌晶球;其中,硬化剂溶液的配方包括壳聚糖7g,葡聚糖16g,纯水1000g,ph7.0。
8、缓释抗逆性青春双歧杆菌晶球干燥:将步骤7硬化的缓释抗逆性青春双歧杆菌晶球放入真空冷冻干燥机,进行晶球干燥,产品的装液量为0.8-1.3kg/盘,设置参数为:
(1)产品预冻:导热油温度-43~-50℃,自然压力下,当品温降至-40℃,则终止预冷,保持品温≤-40℃1-2h;
(2)冷阱预冷:导热油温度-43~-50℃,自然压力下,当冷阱温度降至-50℃以下,则终止预冷,保持品温≤-40℃、真空度0.01-0.03mbar1-2h;
(3)一次升华:导热油温度6-10℃、冷阱温度≤-50℃、真空度0.18-0.22mbar升温18-28h,再保温2-3h;
(4)解析干燥:导热油温度27-30℃、冷阱温度≤-50℃、真空度0.18-0.22mbar升温1-4h,再在真空度0.005-0.015mbar下保温4h以上直到真空度升至0.025mbar,停止干燥。
实施例3
采用传统方法生产或购买得到青春双歧杆菌菌粉。将实施例2制备的缓释抗逆性青春双歧杆菌晶球与青春双歧杆菌菌粉于25℃储存12月后、在模拟胃酸和胆汁储存24h后的活菌存量进行对比,并重复三次实验。
结果如表1-3所示,在25℃储存12月、模拟胃酸和胆汁储存24h后,本发明制备的缓释抗逆性青春双歧杆菌晶球的终止活菌数均远高于青春双歧杆菌菌粉的终止活菌数,说明本发明的晶球制备工艺在益生菌菌种抗逆性与储藏稳定性均优于益生菌菌粉,并能够很好的增加益生菌菌种保存的存活率和稳定性,更有利于益生菌功能的发挥。
表125℃储存12月活菌存量对比
表2模拟胃酸储存24h活菌存量对比
表3模拟胆汁储存24h活菌存量对比
以上实施例仅用以说明本发明的技术方案,而非对其进行限制;尽管参照前述实施例对本发明进行了详细的说明,对于本领域的普通技术人员来说,依然可以对前述实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换;而这些修改或替换,并不使相应技术方案的本质脱离本发明所要求保护的技术方案的精神和范围。
- 还没有人留言评论。精彩留言会获得点赞!