一种用于PET图像衰减校正的CT图像生成方法与流程
本发明涉及医学图像重建领域,尤其涉及一种基于深度学习并用于pet图像衰减校正的ct图像生成方法。
背景技术:
pet(positronemissiontomography,pet)的全称为正电子发射型计算机断层显像,是广泛用于解剖形态方式进行功能、代谢和受体显像的医学影像技术,代表了医学影像学发展的最新最前沿技术。与ct(computedtomography,ct)、mri(magneticresonanceimaging,mri)的解剖成像不同,pet可对代谢过程的生理和生化改变进行观测,从而在生化血液浓度或机体结构改变之前发现异常而发现病变,pet在临床上被广泛运用于肿瘤检查。
在进行pet扫描前,会对生物活体注入同位素示踪剂,示踪剂在参与生理代谢时发生衰变产生正电子,其发射的正电子在继续前行1~2mm后会和邻近的电子发生湮没效应,产生一对方向相反(互为180°)、能量相等(511kev)的γ光子。γ光子在穿过物体到进入探测器的过程中,会有一定概率与物体中的电子碰撞发生光电效应或康普顿散射,使γ光子消失或自身能量降低,或改变运行方向。当光子能量低于pet设备的低能探测阈值时(通常为400~450kev)将无法被探测器有效探测,为了准确定量并分析放射性药物在体内的分布情况,就必须对γ射线的衰减进行衰减校正。衰减校正不但能提高pet图像的对比度,获得更加精确的suv(standarduptakevalue,suv)值,以便对病情做出更加精准的定量分析。
pet图像的衰减校正问题一直是医学图像重建领域中的一个热点问题,不少国内外的专家和学者都提出了各自的方法。计算校正法是最早提出的衰减校正方法,该方法利用探测器所探测到的射线强度推算出射线的原始强度,该方法虽然简单,但在实际使用该方法需要的条件及使用的限制过多,如要知道每一个像素点的线性衰减系数值以及该点所发生湮灭事件所放出的光子到探测器之间所经过的距离。当物体形状不规则时这些条件很难满足,这会影响衰减校正的准确性,随着其他衰减校正方法的不断成熟,该方法使用的情景也越来越少。测量校正法也可用于pet图像的衰减校正,该方法采用空白扫描和穿透式扫描分别在没有患者和有患者的情形下进行扫描,最终任一条符合线的衰减校正因子就等于这条线上空白扫描和透射扫描的计数比值。但该方法需要额外的穿透式扫描操作,这会增加扫描时间增加,提高成像的成本,并且采用该方法是患者受到的辐射剂量也因而增加。此外,在进行穿透式扫描时,受限于扫描时间限制和源剂量,实际使用中经常出现符合事件计数不足的情形,最终影响衰减校正的效果。因此使用测量校正法得到的衰减校正因子存有很大的误差,最终会影响生成pet图片的准确性,严重时会在pet图像中出现伪影。
近年来,随着传感器技术和数字处理技术的迅速发展,科研人员将pet设备和ct设备融合在一起而发展出了pet/ct成像设备。由于ct设备采用的x射线和pet设备需要捕捉的γ射线同为高频电磁波,二者在人体内部的穿透能力和衰减规律具有一定的联系,因此科研人员也越来越关注以ct数据为基础的衰减校正法。相比pet,ct技术更加成熟,并且ct采用外部生成x射线,可以提供高分辨率的诊断图像,该图像即为x射线对人体组织器官的衰减系数分布图,因此,可以利用ct扫描得到的数据对pet图像进行衰减校正。与传统的计算校正法和测量校正法相比,ct扫描具有很大的优势,如扫描速度快,获得患者体内信息更多,不会对pet传感器捕捉511kevγ光子进行干扰,噪声低等。在以ct数据为基础的衰减校正方法中,最核心的思想是将ct图像在特定管电压下扫描生成的图像中每个像素的灰度值转换成511kev能量γ光子下的衰减系数,这一步常被称为能量转换。针对该问题,不少学者提出了各自的方法,如比例法、分割计算法和双线性转换法等。比例法首先计算511kev能量下γ光子与x射线(通常选择在50~80kev范围内)在水中的衰减系数比值,接着与ct图像的像素对应的衰减系数相乘从而完成衰减校正。该方法使用时相对简单,针对衰减主要由康普顿散射造成的情形,此方法较为精确,但当被测物体存在较高原子序数的组织(如骨骼等),该方法的误差较大。x射线在骨骼等高原子序列的组织中主要产生光电效应而造成能量衰减,而511kevγ光子的能量很高,光电效应造成的能量衰减对射线的捕捉没有太大影响。分割计算方法是根据ct图像将患者划分成软组织、骨骼和肺三个区域,接着分别将每个区域图像的ct图对应的x射线衰减系数转换成511kev能量下的衰减系数值。该方法依靠精确的分割,但当测量区域存在骨骼连续变换的软组织区域和密度梯度较大的同类组织区域,仅仅使用三种离散的值来代替并不准确,会照成较大的误差。倘若分割后的ct图和pet图的配准不精确,校正误差也会增大。由于很多能量转换方法一般由执行困难,受限条件过多等优点。
技术实现要素:
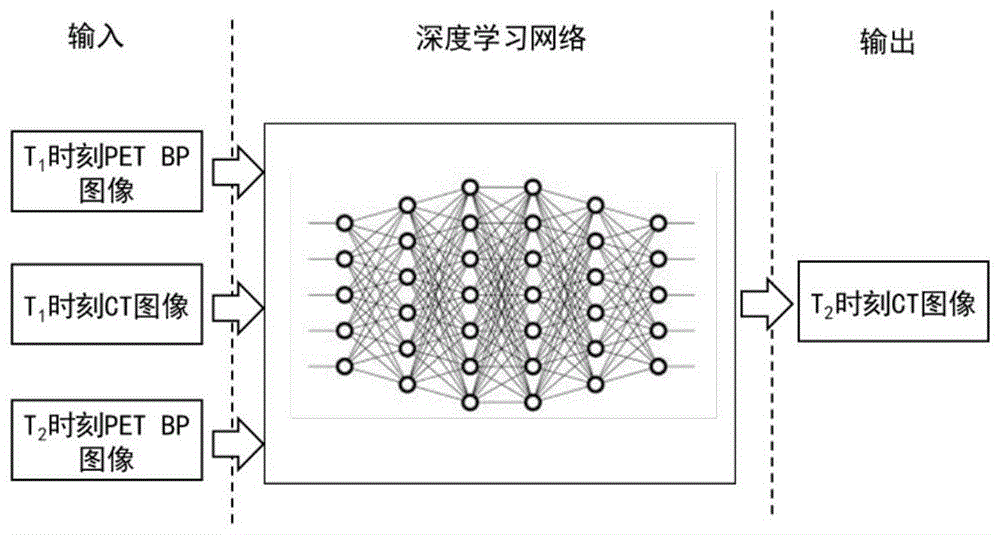
本发明针对现有技术的不足,提出了一种用于pet图像衰减校正的ct图像生成方法,该方法采用t1时刻的petbp(backprojection)图像和ct图像以及t2时刻的petbp图像生成t2时刻的ct图像,该方法可以减轻整个流程中患者受到的x射线辐射剂量,从而减轻患者身体或心理上受到的压力。
本发明的目的是通过以下技术方案来实现的:一种用于pet图像衰减校正的ct图像生成方法,包括以下步骤:
步骤一:通过pet/ct设备采集若干位病人在t1时刻的ct图像和pet图像,再采集所述病人在t2时刻的ct图像和pet图像。
步骤二:将步骤一采集得到的t1时刻的ct图像和pet图像、t2时刻的ct图像和pet图像输入深度学习网络中进行训练,以t1时刻的ct图像和pet图像以及t2时刻的pet图像作为输入,以t2时刻的ct图像作为标签,使得损失函数收敛并稳定,完成对深度学习网络的训练。
步骤三:使用pet/ct设备采集新病人t1时刻的ct图像和pet图像,并采集所述新病人t2时刻的pet图像,将三幅图像输入步骤二训练好的深度学习网络中,得到所述新病人t2时刻的ct图像。
进一步地,步骤一还可以为:通过pet/ct设备采集若干位病人在t1时刻的ct图像和pet图像,采用薄板样条曲线或b样条曲线等非刚性变形模型对t1时刻采集的ct图像和pet图像加入一个形变生成t2时刻的pet图像和ct图像。
进一步地,步骤一中采集t1时刻的ct图像和采集t1时刻的pet图像的相同坐标的像素对应体内相同的位置;采集t2时刻的ct图像和采集t2时刻的pet图像的相同坐标的像素对应体内相同的位置。
进一步地,步骤二中所采用的深度学习网络选自unet、gan。
进一步对,步骤三中,采用反向传播方法对深度学习网络进行训练,使得所述新病人t2时刻的ct图像和所述新病人t2时刻的pet图像中的相同坐标的像素对应体内相同的位置。
进一步地,所述pet图像为petbp图像、petnac或petfbp。
本发明的有益效果是,本发明的方法在患者需要进行多次pet扫描时,只需要在第一次进行ct扫描获得组织的解剖信息,后续的pet扫描中无需进行ct扫描操作,可以通过第一次pet和ct扫描得到的信息以及后几次pet扫描得到的原始图像信息或bp图像信息即可获得衰减校正需要的解剖信息,用于pet图像的衰减校正,从而实现精准的pet重建。本发明的方法避免了反复采集病人ct图像的操作,减少整个图像采集阶段病人受到的x射线的剂量,减轻病人生理和心理上受到的压力。另外,后期以测量只需要pet成像设备,不需要pet/ct设备,可以增强成像资源分配的成本,降低整个阶段成像的费用。
附图说明
图1是基于用于pet图像衰减校正的ct图像生成方法流程图;
图2为unet的监督学习网络。
具体实施方式
下面根据实施例和附图详细说明本发明。
实施例1
如图1为本发明一种用于pet图像衰减校正的ct图像生成方法流程图,该方法包括以下步骤:
步骤一:通过pet/ct设备采集若干位病人在t1时刻的ct图像和pet图像,这两幅图像相同坐标的像素对应体内相同的位置;再采集所述病人在t2时刻的ct图像和pet图像,这两幅图像相同坐标的像素对应体内相同的位置。这是由于同一时刻采集的同个人的ct图像和pet图像对应的同样的解剖信息。
步骤二:将步骤一采集得到的t1时刻的ct图像和pet图像、t2时刻的ct图像和pet图像输入深度学习网络中进行训练,这里所采用的深度学习网络选自unet、gan(generaladversarialnetwork)。如图2为unet的监督学习网络,以t1时刻的ct图像和pet图像以及t2时刻的pet图像作为输入,以t2时刻的ct图像作为便签,使得损失函数收敛并稳定,完成对深度学习网络的训练。这里采用深度学习网络是为了找到t1时刻的pet图像和ct图像之间的灰度对应关系,然后将t2时刻的pet图像转换成ct图像。
步骤三:使用pet/ct设备采集新病人t1时刻的ct图像和pet图像,并采集所述新病人t2时刻的pet图像,将三幅图像输入步骤二训练好的深度学习网络中,得到所述新病人t2时刻的ct图像。采用反向传播方法对深度学习网络进行训练,使得所述新病人t2时刻的ct图像与所述新病人t2时刻的pet图像对齐。
将上述实施例得到的所述新病人t2时刻的ct图像生成每个像素的衰减系数值,根据衰减系数值可以生成更加清晰的petac图像,获得更加精确的suv值,以便对病情做出更加精准的定量分析。
实施例2
本发明一种用于pet图像衰减校正的ct图像生成方法,该方法包括以下步骤:
步骤一:通过pet/ct设备采集若干位病人在t1时刻的ct图像和pet图像,采集t1时刻的ct图像中与采集t1时刻的pet图像相同坐标的像素对应体内相同的位置;采用薄板样条曲线或b样条曲线等非刚性变形模型对t1时刻采集的ct图像和pet图像加入一个形变生成t2时刻的pet图像和ct图像。
步骤二:将步骤一采集得到的t1时刻的ct图像和pet图像、t2时刻的ct图像和pet图像输入深度学习网络中进行训练,这里所采用的深度学习网络选自unet、gan(generaladversarialnetwork)。以t1时刻的ct图像和pet图像以及t2时刻的pet图像作为输入,以t2时刻的ct图像作为标签,使得损失函数收敛并稳定,完成对深度学习网络的训练。
步骤三:使用pet/ct设备采集新病人t1时刻的ct图像和pet图像,并采集所述新病人t2时刻的pet图像,将三幅图像输入步骤二训练好的深度学习网络中,得到所述新病人t2时刻的ct图像。采用反向传播方法设对度学习网络进行训练,使得所述新病人t2时刻的ct图像与所述新病人t2时刻的pet图像对齐。
将上述实施例得到的所述新病人t2时刻的ct图像生成每个像素的衰减系数值,根据衰减系数值可以生成更加清晰的pet图像,获得更加精确的suv值,以便对病情做出更加精准的定量分析。
本发明中所采用的pet图像为petbp图像、petnac(nonattenuationcorrection)、petfbp(filteredbackprojection)等。
本发明主要用于pet/ct设备,但也可扩展到pet/mri设备。
- 还没有人留言评论。精彩留言会获得点赞!