一种急性缺血性脑卒中磁共振灌注-弥散影像配准方法与流程
本发明属于磁共振成像和数字图像技术领域,具体涉及一种急性缺血性脑卒中磁共振灌注-弥散影像配准方法。
背景技术:
脑卒中(又称中风)是一种常见的脑血管病,发病率为246.8/10万,死亡率为114.8/10万,其中缺血性脑卒中约占87%,脑出血约占10%,蛛网膜下腔出血约占3%,给社会带来沉重的负担。急性缺血性脑卒中又称急性脑梗死,是由局部脑组织的血液供应中断所导致的局灶性脑功能缺损性疾病,占我国脑卒中的69.6%。一旦发病,准确定义疾病所处的时期(时间窗)、抢救缺血半暗带(组织窗)、争取责任血管的再通以及建立良好的侧支循环是治疗及预后的关键。
急性缺血性脑卒中的诊断主要依靠临床病史、症状体征及影像学检查。临床中疑似缺血性脑卒中的患者都需进行常规计算机断层扫描(computedtomography,ct)或磁共振成像(magneticresonanceimaging,mri)检查,以确定脑内是否存在缺血灶,并与出血性卒中、脑肿瘤、脑外伤及颅内感染性疾病进行鉴别。急性缺血性脑卒中病变在ct影像上呈低密度表现,但与相邻区域脑组织的密度差别不大,易漏诊。相比ct而言,mri具有无电离辐射,诊断灵敏度高、特异性高等优点,可为脑梗死早期诊断及有效治疗提供丰富且可靠的影像学依据。
影像引导的急性脑梗死治疗已从“时间就是大脑”逐渐向“生理就是大脑”转变,而判断梗死灶、缺血半暗带存在是早期有效治疗的重要依据。评价梗死(局部缺血核心)的最佳指标可通过磁共振弥散加权成像(diffuseweightedimaging,dwi)序列提供。dwi是目前唯一无创反映活体组织内水分子扩散运动的检查方法,对急性脑缺血具有高度的敏感性、特异性和准确性,为脑卒中的早期及时治疗提供了直观和重要依据。而利用磁共振脑灌注成像评价缺血脑组织的血流动力学变化,为临床治疗方案的选择、是否需要溶栓治疗及疾病预后判断提供重要的参考价值。灌注-弥散不匹配(perfusion-diffusionmismatch,pdm)被视为临床判断缺血半暗带的“金标准”,可以对缺血范围、程度、类型做出评价。
磁共振灌注成像包括需要注射对比剂的动态磁敏感对比增强灌注成像和动态增强扫描的灌注加权成像(perfusionweightedimaging,pwi)和无需注射对比剂的动脉自旋标记(arterialspinlabeling,asl)灌注成像技术。asl是一种非侵入的定量灌注成像方式,它利用内源性造影剂(动脉血中的水分子),通过反转射频脉冲以获得不同区域的脑血流灌注信息,避免了钆对比剂的肾毒性,可重复性高。然而,在梗死发生的早期,梗死区可能同时出现弥散受限无灌注区和低灌注区,弥散受限无灌注区由不可逆性损伤的脑细胞组成,低灌注区由可逆性损伤的脑细胞组成。因此尽可能挽救低灌注区内脑细胞是卒中治疗的核心。这涉及到脑卒中患者的asl灌注像和弥散加权像(dwi)的高精度配准。
梗死灶、缺血半暗带定量化指标的获取对于脑卒中诊断及预后判断具有重要意义。但是,不同成像方式导致脑卒中患者的结构像和功能像(如灌注像、弥散像)在分辨率、对比度、几何形变等存在很大差异,造成多模态影像配准面临很大难度和复杂性,并且较小配准误差会对脑卒中的诊疗产生较大影响(h.j.m.m.mutsaerts,j.petr,d.l.thomas,etal.comparisonofarterialspinlabelingregistrationstrategiesinthemulti-centergeneticfrontotemporaldementiainitiative(genfi),j.magneticresonanceimaging,47,131-140,2018)。目前一般采用刚性变换或仿射变换解决dwi和asl配准问题(g.crisi,s.filice,u.scoditti,arterialspinlabelingmritomeasurecerebralbloodflowinuntreatedischemicstroke,j.neuroimaging,29,193-197,2019)。因脑组织是多形变器官,上述方法的配准误差较大。脑卒中处理的商业软件rapid(rapidprocessingofperfusionanddiffusion)可以通过磁共振弥散加权像(dwi)和灌注加权像(pwi)提取感兴趣脑参数图(m.straka,g.w.albers,r.bammer,real-timediffusion-perfusionmismatchanalysisinacutestroke,j.magneticresonanceimaging,32,1024-1037,2010),但难以解决dwi和asl精确配准问题。因此,如何提高磁共振灌注-弥散影像配准精度是急性缺血性脑卒中所需急迫解决的重大挑战。
技术实现要素:
本发明是针对现有脑卒中灌注-弥散影像配准方法存在的上述技术问题,提供了一种急性缺血性脑卒中磁共振灌注-弥散影像配准方法。该方法将脑卒中的结构影像和功能影像映射到模板空间,实现脑卒中的灌注-弥散影像在空间解剖位置上对应,从而有效定量分析灌注-弥散不匹配、体积等临床诊疗指标。
一种急性缺血性脑卒中磁共振灌注-弥散影像配准方法,包括以下步骤:
步骤1、重采样脑卒中的结构影像、功能影像及模板空间,使结构影像、功能影像及模板空间的空间分辨率保持一致,功能影像包括脑血流量图和弥散扩散加权像,脑血流量图由控制影像和标记影像计算获得;
步骤2、结构影像向控制影像配准,获得第一形变向量场及配准后的结构影像;配准后的结构影像向模板空间配准,获得第二形变向量场和形变的结构影像;
步骤3、将第二形变向量场应用到脑血流量图,得到形变的脑血流量图;将第一形变向量场和第二形变向量场应用到弥散扩散加权像,得到形变的弥散扩散加权像。
一种急性缺血性脑卒中磁共振灌注-弥散影像配准方法,还包括以下步骤:
在形变的脑血流量图中,利用低灌注阈值提取低灌注区;在形变的扩散加权像中,利用梗死核心阈值提取梗死核心区,获得低灌注区和梗死核心区的大小、体积和位置。
如上所述的步骤2中:
采用弹性形变模型实现结构影像向控制影像的配准;采用弹性形变模型实现配准后的结构影像向模板空间配准。
本发明与现有技术相比,具有以下优点:
1.不同磁共振成像序列导致脑卒中的结构影像和功能影像在空间分辨率上差异较大。为保持脑卒中的结构影像和功能影像的空间分辨率一致,通过高分辨率重建实现高分辨率影像的下采样,避免过度损失细节信息;通过低分辨率重建实现低分辨率影像的上采样,避免过度引入伪影和噪声。
2.为有效配准脑卒中的磁共振灌注-弥散影像,首先将结构影像配准模板空间,获得形变向量场,其次将功能影像(脑血流量图和弥散扩散加权像)映射到模板空间,然后对比分析空间对应的脑血流量图和弥散扩散加权像,提取低灌注区和梗死核心区,定量其大小、体积及灌注-弥散不匹配等临床指标,实现从原始多模态数据到临床指标的一站式报表。
3.本发明定量分析脑卒中磁共振弥散-灌注影像的梗死核心/半暗带的不匹配、大小、体积、位置等临床诊疗指标,有助于脑卒中诊断及预后判断。
附图说明
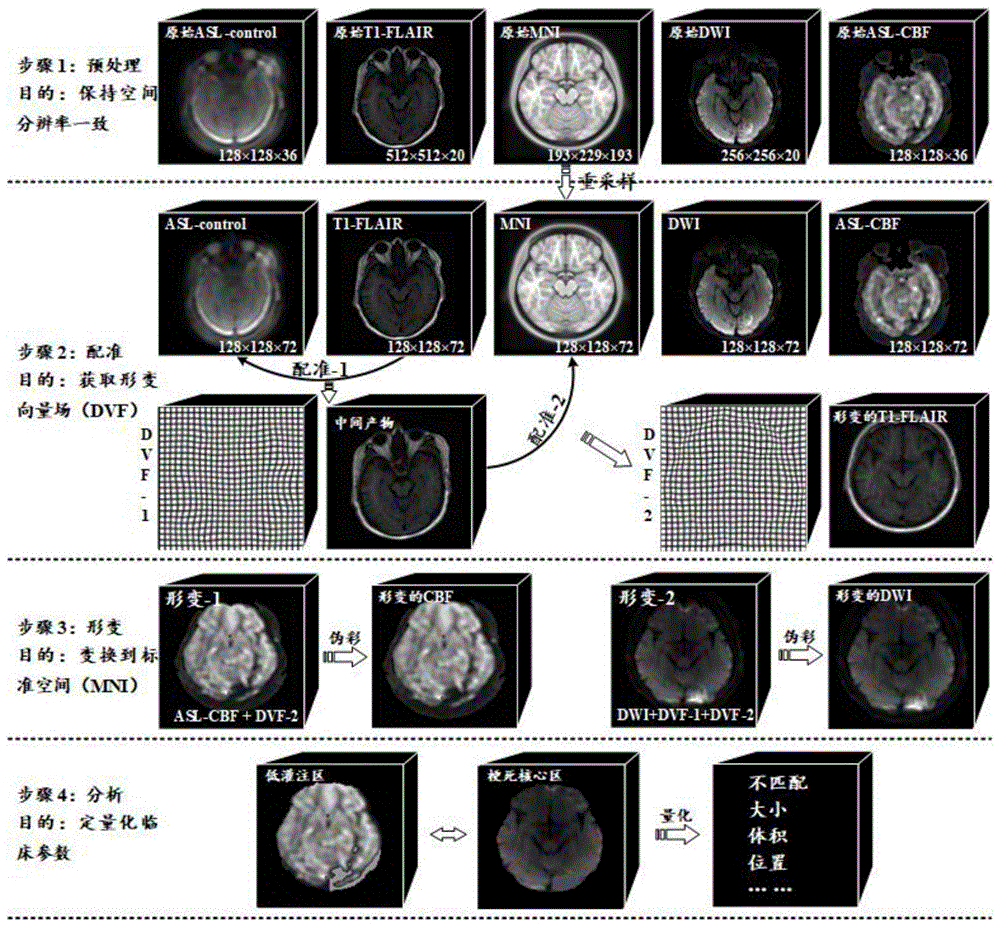
图1为本发明的流程图,包括四个步骤:1.预处理,使得脑卒中的磁共振灌注-弥散影像在空间分辨率方面保持一致;2.配准,将脑卒中的结构影像和功能影像映射到模板空间,获得其变换的形变向量场;3.形变,将脑卒中的磁共振灌注成像和弥散扩散加权像映射到模板空间,实现磁共振灌注-弥散影像的配准;4.分析,对比分析已配准好的脑卒中的磁共振灌注-弥散影像,定量化脑卒中相关临床指标。
图2为急性缺血性脑卒中患者的灌注-弥散影像及分析结果,其中a为原始的结构影像(t1-flair),b为原始的弥散扩散加权像,c为原始的脑血流量图;将a,b和c映射到模板空间,d为形变的结构影像(t1-flair),e为形变的弥散扩散加权像,f为形变的脑血流量图;去除脑壳后,g为d图去除脑壳后的结果,h为e图去除脑壳后提取的梗死核心区,i为f图去除脑壳后提取的低灌注区。
具体实施方式
为了便于本领域普通技术人员理解和实施本发明,下面结合实施例对本发明作进一步的详细描述,应当理解,此处所描述的实施示例仅用于说明和解释本发明,并不用于限定本发明。
一种急性缺血性脑卒中磁共振灌注-弥散影像配准方法,包括以下步骤:
步骤1,预处理,目的是使脑卒中的磁共振灌注-弥散影像在空间分辨率方面保持一致,提高配准精度。
模板空间(montrealneurologicalinstitute,mni152)能提供脑部不同解剖结构的空间位置,得到诸如白质、灰质、额叶、顶叶、枕叶、颞叶、壳核、后沟带回、丘脑、海马等脑区。将脑卒中的磁共振灌注-弥散影像配准到模板空间,磁共振灌注-弥散影像包括结构影像和功能影像,功能影像包括脑血流量图和弥散扩散加权像,磁共振灌注成像包括控制影像和标记影像,脑血流量图由控制影像和标记影像计算获得,即可分析不同脑区的灌注、弥散功能,及健康侧、患病侧的功能变化等,这有利于脑卒中诊疗方案的确定和优化。但是,不同成像序列导致脑卒中的磁共振灌注-弥散影像在空间分辨率上存在大不同(见附图1),如结构影像(t1/t2-flair,fluidattenuatedinversionrecovery)的大小为512×512×20,功能影像如弥散扩散加权像(diffuseweightedimaging,dwi)的大小为256×256×20,模板空间大小为193×229×193,而动脉自旋磁共振灌注成像(arterialspinlabeling,asl)中的控制影像(asl-control)和标记影像(asl-labeling)的大小为128×128×36。通过三维高分辨率/低分辨率重建方法重采样脑卒中的结构影像、功能影像及模板空间,使结构影像、功能影像及模板空间的空间分辨率保持一致,如128×128×72。对于高空间分辨率影像,可以通过三维低分辨率重建方法(或下采样策略),降低其空间分辨率;而对于低空间分辨率影像,可以通过三维高分辨率重建方法(或上采样策略),提升其空间分辨率。
步骤2,配准,目的是使脑卒中的结构影像(t1/t2-flair)和功能影像(脑血流量图和弥散扩散加权像)映射到模板空间(mni152),获得其变换的形变向量场(deformationvectorfield,dvf)。
在急性缺血性脑卒中的临床磁共振检查中,成像序列扫描顺序一般是先结构成像(t1/t2-flair),后功能成像(弥散扩散加权成像和动脉自旋磁共振灌注成像)。动脉自旋磁共振灌注成像的控制影像(asl-control)和标记影像(asl-labeling)用于计算脑血流量图(cerebralbloodflow,cbf),其提供脑血流灌注动力学信息。弥散扩散加权像(dwi)和结构影像(t1/t2-flair)之间的配准可以通过刚性变换、仿射变换或弹性形变模型(如微分同胚)实现,且控制影像(asl-control)和标记影像(asl-labeling)也可以利用刚性变换、仿射变换或弹性形变模型实现两者配准。
配准-1:实现脑卒中结构影像(t1/t2-flair)向控制影像(asl-control)配准,如附图1所示。由于该两种成像序列成像间隔时间稍长,故可采用弹性形变模型(如微分同胚)实现结构影像(t1/t2-flair)向控制影像(asl-control)的配准,获得第一形变向量场(dvf-1)及配准后的结构影像(t1/t2-flair)(即附图1中的中间产物)。
配准-2:实现配准后的结构影像(t1/t2-flair)向模板空间(mni152)配准,如附图1所示。由于是组间配准,我们采用弹性形变模型(如微分同胚)实现两者之间的配准,获得第二形变向量场(dvf-2)和形变的结构影像(t1/t2-flair)(见附图1)。
步骤3,形变,目的是将脑卒中的脑血流量图(cbf)和扩散加权像(dwi)映射到模板空间(mni152),从而实现灌注-弥散影像的配准,包括形变-1和形变-2两步。
形变-1:利用前述的控制影像(asl-control)和标记影像(asl-labeling)计算脑卒中的脑血流量图(cbf),其提供不同脑区的脑血流灌注信息。将第二形变向量场(dvf-2)应用到脑血流量图(cbf),实现脑血流量图(cbf)映射到模板空间(mni152),得到形变的脑血流量图(cbf)(见附图1)。
形变-2:如附图1所示,将第一形变向量场和第二形变向量场(dvf-1和dvf-2)应用到弥散扩散加权像(dwi),实现弥散扩散加权像(dwi)与模板空间(mni152)的空间对应,得到形变的弥散扩散加权像(dwi)。
步骤4,分析,目的是对比分析已配准好的脑卒中的磁共振灌注-弥散影像,定量化脑卒中相关临床指标。
通过步骤1-步骤3将脑卒中的脑血流量图和弥散扩散加权像映射到模板空间(mni152),实现脑卒中的脑血流量图在空间位置上与弥散扩散加权影像对应。由于模板空间(mni152)可以提供不同脑区的空间位置,则可分析不同脑区的脑血灌注和扩散等信息。如附图1所示,在形变的脑血流量图中,利用低灌注阈值提取低灌注区;在形变的扩散加权像中,也可利用梗死核心阈值提取梗死核心区。进一步可以分析低灌注区/梗死核心区的大小、体积和位置等信息。
本文中所描述的具体实施例仅仅是对本发明精神作举例说明。本发明所属技术领域的技术人员可以对所描述的具体实施例做各种各样的修改或补充或采用类似的方式替代,但并不会偏离本发明的精神或者超越所附权利要求书所定义的范围。
- 还没有人留言评论。精彩留言会获得点赞!