一清复方制剂在制备抗新型冠状病毒感染药物中的应用的制作方法
本发明涉及一种药物的新用途,具体为一清复方制剂在制备预防/治疗新型冠状病毒感染药物中的应用,属于中药应用技术领域。
背景技术:
一清颗粒为民族药配方制剂,中成药,具有清热泻火解毒之功效;临床用于治疗火毒血热所致的目赤口疮、咽喉牙龈肿痛、大便秘结;咽炎、扁桃体炎、牙龈炎等疾病。主要原料成分包括黄连、大黄、黄芩药材。
冠状病毒是一种具有包膜的单股正链rna病毒,广泛存在于人类、哺乳动物和鸟类宿主,可以导致呼吸道、肠道、肝脏和神经系统疾病。人类已知的冠状病毒有六种,其中四种一般仅引起类似普通感冒的轻微呼吸道症状,另外两种冠状病毒严重急性呼吸综合征冠状病毒(sars)和中东呼吸综合征冠状病毒(mers),可引起严重的呼吸系统疾病。新型冠状病毒(covid-19)是人类冠状病毒中的第七种,属于beta冠状病毒。
新冠病毒“covid-19”感染肺炎患者以发热、乏力、干咳为主要表现,少数患者伴有鼻塞、流涕、腹泻等症状,重型病例多在1周后出现呼吸困难,严重者快速进展为急性呼吸窘迫综合征、脓毒症休克、难以纠正的代谢性酸中毒和出凝血功能障碍,部分轻型患者并无肺炎表现。血常规提示白细胞计数正常或减少,淋巴细胞减少,病毒核酸检测阳性。ct表现多为双肺多发磨玻璃密度影(ggo),以双肺胸膜下分布为主,可伴空气支气管征、小叶间隔增厚和胸膜增厚,极少数或少数伴胸腔积液或淋巴结肿大。相关研究推断其自然宿主可能是蝙蝠。通过s-蛋白与人体内血管紧张素转化酶(ace2)结合并ii型跨膜丝氨酸蛋白酶(tmprss2)激活的分子机制,来感染人的呼吸道上皮细胞。
《science》近日报道了瑞德西韦用于新型冠状病毒治疗的可能性。据报道中国科学院武汉病毒研究所和北京毒物药物研究所也在进行这个“老药”的抗新型冠状病毒作用研究,这将为无药可治的新型冠状病毒患者提供用药的机会。国家卫健委等发布了“关于印发新型冠状病毒感染的肺炎诊疗方案(试行第三版)”的通知,其中抗病毒治疗方案推荐洛匹那韦和利托那韦为候选药物。另有研究表明基于氨溴索对于呼吸性疾病治疗的临床价值,可能有益于新型冠状病毒感染的治疗,已经进入了国家卫健委的诊疗方案(第三和第四版)。但截至目前尚无新型冠状病毒感染的特效药物。
根据2020年1月7号科学家报道的新型冠状病毒基因序列和ace2是该病毒进入靶细胞的受体,靶细胞的ii型跨膜丝氨酸蛋白酶(tmprss2)能促使新型冠状病毒刺突蛋白与ace2结合并进入细胞,本发明构建阻断冠状病毒刺突蛋白与ace2结合的药物筛选模型,并利用这个模型对多个贵州民族药复方制剂进行了体外活性筛选,首次发现“一清”复方制剂有新的用途。
技术实现要素:
本发明的目的在于提供一清复方制剂在制备预防/治疗新型冠状病毒感染药物中的应用;一清复方制剂能有效抑制新型冠状病毒刺突糖蛋白与靶细胞受体ace2结合和ii型跨膜丝氨酸蛋白酶(tmprss2)表达而阻止病毒进入靶细胞,并且能有效降低病毒感染细胞产生炎症因子(il-2,il-6,tnf-a,il-8和cxcl-10)。
本发明的技术方案如下:
一清复方制剂在制备预防/治疗新型冠状病毒感染药物中的应用,所述一清复方制剂是由黄连165重量份、大黄500重量份和黄芩250重量份为原料药制成的。
前述应用中,所述一清复方制剂的制法为:称取三味原料药,分别加水煎煮二次,第一次1.5小时,第二次1小时,合并煎液,滤过,滤液减压浓缩至70℃相对密度为1.25,喷雾干燥成干浸膏粉,将三种浸膏粉合并,然后加入辅料或者不加辅料制成各种口服制剂。
前述应用中,所述一清复方制剂是往合并后的浸膏粉中加入适量蔗糖与糊精,混匀,制成颗粒,干燥,分装制得的颗粒剂。
本发明的有益效果:本发明通过构建阻断新型冠状病毒刺突糖蛋白与靶细胞受体血管紧张素转化酶2(ace2)的药物筛选模型,对多种中药复方制剂进行筛选,发现一清复方制剂有抑制新型冠状病毒刺突糖蛋白与靶细胞受体(ace2)结合和ii型跨膜丝氨酸蛋白酶(tmprss2)表达而阻止病毒进入靶细胞的活性,并能显著抑制病毒感染细胞产生炎症因子(il-2,il-6,tnf-a,il-8和cxcl-10),可将其用于新型冠状病毒感染性疾病的预防和治疗,为新冠肺炎患者提供了用药选择,对当前的疫情防控具有重要作用和意义。
附图说明
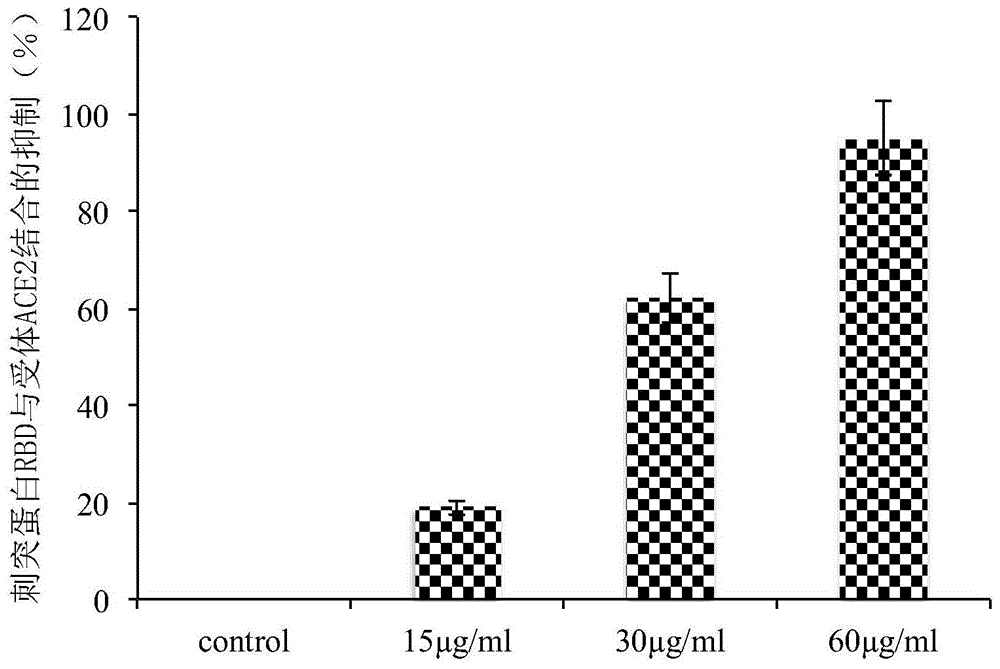
图1是一清颗粒抑制rbd-fc与ace2的结合效果图;利用流式细胞仪测定rbd-fc对293t/ace2细胞表达ace2结合抑制作用,rbd-fc的浓度为1μg/ml,一清颗粒的浓度分别是15μg/ml、30μg/ml、60μg/ml,以dmso作为对照。
图2是一清颗粒对感染病毒细胞的tmprss2表达的影响;用不同浓度一清颗粒处理细胞24小时后,利用实时定量qpcr测量tmprss2mrna。误差棒表示来自3组独立实验的平均值的sd。
图3-1是一清颗粒对vsv-covid-19-st19/gfp进入肺泡ⅱ型上皮细胞(at2)的抑制作用;图3-2是不同浓度一清颗粒处理后病毒感染细胞的百分数;(a)将vsdvg*接种到表达所示糖蛋白的293t细胞上24小时后,收集培养上清液,通过0~22mm孔径的过滤器过滤并接种到at2细胞上,在荧光显微镜下检查gfp的表达;(b)通过流式细胞术评估不同浓度药物处理后gfp阳性细胞数(n=7)。
图4是一清颗粒对vsv-covid-19-st19/gfp对病毒感染肺泡上皮细胞的抑制作用;将vsv-covid-19-st19/gfp接种到表达所示糖蛋白的293t细胞上24小时后,收集培养上清液,通过0~22mm孔径的过滤器过滤并接种到ii型肺泡上皮细胞(at2)上,通过相应的病毒浓缩的方法获得vsv-covid-19-st19/gfp病毒滴度,病毒滴度由egfp基因(iu/ml)的表达确定。
图5是一清颗粒对肺泡ii型细胞感染病毒后产生炎症因子的影响;ii型上皮细胞培养并接种vsv-covid-19-st19/gfp24小时后,利用elsa定量细胞炎症因子的含量,*p<0.05、**p<0.01、***p<0.001,结果来自3个独立实验。
下面结合附图和具体实施方式对本发明作进一步的说明。
具体实施方式
实施例1:一清颗粒剂的应用:
一清颗粒剂可从市场上购买,也可按照《中国药典》2015年版一部第427页中“一清颗粒”的制法制备,所得颗粒剂可直接用于预防/治疗新型冠状病毒感染性疾病。用法用量:口服,6.5g/次,3次/天。
实施例2:一清复方制剂的应用:
称取黄连165g、大黄500g和黄芩250g,分别加水煎煮二次,第一次1.5小时,第二次1小时,合并煎液,滤过,滤液减压浓缩至70℃相对密度为1.25,喷雾干燥成干浸膏粉,将三种浸膏粉合并,然后采用现有制剂成型工艺制成各种口服制剂。所得一清口服制剂可用于预防/治疗新型冠状病毒感染性疾病。用法用量:口服,6.5g/次,3次/天。
实施例3:一清复方制剂的应用:
称取黄连165g、大黄500g和黄芩250g,采用常规提取工艺和制剂成型工艺制成各种口服制剂。所得一清口服制剂可用于预防/治疗新型冠状病毒感染性疾病。用法用量:口服,6.5g/次,3次/天。
实验例:
本发明人构建了稳定的covid-19的rbd-fc表达细胞系,可以将rbd刺突蛋白分泌到培养基中,并可用蛋白a亲和色谱法轻松纯化;所构建的vsv-covid-19-st19伪病毒能和受体ace2结合进入靶细胞但是该伪病毒无法产生后代病毒,因此该系统可用于筛选靶向vsv-covid-19-s蛋白介导的细胞进入的药物。
一、实验材料
1.被测样品溶液的配制:按需称取适量一清颗粒,用dmso配制成不同浓度(50ug/ml,25ug/ml,12.5ug/ml,6.25ug/ml,3.125ug/ml)的溶液。
2.细胞系:人类胚胎肾293t用于产生带有covid-19-s蛋白的水泡性口腔炎病毒(vsv)假型病毒。肺泡ⅱ型上皮细胞(at2)用于vsv假型病毒感染的靶细胞。
3.改良的eagle培养基,该培养基具有高葡萄糖浓度,并补充了10%胎牛血清(dmem10%fcs),用于培养293t和at2细胞。
4.高压灭菌的磷酸盐缓冲盐水(pbs):0.14μmnacl,2μmkcl,3μmna2hpo4、1.5μmkh2po4,ph7.2。
5.转染试剂(德国qiagen)。
6.编码covid-19-s蛋白的人表达质粒,其c端具有19个氨基酸。为了产生高病毒滴度的vsv假型,请制备编码s蛋白c端截短形式的质粒,因为已经证明c端19个氨基酸的截短可导致s蛋白有效掺入vsv颗粒中,然后,vsv假型显示出对靶细胞有很强的感染能力。
7.vsvg-gfp是带有vsv-g蛋白的vsv假型,其中vsv-g基因被gfp基因取代。具有vsv-g蛋白的假型被用作“种子”病毒,以产生带有vsv假体的s蛋白。vsvg-gfp系统从美国biogeninc公司购买。
8.0.22μm孔径无菌过滤器。
9.用于检测gfp表达的荧光显微镜。
10.elisa试剂盒用于分析炎症细胞因子在细胞培养液中含量。
二、实验方法
1.重组质粒的构建
covid-19刺突蛋白的氨基酸438-506被定位为ace2结合域(rbd)。以含人密码子优化的covid-19刺突蛋白编码序列的质粒puc18-s作为模板,通过pcr扩增编码rbd的cdna片段,引物(正向:5'-ggcgctagccatcaccaacctgtgcccc-3',含有nhei识别位点;反向:5'-cgcggatccgtcacggtggcgggggcgttc-3',含有bamhi识别位点)。用nhei和bamhi消化pcr产物,然后将其克隆到peak13表达载体cd5抗原前导肽下游和igg1(fc)fc部分上游,peak13表达载体也用nhei消化和bamhi。所得重组质粒命名为peak13-rbd-fc。
2.稳定表达rbd-fc细胞系建立
转染前一天,将hek293细胞用胰蛋白酶消化,并以每孔1×105细胞的密度接种到6孔板中。第二天,按照试剂公司说明书操作步骤,用lipofectaminetm2000(invitrogen)将经avrii线性化的0.5μgpeak13-rbd-fc质粒或等体积的h2o转染到hek293细胞。48小时后,将等分的转染细胞转移至含有浓度递增的嘌呤霉素(0.3、0.4、0.5、0.6和0.7μg/ml)的选择培养基中。3天后,选择合适嘌呤霉素浓度筛选的转染hek293细胞,在该浓度下,peak13-rbd-fc质粒转染的细胞存活,但经h2o转染的细胞全部死亡,用有限稀释度的方法将peak13-rbd-fc质粒转染的细胞转移至96孔板中。培养10天后,使用抗人igg过氧化物酶偶联抗体(sigma),通过elisa测定法选择rbd-fc表达量最高的细胞用于生产重组蛋白rbd-fc。
3.酶联免疫吸附实验(elisa)
将来自每个rbd-fc-293细胞克隆的2×105细胞接种到6孔板中,并用2ml培养基(含有10%fbs的dmem)培养72小时。用elisa测定法定量培养上清液中rbd-fc蛋白的浓度,利用试剂盒bdopteiatm(bdbiosciences),按照试剂公司说明书的操作步骤,简而言之,将96孔平底eia/ria板(纽约州康宁)在4℃下用100μl培养基,在培养液(10ng至30μg/ml)中连续稀释的人igg标准品包被过夜每个rbd-fc-293细胞克隆的培养上清液。然后,将孔用洗涤液洗涤一次,在室温下用测定稀释剂封闭1小时,然后用洗涤液洗涤3次。接下来,在每个孔中加入在assaydiluent(1:5000)中稀释的抗人igg过氧化物酶结合的抗体(sigma),并在室温下轻轻搅拌1小时。洗涤三次后,将100μl底物试剂添加到每个孔中,并将孔在室温黑暗中孵育30分钟。最后,使用终止溶液终止反应,并在450nm的波长下监测显色。
4.蛋白质纯化
收集rbd-fc-293细胞的培养上清液,并在8小时内用溶液(20mm磷酸钠和1mmedta,ph7.0)透析。在4000rpm离心30分钟后,将上清液通过0.45μm杜拉孔膜滤器(millipore,爱尔兰)过滤。按照说明书的步骤操作,用hitrapproteinahp5ml色谱柱(gehealthcareamershambiosciencesab)和econotm梯度泵管试剂盒(美国bio-rad)进行rbd-fc蛋白的纯化。简而言之,首先用10倍柱体积的结合缓冲液(20mm磷酸钠,ph7.0)以5ml/min的流速洗涤该柱。然后将细胞培养上清液泵送到柱上。接下来,用20倍柱体积的结合缓冲液洗涤该柱,然后用上清液洗涤。最后用2-5倍柱体积的洗脱缓冲液(0.1m甘氨酸,ph3.1)洗脱rbd-fc蛋白。将中和缓冲液(60–200μl,1mtris–hcl,ph9.0)添加到每个收集管中。使用hitrapproteinahp1ml色谱柱(gehealthcareamershambiosciencesab)进一步纯化rbd-fc蛋白。根据说明书操作步骤,使用蛋白质测定染料试剂浓缩液(bio-rad)确定蛋白质浓度,其中以牛血清白蛋白(bsa)为标准。
5.rbd-fc与受体ace2的结合抑制测定
通过流式细胞仪技术测量药物对rbd-fc与细胞受体ace2结合的抑制作用。收集分离2x106个表达ace2的293t细胞,并用hbss(sigma-aldrich)洗涤。在加或不加50μg/ml药物的情况下,用1μg/mlrbd-fc处理细胞,然后将这些细胞在室温下孵育30分钟。用hbss洗涤细胞,并在室温下以1/50稀释度与抗人igg-fitc一起温育30分钟。洗涤后,将细胞用pbs中的1%甲醛固定,并用cellquest软件在facscalibur流式细胞仪(bdbiosciences)中进行分析。
6.表达ace2细胞系建立
用携带ace2基因的ptarget质粒(promega)pcdna转染at2细胞,然后用含有g418的培养基进行筛选得到高表达ace2的细胞(at2-ace2)。这些细胞在5%胎牛血清的dmem培养基中生长和保存。
7.假病毒vsv-covid-19-s蛋白假病毒的构建
为了构建产生covid-19-s蛋白假型的vsv,首先构建了一编码全长covid-19-s蛋白表达质粒。用正向引物s-bam-f(5'-ggatccaagtgatattcttgttaacaac-3')和反向引物s-bam-r(5'-ggatccaagagtaaaaaattccatcat-3c)扩增covid-19-s蛋白的cdna,并将其克隆到表达载体pks336。再使用正向引物s-bam-f和反向引物s-bam19r(5'-gggatccttagcagcaagaaccacaagagcatg-3')从pks-sars-s中扩增出c末端截短的covid-19-s蛋白的cdna,然后克隆至pks336。所得质粒pks-covid-19-st19,除了c末端19′aa外,还编码全长covid-19-s蛋白。用表达质粒pks-covid-19-st19转染293t细胞后,在细胞膜上检测到s蛋白的表达。为了产生具有c端截短的covid-19-st19蛋白的vsv假型,将vsvδg*接种到转染了pks-sars-st19的293t细胞上。vsvg-gfp用作阳性对照,从用pks-covid-19-st19转染的293t细胞获得的covid-19-s蛋白vsv假型,即vsv-covid-19-st19,可以有效感染肺部上皮细胞。vsv-covid-19-st19的效价为5.0×105iu/ml。
8.vsv-covid-19-st19进入细胞的检测
为了检测vsv-covid-19-st19对靶细胞的感染能力,进行了gfp表达的时间依赖性分析。用vsv-covid-19-st19感染24孔玻璃载玻片上的单层肺泡细胞。在不同的时间点感染病毒,荧光显微镜下拍摄细胞。使用imagej软件(http://rsb.info.nih.gov/ij/)对照片中表达gfp的细胞的数目进行计数。由于伪病毒无法产生后代病毒,因此该系统可用于评估vsv-covid-19-s蛋白介导的细胞进入机制。对gfp阳性细胞数量进行时程分析表明,在病毒感染6小时后可以定量vsv-covid-19-st19感染。
9.ace2和tmprss2的mrna测定
利用所用定量qpcr仪lightcycler(rochediagnostics),按照试剂公司说明书操作步骤,用试剂盒从用不同浓度的药物处理过的病毒感染细胞中提取总rna。用引物5′-ctctacggaccaaacttcatc-3′和5′-ccactattccttggctagagtaa-3′扩增tmprss2mrna。用引物5'-ccgtatcaatgatgctttccg-3'和5'-cagtgaagatcaggatgacaatg-3'扩增ace2。
10.炎症细胞因子的测定
利用不同浓度药物处理感染病毒细胞24小时后,收集细胞培养上清液。利用高灵敏度elisa试剂盒(quantikinetmhs,r&dsystems),按照试剂公司说明书操作步骤检测细胞培养液中细胞炎症因子tnf-a、il-6和il-2等含量。绘制标准曲线计算灵敏度。
三、实验结果
1.利用流式细胞仪测定一清颗粒对新型冠状病毒的刺突蛋白rbd与其靶细胞受体ace2结合的影响,结果发现一清颗粒能明显抑制新型冠状病毒刺突蛋白rbd与受体ace2结合,并且有剂量依赖效应(见图1)。这表明一清复方制剂能抑制新型冠状病毒进入细胞。
2.利用实时定量qpcr测定一清颗粒对新型冠状病毒靶细胞tmprss2mrna表达的影响,结果发现一清颗粒对感染病毒细胞的tmprss2表达有明显抑制作用,而且具有剂量依赖效应(见图2)。这表明一清复方制剂能通过抑制ii型跨膜丝氨酸蛋白酶(tmprss2)表达而抑制新型冠状病毒刺突糖蛋白与靶细胞受体ace2结合以阻止病毒进入靶细胞。
3.利用一清颗粒处理假型病毒vsv-covid-19-st19/gfp感染的肺泡ⅱ型上皮细胞(at2),在荧光显微镜下检查病毒的量(gfp表达量),结果发现一清颗粒能使病毒进入细胞的量明显减少(见图3-1和3-2)。这表明一清复方制剂能阻止病毒感染细胞。
4.利用病毒梯度法测定一清颗粒对新型冠状病毒进入细胞的影响,结果发现一清颗粒对病毒感染肺泡上皮细胞有明显的抑制作用,并且有剂量依赖效应(见图4)。这表明一清复方制剂对病毒进入肺泡上皮细胞有明显抑制作用,临床可以预防和治疗新型冠状病毒。
5.利用酶联免疫反应(elsa)定量测定一清颗粒对肺泡ii型细胞感染病毒后产生炎症因子的影响,结果表明一清颗粒能降低病毒感染细胞产生炎症因子(il-2,il-6,tnf-a,il-8和cxcl-10)的量,并有剂量依赖效应(见图5)。这表明一清复方制剂可以用于临床治疗新型冠状病毒感染引起的炎症风暴。
- 还没有人留言评论。精彩留言会获得点赞!