包载大蒜素的细胞微颗粒载药系统及其制备方法和应用与流程
本发明属于医药
技术领域:
,特别是涉及一种包载大蒜素的含药细胞微颗粒载药系统、其制备方法与在抗肿瘤肺转移中的应用。
背景技术:
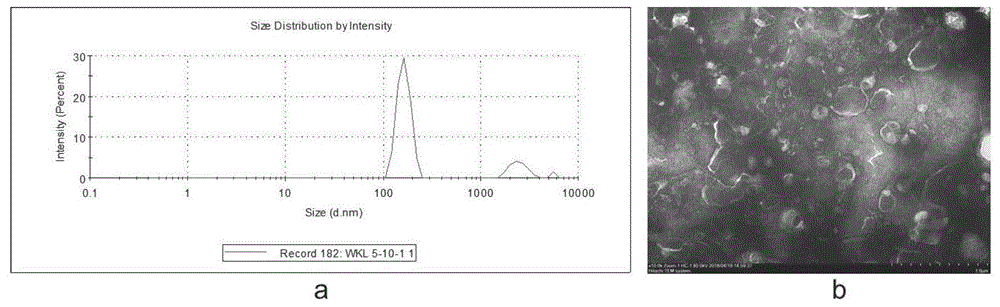
:肿瘤转移是临床致死的重要原因,约有90%的恶性肿瘤死于肿瘤远端转移。肿瘤细胞浸润到周围的组织,通过血液系统和淋巴系统扩散到机体的其他组织器官形成转移,最终导致患者死亡。肺是所有恶性肿瘤最主要的转移靶器官,约有30%-54%的恶性肿瘤在自然病程中发生肺转移。据尸检报告,几乎1/3死于癌症的患者均伴有肺转移。现有的抗转移治疗策略多限于原位切除加广谱化疗但效果不佳的原因主要在于:化疗药物选择性差,无法识别转移灶的肿瘤细胞,从而导致全身性的机体损伤和免疫抑制。大蒜有机硫化物大蒜素是中药大蒜(alliumsativuml.)抗肿瘤活性最强的活性成分,本课题组前期研究发现大蒜素具有良好的体内外抗肿瘤转移的潜能:可抑制乳腺癌细胞迁移和侵袭;在mda-mb-231裸鼠乳腺癌原位转移模型和实验性转移模型中减少裸鼠肺部肿瘤结节的数目,抑制癌细胞远端转移;在小鼠黑色素瘤实验性转移模型中抑制paf介导的肺转移。抑制肺转移的机制可能与其干预了肿瘤微环境相关:大蒜素通过降低缺氧诱导的肿瘤血管生成,抑制核转录因子nf-κb的转录调控以及mmp2/9的表达,抑制肿瘤细胞mapk的活化,调控细胞外基质重构,以及降低炎症因子tnf-α、il-6等因子的水平等。综上,大蒜素不仅能直接抑制肿瘤细胞的转移恶性生物学行为,并且可通过改善肿瘤微环境的作用从而抑制肿瘤转移的发生。然而,由于大蒜素的理化性质普遍较差,易挥发不稳定,现有的载药系统虽部分解决了上述的问题,但仍无法实现精准靶向运输致转移灶,更好地发挥其抗肿瘤转移的作用。细胞微颗粒是细胞分泌的具有双层脂质膜结构的一种微小囊泡,直径约为100-1000nm。研究表明,这种胞外的囊泡是由膜脂与膜蛋白构成的生物膜围绕,其结构和成分均类似于细胞膜。其中,膜脂成分中较细胞膜相比,富含胆固醇,神经酰胺,鞘磷脂及脂筏结构。微颗粒能够将携带的多种蛋白质、mrna、mirna等传递给相应的细胞或组织,参与并维持许多正常的生理功能,如组织修复、免疫监视、和凝血等。近年来的研究发现,微颗粒可作为一些小分子药物的载体用于某些疾病的治疗。细胞微颗粒作为药物传递载体呈现出多种优势:首先,其来源于病人自身的细胞,因此在药物传递过程中减少了免疫原性;其次,作为一种膜结构载体,微颗粒具有与脂质体类似的结构,能够通过其表面的膜蛋白与靶细胞膜融合,从而将其负载的药物直接运送到受体细胞中,避免了细胞吞噬-溶酶体途径带来的药物降解及细胞毒性等问题;此外,不同来源的微颗粒因其供体细胞的差异性而呈现出不同的特性,即具有特定的器官亲和性,如肺转移肿瘤细胞衍生的微颗粒因其表面表达整合素α6β1和α6β4因而会特定的到达肺部,并被宿主肺部组织的细胞如肺上皮细胞、肺部肿瘤细胞等摄取。因此,如果能够将药物装载在这种具有特定功能性的微颗粒中,则有可能实现器官靶向治疗肿瘤转移的疗效。技术实现要素:本发明提供了一种精准靶向肿瘤转移灶的载药系统,该载药系统是将具有抗肿瘤转移作用的活性成分大蒜素荷载入高肺转移肿瘤细胞衍生的微颗粒中,该载药系统能够精准靶向转移灶,最终提高了药物的抗肿瘤转移的疗效,实现肿瘤转移的精准治疗。针对上述发明目的,本发明提供以下技术方案:一种包载大蒜素的细胞微颗粒载药系统,其包含提取自器官亲和性的细胞的微颗粒和具有抗肿瘤转移活性的药物,所述药物为大蒜有机硫化物。进一步的,所述的器官亲和性的细胞种类为肺转移肿瘤细胞;可为小鼠黑色素瘤肺转移细胞b16bl6、b16f10、小鼠lewis肺癌细胞llc、乳腺癌mda-mb-231肿瘤细胞或小鼠乳腺癌细胞4t1等。所述的大蒜有机硫化物可为二烯丙基三硫化物dats、二烯丙基二硫化物dads、二烯丙基一硫化物das、烯丙基半胱氨酸sac、s-烯丙基-l-半胱氨酸亚砜acso中的一种。本发明的另一目的在于提供上述载药系统的制备方法,包括:取对数生长期的肺转移肿瘤细胞,刺激肿瘤细胞释放微颗粒,在肿瘤细胞处于刺激状态下加入大蒜有机硫化物溶液与细胞进行共孵育,孵育完成后,取细胞培养上清液离心,获取含大蒜有机硫化物微颗粒沉淀,即包载大蒜素的细胞微颗粒。现有技术一般提取外囊泡后再与药物共孵育,但针对大蒜有机硫化物,这种方式载药量偏低,裂解后的药物浓度低于检测值。本发明的方式给予细胞一定刺激,而不让细胞产生凋亡,在细胞处于刺激状态下同时加入药物,促使细胞产生更多的含药微颗粒。进一步的,本发明采用紫外照射的方式刺激肿瘤细胞;优选的,紫外照射的时间为1~2h,在这个时间范围内微颗粒达到合适的释放量,超过2h则会出现细胞死亡。进一步的,所述的大蒜有机硫化物溶液的孵育浓度为10μm~200μm;优选60~120μm。进一步的,所述的共孵育时间为1~24h。进一步的,孵育完成后,取细胞培养上清液离心,弃除沉淀,取上清液再次离心,获取含大蒜有机硫化物微颗粒沉淀。本发明的又一目的在于提供上述载药系统在制备抗肿瘤转移药物中的应用。本发明利用高肺转移肿瘤细胞衍生的细胞微颗粒构建大蒜素-细胞微颗粒递药系统,其具有器官亲和性(转移灶靶向性)又具有载药功能,有效增强了靶向转移灶的功能,优化了组织亲和力。由于该体系提高了药物在肺组织中的分布,进而表现出更为出色的抗肿瘤肺转移的治疗效果。具体而言,大蒜素-含药细胞微颗粒的抗肿瘤肺转移活性明显优于对照的裸药,展现出极高后续的应用价值和潜力。与现有技术相比,本发明具有以下优点:1.大蒜素作为药食同源的中药大蒜的活性成分,含量丰富,经济成本低,具有显著的抗癌活性和抗肿瘤转移作用。大蒜素可作用于肿瘤细胞,抑制肿瘤细胞的迁移、侵袭能力,发挥抗肿瘤转移的功效;大蒜素还可作用于肿瘤微环境,其抗氧化、抗炎能够抑制肿瘤微环境中炎性细胞的浸润、降低炎性因子的释放,改善局部组织炎性程度,在此基础上实现对肿瘤转移的有效抑制。大蒜素因其来源于药食同源的大蒜,相对于目前常规的药物,具有毒性低,多靶点的优势。2.大蒜素-细胞微颗粒递药系统构成合理,所述微颗粒来自肿瘤细胞的上清液,其来源于生物系统,具有较好的生物相容性和安全性。该载药系统优化了组织分布特性,提高了药物在转移灶的分布,使其能够被肿瘤细胞和肺组织的宿主细胞肺上皮细胞摄取,从抑制肿瘤细胞恶性生物学行为和干预局部组织炎性微环境两方面共同产生抗肿瘤转移的作用,达到增效的制剂目标。附图说明图1为本发明所述的dats-微颗粒分散于水后的粒径分布及形态特征图。图2为本发明所述的dats-微颗粒被小鼠黑色素瘤细胞b16bl6细胞和小鼠肺上皮细胞tc-1细胞的摄取图。图3为本发明所述的dats-微颗粒在小鼠黑色素瘤肺转移模型中的组织分布图。图4为本发明所述的dats-微颗粒对小鼠黑色素瘤肺转移模型的影响图。图5为本发明所述的dats-微颗粒对小鼠肺组织炎性蛋白表达的影响图。具体实施方式下面将通过几个具体实施例,进一步阐明本发明,这些实施例只是为了说明问题,并不是一种限制。实施例1dats-含药微颗粒的制备、表征及载药量检测取对数生长期的b16bl6细胞4×107个/ml,紫外照射1h,加入浓度为60μm的dats,在培养箱中继续孵育10h,收集细胞培养上清液,在14000g,4℃条件下,离心2min,弃去沉淀,取上清,14000g,4℃条件下,离心70min,得到含dats微颗粒沉淀,即dats-含药微颗粒。制备所得的dats-含药微颗粒为白色沉淀于离心管底部。取dats-含药微颗粒10μl,用纯水稀释至1ml,缓慢注入马尔文粒径测定仪的样品池中,测定dats-微颗粒各自的平均粒径、多分散系数(pdi)及电位。测得微颗粒的粒径为(298.36±3.76)nm,多分散系数为(0.53±0.18),微颗粒粒径分布较广(图1a),zeta电位为(-20.21±3.52)mv。吸取dats-微颗粒20μl,分别滴至载有formvar支持膜的铜网上,5s后滤纸吸干,再滴加20μl1%磷钨酸,5s后滤纸吸干,红外灯下干燥,最后置于jem-2100型透射电镜下观察微乳粒子的形态。电镜观察,dats-mes呈类球形,外观较为圆整,分散较均匀(图1b)。通过bca和hplc分别检测含药微颗粒的蛋白含量以及裂解后药物的浓度,计算载药量,测得裂解后的药物浓度为4.77μg/ml,载药量为0.17%。采用同样的方法调整大蒜有机硫化物浓度,载药量如表1所示:表1大蒜素浓度(μm)103060120200240载药量(%)0.09±0.010.12±0.020.17±0.010.18±0.020.12±0.020.03±0.01大蒜有机硫化物浓度低于10μm时,载药量较低,而高于200μm时则诱发肿瘤细胞死亡。实施例2dats-含药细胞微颗粒被细胞的摄取情况和体内组织分布情况1.dats-微颗粒载药系统被b16bl6及tc-1细胞的摄取研究空白微颗粒提取:取对数生长期的b16bl6细胞4×107个/ml,紫外照射1h,在培养箱中继续孵育10h,收集细胞培养上清液,在14000g,4℃条件下,离心2min,弃去沉淀,取上清,14000g,4℃条件下,离心70min,即得blankmps。pkh26-dats-微颗粒制备:取dats-微颗粒,将其均稀释成总蛋白浓度为800ug/ml,取dats-mps0.1ml,重悬在0.5ml的diluentc中,记为a,取2μl的pkh26加入到0.5ml的diluentc中,记为b,然后将a与b混合,25℃孵育3min,然后加入等体积血清,终止反应,然后dats-mps混合液在14000g条件下离心,去上清,重悬,用pbs清洗3遍,去除未结合染料,即得pkh26-dats-微颗粒。b16bl6及tc-1细胞均分为2组,分别加入blankmps、dats-mps,2h后,将各孔中培养基吸出,pbs洗三遍,在荧光显微镜下观察各组细胞中摄取情况结果,用流式细胞仪测定各组相对吸光度值。结果显示,tc-1及b16bl6细胞均能有效摄取含药微颗粒,其中b16bl6的摄取能力更强(图2)。2.dats-微颗粒载药系统在小鼠体内分布情况模型的建立:取对数生长期b16bl6细胞,用含edta的0.25%胰酶消化液进行消化,于培养箱中孵育2min,待细胞在显微镜下变圆时,立即加入dmem完全培养基终止消化,细胞吹打均匀后,转移至离心管中,于1000r/min离心5min,弃上清,收集离心管底部细胞,用灭菌的pbs溶液将细胞制成细胞悬液,并将细胞密度调整至1×106/ml。制备好的细胞悬液,迅速进行接种。用酒精棉球擦拭小鼠左后足注射区域,将细胞悬液吹打均匀,用1.0ml一次性医用注射器迅速在每只c57bl/6小鼠左后足皮下注射0.05ml新鲜制备的b16bl6细胞悬液。小鼠接种肿瘤细胞后23天,对小黑鼠进行原位肿瘤切除手术,即对小鼠左后足进行截肢手术处理,操作台、棉麻绳、手术剪刀进行消毒处理,用棉麻绳绑紧小鼠左后足脚踝上部,用手术剪刀沿麻绳部位以下迅速剪下小鼠左后足,然后用碘伏对截肢部位进行消毒处理,原发位肿瘤手术切除可以促进小鼠黑色素瘤进行肺转移。给药制剂的制备:空白微颗粒提取:取对数生长期的b16bl6细胞4×107个/ml,紫外照射1h,在培养箱中继续孵育10h,收集细胞培养上清液,在14000g,4℃条件下,离心2min,弃去沉淀,取上清,14000g,4℃条件下,离心70min,即得blankmps。pkh26-dats-微颗粒制备:取dats-微颗粒,将其均稀释成总蛋白浓度为800ug/ml,取dats-mps0.1ml,重悬在0.5ml的diluentc中,记为a,取2μl的pkh26加入到0.5ml的diluentc中,记为b,然后将a与b混合,25℃孵育3min,然后加入等体积血清,终止反应,然后dats-mps混合液在14000g条件下离心,去上清,重悬,用pbs清洗3遍,去除未结合染料,即得pkh26-dats-微颗粒。小黑鼠分为正常小鼠组和黑色素瘤肺转移模型小鼠组,分别给予pkh26-free及pkh26微颗粒。小黑鼠提前一天进行腹部脱毛处理,禁食禁水24h后,取pkh26-free组及pkh26-微颗粒组各0.5ml,通过尾静脉注射入小鼠体内,给药完毕后小黑鼠置于异氟烷的气雾压力为200mmhg的腔体中进行麻醉,5~10min后将小鼠俯卧位平放于小动物活体成像系统的记录暗箱中,分别在给药后1、4、8h进行活体成像记录,并于8h后解剖各组小黑鼠取肺,于记录暗箱中观察小黑鼠肺部荧光分布情况。结果见图3,小黑鼠活体成像中,无论是正常小鼠体内,还是黑色素瘤肺转移模型小鼠体内,pkh26-free组与pkh26-微颗粒组在1、4、8h均难以看出明显的差别,但在8h解剖小鼠后,小黑鼠肺部的红外图中可以看出,在正常小鼠及黑色素瘤肺转移模型小鼠体内,游离的pkh26染料组均未在小鼠肺中聚集,pkh26微颗粒则均在肺上观察到了荧光显示,表明小鼠黑色素瘤细胞b16bl6无论在正常小鼠还是黑色素瘤肺转移小鼠体内,均具有很好的肺靶向作用。实施例3dats-微颗粒对小鼠黑色素瘤肺转移的治疗作用评价及炎性微环境的干预将体重在18g左右的c57bl6小黑鼠适应性饲养7d后,从尾静脉注射5×105/ml的b16bl6黑色素瘤细胞,小黑鼠接种肿瘤细胞后,将各组小黑鼠随机分为模型组,空白微颗粒组,dats-微颗粒以及dats裸药组,每组5只。每天称量小黑鼠体重,观察并记录动物的状态及死亡情况,23天后开始给药,腹腔注射,给药浓度为1.8mg/kg,隔天给药,14天后摘眼球取血,脱颈椎处死小黑鼠,解剖,取小鼠肺组织,并计算内脏指数(组织/体重)。结果表明,das-微颗粒可以有效抑制肺转移,降低肺重。对剥离的肺组织进行h&e染色,结果表明,dats-微颗粒与裸药相比更多的减少肺结节数目,减少肺部转移的肿瘤面积,显著降低肺转移(图4)。进一步检测肺组织的炎性蛋白mpo、fibronectin、mrp8等,结果表明,本发明所述的dats-微颗粒能够降低炎性蛋白的表达(图5)。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1
- 用于治疗中性粒细胞减少症的组合物和方法与制造工艺
- 一种检测与结直肠癌靶向用药西妥昔单抗治疗敏感性相关基因的多态性的试剂盒及其应用的制造方法与工艺
- 酶法制备明胶工艺的制造方法与工艺
- 原细纤维结合抗体及其治疗和诊断帕金森氏症、路易体痴呆和其他α‑共核蛋白病的应用的制造方法与工艺
- 一种壳聚糖基多层纳米纤维膜敷料及其制备方法和应用与制造工艺
- 一种罗氟司特纳米粒、制剂及其制备方法与制造工艺
- 中性粒细胞明胶酶相关脂质运载蛋白检测试剂盒的制造方法与工艺
- 一种纤维结合蛋白检测试剂盒的制造方法与工艺
- 经取代的双环二氢嘧啶酮及其作为嗜中性粒细胞弹性蛋白酶活性的抑制剂的用途的制造方法与工艺
- 一种治疗阑尾炎的药物及其制备方法与制造工艺