一种溶酶体作为制备治疗蛋白错误折叠或加工类疾病药物领域的应用的制作方法
本发明细胞修复领域,涉及溶酶体作为制备治疗蛋白错误折叠或加工类疾病药物领域的应用。
背景技术:
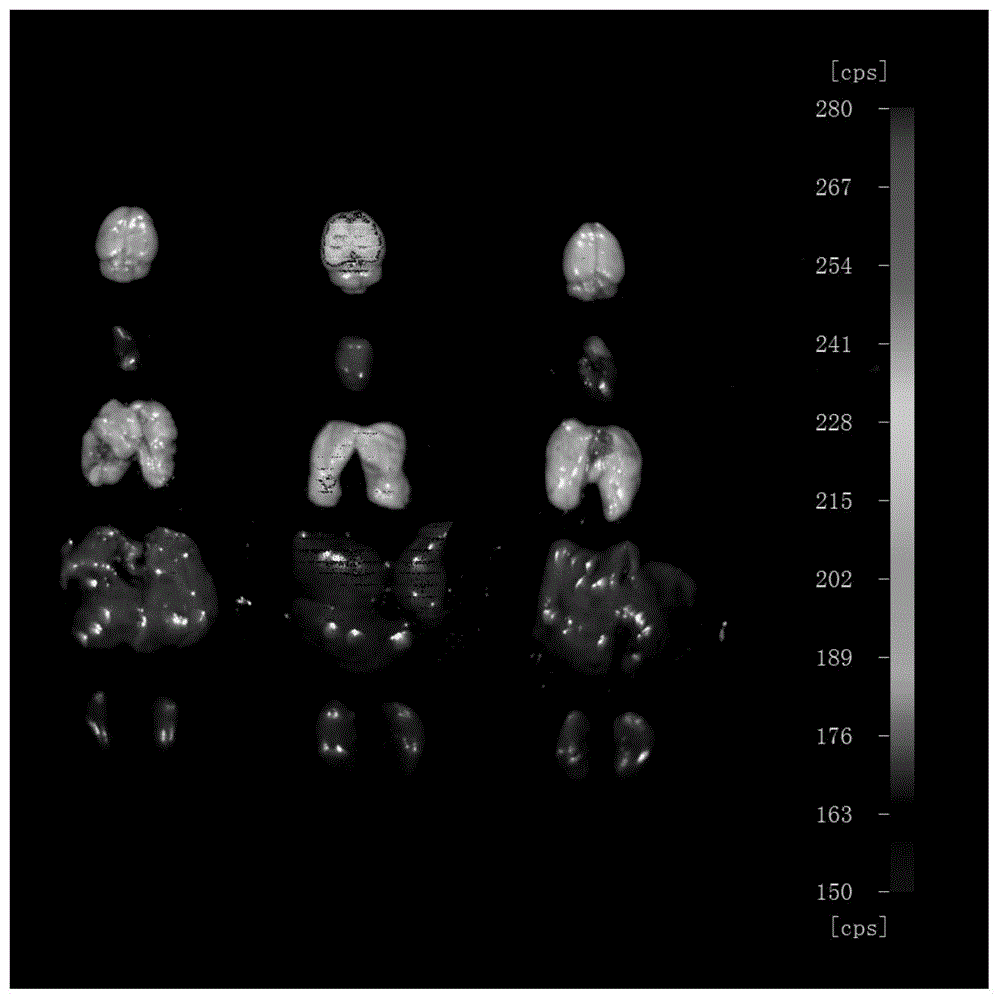
:神经系统的复杂性使很多药物无法进入大脑,而神经细胞的自我修复能力有限,这造成许多神经系统疾病的不可逆转和进行性,最终导致结果的严重性,造成巨大的经济损失和社会负担(fernandeslf,bruchge,massensiniarandfrézardf.recentadvancesinthetherapeuticanddiagnosticuseofliposomesandcarbonnanomaterialsinischemicstroke.frontneurosci.2018;12:453.)。阿尔兹海默症(ad)、帕金森综合征(pd)、亨廷顿氏症(hd)都是高发病率的中枢神经系统疾病,这些疾病的病因都是蛋白异常折叠或加工,导致神经元死亡,病情发展后严重影响病人的生活和寿命。ad是痴呆症最常见的一种形式,它的主要症状有两个:β-淀粉样蛋白在神经元细胞外异常沉积形成老年斑和tau蛋白异常磷酸化形成神经元纤维缠结(cheraym,stratouliasv,josephbandgrabertk.therulesofengagement:domicrogliasealthefateintheinverserelationofgliomaandalzheimer'sdisease?frontcellneurosci.2019;13:522.)。其致病原因在于:淀粉样蛋白(app)作为i型跨膜蛋白,具有膜受体样结构,分子间可以进行反式二聚化,促进细胞黏附。但app的降解产物β-淀粉样蛋白可以加速app的聚集,引发细胞凋亡。tau蛋白作为微管相关蛋白可促进微管蛋白聚合形成微管,维持微管稳定性,降低微管蛋白分子的解离,并诱导微管成束。而tau蛋白异常过度磷酸化,会丧失维持微管稳定的作用,导致微管结构广泛破坏,正常轴突转运受损,引起突触丢失神经元功能损伤,发生脑神经退行性病变。伴随着脑内淀粉样前体蛋白和tau蛋白的异常折叠与加工,ad患者神经突触变性,记忆力和其他认知功能逐渐下降。pd是一种慢性进行性神经退行性疾病,它的特征是细胞内蛋白——α-突触核蛋白(α-synuclein)的广泛传播和黑质致密部中多巴胺能神经元的早期突出死亡(radhakrishnandmandgoyalv.parkinson'sdisease:areview.neurolindia.2018;66:s26-s35.)。其致病原因在于:正常的α-synuclein呈无序单体状态,在调整膜脂成分结构和囊泡转运过程中发挥作用。而在各种因素的影响下,α-synuclein异常表达和聚集,参与形成路易小体,产生氧化应激,会导致多巴胺能神经元死亡(kalialv,diagnosticbiomarkersforparkinson'sdisease:focusonα-synucleinincerebrospinalfluid.parkinsonismrelatdisord.2019;59:21-25.)。hd是常染色体显性遗传性神经退行性疾病,它的特征是亨廷顿蛋白(htt)n端序列中的谷氨酰胺序列(polyq)异常扩增(saudoufandhumberts.thebiologyofhuntingtin.neuron.2016;89(5):910-26.)。其致病原因在于:正常的htt蛋白是纺锤体定向及神经发生的重要因素,而突变的htt蛋白基因组特定区域胞嘧啶-腺嘌呤-鸟嘌呤三核苷酸重复序列因动态突变发生病理性扩增引起polyq链异常延长,导致伴有步态障碍的舞蹈样运动,运动迟缓和僵硬,认知减慢,注意力和心理灵活性下降。除hd外,三核苷酸重复序列疾病还有脊髓延髓肌萎缩症,齿状核红核蛋白球路易体萎缩,脊髓小脑共济失调。现有技术中,包括抗炎药、他汀类药物、激素疗法和螯合剂等在内的治疗方法均未能取得成功;而降低神经变性速率或停止疾病进程的疾病缓解疗法仍然难以捉摸(waitelm.treatmentforalzheimer’sdisease:hasanythingchanged?austprescr.2015;38(2):60–63.)。现有研究表明纳米材料的独特性能使它们能够进入大脑发挥治疗作用。但是,它们也可能引起意想不到的影响,纳米材料的稳定性及代谢毒性是纳米材料进入临床试验的主要限制因素。氧化应激可引起免疫毒性和遗传毒性,表观遗传修饰带来的毒性可能导致对表观基因组的不利影响。因此,虽然部分纳米材料在动物实验中有一定成效,但纳米材料的安全性和毒理学仍是社会各界的重点关注问题,还需开发改进标准化的检测方法来进行监测(dusinskam,tulinskajelyamaninetal.immunotoxicity,genotoxicityandepigenetictoxicityofnanomaterials:newstrategiesfortoxicitytesting?foodchemtoxicol.2017;109:797-811.)。有文献报道过,线粒体能够到维持蛋白质合成和蛋白质清除之间的平衡的作用。但是对于在后生动物中,线粒体基因组(mtdna)是一个小的圆形分子,平均长度为16.5kb(chongra,etal.polymorphicduplicategenesandpersistentnon-codingsequencesrevealheterogeneouspatternsofmitochondrialdnalossinsalamanders.bmcgenomics.2017.),是一种新兴的表型特征和疾病的决定因素。尽管mtdna的基因含量在进化上是保守的,但它们的基因序列却呈现多样性,并以严格的母系遗传方式在受精卵线粒体群中遗传(stjohnjc,etal.theassociationofmitochondrialdnahaplotypesandphenotypictraitsinpigs.bmcgenet.2018.)。因此,外源线粒体给予可能对机体产生如下影响:1、外源mtdna自身的复制带来的随机损失会可能使机体自身内源mtdna丢失;2、增多的mtdna暴露于诱变的活性氧产生基因突变的可能性增大;3、增多的mtdna突变可能进一步导致衰老及其它相关退行性疾病;4、突变的mtdna可能随着卵母细胞遗传给下一代(allenjf,etal.mitochondrialgenomefunctionandmaternalinheritance.biochemsoctrans.2013.)。综上所述,针对蛋白错误折叠和加工类疾病的治疗,现有药物疗法不能有效延缓疾病进展,动物模型中有效的纳米材料的毒理学未知。因而,亟需一种细胞毒性低,安全且有效的药剂和治疗方法,以解决现有技术中的问题。技术实现要素:本发明所要解决的技术问题是提供一种细胞毒性低,安全且有效的药剂和治疗方法。本发明公开了一种溶酶体作为制备治疗蛋白错误折叠或加工类疾病药物领域的应用,用于治疗蛋白错误折叠或加工类疾病。进一步地,所述治疗蛋白错误折叠或加工类疾病,包括阿尔兹海默症、帕金森综合征、亨廷顿氏症、疯牛病、克雅氏综合征、皮层纹状体脊髓变性、肌萎缩性侧索硬化症、脊髓小脑共济失调症、囊性纤维化、遗传性白内障、ⅱ-型糖尿病、常染色体显性遗传肾小管间质性肾病中至少一种。本发明还公开了一种治疗蛋白错误折叠或加工类疾病的药物,包括溶酶体。优选地,所述溶酶体提取自bv2细胞。优选地,所述溶酶体的浓度为5-55μg/ml。优选地,所述溶酶体的浓度不高于500μg/ml。本发明的有益效果在于:1、提供了一种新的治疗蛋白错误折叠或加工类疾病的途径;2、原料获取容易,成本低;3、具有靶向性,且不存在细胞毒性;4、利用的细胞器不含有遗传物质,不会对受体产生不良影响。附图说明图1溶酶体在不同器官中的聚集测试图;图2溶酶体在不同样本脑部中的靶向聚集测试图;图3溶酶体细胞毒性测定表;图4溶酶体对细胞外环境的影响表;图5溶酶体对脑部海马的毒性蛋白的降解测试表;图6溶酶体对皮层的毒性蛋白的降解测试表;图7溶酶体改善阿尔兹海默症小鼠对事物的识别能力数据表;图8溶酶体改善阿尔兹海默症小鼠对事物的记忆能力数据表;图9溶酶体改善阿尔兹海默症小鼠筑巢能力数据表;图10大浓度溶酶体对脑部海马的毒性蛋白的降解作用;图11溶酶体对帕金森症相关毒性蛋白的降解测试表。具体实施方式下面结合实施例对本发明的具体实施方式作进一步描述,以下实施例仅用于更加清楚地说明本发明的技术实施例,而不能以此来限制本发明的保护范围。提取溶酶体溶酶体提取方法根据市售溶酶体提取试剂盒说明书进行。具体步骤如下:1、离心洗涤。0.25%胰蛋白酶消化收集2-5×107个细胞,用pbs离心洗涤;2、细胞破壁。离心后弃上清,将细胞沉淀置于冰上,加入400μl细胞胀破缓冲液,在冰上静置10min;利用匀浆器匀浆30-40下,收集匀浆产物至一新离心管中;3、离心分离溶酶体。按下述顺序梯次离心,每次离心后均取上清液,并移至新离心管中进行下一步:1000×g下离心5min——3000×g下离心10min——5000×g下离心10min——20000×g下离心30min;最后一次离心后取沉淀,并用洗涤缓冲液悬起,再次20000×g下离心30min,得到沉淀称重后利用储存液悬起,置于冰箱中4℃保存。4、标记并鉴定。向步骤3得到的产物中加入溶酶体标记探针(lysotracker,red),以体积份数计,标记探针:溶酶体悬液=1:20000,2h后取5μl溶酶体悬液,即为标记后的溶酶体。将其滴于载玻片上,盖上盖玻片,封片后在共聚焦显微镜下鉴定。作为实验动物的b6c3f1阿尔茨海默症小鼠(12月龄)和b6c3f1野生型小鼠(6月龄、12月龄)购自华阜康有限公司(北京,中国)。实验期间小鼠在中国医学科学院放射医学研究所实验动物中心饲养。为证明溶酶体在治疗阿尔茨海默症及老年智力衰退方面的作用,设计实施例1-11:实施例1随机选取b6c3f1阿尔茨海默症小鼠(12月龄),并向其尾静脉注射1mg溶酶体标记探针标记后的溶酶体,2h后使用生理盐水灌流,取下主要器官(心、肝、脾、肺、肾、脑)。为了证明溶酶体会靶向富集在病灶部位,特设置如下对比例1-2:对比例1随机选取b6c3f1阿尔茨海默症小鼠(12月龄),并向其尾静脉注射等体积pbs;其他条件与实施例1相同;对比例2随机选取b6c3f1野生型小鼠(6月龄)并向其尾静脉注射等体积pbs;其他条件与实施例1相同。使用小动物成像系统进行荧光成像,酶联免疫检测仪测定吸光度,得到结果如附图1(从右到左依次分别为实施例1、对比例1、对比例2;每列从上到下依次分别为脑、心、肺、肝、肾,其中肝的右侧较小的为脾)所示,实验测试数据如表1:表1溶酶体器官靶向实验数据表由上可知,与其他器官相比较,溶酶体会靶向进入阿尔兹海默症小鼠脑部,并在阿尔兹海默症小鼠脑内积累。对上述荧光成像数据应用graphpad软件进行统计学分析,得到如附图1所示,也进一步印证了上述结论。实施例2实施例2与实施例1相同。对比例3随机选取b6c3f1野生型小鼠(12月龄),并向其尾静脉注射等体积pbs;其他条件与实施例1相同;对比例4随机选取b6c3f1野生型小鼠(12月龄),并向其尾静脉注射1mg溶酶体标记探针标记后的溶酶体;其他条件与实施例1相同;对比例5随机选取b6c3f1野生型小鼠(6月龄)并向其尾静脉注射1mg溶酶体标记探针标记后的溶酶体;其他条件与实施例1相同。使用小动物成像系统进行荧光成像,酶联免疫检测仪测定吸光度,得到结果如附图2(从上到下依次分别为对比例3、对比例4、实施例2、对比例5)所示。实验测试数据如表2:表2溶酶体异常脑靶向实验数据表由上可知,不同类型的鼠相比较,可得到如下结论:通过实施例2与对比例3的比较可知,外源注射的溶酶体会在患病小鼠脑部富集;通过实施例2与对比例5的比较可知,外源注射的溶酶体会在患病小鼠脑部富集,不会在年轻小鼠脑部富集;通过对比例4与对比例5的比较可知,外源注射的溶酶体会在老年小鼠脑部富集,不会在年轻小鼠脑部富集。结合老年小鼠和患病小鼠都会在脑部产生异常蛋白和糖缀合物,可得到如下结论:溶酶体可以靶向进入患病小鼠病灶部位;溶酶体会对延缓老年记忆力衰退产生作用。实施例3-7溶酶体细胞毒性测定:首先按常规方法提取新生鼠原代神经元,将原代神经元按5×106/孔密度接种于96孔板中,每孔100μl,在37℃的co2培养箱孵育。每2-3天换半液,第7天时向96孔板中加入不同浓度的溶酶体(100、200、300、400、500μg/ml)(依次记做实施例3-7)。24小时后,吸弃培养基,向每孔加入1mg/ml的mtt100μl,在37℃的co2培养箱避光孵育4小时。吸弃mtt,向每孔加入150μl二甲基亚砜(dmso),在摇床上避光溶解10分钟。使用酶联免疫检测仪在490nm波长下测定吸光度,计算细胞存活率。应用graphpad软件进行统计学分析(见附图3),组间比较采用t-test比较,无显著性差异。结果显示,溶酶体不会影响细胞的存活率。实施例8溶酶体对细胞外环境的影响:将n2a细胞接种于6孔板中,在37℃的co2培养箱孵育。待细胞铺满孔板80-90%时,在第0、4、6、8、10、12h,分别用含50μg/ml溶酶体的培养基替换相对应的6孔板中的旧培养基培养,期间于37℃的co2培养箱中继续孵育。取各孔培养基至离心管中,用ph测试仪测定溶酶体作用不同时间(0、2、4、6、8、12h)培养基的ph值。(见表3及附图4,其中附图4横坐标表示溶酶体加入的时间长度,从左到右数值分别依次对应表3的加入溶酶体的时间点)表3溶酶体对环境影响实验数据表应用graphpad软件进行统计学分析,组间比较采用t-test,无显著性差异。结果显示,溶酶体不会影响细胞外环境的ph值。实施例9取b6c3f1阿尔茨海默症小鼠(12月龄)尾静脉注射0.5mg/kg溶酶体,每3天注射一次,连续注射一个月。给药结束后,麻醉实验小鼠,用0.9%生理盐水灌流小鼠,提取脑部海马和皮层蛋白质。(记为app/ps1ly组)为了对比说明溶酶体对阿尔兹海默症鼠毒性蛋白的降解及自噬途径的推动,特设置对比例6-7:对比例6:与实施例9相似,区别在使用等体积的pbs替代溶酶体。(记为app/ps1组)对比例7:与对比例6相似,区别在选用b6c3f1野生小鼠(12月龄)。(记为wt组)对实施例9、对比例6-7分别使用app抗体(biolegend,#sig-39320)、p62抗体(博尔迈生物技术,pm045)、lc3抗体(细胞信号科技,#2775)、actin抗体(柏奥易杰,be0021-100)和tetramer抗体(即app抗体,biolegend,#sig-39320),通过蛋白质印迹分析不同组别样品蛋白质的变化。(如附图5-6)。结果显示,尾静脉注射溶酶体可促进阿尔兹海默症小鼠脑内表达的毒性蛋白的降解。实施例10随机选取b6c3f1阿尔茨海默症小鼠(12月龄),并根据小鼠体重向其尾静脉注射0.5mg/kg的溶酶体标记探针标记后的溶酶体,每3天注射一次,连续注射一个月。设置对比例8,随机选取b6c3f1野生型小鼠(12月龄),并根据小鼠体重向其尾静脉注射与实施例3等体积的pbs,其他条件与实施例3相同。设置对比例9,随机选取b6c3f1阿尔茨海默症小鼠(12月龄),并根据小鼠体重向其尾静脉注射与实施例3等体积的pbs,其他条件与实施例3相同。连续注射一个月后,分别对实施例10和对比例8-9进行如下测试:新事物识别实验(nor)应用旷场测试箱,利用啮齿类动物喜欢接触和探索新奇事物的天性检测动物非空间记忆能力。实验分为三步:①适应阶段:将小鼠依次放入没有任何物体的测试箱中,适应实验环境,连续2天,每天2次。②熟悉阶段:在距侧壁10cm处放入两个相同物体(a和b),将小鼠以背对物体方向放入,自由探索10min后将小鼠取出,记录小鼠物体探索时间及嗅探物体次数,连续3天,每天2次。③测试阶段:24h后进行测试,将两个相同物体中b替换成另一物体c,即熟悉物体(a)和新奇物体(c),记录小鼠10min对两物体的探索时间及嗅探次数。a和c的位置随机置换,以避免位置偏倚。探索活动定义为:小鼠鼻子在≤5cm范围内直指向物体或直接接触物体时的行为,小鼠转头或坐在物体上时不被认为是对物体的探索。应用graphpad软件进行统计学分析,组间比较采用one-way。p<0.05为差异有统计学意义。结果如附图7-8所示:尾静脉注射溶酶体可改善阿尔兹海默症小鼠对事物的识别能力,改善海马相关学习记忆功能。筑巢实验:小鼠夜节律前2h,在鼠笼内放一些2cm×2cm的正方形纸巾(共三张厨房用纸),24h后统计鼠的筑巢情况并拍照记录。评分标准如下:纸巾均匀铺展且未形成团簇为1分;纸巾均匀铺展且形成松散团簇为2分;纸巾均匀铺展在笼内1/2且形成团簇为3分;纸巾均匀铺展在笼内1/3且形成团簇为4分;纸巾均匀铺展在笼内1/4且形成团簇为5分。应用graphpad软件进行统计学分析,组间比较采用one-way。结构如附图8,给药组筑巢评分较高,证明尾静脉注射溶酶体也会改善阿尔兹海默症小鼠的社会性行为。实施例11按常规方法提取app/ps1新生鼠原代神经元,将原代神经元按5×106/孔密度接种于6孔板中,在37℃的co2培养箱孵育。每2-3天换半液,7天后一次性给500μg/ml溶酶体,7天后提取蛋白质。为了对比说明大浓度溶酶体对阿尔兹海默症小鼠原代神经元毒性蛋白的降解及自噬途径的作用,特设置对比例10-11:对比例10:按常规方法提取正常野生型新生鼠原代神经元,将原代神经元按5×106/孔密度接种于6孔板中,在37℃的co2培养箱孵育。每2-3天换半液,14天后提取蛋白质。(记为正常原代神经元组)对比例11:与实施例11相似,区别在不使用溶酶体进行给药。对实施例11、对比例10-11分别使用app抗体(biolegend,#sig-39320)、p62抗体(博尔迈生物技术,pm045)、actin抗体(柏奥易杰,be0021-100),通过蛋白质印迹分析不同组别样品蛋白质的变化。(如附图10)结果显示,一次性外源给予大量溶酶体无法有效降解app蛋白。为证明溶酶体在治疗帕金森症方面的作用,设计实施例12:实施例12设计帕金森模型:c57bl/6j小鼠(10周龄,20±3g)腹腔注射25mg/kg1-甲基-4-苯基-1,2,3,6-四氢吡啶(mptp)溶液,每天1次,共7天。随机分为两组,分别为mptp组(对比例13)、给药组(实施例12)。同时取正常c57bl/6j小鼠(10周龄,20±3g)不做处理作为假手术组(对比例12)。对于给药组(实施例12),根据小鼠体重向其尾静脉注射0.5mg/kg的溶酶体标记探针标记后的溶酶体,每3天注射一次,连续注射一个月。对于假手术组(对比例12),操作与实施例12相同,区别在使用等体积的pbs替代溶酶体。对于mptp组(对比例13),操作与实施例12相同,区别在使用等体积的pbs替代溶酶体。对实施例12、对比例12-13通过蛋白质印迹分析不同组别样品蛋白质的变化。(如附图11)。结果显示,尾静脉注射溶酶体可促进α-突触核蛋白的降解。α-突触核蛋白(α-synuclein),是一种在中枢神经系统突触前及核周表达的可溶性蛋白质,它与帕金森病的发病机制和相关功能障碍密切相关,脑中多见该蛋白的错配聚集,以及表达量的升高。给药组α-突触核蛋白的表达量明显减少,说明药物具有促进α-突触核蛋白解聚、缓解帕金森病理表现的作用。实施例13标志性错配蛋白在加入溶酶体后的改善效果测试分别取表中错配蛋白的质粒(4μg)及5μllipo2000,分别与250μl的opti-mem混匀,室温静止5min。将两者轻柔混匀室温放置20min。取出已经培养在六孔板中24h的293t细胞,倒掉旧培养基,加入1.5ml的无血清无双抗的培养基,把质粒混合液轻轻的加入到培养基中,于37℃、5%co2的细胞培养箱中进行培养6h,再更换正常培养基培养48h,提取蛋白,用于westernblots检测。测试结果如表4:表4多种疾病模型中,标志性错配蛋白在加入溶酶体后的改善效果疾病名称细胞过表达错配蛋白名称给药后改善效果(%)阿尔茨海默症app53.2帕金森症α-synuclein44.7亨廷顿舞蹈症mhtt10.3肌侧索硬化症tdp4326.6最后应说明的是:以上各实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述各实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1