一种光触发可控释放药物的聚倍半硅氧烷基纳米载药系统及其制备方法与流程
本发明属于高分子纳米材料载药/释药领域,具体涉及一种光触发可控释放药物的聚倍半硅氧烷基纳米载药系统及其制备方法。
背景技术:
刺激响应性可控释放药物系统可以在一定的刺激条件下,如ph、光、热、氧化或还原反应等,系统装载的药物以合适的速率和浓度在指定位置进行释放,提高药物疗效,有利于解决传统给药方式药物利用率低、副作用大等缺点,在生物医药领域具有重要应用前景。
光作为一种非接触性刺激源,具有可控、高效等优点,通过精确调控光的照射波长、照射强度、照射时间和照射位置等参数,可以有效控制光响应性可控载药系统药物的释放速率、释放位置和释放浓度,实现时间空间可控,这种精确控制性是其他刺激手段无法达到的,因此光触发可控释放药物的载药系统具有重要的应用优势。
目前所公开报道的光触发可控释放系统主要策略为通过带有光敏基团的共价键将载体与目标分子结合起来,在光照条件下,由于光敏基团的光致断裂反应,实现药物的可控释放。赵一兵等人(chem.commun.(2008)23,2662–2664)通过光敏基团邻硝基苄基溴将染料分子罗丹明共价连接在二氧化硅纳米粒子表面,构建了一种光控释放系统。朱麟勇(j.am.chem.soc.(2010)132,10645–10647)将药物苯丁酸氮芥与香豆素分子经化学反应共价连接,再以化学键固定在介孔二氧化硅的孔道内,在光照条件下实现药物可控释放。pradeepsingh等人(acsappl.mater.interfaces(2013)5,5232-5238;j.mater.chem.b(2014)2,7971-7977)也是通过化学共价键方式,将药物苯丁酸氮芥分别连接在修饰了喹啉和香豆素的二氧化硅纳米载体表面,利用光敏基团的光致断裂反应实现光控药物释放。这类光触发可控释放药物系统的制备过程复杂,需要多步化学反应才能将药物与载体结合在一起,特别是,基于共价化学反应的连接会影响药物的原始生物特性,从而影响药物疗效,甚至导致副作用的发生。
很多药物分子本身带有电荷,可以利用静电相互作用将药物分子结合到具有带异性电荷的光响应性纳米载体上,构建光响应型纳米载药系统。本发明的发明人所在课题组将光响应型聚倍半硅氧烷基微粒载体与药物分子阿霉素结合制备了一种具有光响应型载药系统(参见:光响应桥联聚倍半硅氧烷纳米粒子的制备及作为药物载体的应用.中国化学会高分子学科委员会.中国化学会2017全国高分子学术论文报告会摘要集——主题g:药物控释载体高分子.中国化学会高分子学科委员会:中国化学会,2017:1.)。该聚倍半硅氧烷基微粒载体的粒径为300nm,最大载药量为14.38%。纳米药物载体的粒径尺寸对载药量和释放量的影响已经被广泛报道,研究表明粒径小的纳米药物载体,尤其小于200nm的药物载体能够负载更多的药物,更好地在体内循环,从而达到预期的治疗效果。上述聚倍半硅氧烷基微粒载体的粒径尺寸明显大于200nm,极大限制了该载体在生物医学领域中的应用,实际应用价值不高。因此,控制制备粒径尺寸小于200nm的纳米载药系统,对提高药物载药量、释放量和调控药物释放速率量具有重要的研究意义和应用价值,为此,提出本发明。
技术实现要素:
针对现有技术的不足,尤其是现有的光响应聚倍半硅氧烷纳米粒子粒径尺寸大,导致在生物医学领域中的应用受到很大限制。本发明提供一种光触发可控药物释放的纳米载药系统及其制备方法,该载药系统粒径尺寸小于200nm,能有效提高载药量,易于在生物体内循环,实现对具有正电荷性质的药物成分的释放量和释放速率精确控制,在生物医学领域中具有十分重要的应用价值。
本发明的光触发可控药物释放的聚倍半硅氧烷基纳米载药系统的粒径尺寸小于200nm,具有生物体内循环能力,其释药方式具有光触发性、逐步性和精确可控性。本发明的聚倍半硅氧烷基纳米载药系统包含具有光响应性电荷反转的邻硝基苄基桥联结构,可负载和光控释放具有正电荷性质的药物成分。聚倍半硅氧烷基纳米粒子粒径尺寸小于200nm,粒子表面具有负电性质,带正电荷的药物成分通过静电相互作用结合到聚倍半硅氧烷基纳米颗粒表面;光照条件下该载药系统的光敏性基团邻硝基苄基会发生光致断裂反应,在聚倍半硅氧烷桥联基团上产生碱性较强的亚氨基,亚氨基与氢质子形成铵离子,聚倍半硅氧烷纳米载体表面正电性增强,排斥了纳米载体表面带正电性的药物成分,药物与聚倍半硅氧烷纳米载体表面分离,达到了药物释放效果。该纳米载药系统可通过改变光照参数(光照时间和光照强度)对药物的释放速率和释放量进行精确控制。
术语说明:
式ⅰ化合物:2–硝基苄醇(i);
式ⅱ化合物:2–硝基苄基氯甲酸酯(ii);
式ⅲ化合物:二(3–三烷氧基硅烷丙基)胺(iii),结构式中,取代基r为甲基或乙基;
式ⅳ化合物:2–硝基苄基桥联倍半硅氧烷单体(iv),结构式中,取代基r同式ⅲ化合物;
式ⅴ化合物:2–硝基苄基桥联聚倍半硅氧烷(ⅴ);
本说明书中,化合物编号与结构式编号完全一致,具有相同的指代关系,以化合物结构式为依据。
室温:指25℃±5℃。
本发明的技术方案如下:
一种光触发可控释放药物的聚倍半硅氧烷基纳米载药系统,该载药系统具有式v所示的分子结构:
本发明的纳米载药系统是一种交联网状聚合物材料,纳米粒子表面含有大量硅醇基(–si-oh),硅醇基会在表面形成硅氧负离子(sio-),带正电荷的药物分子通过静电相互作用结合到纳米粒子表面,得到聚倍半硅氧烷基纳米载药系统。
根据本发明,优选的,载药系统的聚倍半硅氧烷基纳米载体粒径尺寸小于200nm,进一步优选小于150nm。
根据本发明,优选的,载药系统的载药量为15~35%。
根据本发明,优选的,载药系统总释药率为10~86%。
根据本发明,上述光触发可控释放药物的聚倍半硅氧烷基纳米载药系统的制备方法,包括步骤如下:
(1)在氮气保护下,将式ⅰ化合物溶于溶剂a中,加入催化剂a,在0~4℃冰水浴条件下逐滴加入三光气的溶剂a溶液,冰水浴下反应,之后在室温下继续反应;反应结束后,用去离子水洗涤产物,用二氯甲烷萃取水层,合并所有有机相,干燥剂干燥后,有机相经蒸发溶剂浓缩后,柱层析提纯得到式ⅱ化合物;
(2)在氮气保护下,将式ⅲ化合物溶于溶剂b中,加入三乙胺,在0~4℃冰水浴条件下逐滴加入式ⅱ化合物的溶剂b溶液;滴加完毕后,将反应体系升至室温,在室温下继续反应;反应结束后,过滤除去三乙胺盐化合物,滤液经蒸发溶剂浓缩后,柱层析提纯得到式ⅳ化合物;
(3)配制催化剂b溶液,在搅拌条件下将式ⅳ化合物逐滴加入至上述催化剂b溶液中,继续搅拌反应,经离心分离收集下层固体,分别用乙醇和去离子水洗涤,干燥,得到式ⅴ化合物。即为本发明光触发可控释放药物的聚倍半硅氧烷基纳米载药系统,为白色粉末状物质。
根据本发明,优选的,步骤(1)中所述溶剂a为甲苯、正己烷、三氯甲烷、丙酮、二氯甲烷或四氢呋喃;进一步优选为二氯甲烷或四氢呋喃。
根据本发明,优选的,步骤(1)中所述溶剂a与式ⅰ化合物的体积摩尔比为1~3ml:1mmol。
根据本发明,优选的,步骤(1)中所述催化剂a为三乙胺、吡啶、4-(n,n-二甲基)氨基吡啶、n,n-二异丙基乙胺,进一步优选为n,n-二异丙基乙胺。
根据本发明,优选的,步骤(1)中所述式ⅰ化合物与催化剂a的摩尔比为1:1~3,进一步优选为1:1.5~3。
根据本发明,优选的,步骤(1)中所述催化剂a与三光气的摩尔比为3:1。
根据本发明,优选的,步骤(1)中溶剂a与三光气的体积摩尔比为1~3ml:1mmol。
根据本发明,优选的,步骤(1)中所述冰水浴反应时间为0.5~2h。
根据本发明,优选的,步骤(1)中所述反应时间为2~4h。
根据本发明,优选的,步骤(1)中所述的干燥剂为无水硫酸镁、无水硫酸钠、无水氯化钙或分子筛。
根据本发明,优选的,步骤(1)中所述柱层析提纯方法中,固定相为硅胶,洗脱剂为二氯甲烷和石油醚的混合溶剂,所述混合溶剂中二氯甲烷和石油醚体积比为1~3:1,进一步优选为1~2:1。
根据本发明,优选的,步骤(2)中所述溶剂b为甲苯、正己烷、三氯甲烷、丙酮、二氯甲烷或四氢呋喃;进一步优选为二氯甲烷或三氯甲烷;所述溶剂b经无水处理。
根据本发明,优选的,步骤(2)中所述溶剂b与式ⅲ化合物的体积摩尔比为1~3ml:1mmol。
根据本发明,优选的,步骤(2)中所述式ⅲ化合物与三乙胺的摩尔比为1:1~2。
根据本发明,优选的,步骤(2)中所述式ⅲ化合物与式ⅱ化合物摩尔比为1:1~2。
根据本发明,优选的,步骤(2)中所述式ⅱ化合物与三乙胺的摩尔比为1:1。
根据本发明,优选的,步骤(2)中所述溶剂b与式ⅱ化合物的体积摩尔比为1~3ml:1mmol。
根据本发明,优选的,步骤(2)中所述反应时间为3~6h。
根据本发明,优选的,步骤(2)中所述柱层析提纯方法中,固定相为硅胶,洗脱剂为乙酸乙酯和正己烷的混合溶剂,所述混合溶剂中乙酸乙酯和正己烷体积比为1:1~3,进一步优选为1:1~2。
根据本发明,优选的,步骤(3)中所述催化剂b主要成分为0.5ml0.1m碱金属氢氧化钠、1ml0.1m氟化盐化合物、0.5ml醇类化合物和8ml水。
根据本发明,优选的,步骤(3)中反应温度为25~80℃,进一步优选65~80℃。
根据本发明,优选的,步骤(3)中搅拌速率为800rpm~1500rpm,进一步优选为1000rpm~1500rpm。搅拌速率对于得到粒径较小的粒子比较重要,如果搅拌速率小,聚合反应体系不稳定,将会导致粒径变大,粒径分散度高。
根据本发明,优选的,步骤(3)中式ⅳ化合物的体积为0.05~0.1ml。
根据本发明,优选的,步骤(3)中反应时间为2~8h。
本发明光触发可控释放药物的聚倍半硅氧烷基纳米载药系统的制备路线如下:
根据本发明,利用上述光触发可控释放药物的聚倍半硅氧烷基纳米载药系统进行载药的方法,包括步骤如下:
将式ⅴ化合物和带电药物按照不同质量比分散在磷酸盐缓冲溶液中,置于恒温振荡器中,在37℃下反应一段时间后,采用离心分离法收集下层载药纳米粒子,分别用乙醇和去离子水洗涤三次,60℃干燥8h,得到红色粉末状聚倍半硅氧烷基载药纳米粒子。
根据本发明,优选的,磷酸盐缓冲溶液的ph为7.4。
根据本发明,优选的,所述带电药物为阿霉素、紫杉醇、喜树碱或多西紫杉醇。
根据本发明,优选的,所述式ⅴ化合物与带电药物的质量比为1:1~10;式ⅴ化合物与带电药物的总质量与磷酸盐缓冲溶液的体积比为1mg:2ml。
根据本发明,优选的,所述反应时间为24~36h。
根据本发明,将载药后的聚倍半硅氧烷基载药纳米粒子进行光控释药,包括步骤如下:将得到的聚倍半硅氧烷基载药纳米粒子分散于磷酸盐缓冲溶液中,得到一定浓度的聚倍半硅氧烷基载药纳米粒子磷酸盐缓冲溶液。将该溶液置于254nm波长的紫外光下,通过改变光的照射强度、照射时长和照射方式,调节载药纳米粒子的释药速率和释放量,采用紫外-可见分光光度法检测药物释放量。
根据本发明,所述式ⅴ化合物的磷酸盐缓冲溶液浓度为5~15mg/ml,所述照射强度为60mw/cm2、160mw/cm2和200mw/cm2;所述照射时长为0~16h,所述照射方式为连续照射和“on/off”间隔照射,“on”表示打开254nm紫外光光源,“off”表示关闭254nm紫外光光源。
本发明的聚倍半硅氧烷基纳米载药系统载药与光控释药机制如下:
本发明通过分光光度法对药物释放量进行了监测,证明了制备的聚倍半硅氧烷纳米载体在254nm光照条件下释放药物具有光触发性、逐步性和精确可控性,详细说明参见实施例。
与现有技术相比本发明的特点及优良效果如下:
纳米载体为聚倍半硅氧烷属于有机-无机杂化材料,性能稳定,结构容易控制,可加工性强;制备的聚倍半硅氧烷基纳米载体粒径尺寸小于200nm,能够实现体内循环,与药物成分通过简单的静电相互作用结合在一起,方法迅速简单,且不会影响药物的原始生物特性,并且载药量明显提高;通过调控光的照射强度、照射时间和照射方式,能精确控制药物的释放速率和释放浓度,具有光触发性、逐步性和精确可控性,总释放率最高达到86%。
附图说明
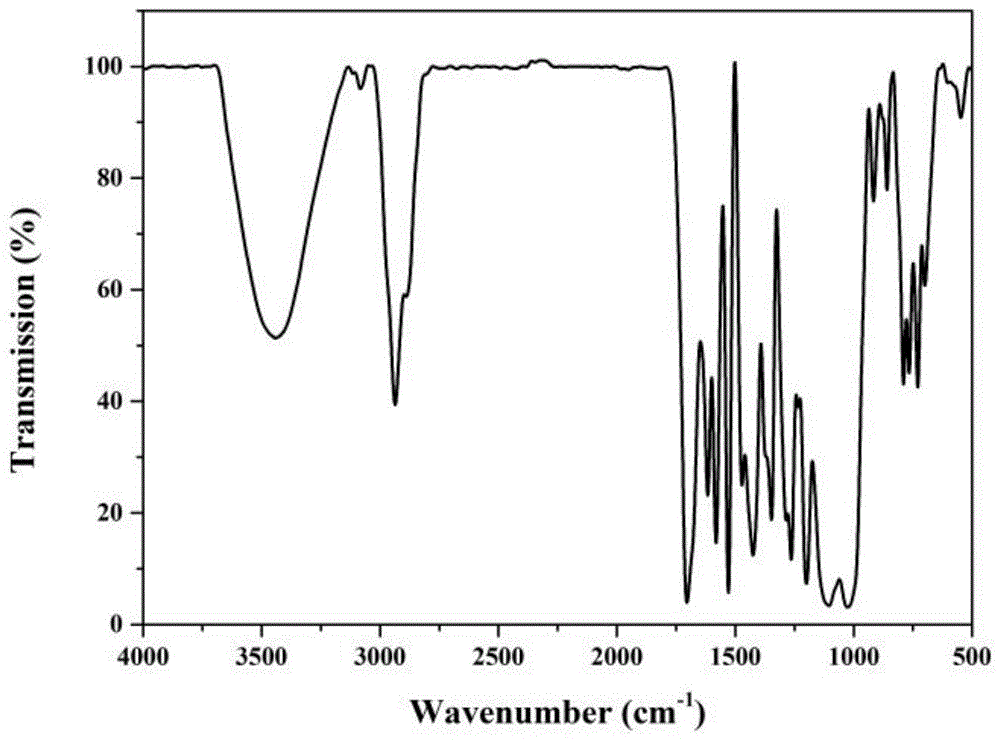
图1为实施例1中制备的硝基苄基桥联聚倍半硅氧烷纳米载体的红外光谱图。
图2为实施例1中聚倍半硅氧烷基纳米载体的扫描电子显微镜图。
图3为实施例1、2、3中不同照射强度下(200mw/cm2、160mw/cm2和60mw/cm2)连续照射16h后药物阿霉素的释药率。
图4为实施例4不同照射循环下药物阿霉素的释药率;
图中,“on”为打开光源,即光照条件下,“off”为关闭光源,即黑暗条件下。
具体实施方式:
借助以下实施例对本发明做进一步描述,应理解,以下实施例是示范性的,而不是限制性的,可根据上述发明的技术方案和实际情况,来确定具体的实施方法。
实施例1、
光触发可控释放药物的聚倍半硅氧烷基纳米载药系统的制备方法,包括步骤如下:
(1)在氮气保护下,将2–硝基苄醇(3.80g,24.8mmol)溶于25ml二氯甲烷中,向上述溶液中加入n,n-二异丙基乙胺(4.81g,37.2mmol),在0~4℃冰水浴条件下逐滴加入15ml三光气(3.68g,12.4mmol)的二氯甲烷溶液。将反应混合物在冰水浴下反应0.5h,之后在室温下继续反应4h。反应结束后,分别用20ml去离子水洗涤产物三次,用30ml二氯甲烷萃取水层,合并所有有机相,用无水硫酸镁干燥。抽滤、蒸发溶剂浓缩后,使用柱层析提纯得到产物,所述柱层析提纯的条件为:固定相为硅胶,洗脱剂为二氯甲烷和石油醚的混合溶剂,其中混合溶剂中二氯甲烷和石油醚的体积比为3:1,经蒸馏得到黄色固体2–硝基苄基氯甲酸酯,产率为78%。
(2)在氮气保护下,将二(3–三甲氧基硅烷丙基)胺(3.41g,10.3mmol)溶于30ml无水二氯甲烷中,加入三乙胺(1.57g,15.5mmol),在0~4℃冰水浴条件下逐滴加入20ml2–硝基苄基氯甲酸酯(3.33g,15.5mmol)的二氯甲烷溶液。滴加完毕后,将反应体系升至室温,在室温下继续反应6h。反应结束后,过滤除去三乙胺盐化合物,滤液经蒸发溶剂浓缩后,使用柱层析提纯得到产物,所述柱层析提纯的条件为:固定相为硅胶,洗脱剂为乙酸乙酯和正己烷的混合溶剂,其中混合溶剂中乙酸乙酯和正己烷的体积比为4:7,经蒸馏得到黄色油状物2–硝基苄基桥联倍半硅氧烷单体,产率为64%。
(3)配制10ml的催化剂b溶液(0.5ml0.1m氢氧化钠溶液、1ml0.1m氟化钾溶液、0.5ml异丙醇和8ml水),在80℃1500rpm条件下将0.05ml2–硝基苄基桥联倍半硅氧烷单体逐滴加入至上述催化剂b溶液中,反应8h后,离心收集下层固体,分别用乙醇和去离子水洗涤三次,60℃烘箱中干燥8h,得到白色粉末状聚倍半硅氧烷基纳米粒子,产率为92%,粒径尺寸为126nm。
利用上述光触发可控释放药物的聚倍半硅氧烷基纳米载药系统进行载药的方法,包括步骤如下:
将5mg聚倍半硅氧烷基纳米粒子和5mg带电药物阿霉素分散在20ml磷酸盐缓冲溶液(ph为7.4)中,置于恒温振荡器中,在37℃下反应36h,采用离心分离法收集下层载药纳米粒子,分别用乙醇和去离子水洗涤三次,60℃烘箱中干燥8h,得到红色粉末状聚倍半硅氧烷基载药纳米粒子,利用紫外–可见分光光度法可知聚倍半硅氧烷基载药纳米粒子的载药量为34%。
将载药后的聚倍半硅氧烷基载药纳米粒子进行光控释药,包括步骤如下:
将得到的聚倍半硅氧烷基载药纳米粒子分散于磷酸盐缓冲溶液(ph为7.4)中,得到10mg/ml的聚倍半硅氧烷基载药纳米粒子磷酸盐缓冲溶液,将该溶液置于波长为254nm、照射强度为200mw/cm2的紫外灯下,对载药纳米粒子溶液连续光照16h,每1小时取出5ml样品,采用紫外–可见分光光度法检测总释药率为86%。
实施例2、
光触发可控释放药物的聚倍半硅氧烷基纳米载药系统的制备方法,包括步骤如下:
(1)在氮气保护下,将2–硝基苄醇(2.68g,17.5mmol)溶于20ml二氯甲烷中,向上述溶液中加入n,n-二异丙基乙胺(3.38g,26.3mmol),在0~4℃冰水浴条件下逐滴加入10ml三光气(2.60g,8.8mmol)的二氯甲烷溶液。将反应混合物在冰水浴下反应1h,之后在室温下继续反应4h。反应结束后,分别用20ml去离子水洗涤产物三次,用30ml二氯甲烷萃取水层,合并所有有机相,用无水硫酸镁干燥。抽滤、蒸发溶剂浓缩后,使用柱层析提纯得到产物,所述柱层析提纯的条件为:固定相为硅胶,洗脱剂为二氯甲烷和石油醚的混合溶剂,其中混合溶剂中二氯甲烷和石油醚的体积比为3:1,经蒸馏得到黄色固体2–硝基苄基氯甲酸酯,产率为77%。
(2)在氮气保护下,将二(3–三甲氧基硅烷丙基)胺(3.41g,10.3mmol)溶于30ml无水二氯甲烷中,加入三乙胺(1.04g,10.3mmol),在0~4℃冰水浴条件下逐滴加入20ml2–硝基苄基氯甲酸酯(2.21g,10.3mmol)的二氯甲烷溶液。滴加完毕后,将反应体系升至室温,在室温下继续反应5h。反应结束后,过滤除去三乙胺盐化合物,滤液经蒸发溶剂浓缩后,使用柱层析提纯得到产物,所述柱层析提纯的条件为:固定相为硅胶,洗脱剂为乙酸乙酯和正己烷的混合溶剂,其中混合溶剂中乙酸乙酯和正己烷的体积比为4:7,经蒸馏得到黄色油状物2–硝基苄基桥联倍半硅氧烷单体,产率为62%。
(3)配制10ml的催化剂b溶液(0.5ml0.1m氢氧化钠溶液、1ml0.1m氟化钾溶液、0.5ml异丙醇和8ml水),在70℃1000rpm条件下将0.05ml2–硝基苄基桥联倍半硅氧烷单体逐滴加入至上述催化剂b溶液中,反应8h后,离心收集下层固体,分别用乙醇和去离子水洗涤三次,60℃烘箱中干燥8h,得到白色粉末状聚倍半硅氧烷基纳米粒子,产率为90%,粒径尺寸为135nm。
利用上述光触发可控释放药物的聚倍半硅氧烷基纳米载药系统进行载药的方法,包括步骤如下:
将4mg聚倍半硅氧烷基纳米粒子和8mg带电药物阿霉素分散在24ml磷酸盐缓冲溶液(ph为7.4)中,置于恒温振荡器中,在37℃下反应36h,采用离心分离法收集下层载药纳米粒子,分别用乙醇和去离子水洗涤三次,60℃干燥8h,得到红色粉末状聚倍半硅氧烷基载药纳米粒子,利用紫外–可见分光光度法可知聚倍半硅氧烷基载药纳米粒子的载药量为31%。
将载药后的聚倍半硅氧烷基载药纳米粒子进行光控释药,包括步骤如下:
将聚倍半硅氧烷基载药纳米粒子分散于磷酸盐缓冲溶液(ph为7.4)中,得到10mg/ml的聚倍半硅氧烷基载药纳米粒子磷酸盐缓冲溶液,将该溶液置于波长为254nm、照射强度为160mw/cm2的紫外灯下,对载药纳米粒子溶液连续光照16h,每隔1h打开光源照射1h,每1小时取出5ml样品,采用紫外–可见分光光度法检测总释药率为45%。
实施例3、
光触发可控释放药物的聚倍半硅氧烷基纳米载药系统的制备方法,包括步骤如下:
(1)在氮气保护下,将2–硝基苄醇(3.80g,24.8mmol)溶于25ml二氯甲烷中,向上述溶液中加入n,n-二异丙基乙胺(4.81g,37.2mmol),在0~4℃冰水浴条件下逐滴加入15ml三光气(3.68g,12.4mmol)的二氯甲烷溶液。将反应混合物在冰水浴下反应1h,之后在室温下继续反应3h。反应结束后,分别用20ml去离子水洗涤产物三次,用30ml二氯甲烷萃取水层,合并所有有机相,用无水硫酸镁干燥。抽滤、蒸发溶剂浓缩后,使用柱层析提纯得到产物,所述柱层析提纯的条件为:固定相为硅胶,洗脱剂为二氯甲烷和石油醚的混合溶剂,其中混合溶剂中二氯甲烷和石油醚的体积比为3:1,经蒸馏得到黄色固体2–硝基苄基氯甲酸酯,产率为75%。
(2)在氮气保护下,将二(3–三甲氧基硅烷丙基)胺(3.41g,10.3mmol)溶于30ml无水二氯甲烷中,加入三乙胺(1.57g,15.5mmol),在0~4℃冰水浴条件下逐滴加入20ml2–硝基苄基氯甲酸酯(3.33g,15.5mmol)的二氯甲烷溶液。滴加完毕后,将反应体系升至室温,在室温下继续反应4h。反应结束后,过滤除去三乙胺盐化合物,滤液经蒸发溶剂浓缩后,使用柱层析提纯得到产物,所述柱层析提纯的条件为:固定相为硅胶,洗脱剂为乙酸乙酯和正己烷的混合溶剂,其中混合溶剂中乙酸乙酯和正己烷的体积比为4:7,经蒸馏得到黄色油状物2–硝基苄基桥联倍半硅氧烷单体,产率为59%。
(3)配制10ml的催化剂b溶液(0.5ml0.1m氢氧化钾溶液、1ml0.1m氟化铵溶液、0.5ml异丙醇和8ml水),在80℃1500rpm条件下将0.05ml2–硝基苄基桥联倍半硅氧烷单体逐滴加入至上述催化剂b溶液中,反应8h后,离心收集下层固体,分别用乙醇和去离子水洗涤三次,60℃烘箱中干燥8h,得到白色粉末状聚倍半硅氧烷基纳米粒子,产率为86%,粒径尺寸为138nm。
利用上述光触发可控释放药物的聚倍半硅氧烷基纳米载药系统进行载药的方法,包括步骤如下:
将2mg聚倍半硅氧烷基纳米粒子和10mg带电药物阿霉素分散在24ml磷酸盐缓冲溶液(ph为7.4)中,置于恒温振荡器中,在37℃下振荡36h,采用离心分离法收集下层载药纳米粒子,分别用乙醇和去离子水洗涤三次,60℃干燥8h,得到红色粉末状聚倍半硅氧烷基载药纳米粒子,利用紫外–可见分光光度法可知聚倍半硅氧烷基载药纳米粒子的载药量为23%。
将载药后的聚倍半硅氧烷基载药纳米粒子进行光控释药,包括步骤如下:
将得到的聚倍半硅氧烷基载药纳米粒子分散于磷酸盐缓冲溶液(ph为7.4)中,得到10mg/ml的聚倍半硅氧烷基载药纳米粒子磷酸盐缓冲溶液,将该溶液置于波长为254nm、照射强度为60mw/cm2的紫外灯下,对载药纳米粒子溶液连续光照16h,每隔1h打开光源照射1h,每1小时取出5ml样品,采用紫外–可见分光光度法检测总释药率为23%。
实施例4、
光触发可控释放药物的聚倍半硅氧烷基纳米载药系统的制备方法,包括步骤如下:
(1)在氮气保护下,将2–硝基苄醇(1.53g,10.0mmol)溶于30ml四氢呋喃中,向上述溶液中加入n,n-二异丙基乙胺(3.87g,30.0mmol),在0~4℃冰水浴条件下逐滴加入10ml三光气(2.97g,10.0mmol)的四氢呋喃溶液。将反应混合物在冰水浴下反应2h,之后在室温下继续反应3h。反应结束后,蒸发溶剂浓缩后,重新溶于30ml二氯甲烷中,分别用20ml去离子水洗涤产物三次,用30ml二氯甲烷萃取水层,合并所有有机相,用无水硫酸镁干燥。抽滤、蒸发溶剂浓缩后,使用柱层析提纯得到产物,所述柱层析提纯的条件为:固定相为硅胶,洗脱剂为二氯甲烷和石油醚的混合溶剂,其中混合溶剂中二氯甲烷和石油醚的体积比为3:1,经蒸馏得到黄色固体2–硝基苄基氯甲酸酯,产率为70%。
(2)在氮气保护下,将二(3–三甲氧基硅烷丙基)胺(3.41g,10.3mmol)溶于30ml无水二氯甲烷中,加入三乙胺(1.04g,10.3mmol),在0~4℃冰水浴条件下逐滴加入20ml2–硝基苄基氯甲酸酯(2.21g,10.3mmol)的二氯甲烷溶液。滴加完毕后,将反应体系升至室温,在室温下继续反应3.5h。反应结束后,过滤除去三乙胺盐化合物,滤液经蒸发溶剂浓缩后,使用柱层析提纯得到产物,所述柱层析提纯的条件为:固定相为硅胶,洗脱剂为乙酸乙酯和正己烷的混合溶剂,其中混合溶剂中乙酸乙酯和正己烷的体积比为4:7,经蒸馏得到黄色油状物2–硝基苄基桥联倍半硅氧烷单体,产率为56%。
(3)配制10ml的催化剂b溶液(0.5ml0.1m氢氧化钾溶液、1ml0.1m氟化铵溶液、0.5ml异丙醇和8ml水),在80℃1000rpm条件下将0.1ml2–硝基苄基桥联倍半硅氧烷单体逐滴加入至上述催化剂b溶液中,反应6h后,离心收集下层固体,分别用乙醇和去离子水洗涤三次,60℃烘箱中干燥8h,得到白色粉末状聚倍半硅氧烷基纳米粒子,产率为85%,粒径尺寸为156nm。
利用上述光触发可控释放药物的聚倍半硅氧烷基纳米载药系统进行载药的方法,包括步骤如下:
将1mg聚倍半硅氧烷基纳米粒子和10mg带电药物阿霉素分散在22ml磷酸盐缓冲溶液(ph为7.4)中,置于恒温振荡器中,在37℃下反应24h,采用离心分离法收集下层载药纳米粒子,分别用乙醇和去离子水洗涤三次,60℃烘箱中干燥8h,得到红色粉末状聚倍半硅氧烷基载药纳米粒子,利用紫外–可见分光光度法可知聚倍半硅氧烷基载药纳米粒子的载药量为19%。
将载药后的聚倍半硅氧烷基载药纳米粒子进行光控释药,包括步骤如下:
将得到的聚倍半硅氧烷基载药纳米粒子分散于磷酸盐缓冲溶液(ph为7.4)中,得到5mg/ml的聚倍半硅氧烷基载药纳米粒子磷酸盐缓冲溶液,将该溶液置于波长为254nm、照射强度为200mw/cm2的紫外灯下,采用“on/off”间隔照射的照射方式对载药纳米粒子溶液进行光照,每隔1h打开光源照射1h,每1小时取出5ml样品,采用紫外–可见分光光度法检测总释药率为61%。
实施例5、
光触发可控释放药物的聚倍半硅氧烷基纳米载药系统的制备方法,包括步骤如下:
(1)在氮气保护下,将2–硝基苄醇(2.34g,13.5mmol)溶于20ml四氢呋喃中,向上述溶液中加入n,n-二异丙基乙胺(3.48g,27.0mmol),在0~4℃冰水浴条件下逐滴加入10ml三光气(2.66g,9.0mmol)的四氢呋喃溶液。将反应混合物在冰水浴下反应2h,之后在室温下继续反应2h。反应结束后,蒸发溶剂浓缩后,重新溶于30ml二氯甲烷中,分别用20ml去离子水洗涤产物三次,用30ml二氯甲烷萃取水层,合并所有有机相,用无水硫酸镁干燥。抽滤、蒸发溶剂浓缩后,使用柱层析提纯得到产物,所述柱层析提纯的条件为:固定相为硅胶,洗脱剂为二氯甲烷和石油醚的混合溶剂,其中混合溶剂中二氯甲烷和石油醚的体积比为3:1,经蒸馏得到黄色固体2–硝基苄基氯甲酸酯,产率为66%。
(2)在氮气保护下,将二(3–三甲氧基硅烷丙基)胺(1.71g,5.15mmol)溶于30ml无水二氯甲烷中,加入三乙胺(1.04gml,10.3mmol),在0~4℃冰水浴条件下逐滴加入20ml2–硝基苄基氯甲酸酯(2.21g,10.3mmol)的二氯甲烷溶液。滴加完毕后,将反应体系升至室温,在室温下继续反应3h。反应结束后,过滤除去三乙胺盐化合物,滤液经蒸发溶剂浓缩后,使用柱层析提纯得到产物,所述柱层析提纯的条件为:固定相为硅胶,洗脱剂为乙酸乙酯和正己烷的混合溶剂,其中混合溶剂中乙酸乙酯和正己烷的体积比为4:7,经蒸馏得到黄色油状物2–硝基苄基桥联倍半硅氧烷单体,产率为51%。
(3)配制10ml的催化剂b溶液(0.5ml0.1m氢氧化钠溶液、1ml0.1m氟化钾溶液、0.5ml异丙醇和8ml水),在60℃1000rpm条件下将0.05ml2–硝基苄基桥联倍半硅氧烷单体逐滴加入至上述催化剂b溶液中,反应8h后,离心收集下层固体,分别用乙醇和去离子水洗涤三次,60℃烘箱中干燥8h,得到白色粉末状聚倍半硅氧烷基纳米粒子,产率为82%,粒径尺寸为160nm。
利用上述光触发可控释放药物的聚倍半硅氧烷基纳米载药系统进行载药的方法,包括步骤如下:
将1mg聚倍半硅氧烷基纳米粒子和10mg带电药物阿霉素分散在22ml磷酸盐缓冲溶液(ph为7.4)中,置于恒温振荡器中,在37℃下反应24h,采用离心分离法收集下层载药纳米粒子,分别用乙醇和去离子水洗涤三次,60℃干燥8h,得到红色粉末状聚倍半硅氧烷基载药纳米粒子。利用紫外–可见分光光度法可知聚倍半硅氧烷基载药纳米粒子的载药量为19%。
将载药后的聚倍半硅氧烷基载药纳米粒子进行光控释药,包括步骤如下:
将得到的聚倍半硅氧烷基载药纳米粒子分散于磷酸盐缓冲溶液(ph为7.4)中,得到5mg/ml的聚倍半硅氧烷基载药纳米粒子磷酸盐缓冲溶液,将该溶液置于波长为254nm、照射强度为60mw/cm2的紫外灯下,采用“on/off”间隔照射的照射方式对聚倍半硅氧烷基载药纳米粒子的磷酸盐缓冲溶液进行光照,每隔1h打开光源照射1h,每1小时取出5ml样品,采用紫外–可见分光光度法检测总释药率为48%。
对比例1、
(1)在氮气保护下,将2–硝基苄醇(2.34g,13.5mmol)溶于20ml四氢呋喃中,向上述溶液中加入n,n-二异丙基乙胺(3.48g,27.0mmol),在0~4℃冰水浴条件下逐滴加入10ml三光气(2.66g,9.0mmol)的四氢呋喃溶液。将反应混合物在冰水浴下反应2h。反应结束后,蒸发溶剂浓缩后,重新溶于30ml二氯甲烷中,分别用20ml去离子水洗涤产物三次,用30ml二氯甲烷萃取水层,合并所有有机相,用无水硫酸镁干燥。抽滤、蒸发溶剂浓缩后,使用柱层析提纯得到产物,所述柱层析提纯的条件为:固定相为硅胶,洗脱剂为二氯甲烷和石油醚的混合溶剂,其中混合溶剂中二氯甲烷和石油醚的体积比为3:2,经蒸馏得到黄色固体2–硝基苄基氯甲酸酯,产率为58%。
(2)在氮气保护下,将二(3–三甲氧基硅烷丙基)胺(1.71g,5.15mmol)溶于30ml无水二氯甲烷中,加入三乙胺(1.04g,10.3mmol),在0~4℃冰水浴条件下逐滴加入20ml2–硝基苄基氯甲酸酯(2.21g,10.3mmol)的二氯甲烷溶液。滴加完毕后,将反应体系升至室温,在室温下继续反应2h。反应结束后,过滤除去三乙胺盐化合物,滤液经蒸发溶剂浓缩后,使用柱层析提纯得到产物,所述柱层析提纯的条件为:固定相为硅胶,洗脱剂为乙酸乙酯和正己烷的混合溶剂,其中混合溶剂中乙酸乙酯和正己烷的体积比为4:7,经蒸馏得到黄色油状物2–硝基苄基桥联倍半硅氧烷单体,产率为45%。
(3)配制10ml的催化剂b溶液(0.5ml0.1m氢氧化钠溶液、1ml0.1m氟化钾溶液、0.5ml异丙醇和8ml水),在25℃1000rpm条件下将0.05ml2–硝基苄基桥联倍半硅氧烷单体逐滴加入至上述催化剂b溶液中,反应2h后,离心收集下层固体,分别用乙醇和去离子水洗涤三次,60℃烘箱中干燥8h,得到白色粉末状聚倍半硅氧烷基纳米粒子,产率为72%,粒径尺寸为190nm。
(4)将1mg聚倍半硅氧烷基纳米粒子和10mg带电药物阿霉素分散在22ml磷酸盐缓冲溶液(ph为7.4)中,置于恒温振荡器中,在37℃下反应12h,采用离心分离法收集下层载药纳米粒子,分别用乙醇和去离子水洗涤三次,60℃干燥8h,得到红色粉末状聚倍半硅氧烷基载药纳米粒子。利用紫外–可见分光光度法可知聚倍半硅氧烷基载药纳米粒子的载药量为15%。
(5)将步骤(4)中得到的聚倍半硅氧烷基载药纳米粒子分散于磷酸盐缓冲溶液(ph为7.4)中,得到5mg/ml的聚倍半硅氧烷基载药纳米粒子磷酸盐缓冲溶液,将该溶液置于波长为254nm、照射强度为45mw/cm2的紫外灯下,对载药纳米粒子溶液连续光照16h,每隔1h打开光源照射1h,每1小时取出5ml样品,采用紫外–可见分光光度法检测总释药率为18%。
通过本对比例可知,照射强度对该聚倍半硅氧烷基纳米载药系统的总释放率影响显著,随着光照强度的增加,该纳米载药系统的总释放率也显著增加。当照射强度较低时,该纳米粒子的光解速率较慢,在相同的光照时间内,纳米粒子的表面电荷变化较小,粒子与药物之间的静电斥力相对较弱,最终释放药物量减少。
对比例2、
(1)在氮气保护下,将2–硝基苄醇(2.25g,13.0mmol)溶于20ml四氢呋喃中,向上述溶液中加入n,n-二异丙基乙胺(3.51g,26.0mmol),在0~4℃冰水浴条件下逐滴加入10ml三光气(3.26g,8.67mmol)的四氢呋喃溶液。将反应混合物在冰水浴下反应2h。反应结束后,蒸发溶剂浓缩后,重新溶于30ml二氯甲烷中,分别用20ml去离子水洗涤产物三次,用30ml二氯甲烷萃取水层,合并所有有机相,用无水硫酸镁干燥。抽滤、蒸发溶剂浓缩后,使用柱层析提纯得到产物,所述柱层析提纯的条件为:固定相为硅胶,洗脱剂为二氯甲烷和石油醚的混合溶剂,其中混合溶剂中二氯甲烷和石油醚的体积比为3:2,经蒸馏得到黄色固体2–硝基苄基氯甲酸酯,产率为57%。
(2)在氮气保护下,将二(3–三甲氧基硅烷丙基)胺(1.85g,5.58mmol)溶于30ml无水二氯甲烷中,加入三乙胺(1.13g,11.2mmol),在0~4℃冰水浴条件下逐滴加入20ml2–硝基苄基氯甲酸酯(2.40g,11.2mmol)的二氯甲烷溶液。滴加完毕后,将反应体系升至室温,在室温下继续反应2h。反应结束后,过滤除去三乙胺盐化合物,滤液经蒸发溶剂浓缩后,使用柱层析提纯得到产物,所述柱层析提纯的条件为:固定相为硅胶,洗脱剂为乙酸乙酯和正己烷的混合溶剂,其中混合溶剂中乙酸乙酯和正己烷的体积比为4:7,经蒸馏得到黄色油状物2–硝基苄基桥联倍半硅氧烷单体,产率为43%。
(3)配制10ml的催化剂b溶液(2.00ml0.1m碳酸钠溶液、0.50ml异丙醇和7.50ml水),在60℃500rpm条件下将0.05ml2–硝基苄基桥联倍半硅氧烷单体逐滴加入至上述催化剂b溶液中,反应2h后,离心收集下层固体,分别用乙醇和去离子水洗涤三次,60℃烘箱中干燥8h,得到白色粉末状聚倍半硅氧烷基纳米粒子,产率为72%,粒径尺寸为310nm。
(4)将5mg聚倍半硅氧烷基纳米粒子和5mg带电药物阿霉素分散在20ml磷酸盐缓冲溶液(ph为7.4)中,置于恒温振荡器中,在37℃下反应12h,采用离心分离法收集下层载药纳米粒子,分别用乙醇和去离子水洗涤三次,60℃干燥8h,得到红色粉末状聚倍半硅氧烷基载药纳米粒子。利用紫外–可见分光光度法可知聚倍半硅氧烷基载药纳米粒子的载药量为14%。
(5)将步骤(4)中得到的聚倍半硅氧烷基载药纳米粒子分散于磷酸盐缓冲溶液(ph为7.4)中,得到5mg/ml的聚倍半硅氧烷基载药纳米粒子磷酸盐缓冲溶液,将该溶液置于波长为254nm、照射强度为45mw/cm2的紫外灯下,对载药纳米粒子溶液连续光照16h,每隔1h打开光源照射1h,每1小时取出5ml样品,采用紫外–可见分光光度法检测总释药率为13%。
通过本对比例可知,在制备聚倍半硅氧烷基纳米粒子过程中,纳米粒子尺度受搅拌速率的影响,低的搅拌速率会导致纳米粒子粒径尺寸变大。
- 还没有人留言评论。精彩留言会获得点赞!