EGCG在制备改善或治疗内源性内毒素血症药物或保健食品中的应用的制作方法
本发明涉及生物学及药学领域,具体公开egcg在改善或治疗高脂饮食诱导的内源性内毒素血症的药物或保健食品中的应用。
背景技术:
:内毒素血症是一种全身性炎症反应综合征,医学上,可分为内源性内毒素血症和外源性内毒素血症,前者指肠道革兰氏阴性菌释放大量的内毒素,超过了机体清除能力从而进入血液引起;后者则指外源性感染大量内毒素,从而引发疾病。内毒素可以引起身体多个器官或组织出现功能障碍或衰竭,如肝功能受损、肾功能受损、肌肉和脂肪组织炎症水平增加、胰岛素抵抗等,严重患者甚至导致死亡,据有关文献报道,仅美国全年有3~10万病人因得不到有效治疗而死亡。脂多糖(lipopolysaccharide,lps)很难从细胞壁脱落,当细菌死亡等时它会通过溶解、破坏细胞来脱落,并通过作用于细胞等而发挥其毒性。由于这种性质,它不是细菌分泌到体外的毒素(外毒素),而是不被分泌的“存在于细菌体内的毒素”,所以又被称为内毒素。内毒素主要有以下特征,首先革兰氏阴性菌死亡后可以在肠道内持续产生lps,产生的lps通过tlr4依赖机制移位至肠毛细血管内,之后与食物中的脂质一同组装成为乳糜微粒,从而跨肠上皮输送到目标组织器官,最后被器官或组织细胞表面的tlr4受体识别后,触发促炎细胞因子的分泌。因此,减少lps的分泌及其全身性输送是治疗内毒素血症的有效措施。研究表明高脂饮食可通过增加产lps肠道细菌的量、破坏肠屏障及促进lps整合到乳糜微粒等引发内源性内毒素血症。厚壁菌门firmicutes和拟杆菌门bacteroidetes是肠道菌群的两大主要分类,其中firmicutes呈革兰氏阳性,bacteroidetes呈革兰氏阴性,革兰氏阴性菌的细胞壁成分之一是lps,高脂饮食会造成f/b(firmicutes/bacteroidetes)的比例升高。表没食子儿茶素没食子酸酯egcg是绿茶的主要活性成分,约占绿茶儿茶素总量的50-60%,具有抗氧化、抗炎、抗癌抑菌等多种生物活性。现有技术有公开egcg在制备改善肝脏验证和胰岛素抵抗药物中的应用,但肝损伤还可能由脂肪堆积、氧化应激、酒精摄入过量等很多因素引起,糖尿病也是,成病原因很多,是否由于内源性内毒素引起的并不明确。egcg生物利用率低,大部分不被吸收,主要存在于肠道中,因此肠组织是egcg的重要靶器官,egcg能否通过调节肠组织中乳糜微粒的合成,改善和治疗高脂饮食诱导的内源性内毒素血症,目前尚未有相关报道。技术实现要素:本发明的目的是提供一种egcg在改善或治疗高脂饮食诱导的内源性内毒素血症的应用。egcg在制备改善或治疗内源性内毒素血症药物中的应用,所述的应用是将egcg用于改善和治疗高脂饮食引起的内源性内毒素血症的药物。所述的内源性内毒素血症由高脂饮食引起内源性内毒素的产生和吸收增加引起。高脂饮食引起的内源性内毒素吸收增加主要经乳糜微粒运载吸收进入体内。所述egcg来源于绿茶。一种egcg在制备改善内源性内毒素血症保健食品中的应用,所述的应用是将egcg用于改善高脂饮食引起的内源性内毒素血症的保健食品。所述的内源性内毒素血症由高脂饮食引起内源性内毒素的产生和吸收增加引起。高脂饮食引起的内源性内毒素吸收增加主要经乳糜微粒运载吸收进入体内。所述egcg来源于绿茶。革兰氏阴性细菌细胞壁成分脂多糖(lps)即内毒素是引起内源性内毒素血症的主要致病因子,lps可被多个器官或组织表面的tlr4受体识别从而引发一系列炎症反应并损害其功能,高脂饮食可通过增加肠道产lps细菌的数量、破坏肠屏障及通过合成乳糜微粒促进lps吸收等引发内源性内毒素血症。本发明采用c57bl/6j小鼠高脂模型,通过酶联免疫法检测egcg对高脂饮食引起的内源性内毒素血症的影响,结果表明egcg显著降低血清lps水平;之后检测肠道乳糜微粒合成相关基因apob48表达情况,发现egcg显著降低乳糜微粒合成标志基因apob48的表达水平;用不同浓度egcg处理使用transwell培养的caco2细胞,结果也显示egcg可显著降低apob48的表达水平;实验证明,egcg可以降低乳糜微粒的合成,减少高脂饮食中肠道lps的吸收,这与内源性内毒素血症的改善有关。与现有技术相比,本发明具有如下优点和有益效果:(1)本发明为目前改善高脂饮食诱导的内源性内毒素血症的应用提供了一种全新的选择和思路,也为该
技术领域:
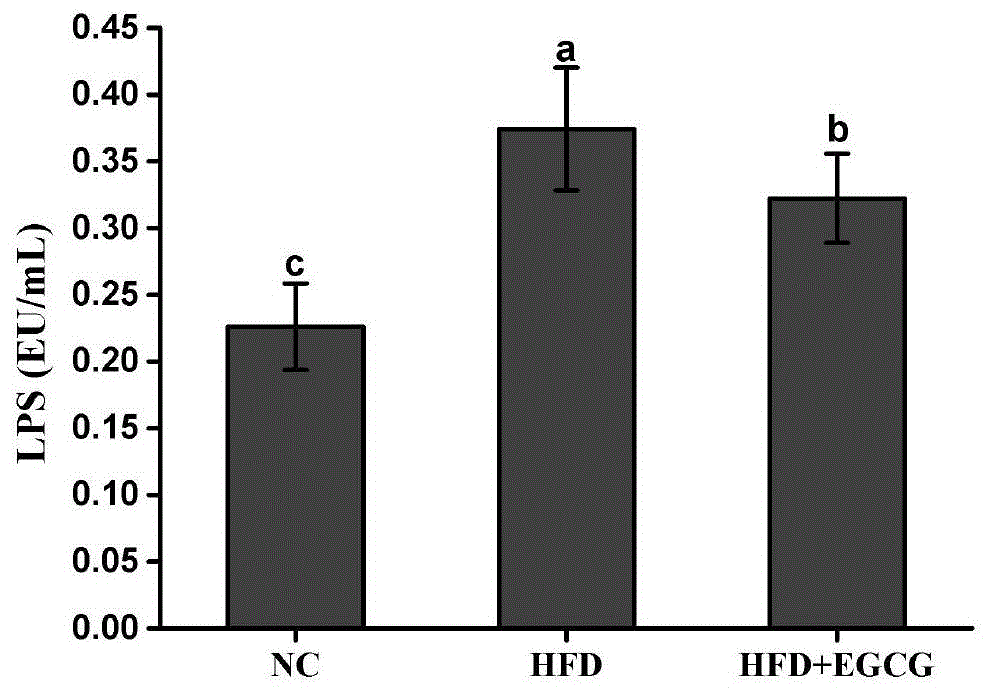
的发展做出了贡献。(2)本发明首次证实绿茶中的成分egcg能够通过调节肠组织中乳糜微粒合成,进而改善内毒素血症。(3)本发明提供egcg在制备改善或治疗高脂饮食诱导的内源性内毒素血症药物中的应用和制备改善高脂饮食诱导的内源性内毒素血症保健食品中的应用,方法简单,安全无毒副作用。附图说明图1为实施例1所得不同组小鼠血清内毒素水平。图2为实施例2所得不同组小鼠回肠乳糜微粒合成标志性蛋白apob48的表达水平。图3为实施例3所得egcg干预对caco2细胞乳糜微粒合成标志性蛋白apob48表达水平的影响具体实施方式为了使本领域技术人员更好地理解本发明的技术方案能予以实施,以下结合附图和实例对本发明的具体实施作进一步说明,不应视为对本发明的范围进行限定,本发明的所有范围限定以权利要求书中的限定为准。需指出的是,以下若有未特别详细说明之过程,均是本领域技术人员可参照现有技术实现或理解的。所用试剂或仪器未注明生产厂商者,视为可以通过市售购买得到的常规产品。实施例1实验动物分组及高脂饮食诱导的内源性内毒素模型建立实验材料及动物:表没食子儿茶素没食子酸酯(egcg)购自上海源叶生物科技有限公司,货号s27863,脂多糖(lps)测定试剂盒购自北京华英生物技术研究所,实验用雄性c57bl/6j购自南开大学实验动物中心,高脂饲料d12492和低脂对照饲料d12450j均为纯化饲料,购自江苏协同医药生物工程有限责任公司。实验方法:(1)将30只6周龄c57bl/6小鼠置于室温为20~25℃,12h光照/12h黑暗循环的环境中适应性喂养1周后,将小鼠随机分为3组:正常饲料对照组(nc)、高脂饲料模型对照组(hfd)、egcg干预组(hfd+egcg),饮水中加入egcg,终浓度为2g/l,每7天称重1次。实验期间,所有小鼠不限制进食和饮水。每天每只小鼠大概饮水2-3ml,连续干预8周后,禁食12h,处死小鼠,收集血液、肝脏、回肠、盲肠和结肠,用预冻盐水清洗后用滤纸吸干。血液4℃过夜后,在4000rpm离心15min获得血清,置于-20℃保存,所有组织立即在液氮中冷冻,并保存在-80℃冰箱用于后期分析。(2)血清内毒素检测:内源性内毒素lps按照相应试剂盒说明书进行测定。实验结果:如图1所示,高脂模型组小鼠血清lps水平显著高于正常对照组小鼠体重(p<0.05),egcg干预可显著降低内毒素lps水平(p<0.05)。实施例2egcg对乳糜微粒合成标志基因apob48的影响实验材料:trizol购自美国ambion公司,反转录试剂盒lunascriptsupermixkit和qpcr试剂盒lunauniversalqpcrmastermix购自美国neb公司。实验方法:用trizol试剂提取回肠组织中的总rna,用nanophotometer检测rna的纯度,并配制1%(w/v)的琼脂糖凝胶进行检测其完整性。使用反转录试剂盒合成cdna,将其保存于-80℃备用。通过qpcr分析mrna的表达水平,qpcr体系(20μl):lunauniversalqpcrmix10μl、cdna模板4μl、上游引物(10μm)0.5μl、下游引物(10μm)0.5μl、ddh2o补充至20μl。pcr反应程序为:预变性95℃60s,变性95℃15s,延伸60℃30s,40次循环。熔融曲线为65℃升温到95℃,持续时间5s。以β-actin为内参基因,采用deltadeltact法对相关基因的表达水平进行分析,引物序列如表1所示。引物名称上游引物(5'-3')下游引物(5'-3')β-actinacagcagttggttggagcaaacgcgaccatcctcctcttaapob48tacttccacccacagtcccctccttagaagccttgggcacat实验结果:如图2所示,高脂组小鼠回肠内乳糜微粒合成标志性蛋白apob48表达量显著升高,apob48基因表达升高代表乳糜微粒合成增加,egcg可显著降低apob48的表达量,即可显著降低乳糜微粒的合成。实施例3egcg对caco2细胞乳糜微粒合成的影响实验材料:油酸购自美国sigma,货号01008实验方法:(1)caco2细胞单层模型的建立与验证:用含10%胎牛血清、1%青霉素-链霉素双抗液以及1%谷氨酰胺的dmem高糖培养基,在37℃,含5%co2的环境下培养caco2细胞。在悬于12孔板中的transwell小室(0.4μm,1.12cm2)上室接种密度为1×106个/ml的caco-2细胞悬液0.5ml,随后在下室放入1.5ml空白培养液,培养至14-21天,使之分化,从而模拟小肠上皮细胞紧密连接蛋白结构,当跨膜电阻值>600ω时,即可认为细胞单层致密完整。(1)用egcg处理细胞:当caco2细胞单层模型建立成功之后,按照前述细胞分组方式(见3.1),并按如下方式给药。①油酸处理组:培养基加入0.81mm的油酸;②油酸+egcg处理组:培养基加入0.81mm的油酸,并分别加入终浓度10、20、40μm的egcg。处理8h后,加入trizol试剂吹打收集细胞,提取其rna,进行实时荧光定量pcr实验,引物如下表2所示。引物名称上游引物(5'-3')下游引物(5'-3')gapdhcaacggatttggtcgtattgggaaggggtcattgatggcaacapob48tgtcagtacacactggacgctcaaatgcgaggcccatctt实验结果:如图3所示,油酸可以诱导回肠内乳糜微粒的合成,加入egcg后,乳糜微粒标志性蛋白apob48的表达随着egcg浓度的增加而显著下降,从而在细胞水平上验证了egcg可以降低乳糜微粒的合成。lps可与食物中的脂质一起进入肠上皮细胞,形成乳糜微粒,从而被吸收进入血液,乳糜微粒的减少,有助于减少脂质和lps的吸收。由以上实施例可以看出egcg具有改善和治疗内源性内毒素血症的功能,因此按照药品或保健食品的制备方法制备含有egcg的药品可以改善或治疗内源性内毒素血症。以上实施例仅为本发明较优的实施方式,仅用于解释本发明,而非限制本发明,本领域技术人员在未脱离本发明精神实质下所作的改变、替换、修饰等均应属于本发明的保护范围。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1